PEMBUATAN DAN PENCIRIAN ELEKTRODE SELEKTIF
ION H
2PO
4
DAN PENERAPANNYA PADA
TANAMAN HIDROPONIK
ARI NUR RAHMAT
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2007
ABSTRAK
ARI NUR RAHMAT. Pembuatan dan Pencirian Elektrode Selektif Ion H2PO4
-fotometeri menggunakan pereaksi vanadat-molibdat dan elitiannya pun mendekati sama. Akan tetapi, metode ini tidak memerlukan perlakuan endahuluan yang rumit.
-i
with the ectrophotometry using molibdate-vanadate reagents and the accuracy close result. evertheless, this method did not require a complicated preliminary treatment.
dan Penerapannya pada Tanaman Hidroponik. Dibimbing oleh DYAH ISWANTINI PRADONO dan DEDEN SAPRUDIN.
Salah satu nutrisi tanaman penting adalah unsur fosforus yang diserap dalam bentuk H2PO4-. Pemberian unsur ini perlu dikendalikan agar penggunaan larutan nutrisi
hidroponik efektif dan efisien. Potensiometri menggunakan elektrode selektif ion (ESI) fosfat adalah metode yang baik penggunaannya bila dibandingkan metode umum berdasarkan daya hantar listrik. Akan tetapi, ESI fosfat yang dibuat perlu dicirikan terlebih dahulu.
Berdasarkan hasil penelitian didapatkan rerata faktor Nernst dari ketiga ESI nitrat sebesar 55,67 mV/dekade dengan r sebesar 99,86%. Trayek pengukuran larutan standar dengan konsentrasi 10-2 sampai 10-5 M memiliki rerata limit deteksi sebesar 10,53 × 10-6
M. Waktu respons kurang dari tiga menit. Metode ini memberikan hasil yang sama dengan metode spektro
ket p
ABSTRACT
ARI NUR RAHMAT. Making and Characterization H2PO4 Ion Selective Electrode and
Its Application for Hydrophonic Plant. Supervised by DYAH ISWANTINI PRADONO and DEDEN SAPRUDIN.
One of the most important plant nutritions is phosphorous which is absorbed as H2PO4-. The distribution of that element need to be controlled so the use of hydrophonic
nutrition solution may be efficient and effective. Potentiometry using phosphate ion select ve electrode (ISE) is a good method as compared to common methods based on electrical conductivity. However, preliminary characterization is required for phosphate ISE.
Based on this research result, the average Nernst factor from all phosphate ISEs were 55,67 mV/decade with r of 99,86%. Standard solution measurement with concentration of 10-2 to 10-5 M showed an average detection limit of 10,53 × 10-6 M. The
responsse time was more than one minute. This method gave the same result sp
PEMBUATAN D
DE SELEKTIF
ION H
2PO
4DAN PENERAPANNYA PADA
TANAMAN HIDROPONIK
ARI NUR RAHMAT
sebagai salah s peroleh gelar Sarjana Sains pada
Departem mia
FAKULTAS MATEMATIKA
U PENGETAHUAN ALAM
INSTITUT PE
IAN BOGOR
2007
AN PENCIRIAN ELEKTRO
-Skripsi atu syarat untuk mem
en Ki
DEPARTEMEN KIMIA
DAN ILM
RTAN
BOGOR
Judul : Pembuatan dan Pencirian Elektrode Selektif Ion H2PO4- dan Penerapannya pada
Tanaman Hidroponik ama : Ari Nur Rahmat IM : G44202025
Menyetujui:
Pembimbing I, Pembimbing II,
Dr. Dyah Iswantini Pradono, M.Agr
NIP 132 956 706 Drs. Deden Saprudin, MS NIP 132 126 040
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
Tanggal Lulus: N
N
PRAKATA
Puji syukur kepada Allah SWT atas segala rahmat dan hidayah-Nya sehingga Penulis dapat menyelesaikan karya ilmiah ini. Tema penelitian yang dipilih dalam penelitian ini adalah pembuatan dan pencirian elektrode selektif ion H2PO4- dengan judul
Pembuatan dan Pencirian Elektrode Selektif Ion H2PO4
-IPB atas bantuannya, kepada rekan tim ESI
atas s udi KS, Chiyo, Yudi PH, Away dan Ricky
serta Evi atas kasih sayang dan dukungannya. S oga karya ilmiah ini bermanfaat.
Bogo
Ari Nur Rahmat
dan Penerapannya pada Tanaman Hidroponik. Dana penelitian ini diperoleh dari Program Hibah Kompetisi A2 Departemen Kimia, Institut Pertanian Bogor.
Dalam penelitian ini penulis banyak mendapatkan bantuan dan bimbingan dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada Dr. Dyah Iswantini Pradono, MAgr dan Drs. Deden Saprudin, MS selaku pembimbing yang telah memberikan bimbingan dan arahan selama penelitian dan penulisan karya ilmiah ini kepada orang tua tercinta atas dukungan moril dan materil selama ini. Penghargaan penulis sampaikan kepada Bapak Eman, Kak Zulhan, Bapak Dede dan staf Laboratorium Kimia Analitik dan Laboratorium Kimia Fisik
aran-sarannya, Joko, Tri, Joe, Obi, Y
em
RIWAYAT HIDUP
Penulis dilahirkan di Cirebon pada tanggal 10 Februari 1984 dari ayah Achmad Dulmanan dan ibu Ety. Penulis merupakan putra ketujuh dari tujuh bersaudara.
Tahun 2002 penulis lulus SMA Negeri 3 Cirebon dan pada tahun yang sama masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, IPB.
Selama mengikuti perkuliahan, penulis pernah menjadi staf Departemen Keilmuan Imasika (Ikatan Mahasiswa Kimia) tahun ajaran 2002/2003, staf Departemen Pengabdian Pada Masyarakat (P2M) tahun ajaran 2003/2004, asisten praktikum Kimia Anorganik II
ahun ajaran 2005/2006, Kimia Fisik t
a
tahun ajaran 2006/2007, dan Elektroanalitik tahun jaran 2006/2007. Pada tahun 2004 penulis melaksanakan praktik lapangan di PT
docement Tunggal Prakarsa, Tbk. In
DAFTAR ISI
iv PEND TINJA SI... 3 BAHA ... 4 HASI USTAKA ... 8 AMPIRAN... 10 Halaman DAFTAR TABEL...iiDAFTAR GAMBAR ...iii
DAFTAR LAMPIRAN... AHULUAN ... 1
UAN PUSTAKA Hidroponik ... 2
Larutan Nutrisi ... 2
Elektrode Selektif Ion ... 2
Prinsip Penggunaan E Pencirian ESI Fosfat... 4
N DAN METODE Bahan dan Alat... Metode Penelitian... 4
L DAN PEMBAHASAN Faktor Nernst dan Trayek Pengukuran ... 6
Limit Deteksi ... 7
Waktu Respons... 7
Umur Pakai... 7
Penentuan Konsentrasi Fosfat pada Contoh Nutrisi Hidroponik ... 8
SIMPULAN DAN SARAN... 8 DAFTAR P
DAFTAR TABEL
... 8
8 10 Potensial ukuran konsentrasi fosfat contoh nutrisi hidroponik menggunakan metode ESI fosfat ... 16
Halaman 1 Potensial elektrode pada ketiga ESI... 6
2 Nilai faktor Nernst dan koefisien korelasi (r) ... 7
3 Limit deteksi ESI fosfat ... 7
4 Waktu respons ESI fosfat... 7
5 Nilai faktor Nernst ketiga ESI fosfat selama 10 hari ... 7
6 Koefisien korelasi (r) ketiga ESI fosfat selama 10 hari ... 7
7 Konsentrasi fosfat pada contoh nutrisi hidroponik ... Transmitans (T) dan absorbans (A) standar fosfat spektrofotometri ... 15
9 Pengukuran konsentrasi fosfat contoh nutrisi hidroponik menggunakan spektrofotometri... 15
Elektrode (E) standar fosfat metode ESI fosfat... 15 11 Peng
DAFTAR GAMBAR
6 III... 6 ... 12 ... 12 ... 12 ... 132 Kurva Kalibrasi standar fosfat menggunakan Spektrofotometri... 15
3 Kurva Kalibrasi standar fosfat menggunakan metode ESI fosfat ... 15
DAFTAR LAMPIRAN
1 7 Uji-F metode ESI dan spektrofotometri ... 168 Gambar ESI fosfat terlapis membran ... 17
Halaman 1 Struktur dibutil sebakat (DBS)... 1
2 Rangkaian pengukuran dengan ESI... 4
-2 Kurva hubungan antara –log [H2PO4] dan potensial (mV/dekade) pada ESI I ... 6
-3 Kurva hubungan antara –log [H2PO4] dan potensial (mV/dekade) pada ESI II ... 4 Kurva hubungan antara –log [H2PO4-] dan potensial (mV/dekade) pada ESI 5 Kurva hubungan –log [H2PO4-] terhadap potensial (mV) menggunakan empat konsentrasi (a) dibandingkan dengan menggunakan enam konsentrasi (b) pada ESI kode I... 6 Kurva hubungan –log [H2PO4-] terhadap potensial (mV) menggunakan empat konsentrasi (a) dibandingkan dengan menggunakan enam konsentrasi (b) pada ESI kode II... 7 Kurva hubungan –log [H2PO4-] terhadap potensial (mV) menggunakan empat konsentrasi (a) dibandingkan dengan menggunakan enam konsentrasi (b) pada ESI kode III ... 8 Kurva hubungan –log [H2PO4-] terhadap potensial (mV) yang menggambarkan limit deteksi yaitu pada perpotongan garis y = 56,7x + 44,8 dengan garis y = 11x + 263 pada ESI kode II... 9 Kurva hubungan –log [H2PO4-] terhadap potensial (mV) yang menggambarkan limit deteksi yaitu pada perpotongan garis y = 50,5x + 44,5 dengan garis y = -52x + 595 pada ESI kode III ... 13
10 Grafik hubungan antara hari ke- dan faktor Nernst dari umur ESI... 14
11 Grafik hubungan antara hari ke- dan koefisien korelasi (r) dari umur ESI ... 14
1 1 Halaman Bagan alir metode penelitian ... 11
2 Perbandingan kurva trayek pengukuran menggunakan empat konsentrasi dan enam konsentrasi pada ketiga ESI ... 12
3 Penentuan limit deteksi pada kedua ESI ... 13
4 Umur pakai dari ketiga ESI fosfat ... 14
5 Data konsentrasi fosfat standar, contoh, dan kurva kalibrasi ... 15
PENDAHULUAN
Indonesia merupakan negara agraris namun kebutuhan pangan belum terpenuhi dikarenakan semakin berkurangnya lahan pertanian. Hal ini disebabkan pembangunan perumahan dan kawasan industri yang menggunakan lahan pertanian. Untuk mengatasi krisis pangan, maka dikembangkan suatu teknik pertanian yang dikenal dengan istilah hidroponik.
Hidroponik adalah suatu cara bercocok tanam tanpa menggunakan tanah sebagai tempat menanam tanaman. Istilah hidroponik dikalangan umum lebih populer dengan sebutan berkebun tanpa tanah, termasuk dalam hal ini tanaman dalam pot atau wadah lain yang menggunakan atau bahan berpori lainnya seperti kerikil, pecahan genteng, pasir kali, gabus putih.
Salah satu hal yang harus diperhatikan pada budidaya secara hidroponik adalah nutrisi tanaman yang sebagian besar diberikan dari luar media (bukan secara alami telah ada pada media). Unsur-unsur yang termasuk dalam nutrisi tanaman di antaranya C, H, O, N, P, K, Ca, S, Mg, Fe, Mn, Cu, Zn, B, Mo, dan Cl (Leiwakabessy 1988, diacu dalam Napitupulu 2003). Salah satu nutrisi penting yang dibutuhkan tanaman adalah fosforus. Fosforus diambil oleh akar dalam bentuk H2PO4- dan HPO4-. Sebagian besar fosforus
dalam tanaman adalah sebagai zat pembangun dan terikat dalam senyawa-senyawa organis. Sebagian kecil ion-ion fosfat terdapat dalam bentuk anorganis (Lingga 1993).
Alat yang spesifik dan cepat sangat diperlukan untuk mentukan kandungan fosforus. Morgan (2000) telah menganalisis hanya berdasarkan daya hantar listrik (DHL). Analisis dengan menggunakan DHL hanya mampu memberikan indikasi mengenai nutrisi yang terkandung pada larutan yang diserap oleh akar, tetapi tidak dapat memberikan informasi kandungan nutrisi secara spesifik terhadap ion tertentu berupa jumlah atau konsentrasi. Oleh karena itu, diperlukan suatu alat yang dapat menentukan kandungan ion-ion tersebut secara spesifik, selektif, efisien, dan cepat. Penelitian ini dilakukan untuk membuat elektrode selektif ion (ESI) yang dapat digunakan untuk menentukan kandungan ion fosfat (ESI fosfat) secara langsung pada larutan nutrisi hidroponik sehingga penggunaan air dan nutrisi tanaman akan lebih efisien dan terkendali.
Keefektifan ESI disebabkan oleh gangguan terhadap kinerja ESI hanya sedikit
dan mudah diatasi. Salah satu contoh dari keefektifan ESI adalah kekeruhan (berwarna sampai batas tertentu) tidak menyulitkan pengukuran dan prosedurnya sederhana sehingga hanya memerlukan waktu yang singkat, alat-alat sederhana, dan mudah dilakukan. Oleh karena itu, ESI dapat digunakan untuk pengukuran pada analisis rutin (Wang & Joseph 1994).
Penelitian mengenai ESI kawat terlapis yang telah diakui yaitu ESI nitrat (Fardiyah 2003). ESI nitrat dibuat dengan menggunakan bahan ionofor aliquot 336 ke dalam campuran komposisi membran yang dilapiskan pada kawat platina. Selain itu, sebagai bahan pendukung digunakan PVC sebagai matriks polimer, DOP (dioktil ftalat) atau DBP (dibutil ftalat) sebagai pemlastis. Karakteristik ESI nitrat tipe kawat terlapis yang telah dibuat memiliki nilai faktor Nernst 59 mV/dekade, trayek pengukuran pada konsentrasi 10-1-10-4
waktu respon 30-60 detik, dan dapat digunakan pada pH 3-9.
Pemilihan membran PVC dikarenakan PVC memiliki beberapa keunggulan sebagai polimer, seperti tidak mudah rusak oleh kelembaban, kaku, tahan terhadap pelarut, berpori kecil (mikroporus), tidak berpengaruh pada korosi, kelenturan yang baik, stabilitas panas yang baik, stabilitas yang baik terhadap bahan kimia dan air, kekuatan struktural yang sempurna, tahan panas, dan tahan terhadap cuaca (Celuform 2007).
Kinerja ESI dipengaruhi oleh beberapa faktor, seperti: komposisi membran, koefisien selektivitas, pH, dan tipe elektrode. Pembuatan ESI untuk target anion yang sedang dikembangkan saat ini adalah pembuatan ESI anion perklorat dengan menggunakan teknologi lapis tipis. Teknologi ini memerlukan biaya rendah, produksi skala besar, pembuatan yang sederhana dan dapat diterapkan pada elektrokimia dan biosensor (Segui et al. 2006). ESI perklorat ini dibuat dengan ionofor 1,4,7,10,13-penta(n-oktil)-1,4,7,10,13-pentaazasiklopentadekana, mem- bran PVC yang berisi pemlastis dibutil sebakat (DBS) menghasilkan faktor Nernst 57 mV/dekade dengan kisaran konsentrasi 10-1-
10-4 M.
O
O
O O
Penelitian mengenai ESI fosfat telah membran PVC baru dilakukan oleh Edioloegito (2005). Penelitian tersebut hanya menyelidiki bagaimana pengaruh pH terhadap kinerja ESI fosfat sedangkan pada penelitian ini dilakukan penentuan faktor Nernst, limit deteksi, waktu respons, dan usia pemakaian. Penelitian ini diharapkan dapat menjelaskan penentuan jumlah fosfat dalam larutan nutrisi hidroponik dengan cara yang mudah dan cepat.
TINJAUAN PUSTAKA
Hidroponik
Istilah hidroponik berasal dari kata hydro (air) dan phonos (kerja) yang berarti melakukan pekerjaan dengan air (Soeseno 1999). Beberapa istilah yang berkaitan dengan budidaya tanaman melalui media air adalah
soilless culture, aquaculture, dan nutriculture.
Sistem ini mencoba memberikan fungsi sebagai media penyangga tanaman serta sumber air dan nutrisi seperti yang diberikan oleh tanah (Schwartz 1995, diacu dalam Retariandalas 2003).
Menurut Lingga (1993), keuntungan bercocok tanam secara hidroponik, yaitu produksi tanaman lebih tinggi dibandingkan menggunakan media tanam tanah biasa, tanaman lebih terbebas dari hama dan penyakit, tanaman tumbuh lebih cepat dan pemakaian pupuk lebih hemat, penggantian tanaman yang mati dengan yang baru lebih mudah, tanaman akan memberikan hasil yang kontinyu, pengerjaannya lebih mudah dan tidak membutuhkan tenaga kasar, kualitas daun, buah atau bunga yang lebih sempurna dan tidak kotor, efisiensi kerja kebun hidroponik menyebabkan perawatannya tidak membutuhkan banyak biaya dan peralatan.
Perkembangan hidroponik hingga saat ini telah menunjukkan kemajuan yang sangat pesat. Perkembangan tersebut meliputi hidroponik di pasir pantai, kapal induk, bahkan untuk selanjutnya akan dikembangkan di luar angkasa.
Larutan Nutrisi
Tanaman memerlukan unsur hara agar dapat berkembang dengan baik. Sebagian besar unsur hara tanaman diperoleh di dalam tanah yang diserap melalui akar. Dalam sistem hidroponik, media tanam yang digunakan tidak berfungsi sebagai tanah. Media tanam
hanya berfungsi untuk menopang tanaman dan meneruskan larutan atau air yang berlebihan atau yang tidak diperlukan oleh tanaman lagi. Media tanam yang digunakan harus berasal dari bahan yang berpori dan steril. Garam pupuk yang diberikan harus mengandung semua unsur yang diperlukan oleh tanaman (Lingga 1993).
Berdasarkan kebutuhan tanaman, pupuk buatan dapat dibedakan menjadi dua golongan, yakni pupuk makro dan mikro. Terdapat enam belas unsur penting yang dibutuhkan dalam pertumbuhan dan perkembangan tanaman. Tiga belas unsur fungsional diperoleh tanaman dalam tanah antara lain nitrogen (N), fosforus (P), kalium (K), kalsium (Ca), magnesium (Mg), dan sulfur (S). Unsur-unsur tersebut diperlukan dalam jumlah banyak sehingga disebut unsur hara makro. Unsur besi (Fe), mangan (Mn), tembaga (Cu), zink (Zn), boron (Bo), molibdenum (Mo), dan klorin (Cl) digunakan dalam jumlah sedikit sehingga disebut unsur hara mikro. Unsur-unsur lain seperti karbon (C) dan oksigen (O) diperoleh langsung dari udara dan hidrogen (H) diperoleh baik langsung maupun tidak langsung dari dalam tanah (Soepardi 1983).
Ketersediaan semua nutrisi penting berada pada pH 5,4-6,0 untuk media tanpa tanah. Rendahnya pH menyebabkan peningkatan kandungan Fe, Mg, dan Al yang terlarut dan ketersediaan Ca, S, dan Mo akan menurun, sedangkan pH tinggi menyebabkan penurunan P, Fe, Mg, Zn, Cu, dan B (Nelson 1998, diacu dalam Nurfinayati 2004). Soepardi (1983) menambahkan bahwa pH merupakan hal yang harus diperhatikan kerena berhubungan dengan kemudahan Ca dan Mg saling bertukar, kelarutan aluminium dan unsur-unsur mikro, ketersediaan fosforus, dan kegiatan jasad mikro.
Elektrode Selektif Ion
ESI merupakan suatu sensor yang mengubah aktivitas dari suatu ion spesifik terlarut pada larutan ke dalam suatu potensial listrik yang dapat diukur oleh voltmeter atau pH-meter (Wikipedia 2004). Secara teoretis, potensial bergantung pada logaritma dari aktivitas ion yang termasuk ke dalam persamaan Nernst. Bagian dari elektrode yang merespons biasanya terbuat dari membran ion spesifik.
Walter Nernst (1864-1941) adalah salah
seorang yang merintis dasar-dasar kesetimbangan elektrokimia dan potensial
3
elek
milivolt, selektif terhadap ion yang diinginkan, dan dapat digunakan pada berb ai macam pH. Penentuan ESI juga tidak
terpeng praktis
alam analisis contoh lingkungan karena ntuan in sit ukan.
Penggunaan ESI
ESI terdi bran dan satu elekt
Esel =
trode. Persamaan Nernst digunakan untuk perhitungan semua potensial setengah sel, yaitu pada saat kesetimbangan reaksi setengah sel oksidasi reduksi (Skoog & Douglas 1980).
Penggunaan ESI dalam analisis lingkungan memberikan beberapa kelebihan dibandingkan dengan metode lain, yaitu biaya dalam perancangan analisisnya rendah dibandingkan dengan metode lain seperti spektrofotometer serapan atom (SSA) atau kromatografi ion, dapat membaca potensial sampai
ag
aruh warna contoh dan lebih d
pene u sering diperl
Beberapa sifat yang harus dimiliki oleh membran selektif ion agar elektrode tersebut mempunyai sensitivitas dan selektivitas yang baik terhadap kation dan anion, yaitu tidak larut air, dapat menghantarkan listrik, bereaksi secara selektif dengan ion-ion analat melalui tiga tipe ikatan, yaitu pertukaran ion, kristalisasi, dan kompleksasi (Bailey 1983, diacu dalam Fardiyah 2003).
ESI terlapis-membran terdiri atas elektrode kerja yang dilapisi membran (logam dopan) dan elektrode pembanding. Ada dua cara pelapisan membran pada logam (pendopan) yang sering dilakukan, yaitu dengan penambahan langsung dopan pada saat pembuatan membran dan perendaman pada larutan dopan. Pendopanan dengan perendaman akan memberikan membran konduktif yang merata pada seluruh bagian permukaan sehingga sensitivitasnya meningkat, tahan lama, dan reprodusibel (Yang et al. 1997 dalam Gea et al. 2005). Cara lain untuk meningkatkan konduktivitas membran adalah dengan menambahkan sejumlah tertentu pemlastis. Hal ini bertujuan meningkatkan kelenturan dan kelembutan membran sehingga rantai-rantai polimer bergerak bebas serta memperbaiki kontak permukaan antar logam dopan dengan polimer aktifnya (Golodnitsky et al. 1996 dalam Gea
et al. 2005)
Prinsip
ri atas sebuah mem
rode pembanding yang tercelup pada larutan dalam membran (ai int) (Strobel
1992). Elektrode dicelupkan dalam larutan contoh yang mengandung analat dengan aktivitas ion (ai). Sedangkan elektrode
pembanding luar adalah bagian membran
yang langsung berinteraksi dengan larutan contoh (ai ext). Kedua elektrode ini
merupakan penyusun setengah reaksi sel elektrokimia. Potensial yang terukur merupakan selisih potensial antara elektrode pembanding luar (Eref ext) dengan elektrode
pembanding dalam (Eref int) ditambah
potensial membran (Ememb) dan potensial
sambungan cair (Elj). E1j adalahpotensial pada
pertemuan antara Eref ext dengan larutan
contoh. Hubungan tersebut dapat ditulis:
Esel = Eref ext - Eref int + Ememb + E1j
(1)
Membran yang dipakai bersifat selektif terhadap ion tertentu (i) sehingga potensial yang dihasilkan antara kedua sisi membran akan bergantung pada ai pada kedua sisi.
Ememb = RT/nF ln (ai contoh/ ai ln t) (2)
n = elektron yang terlibat dalam proses
oksidasi dan reduksi
Bila persamaan (2) diatas disubstitusikan ke persamaan (1) maka akan menghasilkan persamaan (3):
Esel = Eref ext - Eref int + RT/nF ln (1/ ai ln
t) + RT/nF ln (ai contoh) + E1j
(3)
Potensial setengah sel kedua elektrode pembanding bersifat konstan. Kondisi larutan contoh dapat dikontrol sehingga E1j akan
konstan demikian juga kondisi larutan di dalam membran. Persamaan diatas dapat disederhanakan lagi menjadi:
contoh
ln a
RT
inF
Keterangan: K = KetetapanR = Konstanta molar gas (8.314 J/K mol) T = Suhu (K)
a
K
+
(4)i = Aktivitas ion
n = Muatan ion
Hubungan antara potensial ESI dan aktivitas analat ini merupakan dasar kerja ESI sebagai alat analisis.
Potensial suatu ESI dapat ditentukan menggunakan elektrode pembanding
perak/perak klorida (Ag/AgCl), elektrode kalomel jenuh (Hg/Hg2Cl2), atau elektrode gas
hidrogen. Beda potensial antara ESI dengan elektrode pembanding merupakan potensial
Membran ESI yan limit deteksi, but t proses kesetimbangan.
Umur pakai ESI adalah lamanya suatu
ESI masih kai dapat
dilih
a. pen uments pH510), spektrofotometer tampak pectronic 20), elektrode kalomel jenuh, nera
Metode Penelitian
L igunakan sebagai
tandar memiliki konsentrasi 0,1 M. Larutan ir bebas ion.
m dengan
corong h, dikocok selama 10 menit, emudian didiamkan sampai terjadi
Fardiyah 2003). Pembuatan Elektrode
tan Badan ESI
berdiameter 0,5 mm sepanjang gkan dengan 5 cm kawat an gian na) dibiarkan terbuka untuk
a membran dan 1,5 cm an atas (kawat tembaga) ihubungkan dengan potensiometer.
ran dibuat dengan mel
g terukur. Rangkaian pengukuran dapat dilihat pada Gambar 1.
Gambar 2 Rangkaian Pengukuran dengan ESI.
Pencirian ESI Fosfat
Pencirian ESI fosfat meliputi faktor Nernst, trayek pengukuran,
waktu respons, dan umur pakai. Penentuan Faktor Nernst menggunakan ESI yang tercelup dalam larutan ion (i) biasanya dilakukan dengan membuat kurva hubungan potensial elektrode (E) terhadap logaritma bernilai negatif dari aktivitas ion (-log a) yang ada dalam larutan. Bentuk kurva dari persamaan Nernst berupa daerah linear. Bila kurva yang dihasilkan mulai tidak linear lagi pada konsentrasi yang encer maka kurva ini tidak memenuhi persamaan Nernst. Sementara itu kurva linear merupakan trayek pengukuran dan batas daerah linear dan non-linear dise limit deteksi dari ESI.
Waktu respons adalah waktu yang diperlukan ESI untuk memberikan potensial yang konstan. Semakin cepat suatu elektrode memberikan potensial yang konstan maka semakin baik elektrode tersebut. Waktu respons dipengaruhi oleh konsentrasi dan pengadukan yang berfungsi untuk mempercepa
layak digunakan. Umur pa
at dari nilai faktor Nernst ESI yang penyimpangnya tidak terlalu besar dari nilai teoretis dengan nilai koefisien korelasi (r) mendekati satu. Lama pemakaian ESI bermembran dipengaruhi oleh suhu, pH, pelarut organik, dan stabilitas mekanik (Atikah 1994).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan di antara-nya adalah air bebas ion, KH2PO4, metil
trioktilamonium klorida (aliquot 336), dioktilftalat (DOP), PVC (36000 g/mol)
Merck, tetrahidrofuran (THF), amonium
molibdat, amonium vanadat, HNO3, larutan
nutrisi hidroponik, kawat platina (Pt) berd ameter 0,5 mm, dan plastik polietilen Larutan contoh Elektrode Pembanding i Elektrode
selektif ion ini di antaranya potensiometer (EUTECH Alat-alat yang digunakan pada elitian Instr
(S
ca analitik (AND GR-200), oven, pengaduk magnet, pengukur waktu, dan alat-alat kaca.
Pembuatan Larutan Pembuatan Larutan KH2PO4
arutan KH2PO4 yang d
s
baku fosfat ini dibuat dari kristal KH2PO4.
Sebanyak 1,36 g kristal tersebut dilarutkan dalam 100 ml a
Pe buatan Larutan Aliquot 336 Fosfat Sebanyak 12,5 ml aliquot 336 diekstraksi
10 ml KH2PO4 0,1 M menggunakan
pisa k
pemisahan fase minyak dan air. Fase minyak diekstraksi kembali dengan KH2PO4 1 M
sampai fase air tidak mengandung ion klorida (diuji dengan AgNO3 0,01 M). Fase minyak
yang sudah bebas dari klorida adalah larutan
aliquot 336 fosfat (modifikasi
Pembua Kawat Pt 2 cm disambun
tembaga. Kawat tersebut ditutup deng plastik polietilena dengan 1 cm pada ba bawah (kawat plati
tempat menempelny ujung kawat bagi d
Pelapisan Membran pada Badan ESI Larutan memb
arutkan 0,85 g PVC, 0,07 g aliquot 336 fosfat, dan 0,58 g DOP dalam 10 ml THF.
Campuran tersebut diaduk selama 3 jam. Kawat Pt pada elektrode dibersihkan kemudian dicelupkan ke dalam larutan membran yang telah dibuat sampai membran menempel pada kawat secara merata dan tipis, lalu dikeringkan pada o
jam odifikasi Buchari & Irdhawati 2002). suhu 40 C selama 24 ang telah jadi diprak
tan KH2PO4 0,1 M selam ,
di tempat kering. ESI y n igunakan harus diprakondisikan lagi dalam
H2PO4 0,1 M minimal 2 jam
igunakan dalam pengukuran. ESI f ibuat sebanyak 3 buah dan potensi
itentukan dengan menggunakan elektrode alomel jenuh sebagai elektrode pe
Pencirian ESI Fosfat aktor Nernst dan Trayek Pengukuran
at, M sampai 10-1 M. Potensial
lektrodenya diukur berturut-turut, mulai dari
larutan pali .
(59,2 m akin
ndah kualitas ESI.
Pengukuran pada
Con
ketelitian (uji-F) konsentrasi dari
kedu meto 1991).
Untuk uji n dengan
menggunaka itab-14.
bility) dari tiap
rode ESI
tersebut ti le 1995).
Simpangan ri rumus:
V/dekade, pada 25oC) maka sem
re
Konsentrasi Fosfat toh Nutrisi Hidroponik
Pengukuran konsentrasi contoh diawali dengan metode molibdat-vanadat sebagai metode pembanding. Molibdat-vanadat sebanyak 10 ml ditambahkan pada larutan standar fosfat, mulai dari konsentrasi 10-5 M
sampai 10-2 M dan larutan nutrisi hidroponik,
kem (m ESI y ondisikan a 12 jam ang aka dalam laru dan disimpan d sebelum osfat yang al larutan
K udian ditentukan serapannya pada
panjang gelombang 460 nm. Pengukuran menggunakan ESI fosfat dilakukan dengan mengukur larutan standar fosfat dimulai dari konsentrasi 10-5 M sampai 10-2 M, kemudian
ditentukan potensialnya.
Uji statistika dilakukan terhadap hasil (uji- dan d d d k mbanding. t) a F
Beberapa konsentrasi H2PO4- dibu de (Miller JC & Miller JN
-t dan uji-F dilakuka mulai dari 10-7
e n perangkat lunak Min
ng encer sampai paling pekat Hasil pengukuran tersebut dibuat menjadi kurva hubungan antara –log [H2PO4-] terhadap
potensial (E) (persamaan 4). Kurva yang diperoleh merupakan garis linear pada selang kon-sentrasi tertentu (dalam trayek pengukuran) dengan kemiringan sebesar 2,303RT/nF (nilai faktor Nernst yang diturunkan dari logaritma). Ekstrapolasi ke sumbu-Y (E) akan menghasilkan nilai intersep (K) (Fardiyah 2003).
Limit Deteksi
Limit deteksi ditentukan dengan membuat garis singgung pada fungsi garis lurus dan garis melengkung kurva antara –log [H2PO4-]
dengan E (mV) yang saling memotong. Titik poto
HASIL DAN PEMBAHASAN
Pencirian ESI dilakukan dengan memakai tiga elektrode yang dimaksudkan untuk melihat keterulangan (repeata
ESI. Perlakuan dari masing-masing elekt tidak ada yang berbeda. Masing-masing diberi nomor I, II, dan III. Data potensial ketiga elektrode pada kisaran konsentrasi 10-1
-10-7 dapat dilihat pada Tabel 1. Simpangan
baku (SB) dan simpangan baku relatif (SBR) yang diperoleh dari masing-masing elektrode pada tiap konsentrasi sangat besar. Simpangan baku yang besar menunjukkan keragaman yang besar yang berarti nilai-nilai yang diperoleh menyebar jauh dari nilai tengahnya sehingga dapat disimpulkan data potensial ng dari kedua garis singgung tersebut
merupakan limit deteksi pengukuran. Waktu Respons
Waktu respons ESI ditentukan dengan membuat beberapa konsentrasi larutan standar dan setiap konsentrasi larutan tersebut diukur waktunya, mulai saat elektrode bersentuhan den
dak homogen (Walpo baku relatif diperoleh da
rerata
SB
x 100%.
Menurut AOAC (1993), kriteria %SBR yang sesuai standar adalah sebagai berikut jika %SBR <1 sangat teliti, 1-2 teliti, 2-5 sedang, dan >5 tidak teliti. Dari Tabel 1 dapat dilihat %SBR yang sangat besar
gan larutan sampai E yang terukur pada potensiometer menunjukkan nilai yang konstan.
Umur pakai
Umur pakai ESI ditentukan dengan menghitung nilai faktor Nernst pada selang waktu 5 hari selama 1 bulan. Semakin jauh penyimpangan dari nilai faktor Nernst teoretis
(>>5%), tidak yang menunjukkan hasil yang diperoleh teliti. Dari nilai %SBR dapat disimpulkan bahwa keterulangan data yang diperoleh kurang baik.
6
(
log[ ])
303 , 2 4 2 − − + = H PO nF RT K ETabel 1 Potensial elektrode untuk ESI I, II, dan III E (mV) [H (M2 PO4-] ) I II III Rerata SB SBR(%) 10-1 403 354 251 336 77,58 23,09% 10-2 10-3 10-4 10-5 10-6 10-7 233 155 159 182,3 43,92 24,09% 288 220 206 238 43,86 18,43% 349 271 226 282 62,23 22,07% 412 327 299 346 58,85 17,01% 212 329 283 274,7 58,94 21,46% 414 340 231 328.3 92,06 28,04% Perbedaan nilai potensial dapat disebabkan oleh banyak faktor yang berasal dari fisik elektrode itu sendiri, di antaranya
keseragama ifat fisik
membran, kea platina, wat
Pt ( a
uksi, berarti untuk ESI harga n = 1 adalah 59,20
Nernst relasi. Faktor Nernst juga
erja ES
pengukurannya karena nilai faktor sangat mendekati nilai yang n tebal membran, s
daan permukaan kawat dan sifat antarmuka membran dengan ka
Buchari & Irdhawati 2002; Wah b et al. 2005).
Faktor Nernst dan Trayek Pengukuran Faktor Nernst adalah kemiringan kurva dari persamaan Nernst,
Nilai faktor Nernst adalah 2.303RT/F. Nilai faktor Nernst berdasarkan persamaan tersebut pada 25oC adalah 59,2/n mV/dekade dengan n
adalah jumlah elektron yang terlibat dalam roses oksidasi dan red
p
H2PO4- dengan
mV/dekade dengan faktor Nernst yang diperbolehkan 55/n mV/dekade (Evans 1987, diacu dalam Gea et al. 2005). Syarat linearitas menurut AOAC (1993) adalah lebih besar dari 99,95%.
Faktor-faktor fisik ESI tersebut dapat empengaruhi baik tidaknya faktor
m
dan koefisien ko
dapat disebut sebagai sensitivitas dari suatu elektrode.
ESI I menghasilkan kemiringan Nernstian 59,80 mV/dekade dan koefisien korelasi (r) sebesar 99,95% pada kisaran konsentrasi H2PO4- 10-2-10-5 M seperti terlihat pada
Gambar 2. Hal ini berarti kin I I cukup aik dalam
b
Nernst yang
sesuai persamaan dan linearitas yang mendekati standar AOAC.
y = 5 400 500 9,8x + 111,2 r = 99,95% [H
hat pada Gambar 3. Sep 0 0 1 2 3 4 5 6 -log 2PO4 -]
Gambar 3 Kurva hubungan antara –log [H 100 200 E ( 300 m V ) 2PO4-] dan potensial
(mV/dekade) pada ESI I.
ESI II menghasilkan slope Nernst 56,70 mV/dekade dan koefisien korelasi (r) sebesar 99,88% pada kisaran konsentrasi H2PO4- 10-2
-10-5 M seperti yang terli
erti halnya ESI I, ESI II pun memberikan hasil yang baik karena walaupun sedikit jauh dari nilai faktor Nernst ideal namun masih dalam kisaran yang diperbolehkan.
y = 56,7x + 44,8 r = 99,88% 0 50 100 150 0 1 2 3 4 5 6 -log [H2PO4-]
Gambar 4 Kurva hubungan antara –log [H 200 250 300 350 E ( m V ) 2PO4-] dengan potensial
(mV/dekade) pada ESI II. Kinerja ESI III menghasilkan slope Nernstian sebesar 50,50 mV/dekade dan koefisien korelasi (r) sebesar 99,74% pada kisaran konsentrasi H2PO4- 10-2-10-5 M seperti terlihat
pada Gambar 4. Nilai faktor Nernst yang diperoleh jauh dari nilai yang diperbolehkan sehingga kinerja ESI III kurang baik dalam pengukurannya. y = 50,5x + 44,5 r = 99,74% 0 50 100 150 200 0 1 2 3 4 5 6 -log [H2PO4-] E (
Gambar 5 Kurva hubungan antara –log [H 250 300 350 m V )
V/dekade) pada ESI kode A.
2PO4-] dengan potensial
7
Tabel 2 memperlihatkan rerata nilai faktor an nilai koe
Nernst d fisien korelasi (r) dari E a kisaran ko nt 10-2 -5
. Re a or er n dip
ermasuk dal tor y
perbol n h a p nerja a ut erband n a a pen o t n 1 ilihat p L ir 2 a to r t g a u ra ketiga M SI pad nse nst ya rasi g -10 eroleh rat fakt N t am ki
se inggsaran fa dapatk Nernstdisim ulkan ang di
ki dari ketig ESI terseb cukup baik. ehka P inga ant ra tr yek gukuran ESI pada k nsen rasi 10-1-10-7 da 0-2-10-5 dapat
d ada amp an 2.
Tabel Nil
peni fakukur n larr Nenst dantan nit r pada t 10-2-10rayek -5 M Kode ESI
Ciri
ESI I II III Rerata
Faktor Nernst (mV/dekade)
59,80 56,70 50,50 55,67 r 99,95% 99,88% 99,74% 99,86%
Dari Tabel 2 dapat disimpulkan bahwa urut elekan trode dari faktor Nernst yang paling ba
sfat ditentukan rdasarkan titik potong kurva yang linear dan onlinear dapat dilihat pada Lampiran 3. Tabel
imit deteksi ESI fosfat ik hingga kurang baik adalah I>II>III.
Limit Deteksi Limit deteksi dari ESI fo be
n
3 memperlihatkan hasil penentuan limit deteksi dari kedua ESI fosfat. ESI I tidak dapat ditentukan karena tidak ada perpotongan antara garis yang linear dan non-linear seperti yang terlihat pada Lampiran 3. Nilai limit deteksi ini mengindikasikan bahwa ESI fosfat yang dibuat tidak dapat digunakan pada konsentrasi yang lebih kecil dari limit deteksi tersebut karena pada konsentrasi tersebut tidak memenuhi r yang baik.
Tabel 3 L Kode ESI Limit deteksi II III Rerata -log [H2PO4-] 4,77 5,37 5,07 [H2PO4-](10-6M) 16,8 4,26 10,53
Limit deteksi yang diperoleh dari tiap elektrode sangat berbeda-beda. Lain halnya dengan pengukuran ESI nitrat yang nilai limit deteksinya cukup berdekatan yaitu 7,76x10-5
M, 8,13x10-5 M dan 8,7x10-5 M (Hartaman
2007). Dari hasil limit deteksi diperoleh kesimpulan bahwa limit deteksi elektrode II lebih rendah dari elektrode III.
Waktu Respons
Waktu respons dari ESI fosfat juga dipelajari pada penelitian ini. Waktu respons
sangat dipengaruhi oleh tebalnya membran, konsentrasi larutan, dan umur pakai dari ESI (Buchari & Irdhawati 2002).
Tabel 4 memperlihatkan pengaruh konsentrasi terhadap waktu respons. Waktu respons yang diperoleh tiap elektrode kurang dari 3 menit. Semakin tinggi konsentrasi maka waktu respons dari elektrode akan semakin cepat. Hal ini disebabkan difusi dari ion 1986).
contoh melalui lapisan tetap yang menempel pada permukaan membran (Oesch et al. Tabel 4 Waktu respons ESI fosfat
Waktu respons (detik) pada [H2PO4-] (M) ESI 10-2 10-3 10-4 10-5 100 120 130 150 60 70 120 150 I II III 90 110 130 170 Jika dibandingkan dengan waktu respons yang dibutuhkan ESI nitrat dengan prakondisi pada konsentrasi larutan standar 10-1 M lebih
dari 3 menit. Hal ini berarti kinerja ESI fosfat masih lebih cepat untuk membaca potensial yang terukur. Dari data waktu respons dapat disimpulkan bahwa elektrode II lebih cepat dari elektrode III dan elektrode III lebih cepat dari elektrode I.
Kinerja alami
peni gkatan hingga hari keempat, namun
rnst hari ke- (mV/dekade)
Umur Pakai
ESI fosfat awalnya meng n
setelah itu mengalami penurunan pada hari kelima dan hari ke-10 seperti yang terlihat pada Tabel 5 dan 6 dan Gambar 12 dan 13 (Lampiran 4).
Tabel 5 Nilai faktor Nernst ketiga ESI fosfat selama 10 hari Faktor Ne ESI 1 2 4 5 10 I 59,80 57,90 59,80 42,10 63,30 II 56,70 58,40 63,20 43,50 39,60 III 50,50 52,00 51,40 79,60 35,50
Tabel 6 Koefisien korelasi (r) ketiga ESI fosfat selama 10 hari
Koefisien korelasi (r) hari ke- (%) ESI 1 2 4 5 10 I 99,95 98,70 98,77 99,97 98,21 II 99,88 99,39 97,77 98,92 95,89 98,43 99,85 95,19 96,66 III 99,74
Umur pakai dari elektrode membran terlapis polimer dipengaruhi oleh hilangnya komponen-komponen membran seperti, ionofor, pemlastis, dan sebagainya (Oesch et
al. 1986). Dari Tabel 5 dan 6 dapat
disimpulkan bahwa ESI I memiliki nilai faktor Nernst dan koefisien korelasi (r) yang relatif tinggi hingga hari ke-10.
Penentuan Konsentrasi Fosfat pada Contoh Nutrisi Hidroponik ntr
dari E /dekade dan n kore (r) sebesar 99 5%. Nilai
dekati te . F
na merupakan acuan layak aknya ESI d igu
nsentra fosfat si o dite ukan dengan dua metode. Hal ini
tode baku (spektro an molibdat-vana
ESI yang dipilih untuk mengukur asi fosfat ESI I karena faktor konse yaitu
I 59,8 Nernst S
lasi mV nilai koefisie
ini men nilai oretis aktor Nernst,9 dipilih kare
tid apat d
si nakan. nutri Ko
nt hidr ponik
dilakukan untuk melihat kesamaan nilai konsentrasi dan ketelitian yang diberikan bila menggunakan metode ESI terhadap me
fotometri deng dat).
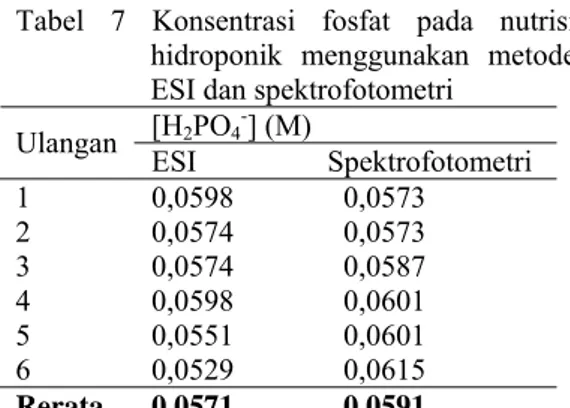
Konsentrasi fosfat pada nutrisi hidroponik menggunakan metode ESI memberikan nilai yang hampir sama dengan nilai konsentrasi bila menggunakan spektrofotometri seperti terlihat pada Tabel 7. Nilai rerata konsentrasi menggunakan metode ESI sebesar 0,0571 M sedangkan bila menggunakan spektrofotometri sebesar 0,0591 M.
Tabel 7 Konsentrasi fosfat pada nutrisi hidroponik menggunakan metode ESI dan spektrofotometri
[H2PO4-] (M)
Ulangan ESI Spektrofotometri 1 0,0598 0,0573 2 0,057 057 7 87 0 0 4 0, 0, 3 3 0,05 4 0,0594 050,06 1 5 0,0558 1 0,06 1 6 0,0529 0,0615 Rerata 0,0571 0,0591
Uji statistik yang digunakan untuk membandingkan kedua metode tersebut, yaitu menggunakan uji-t dengan pengambilan dua contoh bebas (Lampiran 6). Nilai konsentrasi dari kedua metode tersebut sama dengan diterimanya H0 (p = 0,256 > α = 0,05) pada
ngkat keperc , metode ESI fosfat dapat a penentuan kon
tersebut berbeda kare
luan yang rumit dibandingkan metode ESI fosfat yang jauh lebih sederhana
Me lebih murah
a karena ESI di aha ila ah wati umur pakainy nga ng ti membran da ba le . G ar ode dapat
hat p La n 8
da walaupun perlakuan pada etiganya sama dengan rerata faktor Nernst sebesar 55,67 an r sebesar 99,8
onsentrasi nutrisi hidroponik
pereaksi a tingkat
rca
r
Per ku en l n
ciri s n l .
yang rat lagi
and
sfat a m n p ek
ih ta a ti ayaan 95%. Jadi
digunakan pad
sentrasi fosfat dalam nutrisi hidroponik.
Penentuan ketelitian ESI fosfat diuji dengan uji keragaman (uji-F) (Lampiran 7). Ketelitian dari kedua metode
na diterimanya H1 (p = 0,331 > α = 0,05)
pada tingkat kepercayaan 95%. Jadi, ketelitian dari kedua metode tersebut dapat dianggap sama karena keragaman dari kedua metode hampir sama. Metode spektrofotometri lebih efisien karena memiliki nilai ragam yang lebih kecil (Lampiran 7) tetapi metode ini kurang praktis karena memerlukan perlakuan pendahu
(Hartaman 2007).
tode ESI fosfat dibandi
dapat ngkan metode lainnyperb a de rui bn hanya me sud ganmele pa dan e ktrode
a
amb elektr dili ada mpir .
SIMPULAN DAN SARAN
Simpulan
Kinerja ESI II lebih baik dari III dan I pada penentuan limit deteksi dan waktu respons namun ESI I memiliki faktor Nernst dan koefisien korelasi mendekati teoretis. Potensial elektrode yang dihasilkan dari ketiga ESI fosfat berbe
k
mV/dekade d
6%. Trayek pengukuran larutan standar dapat dilakukan pada kisaran konsentrasi 10-2
M sampai 10-5 M dengan rerata limit deteksi
konsentrasi sebesar 10,53 × 10-6 M. Waktu
respons ESI fosfat cukup singkat, yaitu kurang dari 3 menit. Umur pakai ESI fosfat selama 10
ari. Penentuan k h
metode ESI fosfat memberikan hasil yang sama dengan spektrofotometri menggunakan
molibdat-vanadat pad kepe yaan 95%.
Sa an lu dila
kan ke elektifakan p dari eelitian ektrodeanjuta Perlu untuk m
ditambahkan senyawa atau pencetak membran en agar ketiga membran memiliki permukaan
dan seragam. Perlu
a dicari
ingan komposisi membran untuk
perb ESI
fo gar me berika umur akai el trode leb han lam .
DAFTAR PUSTAKA
[AOAC] Association Official of Analytical Chemistry Chemistry. 1993. AOAC
Peer – Verified Methods Program.
USA: AOAC International.
Atikah. 1994. Pembuatan dan karakterisasi elektrode selektif nitrat tipe kawat na, Edi is untuk Ki et al embuatan elektrode l on C po oksida m
Stu a, Fakul matika dan Ilm ngetah Universitas Su ara.
rtaman Pencir nggunaan ele selektif itrat untuk
pe nu hidroponik
[skripsi]. Bogor: Fakultas Matematika
g? The importance of oxygen in
ultas Pertanian, IPB.
ai sumber hara budidaya caisin kultivar tosakan secara hidroponik [skripsi]. Bogor:
et al n ion-selective electrode perchlorate in
menggunakan ionofor DBA218C6. inar Nasional
FMIPA Un Indonesia. Depok.
. Ion selective electrode.
[terhubung berkala] http://www.en.wikipedia.org/wiki/Ion
terlapis [tesis]. Bandung: Program arja Studi Kimia, Program Pasca S ITB.
Buchari & Irdhawati. 2002. Pembuatan dan karakterisasi ESI nitrat tipe kawat terlapis membran PVC dengan dopan metiltrioktil amonium nitrat sebagai ionofor. Prosiding seminar kimia bersama UKM ITB K-5, Universiti Kebangsaan Malaysia, Bangi, Selangor. hlm 159-168.
Celuform. 2007. PVC the advantages. [terhubung berkala] http://
www.celuform.co.uk/celuform/pvc-adv.htm. [22 Agustus 2007]
oloegito W. 2005. Pengaruh pH terhadap kinerja elekroda selektif ion H2PO4
-menggunakan membran berpendukung PVC dengan aliquat
336. Seminar nasional MIPA
Universitas Hasanudin, Makassar. Fardiyah Q. 2003. Aplikasi elektrode selektif
ion nitrat tipe kawat terlap
penentuan secara tak langsung gas NO [tesis]. Bandung: Program Studi
mia, ITB. Gea S
seektif – i. 2005. Pu (II) dari kitosan – . : Progra lietilen Medan
di Kimi tas Mate
u Pe uan,
matra Ut
Ha L. 2007. ian dan pe ktrode ion n ngukuran trisi
dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lingga P. 1993. Hidroponik Tanam tanpa
Tanah. Jakarta: Penebar Swadaya.
Miller JC & Miller JN. 1999. Statistika untuk
Kimia Analitik. Ed Ke-2. Terjemahan
Suroso. Bandung: Penerbit ITB Morgan L. 2000. Are your plants suffocatin
hydroponic. The Growing Edge 12: 50-54.
Napitupulu L. 2003. Pengaruh aplikasi pupuk daun dalam sumber nutrisi berbeda pada teknologi hidroponik sistem terapung tanaman selada (Lactuca
sativa L. var. Garnd Rapids) [skripsi].
Bogor: Fakultas Pertanian, IPB.
Nurfinayati. 2004. Pemanfaatan berulang larutan nutrisi pada budidaya selada (Lactuca sativa L.) dengan tekniologi hidroponik sistem terapung [skripsi]. Bogor: Fak
Oesch U et al. 1986. Ion – selective membrane electrodes for clinical use. Clinical
Chemistry 32: 1448-1459.
Retariandalas. 2003. Pemanfaatan pupuk majemuk sebag
Fakultas Pertanian, IPB. Segui JM . 2006. A
for anion
thick-film technology. Valencia: Universidad Politécnica de Valencia. Soepardi G. 1983. Sifat dan Ciri Tanah.
Bogor: Fakultas Pertanian IPB. Soeseno S. 1999. Bisnis Sayuran Hidroponik.
Jakarta: Gramedia.
Strobel HA, Heineman WR. 1992. Chemical
Instrumentation: A Systematic Approach. Ed. Ke-3. New York: John
Wiley & Son.
Skoog A, Douglas. 1980. Preinciple of
Instrumental Analysis. Ed. Ke-3.
Philadelphia: Saunders.
Wahab et al. 2005. Pengaruh komposisi membran berpendukung PVC terhadap kinerja elektrode selektif ion (ESI)-Hg(II)
Sem
iversitas
Walpole RE. 1995. Pengantar Statistika. Ed Ke-3. Jakarta: Gramedia Pustaka Utama.
Wang, Joseph. 1994. Analytical
Electrochemistry. New York: VCH.
10
_ Feb
12
Pembuatan Elektrode
Pencirian ESI
Lampiran 1 Bagan alir metode penelitian
Pembuatan Larutan Untuk ESI
Pembuatan bad n elektrode a
Pelapisan membran pada kawat Pt
Penentuan faktor Ners dan trayek pengukuran t
Penentuan l it deteksi im
Penentuan Umur Pakai Penentuan waktu respon
13
y = -5,5714x + 369,57 r = 2,630% 0 50 100 150 200 E ( 250 300 350 400 450 0 2 4 6 8 -log [H2PO4-] m V) y = 59,8x + 111,2 r = 99,95% 0 100 20 30 400 500 0 1 2 3 4 5 6 -log [H2PO E ( m V) 0 0 4-] y = 14,75x + 226.14 r = 18,57% 0 50 100 150 200 250 300 0 0 0 2 4 6 8 -log [H2PO4-] E ( m V) 35 40 y = 56,7x + 44,8 r = 99,88% 0 50 100 150 E ( 200 250 0 1 2 3 4 5 6 -log [H2PO4-] m V) 300 350 y = 10.036x + 196.29 r = 21,11% 0 50 100 150 200 250 300 350 0 2 4 6 8 -log [H2PO4-] E ( m V) y = 50, 150 200 E ( m V) 5x + 44,5 r = 99,74% 0 50 100 250 300 350 0 1 2 3 4 5 6 -log [H2PO4-]ngukuran menggunakan empat
konentrasi dan tujuh konsentrasi
a)
b)
ambar 6 Kurva hubungan – log [H2PO4-] terhadap potensial (mV) menggunakan empat
konsentrasi (a) dibandingkan dengan menggunakan enam konsentrasi (b) pada ESI I.
a)
b)
ambar 7 Kurva hubungan – log [H2PO4-] terhadap potensial (mV) menggunakan empat
konsentrasi (a) dibandingka n enam konsentrasi (b) pada ESI II.
a)
b)
ambar 8 Kurva hubungan – log [H2PO4-] terhadap potensial (mV) menggunakan empat
konsentrasi (a) dibandingkan dengan menggunakan enam konsentrasi (b) pada ESI III.
Lampiran 2 Perbandingan kurva trayek pe
G
G n dengan menggunaka
G
14
y = 56,7x + 44,8 y = 11x + 263 0 50 100 150 200 250 300 350 400 450 500 0 2 4 6 8 -log [H2PO4-] E ( m V ) y = 44x + 68,5 y = -52x + 595 0 0 0 0 0 0 0 0 0 2 4 6 8 -log [H2PO4-] E ( m V ) 50 100 15 20 25 30 35 40 45 y = 59,8x + 111,2 y = 202x - 1000 0 50 100 0 0 0 0 2 4 6 8 -log [H2PO4 -] E ( m V)ambar 9 Kurva hubungan – log [H2PO4-] te
deteksi yaitu pada perpotongan garis
ambar 10 Kurva hubungan – log [H PO-] terhadap potensial (mV) yang menggambarkan
+
,7x + 44,8 = 11x + 263 x = 4,77 og [H2PO4-] = 4,77
[H2PO4-] = 1,68 x 10-5 M
ambar 11 Kurva hubungan – log [H2PO4-] terhadap potensial (mV) yang menggambarkan
limit deteksi yaitu pada perpotongan garis y = 56,7x + 44,8 dengan garis y = 11x + 263 pada ESI II.
imit deteksi konsentrasi pada ESI II: 50,5x + 44,5 = -52x + 595
x = 5,37 og [H2PO4-] = 5,37
[H2PO4-] = 4,26 x 10-6 M
Lampiran 3 Kurva penentuan limit deteksi pada ketiga ESI
15 20 25 300 350 400 450
G rhadap potensial (mV) yang menggambarkan limit
y = 59,8x + 111,2 dengan garis y = 11x + 263
pada ESI I.
G 2 4
limit deteksi yaitu pada perpotongan garis y = 56,7x + 44,8 dengan garis y = 11x 263 pada ESI II.
Li
56mit deteksi konsentrasi pada ESI II: -l G L -l
15
0 10 20 30 40 50 60 70 1 2 4 5 10 Hari ke-F akto r N e rn st (m V /d ekad e)Lampiran 4 Umur pakai dari ketiga ESI fosfat
95 96 97 98 99 100 1 2 4 5 Hari ke-r 101 10
ambar 13 Grafik hubungan antara koefisien korelasi (r) dan hari ke- dari umur ESI Gambar 12 Grafik hubungan antara faktor Nernst dan hari ke- dari umur ESI
(%
)
16
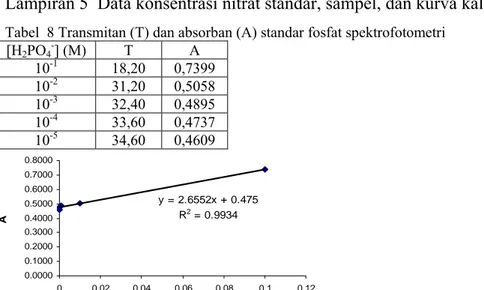
y = 56x + 226.5 R2 = 0.9971 0 100 200 300 400 500 600 0 1 2 3 4 5 6 -log [H2PO4-] E ( m V) y = 2.6552x + 0.475 R = 0.9934 0.3000 0.4000 2 0.0000 0.1000 0.2000 0.5000 0.6000 0.7000 0.8000 0 0.02 0.04 0.06 0.08 0.1 0.12 [H2PO4-] (M) Apel, dan kurva kalibrasi
abel 8 Transmitan (T) dan absorban (A) standar fosfat spektrofotometri
2PO4-] (M) T A
Lampiran 5 Data konsentrasi nitrat standar, sam
T [H 10-1 18,20 0,7399 10-2 31,20 0,5058 10-3 32,40 0,4895 10-4 33,60 0,4737 10-5 34,60 0,4609
Gambar 14 Kurva Kalibrasi standar fosfat menggunakan spektrofotometri
abel 9 Pengukuran konsentrasi fosfat contoh nutrisi hidroponik menggunakan spektrofotometri T A [H2PO4-] T X [x-X] [x-X]^2 (10-6) 23,60 0,6271 0,0573 0,0019 3,4821 23,60 0,6271 0,0573 0,0019 3,4821 23,20 0,6345 0,0601 0,0009 0,8649 23,20 0,6345 0,0601 0,0009 0,8649 23,00 0,6383 0,0615 0,0023 5,5043 Σ 0,3550 10,9410 23,40 0,6308 0,0587 0,0005 0,2247 0,0591 ragam (S2) = 1 n X X 2 − −
∑
=1
-6
10,9410
= 2,8846 x 10-6el 10 Potensial Elektrode (E) standar fosfat metode ESI fosfat
2PO4-] (M) -log [H2PO4-] E (mV) Tab [H 10-2 2 335 10-3 3 400 10-4 4 450 10-5 5 505
17
Lanjutan lampiran 5
guku konsen i fosfat contoh nutrisi hidroponik mengg Tabel 11 Pen
fosf
ran tras unakan metode ESI
at -lo O4 4 -] E g [H2P -] [H PO2 X Ix-XI Ix-XI^2 (10 -6 ) 295 1,2232 0,0598 0,0027 7,5458 296 1,2411 74 0,0003 0,1139 74 0,0003 0,1139 295 1,2232 0,0598 0,0012 1,4400 297 1,2589 0,0551 0,0020 3,9001 298 1,2768 0,0529 0,0571 0,0042 17,5900 Σ 0,3424 30,7040 0,05 296 1,2411 0,05 ragam (S2) = 1 n X X 2 − −
∑
=1
-6
30,7040
= 6,1408 x 10-6Lam an 6 U t dengan pengambilan dua contoh bebas un
SI dan
foto
Hipotesis:
H0 n fosfat etode sama
H1 n fosfat etode t a
Paired T for [H
2P
SI - [H
2PO
4-]Spektro
N Mean StDev SE Mean
[H
2PO
4
-]ESI 6 0.057067 0.002698 0.001101
pektro 6 0.059167 0.001695 0.000692
Difference 6 -0.002100 0.004013 0.001638
-Tes
ifference = 0 (vs not = 0): TValue =
-pir
ji-
tuk metode E
spektro
metri
= Nilai ko sentrasi kedua m
= Nilai ko sentrasi kedua m idak sam
O
4-]E
[H
2PO
4-]S
95% CI for mean difference: (-0.006312, 0.002112)
T
t of mean d
1.28 P-Value = 0.256
U
(
ntuk metode ESI dan spektrofotometri
Hipotesis:
H0 = Ketelitian kedua m de sama 1 = Ketelitian kedua m de tidak
est for Equal Variances: [H
2PO
4-]Spektro, [H
2PO
4-]ESI
5% Bonferroni confidence intervals for standard
eviations
N Lower StDev Upper
H
2PO
4
-]ESI 6 0.0015819 0.0026979 0.0077185
anjutan Lampiran 7
2 4
Lampi an 7
r
ji keragaman uji-F) u
eto eto sama H
![Tabel 1 Potensial elektrode untuk ESI I, II, dan III E (mV) [H (M 2 PO 4 - ] ) I II III Rerata SB SBR(%) 10 -1 403 354 251 336 77,58 23,09% 10 -2 10 -3 10 -4 10 -5 10 -6 10 -7 233 155 159 182,3 43,92 24,09% 288 220 206 238 43,86 18,43% 349 271](https://thumb-ap.123doks.com/thumbv2/123dok/2111950.3536367/15.892.147.469.154.346/tabel-potensial-elektrode-untuk-esi-iii-iii-rerata.webp)