3
II. TINJAUAN PUSTAKA
2.1
Jarak Pagar
Jarak pagar (Jatropha curcas L.) telah lama dikenal oleh masyarakat di berbagai daerah di Indonesia, yaitu sejak diperkenalkan oleh bangsa Jepang sekitar tahun 1942. Ketika itu masyarakat diperintahkan untuk menanam jarak pagar di pekarangan rumahnya. Jarak pagar tersebut kemudian diambil minyaknya untuk dimanfaatkan sebagai bahan bakar kendaraan untuk perang pada masa itu (Hambali et al. 2006).
Jarak pagar merupakan golongan pohon perdu dengan ketinggian mencapai 3 hingga 7 meter, dan memiliki cabang yang tidak teratur. Jarak pagar dapat tumbuh dengan baik pada daerah dengan ketinggian 0-1,700 m dpl dan suhu 19-38 oC. Kisaran curah hujan daerah penyebarannya bervariasi antara 200-2,000 mm/tahun, tetapi ada pula yang sampai lebih dari 4,000 mm/tahun. Secara umum jarak pagar dapat tumbuh pada daerah kurang subur (Hambali et
al. 2006).
Tanaman jarak pagar termasuk famili Euphorbiaceae. Klasifikasi tanaman jarak pagar adalah sebagai berikut.
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledone Ordo : Euporbiales Famili : Euphorbiaceae Genus : Jatropha
Spesies : Jatropha curcas Linn.
Jarak pagar memiliki buah berupa buah kotak berbentuk bulat telur dengan diameter 2 – 4 cm, berwarna hijau ketika masih muda dan kuning jika sudah masak. Buah terbagi menjadi tiga ruang, masing-masing ruang berisi satu biji. Bahan penyusun biji jarak pagar dapat dilihat pada Tabel 1. Biji jarak pagar berbentuk bulat lonjong, berwarna coklat kehitaman, dan mengandung banyak minyak (Sinaga 2006).
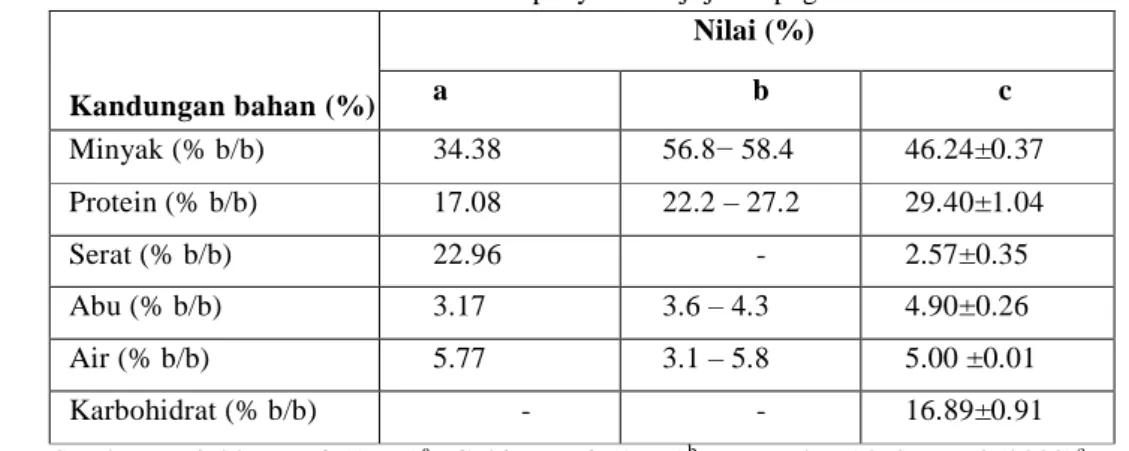
Tabel 1. Bahan penyusun biji jarak pagar
Kandungan bahan (%) Nilai (%) a b c Minyak (% b/b) 34.38 56.8− 58.4 46.24±0.37 Protein (% b/b) 17.08 22.2 – 27.2 29.40±1.04 Serat (% b/b) 22.96 - 2.57±0.35 Abu (% b/b) 3.17 3.6 – 4.3 4.90±0.26 Air (% b/b) 5.77 3.1 – 5.8 5.00 ±0.01 Karbohidrat (% b/b) - - 16.89±0.91
Sumber : Winkler et al. (1997)a ; Gubitz et al. (1999)b ; Peace dan Aladesanmi (2008)c
4
sebagian besar minyak atau lemak dengan rata-rata komposisinya 50% dari total asam lemak. Menurut Hamilton (1983) semakin tinggi jumlah asam lemak tak jenuh dalam suatu minyak, maka akan menyebabkan minyak tersebut semakin mudah teroksidasi. Komposisi asam lemak minyak jarak pagar dapat dilihat pada Tabel 2.
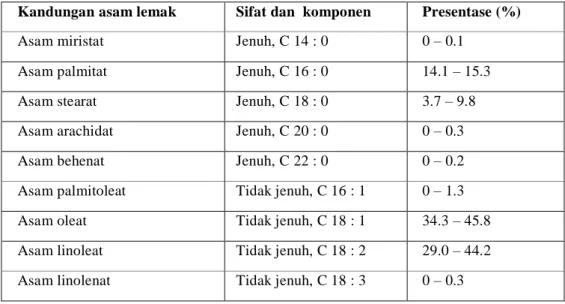
Tabel 2. Komposisi asam lemak minyak jarak pagar
Kandungan asam lemak Sifat dan komponen Presentase (%)
Asam miristat Jenuh, C 14 : 0 0 – 0.1
Asam palmitat Jenuh, C 16 : 0 14.1 – 15.3
Asam stearat Jenuh, C 18 : 0 3.7 – 9.8
Asam arachidat Jenuh, C 20 : 0 0 – 0.3
Asam behenat Jenuh, C 22 : 0 0 – 0.2
Asam palmitoleat Tidak jenuh, C 16 : 1 0 – 1.3
Asam oleat Tidak jenuh, C 18 : 1 34.3 – 45.8
Asam linoleat Tidak jenuh, C 18 : 2 29.0 – 44.2
Asam linolenat Tidak jenuh, C 18 : 3 0 – 0.3
Sumber: Gubitz et al. (1999)
Tanaman jarak pagar menghasilkan biji yang memiliki kandungan minyak cukup tinggi, sekitar 30 – 50%, sehingga sangat prospektif untuk digunakan sebagai bahan baku produk oleokimia seperti surfaktan. Kelebihan minyak jarak pagar apabila dibuat menjadi metil ester antara lain adalah minyak jarak pagar tidak termasuk kategori minyak makan (edible oil) sehingga pemanfaatannya tidak mengganggu penyediaan kebutuhan minyak makan. Minyak jarak pagar tidak dapat dikonsumsi manusia karena mengandung senyawa forbol ester dan cursin yang bersifat toksik (Hambali et al. 2006). Sifat fisikokimia minyak jarak pagar dapat dilihat pada Tabel 3.
Tabel 3. Sifat fisikokimia minyak jarak
Analisis Satuan Nilai
Kadar Airc % 0.07
Bilangan Asama mg KOH/g lemak 3.21±0.21
Bilangan Iodb mg iod/g lemak 96.5
Bilangan Penyabunana mg KOH/g lemak 198.5±0.5
Densitasa g/cm3 0.911
Sumber : Peace dan Aladesanmi (2008)a ; Hambali et al. (2006)b ; Gubitz et al. (1999)c
2.2
Surfaktan dan Kinerja Surfaktan
5
terserap ke dalam permukaan partikel minyak atau air sebagai penghalang yang akan mengurangi atau menghambat penggabungan (coalescence) dari partikel yang terdispersi.
Apabila surfaktan ditambahkan ke suatu cairan pada konsentrasi rendah, maka dapat mengubah karakteristik tegangan permukaan dan antarmuka cairan tersebut. Antarmuka adalah bagian dimana dua fasa saling bertemu atau kontak sedangkan permukaan yaitu antarmuka dimana satu fasa kontak dengan gas (biasanya udara). Sebagian besar surfaktan, pada tingkat 0.1% akan mengurangi tegangan permukaan air dari 72 menjadi 32 mN/m (dyne/cm). Hal ini terjadi karena molekul-molekul dalam sebagian besar cairan saling tertarik satu sama lain oleh gaya Van der Walls yang menggantikan ikatan hidrogen air (Hargreaves 2003). Pada Gambar 1 ditunjukkan bagaimana cara kerja surfaktan dalam menurunkan tegangan antarmuka dua cairan yang berbeda kepolarannya. Tarikan antar molekul akan terjadi pada dua cairan, dimana bagian kepala (hidrofilik) akan menarik lapisan air sedangkan bagian ekornya (hidrofobik) akan menarik lapisan minyak, sehingga air dan minyak dapat bercampur.
Gambar 1. Tarikan antar molekul di permukaan cairan (Nave 2009)
Tegangan permukaan dan tegangan antarmuka merupakan faktor penting pada berbagai aplikasi surfaktan. Aplikasi surfaktan pada industri sangat luas, contohnya yaitu sebagai bahan utama pada industri deterjen dan pembersih lainnya, bahan pembusaan dan emulsifier pada industri kosmetik dan farmasi (Hui 1996). Pemakaian terbesar surfaktan adalah untuk aplikasi pencucian dan pembersihan (washing and cleaning applications), namun surfaktan banyak pula digunakan untuk produk pangan, produk kosmetika dan produk perawatan diri, cat dan pelapis, kertas, tekstil, serta pertambangan (Flider 2001).
Menurut Shaw (1980) tegangan antarmuka merupakan faktor penting pada proses
enhanced oil recovery (EOR) dalam bidang pertambangan. Surfaktan dapat menurunkan tegangan
antarmuka antara fluida dengan fluida, fluida dengan batuan, dan fluida dengan hidrokarbon. Di samping itu, surfaktan dapat memecah tegangan permukaan dari emulsi minyak yang terikat dengan batuan (emulsion blocks), mengurangi terjadinya water blocking dan mengubah sifat kebasahan (wettability) batuan menjadi suka air (water wet). Dalam kondisi batuan yang bersifat
water wet, minyak menjadi fasa yang mudah mengalir dan dengan demikian water cut dapat
diturunkan.
Pada umumnya surfaktan dapat disintesis dari minyak nabati melalui senyawa antara metil ester dan alkohol lemak. Proses-proses yang dapat diterapkan untuk menghasilkan surfaktan diantaranya yaitu asetilasi, etoksilasi, esterifikasi, sulfonasi, amidasi, sukrolisis, dan saponifikasi (Sadi 1993). Produksi surfaktan dengan bahan baku metil ester dapat berasal dari minyak kelapa, stearin sawit, kernel sawit (PKO), dan lemak hewan (MacArthur dan Sheats 2002).
6
tersebut adalah surfaktan kationik, anionik, nonionik, dan amfoterik. Data jumlah konsumsi surfaktan dunia menunjukkan bahwa surfaktan anionik merupakan surfaktan yang paling banyak digunakan yaitu sebesar 50%, kemudian disusul nonionik 45%, kationik 4%, dan amfoterik 1% (Watkins 2001).
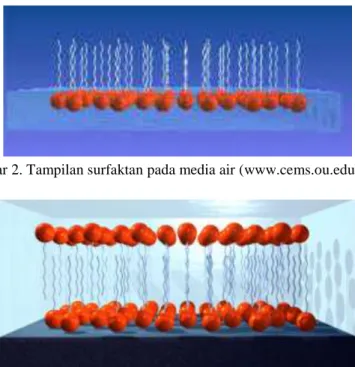
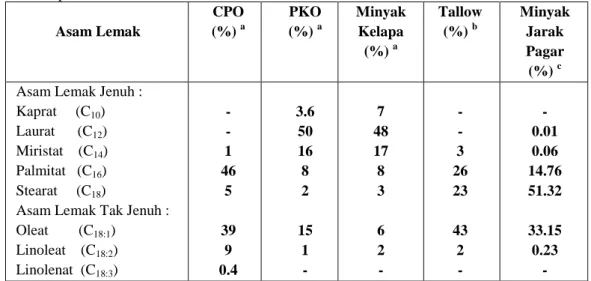
Pada Gambar 2 dapat dilihat bagaimana tampilan visual orientasi bagian kepala surfaktan pada media air karena sifatnya hidrofilik. Kemudian surfaktan tersebut saling berikatan hingga membentuk satu lapisan seperti terlihat pada Gambar 3.
Gambar 2. Tampilan surfaktan pada media air (www.cems.ou.edu 2009)
Gambar 3. Visualisasi surfaktan yang membentuk satu lapisan (www.cems.ou.edu 2009) Menurut Matheson (1996) surfaktan anionik mempunyai karakteristik hidrofilik akibat adanya gugus ionik yang cukup besar, yang biasanya berupa golongan sulfat atau sulfonat. Beberapa contoh surfaktan anionik yaitu linear alkilbenzen sulfonat (LAS), alkohol sulfat (AS), alkohol eter sulfat (AES), alfa olein sulfonat (AOS), parafin (secondary alkalene sulfonate, SAS) dan metil ester sulfonat (MES).
2.3
Metil Ester
Metil ester merupakan salah satu bahan oleokimia dasar yang merupakan turunan dari trigliserida (minyak atau lemak). Menurut Freedman et al. (1984) reaksi pembentukan metil ester melibatkan lemak atau asam lemak dengan alkohol rantai pendek seperti etanol atau metanol yang dipercepat dengan menggunakan katalis asam maupun katalis basa. Pada reaksi tersebut terjadi pemindahan alkohol menjadi alkohol lain dalam proses yang sama seperti hidrolisis. Jika pada reaksi ini alkohol yang digunakan adalah metanol, maka reaksinya disebut metanolisis dan ester yang dihasilkan berupa metil ester.
7
Transformasi kimia lemak mejadi metil ester melibatkan transesterifikasi spesies gliserida dengan alkohol membentuk alkil ester. Di antara beberapa alkohol yang mungkin digunakan, metanol disukai karena harganya lebih murah (Lotero et al. 2004; Meher et al. 2005).
Metil ester merupakan suatu senyawa yang mengandung gugus –COOR dengan R dapat membentuk alkil suatu ester. Suatu ester dapat dibentuk langsung antara suatu asam lemak dengan alkohol yang dinamakan dengan esterifikasi. Suatu asam karboksilat merupakan suatu senyawa organik yang mengandung gugus karboksil –COOH. Gugus karboksil mengandung sebuah gugus karbonil dan sebuah gugus hidroksil (Fessenden dan Fessenden 1982).
Minyak yang mengandung asam lemak bebas tinggi serta mengandung air lebih dari 0.3% dapat menurunkan rendemen transesterifikasi minyak (Freedman et al. 1984). Minyak dengan asam lemak bebas tinggi akan lebih efisien jika melalui dua tahap reaksi. Asam lemak bebas dalam minyak diesterifikasi dahulu dengan melibatkan katalis asam. Selanjutnya, transesterifikasi dapat dilakukan untuk mengkonversi sisa minyak atau trigliserida yang ada dengan melibatkan katalis basa (Canaki dan Gerpen 2001). Reaksi esterifikasi asam lemak dan alkohol mengkonversi asam lemak menjadi metil ester. Reaksi esterifikasi ditunjukkan seperti pada Gambar 4.
RCOOH + R’OH RCOOR’ + H2O
Asam Lemak Alkohol Ester Air
Gambar 4. Reaksi esterifikasi antara asam lemak dengan metanol (Hui 1996)
Dari Gambar 4 ditunjukkan bahwa kesetimbangan antara ester dan air akan tercapai pada reaksi esterifikasi apabila asam lemak (asam karboksilat) dan alkohol (metanol) dipanaskan dengan katalis asam. Reaksi kesetimbangan ini dapat digeser ke kanan dengan penambahan alkohol berlebih. Air yang terbentuk berasal dari gugus hidroksil asam dan hidrogen dari alkohol, artinya dalam reaksi esterifikasi tersebut gugus –OCH3 dari alkohol menggantikan gugus –OH
dari asam.
8
Gambar 5. Mekanisme reaksi esterifikasi antara asam lemak dan metanol dengan katalis asam (Hart et al. 2003)
Transesterifikasi merupakan suatu reaksi kesetimbangan. Untuk mendorong reaksi agar bergerak ke kanan sehingga dihasilkan metil ester maka perlu digunakan alkohol dalam jumlah berlebih atau salah satu produk yang dihasilkan harus dipisahkan. Proses transesterifikasi dipengaruhi oleh berbagai faktor tergantung kondisi reaksinya (Meher et al. 2005). Faktor tersebut diantaranya adalah kandungan asam lemak bebas dan kadar air minyak, jenis katalis dan konsentrasinya, perbandingan molar antara alkohol dengan minyak dan jenis alkoholnya, suhu dan lamanya reaksi, intensitas pencampuran dan penggunaan cosolvent organik. Bahan cosolvent yang digunakan sebaiknya tidak mengandung air dan semakin banyak jumlah cosolvent yang ditambahkan semakin baik karena akan meningkatkan kelarutan minyak. Contoh cosolvent yang baik adalah eter siklis seperti tetrahidrofuran (THF), 1,4-dioxane, dietil eter, metil tersier butil ester (MTBE) dan diisopropyl eter (Baidawi et al. 2009).
Kualitas metil ester dipengaruhi oleh: kualitas minyak (feedstock), komposisi asam lemak dari minyak, proses produksi dan bahan lain yang digunakan dalam proses dan parameter pasca-produksi seperti kontaminan (Gerpen et al. 2004). Kontaminan tersebut diantaranya adalah bahan tak tersabunkan, air, gliserin bebas, gliserin terikat, alkohol, FFA, sabun, residu katalis (Gerpen et
al. 1996).
9
RCOOCH2 CH2OH
RCOOCH + 3 CH3OH 3 RCOOCH3 + CHOH
RCOOCH2 CH2OH
Trigliserida Metanol Metil Ester Gliserol
Gambar 6. Reaksi transesterifikasi trigliserida dan metanol (Gerpen et al. 2004)
Pada Gambar 7 dapat dilihat bagaimana mekanisme transesterifikasi menggunakan katalis basa yang terdiri dari beberapa tahapan, yaitu diawali dari terjadinya reaksi basa dengan alkohol yang akan menghasilkan alkoksida dan katalis yang terprotonasi. Kemudian nukleofilik akan menyerang alkoksida pada gugus karbonil trigliserida membentuk molekul intermediet tetrahedral (reaksi 2), dari alkil ester dan anion digliserida terbentuk. Tahap selanjutnya protonasi katalis membentuk senyawa aktif (reaksi 4) yang dapat bereaksi dengan molekul alkohol untuk memulai alur proses katalis yang lain. Digliserida dan monogliserida dirubah melalui mekanisme yang sama untuk menghasilkan campuran alkil ester dan gliserol.
ROH + B RO– + BH– (1) R’COO–CH2 R’COO–CH2 | | R”COO–CH + –OR R”COO–CH OR (2) | | | H2C–OCR” H2C–O–C–R” || | O O– R’COO–CH2 R’COO–CH2 | |
R”COO–CH OR R”COO–CH + ROOCR” (3)
| | | H2C–O–C–R” H2C–O– | O– R’COO–CH2 R’COO–CH2 | | R”COO–CH + BH– R”COO–CH + B (4) | | H2C–O– H2C–OH
Gambar 7. Mekanisme transesterifikasi minyak dengan katalis basa (Schuchardt et al. 1998)
2.4
Metil Ester Sulfonat
10
Tabel 4. Komposisi asam lemak beberapa jenis minyak yang dapat digunakan sebagai bahan baku pembuatan MES Asam Lemak CPO (%) a PKO (%) a Minyak Kelapa (%) a Tallow (%) b Minyak Jarak Pagar (%) c
Asam Lemak Jenuh : Kaprat (C10)
Laurat (C12)
Miristat (C14)
Palmitat (C16)
Stearat (C18)
Asam Lemak Tak Jenuh : Oleat (C18:1) Linoleat (C18:2) Linolenat (C18:3) - - 1 46 5 39 9 0.4 3.6 50 16 8 2 15 1 - 7 48 17 8 3 6 2 - - - 3 26 23 43 2 - - 0.01 0.06 14.76 51.32 33.15 0.23 -
Sumber : a Hui (1996), b Watkins (2001), c Setyaningsih (2007)
Metil ester sulfonat (MES) merupakan surfaktan yang dihasilkan melalui proses sulfonasi metil ester (MacArthur et al. 1998). Metil ester dihasilkan melalui reaksi transesterifikasi antara trigliserida yang berasal dari minyak sawit, minyak kelapa, minyak jarak, atau lemak hewan dengan metanol.
Proses produksi surfaktan MES dilakukan dengan mereaksikan metil ester dengan agen sulfonasi. Menurut Bernardini (1983) dan Pore (1976), pereaksi yang dapat dipakai pada proses sulfonasi antara lain asam sulfat (H2SO4), oleum (larutan SO3 di dalam H2SO4), sulfur trioksida
(SO3), NH2SO3H, dan ClSO3H. Untuk menghasilkan kualitas produk terbaik, beberapa perlakuan
penting yang harus dipertimbangkan adalah rasio mol, suhu reaksi, konsentrasi grup sulfat yang ditambahkan, lama proses netralisasi, jenis dan konsentrasi katalis, pH dan suhu netralisasi (Foster 1996).
Pada Gambar 8 terlihat bahwa peluang terikatnya SO3 pada molekul asam lemak untuk
pembuatan MES dapat terjadi pada tiga sisi yaitu (1) gugus karboksil; (2) bagian α-atom karbon; (3) rantai tidak jenuh (ikatan rangkap).
H H H O | | | || H---C---C---CH = CH---C---CH2---C 1 | | | | H H H OH 3 2
11
adalah rasio mol reaktan, suhu rekasi, konsentrasi grup sulfat yang dihasilkan (SO3, NaHSO3,
atau asam sulfit), waktu netralisasi, pH, dan suhu netralisasi (Foster 1997).
Mekanisme reaksi yang terjadi selama reaksi sulfonasi dapat dijelaskan pada Gambar 9 berikut. Urutan proses yang terjadi adalah metil ester (I) bereaksi dengan gas SO3 membentuk
senyawa intermediet (II), pada umumnya berupa senyawa anhidrad. Dalam kondisi reaksi yang setimbang, senyawa intermediet (II) tersebut akan mengaktifkan gugus alfa (α) pada rangkaian gugus karbon metil ester sehingga membentuk senyawa intermediet (III). Selanjutnya, senyawa intermediet (III) tersebut mengalami restrukturisasi dengan melepaskan gugus SO3. Gugus SO3
yang dilepaskan bukanlah gugus yang terikat pada ikatan alfa. Dengan terlepasnya gas SO3
selama proses post digestion tersebut, maka terbentuklah MESA (IV).
O O
|| ||
R – CH2 – C – OCH3 (I) + SO3 R – CH2 – (C – OCH3): SO3 (II)
O O || ||
R – CH2 – (C – OCH3): SO3 (II) + SO3 R – CH– (C – OCH3): SO3 (III)
| SO3H
O O
|| ||
R – CH– (C – OCH3): SO3 (III) R – CH– C – OCH3 (IV)+ SO3
| |
SO3H SO3H
Gambar 9. Mekanisme reaksi pembentukan MESA (MacArthur et al. 2002)
2.5
Proses Aging
Proses aging merupakan proses pemaparan suatu bahan pada kondisi lingkungan tertentu sehingga menyebabkan perubahan sifat-sifat bahan dari kondisi semula. Ada beberapa faktor yang dapat mempengaruhi proses aging antara lain faktor kondisi lingkungan, mekanisme degradasi kritis dan akselerasi aging. Kondisi lingkungan antara lain pemanasan dan kelembaban, sedangkan mekanisme degradasi kritis merupakan fakta bahwa semua sistem emulsi rentan terhadap serangkaian faktor lingkungan. Oleh karenanya akselerasi aging merupakan proses yang diperlukan untuk mendapatkan mekanisme tertentu sehingga diperoleh perubahan yang sama dengan kondisi sebenarnya, namun dalam waktu yang lebih singkat. Dalam hal ini yang menjadi pembatas dalam proses aging MESA yaitu mekanisme aging pada kondisi lingkungan tertentu untuk terjadinya perubahan struktur, namun tidak mengarah pada degradasi produk (Gates dan Grayson 1998).
Proses aging merupakan tahapan proses yang tidak terlepas dari proses sulfonasi pada reaktor falling film, yaitu kelebihan SO3 terhadap metil ester harus tetap terjaga untuk
12
ini diduga hasil polimerisasi dari senyawa hasil degradasi pada suhu tinggi yang banyak
mengandung SO3.
Pada tahapan aging dimana senyawa intermediet bereaksi dan konversi Metil Ester menjadi produk sulfonasi berjalan sempurna. Tahapan aging MESA lebih intensif dibandingkan tahapan aging linier alkylbenzene (LAB) dimana memerlukan suhu sekurang-kurangnya 80 ⁰C. Waktu tinggal (aging) yang diperlukan tergantung pada temperatur yang digunakan, rasio mol SO3 terhadap Metil Ester, target konversi dan karakteristik reaktor. Pada reaktor batch atau pada
PFR ideal dan rasio mol 1.2, membutuhkan 45 menit pada 90 ⁰C atau 3.5 menit pada 120 ⁰C yang memberikan tingkat konversi 98%. Pada tangki reaktor kontinyu berpengaduk (CSTR) ideal, waktu aging memerlukan dua kali lipat. Biasanya tahapan ini dilaksanakan pada reaktor kontinyu yang mempunyai karakteristik antara PFR ideal dan CSTR ideal.
Secara teoritis, proses aging menghasilkan sebagian besar produk MESA
(RCH(SO3)COOCH3) dan sisa campuran anhidrida (RCH(SO3)COOSO3CH3). MESA jika
dinetralkan maka akan menghasilkan MES (reaksi 1). Sedangkan campuran anhidrida ini jika langsung dinetralkan dengan NaOH maka akan menyebabkan terbentuknya disalt dan sodium
metil sulfat (reaksi 2). Oleh karena itu untuk meningkatkan yield MES maka campuran anhidrida
ini harus direaksikan dengan metanol untuk reesterifikasi membentuk MESA sehingga jika dinetralkan dengan metanol akan dihasilkan MES (reaksi 3). Demikian pula menurut MacArthur
et al. (1999) bahwa untuk menghindari terbentuknya disalt dilakukan proses aging pasca
sulfonasi pada reaktor falling film dan penambahan metanol sebelum netralisasi. Reaksi selengkapnya mengenai hal tersebut di atas disajikan pada Gambar 10.
Reaksi 1...
O O
|| ||
R – CH– C – OCH3 (IV) + NaOH R – CH– C – OCH3 (VI) + H2O
| |
SO3H SO3Na
Reaksi 2...
O O
|| ||
R – CH– (C – OCH3): SO3 (III) + 3NaOH R – CH– C – ONa (V) + 2H2O + CH3OSO3Na
| | SO3H SO3Na
Reaksi 3...
O O
|| ||
R – CH– (C – OCH3): SO3 (III) + CH3OH R – CH– C – OCH3 (IV)+ CH3OSO3H
| |
SO3H SO3H