78
PENENTUAN STRUKTUR SENYAWA
COUMARINOLIGNAN
PADA FRAKSI
DIKLOROMETANA KULIT BATANG DURIAN KLAWING (
Durio graveolens
Becc.)
Yoga Pratama1*, Rudiyansyah1, Harlia1 1
Program Studi Kimia, Fakultas MIPA Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi, *Email: pratamayoga41@yahoo.co.id.
ABSTRAK
Durian klawing (D. graveolens Becc.) merupakan tumbuhan durian yang menghasilkan daging buah berwarna merah dan pada tiap ruasnya memiliki satu buah biji. Tumbuhan durian ini merupakan salah satu tumbuhan endemik di Kalimantan. Tujuan penelitian adalah untuk mengisolasi, memurnikan, dan menentukan struktur senyawa coumarinolignan dari fraksi DCM kulit batang D. graveolens Becc. Isolat yang dihasilkan berbentuk kristal jarum bening sebanyak 14 mg. Penentuan struktur senyawa menggunakan NMR-H1, NMR-C13, COSY, HSQC, dan HMBC. Data spektrum NMR-1H isolat YGP22 -21O (C 0.075; (CH3)2CO) (CD3OD, 500 MHz)
δ (ppm), HRMS-ESI-TOF m/z: 401.0510 [M+H]- (C 20H19O9): 7,88 (1H, d, J = 9,55 Hz, H-3); 6,30 (1H, d, J = 9,5 Hz, H-4); 6,80 (1H, s, H-5); 6,60 (1H, d, J = 1,25 Hz, H-2’); 6,62 (1H, s, H-6’); 4,95 (1H, d, J= 8 Hz, H-7’); 4,14 (1H, t, J= 4,1 Hz, H-8’); 3,55 (1H, dd, J=12,65; 3,85 Hz, H-9’); 3,86 (1H, d, 3’-OMe); 3,84 (1H, s, 5’-OMe); 13C-NMR(CD 3OD, 500 MHz) δ (ppm): 146,3(C3); 114,0(4); 101,9(C5); 109,554(C2’); 104,1(C6’); 78,2(C7’); 79,9(C8’); 61,7(C9); 56,8(3’-OMe); 56,6(5’OMe). Berdasarkan data dan kajian literatur isolat YGP22 adalah daphnecin.
Kata Kunci: coumarinolignan, D. graveolens Becc., daphnecin, durian
PENDAHULUAN
Kalimantan merupakan pulau yang memiliki hutan dengan keanekaragaman tergolong tertinggi di dunia. Tumbuhan durian (Durio) sangat subur tumbuh di tanah Kalimantan, dan berdasarkan literatur terdapat 19 spesies tumbuh di Kalimantan dari 28 spesies yang telah ditemukan (Uji, 2004; 2005).Tumbuhan durian termasuk famili Malvaceae. Famili Malvaceae terdiri dari 243 genus dan 4300 jenis. Sebagian besar tumbuhan famili Malvaceae diketahui memiliki kandungan senyawa golongan fenol (Hardiana R., 2012).
Sejumlah penelitian terhadap spesies durian yang telah dilakukan kandungan fenolik antara lain, yaitu, D. kutejensis, D. zibethinus, D. oxleyanus, dan D. affinis Becc. Pada durian spesies D. kutejensis, D. zibethinus, D. affinis Becc., dan D. oxleyanus telah ditemukan senyawa turunan kumarin seperti fraksidin dan skopoletin (Rudiyansyah dkk, 2015; Saziati O., 2010).
Penelitian tentang kandungan kimia pada kulit batang D. graveolens khususnya senyawa fenolik sampai sekarang belum
dilaporkan. Oleh karena itu, perlu dilakukan penelitian kandungan metabolit sekunder terhadap kulit batang D. graveolens dari fraksi diklorometan (DCM). Hasil penelitian ini diharapkan dapat mengungkap kandungan senyawa metabolit sekunder khususnya turunan kumarin untuk dapat menambah referensi baru mengenai senyawa golongan fenol yang terdapat pada durian.
METODOLOGI PENELITIAN Alat dan Bahan
Alat-alat yang digunakan diantaranya alat gelas, alat evaporasi, peralatan kromatografi, spektroskopi NMR BRUKER-500 MHz dan MS Waters LCT Premier XE HRMS ESI-TOF.
Bahan-bahan yang digunakan adalah berbagai jenis pelarut organik, kulit batang durian klawing (D. graveolens Becc.) pereaksi uji fitokimia, reagen serium sulfat 5%, plat KLT silika gel 60 F254, silika gel 60
(60-70 mesh), silika gel 60 (230-400 mesh), silika gel 60 GF254.
79 Prosedur Kerja
Preparasi Sampel Kulit Batang Durian Klawing
Sampel kulit batang durian klawing (D. graveolens Becc.) dibersihkan dari jamur dan lumut, dipotong-potong kemudian dikeringkan dalam ruangan. Sampel yang telah bersih kemudian diserbukkan di Workshop of Wood Fakultas Pertanian Universitas Tanjungpura Pontianak.
Maserasi dan Partisi
Sebanyak 3,7 kg serbuk kulit batang durian klawing dimaserasi dengan metanol yang telah didestilasi selama 3x24 jam pada suhu kamar. Maserat kemudian disaring, fitrat yang diperoleh diuapkan pelarutnya menggunakan rotary evaporator sehingga diperoleh 406,779 g (rendemen 10,99 %) maserat kental metanol.
Maserat kental metanol dipartisi berturut-turut dengan n-heksana dan diklorometan, sehingga diperoleh fraksi n -heksana, diklorometan dan metanol. Fraksi diklorometan dipekatkan menggunakan rotary evaporator diperoleh 6,53 g (rendemen 1,60 %) fraksi diklorometan. Uji Fitokimia
Uji
fitokimia
dilakukan
terhadap
masing-masing
fraksi
untuk
mengidentifikasi adanya senyawa golongan
fenolik. Tiap fraksi ditambahkan pereaksi
FeCl
3untuk identifikasi golongan senyawa
fenol dengan penandaan warna kuning
kehijauan.
Fraksinasi dan Pemurnian
Fraksi dikloroform (6,53 g) difraksinasi dengan KCV tahap I. Sampel dielusi dengan kombinasi pelarut bergradien n -heksana 100%, n-heksana:EtOAc (9:1), (8:2), (7:3), (6:4), (1:1), (4:6); (3:7), (2:8), (1:9), EtOAc 100%, dan MeOH 100%. Fraksi gabungan yang didapatkan sebanyak 11 fraksi (Y1-Y11). Fraksi Y10 (0,90 g) dengan pola pemisahan yang baik dan massa yang besar dipilih untuk dilakukan pemurnian pada KVC tahap II. Fraksi Y10 (0,90 g) dielusi dengan eluen DCM: EtOAc (7:3); (1:1); (3:7); (1:9); EtOAc
100%, dan MeOH 100%, sehingga diperoleh 6 fraksi (YG1-YG6). Fraksi YG2 (0,83 g) dengan pola pemisahan kromatogram yang baik dan dipilih untuk dilakukan pemurnian ke tahap KKG.
Fraksi YG2 (0,83 g) dilakukan pemurnian menggunakan KKG dan dielusi menggunakan kombinasi eluen bergradien dari hasil analisis KLT yaitu DCM:EtOAc (4:6); (3:7); (2:8); (1:9), EtOAc 100%, dan MeOH 100%, sehingga diperoleh 44 fraksi (YGP1-YGP44). Fraksi YGP22 menghasilkan 14 mg kristal jarum bening. Uji kemurnian dilakukan dengan KLT satu dimensi menggunakan kombinasi eluen DCM:EtOAc (1:1), n-heksana:EtOAc (3:7), DCM:MeOH (95:5), yang menunjukkan kemurnian yang cukup tinggi.
HASIL DAN PEMBAHASAN
Uji Isolasi Golongan Senyawa Isolat YGP22
Uji fitokimia dilakukan pada fraksi DCM dengan menggunakan uji FeCl3. Uji FeCl3
digunakan untuk menandakan positif kandungan senyawa fenol dengan terbentuknya warna hijau kehitaman seperti yang ditunjukkan pada GAMBAR 1.
Gambar 1. Uji fenol dengan FeCl3 Karakterisasi Struktur Senyawa
Fraksi diklorometan dari hasil ekstraksi kulit batang durian klawing (D. graveolens) telah melalui tahap fraksinasi dan pemurnian menggunakan serangkaian alat kromatografi untuk mendapatkan isolat YGP22 (GAMBAR 2). Struktur isolat YGP22 ditentukan melalui spektroskopi NMR-H, dan NMR-C13, serta NMR 2 dimensi HSQC, COSY, HMBC, dan MS.
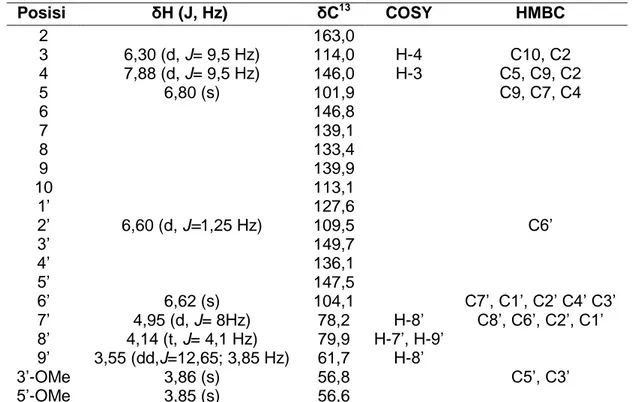
80 Tabel 1. Data Spektrum Isolat YGP22
Posisi δH (J, Hz) δC13 COSY HMBC 2 163,0 3 6,30 (d, J= 9,5 Hz) 114,0 H-4 C10, C2 4 7,88 (d, J= 9,5 Hz) 146,0 H-3 C5, C9, C2 5 6,80 (s) 101,9 C9, C7, C4 6 146,8 7 139,1 8 133,4 9 139,9 10 113,1 1’ 127,6 2’ 6,60 (d, J=1,25 Hz) 109,5 C6’ 3’ 149,7 4’ 136,1 5’ 147,5 6’ 6,62 (s) 104,1 C7’, C1’, C2’ C4’ C3’ 7’ 4,95 (d, J= 8Hz) 78,2 H-8’ C8’, C6’, C2’, C1’ 8’ 4,14 (t, J= 4,1 Hz) 79,9 H-7’, H-9’ 9’ 3,55 (dd,J=12,65; 3,85 Hz) 61,7 H-8’ 3’-OMe 3,86 (s) 56,8 C5’, C3’ 5’-OMe 3,85 (s) 56,6
TABEL 2. Perbandingan data δ spektrum NMR-1H dan NMR-13C dari senyawa Daphnecin pelarut C5D5N dan isolat YGP22 pelarut CD3OD
Isolat YGP22 Daphnecin
Posisi δH (mult., J, Hz) δC δH (mult., J, Hz) δC
2 163,0 160,5 3 6,30 (d, J= 9,5) 114,0 6,38 (d, J=9,5) 113,3 4 7,88 (d, J= 9,5) 146,0 7,70 (d, J=9,5) 144,5 5 6,80 (s) 101,9 6,62 (s) 101.5 6 146,8 145,5 7 139,1 136,8 8 133,4 131,4 9 139,9 144,3 10 113,1 113,7 1’ 127,6 126,6 2’ 6,60 (d, J=1,25) 109,5 7,18 (s) 106,4 3’ 149,7 147,9 4’ 136,1 138,5 5’ 147,5 147,9 6’ 6,62 (s) 104,1 7,18 (s) 106,4 7’ 4,95 (d, J= 8) 78,2 5,59 (d, J=7,9) 77,9 8’ 4,14 (t, J= 4,1) 79,9 4,43 (m) 80,1 9’ 3,55 (dd,J=12,65; 3,85) 61,7 4.31 (dd, J=12.7; 7.5) 3.96 (dd, J=12.7; 3.5) 60,8 3’-OMe 3,86 (s) 56,8 3,81 (s) 56,5 5’-OMe 3,85 (s) 56,6 3,81 (s) 56,5
81 Isolat YGP22 yang didapatkan berupa padatan kristal jarum sebanyak 14 mg, formula kimianya C20H18O9 menunjukan
puncak pada HRMS-ESI-TOF m/z: 401.0510 [M+H]-. Pada NMR-C13 isolat YGP22 memiliki 10 karbon kuarterner, 7 karbon metin, 2 metil, dan 1 metilen. Spektrum H-NMR menggunakan pelarut CD3OD menunjukan dua sinyal karakteristik
untuk struktur kumarin pada geseran kimia δ 7,88(H4) dan δ 6,30(H3) (d, J= 9,5 Hz). Kedua geseran kimia proton tersebut menunjukan adanya sistem alkena yang tersubtitusi pada cincin benzena.
Menurut Yeon dkk (2005), pada geseran kimia sekitar δ 7,88(H4) dan δ 6,30(H3) dengan nilai kopling (J) 9,5 Hz menunjukan inti kumarin. Terdapat sinyal metin aromatik pada δ 6,80(H5); δ 6,62 (H6’); dan δ 6,60 (H2’). Sinyal pada geseran δ 4,95(H7’) adalah untuk proton oxybenzil dan δ 4,14 (H8’) menunjukan adanya proton oxy metin
(Yeon dkk, 2005
). Kedua sinyal tersebut dan geseran δ 3,55 (H9’) menurut Bong-Sik dkk (2001) adalah bagian propanoid (CH3-CH(-O-)-CH(-O-)-). Padaspektrum ini juga terdapat dua gugus metoksi (-OCH3) yang berada digeseran δ 3,86; dan δ 3,84.
Spektrum C13-NMR menunjukan adanya lima sinyal untuk karbon metin (δ 146,3(C4); 114,0(C3); 109,5(C2’); 104,1(C6’); 101,9(C5)) dan sepuluh karbon kuarterner (δ 163,0(C2); 149,7(C3’); 147,5(C5’); 146,8(C6); 139,9(C9); 139,1(C7); 136,1(C4’); 133,4(C8); 127,6(C1’); 113,1(C10)). Informasi lainnya menunjukan adanya dua gugus CH-O (δ 78,2(C7’); 79,9(C8’)), sinyal gugus C-OH (δ 61,7(C9’)), dan dua gugus metoksi (δ 56,8(3’-OMe); 56,6(5’-OMe)) (Syah 2016). Hasil dari H-NMR dan C-NMR memberikan informasi sinyal gugus metin masing-masing berintegrasi 1H (δ 146,3(C3); 114,0(C4); dan 101,9(C5)) menunjukan keberadaan karbon yang terikat pada proton δ 7,88(H4); δ 6,30(H3); dan δ 6,80(H5). Satu gugus karbon kuarterner δ 146,8(C6) berikatan dengan gugus hidroksil (OH), dan dua gugus karbon kuarterner δ 133,4(C8); dan δ 139,9(C9) berikatan dengan oksigen dari proton oxybenzil dan proton oxy metin.
Unit separuh lignan C6C3 ditunjukkan
melalui informasi pembentukan cincin aromatik (unit C6) dari 2 gugus metoksi
pada geseran δ 3,86; dan δ 3,84. Dua gugus metoksi δ 3,86 (δ 56,8); dan δ 3,84 (δ 56,6) berikatan dengan karbon kuarterner δ 149,7(C3’); 147,5(C5’). Sinyal gugus metin berintegrasi 1H (δ 109,5(C2’); dan 104,1(C6’)) menunjukan keberadaan karbon yang terikat pada proton δ 6,62 (H6’); dan δ 6,60 (H2’). Satu gugus karbon kuarterner δ 136,1(C4’) berikatan dengan gugus hidroksil (OH) dan satunya lagi δ 127,6(C1’). Grup ini membentuk 3’,5’-dimetoksi-4’hidroksifenil dan terikat dengan bagian propanoid (CH3-CH(-O-)-CH(-O-)-)
(unit C3).Berdasarkan TABEL 2 didapatkan informasi bagian propanoid (CH3
-CH(-O-)-CH(-O-)-) melalui sinyal pada geseran δ 4,95(H7’) memiliki proton oxybenzil dan δ 4,14 (H8’) menunjukan adanya proton oxy metin integrasi 1H (δ 78,2(C7’); dan 79,9(C8’)) bersama geseran δ 3,55 (H9’) integrasi 2H (δ 61,7(C9’)) yang berikatan dengan hidroksil (OH). Kerangka kumarin (C6C3) dan separuh lignan (C6C3)
dihubungkan oleh cincin benzodioxan sehingga terbentuk senyawa coumarinolignan (Bong-Sik dkk, 2001).
Gambar 2. Struktur isolat YGP22 Senyawa daphnecin pertama kali ditemukan oleh Rasool M.A dkk (2010) dari spesies Daphne mucronate, ordo Malvales, famili Thymelaeaceae. Hasil geseran kimia pada TABEL 2 menunjukan banyak kemiripan. Perbedaan yang dihasilkan karena penggunaan pelarut berbeda. Daphnecin yang telah ditemukan menggunakan pelarut C5D5N sedangkan
isolat YGP22 yang ditemukan pada penelitian ini menggunakan pelarut CD3OD.
Hasil perbandingan menunjukan banyak kesamaan. Pada NMR-C13 senyawa isolat YGP22 dan dephnecin sama-sama memiliki 10 karbon kuarterner, 7 karbon
O O O O H O OH OH H3CO OCH3 2 3 4 5 6 7 8 9 1' 2' 3' 4' 5 ' 6' 7' 8' 9' 10
82 metin, 2 metoksi, dan 1 metilen. Hasil HMBC (TABEL 1) menunjukan adanya bagian propanoid CH(O)CH(O)CH2OH dan kerangka kumarin pada sinyal proton δ 4,95 yang berkorelasi dengan δ 79,9(C8’), δ 104,1(C6’), dan δ 109,5(C2’), sehingga diketahui urutan 3 karbon pembentuk struktur 3’,5’-dimetoksi-4’hidroksifenil. Spektrum COSY menunjukan adanya hubungan proton δ 4,14 dengan proton δ 4,95, dan δ 3,55 membentuk propanoid (CH3-CH(-O-)-CH(-O-)-). Korelasi pada
HMBC dan COSY dapat dilihat pada GAMBAR 3. Pada posisi C7’ dan C8’ menunjukan konstanta kopling J= 8 Hz yang menandakan stereokimia trans. Nilai putaran optik isolat YGP22 -21O (C 0.075; (CH3)2CO) sedangkan daphnecin
+ 2(C 0.3 ; (CH3OH)).
Gambar 3. Korelasi 1H-1H COSY dan HMBC untuk senyawa
daphnecin
SIMPULAN
Hasil dari penelitian ini didapatkan senyawa daphnecin berbentuk kristal jarum bening sebanyak 14 mg dari fraksi DCM durian klawing (D. graveolens Becc). Penemuan senyawa daphnecin pertama kali dilaporkan pada genus Durio, sehingga membuka pengetahuan keberadaan senyawa coumarinolignan pada genus Durio.
DAFTAR PUSTAKA
Arum, Y. P., Supartono, Sudarmin, 2012, Isolasi dan Uji Daya Antimikroba Ekstrak Daun Kersen (Muntingia Calabura), Jurnal MIPA 35
(2):165-174 (2012), ISSN 0215-9945, UNNES
Bong-Sik Yun, In-Kyoung Lee, In-Ja Ryoo dan Ick-Dong Yoo, 2001, Coumarins with Monoamine Oxidase Inhibitory Activity and Antioxidative Coumarino-lignans from Hibiscus syriacus. J Nat Prod 64: 1238
Hardiana R., 2012, Aktivitas Antioksidan Senyawa Golongan Fenol dari Beberapa Jenis Tumbuhan Famili Malvaceae, Jurnal Kimia Khatulistiwa, Vol 1 No 1 hal 8-13 Rasool M.A., Khan R., Malik A., Bibi N., dan
Kazmi S.U., 2010 Structural Determination of Daphnecin, a New Coumarinolignan from Daphne macronata, Journal of Asian Natural Product Research, Vol 12 No 4 hal 324-327
Rudiyansyah; Panthong, K.. dan Garson, M.J., 2015, Chemistry and Pharmacognosy of the Genus Durio, Natural Product Communications Vol. 10 (11) Saziati, O., 2010, Penentuan Struktur
Senyawa Kumarin dari Fraksi Kloroform Kulit Batang Durian Burung (Durio affinis Becc.), Universitas Tanjungpura, Fakultas Matematika dan Ilmu Pengetahuan Alam, Pontianak, (Skripsi).
Syah Y. M., 2016, Dasar-dasar Penentuan Struktur Molekul Berdasarkan Data Spektrum 1H & 13C NMR, Perpustakaan Nasional RI. Data Katalog dalam Terbitan
Uji, T., 2004, Keanekaragaman Jenis, Plasma Nutfah dan Potensi Buah-buahan Asli Kalimantan, Herbarium Bogoriense, Bidang Botani, Pusat Penelitian Biologi- LIPI, Bio Smart, 6: 117-125.
Uji, T., 2005, Keanekaragaman Jenis dan Sumber Plasma Nutfah Durian (Durio spp.) di Indonesia, Buletin Plasma Nutfah, 11: 28-33.
Yeon, K.S., Ming, H.L., dan Yong, N.H., 2005, A New Antisepsychotic Effective Neolignan from Firmiana Simplex, Arch Pharm Res Vol 28, No 1, 34-38 O O O OH H3CO OCH3 OH O O H H H H H H H H H COSY HMBC