UJI BARFOED
Diajukan Untuk Memenuhi Persyaratan Praktikum Biokimia Pangan
Oleh :
Nama : Giffary Pramafisi S. NRP : 123020077
Kel/Meja : C/10
Asisten : Rayi Annisa T. Tgl. Percobaan : 18 Maret 2014
LABORATORIUM BIOKIMIA PANGAN
JURUSAN TEKNOLOGI PANGAN
FAKULTAS TEKNIK
UNIVERSITAS PASUNDAN
BANDUNG
2014
I PENDAHULUAN
Bab ini akan menguraikan mengenai (1) Latar belakang percobaan (2) Tujuan Percobaan (3) Prinsip Percobaan, dan (4) reaksi Percobaan.
1.1. Latar Belakang Percobaan
Karbohidrat dalam alam memiliki beberapa turunan-turunan dan salah satunya adalah monosakarida yang merupakan gula paling sederhana. Kandungan monosakarida dalam bahan pangan tidaklah sedikit. Untuk mengetahui adanya monosakarida pereduksi yang terdapat dalam bahan makanan maka dilakukan uji Barfoed ini.
1.2. Tujuan Percobaan
Tujuan uji Barfoed ini adalah untuk mengetahui adanya monosakarida pereduksi dalam bahan pangan.
1.3. Prinsip Percobaan
Prinsip dari uji Barfoed ini adalah berdasarkan kepada adanya gugus karbonil bebas yang mereduksi Cu2+ dalam
suasana asam membentuk Cu2O (endapan merah bata). 1.4. Reaksi Percobaan
R– C– H + Cu2+ Cu2O + R– C– OH
II METODE PERCOBAAN
Bab ini akan menguraikan tentang (1) Bahan yang digunakan, (2) Pereaksi yang digunakan, (3) Alat yang digunakan, dan (4) Metode percobaan.
2.1. Bahan Yang Digunakan
Bahan yang digunakan dalam percobaan uji Barfoed ini adalah Larutan Barfoed, dan sampel yang akan dianalisis kandungan monosakarida pereduksinya.
2.2. Pereaksi Yang Digunakan
Pereaksi yang digunakan dalam uji Barfoed ialah Larutan Barfoed yang terdiri dari 13.3 gram Cu-asetat dalam 200 mL ditambah 1.9 mL asam asetat glacial.
2.3. Alat Yang Digunakan
Peralatan yang digunakan pada uji Barfoed ini antara lain (1) tabung reaksi sejumlah sampel yang digunakan, (2) pipet tetes sejumlah sampel yang akan dianalisis, dan (3) Waterbath untuk pemanasan
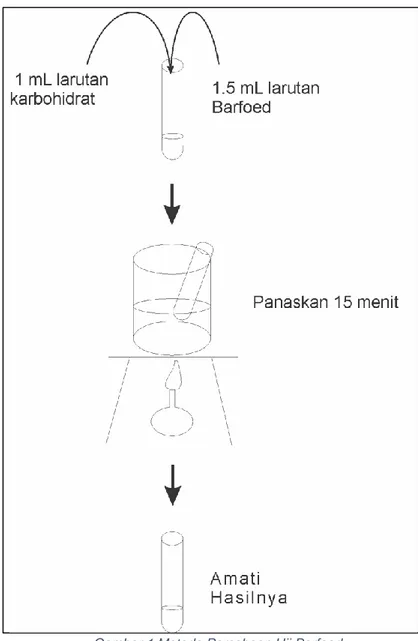
2.4. Metode Percobaan
Metode percobaan yang digunakan dalam uji Barfoed adalah seperti pada gambar di bawah ini :
III HASIL PENGAMATAN
Bab ini akan menguraikan mengenai (1) Hasil Pengamatan, dan (2) Pembahasan.
3.1. Hasil Pengamatan
Tabel 1 Hasil Pengamatan Uji Barfoed
Sampel Pereaksi Warna Hasil 1 Hasil 2
B A R FO E D Sebelum Pemanasan Setelah Pemanasan
Kecap Hijau lumut Hijau - +
Larutan Sukrosa
Biru Biru - -
Vitamin C IPI
Biru kuning Biru muda + +
Chitato Biru Biru - +
Sari Kacang Hijau
Hijau Biru Biru - +
Sumber : Hasil 1 : Giffary dan Fitria, Kelompok C, Meja 10. 2014 Hasil 2 : Laboratorium Biokimia Pangan, 2014 Keterangan : (+) terbentuknya endapan merah bata
Gambar 2 Hasil Pengamatan Uji Barfoed
3.2. Pembahasan
Karbohidrat merupakan senyawa makromolekul polihidroksi aldehid atau polihidroksi keton. Karbohidrat terdapat dalam jaringan tumbuhan, hewan dan mikroorganisme dalam berbagai bentuk dan aras. Karbohidrat memiliki rumus empiris (CH2O)n dan biasa disebut dengan “hidrat” dari sebuah
karbon (Lehninger, 1970).
Sifat-sifat Karbohidrat antara lain sebagai pereduksi, sebagai pembentuk furfural, pembentuk osazon, pembentuk ester dan pembentuk glikosidik (Poedjiadi, 1994).
Pembentukan Glikosidik adalah ikatan yang terjadi antara gugus metil dengan monosakarida disebut ikatan glikosida dan gugus ―OH yang bereaksi disebut dengan gugus ―OH glikosidik
Karbohidrat memiliki beberapa sifat khas dan salah satunya adalah sifat mereduksi. Sifat ini dijadikan dasar dari uji
Barfoed dimana monosakarida akan mereduksi ion logam sehingga akan menimbulkan endapan (Poedjiadi. 1994).
Sifat Mereduksi pada monosakarida dan beberapa disakarida lebih kuat dalam suasana basa. Sifat mereduksi ini disebabkan karena adanya gugus karbonil bebas dan aktif sehingga dapat mereduksi ion-ion logam misalnya Cu2+ atau
Ag+ yang terdapat pada pereaksi-pereaksi tertentu dan salah
satunya adalah pereaksi Barfoed (Poedjiadi, 1994).
Pereaksi Barfoed terdiri atas larutan kupriasetat dan asam asetat glasial dalam air. Suasana asam pada larutan ini diberikan oleh asam asetat glasial sedangkan Cu-asetat berfungsi sebagai pengendap (Poedjiadi, 1994)
Perbedaan uji barfoed dan benedict pertama adalah pada suasana nya. Suasana dalam uji Barfoed adalah suasana asam karena ada senyawa asetat sedangkan pada uji benedict suasananya adalah basa. Asam nya suasana pada uji barfoed ini dapat dikaitkan dengan tujuan uji ini yaitu untuk mengetahui gula monosakarida pereduksi saja karena itu suasana asam pada uji barfoed ini berfungsi untuk menguraui terlebih dahulu senyawa gula kompleks menjadi monosakarida terlebih dahulu. Selain suasana, perbedaan dalam waktu pemanasan pun berbeda. Dalam uji barfoed dilakukan pemanasan selama 15 menit sedangkan dalam uji benedict selama 5 menit. Hal ini memiliki dua alasan yaitu pertama ditinjau dari banyaknya reagen yang ditambahkan. Uji barfoed menggunakan reagen sebanyak 1.5 mL sedangkan benedict sebanyak 3 mL. alasan kedua adalah sifat karbohidrat secara umum adalah lebih cepat mereduksi pada suasana basa maka pemanasan tidak dibutuhkan terlalu lama dan alasan terakhir adalah meninjau dari tujuan dimana uji barfoed membutuhkan waktu lebih lama untuk mengurai gula yang kompleks menjadi monosakarida(Poedjiadi, 1994).
Dalam uji Barfoed, gula monosakarida lah yang direduksi. Gula pereduksi adalah gula yang memiliki gugus karbonil bebas yang dapat mereduksi ion-ion logam. Contohnya adalah
glukosa yang memiliki gugus aldehid bebas dan fruktosa yang memiliki gugus keton bebas yang bisa mereduksi logam seperti Cu2+. Lain dengan sukrosa yang tidak bersifat mereduksi. Tidak
seperti kebanyakan disakarida dan oligosakarida, sukrosa tak memiliki gugus anomer bebas karena kedua gugus anomerik dari kedua heksosa saling berikatan satu sama lain. Karena ini lah sukrosa tidak ber-mutarotasi, tidak bereaksi dengan phenilhydrazine membentuk osazon dan tak bersifat reduktor (Lehninger, 1970).
Mekanisme terbentuknya merah bata adalah logam Cu2+
akan terreduksi oleh monosakarida menjadi Cu+. Monosakarida
dapat mereduksi lebih cepat dari disakarida. Cu+ yang
terbentuk memiliki warna kuning dan dengan pemanasan akan terbentuk endapan sebagai Cu2O berupa endapan merah bata
(David, 1998). Apabila karbohidrat mereduksi suatu logam, karbohidrat ini akan teroksidasi. Gugus aldehid pada karbohidrat akan teroksidasi menjadi karboksilat (Poedjiadi, 1994). Dalam susasana asam ini gula pereduksi yang termasuk disakarida memberikan reaksi sangat lambat dengan larutan barfoed sehingga tidak memberi endapan merah kecuali dengan waktu yang diperlama (Sudarmadji, 2010).
Pemanasan pada uji barfoed dilakukan selama 15 menit. Hal ini dilakukan agar gula-gula kompleks terurai terlebih dahulu menjadi monosakarida pereduksi. Selain itu, uji barfoed adalah uji yang bersuasana asam dimana karbohidrat monosakarida akan lebih cepat mereduksi di suasana basa maka dari itu pemanasan juga berfungsi untuk mempercepat reaksi (Poedjiadi, 1994).
Pada praktikum yang dilakukan oleh praktikan, terjadi kesalahan atau ketidaksesuaian dengan hasil yang didapat oleh Laboran Laboratorium Biokimia Pangan Unpas. Sampel Kecap, Chitato dan sari kacang hijau seharusnya memberikan hasil positif terhadap uji Barfoed, sedangkan hasil yang didapat adalah berupa hasil negative (tidak ada monosakarida pereduksi). Hal ini dikarenakan kurang telitinya praktikan dalam waktu pemanasan sampel. Waktu pemanasan yang terlalu
sebentar (<15 menit) tidak akan memberikan waktu banyak untuk gula kompleks untuk terurai menjadi monosakarida terlebih dahulu sehingga yang praktikan dapatkan bukanlah endapan merah bata melainkan serpihan-serpihan kecil yang mengapung dan berwarna merah bata. Ini mengindikasikan kurang lamanya waktu pemanasan
IV KESIMPULAN DAN SARAN 4.1. KESIMPULAN
Gula monosakarida pereduksi banyak terdapat pada bahan pangan. Dimana monosakarida pereduksi adalah monosakarida yang mempunyai gugus karbonil bebas sehingga dapat mereduksi ion logam dalam pereaksi barfoed. Uji Barfoed ini spesifik untuk mendeteksi ada atau tidaknya monosakarida pereduksi dalam suasana asam
4.2. SARAN
Yang perlu diingat dalam uji barfoed ini adalah tujuannya dan prinsip uji ini. Tujuan dari uji Barfoed didukung dengan penggunaan suasana asam pada uji ini. Waktu Pemanasan pun sangat perlu diperhatikan
V DAFTAR PUSTAKA
Holme, J. David.1998. Analytical Biochemistry 3rd Edition.
England; Pearson Education Limited
Lehninger, Albert L.1970. Biochemistry 2nd Edition. New York; Worth Publisher, INC
Poedjiadi, Anna.1994. Dasar-dasar Biokimia. Jakarta; Penerbit UI-Press
Sudarmadji, Slamet.2010. Analisis Bahan Makanan dan Pertanian. Yogyakarta; Yogyakarta Liberty