PENDAHULUAN
Darah merupakan media cair yang terdiri dari sel-sel yang diproduksi oleh jaringan hemopoietika yang disirkulasikan ke dalam sel-sel tubuh sebagai pembawa nutrien menuju jaringan tubuh, pembawa oksigen dari paru-paru ke jaringan , pembawa karbon dioksida dari jaringan ke paru-paru, pembawa produk buangan dari berbagai jaringan menuju ginjal untuk dieksresikan, berperan penting dalam mengendalikan suhu tubuh, berperan dalam sistem buffer, juga berperan dalam pembekuan darah untuk mencegah terjadinya kehilangan darah yang berlebihan pada luka dan mengandung faktor-faktor penting untuk mempertahankan tubuh terhadap penyakit
Pembekuan darah disebut juga koagulasi darah. Adapun faktor yang diperlukan dalam penggumpalan darah yaitu ion kalsium, dinding pembuluh yang luka yang membebaskan trombokinase, trombin dari protrombin dan fibrin yang terbentuk dari fibrinogen. Mekanisme pembekuan darah terjadi setelah trombosit meninggalkan pembuluh darah dan pecah, maka trombosit akan mengeluarkan tromboplastin bersama dengan ion kalsium dan tromboplastin mengaktifkan protrombin menjadi trombin (Evelyn, 1989). Trombin adalah enzim yang mengubah fibrinogen menjadi fibrin. Fibrin inilah yang berfungsi menjaring sel-sel darah merah menjadi gel atau menggumpal (Poedjiadi, 1994). koagulasi darah terjadi pada kisaran waktu 15 detik sampai 2 menit dan umumnya akan berakhir dalam waktu 5 menit, gumpalan darah normal menjadi sekitar 40% dari volume semula dalam waktu 24 jam (Frandson,1992). Koagulasi dapat dicegah dengan
penambahan kalium sitrat atau natrium sitrat yang menghilangkan garam kalsium.
Seiring dengan perkembangan teknologi dalam kedokteran, ditemukan lebih dari 50 macam zat penting yang mempengaruhi pembekuan darah. Beberapa diantaranya mempermudah terjadinya pembekuan, disebut prokoagulan, dan menghambat pembekuan, disebut antikoagulan. Terjadinya pembekuan tergantung pada keseimbangan antar kedua golongan zat ini. Dalam keadaan normal, antikoagulan lebih dominan sehingga darah tidak membeku, tetapi bila pembuluh darah rusak, prokoagulan di daerah yang rusak menjadi “teraktivasi” dan melebihi aktivitas antikoagulan, dan bekuan pun terbentuk
Sering kali banyak dihadapi permasalahan di bidang non-matematika, misalnya pada bidang kedokteran, fisika, teknik, ilmu sosial dan lain sebagainya tidak dapat diselesaikan secara langsung. Salah satu cara untuk mengatasi masalah tersebut adalah matematika. Secara umum pengertian model adalah suatu usaha menciptakan replika/tiruan dari suatu fenomena alam. Pada model Matematika replika/tiruan tersebut dilakukan dengan mendeskripsikan fenomena alam dengan satu set persamaan (dapat berupa persamaan differensial, sistem persamaan atau ekspresi-ekspresi matematika yang lain) yang diturunkan dari fenomena tersebut [1].
Dalam pemodelan matematika, ilmuwan hanya mencari persamaan-persamaan atau rumus-rumus yang berlaku pada fenomena, sehingga ditemukannya suatu model matematika. [2]. Dengan adanya model matematika tersebut, akan dibahas apakah model tersebut sesuai dengan keadaan yang terjadi pada MATHEMATICAL MODELING THE FORMATION OF THROMBIN ON PROCESS
Oleh
Ila Fitriani1, Drs. Asrul Sani, M.Sc, Ph.D2, La Gubu, S.Si.,MSi3
Program Studi Matematika, Fakultas Matematika dan Ilmu pengetahuan Alam Universitas Halu Oleo This study was conducted to analyze the dynamics of thrombin in the coagulation process model with Michaelis Menten. mathematical model is formulated with a system of ordinary differential equations which consists of five components in the thrombin generation factor, namely the factor X (stuart-power) is substrak, factor Xa (aktifator prothrombin) form of the enzyme, factor II (prothrombin) in the form of substrak, factor Xa:II (aktifator prothrombin:protrombin) in the form of complex substrak enzymes and factors substrak and IIa (thrombin) form of the enzyme. The modeling process into three stages, namely the formulation of the problem, made to look for relationships between variables that formed the assumptions that will be used in the modeling. The next stage is to make the scheme and a mathematical model by forming a mathematical equation in accordance with the assumptions that formed earlier. Last step is to find behavioral models finished by finding the equilibrium point to analyze the stability of the equilibrium point, and perform numerical simulations using matlab software. of the model gained two points of equilibrium. that is. and after analysis at the point of aquilibrium
, saddle point and stable spiral. The opposite point of equilibrium saddle point and stable spiral on numerical simulation cases I where and with and
saddle point on simulation cases II with and
where also has an saddle point. on this model substrak lower number concentration and the reaction rate will be growing.
keadaan biologis untuk pembentukan trombin dalam proses koagulasi yang dapat dilakukan melalui pendekatan matematika pada reaksi Michaelis Menten yang merupakan salah satu reaksi enzim sederhana yang dikemukakan oleh Michaelis dan Menten pada tahun 1913. [3]. . Reaksi kimia yang terjadi dalam sistem biologis selalu melibatkan katalis. Katalis ini dikenal sebagai katalis biologis (biokatalisator) berupa protein yang sangat spesifik yang disebut enzim. Percepatan reaksi terjadi karena enzim menurunkan energi pengaktifan yang dengan sendirinya akan mempermudah terjadinya reaksi. Enzim mengikat molekul substrat membentuk kompleks enzim substrat yang bersifat sementara dan lalu terurai membentuk enzim bebas dan produknya [4].
Pada penelitian kali ini akan dibahas pembentukan protrombin menjadi trombin yang dipengaruhi oleh aktifator protrombin. Sehingga penulis tertarik menggangkat judul penelitian “ Model Matematika Pembentukan Trombin Pada Proses koagulasi “ diharapkan dapat memberikan masukan yang positif dalam model matematika yang digunakan dalam proses koagulasi.
Tujuan dalam penelitian ini untuk mengetahui bagaimana pemodelan matematika pembentukan trombin pada proses koagulasi dan menentukan kestabilan dari titik kesetimbangan.
TINJAUAN PUSTAKA Pembekuan Darah
Bekuan mulai terbentuk dalam 15-30 detik bila trauma pembuluh sangat hebat dan dalam 1-2 menit bila traumanya kecil. Banyak sekali zat yang mempengaruhi proses pembekuan darah juga disebut dengan zat prokoagulan yang mempermudah terjadinya pembekuan dan sebaliknya zat yang menghambat proses pembekuan disebut dengan zat antikoagulan. Dalam keadaan normal zat antikoagulan lebih dominan sehingga darah tidak membeku, tetapi bila pembuluh darah rusak aktivitasi prokoagulan di daerah yang rusak meningkat dan bekuan akan terbentuk. Secara umum proses pembekuan darah terjadi melalui tiga langkah utama yaitu (1) pembentukan aktivator protombin sebagai reaksi terhadap pecahnya pembuluh darah, (2) perubahan protrombin menjadi trombin yang dikatalis oleh aktivator protrombin, dan (3) perubahan fibrinogen menjadi benang fibrin oleh trombin yang akan menyaring trombosit, sel darah, dan plasma sehingga terjadi bekuan darah.
Trombin
Trombin adalah protein yang membantu proses pembekuan berupa enzim pembekuan darah, enzim ini hanya dihasilkan di tempat yang terluka yang terbentuk karena reaksi kimia antara protein Protrombin , enzim trombokinase, vit K dan Ca, jumlahnya tidak boleh
melebihi atau pun kurang dari yang diperlukan, pada proses ini terjadi melalui pengawasan yang begitu ketat sehingga trombin hanya terbentuk saat benar-benar ada luka pada dinding pembuluh setelah enzim trombin mencapai jumlah yang memadai di dalam tubuh maka fibrinogen yang ada di plasma darah berupa protein-protein membentuk juluran benang yang disebut fibrin yang menjaring sel-sel darah merah menjadi gel atau menggumpal
Dasar- Dasar Model Matematika 1. Michaelis-Menten Reaksi kinetika
Mekanisme Michaelis Menten merupakan salah satu reaksi enzim sederhana yang dikemukakan oleh Michaelis dan Mentan pada tahun 1913. Dalam mekanisme ini molekul substrak dikombinasikan dengan molekul enzim yang membentuk komplek substrat-enzim yang kemudian menghasilkan molekul produk dan molekul (Briggs dan Haldane, 1995).
Gambar 1. Skema Michaelis-Menten Reaksi kinetika Misal :
= konsentrasi substrat pada saat konsentrasi enzim pada saat
konsentrasi komplek substrat-enzim pada saat
konsentrasi produk pada saat
Maka reaksi enzim dalam pers.(2.1) dapat dimodelkan dalam bentuk sistem persamaan diferensial sebagai berikut:
Selanjutnya, misalkan menyatakan enzim total yaitu jumlah enzim bebas dan enzim terikat maka
Ketika sistem reaksi berada dalam keadaan seimbang maka kecepatan pembentukan sama dengan kecepatan penguraian sehingga berlaku
Apabila konsentrasi substrat cukup besar sehingga semua enzim terikat kepadanya yaitu dalam bentuk kompleks , maka akan didapatkan
maksimum yaitu sehingga merupakan laju maksimum reaksi enzim. Sehingga diperoleh persamaannya yaitu,
Persamaan Michaelis Menten sering digunakan untuk menggambarkan laju pertumbuhan populasi yang bergantung pada konsentrasi nutrisi dan dapat mencapai kondisi jenuh saat konsentrasi nutrisi cukup besar.
2. Sistem Persamaan Differensial
Sistem persamaan differensial adalah suatu sistem persamaan yang memuat buah fungsi yang tidak diketahui, dimana merupakan bilangan bulat positif ≥ 2 ( Finizio, 1982).
Persamaan differensial seringkali muncul dalam model matematika yang mencoba menggambarkan keadaan kehidupan nyata. Sebagai contoh, dalam biologi yaitu laju pertumbuhan populasi. Diberikan sistem persamaan differensial nonlinear orde 1 , dapat dinyatakan dalam bentuk matriks yakni: (2.6) dimana dan adalah transpose.
Sistem (2.6), dikatakan nolinear apabila funngsi tak linear dan kontinu yang dapat berbentuk:
dikatakan sistem autonomous apabila fungsi tidak bergantung terhadap waktu, yakni:
3. Nilai Eigen dan Vektor Eigen
Definisi 2.2 Jika A adalah matriks berukuran maka vektor tak nol x didalam dikatakan vektor eigen (eigen vector) dari A jika Ax adalah kelipatan skalar dari x , yakni:
untuk suatu skalar . selanjutnya dikatakan nilai eigen (eigen value) dari A dan vektor dikatakan vektor eigen yang bersesuaian dengan . Nilai eigen matriks A yang berukuran dapat ditentukan dengan menyelesaikan sebagai berikut:
dengan adalah matriks identitas berukuran Agar dikatakan nilai eigen dari maka harus ada selesaian tak nol (nontrivial) dari persamaan (2.9). persamaan (2.9) mempunyai selesaian tak nol (nontrivial) jika dan hanya jika:
( 4 Analisis Kestabilan
Dalam menentukan titik kestabilan pada persamaan linear adalah dengan menguji sekitaran titik kestabilan dan sistem yang sederhana untuk menentukan nilai eigen yang menghasilkan matriks Jacobian sedangkan penentuan titik stabil pada sistem nonlinear juga sangat penting dalam perilaku sistemnya.
Kestabilan suatu titik kesetimbangan dapat diperiksa berdasarkan nilai eigen dengan menyelesaikan dengan adalah matriks (2.9) yang berukura menghasilkan polynnomial dengan derajat yang sama dengan ukuran matriks yang mempunyai bentuk umum
Stabilitas titik kesetimbangan ditentukan berdasarkan tanda bagian real pada nilai eigen yang dibagi menjadi tiga, yaitu:
1. Stabil
Titik kesetimbangan dikatakan stabil jika dan hanya jika nilai eigen adalah real dan negative atau mempunyai bagian real tak positif.
2. Stabil Asimtotik
Titik kesetimbangan dikatakan stabil asimtotik jika dan hanya jika nilai eigen adalah real dan negative atau mempunyai bagian real negative.
3. Tidak Stabil
Titik kesetimbangan dikatakan tidak stabil jika dan hanya jika nilai eigen adalah real dan positif atau mempunyai paling sedikit satu nilai eigen dengan bagian real positif
METODE PENELITIAN Waktu Dan Tempat
Penelitian ini dilaksanakan mulai bulan Februari 2016 sampai bulan Mei 2016. Kegiatan ini berlangsung di Laboratorium Komputasi Matematika (Lab. Aljabar) Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Halu Oleo.
Prosedur Penelitian
1. Indentifikasi masalah, yaitu membaca dan memahami literatur yang berkaitan dengan proses pembekuan darah dan pemodelan matematika, sehingga dapat menentukan faktor-faktor yang akan digunakan dalam model.
2. Membuat asumsi, yaitu dalam pembuatan model matematika tidak semua faktor yang berpengaruh dalam proses pembentukan trombin sehingga dapat dimodelkan secara matematika, oleh karena itu perlu disederhanakan dengan melakukan reduksi faktor-faktor yang berpengaruh terhadap peristiwa ini.
3. Menyelesaikan dan Menginterpretasikan Model, setelah model terbentuk, perlu diselesaikan secara matematika yaitu melakukan analisis parameter dengan mencari nilai eigen, menentukan titik kestabilan dan diskrititasi menggunakan metode runge-kutta.
4. Penarikan kesimpulan. HASIL DAN PEMBAHASAN
1. Model Pembentukan Trombin Pada Michaelis Menten Reaksi Kinetika Model pembentukan trombin pada michaelis menten reaksi kinetika dalam sistem ini sangat kompleks, sehingga diperlukan beberapa asumsi agar menjadi sederhana.
2. Asumsi
Asumsi yang digunakan dalam penelitian ini dipaparkan sebagai berikut:
1. Terdapat 5 faktor yang digunakan dalam proses pembentukan trombin yaitu faktor II (protrombin), faktor X (stuart-power), faktor Xa (Aktifator protrombin), faktor IIa (trombin) dan faktor kompleks Xa:II (Aktifator protrombin:protrombin). 2. faktor II (protrombin), faktor X (stuart-power) dan
faktor kompleks Xa:II (Aktifator protrombin:protrombin) diasumsikan sebagai subtrak sedangkan faktor Xa (Aktifator protrombin) dan faktor IIa (trombin) diasumsikan sebagai enzim.
3. Faktor X (stuart-power) bereaksi membentuk faktor Xa (Aktifator protrombin) menjadi aktif dengan laju reaksi sebesar k3.
4. Faktor II (protrombin) dikombinasikan dengan faktor Xa (Aktifator protrombin) bereaksi membentuk faktor kompleks Xa:II (Aktifator
protrombin:protrombin) dengan laju reaksi sebesar k1.
5. Terjadi reaksi umpan balik antara faktor kompleks Xa:II (Aktifator protrombin:protrombin) bereaksi membentuk faktor Xa (aktifator protrombin) dan faktor IIa (trombin) dengan laju reaksi sebesar k1. 6. Faktor kompleks Xa:II (Aktifator
protrombin:protrombin) yang terbentuk bereaksi dan menghasilkan bentuk aktif dan terurai menjadi faktor IIa (trombin) dan faktor Xa (aktifator protrombin) dengan laju reaksi sebesar k2.
7. Konsentrasi laju reaksi pada reaktan mengalami penurunan setiap waktu.
8. Laju reaksi berbanding lurus dengan konsentrasi zat pereaksi.
3. Skema Model
Berdasarkan asumsi di atas, maka diperoleh skema model Michaelis menten yang digunakan dalam pembentukan trombin dari protrombin pada proses koagulasi pada Gambar 2
Gambar 2 Skema model pembentukan trombin dari protrombin yang dipengaruhi oleh aktifator protrombin.
Keterangan:
II = faktor Protrombin dalam satuan nM
Xa = faktor Aktifator protrombin dalam satuan nM IIa = faktor Trombin dalam satuan nM
X = faktor stuart-power dalam satuan nM
Xa:II = faktor kompleks Aktifator protrombin: Protrombin dalam satuan nM
3. Model
Berdasarkan Asumsi dan skema di atas maka
diperoleh model pembentukan trombin yang dapat dimodelkan dalam sistem persamaan berikut:
Keterangan:
: merupakan tetapan (konstanta) kecepatan laju reaksi pembentukan kompleks faktor Xa:II (Aktifator protrombin:Protrombin) 2
: merupakan tetapan (konstanta) kecepatan
laju reaksi umpan balik antara kompleks faktor Xa:II (aktifator
protrombin:protrombin) menjadi faktor Xa (aktifator protrombin) dan faktor II (protrombin)
: merupakan tetapan (konstanta) kecepatan laju reaksi penguraian kompleks faktor Xa:II (aktifator protrombin:protrombin) menjadi bentuk aktif faktor IIa (trombin) dan faktor Xa (aktifator protrombin)
: merupakan tetapan (konstanta) kecepatan laju reaksi faktor X (stuart-power) menjadi faktor Xa (aktifator protrombin)
: konsentrasi Aktifator protrombin dalam satuan nM
: konsentrasi protrombin dalam satuan nM [X] : konsentrasi stuart-power dalam satuan nM [IIa] : konsentrasi Trombin dalam satuan nM [Xa:II] : konsentrasi kompleks Aktifator
protrombin: protrombin dalam satuan Nm 4. Titik Kesetimbangan
Analisis titik kesetimbangan pada sistem persamaan diferensial digunakan untuk menentukan suatu selesaian yang tidak berubah terhadap waktu . Sistem (4.1) titik kesetimbangannya dinyatakan ke dalam bentuk titik kesetimbangan dari (4.1) akan diperoleh dengan menyelesaikan:
Sehingga sistem (4.2) menjadi:
Terdapat dua titik kesetimbangan pada sistem (4.3) yaitu
5. Analisis Kestabilan Sistem di sekitar Titik
Kesetimbangan
Pada bagian ini akan dilakukan analisis kestabilan titik kesetimbangan dengan terlebih dahulu dilakukan pelinearisasian sistem model pembentukan trombin. Persamaan yang akan dilinearisasikan adalah sebagai berikut:
Linearisasi sistem persamaan diatas adalah matriks jacobian ,
Selanjutnya hasil penelitian di atas disubtitusikan ke dalam matriks jacobian , sehingga diperoleh:
6. Kestabilan Sistem di Titik Kesetimbangan Jika titik kesetimbangan disubtitusikan pada J maka diperoleh:
Untuk mencari nilai eigen matriks jacobian yang berukuran 5 x 5, maka matriks jacobian ditulis sebagai:
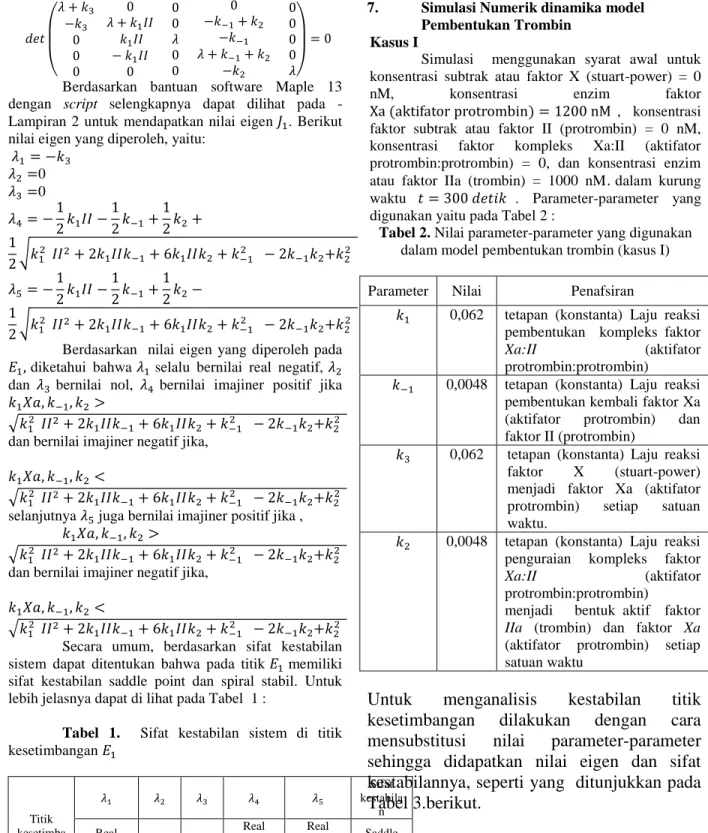
Berdasarkan bantuan software Maple 13 dengan script selengkapnya dapat dilihat pada -Lampiran 2 untuk mendapatkan nilai eigen . Berikut nilai eigen yang diperoleh, yaitu:
0 0
Berdasarkan nilai eigen yang diperoleh pada diketahui bahwa selalu bernilai real negatif, dan bernilai nol, bernilai imajiner positif jika
dan bernilai imajiner negatif jika,
selanjutnya juga bernilai imajiner positif jika ,
dan bernilai imajiner negatif jika,
Secara umum, berdasarkan sifat kestabilan sistem dapat ditentukan bahwa pada titik memiliki sifat kestabilan saddle point dan spiral stabil. Untuk lebih jelasnya dapat di lihat pada Tabel 1 :
Tabel 1. Sifat kestabilan sistem di titik kesetimbangan Titik kesetimba ngan Sifat kestabila n Real
negative Nol Nol
Real Imajiner Positif Real Imajiner Positif Saddle Point Real
negative Nol Nol
Real Imajiner negatif Real Imajiner Negative Spiral Stabil
7. Simulasi Numerik dinamika model Pembentukan Trombin
Kasus I
Simulasi menggunakan syarat awal untuk konsentrasi subtrak atau faktor X (stuart-power) = 0
nM, konsentrasi enzim faktor
, konsentrasi faktor subtrak atau faktor II (protrombin) = 0 nM, konsentrasi faktor kompleks Xa:II (aktifator protrombin:protrombin) = 0, dan konsentrasi enzim atau faktor IIa (trombin) = 1000 nM dalam kurung waktu . Parameter-parameter yang digunakan yaitu pada Tabel 2 :
Tabel 2. Nilai parameter-parameter yang digunakan dalam model pembentukan trombin (kasus I) Parameter Nilai Penafsiran
0,062 tetapan (konstanta) Laju reaksi pembentukan kompleks faktor
Xa:II (aktifator
protrombin:protrombin)
0,0048 tetapan (konstanta) Laju reaksi
pembentukan kembali faktor Xa (aktifator protrombin) dan faktor II (protrombin)
0,062 tetapan (konstanta) Laju reaksi faktor X (stuart-power) menjadi faktor Xa (aktifator protrombin) setiap satuan waktu.
0,0048 tetapan (konstanta) Laju reaksi penguraian kompleks faktor
Xa:II (aktifator
protrombin:protrombin)
menjadi bentuk aktif faktor IIa (trombin) dan faktor Xa (aktifator protrombin) setiap satuan waktu
Untuk
menganalisis
kestabilan
titik
kesetimbangan
dilakukan
dengan
cara
mensubstitusi
nilai
parameter-parameter
sehingga didapatkan nilai eigen dan sifat
kestabilannya, seperti yang ditunjukkan pada
Tabel 3.berikut.
Tabel 3. Titik kesetimbangan, nilai eigen, dan sifat kestabilan sistem (Kasus I)
Titik kesetimbangan Nilai eigen Sifat kestabilan
Saddle Point Saddle Point
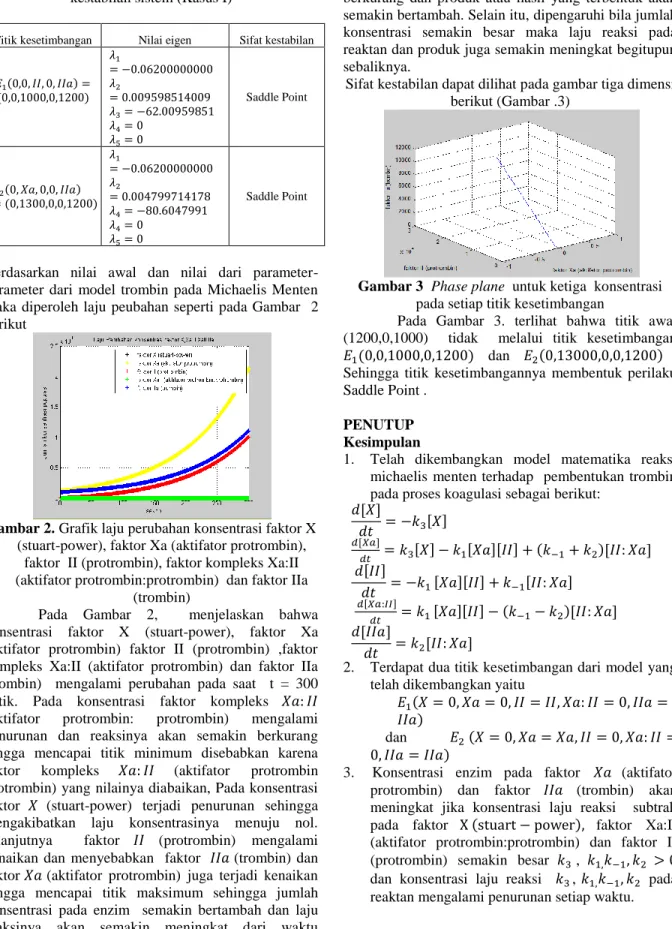
Berdasarkan nilai awal dan nilai dari parameter-parameter dari model trombin pada Michaelis Menten maka diperoleh laju peubahan seperti pada Gambar 2 berikut
Gambar 2. Grafik laju perubahan konsentrasi faktor X (stuart-power), faktor Xa (aktifator protrombin),
faktor II (protrombin), faktor kompleks Xa:II (aktifator protrombin:protrombin) dan faktor IIa
(trombin)
Pada Gambar 2, menjelaskan bahwa konsentrasi faktor X (stuart-power), faktor Xa (aktifator protrombin) faktor II (protrombin) ,faktor kompleks Xa:II (aktifator protrombin) dan faktor IIa (trombin) mengalami perubahan pada saat t = 300 detik. Pada konsentrasi faktor kompleks (aktifator protrombin: protrombin) mengalami penurunan dan reaksinya akan semakin berkurang hingga mencapai titik minimum disebabkan karena faktor kompleks (aktifator protrombin protrombin) yang nilainya diabaikan, Pada konsentrasi faktor (stuart-power) terjadi penurunan sehingga mengakibatkan laju konsentrasinya menuju nol. selanjutnya faktor (protrombin) mengalami kenaikan dan menyebabkan faktor (trombin) dan faktor (aktifator protrombin) juga terjadi kenaikan hingga mencapai titik maksimum sehingga jumlah konsentrasi pada enzim semakin bertambah dan laju reaksinya akan semakin meningkat dari waktu
kewaktu. hal ini disebabkan reaktan semakin berkurang dan produk atau hasil yang terbentuk akan semakin bertambah. Selain itu, dipengaruhi bila jumlah konsentrasi semakin besar maka laju reaksi pada reaktan dan produk juga semakin meningkat begitupun sebaliknya.
Sifat kestabilan dapat dilihat pada gambar tiga dimensi berikut (Gambar .3)
Gambar 3 Phase plane untuk ketiga konsentrasi pada setiap titik kesetimbangan
Pada Gambar 3. terlihat bahwa titik awal (1200,0,1000) tidak melalui titik kesetimbangan dan . Sehingga titik kesetimbangannya membentuk perilaku Saddle Point .
PENUTUP Kesimpulan
1. Telah dikembangkan model matematika reaksi michaelis menten terhadap pembentukan trombin pada proses koagulasi sebagai berikut:
2
2. Terdapat dua titik kesetimbangan dari model yang telah dikembangkan yaitu
dan
3. Konsentrasi enzim pada faktor (aktifator protrombin) dan faktor (trombin) akan meningkat jika konsentrasi laju reaksi subtrak pada faktor faktor Xa:II (aktifator protrombin:protrombin) dan faktor II (protrombin) semakin besar ,
dan konsentrasi laju reaksi , pada
Saran
Pada tugas akhir ini, penulis melakukan penelitian tentang model matematika pembentukan trombin pada proses koagulasi. Disarankan untuk penelitian selanjutnya membahas mengenai Dinamika model pembentukan fibrin hingga terbentuknya suatu bekuan darah pada proses koagulasi dengan asumsi yang lebih kompleks.
DAFTAR PUSTAKA
[1] Arthur, C., Guyton., John, E. dan Hall. 1997. Buku Ajar Fisiologi Kedokteran. Edisi 9. Jakarta : EGC.
[2] Arrowsmith, D.K. dan Place, C.M., 1982. Ordinary Differential Equations (Chapman and Hall Mathematics Series). Westfiled College University of London.
[3] Baiduri. 2002. Persamaan Diferensial & Matematika Model. Malang: Universitas Muhammadiyah Malang Press.
[4] Briggs, G.E. dan Haldane, J.B.S.1995. A Note on the Kinetics of Enzyme Action. Biochemical Journal, 1995. 19(2): p. 338-339.
[5] Frandson, R.D. 1992. Anatomi dan Fisiologi Ternak Edisi ke-4. Gadjah Mada University Press
[5] Guyton dan Arthur, C. 1983. Fisiologi Manusia dan Mekanismenya terhadap Penyakit. EGC Penerbit Buku kedokteran : Jakarta