Uji stabilitas mikrobiologis pembersih gigi tiruan
dengan bahan minyak atsiri kulit batang kayu manis
(
Cinnamomum burmannii
)
(Microbiological stability test on denture cleanser with ingredients of
essential oil of Cinnamon Bark (Cinnamomum burmannii))
Niken Pristianingrum,1 Soebagio,2dan Elly Munadziroh2
1Mahasiswa Strata 1
2Departemen Material Kedokteran Gigi
Fakultas Kedokteran Gigi Universitas Airlangga Surabaya – Indonesia
ABSTRACT
Background: Denture cleaners are products designed to clean stains, deposits, and debris from the surface of the denture, by soaking or brushing with tooth brush and toothpaste for dentures. Cinnamon is a tree with aromatic bark has a very strong odor. Cinnamon has the effect of antifungal, antiviral, bactericidal, and larvasidal. Purpose: The aim of this research made denture cleaning preparations with ingredients of essential oil of cinnamon bark and microbiological stability test to be have done. Method: In this research, microbiological stability test that includes total plate count test and pathogen microbial test denture cleaning with ingredients of essential oil cinnamon bark 2%, which is stored in a period of 1 week, 2 weeks, 3 weeks, 4 weeks, 2 months, and 3 months. In addition to supporting the results of the study, researchers conducted a preliminary test of the effectiveness of essentials oil of cinnamon bark against Candida albicans. Results: Showed that there was no change in total plate count and the growth of microbial pathogens in denture cleaning preparations with the ingredients of essential oil of cinnamon bark up to 3 months. This shows that the stocks stable in storage at room temperature until the 3 months. Conclusion: Denture cleaning preparations was stable in storage up to 3 months.
Key words: Cinnamon, denture cleanser, total plate count
Korespondensi (correspondence): Niken Pristianingrum,Mahasiswa Strata 1, Fakultas Kedokteran Gigi Universitas Airlangga. Jl. Mayjend. Prof. Dr. Moestopo no. 47 Surabaya 60132, Indonesia. E-mail: [email protected]
PENDAHULUAN
Bahan resin akrilik polimetil metakrilat (PMMA) merupakan bahan yang banyak digunakan untuk basis gigi tiruan lepasan. Bahan resin akrilik telah diterima dengan baik untuk basis gigi tiruan di bidang kedokteran gigi sejak tahun 1946.1 Resin akrilik dipakai sebagai basis gigi tiruan
oleh karena bahan ini memiliki sifat tidak toksik, tidak iritasi, tidak larut dalam cairan mulut, estetik baik, mudah dimanipulasi, reparasinya mudah dan
perubahan dimensinya kecil.2
Keradangan rongga mulut pada pemakai gigi tiruan lepasan dengan basis resin akrilik yang
disebut denture stomatitis prevalensinya di
masyarakat Indonesia cukup tinggi. Candida albicans
memberikan kontribusi yang besar terhadap
terjadinya denture stomatitis. Candida albicans
disamping merupakan flora normal dengan prevelensi sekitar 45%, prevelensi tersebut dilaporkan meningkat pada pemakai gigi tiruan dengan keadaan rongga mulut sehat yaitu 47,5%
sampai 55,6%.3 Salah satu cara untuk mencegah
denture stomatitis adalah dengan membersihkan gigi tiruan. Pembersihan gigi tiruan dengan larutan
pembersih dilaporkan sangat efektif.4 Menurut
Abelson cit. Donata,5 larutan pembersih gigi tiruan
dijangkau oleh sikat gigi, sehingga pembersihan terhadap noda, deposit, dan debris dari permukaan gigi tiruan lebih optimal.
Mosby’s Dental Dictionary6 mendefinisikan
pembersih gigi tiruan adalah produk yang dirancang untuk membersihkan noda, deposit, dan debris dari permukaan gigi tiruan, dengan cara merendam atau menyikat dengan sikat dan pasta gigi untuk gigi tiruan. Suatu produk harus memiliki stabilitas dalam penyimpanan. Stabilitas sediaan obat adalah kemampuan suatu produk untuk mempertahankan sifat dan karakteristiknya agar sama dengan yang dimilikinya pada saat dibuat (identitas, kekuatan, kualitas, kemurnian) dalam batasan yang ditetapkan sepanjang periode
penyimpanan dan penggunaan (shelf-life).7
Selama masa penyimpanan suatu sediaan, dimungkinkan terjadi kontaminasi. Kontaminasi mikroba dalam sediaan menyebabkan turunnya kualitas produk dan mempengaruhi kesehatan konsumen. Kontaminasi ini dapat menyebabkan perubahan bau, warna, viskositas, dan penampilan sediaan. Perubahan ini disebabkan oleh kemampuan mikroorganisme memecah komponen-komponen produk dan atau merupakan metabolit mikroba. Seringkali perubahan ini tidak nyata tetapi dalam waktu beberapa bulan baru menunjukkan
perubahan.8
Sumber kontaminan mikroba dapat berasal dari bahan dasar (terutama bahan alam), air yang digunakan dalam proses produksi, proses pembuatan, alat-alat, lingkungan tempat produksi, dan bahan pengemas serta operator. Sumber kontaminasi yang berbahaya adalah mikroorganisme patogen, tetapi mikroorganisme nonpatogen dapat juga menyebabkan penyakit jika dalam jumlah besar dan dalam kondisi yang sesuai bagi pertumbuhan
mikroorganisme.8
Suatu sediaan tidak harus steril, tetapi kontaminan sediaan harus dibatasi jumlahnya.8 Uji mikrobiologis
(uji batas mikroba dan identifikasi mikroba patogen) dilakukan untuk mengetahui stabilitas sediaan tersebut terhadap mikroba. Uji batas mikroba dilakukan untuk memperkirakan jumlah mikroba hidup dalam semua jenis produk farmasi mulai dari bahan baku hingga sediaan jadi dan untuk menyatakan produk farmasi
tersebut bebas dari spesies mikroba tertentu.9 Uji
batas mikroba dilakukan dengan menghitung jumlah mikroba pada cawan petri pada pengenceran
tertentu dan dinyatakan dalam total plate count
(Angka Lempeng Total).10 Persyaratan untuk uji
batas mikroba menurut CTF (The Toilet Preparation
Federation) yaitu mengandung mikroorganisme aerob kurang dari 1000 per gram atau ml. Identifikasi mikroba patogen pada sediaan yang
berasal dari bahan alam meliputi Pseudomonas
aeruginosa, Escherichia coli, Staphylococcus aureus, dan
Candida albicans.9 karena merupakan penyebab
penyakit infeksi yang umum pada manusia. Seiring perkembangan ilmu pengetahuan, pemakaian dan pendayagunaan obat tradisional di Indonesia mengalami kemajuan yang sangat pesat. Obat-obatan tradisional kembali digunakan masyarakat sebagai salah satu alternatif pengobatan,
di samping obat-obatan yang berkembang di pasar.11
Kayu manis adalah pohon dengan kulit batang memiliki bau aromatik yang sangat kuat. Kandungan kimia yang terdapat dalam kayu manis antara lain minyak atsiri, safrole, eugenol, sinamaldehid, tanin,
damar, kalsium oksalat, dan zat penyamak.12World
Health Organization monographs on selected medicinal plants13 menjelaskan dalam uji eksperimental
farmakologi, kayu manis memiliki efek antijamur
dan antibakteri. Barnes14 menyatakan bahwa kayu
manis memiliki efek antifungal, antiviral, bakterisidal,
dan larvasidal. Secara in vitro, kayu manis telah
terbukti sebagai anti jamur Candida albicans.13,14 Yulinah
et al.15 menyatakan aktivitas antifungi minyak atsiri
kulit batang kayu manis terhadap Candida albicans
dengan konsentrasi hambat minimum 1%.
Berdasarkan uraian di atas, peneliti ingin membuat suatu sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis 2%. Pada penelitian ini akan dilakukan uji stabilitas mikrobiologis sediaan yang disimpan dalam jangka waktu 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan. Jangka waktu penyimpanan ini sesuai dengan standar penyimpanan sediaan pada suhu kamar. Selain itu untuk mendukung hasil penelitian, peneliti melakukan penelitian pendahuluan yaitu uji efektifitas minyak atsiri kulit batang kayu manis terhadap Candida albicans. Uji efektifitas minyak atsiri
kulit batang kayu manis terhadap Candida albicans
dilakukan pada konsentrasi 0,25%, 0,5%, 1%, 1,5%, dan 2%. Uji efektifitas bertujuan untuk menetapkan konsentrasi yang tepat untuk pembuatan sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis. Tujuan penelitian ini menghitung angka lempeng total sediaan pembersih gigi tiruan dengan bahan aktif minyak atsiri kulit batang kayu manis 2% setelah penyimpanan selama 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan dan mengidentifikasi mikroba patogen
aureus, dan Candida albicans pada sediaan pembersih gigi tiruan dengan bahan aktif minyak atsiri kulit batang kayu manis 2% setelah penyimpanan selama 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan.
BAHAN DAN METODE
Bahan yang digunakan dalam penelitian ini adalah minyak atsiri kulit batang kayu manis, aquades, emulgator tween 80, larutan salin, media
biakan Nutrient agar MERCK VM 100650 943 dan
Nutrient borth BD 8072513, Media selektif Manitol salt agar (MSA) OXOID CM 0085, Cetrimide Agar Medium (CETA) MERCK VM 393489 511 , Eosin Methylene Blue (EMB) MERCK VM 219142 411,
Sabouroud Dextrosa Agar (SDA) BD 0012492, Stok
bakteri Pseudomonas aeruginosa ATCC 9027,
Escherichia coli ATCC 8739, Staphylococcus aureus ATCC 653BP, Candida albicans.Alat yang digunakan adalah Autoklaf merek Huxley 340, Inkubator merek Memmert, Mikropipe.
Persiapan sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis dengan membuat sediaan induk pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis dengan konsentrasi 2% (4 ml minyak atsiri kulit batang kayu anis + 2% tween 80 + aquades hingga didapatkan volume 200 ml).
Uji efektifitas kandidat produk pembersih gigi tiruan,dimulai dengan pengenceran sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis dengan konsentrasi 0,25%; 0,5%; 1%; 1,5%. Disiapkan media dasar SDA yang terdiri dari media dasar dan media perbenihan, kemudian membuat lubang sumuran pada media dan ditanam masing-masing konsentrasi sediaan pada sumuran sebanyak 100 mikron. Sediaan
diinkubasi pada suhu 370 C selama 24 jam dan
diamati dan diukur zona hambat tumbuh.
Pelaksanaan uji satabilitas mikrobiologis (Uji batas mikroba (angka lempeng total), identifikasi mikroba patogen) melalui uji batas mikroba (Angka Lempeng Total) dengan cara disiapkan cawan petri dan diberi label pengenceran 101 sampai 105: dibuat
pengenceran sampel dengan larutan salin pada
pernadingan 1 : 9 sampai didapat pengenceran 105.
Tiap-tiap pengenceran diambil 1 ml dan ditanam pada dua cawan petri yang berisi media NA, digoyang agar hasil pengenceran sampel dengan media NA dapat tercampur homogen. Larutan diratakan dan diinkubasi pada suhu 30 ± 20 C 24 jam.
Jumlah koloni dihitung yang tumbuh, kedua lempeng dinyatakan rata-rata jumlah bakteri tiap ml sampel dan dikalikan dengan pengenceran.
Identifikasi mikroba pathogen dilakukan
dengan cara menanam sediaan pada media nutrient
broth untuk memperkaya bakteri dan diinkubasi
pada suhu 37 ± 20 C 24 jam, kemudian digoreskan
pada media selektif. Staphylococcus aureus
menggunakan media Maltosa Salt Agar (MSA),
pseudomonas aeruginosa pada media Cetrimide
Agar Medium (CETA), Escherichia coli pada media
Eosin Methylene Blue (EMB), Candida albicans pada
Sabouroud Dextrosa Agar (SDA). Morfologi masing-masing mikroba dapat dilihat pada Tabel l.
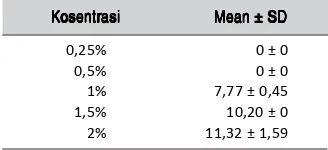
Tabel 2. Hasil uji efektifitas sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis terhadap Candida albicans
K KK K Kosentrosentrosentrosentrosentrasiasiasiasiasi
0,25% 0 ± 0
Tabel 3. Hasil uji efektifitas sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis terhadap Candida albicans pada bulan ke-3
K KK K Kosentrosentrosentrosentrosentrasiasiasiasiasi
0,25% 0 ± 0
Hasil uji efektifitas sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu
manis terhadap Candida albicans dapat dilihat pada
Tabel 2.
Tabel 1. Morfologi mikroba pada media agar selektif
Nama mikroba Nama mikroba Nama mikroba Nama mikroba Nama mikroba
Staphylococcus aureus MSA Kuning dengan zone kuning
Pseudomonas aeruginosa CETA Umumnya kehijauan
Escherichia coli EMB Hitam, biru hitam
Candida albicans SDA Hifa
Media selektif Media selektif Media selektif Media selektif
Uji efektivitas sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis
dengan konsentrasi 1,5% dan 2% terhadap Candida
albicans yang disimpan selama 3 bulan, diperoleh data zona hambat seperti pada Tabel 3. Data zona hambat tersebut dilakukan uji distribusi normal
One-Sample Kolmogorov-Smirnov, didapatkan hasil data berdistribusi normal p = 0,99 (p>0,005). Data
yang sudah didapat dilakukan uji t-test, dan
didapatkan hasil p = 0,31 (p>0,005). Hasil ini menunjukkan bahwa tidak ada perbedaan bermakna antara konsentrasi 1,5% dan 2%.
Escherichia coli menunjukkan hasil negatif, karena sampel tidak membentuk koloni berwarna hitam atau
biru hitam pada media Eosin Methylene Blue (EMB).
Identifikasi Staphylococcus aureus, juga menunjukkan hasil negatif, karena tidak menunjukkan koloni kuning pada Manitol Salt Agar (MSA). Candida albicans yang
ditanam pada Sabouroud Dextrosa Agar (SDA) juga
menunjukkan hasil negatif, karena tidak membentuk koloni berwarna krem dan berbau ragi.
Tabel 4. Hasil uji batas mikroba (angka lempeng total)
W W W W
Waktu penaktu penaktu penaktu penaktu penyimpananyimpananyimpananyimpananyimpanan (minggu/b (minggu/b(minggu/b (minggu/b (minggu/bulanulanulanulanulan
0 0 0
Angka lempeng total (AL Angka lempeng total (AL Angka lempeng total (AL Angka lempeng total (AL Angka lempeng total (ALT)T)T)T)T)
ΣΣΣΣΣ k k k koloni kolonioloniolonioloni RerRerRerRerRerataataataataata
Penelitian uji batas mikroba (angka lempeng total) dilakukan dengan cara sediaan yang telah disimpan selama jangka waktu 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan ditanam
pada media Nutrient agar dengan pengenceran
hingga 10-5, kemudian dilakukan penghitungan
rata-rata jumlah koloni yang tumbuh. Hasil penelitian selama 3 bulan menunjukkan tidak ada pertumbuhan koloni, sehingga dalam penelitian ini tidak didapatkan peningkatan angka lempeng total (ALT) sediaan.
Hasil uji efektifitas terhadap Candida albicans
menunjukkan konsentrasi 2% sebagai konsentrasi
yang baik untuk menghambat pertumbuhan Candida
albicans, sehingga konsentrasi tersebut dijadikan patokan dalam pembuatan sediaan pembersih gigi tiruan. Uji stabilitas mikrobiologis uji batas mikroba (angka lempeng total) menunjukkan hasil penelitian selama 3 bulan menunjukkan tidak ada pertumbuhan koloni, sehingga dalam penelitian ini tidak didapatkan peningkatan angka lempeng total (ALT) sediaan.
Hasil pengamata hingga bulan ke-3 menunjukkan
bahwa sampel tidak mengandung Pseudomonas
aeruginosa, karena tidak didapatkan koloni berwarna
kehijauan pada media Cetrimide Agar Medium (CFTA).
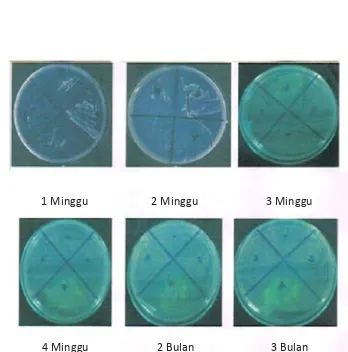
Gambar 1. Koloni Staphylococcus aureus selama 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan. Hasil identifikasi mikroba patogen menunjukkan hasil negatif (hasil gesekkan sampel tidak menunjukkan karakteristik yang sama dengan hasil gesekan positif yang merupakan gesekan positif yang merupakan gesekan mikroba patogen sebagai pembanding).
1 Minggu 2 Minggu 3 Minggu
4 Minggu 2 Bulan 3 Bulan
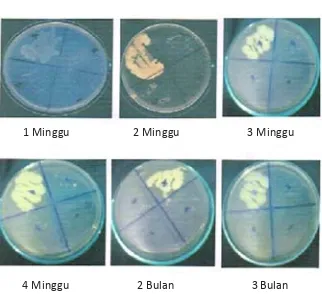
Gambar 2. Koloni Pseudomonas aeruginosa selama 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan. Hasil identifikasi mikroba patogen menunjukkan hasil negatif (hasil gesekkan sampel tidak menunjukkan karakteristik yang sama dengan hasil gesekan positif yang merupakan gesekan positif yang merupakan gesekan mikroba patogen sebagai pembanding).
1 Minggu 2 Minggu 3 Minggu
PEMBAHASAN
Uji stabilitas mikrobiologis dilakukan pada penelitian ini untuk mengetahui ketahanan sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis terhadap pertumbuhan
Candida albicans. Uji stabilitas mikrobiologis terdiri dari uji batas mikroba (angka lempeng total) dan identifikasi mikroba patogen. Selain itu untuk mendukung hasil penelitian, peneliti melakukan penelitian uji efektifitas minyak atsiri kulit batang
kayu manis terhadap Candida albicans.
Uji efektifitas minyak atsiri kulit batang kayu manis terhadap Candida albicans dilakukan sebagai uji pendahuluan untuk mengetahui aktivitas antimikroba sediaan. Pada uji ini didapatkan kadar minimal yang
dapat menghambat pertumbuhan Candida albicans
dengan baik, yaitu konsentrasi 2%. Konsentrasi 2% kemudian dijadikan sebagai standar untuk pembuatan sediaan pembersih gigi tiruan. Pada akhir penelitian dilakukan uji efektivitas sediaan yang telah disimpan selama 3 bulan pada konsentrasi 1,5% dan
2% terhadap Candida albicans. Hasil statistik uji
efektifitas menyatakan bahwa tidak ada perbedaan bermakna antara konsentrasi 1,5% dan 2%, sehingga pada penelitian selanjutnya dapat digunakan minyak atsiri dengan konsentrasi 1,5% sebagai standar pembuatan sediaan pembersih gigi tiruan.
Uji batas mikroba dilakukan dengan menghitung jumlah mikroba pada cawan petri pada pengenceran tertentu dan dinyatakan dalam total plate count (angka lempeng total). Penghitungan angka lempeng total dilakukan pada sediaan yang telah disimpan sesuai suhu kamar dan dalam jangka waktu penyimpanan 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan.
Identifikasi mikroba patogen dilakukan dengan
mengidentifikasi mikroba Staphylococcus aureus,
Pseudomonas aeruginosa, Escherichia coli, Candida albicans yang tumbuh pada sediaan (Gambar 1, 2, 3, dan 4). Selama masa penyimpanan dimungkinkan terjadi kontaminasi. Kontaminasi ini dapat menyebabkan perubahan bau, warna, viskositas, dan penampilan sediaan. Perubahan ini disebabkan oleh kemampuan mikroorganisme memecah komponen-komponen produk dan atau merupakan metabolit mikroba. Seringkali perubahan ini tidak nyata tetapi dalam waktu beberapa bulan baru menunjukkan
perubahan.8
Hasil penelitian menunjukkan bahwa tidak ada perubahan angka lempeng total sediaan hingga bulan ke 3, dan hasil pengamatan terhadap mikroba patogen hingga bulan ke-3 menunjukkan hasil negatif. Berdasarkan hasil penelitian tersebut, dapat dinyatakan bahwa sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis stabil dalam penyimpanan sesuai suhu kamar hingga bulan ke 3. Kestabilan sediaan dimungkinkan karena dalam proses pengerjaan dilakukan secara steril mulai dari bahan baku, peralatan, tempat penyimpanan sediaan, dan tempat pengujian mikrobiologis. Pengerjaan yang steril akan meminimalisir terjadinya kontaminasi. Selain itu, sediaan mengandung minyak atsiri kulit batang kayu manis yang Gambar 3. Koloni Escherichia coli selama 1 minggu, 2 minggu,
3 minggu, 4 minggu, 2 bulan, dan 3 bulan.
Hasil identifikasi mikroba patogen menunjukkan hasil negatif (hasil gesekkan sampel tidak menunjukkan karakteristik yang sama dengan hasil gesekan positif yang merupakan gesekan positif yang merupakan gesekan mikroba patogen sebagai pembanding).
Gambar 4. Koloni Candida albicans selama 1 minggu, 2 minggu, 3 minggu, 4 minggu, 2 bulan, dan 3 bulan.
Hasil identifikasi mikroba patogen menunjukkan hasil negatif (hasil gesekkan sampel tidak menunjukkan karakteristik yang sama dengan hasil gesekan positif yang merupakan gesekan positif yang merupakan gesekan mikroba patogen sebagai pembanding).
1 Minggu 2 Minggu 3 Minggu
4 Minggu 2 Bulan 3 Bulan
1 Minggu 2 Minggu 3 Minggu
mempunyai daya antimikroba, sehingga sediaan juga memiliki ketahanan terhadap kontaminasi. Hal ini
didukung oleh Barnes14 menyatakan bahwa kayu
manis memiliki efek antifungal, antiviral, bakterisidal, dan larvasidal. Berdasarkan pembahasan diatas maka dapat disimpulkan bahwa sediaan pembersih gigi tiruan dengan bahan minyak atsiri kulit batang kayu manis 2% stabil dalam penyimpanan hingga 3 bulan pada suhu kamar.
DAFTAR PUSTAKA
1. Craig RG, O’Brien WJ, Powers JM. Dental material properties and manipulation. 11th ed. St. Louis: The
CV Mosby Co; 1992. p. 271-2.
2. Combe EC. Notes on dental materials. 6th ed.
Edinburg: Churchill Livingstone; 1992. p. 157-8, 224. 3. Soenartyo H. Denture stomatitis: penyebab dan pengelolaannya. Majalah Kedokteran Gigi (Dent J) 2000; 33 (4): 148-51.
4. Rianti D. Ekstrak Coleus ambonicus Lour sebagai bahan pembersih terhadap Candida albicans dengan kekuatan transversa resin akrilik. Tesis. Surabaya: Fakultas Kedokteran Gigi Universitas Airlangga; 2003. h.1-45.
5. Donata T. Efektivitas perendaman resin akrilik dalam berbagai konsentrasi infusa sereh terhadap jumlah koloni Candida albicans. Skripsi. Surabaya: Unair; 2005. h. 3.
6. Mosby. Mosby’s dental dictionary. 2nd ed. Elsevier.Available
from http://medical-dictionary.thefreedictionary.com/ denturecleanser. Accessed January 30th, 2010.
7. Joshita D. Kestabilan obat. Jakarta: UI; 2008. p. 78. Available from http://www.repository.ui.ac.id. Accessed on April 11th, 2010.
8. Brannan DK. Cosmetic microbiology, a practical handbook. New York: CRC Press; 1997. p. 102-104. 9. Suwandi U. Peran media untuk identifikasi mikroba
patogen. penelitian dan pengembangan PT Kalbe Farma. Jakarta: Cermin Dunia Kedokteran; 1999. h. 21-3.
10. Farmakope Indonesia. Farmakope Indonesia IV. 4th ed.
Jakarta: Lembaga Farmasi Nasional Indonesia; 1995. h. 847-54.
11. Wahyuni TS. Formulasi dan Uji Stabilitas Mikrobiologis Sediaan Tabir Surya Krim Kaempferia galangal L. Skripsi. Surabaya: Unair; 2001. h. 3, 4, 26-7.
12. Prapanza I, Lukito AM. Khasiat dan manfaat sambiloto raja pahit penakluk aneka penyakit. Jakarta: Agromedia Pustaka; 2003. h. 10.
13. World Health Organization monographs on selected medicinal plants (1999 p.106) WHO. 1999. World Health Organization monographs on selected medicinal plants Volume 1. Geneva. p. 95-104. 14. Barnes J. Herbal medicines. Third edition. Great
Britain: Pharmaceutical Press; 2007. p. 162.