LAPORAN
PRAKTIKUM KIMIA ORGANIK
UJI KEMURNIAN ASAM ASETIL SALISILAT (ASPIRIN)
Disusun oleh : Asyraq Fahruzzaman 1113102000034 Selvy Nurkhayati 1113102000035 Badriyatun Ni’mah 1113102000075 Tiara Puspitasari 1113102000013 Sri Komalasari 1113102000057 Haka As’ada 1113102000074 Kelompok 2 C
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA OKTOBER 2014
PRAKTIKUM KIMIA ORGANIK
UJI KEMURNIAN ASAM ASETIL SALISILAT (ASPIRIN)
I. TUJUAN PRAKTIKUM Mahasiswa diharapkan mampu :
1. Menentukan kemurnian asam asetil salisilat (aspirin) dengan KLT, uji FeCl3 dan
titik lebur
2. Menentukan Rf aspirin standar dan Rf aspirin sampel pada uji kemurnian dengan KLT
II. TEORI DASAR
Asam asetil salisilat mempunyai nama sinonim asetosal, asam salisilat asetat dan yang paling terkenal adalah aspirin ( brandname produk dari Bayern). Serbuk atau Kristal asam asetil salisilat dari tidak berwarna sampai berwarna putih. Asam asetil salisilat stabil dalam udara kering tapi terdegradasi perlahan jika terkena uap air menjadi asam asetat dan asam salisilat. Aspirin mempunyai densitas 1.40 g/cm³,titik lebur 135 °C (275 °F),titik didih140 °C (284 °F) (decomposes), dan kelarutan dalam air 3 mg/mL (20°C) .
Aspirin atau asam asetil salisilat adalah sejenis obat turunan dari salisilat yang sering digunakan sebagai senyawa analgesik, antipiretik, dan anti-inflamasi (peradangan). Aspirin juga memiliki efek antikoagulan dan dapat digunakan dalam dosis rendah dalam tempo lama untuk mencegah serangan jantung.
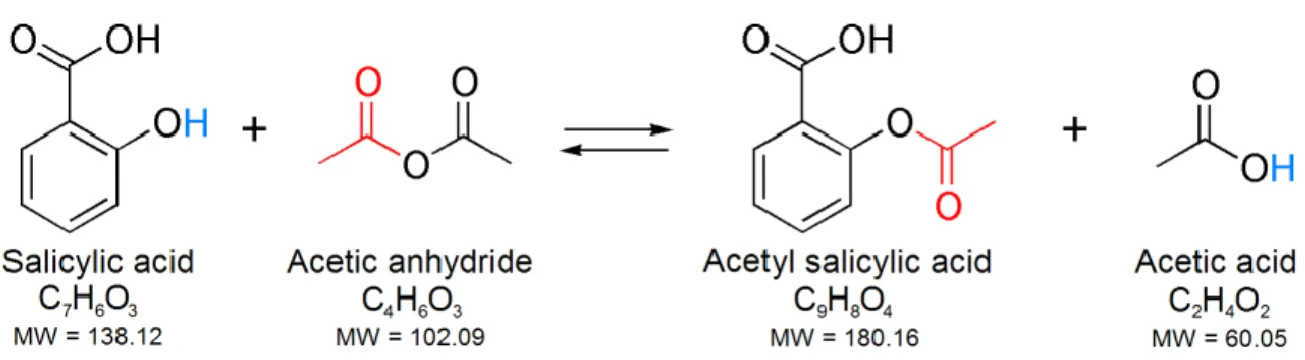
Gambar 1. Reaksi sintesis asam asetil salisilat
Aspirin dibuat dengan mereaksikan asam salisilat dengan anhidrida asam asetat menggunakan katalis H3PO4/H2SO4 sebagai zat penghidrasi. Asam salisilat adalah asam
ini dapat mengalami dua jenis reaksi yang berbeda yaitu reaksi asam dan basa. Reaksi dengan anhidrida asam asetat akan menghasilkan aspirin, Sedangkan reaksi dengan methanol akan menghasilkan metil salisilat.
Rumus Molekul Aspirin
Aspirin ( asam asetil salisilat) yang merupakan salah satu turunan dari fenol monohidris ialah fenol dengan satu gugus hidroksil yang berikatan dengan inti aromatisnya. Fenol tidak dapat didestilasi dalam air secara memuaskan. Oleh karena itu, asetilasi berlangsung baik pada anhidrida asam asetat dengan adanya penambahan sedikit asam mineral yang berfungsi sebagai katalis.
Aspirin digunakan sebagai analgesik untuk nyeri dari berbagai penyebab (sakit kepala, nyeri tubuh, arthritis, dismenore, neuralgia, gout, dan sebagainya), dan untuk kondisi demam, Aspirin juga berguna dalam mengobati penyakit rematik, dan sebagai anti-platelet (untuk mengencerkan darah dan mencegah pembekuan darah) dalam arteri koroner (jantung) dan di dalam vena pada kaki dan panggul. Ada juga artikel yang ditulis dalam literatur medis mendalilkan penurunan kejadian kanker usus besar di antara mereka yang secara teratur mengonsumsi Aspirin pada dosis tertentu. Saat ini banyak dokter dan pasien yang menggunakan Aspirin dosis rendah (baby Aspirin atau Aspirin berdosis 81 mg) setiap hari untuk mengurangi kemungkinan mendapatkan serangan jantung dan stroke melalui aksi anti-plateletnya (pengencer darah dan mencegah pembekuan darah).
Aspirin juga telah digunakan untuk mengatasi anak-anak yang mengalami Sindrom Bartter, dan juga dalam meningkatkan penutupan Patent Ductus Arteriosus (PDA), hubungan abnormal antara aorta (arteri utama terhubung ke jantung) dan arteri pulmonalis (untuk
paru-paru) pada bayi baru lahir. Jika PDA tidak menutup secara normal, operasi mungkin diperlukan untuk menutupnya (menutup dengan cara menjahit) sebelum anak memasuki usia sekolah.
Kromatografi merupakan teknik pemisahan tertentu, pada dasarnya kromatografi menggunakan dua fase yaitu fase tetap (stationary) dan fase bergerak (mobile), pemisahan tergantung pada gerakan relatif dari dua fase ini. Dari beberapa jenis kromatografi, satu di antaranya adalah Kromatografi Lapis Tipis (KLT), kromatografi jenis ini membutuhkan waktu yang lebih cepat dan diperoleh pemisahan yang lebih baik (Susilo, 2005).
Kromatografi Lapis Tipis merupakan suatu metode pemisahan senyawa kimia berdasarkanperbedaan distribusi dua fase yaitu fasa diam dan fasa gerak. Eluen yang baik adalah eluen yang bisa memisakan senyawa dalam jumlah yang banyak dan di tandai dengan munculnya noda (Rompas)
Fase gerak atau pelarut pengembang akan bergerak naik sepanjang fase diam karena adanya gaya kapilaritas pada sistem pengembangan menaik (ascending). Pemilihan fase gerak baik untuk TLC maupun HPTLC didasarkan pada keterpisahan senyawa-senyawa dalam analit yang didasarkan pada nilai Rf atau hRf (100Rf). Nilai Rf diperoleh dari membagi jarak pusat kromatografik dari titik awal dengan jarak pergerakan pelarut dari titik awal. Penghitungan nilai hRf ditunjukkan dengan persamaan dibawah ini.
Harga Rf =
(Ganjar dan Rochman, 2007). Faktor-faktor yang memengaruhi nilai Rf antara lain
1. Struktur kimia dari senyawa yang dipisahkan 2. Sifat penyerap dan aktivitasnya
3. Tebal dan kerataan lapisan penjerap 4. Tingkat kemurnian fase gerak 5. Tingkat kejenuhan uap
6. Jumlah cuplikan yang diinginkan 7. Suhu
Metode KLT memiliki beberapa keuntungan dan kerugian. Keuntungannya, waktu yang dibutuhkan tidak terlalu lama dan jumlah sampel yang digunakan sedikit (2−20 μg). Adapun kerugiannya adalah tidak efektif dalam skala besar. Pemakaian dalam skala besar akan menghabiskan plat KLT yang lebih banyak sehingga biaya analisis pun akan semakin meningkat (Tambunan, 2011).
Kemurnian aspirin bisa diuji dengan menggunakan besi (III) klorida. Hal ini bertujuan untuk mengetahui apakah aspirin yang didapatkan benar-benar murni atau tidak. Besi (III) klorida adalah pereaksi umum untuk golongan fenol. Penambahan fenol akan membentuk senyawa berwarna, dimana jika senyawa berada pada posisi orto akan memberikan warna violet, posisi meta : tidak berwarna dan posisi para akan menghasilkan endapan berwarna kuning. Dimana pada reaksinya akan menghasilkan reaksi samping yang berupa polimer yang mengandung gugus fenol. Jika besi (III) klorida ditambahkan lalu membentuk warna ungu maka terdapat asam salisilat pada aspirin, karena asam salisilat mempunyai gugus fenol.
Namun jika hasil yang didapatkan aspirin yang tidak murni maka dilakukan langkah selanjutnya yaitu residu (kristal) dilarutkan kembali dengan Na2HCO3 yang akan membentuk
garam dan ditambahkan HCl. Sehingga didapatkan asam salisilat dan aspirin dalam bentuk kristal yang kemudian disaring sehingga didapatkan residu. Kemudian untuk memisahkan antara asam salisilat dan aspirin ditambahkan pelarut panas (benzen), dimana pada pemisahannya aspirin akan mengkristal sedangkan asam salisilat tidak mengkristal.
Selain uji dengan FeCl3,uji kemurnian asam asetil salisilat dapat dilakukan dengan uji
titik leleh. Uji titik leleh dapat digunakan karena titik leleh merupakan sifat spesifik suatu zat.. Aspirin murni memiliki titik leleh 135°-136° C. Apabila aspirin tidak murni, maka titik leburnya kurang dari 135°C atau range titik leburnya lebih lebar, lebih dari 2°C.
III. METODE PRAKTIKUM
A. Waktu Dan Tempat Praktikum
Praktikum Kimia Organik (Uji Kemurnian asam asetil salisilat (aspirin) dilakukan pada Kamis, 16 Oktober 2014 Pukul 07.30-09.30 di Laboratorium FKIK UIN Syarif Hidayatullah Jakarta.
B. Alat dan Bahan 1. Kaca Arloji 2. Spatula 3. Beaker Glass 4. Pipet Tetes 5. Pipa Kapiler
6. Lumpang dan Stamfer 7. Aluminium Foil 8. Hair-Dryer 9. Penggaris 10. Pensil 11. Label
12. Melting Point Analyzer 13. Plat Tetes
14. Plat KLT (Kromatografi Lapis Tipis) 15. Produk Aspirin hasil praktikum (Sampel) 16. Standar Asam Asetil Salisilat (Standar Aspirin) 17. Etanol – air 50 %
18. Alkohol 95 % 19. Larutan FeCl3
C. Cara Kerja
Uji Kemurnian dengan FeCl3
1) Menyiapkan sebuah plat tetes dan larutan FeCl3
2) Meletakkan sedikit produk aspirin hasil praktikum (sampel) dan standar aspirin pada plat tetes.
3) Meneteskan pada masing-masing (sampel dan standar aspirin) satu tetes larutan FeCl3.
Uji Kemurnian dengan Titik Leleh
1) Menyiapkan pipa kapiler dan Melting Point Analyzer 2) Menumbuk produk aspirin hasil praktikum (sampel)
3) Menotolkan pipa kapiler pada sampel dan standar aspirin (2-4 mm) 4) Mengatur suhu pada Melting Point Analyzer
5) Memasukkan pipa kapiler pada Melting Point Analyzer 6) Mengamati pipa kapiler saat dipanaskan
7) Mencatat suhu dari sampel dan standar aspirin pertama kali meleleh sampai meleleh sempurna.
8) Melakukan uji kemurnian aspirin dengan titik leleh dua kali (duplo).
Standar Aspirin Sampel (Produk Aspirin Hasil Praktikum)
Uji Kemurnian dengan KLT
1) Melarutkan sedikit produk aspirin yang telah dihasilkan pada praktikum sebelumnya (sampel) dan juga standar asam asetil salisilat (standar aspirin) dengan menggunakan etanol air 90 %.
2) Menotolkan sampel yang telah dilarutkan dan standar aspirin tersebut pada garis-garis batas plat KLT yang telah disediakan.
3) Menuangkan 5 ml eluent (alkohol 95 %) ke dalam beaker glass dan meletakkan plat KLT tersebut (dalam posisi berdiri) ke dalamnya dan tutup dengan aluminium foil atau kaca arloji.
4) Tunggu beberapa menit hingga eluent naik.
5) Menghentikan proses elusi bila jarak eluent mencapai ½ cm dari ujung plat KLT 6) Memberi tanda batas akhir eluent menggunakan pensil
7) Menyemprot plat KLT tersebut dengan larutan FeCl3 dan mengeringkannya
dengan hair-dryer selama beberapa menit hingga spot terlihat.
IV. HASIL DAN PEMBAHASAN HASIL PRAKTIKUM
1. Pengujian FeCl3
Zat Uji Perubahan Warna
Standar Aspirin + FeCl3 Putih – Kuning
Sampel + FeCl3 Putih – Kuning
2. Uji Titik Leleh
I II
Standar Aspirin 134 – 135 °C 134 – 135 °C
Sampel 134 – 136 °C 135 – 137 °C
3. Uji dengan Plat KLT
Jarak spot Jarak Eluent Rf
Standar Aspirin 7 cm 9 cm 0.7
Sampel 7.2 cm 9 cm 0.8
Rf =
PEMBAHASAN
Uji yang dilakukan terhadap produk aspirin hasil praktikum (sampel), pada praktikum kali ini dilakukan dengan tiga metode uji, antara lain dengan uji reaksi FeCl3, uji kromatografi lapis tipis (KLT), dan uji titik leleh.
Pada uji reaksi FeCl3, aspirin direaksikan dengan FeCl3, yang akan
memberikan warna ungu pada asam salisilat. Warna ungu yang terjadi pada asam salisilat yang direaksikan dengan FeCl3 terjadi karena senyawa asam salisilat
mengandung fenol, dan fenol tersebut akan bereaksi dengan FeCl3 membentuk
senyawa kompleks berwarna ungu. Dalam uji yang dilakukan pada aspirin yang telah dibuat pada praktikum sebelumnya direaksikan dengan FeCl3 dengan cara
menetesinya di plat tetes, hasil uji menunjukkan warna kuning dan bukan ungu, menjelaskan bahwa aspirin yang telah dibuat tidak lagi mengandung asam salisilat.
Pada uji kemurnian menggunakan uji tetek leleh,, uji dilakukan dengan menggunakan alat melting point analyzer. Titik leleh dari aspirin yang diuji dibandingkan titik leleh yang tertera pada literature. Pada literature tertulis bahwa titik leleh aspirin adalah 135°-136° C dan titik leleh aspirin yang diuji adalah 134 – 136 °C pada percobaan pertama dan 135 – 137 °C pada percobaan kedua. Dari hasil tersebut terlihat bahwa titik leleh aspirin uji dengan titik leleh di literature hampir sama/masih dalam rentang titik leleh menurut literatur. Hal ini menunjukkan bahwa aspirin yang diuji adalah aspirin murni menurut titik lelehnya dan tidak terdapat zat pengotor yang terdeteksi.
Pada uji kemurnian aspirin dengan plat KLT (Kromatografi Lapis Tipis) belum mendapatkan hasil yang maksimal, walaupun jarak fase gerak sampel (Rf) hampir sama dengan jarak senyawa aspirin murni, namun spot dari sampel maupun standar aspirin yang telah ditotolkan di KLT keluar dari jalur yang sudah ditentukan pada plat. Hal ini dapat dipengaruhi oleh:
Jarak penotolan senyawa terlalu dekat antara satu dengan yang lainnya Faktor kelarutan senyawa dalam pelarut
Faktor dari sifat pelarut, dalam praktikum kali ini pelarut yang digunakan terlalu polar.
Pada percobaan ini, spot dihasilkan dari penyemprotan FeCl3. Spot yang
diperoleh kemudian diukur panjangnya dari tempat penotolan, kemudian ditentukan nilai Rf masing-masing. Jika nilai Rf sebesar 1, secara teori menunjukkan bahwa sampel mempunyai distribusi dan faktor retensi sama dengan nol artinya sampel berpindah dengan kecepatan yang sama dengan fase gerak. Nilai ini merupakan nilai maksimum. Nilai Rf sampel adalah 0.8, Rf dan Rf standar aspirin adalah 0.7. Dekatnya selisih nilai Rf mengindikasikan bahwa sampel yang diuji adalah memenuhi kriteria standar aspirin murni. Rf adalah hasil dari jarak yang ditempuh sampel atau standar (spot) dibagi dengan jarak yang ditempuh fase gerak sampel secara keseluruhan (eluent).
V. KESIMPULAN
- Sampel aspirin (hasil praktikum) yang di uji adalah aspirin murni.
- Uji kemurnian sampel aspirin dengan meneteskan larutan FeCl3 pada plat tetes
menunjukkan warna kuning dan bukan ungu. Hal ini menunjukkan bahwa aspirin yang telah dibuat tidak lagi mengandung asam salisilat.
- Titik leleh sampel aspirin hampir sama/masih dalam rentang titik leleh menurut literatur yaitu 134°-136° C. Hal ini menunjukkan bahwa aspirin yang diuji adalah aspirin murni menurut titik lelehnya dan tidak terdapat zat pengotor yang terdeteksi. - Pada uji kemurnian aspirin dengan plat KLT (Kromatografi Lapis Tipis) belum
mendapatkan hasil yang maksimal, walaupun jarak fase gerak sampel (Rf) hampir sama dengan jarak senyawa aspirin murni yaitu 0.8 dan 0.7.
VI. DAFTAR PUSTAKA
Anonim. 2010. Farmakope Indonesia IV. Jakarta : Departemen Kesehatan Republik Indonesia
Fessenden, Fessenden. 1986. Kimia Organik Jilid 2. Jakarta : Penerbit Erlangga. (halaman 41)
Sastrohamidjojo. 1985. Kromatografi. Penerbit Liberty. Yogyakarta
Susilo, Jatmiko. 2005. Penetapan Kadar Co-Trimoksazol Yang Dilakukan Dengan Menggunakan Spektrofotometer Ultraviolet Secara Simultan – KLT. Jurnal Litbang. Universitas Muhammadiyah Semarang. Semarang
Tambunan A.P. 2011. Profil Kromatografi Cair Kinerja Tinggi Ekstrak Tempuyung Sonchus arvensis L. Dan Toksisitasnya Terhadap Artemia Salinan. Skripsi. Departemen Kimia Fakultas Matematika Dan Ilmu Pengetahuan Alam Institut Pertanian Bogor. Bogor
Gandjar, IG dan Rohman, A. 2007. Kimia Farmasi Analisis. Pustaka Pelajar. Yogyakarta
Rompas, Romario Aldi dan Hosea Jaya Edy dan Adithya Yudistira. Isolasi dan Identifikasi Flavonoid Dalam Daun Lamun (Syringodium isoetifolium). Program Studi Farmasi FMIPA UNSRAT Manado.