BAB II
TINJAUAN PUSTAKA
2.1Definisi dan Klasifikasi Sindroma Koroner Akut
Sindroma koroner akut (SKA) adalah istilah yang digunakan untuk mendiskripsikan gejala yang disebabkan oleh iskemik miokard akut. SKA yang menyebabkan nekrosis sel miokard disebut dengan infark miokard akut (IMA) (Thygensen dkk, 2012 ; Bender dkk, 2011 ; Antman, 2008)
Klasifikasi SKA meliputi yaitu :
1. Infark miokard akut non elevasi segmen ST (IMA NEST) 2. Infark miokard akut elevasi segmen ST (IMA EST) 3. Angina pektoris tak stabil (APTS)
(Bender dkk, 2011 ; Antman, 2008 ; Van de Werf dkk, 2012)
Diagnosis IMA EST ditegakkan apabila memenuhi kriteria antara lain ; adanya nyeri dada khas infark, dijumpai elevasi segmen ST yang persisten atau adanya left bundle branch block (LBBB) yang dianggap baru, peningkatan enzim jantung serial akibat nekrosis miokard (CKMB dan troponin), serta dijumpainya abnormalitas wall motion regional yang baru pada pemeriksaan ekokardiografi (Van de Werf dkk, 2008).
SKA yang tidak disertai dengan elevasi segmen ST digolongkan kedalam IMA NEST dan APTS. Apabila dijumpai peningkatan enzim jantung, maka penderita digolongkan ke dalam IMA NEST, dan apabila tidak dijumpai peningkatan maka digolongkan ke dalam APTS (Van de Werf dkk, 2008 ; Bender dkk, 2011).
2.2 Patogenesis IMA
Patogenesis dasar IMA adalah diawali dengan terbentuknya plak aterosklerosis yang kemudian terjadi erosi atau ruptur yang diikuti oleh respon trombosis. Pembentukan plak aterosklerosis merupakan proses yang berlangsung lama (sekitar 20-30 tahun sebelum timbulnya presentasi klinis SKA) (Rosen dkk, 2009; Bender dkk, 2011).
Proses aterosklerosis diawali oleh kerusakan (disfungsi) endotel. Beberapa faktor risiko antara lain merokok, hipertensi, diabetes mellitus, hiperkolesterolemia, dalam jangka panjang akan menyebabkan kerusakan endotel arteri koroner. (Atnmann dkk 2008; Bender dkk, 2011). Pada saat endotel mengalami kerusakan, makrofag akan menginfiltrasi endotel. Molekul low density lipoprotein (LDL) juga dapat masuk ke lapisan dinding pembuluh darah, yang kemudian diikat oleh makrofag membentuk foam cell.Foam cell merupakan dasar pembentukan plak aterosklerosis. Plak yang melekat pada dinding endotel arteri koroner akan terus membesar dan mengalami kalsifikasi. Pada suatu ketika plak tersebut dapat mengalami ruptur yang kemudian akan diikuti oleh timbulnya reaksi inflamasi lokal, vasokonstriksi koroner, aktivasi trombosit serta pengaktifan sistem koagulasi (Libby 2005, Kumar dkk, 2009).
Terdapat 2 proses trombosis yang saling berkaitan, yaitu hemostasis primer dan hemostasis sekunder. Hemostasis primer diawali dengan perlekatan trombosit pada dinding endotel yang rusak. Matriks subendotel yang terpapar aliran darah akan mengeluarkan elemen-elemen seperti faktor von Willebrand (vWF) dan kolagen. Kedua elemen ini akan berikatan dengan reseptor spesifik pada permukaan trombosit yaitu glikoprotein (GP)-Ib/IX dan GP VI. Ikatan antara GP Ib/IX-vWF dan GP VI-kolagen menyebabkan trombosit dapat melekat pada endotel yang mengalami injury. Reseptor (GP)-Ib/IX dan GP VI yang juga berperan dalam pengaturan adhesi trombosit dengan leukosit yang akan memicu proses vaskular lainnya seperti inflamasi dan aterosklerosis selanjutnya (Badimon dkk 2011, Kumar dkk 2011).
Setelah proses adhesi trombosit ke matriks ekstraselular terjadi, akan terjadi respon produksi mediator autokrin dan parakrin, seperti adenosine diphosphate (ADP), thrombin, epineprin serta asam arakhidonat. Elemen-elemen
ini bertanggung jawab untuk menstimulasi proses agregasi trombosit selanjutnya. Asam arakhidonat merupakan agonis yang berperan dalam produksi tromboksan A2 (TX A2).Tromboksan A2 yang dihasilkan tidak hanya dapat memicu agregasi trombosit selanjutnya, tetapi juga bersifat vasokonstriktor yang poten. Elemen ADP akan berikatan pada reseptor trombosit lainnya yaitu P2Y1, P2Y12 dan P2X yang akan mengakibatkan perubahan bentuk permukaan trombosit dan menimbulkan respon agregasi (Badimon dkk 2011, Kumar dkk 2011).
Hemostasis sekunder adalah pengaktifan sistem koagulasi yang akan menyebabkan trombus yang terbentuk menjadi lebih stabil. Sistem koagulasi melibatkan beberapa protein plasma dalam rangkaian proses yang disebut kaskade koagulasi yang berujung pada pembentukan trombin, suatu zat yang mengkonversi fibrinogen menjadi fibrin. Kaskade koagulasi terbagi atas 2 jalur, yaitu jalur intrinsik dan jalur ekstrinsik.Jalur intrinsik ((faktor XII, XIIa, XI dan XIa) diaktivasi oleh paparan komponen darah terhadap endotel yang mengalami kerusakan. Sedangkan jalur ekstrinsik diaktivasi oleh interaksi faktor VII dengan tissue factor yang dilepaskan oleh dinding endotel yang mengalami kerusakan. Kedua jalur ini kemudian mengaktifkan faktor X yang kemudian akan berinteraksi dengan faktor V, kalsium dan fosfolipid membentuk suatu kompleks yang mengkatalisir konversi protrombin menjadi trombin. Trombin mempunyai banyak fungsi pada proses hemostasis. Fungsi utama trombin adalah mengkonversi fibrinogen plasma menjadi fibrin. Fibrin yang telah mengalami konversi distabilisasi dengan fibrin lainnya melalui cross-link oleh faktor XIIIa sehingga terbentuk trombus besar yang lebih stabil. Fungsi trombin lainnya adalah mengaktivasi faktor V, VIII, XIII dan juga turut menstimulasi sekresi dan agregasi trombosit selanjutnya (Hansson, 2005; Hoffman, 2010; Kumar dkk, 2011).
2.3 EKG pada IMA EST
IMA didefinisikan sebagai kematian atau nekrosis sel miokard yang patologik disebabkan iskemia yang lama yang terjadi secara akut (Thygensen dkk, 2007). IMA EST merupakan salah satu spektrum IMA yang cukup sering terjadi (Bata, 2000 ; Fox, 2000). Diagnosis IMA EST ditegakkan apabila memenuhi kriteria berikut : adanya nyeri dada khas infark (durasi nyeri lebih dari
20 menit, tidak respon sepenuhnya dengan pemberian nitrat, nyeri dapat menjalar ke leher, rahang bawah atau lengan kiri, dapat disertai dengan gejala aktivasi sistem syaraf otonom seperti mual, muntah serta keringat dingin), adanya dijumpai elevasi segmen ST yang persisten (lebih dari 2 mm pada lead V2-V3 atau lebih dari 1 mm pada lead lainnya), atau adanya left bundle branch block (LBBB) yang baru atau yang dianggap baru pada pemeriksaan elektrokardiogram (EKG), peningkatan marker (enzim jantung) serial akibat nekrosis miokard (CKMB dan troponin) (Van de Werf 2012).
EKG merupakan rekaman grafik potensial listrik jantung yang direkam pada permukaan tubuh, yang merupakan perbedaan potensial listrik. Sebagai organ, jantung adalah otot tubuh yang memiliki keunikan karena sifatnya yang dapat membentuk impuls sendiri dan berkontraksi secara teratur. Impuls listrik terbentuk dalam sistem penghantaran listrik sehingga menimbulkan kontraksi otot jantung.Perekaman EKG dilakukan dengan menggunakan elektroda-elektroda yang diletakkan pada beberapa titik di permukaan tubuh, kemudian dihubungkan dengan alat perekam. Hubungan ini akan menyebabkan defleksi ke atas menghasilkan potensial positif dan defleksi ke bawah menghasilkan potensial negatif. Timbulnya perbedaan potensial ini dikarenakan ion-ion masuk melewati membran sel dan menyebabkan perbedaan tegangan sehingga sel miokard teraktivasi.Saat istirahat, cairan intra seluler sebuah sel bermuatan negatif terhadap jaringan disekitarnya (ekstra seluler) (Goldberger, 2015; Hurst, 2001).
Terdapat empat peristiwa elektrofisiologis yang berperan dalam pembentukan EKG yaitu :
1. Pembentukan impuls dan pacu jantung primer 2. Penghantaran impuls
3. Pengaktifan (depolarisasi) miokardium 4. Repolarisasi (relaksasi) miokardium
Pada awal depolarisasi terjadi perubahan permeabilitas membran sel yang cepat dengan masuknya ion Na (natrium) ke dalam sel yang akan mengakibatkan potensial aksi intra sel mengalami peningkatan tajam dari -90 menjadi +20 mV (fase 0).
Setelah fase depolarisasi tersebut, potensial aksi akan melambat secara perlahan ke potensial istirahat (repolarisasi), dimana fase 1 adalah proses kembalinya potensial intrasel cepat ke 0 mV akibat penutupan ion Na; fase 2 terjadi akibat masuknya ion Ca (kalsium) secara lambat ke dalam sel (plateu); fase 3 terjadi akibat pengembalian potensial intrasel ke potensial istirahat akibat pengeluaran ion K dari sel.
Gelombang kompleks QRS timbul akibat potensial aksi sel miokard ventrikel pada fase 0, fase 2 sesuai dengan segmen ST dan fase 3 sesuai dengan gelombang T (Goldman dkk, 1984; Hurst 2001). Gelombang QRS digambarkan dari urutan gelombang yang membentuk kompleks QRS tersebut. Defleksi negatif pertama disebut gelombang Q, gelombang positif yang pertama disebut gelombang R dan gelombang negatif pertama setelah gelombang R tersebut adalah gelombang S (Goldberger, 2015). Pola gelombang aktivasi ventrikel terdiri atas dua yaitu aktivasi septum dan aktivasi dinding ventrikel kiri.
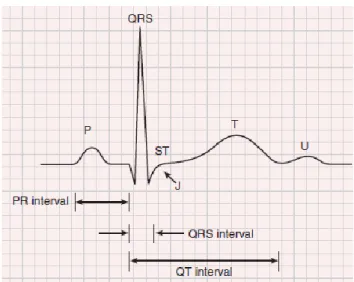
Segmen ST pada EKG adalah bagian EKG yang menggambarkan repolarisasi dari ventrikel. Segmen ST yang dimulai pada J point (pertemuan antara kompleks QRS dan segmen ST) hingga ke awal gelombang T. Pada kondisi normal segmen ST berada tepat di garis dasar EKG (baseline) (Becker, 1988, Goldberger, 2013). Polaritas segmen ST umumnya sama dengan polaritas QRS yang mendahuluinya. Sehingga gelombang T umumnya positif pada lead I, II, aVL dan lead prekordial lateral. Gelombang T akan negative pada lead aVR dan bervariasi pada lead III, lead V1 dan V2.
Gelombang U adalah gelombang amplitudo rendah yang mengikuti gelombang T biasanya < 0,1mV dan memiliki polaritas yang sama dengan gelombang T. dasar elektrofisiologisnya masih belum jelas, mungkin disebabkan oleh repolarisasi lambat serat-serat purkinye oleh aksi potensial yang panjang dari sel miokard. Gelombang ini paling sering terlihatpada denyut jantung rendah dan paling besar terlihat pada lead V1 dan V2 (Goldberger, 2015).
Gambar 2.1 Gelombang-gelombang dan interval EKG normal (Goldberger, 2015)
EKG merupakan salah satu kunci untuk diagnosis SKA. Temuan pada EKG bervariasi dan dipengaruhi empat faktor utama:
1. Durasi proses (akut atau kronis)
2. Luasnya (ukuran dan lokasi transmural)
3. Topografi (anterior, inferior, posterior, lateral atau ventrikel kanan) 4. Adanya kelainan lain yang mendasarinya (misalnya, LBBB,
WPWdan sebagainya) (Goldberger, 2015).
Peran EKG masih sangat penting dalam mendiagnosis secara dini pasien yang dicurigai sebagai IMA. EKG merupakan alat diagnosis pertama yang sangat bermanfaat, banyak tersedia dan umum dipakai.Berdasarkan anamnesis yang cermat dan pemeriksaan EKG awal dapat diambil keputusan terapi dengan cepat terhadap pasien dengan IMA. EKG merupakan alat bantu yang sederhana, murah, mudah dan tepat digunakan untuk mengevaluasi pasien dengan keluhan nyeri dada di unit gawat darurat secara rutin. Sensitivitas dari elevasi ST untuk diagnosis IMA antara 40-50% dan nilai sensitifitas ini akan bertambah tinggi apabila dilakukan rekaman EKG serial. (Estes,dkk 1999; Noris RM, 2000; Chia dkk, 2004).
Nilai ambang elevasi segmen ST untuk diagnosis IMA STE beragam, bergantungkepada usia, jenis kelamin dan dinding jantung yang terkena. Bagi pria, diagnosis ditegakkan jika terdapat elevasi segmen ST di V1-V3 ≥ 2mm pada
usia ≥ 40 tahun dan ≥ 2,5 mm pada usia < 40 tahun. Sementara itu, nilai ambang di sadapan lain adalah ≥ 1 mm. bagi wanita tanpa memandang umur, nilai ambang di V1-V3 adalah ≥ 1,5 mm dan ≥ 1 mm di sadapan lain. Bagi pria dan wanita, nilai ambang elevasi segmen ST di sadapan V3R dan V4R adalah ≥ 0,5 mm, kecuali pria < 30 tahun, nilai ambang ≥ 1mm dianggap lebih tepat ; nilai ambang disadapan V7-V9 adalah ≥ 0,5 mm (Tedjakusuma, 2010).
2.4 Patofisiologi Elevasi Segmen ST dan Depresi Segmen ST pada IMA Patofisiologi perubahan segmen ST pada IMA belum diketahui bagaimana mekanisme terjadinya secara pasti. Temuan yang paling awal dan konsisten selama fase akut adalah deviasi segmen ST sebagai akibat dariinjury yang baru..
Arus sitolik dan diastolik yang abnormal akibat adanya sel miokard yang mengalami injury yang berbatasan dengan zona infark diduga sebagai penyebab perubahan segmen ST pada IMA.
Iskemia akut yang berat dapat mengurangi potensial membran istirahat, mempersingkat durasi potensial aksi, dan menurunkan tingkat kenaikan dan amplitudo fase 0 di daerah iskemik. Gangguan tersebut menyebabkan gradient tegangan listik antara daerah normal dan iskemik. Gannguan arus listrik yang terjadi tampakpada permukaan EKG sebagai deviasi dari segmen ST.
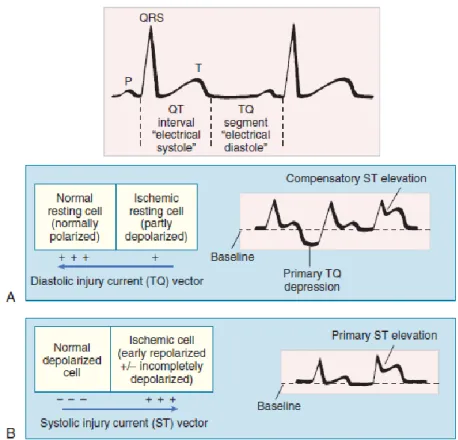
Gambar 2.2Patofisiologi elevasi segmen ST pada IMA (Goldberger dkk, 2015) 2.4.1 Teori Arus Diastolik
Elevasi segmen ST disebabkan perpindahan kebawah (downward) dari baseline diastolik listrik (segmen TQ dari EKG). Teori arus diastolik berpendapat bahwa sel miokard yang injury mampu berdepolarisasi, namun terdapat kebocoran ion potassium sehingga menyebabkan sel miokard yang mengalami injurytersebut tidak dapat berepolarisasi secara penuh. Karena permukaan sel-sel yang berdepolarisasi sebagian ini pada saat keadaan istirahat (diastolik) akan relatif lebih negatif dibandingkan area normal yang berepolarisasi penuh, oleh sebab itu arus ini diarahkan menjauh dari area iskemik yang lebih negatif, menyebabkan garis dasar pada lead EKG di daerah tersebut bergeser ke bawah, menghasilkan depresi segmen TQ. Karena mesin EKG hanya merekan posisi relatif dari pada voltase absolut, deviasi garis dasar ke bawah tersebut tidak tampak. Depresi segmen TQ pada gilirannya muncul sebagai elevasi segmen ST, karena mesin perekam EKG pada praktik klinis menggunakan “alternating current-coupled amplifier” yang secara otomatis mengkompensasi atau
menyesuaikan untuk setiap pergeseran negatif segmen TQ.Sebagai hasil dari efek elektronik ini, segmen ST akan proporsional meningkat.
Pada saat depolarisasi ventrikel, setelah semua sel miokard telah berdepolarisasi penuh ( termasuk yang berada di daerah injury), potensial listrik sekeliling jantung benar-benar nol. Tetapi dibandingkan dengan perubahan garis dasar kearah bawah tadi maka terlihat gambaran elevasi segmen ST. Kemudian miosit berepolarisasi, sel-sel injurykembali ke keadaan abnormal kebocoran ion potassium diastolik, dan EKG kembali pada garis dasar yang bergeser kebawah. 2.4.2 Teori Arus Sistolik
Teori arus sistolik berpendapat bahwa dalam rangka mengurangi potensial membran istirahat, kejadian injuryiskemik memperpendek durasi potensial aksi pada sel-sel yang rusak. Akibatnya sel-sel yang iskemik berepolarisasi lebih cepat dibandingkan miosit normal disekitarnya sehingga muncul voltase tinggi diantar kedua zona, yang membuat arus listrik mengarah menuju area iskemik. Voltase tinggi ini muncul selama interval ST di EKG menghasilkan elevasi ST pada lead di daerah infark.
Tiga faktor dapat membuat sel-sel miokard iskemik akut relatif positif dibandingkan dengan sel yang normal selama arus sistolik listrik (interval QT):
- Repolarisasi awal yang patologis (pemendekan durasi potensial aksi yang) - Penurunan kecepatan upstroke potensial aksi
- Penurunan amplitudo potensial aksi
Terdapatnya satu atau lebih dari yang tersebut diatas akan membentuk gradien tegangan antara daerah normal dan iskemik selama interval QT sehingga saat injury vektor akan diarahkan menuju wilayah iskemik. Mekanisme saat sistolik ini juga mungkin terkait sebagian dengan kebocoran kalium, akan mengakibatkan elevasi segmen STprimer, kadang-kadang dengan gelombang T positif yang tinggi (hiperakut).
Gambar 2.3 Pola vektor ST pada iskemia akut (Goldberger dkk, 2015)
Pada iskemia akut transmural, keseluruhan vektor ST biasanya bergeser ke arah luar (epikardial), dan elevasisegmen ST dan atau kadang-kadang hiperakut T yang dihasilkan lebih dari zona iskemik. Depresi segmen ST resiprokaldapat munculpada lead yang merefleksikan permukaan kontralateral.
Beberapa faktor dapat mempengaruhi amplitudo deviasi segmenST akut iskemik. Elevasiatau depresi segmen ST yang dalam di beberapa lead biasanya menunjukkan iskemia yang sangat parah atau luas. Sebaliknya, resolusi yang cepat dari elevasisegmen ST setelah terapi trombolitik atau intervensi koroner perkutan merupakan penanda spesifik sukses reperfusi. Selanjutnya, peningkatan relatif amplitudo gelombang T (hyperacute) dapat menyertai atau mendahului elevasi segmen ST dengan iskemia dengan atau tanpa infark.
2.5 Gambaran DSST inferior pada IMA EST anterior
DSST inferior yang signifikan didefinisikan sebagai pergeseran ke bawah yang landai (downsloping) atau horizontal ≥ 0,1 mV dalam setidaknya dua lead inferior (II, III dan aVF).
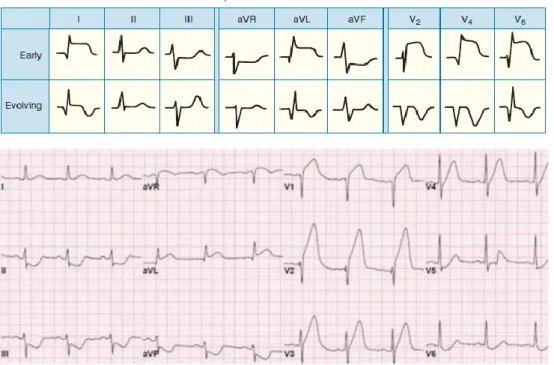
Gambar 2.4 : Infark miokard akut EST anterior yang disertai dengan DSST inferior (Goldberger dkk, 2015)
Terdapat beberapa penjelasan yang masih kontroversi tentang DSST resiprokal pada IMA EST ini yaitu antara lain : disebabkan oleh oklusi arteri koroner yang intermitten, hipotesis multivessel disease, hipotesis electrical reciprocity dan hipotesis infark yang luas (Brymer dkk, 1985)
2.6. Prognosis IMA EST anterior dengan DSST inferior
Pasien denganDSST inferior pada infark transmural anterior akut mengidentifikasi subset dari pasien dengan kerusakan yang luas, disfungsi ventrikel kiri yang lebih besar, komplikasiyang lebih sering di rumah sakit, anginapaska infark dan frekuensi multivessel yang lebih sering (Haraphongse M, 1984)
Abnormalitas Wall motionpada pasien IMA dengan DSST resiprokal dijumpai 17 dari 18 pasien (94%) pada penelitian yang dilakukan oleh Pichler dkk, 1982. Pichler juga mendapatkan hasil bahwa pasien IMA dengan DSST resiprokal memiliki fraksi ejeksi ventrikel kiri yang lebih rendah dan komplikasi selama rawatan di rumah sakit lebih banyak dibandingkan dengan pasien IMA tanpa adanya DSST resiprokal (Pichler dkk, 1982)
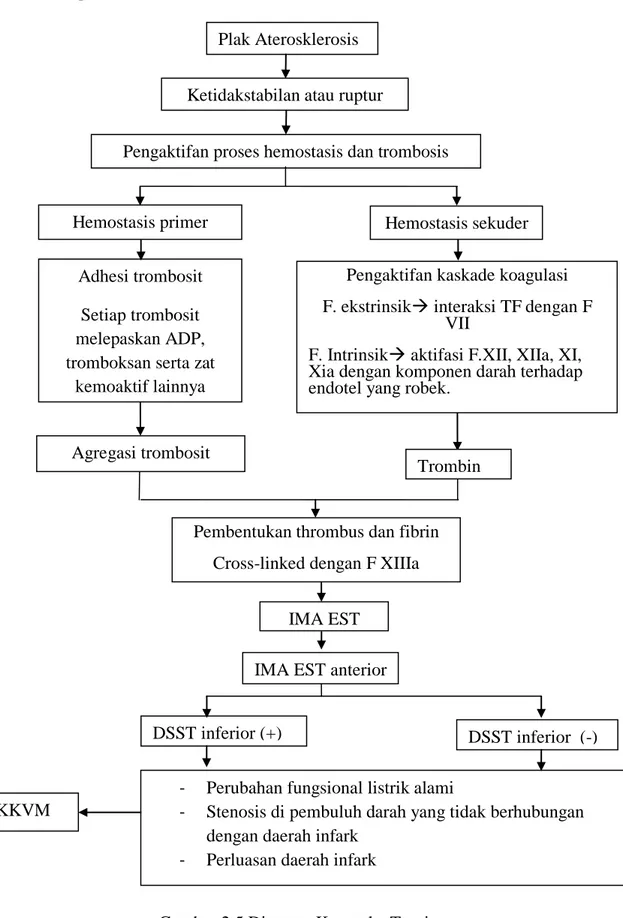
2.7 Kerangka Teori
Gambar 2.5 Diagram Kerangka Teori IMA EST anterior
IMA EST
DSST inferior (+)
- Perubahan fungsional listrik alami
- Stenosis di pembuluh darah yang tidak berhubungan dengan daerah infark
- Perluasan daerah infark
DSST inferior (-) Trombin
Agregasi trombosit
KKVM
Plak Aterosklerosis Ketidakstabilan atau ruptur
plak
Pengaktifan proses hemostasis dan trombosis
Hemostasis primer Hemostasis sekuder
Adhesi trombosit Setiap trombosit melepaskan ADP, tromboksan serta zat
kemoaktif lainnya
Pengaktifan kaskade koagulasi F. ekstrinsik interaksi TF dengan F
VII
F. Intrinsik aktifasi F.XII, XIIa, XI, Xia dengan komponen darah terhadap endotel yang robek.
Kedua jalur F.Xa
Pembentukan thrombus dan fibrin Cross-linked dengan F XIIIa
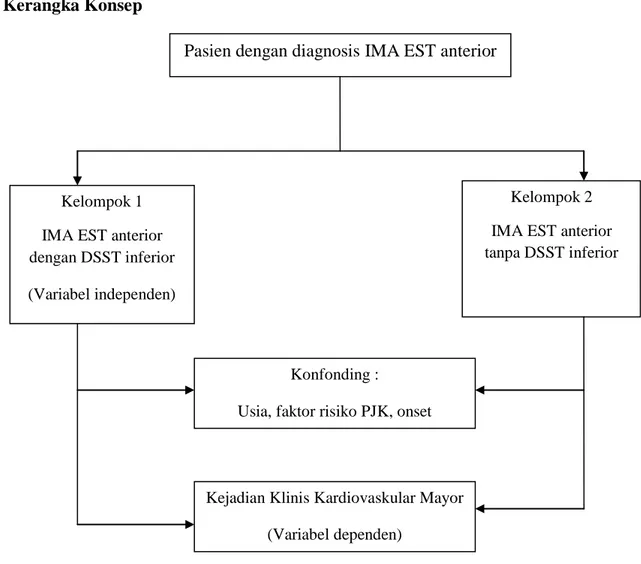
2.8 Kerangka Konsep
Gambar 2.6 Diagram Kerangka Konsep
Pasien dengan diagnosis IMA EST anterior
Kelompok 1 IMA EST anterior dengan DSST inferior (Variabel independen)
Kelompok 2 IMA EST anterior tanpa DSST inferior
Kejadian Klinis Kardiovaskular Mayor (Variabel dependen)
Konfonding :
Usia, faktor risiko PJK, onset 2.