Inkubasi 37 °C selama 5 menit
Bufer 250 - 250 - Enzim - 250 - 250
Inkubasi 37 °C selama 15 menit
Na2CO3 1000 1000 1000 1000
C – S C
Larutan enzim dibuat dengan melarutkan 1,0 mg α-glukosidase dalam larutan buffer fosfat (pH 7) yang mengandung 200 mg serum bovin albumin. Sebelum digunakan enzim diencerkan 25 kali dengan buffer fosfat (pH 7).
Campuran pereaksi terdiri atas ekstrak (kontrol negatif dan sampel) atau DMSO (kontrol positif dan blangko), substrat, dan buffer fosfat, diinkubasi 37°C selama 5 menit, kemudian ditambahkan enzim α-glukosidase (kontrol positif dan sampel) atau bufer fosfat (blangko dan kontrol negatif) dan diinkubasi kembali selama 15 menit. Reaksi enzim dihentikan dengan menambahkan 1 ml Na2CO3 dan absorbans dari p-nitrofenol
diukur pada panjang gelombang 400 nm dengan spektrofotometer.
Konsentrasi larutan standar akarbosa 1 % yang digunakan dibuat dari tablet glucobay yang dilarutkan dalam akuades dan HCl 2N (1:1). Perbandingan bobot tablet glucobay dengan akuades dan HCl 2N adalah 1 : 100. Kemudian larutan glucobay disentrifuse dan supernatannya digunakan sebagai standar. Larutan standar diperlakukan sama dengan ekstrak (Sugiwati 2006).
Setiap pengujian diulang sebanyak 3 kali. Masing-masing pengujian daya hambat ekstrak terhadap aktivitas α-glukosidase dihitung dalam % inhibisi dengan rumus,
% inhibisi = x 100%
C adalah absorbans larutan tanpa adanya ekstrak (kontrol) dan S adalah absorbans larutan dengan pemberian ekstrak dari sampel (Sugiwati 2006).
Separasi dengan Kromatografi Kilas Isolat yang paling aktif menghambat kerja enzim α-glukosidase kemudian diseparasi komponen penyusunnya dengan menggunakan kromatografi kilas. Sistem elusi yang digunakan adalah tipe isokratik dan untuk menentukan sistem eluen yang akan digunakan maka ditentukan sistem yang menghasilkan keterpisahan terbaik dengan KLT analitik. Eluen yang digunakan memiliki polaritas yang meningkat, yaitu dimulai dari pelarut non polar ke polar antara lain metanol,
aseton, dan kloroform. Eluen tunggal dengan pemisahan terbaik kemudian dikombinasikan satu dengan yang lainnya pada berbagai perbandingan sehingga diperoleh eluen dengan hasil pemisahan terbaik yaitu, kloroform:metanol nisbah 9:1.
Proses pemisahannya adalah terlebih dahulu pelarut dipompa ke dalam kolom untuk membasahi seluruh adsorben yang berada di dalam kolom hingga tidak muncul lagi gelembung udara dari dalam kolom. Pada contoh yang digunakan sebanyak 0,5 mg ekstrak komponen kering yang dilarutkan dalam kloroform. Setelah itu aliran pelarut dihentikan dan sampel dimasukkan ke dalam klep contoh menggunakan syringe. Kemudian aliran pelarut kembali dijalankan dengan sistem isokratik dengan laju 10 ml/menit selama proses pemisahan dan fraksi dikumpulkan dalam vial setiap 10 menit. Fraksi yang keluar dari kolom diperiksa hasil pemisahannya dengan KLT preparatif dengan menggunakan eluen yang sama pada saat pemisahan. Fraksi kromatografi kilas yang sama dikumpulkan dan fraksi-fraksi yang diperoleh kembali diuji kinerja inhibisi enzim α-glukosidasenya.
Pemeriksaan dengan Kromatografi Lapis Tipis
Pemisahan dengan kromatografi lapis tipis (KLT) preparatif dilakukan pada fraksi hasil pemisahan ekstrak dari kromatografi kilas, yaitu dengan menotolkan fraksi yang diperoleh tersebut pada plat KLT. Setelah kering dielusi dalam wadah yang telah dijenuhkan dengan eluen pengembang yang sama dengan kromatografi kilas. Spot hasil elusi diamati di bawah lampu UV pada panjang gelombang 254, 302, dan 365 nm.
HASIL DAN PEMBAHASAN Pencirian Bahan Baku
Penentuan kadar air berguna untuk mengetahui banyaknya kandungan air yang terdapat dalam contoh dan juga untuk mengetahui ketahanan contoh terhadap penyimpanan. Contoh yang baik disimpan dalam jangka waktu panjang adalah jika persen kadar airnya dibawah 10%, yaitu untuk menghindari terjadinya perubahan struktur kimia, pembusukan, dan tumbuhnya jamur (Depkes 1985). Hasil penentuan kadar air dari contoh serbuk buah mahkota dewa yang digunakan adalah sebesar 9,42% sehingga serbuk buah
7
mahkota dewa yang digunakan memiliki ketahanan terhadap waktu penyimpanan yang lama dan memiliki kemungkinan yang kecil dari terjadinya pembusukan (Lampiran 3).
Pada awal penelitian dilakukan penentuan pelarut terbaik dalam mengekstrak senyawa metabolit sekunder dari contoh buah mahkota dewa. Pelarut yang digunakan antara lain etanol 96%, n-heksana, dan air destilat. Tabel 2 menunjukkan hasil pengujian fitokimia dari ketiga pelarut tersebut dengan hasil terbaik pada pelarut etanol 96% berdasarkan banyaknya senyawa metabolit yang terdeteksi dan terekstraksi terutama pada kelas flavonoid. Adanya hasil penelitian Tadera et al. (2006) yang membuktikan aktivitas inhibisi α-glukosidase yang tinggi dari subkelas flavonoid juga menjadi salah satu dasar lebih lanjut dalam penelitian ini dalam memilih ekstrak etanol.
Pada umumnya senyawaan flavonoid yang terikat dengan gugus gula glikosida sangat mudah terikat dengan air karena adanya interaksi ikatan hidrogen sedangkan flavonoid yang bebas disebut sebagai aglikon lebih bersifat sedikit kurang polar. Perbedaan yang diperoleh antara hasil fitokimia flavonoid pada air dan etanol menunjukkan bahwa flavonoid lebih banyak yang terekstrak pada etanol. Selain itu perbedaan tersebut juga menunjukkan ekstrak etanol lebih banyak mengandung flavonoid yang bersifat sedikit kurang polar seperti aglikon flavonoid (Harborne 1987, Markham 1988, Markham & Andersen 2006) sehingga dari hasil tersebut dipilihlah etanol sebagai pelarut yang akan
digunakan pada ekstraksi contoh serbuk mahkota dewa pada penelitian ini.
Pencirian dan Uji Inhibisi Hasil Pemisahan Ekstrak
Pemisahan awal dilakukan dengan proses ekstraksi cair-cair untuk mendapatkan senyawaan dengan kepolaran yang berbeda (Lampiran 4). Contoh dihidrolisis terlebih dahulu dengan refluks pada suhu 80°C selama 40 menit sebelum dipartisi. Hidrolisis dilakukan untuk memutuskan ikatan glikosida yang ada pada senyawaan flavonoid sehingga dapat diperoleh aglikon flavonoid. Pemisahan yang terjadi pada ekstraksi adalah yang cukup polar akan larut dalam amil alkohol seperti antosianin dan ke polar yang lebih rendah akan larut dalam etil asetat seperti isoflavon, flavon, flavonol, flavonon sedangkan glikosida hasil hidrolisis akan larut dalam air (Harborne 1987, Markham 1988, Markham & Andersen 2006). Rendemen yang diperoleh dari ekstraksi tersebut fraksi etil asetat 17,86% sedangkan amil alkohol 7,69%.
Uji spesifik antosianin dan flavonol dilakukan terhadap fraksi amil alkohol dan etil asetat untuk mencari informasi senyawaan flavonoid yang mungkin ada pada fraksi-fraksi tersebut. Pada pengujian antosianin, fraksi amil alkohol menunjukkan dugaan adanya kelas sianidin dan pelargonidin serta adanya flavon dan flavonol. Fraksi etil asetat menunjukkan dugaan adanya flavon dan flavonol (Lampiran 5).
Pengujian lebih lanjut dari fraksi amil alkohol dan etil asetat adalah pengujian aktivitas inhibisi enzim α-glukosidase untuk mengetahui kemampuan fraksi dalam menghambat laju kerja enzim yang menguraikan polisakarida menjadi monosakarida. Hasil yang diperoleh menunjukkan fraksi amil alkohol memiliki aktivitas inhibisi lebih tinggi dibandingkan dengan fraksi etil asetat yaitu fraksi amil alkohol 40,04% dan etil asetat 25,26% dengan standar glucobay sebesar 97,45% (Tabel 3). Glucobay sendiri bekerja menghambat kerja enzim α-glukosidase dengan cara bersaing secara langsung dengan polisakarida untuk menutup sisi aktif dari enzim Tabel 3 Hasil uji inhibisi enzim
α-glukosidase.
Contoh Rerata Inhibisi (%)
Amil alkohol 40,04
Etil asetat 25,26
Glucobay 97,45
Tabel 2 Hasil uji fitokimia ekstrak air, etanol, dan n-heksana.
Uji Metabolit Air EtOH n-heksana Alkaloid Wagner +++ +++ +++ Mayer ++ ++ ++ Dragendrof +++ +++ +++ Triterpenoid - - - Steroid + + + Saponin ++ ++ ++ Flavonoid Metode Amil Alkohol ++ +++ - Metode H2SO4 ++ +++ + Hidrokuinon ++ +++ + Tanin +++ +++ - Keterangan
+++ : Intensitas tinggi/adanya endapan yang banyak ++ : Intensitas sedang/adanya endapan yang cukup
banyak
+ : Intensitas rendah/adanya sedikit endapan
(http://dailymed.nlm.nih.gov/dailymed/drugIn fo.cfm?id=6353#nlm34089-3).
Tabel 3 menunjukkan bukti bahwa secara empiris buah mahkota dewa memang memiliki aktivitas anti-hiperglikemik dalam proses penghambatan atau menginhibisi proses kerja enzim α-glukosidase dalam tubuh yang bertugas menguraikan polisakarida menjadi monosakarida yang akan masuk ke dalam darah.
Hasil pengujian ini juga didukung penelitian Sugiwati et al. (2006) yang juga berkaitan dengan aktivitas inhibisi buah mahkota dewa terhadap enzim α-glukosidase secara in-vivo dan in-vitro. Pada penelitian tersebut, Sugiwati berhasil menunjukkan aktivitas tertinggi hingga terendah berturut-turut ada pada ekstrak n-butanol, etil asetat, metanol, dan air. Pelarut air mendidih dan n-butanol juga diujikan secara in-vivo ke dalam tikus uji yang telah ditingkatkan gula darahnya menggunakan sukrosa. Secara umum hasil yang ditunjukkan dari aktivitas ekstrak yang dilakukan Sugiwati et al. (2006) cukup potensial dengan nilai inhibisi terendah pada rebusan air 33% dan tertinggi pada partisi n-butanol 69% dengan konsentrasi 50 ppm.
Gambar 7 Kromatografi lapis tipis fraksi (1) amil alkohol dan (2) etil asetat pada UV 302 nm eluen butanol, asetat, air (BAA).
Karakterisasi awal dengan kromatografi juga dilakukan terhadap kedua fraksi untuk mengetahui gambaran umum senyawa yang ada pada fraksi. Hasil uji KLT analitik terhadap hasil fraksinasi amil alkohol dan etil asetat dengan eluen BAA (butanol; asetat; air 4:1:5) (Gambar 7) sebagai salah satu analisis
kualitatif menunjukkan adanya beberapa senyawa pada masing-masing fraksi. Pada fraksi amil alkohol didapatkan dua spot dengan Rf 60% yang muncul pada sinar tampak dengan warna jingga tua dan Rf 88% yang muncul pada UV 365 nm dengan warna kuning. Fraksi etil asetat diperoleh 3 spot dengan Rf 88% (UV 365 nm), 76% (UV 302 nm), dan 17% (UV 302 nm) dengan warna berturut-turut kuning, jingga, dan jingga. Hasil KLTa tersebut menunjukkan adanya kesamaan senyawa pada kedua fraksi, yaitu yang muncul pada Rf 88% akan tetapi intensitas dari fraksi etil asetat untuk Rf tersebut sangat kecil. Hal ini yang mungkin menyebabkan adanya aktivitas inhibisi pada fraksi etil asetat meski hanya setengah dari fraksi amil alkohol.
Karakteristik UV pada fraksi amil alkohol juga dilakukan untuk menambahkan informasi awal yang diperlukan untuk pemisahan selanjutnya. Hasil yang menunjukkan puncak di 225, 300 dan 325 nm pada Gambar 8 (Lampiran 7) dan ditambah dengan munculnya lembayung lemah pada Rf 88% pada Gambar 7 akan mengarah ke hipotesis dugaan kelas flavanon, isoflavon, flavon, dan flavonol dari grup flavonoid dalam fraksi amil alkohol (Harborne 1987, Markham 1988).
Gambar 8 Ciri serapan UV/Vis contoh fraksi amil alkohol. Puncak 1 Puncak 2 Puncak 3 88% 76%
Fraksinasi Kromatografi Kilas Pemilihan eluen terbaik dilakukan dengan KLT analitik pada fraksi amil alkohol sebelum tahap kromatografi kilas. Pengujian dilakukan dengan mencoba fraksi pada eluen-eluen nonpolar yang digeser ke polar. Pelarut yang digunakan adalah toluena, kloroform, butanol, metanol. Meskipun pada posisi awal pemisahan banyak pigmen jingga yang hanya tertarik memanjang (Gambar 9), hasil yang diperoleh menunjukkan pemisahan yang terbaik ada pada kombinasi koloroform:metanol 9:1 yang menghasilkan paling banyak spot yang terpisah.
17% Mulai Selesai 1 60% 2
Gambar 9 Kromatogram KLTa fraksi amil alkohol pada sinar UV 302 nm.
Keterangan :
1. CH3Cl:MeOH 90:10 2. CH3Cl:Aseton 80:20
3. CH3Cl:MeOH 80:20 4. CH3Cl 100
Gambar 9 juga menjelaskan sedikit lebih lanjut mengenai kandungan yang terdapat dalam fraksi amil alkohol. Pada KLTa dengan eluen BAA (Gambar 7) hanya menunjukkan satu spot UV Rf 88% dan satu spot Vis Rf 60% sedangkan dengan pelarut yang lebih non polar (kloroform:metanol 9:1)(Gambar 9) menghasilkan 4 spot yang terdeteksi pada UV 302 nm disertai pigmen jingga yang tidak terpisah sehingga pemisahan yang terjadi menunjukkan pada spot Rf 60% KLTa BAA tidak terpisah pada saat menggunakan eluen kloroform:metanol (9:1) sedangkan spot Rf 88% KLTa BAA sebenarnya secara kualitatif mengandung 6 spot seperti yang tampak pada KLTa kloroform:metanol 9:1. Hasil pengukuran spektrun UV pada Gambar 8 merepresentasikan banyak senyawa flavonid yaitu dari kelas isoflavon, flavon, flavonol, dan flavanon yang memiliki panjang gelombang UV dan didukung juga dengan spot-spot (Gambar 9) yang kebanyakan tidak muncul di bawah sinar UV (Lampiran 6).
Pemisahan lebih lanjut dilakukan setelah mendapatkan eluen terbaik untuk memisahkan fraksi amil alkohol. Pemisahan dilakukan dengan sistem kromatografi kilas yang bekerja seperti kromatografi kolom terbuka, namun proses pemisahannya dipercepat dengan eluen yang dipompa sehingga efektivitas waktu pemisahan dan penggunaan eluen akan meningkatkan.
Eluen yang terpilih adalah kloroform dengan metanol (9:1) dengan sampel yang dipisahkan sebanyak 1 gram pada packing kolom Buchi catridge system c-675 diameter 12 mm panjang 15 mm dengan fase diam silika 40-63 μm pori 60Å (Si60). Laju alir yang digunakan antara 5 ml/min dan eluen yang keluar ditampung setiap 10 ml selama 2 jam sehingga diperoleh 60 fraksi dari pemisahan tersebut.
Akan tetapi pada saat dilakukan pemisahan ternyata hanya senyawaan non pigmen yang bisa terpisahkan. Pigmen warna jingga tua terjerap kuat pada awal kolom meski sudah dielusi berulang kali dengan metanol. Warna profil pemisahannya sendiri yang dikumpulkan pada fraksi dimulai dengan warna kuning muda pada fraksi 1 hingga 16 kemudian berangsur menjadi tidak berwarna hingga fraksi 60.
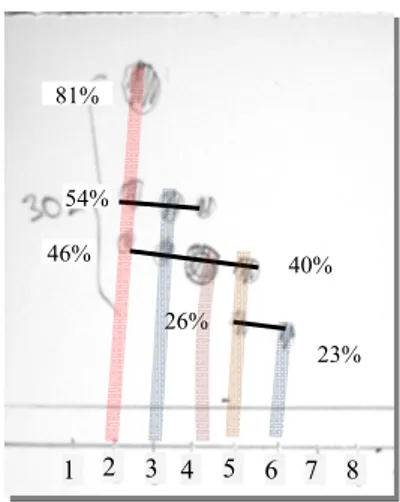
Gambar 10 KLTa fraksi 1-8 pemisahan kromatografi kilas.
Keterangan
Grup 1 : Fraksi 2 Grup 2 : Fraksi 3 + 4 Grup 3 : Fraksi 5 Grup 4 : Fraksi 6
Analisis Fraksi
Fraksi yang diperoleh kemudian diuji dengan KLTa untuk mengetahui pola pemisahan yang terjadi dan diperoleh 5 fraksi yang memiliki spot, yaitu fraksi 2 sampai 6 (Gambar 10). Dua di antara fraksi-fraksi tersebut ternyata memiliki Rf yang berhimpitan, yaitu pada fraksi 3 dan 4 sehingga keduanya digabung dan menghasilkan fraksi akhir aktif sebanyak 4 buah yang kemudian disebut grup. Fraksi yang diperoleh adalah grup 1 (fraksi 2; 3 spot; Rf 81: 54: 46), grup 2 (fraksi 3 & 4; 2 spot; Rf 54: 40), grup 3 (fraksi 5; 2 spot; Rf 40: 26), grup 4 (fraksi 6; 1 spot; Rf 23). Keempat grup
1 2 3 4 1 2 3 4 5 6 7 8 23% 26% 40% 46% 54%
9
81%tersebut kemudian diuji aktivitas inhibisi enzim α-glukosidase untuk mengetahui fraksi yang paling aktif dan untuk melanjutkan ketahap analisis senyawa.
Hasil yang diperoleh dari pengujian keempat grup tersebut terhadap aktivitas inhibisi enzim α-glukosidase, persen inhibisi yang diperoleh dari fraksi 1 sampai dengan 6 berkisar antara 6–10% dengan persen tertinggi terdapat pada grup 1 sebesar 9,72% (Tabel 4). Aktivitas ini lebih kecil dari larutan awalnya, yaitu 40,04%. Hasil yang diperoleh tersebut secara langsung tidak dapat disimpulkan karena hasilnya menghasilkan keterulangan yang tidak baik di keempat ulangan grup. Hal ini diduga karena pemisahan yang terjadi pada kolom kromatografi kilas tidak baik akibat interaksi fase diam dan gerak begitu kuat sehingga masih banyak senyawaan yang tertinggal pada fase diam sehingga sebagian lain terpisahkan begitu cepat yang ditunjukkan oleh sedikitnya keterpisahan yang muncul pada fraksi. Selain itu tidak sempurnanya kelarutan contoh pada eluen juga diperkirakan menyebabkan pemisahan pada kolom kromatografi kilas menjadi tidak sempurna. Adanya aktivitas senyawa adanya kemungkinan sifat senyawa yang jika dipisahkan dari kelompok senyawaannya maka aktivitas enzimatisnya menjadi tidak optimal atau berkurang turut menjadi kemungkinan buruknya hasil pengujian.
SIMPULAN
Buah mahkota dewa memiliki potensi aktivitas inhibisi enzim α-glukosidase pada fraksi amil alkoholnya sebesar 40,04%. Fraksi amil alkohol berdasarkan karakteristik
spektrofotometer UV/vis mengandung campuran kelas isoflavon, flavon, flavonol, dan flavanon dari grup metabolit sekunder flavonoid. Hasil fraksinasi kromatografi kilas aktivitasnya menurun secara signifikan dan memiliki keterulangan yang tidak baik.
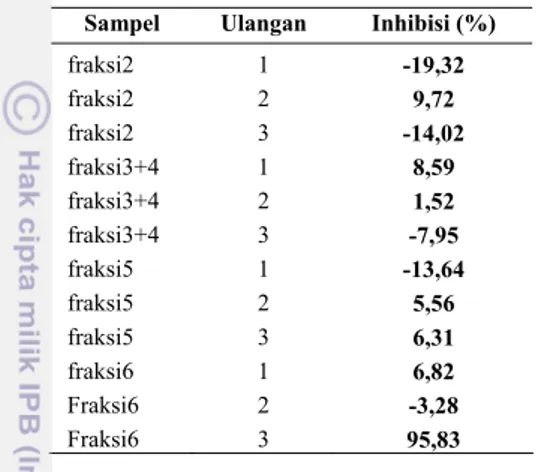
Tabel 4 Uji inhibisi enzim α-glukosidase pada fraksi kromatografi kilasamil alkohol.
SARAN
Sampel Ulangan Inhibisi (%)
fraksi2 1 -19,32
Perlu dilakukan studi lebih lanjut mengenai proses pemisahan dan isolasi yang tepat dari senyawaan flavonoid dari buah mahkota dewa terutama dalam hal pemilihan eluen kromatografi. Selain itu perlu dilakukan penelitian lebih jauh mengenai aktivitas dari senyawaan tunggal atau kelompok yang menghambat enzim α-glukosidase dari buah mahkota dewa.
fraksi2 2 9,72
fraksi2 3 -14,02
fraksi3+4 1
DAFTAR PUSTAKA
Berg JM, Tymozcko JL, Stryer L. 2002. Biochemistry 5th Edition. New York: W.H. Freeman & Co Ltd.
Dailymed. 2008. Precose (acarbose) Tablet (Bayer Pharmaceutical Corporation). [terhubung berkala]. http://dailymed. nlm.nih.gov/dailymed/drugInfo.cfm?id =6353#nlm34089-3 [Feb 2009]
[Depkes] Departemen Kesehatan Republik Indonesia. 1985. Cara Membuat Simplisia. Jakarta: Departemen Kesehatan.
[Depkes] Departemen Kesehatan Republik Indonesia Ditjen POM. 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan.
Diabetesmonitor. 2006. Information about acarbose (precose). [terhubung berkala].http://www. diabetesmonitor. com/acarbose.htm [Feb 2009]
Harbone JB. 1987. Metode Fitokimia, Penuntun Cara Modern Menganalisis Tumbuhan. Bandung: Penerbit ITB. Hendayana S, Kadarohman A, Sumarna AA,
Supriatna A. 1994. Kimia Analitik Instrumen. Edisi ke-1. Semarang: IKIP Semarang Press. 8,59 fraksi3+4 2 1,52 fraksi3+4 3 -7,95 fraksi5 1 -13,64 fraksi5 2 5,56 fraksi5 3 6,31 fraksi6 1 6,82 Fraksi6 2 -3,28 Fraksi6 3 95,83