BAB 2
TINJAUAN PUSTAKA
2.1 Mikroorganisme Termofilik
Sumber air panas merupakan salah satu hasil aktivitas geotermal. Air panas yang keluar melalui rekahan-rekahan bumi mengalir membentuk kolam-kolam kecil dan aliran yang menyerupai sungai (Yani, 2003). Air panas mengandung kadar mineral yang tinggi seperti sulfur dan kalsium. Sumber air panas memiliki pH asam sampai alkali. Air panas yang keluar mengandung hidrogen sulfat, karbon dioksida, senyawa-senyawa karbon organik dengan berat molekul rendah, metana, hidrogen, amonia dan elemen-elemen garam seperti sulfur, besi, karbonat fosfor, bikarbonat dan sebagainya (Brock, 1986).
Sejumlah bakteri termofilik yang telah ditemukan ternyata berasosiasi dengan berbagai lingkungan geotermal (Brock, 1986). Mikroorganisme termofilik hidup di lingkungan ekstrim dengan suhu di atas 50 °C (Rudiana, 2003). Beberapa bakteri termofilik seperti Sulfolobus dapat ditemukan pada sumber air panas dengan pH rendah dan kandungan sulfur yang tinggi. Pyrodictium dapat ditemukan pada sumber air panas dengan pH netral, sedangkan Methanococcus jannasch yang tergolong bakteri termofilik metanogen berhasil diisolasi dari zona laut dalam (Brock, 1986). Genus Bacillus, Clostridium,
Thermoactinomyces, Methanobacterium dan kemungkinan terdapat beberapa genus lain sering ditemukan pada suhu sampai 70 ºC (Zubaidah, 2000).
Pada umumnya kelompok bakteri termofilik mempunyai struktur sel yang
memiliki beberapa kelebihan dibanding kelompok bakteri lainnya (Zubaidah, 2000). Bakteri termofilik memiliki kandungan lipid yang tinggi asam lemak jenuh. Struktur tersebut memungkinkan membran tetap stabil dan fungsional pada suhu tinggi. Protein yang tahan panas didukung oleh peningkatan jumlah ikatan ion antara asam amino basa dan asam, dan memiliki struktur yang sangat hidrofobik. Struktur tersebut kemungkinan dapat menurunkan rusaknya ikatan ionik pada struktur protein, dan protein pada organisme termofilik mempunyai ketahanan alami dalam cairan sitoplasma (Madigan et al. 2009). Stabilitas panas
terjadi akibat interaksi multipoint dengan komponen sel lain dan adanya faktor spesifik penstabil panas (Nam-Soo & Kim, 1991).
2.2 Kitin
Kitin merupakan polimer dari β-1,4 N-asetil-D-glukosamin (Gambar 1.) dan merupakan biopolimer terbesar kedua setelah selulosa (Flach et al. 1992). Lebih kurang 10 gigaton (1 x 1013 kg) kitin disintesis dan didegradasi di biosfer (Muzzarelli, 1999).
Gambar 1. Struktur Kitin (Gooday, 1990)
Kitin merupakan struktur utama penyusun dinding sel fungi (Blumenthal & Roseman, 1957), dan ditemukan juga pada eksoskleton serangga, fungi, yeast, alga, serta golongan
crustacea seperti kepiting, udang kecil dan lobster (Bhattacharya et al. 2007). Pada hewan, kitin merupakan struktur rigid yang terdapat pada eksoskeleton. Hal ini disebabkan pada rantai polimer N-asetil-glukosamin terdapat ikatan hidrogen antar molekul membentuk mikrofibril menghasilkan struktur yang stabil dan rigid, tidak larut dalam air sehingga dapat mengkristal (Shaikh & Deshpande, 1993).
2.3 Kitinase dan Pemanfaatannya
Kitinase adalah enzim yang mampu menghidrolisis kitin menjadi N-asetilglukosamin. Degradasi kitin dapat dilakukan oleh organisme kitinolitik dengan melibatkan enzim kitinase melalui dua jalur yaitu, pertama adalah degradasi kitin oleh mekanisme kitinolitik yang menghidrolisis ikatan β-1,4-glikosida dan kedua dihidrolisis oleh kitosanase (Gooday, 1990).
1. Eksokitinase (EC. 3.2.1.29) dinamakan juga kitobiosidase atau kitin-1,4-ß-kitobiosidase, yaitu enzim yang mengkatalisis secara aktif pembebasan unit-unit diasetilkitobiose tanpa ada unit-unit monosakarida atau oligosakarida yang dibentuk.
2. Endokitinase (EC. 3.2.1.14) yaitu enzim yang memotong secara acak ikatan ß-1,4 bagian internal mikrofibril kitin. Produk akhir yang terbentuk berupa oligomer pendek N-asetilglukosamin (GlcNAc) yang mempunyai berat molekul rendah seperti kitotetraose. Produk yang dihasilkan bersifat mudah larut.
3. ß-1,4-N asetilglukosamidase (EC. 3.2.1.30) adalah suatu enzim kitinolitik yang bekerja pada pemutusan diasetilkitobiose, kitotriose dan kitotetraose dengan menghasilkan monomer-monomer GlcNAc.
Kitinase merupakan salah satu enzim yang menarik untuk diisolasi karena kemampuannya untuk menghidrolisis kitin menjadi turunan kitin yang sangat banyak manfaatnya. Peranan kitinase sebagai pengendali hayati sangat menjanjikan untuk dimanfaatkan sebagai biopestisida yang aman dan ramah lingkungan (Terayama et al. 1993). Kitinase dapat mendegradasi kitin yang merupakan komponen utama dinding sel jamur. Pada tumbuhan, kitinase digunakan sebagai pertahanan dalam melawan serangan patogen yang mengandung kitin. Pemanfaatan isolat kitinolitik lokal asal Sumatera Utara telah digunakan sebagai pengendalian jamur (Suryanto & Munir 2006). Suryanto et al. (2010) melaporkan bakteri kitinolitik mampu menghambat pertumbuhan jamur Fusarium pada benih cabai. Dewi (2011) menunjukkan bahwa 6 isolat bakteri kitinolitik yang diisolasi dari lingkungan perairan budidaya ikan gurami yaitu PB05, PB08, PB13, PB14, PB15, dan PB17 mampu menurunkan tingkat mortalitas serta meningkatkan daya tetas telur yang diinfeksi Saprolegnia sp.
Kitinase juga berperan sebagai agen biokonversi limbah kitin menjadi protein sel tunggal (Kobayashi et al. 1997) atau senyawa turunannya (Rattanakit et al. 2002). Kitinase dari Aspergillus sp. 501 dan Streptomyces A8.13 yang diproduksi dengan fermentor dapat meningkatkan proses hidrolisis kitin menjadi senyawa turunanannya berupa N-asetil-D-glukosamin (GlcNAc) dan D-N-asetil-D-glukosamin (Widhyastuti, 2010) yang banyak digunakan untuk terapi penyakit seperti osteoarthritis, gastritis, alergi makanan dan digunakan sebagai prebiotik. GlcNAc telah diaplikasikan dalam industri pangan yaitu dengan penambahannya ke dalam yoghurt dan teh hijau dengan dosis 0,5-1,6 gram (Aiba, 2009).
Aplikasi kitinase dapat dilakukan melalui kloning gen penyandi kitinase. Dua Gen kitinase yaitu chi A dan chi B dari Serratia marcescens disisipkan ke E. Coli kemudian ke
Pseudomonas fluorescens dan Pseudomonas putida. Hasil menunjukkan strain Pseudomonas
memiliki aktivitas kitinase (Suslow & Jones, 1988). Downing et al. (2000) melaporkan, kloning gen kitinase dari Serratia marcescens ke bakteri Pseudomonas aeruginosa mampu menekan hama penggerek batang pada tebu, Eldana saccharina. Hasil manipulasi genetik dapat meningkatkan jumlah mikroorganisme potensial yang menghasilkan kitinase dalam kontrol patogen tanaman.
2.4 Bakteri Kitinolitik
Sejumlah bakteri ditemukan memiliki aktivitas kitinolitik. Park et al. (2000) berhasil mengisolasi bakteri kitinolitik Vibrio sp. 98CJ11027 dari perairan laut Korea. Bakteri kitinolitik B2-4 dan NA S4-1 berhasil diisolasi dari Gunung Bromo Jawa Timur yang menunjukkan aktivitas kitinolitik tertinggi setelah diinkubasi pada waktu satu dan dua hari (Soeka & Sulistiani, 2011). Hasil isolasi dari sumber air panas Tinggi Raja, Kabupaten Simalungun, Sumatera Utara diperoleh lima isolat yang memiliki aktivitas kitinolitik (Dewi, 2008). Bakteri termofilik Ralstonia sp. A471 telah berhasil diisolasi dari kompos dan diuji aktivitas kitinasenya (Ueda et al. 2005).
Bushan (2000) berhasil mengisolasi Bacillus sp. BG-11 dari lingkungan alkali termal. Pada sumber air panas Danau Ranau diperoleh genus Bacillus yang memiliki aktivitas kitinolitik (Muharni, 2010), Bacillus licheniformis MB-2 juga berhasil diisolasi dari Danau Tompaso, Sulawesi Utara (Toharisman, 2004), dan Hamid et al. (2012) melaporkan S. maltophila memproduksi kitinase termostabil dari tanah Jamia Hamdard, New Delhi.
2.5 Karakteristik Kitinase dari Bakteri Kitinolitik
Suhu dan pH sangat berpengaruh terhadap aktivitas enzim. Pada suhu yang tinggi enzim yang merupakan protein dapat terdenaturasi. Semakin tinggi suhu, proses inaktivasi enzim meningkat (Winarno, 1995).
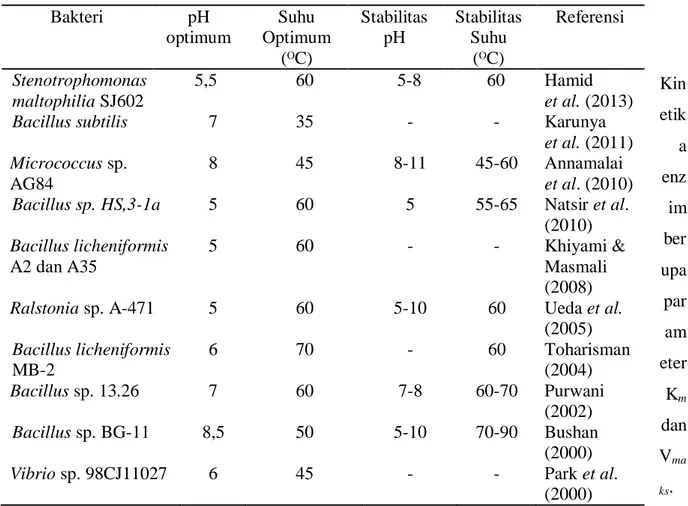
Setiap enzim memiliki kisaran pH optimum yaitu kisaran pH dimana enzim menunjukkan aktivitas maksimum dengan stabilitas yang tinggi (Fresht, 1985). Peningkatan aktivitas enzim pada pH optimum dapat dihubungkan dengan adanya perubahan ionisasi dalam gugus ionik enzim pada sisi aktif sehingga bentuk sisi aktif menjadi lebih efektif dalam mengikat dan mengubah substrat menjadi produk (Webb & Dixon, 1979). Beberapa karakter kitinase dari beberapa bakteri kitinolitik dapat dilihat pada Tabel 1.
Tabel 1. Karakter Kitinase dari Beberapa Bakteri Kitinolitik
Kin etik a enz im ber upa par am eter Km dan Vma ks.
Nilai Km dan Vmaks bersifat spesifik dan berbeda satu sama lain pada enzim. Nilai Km digunakan untuk menentukan ukuran afinitas suatu enzim dalam menghidrolisis substrat yang merupakan indikator kekuatan kompleks enzim substrat. Nilai Km lebih kecil, maka kompleks enzim substrat mantap dan memiliki afinitas enzim terhadap substrat lebih tinggi, sedangkan jika nilai Km lebih besar maka afinitas enzim terhadap substrat lebih rendah (Bintang, 2010).
Dari hasil penelitian yang dilakukan Dahiya et al. (2005) diperoleh nilai Km dan Vmax kitinase Enterobacter sp. NRG4 adalah sebagai berikut 1,43 mg/ml dan 83,33 µM/µg jam
Bakteri pH optimum Suhu Optimum (ᴼC) Stabilitas pH Stabilitas Suhu (ᴼC) Referensi Stenotrophomonas maltophilia SJ602 5,5 60 5-8 60 Hamid et al. (2013)
Bacillus subtilis 7 35 - - Karunya
et al. (2011)
Micrococcus sp. AG84
8 45 8-11 45-60 Annamalai
et al. (2010)
Bacillus sp. HS,3-1a 5 60 5 55-65 Natsir et al.
(2010) Bacillus licheniformis A2 dan A35 5 60 - - Khiyami & Masmali (2008)
Ralstonia sp. A-471 5 60 5-10 60 Ueda et al.
(2005) Bacillus licheniformis MB-2 6 70 - 60 Toharisman (2004) Bacillus sp. 13.26 7 60 7-8 60-70 Purwani (2002) Bacillus sp. BG-11 8,5 50 5-10 70-90 Bushan (2000) Vibrio sp. 98CJ11027 6 45 - - Park et al. (2000)
untuk hidrolisis kitin, 1,41 mg/ml dan 74,07 µM/µg jamuntuk koloidal kitin, 1,8 mg/ml dan 40 µM/µg jamuntuk regenerasi kitin, dan 2 mg/ml dan 33,33 µM/µg jam untuk kitin glikol. Harini & Martiningrum (2006) melaporkan, Vibrio fluvialis memiliki Km sebesar 7,778% dan Vmaks sebesar 0,066 mmol per menit. Karakterisasi isolat Streptomyces sp. IK memiliki enzim kitinase dengan nilai Vmaks 4,26 μg/jam, nilai Km 2,92 mg/ml (Nugroho, 2006).