Diniatik, dkk
PENENTUAN KADAR FLAVONOID TOTAL FRAKSI ETIL ASETAT DAN FRAKSI KLOROFORM HASIL HIDROLISIS EKSTRAK ETANOLIK DAUN KEPEL
(Stelechocarpus burahol (Bl.) Hook f. & Th.) DENGAN METODE
SPEKTROFOTOMETRI MENGGUNAKAN RUTIN SEBAGAI PEMBANDING Diniatik1,2, Suwijiyo Pramono1, Sugeng Riyanto2
Fakultas Farmasi Universitas Gadjah Mada Fakultas Farmasi Universitas Muhammadiyah Purwokerto
ABSTRAK
Daun Kepel telah dimanfaatkan untuk mengatasi asam urat dan menurunkan kadar kolesterol. Buahnya berkhasiat sebagai antioksidan dan daunnya sekarang dipercaya untuk mengatasi penyakit diabetes. Laporan penelitian mengindikasikan bahwa senyawa yang berperan pada aktivitas ini adalah golongan senyawa flavonoid. Penelitian ini bertujuan untuk mendapatkan data kadar flavonoid dalam daun kepel, dengan menggunakan rutin sebagai senyawa pembanding. Daun Kepel diperoleh dari Kabupaten Sleman Propinsi Yogyakarta. Ekstraksi dilakukan dengan menggunakan metode maserasi dengan etanol 70% sebagai cairan penyari. Ekstrak etanol daun kepel dihidrolisis dengan menggunakan HCl 1M, kemudian difraksinasi dengan kloroform dan etil asetat. Penetapan kadar flavonoid total menggunakan metode spektrofotometri dengan larutan pembanding rutin dan aluminium klorida P 10%, 0,1 ml natrium asetat 1M sebagai pembentuk kompleks. Hasil penelitian menunjukkan bahwa kadar rata-rata flavonoid total dalam ekstrak etanol daun kepel adalah 9,8 %(b/b), fraksi etil asetat 75,14%(b/b) dan fraksi kloroform 3,15 %(b/b).
Kata kunci: Stelechocarpus burahol (Bl.) Hook f. & Th.., flavonoid total, rutin, spektrofotometri.
ABSTRACT
Kepel leaf has been used to overcome gout and capable of lowering cholesterol level. The fruits are used as an antioxidant and leaves are now believed to overcome diabetes. Research reports indicate that compounds that play a role in this activity is a class of flavonoid compounds. This study aims to get the data content of flavonoids in S. burahol leaves based on the levels regularly as standard. Kepel leaves obtained from the Sleman District, Province of Yogyakarta. Extraction is done by using maceration method, as solvent is 70% ethanol, total flavonoid assay using spectrophotometric method with reference solution routine, sliding reactants AlCl3 10% and sodium acetate 1M. Ethanolic extract of S. burahol leaves were hydrolyzed by using HCl 1 M, then fractionated with chloroform as first solven, therefore ethyl acetate as second solven. The result showed that the total flavonoid content by spectrophotometric method in ethanolic extract of S. burahol leaves were 9.8% (w/w), ethyl acetate fraction 75.14% (w/w) and chloroform fraction 3.15% (w/w).
Key words: Stelechocarpus burahol (Bl.) Hook f. & Th., total flavonoid, routine, spectrophotometric.
Diniatik, dkk PENDAHULUAN
Daun kepel dimanfaatkan secara empiris untuk mengatasi asam urat dan menurunkan kadar kolesterol. Buahnya mempunyai kandungan vitamin C yang tinggi sehingga berkhasiat sebagai antioksidan dan daunnya sekarang dipercaya untuk mengatasi penyakit diabet (Anonim, 2013; Sunarni, 2007). Pengujian aktivitas antioksidan dengan menggunakan DPPH menunjukkan bahwa ekstrak etil asetat buah dan ekstrak n butanol bunga kepel memiliki aktivitas yang baik yaitu IC50 29,12 ug/ml dan IC50 22,44 ug/ml (Tisnadjaja dkk, 2006). Secara in vivo dilaporkan adanya aktivitas antihiperurisemia ekstrak etanol dan ekstrak heksan dari daun kepel yang potensinya setara dengan alopurinol pada uji penghambatan xantin oksidase dengan menggunakan tikus (Purwantiningsih dkk, 2010). Penggunaan empiris di masyarakat dan hasil penelitian yang diuraikan diatas sangat berkaitan dengan kandungan senyawa dalam tanaman ini. Hasil analisis mutu daun kepel yang diambil dari beberapa daerah, mengandung saponin, alkaloid, tanin, fenolik, flavonoid, triterpenoid, steroid,dan glikosida. Analisa daun dari tanaman kepel di Purworejo yang umurnya lebih dari 100 tahun, dihasilkan kandungan fitokimia yag lebih lengkap dibandingkan dengan tanaman yang lebih muda. Daun kepel yang berasal dari daerah Jawa Barat (Bogor dan Gunung Nagara, Garut), kandungan taninnya tidak terdeteksi, sedangkan daun yang berasal dari Jawa Tengah semua mengandung tanin (Anonim, 2013).
Pada penelitan ini diharapkan dapat diketahui kadar flavonoid total fraksi etil asetat dan fraksi kloroform hasil hidrolisis ekstrak daun kepel serta kadar flavonoid total dari ekstrak etanol daun kepel. Perlakuan hidrolisis terhadap ekstrak ini karena flavonoid di dalam tanaman pada
umum terdapat dalam bentuk glikosida. Senyawa glikosida flavonoid ini pada saat dikonsumsi akan terhidrolisis di lambung menjadi bentuk aglikonnya. Oleh sebab itu perlu dianalisis secara kuantitatif kadar flavonoid dalam bentuk aglikon dengan cara menghidrolisis ekstrak etanol daun kepel. Hidrolisis dilakukan dengan menggunakan asam klorida pada pH 2-3 dengan tujuan memecah glikosida flavonoid menjadi aglikon flavonoid dan gulanya (Hasan & Tahir, 2005; Iwashina & Kokubugata, 2012; Nazaruk, 2003; Matlawska & Sikorska, 2005).
METODE PENELITIAN
Penelitian ini dilakukan dengan cara sebagai berikut:
Determinasi tumbuhan. Tanaman kepel yang digunakan dalam penelitian dideterminasi di Laboratorium Biologi Farmasi Fakultas Farmasi, Universitas Muhammadiyah Purwokerto. Hasil determinasi menyatakan bahwa spesimen tumbuhan tersebut adalah benar – benar tanaman Stelechocarpus burahol, (Bl.) Hook f. & Th. dari famili Annonaceae. Hasil determinasi tersebut berdasarkan buku Flora of Java Vol II (Backer & Van Den Brink, 1965).
Penyiapan alat dan bahan. Daun S. burahol diambil dari kabupaten Sleman, Yogyakarta. Pengeringan dilakukan dengan meletakkan bahan yang telah dicuci bersih pada tampah, kemudian dijemur dibawah sinar matahari dengan ditutupi dengan kain hitam supaya tidak terkena sinar matahari langsung sampai kering. Simplisia yang telah kering (dengan memperhatikan persyaratan kandungan air maksimal dalam simplisia) diserbuk dan ditempatkan dalam botol coklat yang kering.
Bahan yang digunakan dalam penelitian ini adalah etanol, kloroform, etil asetat,
Diniatik, dkk
akuades, metanol pa., pembanding rutin. Alat yang digunakan dalam penelitian ini adalah maserator, alat gelas, rotary evaporator, kompor listrik, corong pisah, spektrofotometer UV, mikropipet, kertas saring.
Pembuatan ekstrak etanol daun S. burahol . Simplisia daun ditimbang kurang lebih 3 kg dibuat serbuk melalui proses penggilingan dan pengayakan. Serbuk kering ditimbang 500 gram kemudian dimaserasi. Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari. Pada penelitian ini untuk meningkatkan efektivitas ekstraksi dilakukan pengadukan dan remaserasi, waktu maserasi selama 2 x 24 jam dengan perbandingan antara simplisia dengan etanol 50% adalah 1:10 untuk hari pertama, dan 1:4 untuk remaserasi hari kedua. Ari disaring dengan kain flanel. Maserat diuapkan sampai diperoleh konsistensi kental yang masih bisa dituang kemudian ditimbang. Pembuatan ekstrak etanol daun S. burahol dilakukan di Laboratorium Biologi Farmasi Universitas Muhammadiyah Purwokerto.
Pembuatan fraksi kloroform dan etil asetat dari ekstrak etanol daun S. burahol. Ekstrak etanol seberat 170 g dihidrolisis dengan menggunakan HCl : Metanol (1:1) sebanyak 400 ml direfluk selama 30 menit. Penyarian dengan kloroform 5 x 200 ml dilakukan terhadap hasil hidrolisis untuk mengambil senyawa-senyawa nonpolar. Penyarian dilanjutkan dengan etil asetat sebanyak 5 x 200ml hingga setelah dipisahkan dan diuapkan didapat fraksi etil asetat. Ekstrak etanol, fraksi kloroform dan fraksi etil asetat kemudian ditetapkan kadar flavonoid totalnya.
Penentuan kadar flavonoid total. Larutan uji untuk ekstrak, ditimbang dengan saksama lebih kurang 0,1-1 g ekstrak, dilarutkan dalam 10 ml etanol 80%, disentrifus 1000 x gravitasi selama 10 menit.
Bagian supernatan (beningan) dimasukkan ke dalam labu ukur 25 ml, residu diekstraksi dua kali, tiap kali dengan 5 ml etanol 80%. Supernatan (beningan) dikumpulkan ke dalam labu ukur yang sama, ditambahkan etanol 80% sampai tanda.
Larutan uji untuk ekstrak cair, diukur seksama sejumlah volume ekstrak cair, diencerkan dengan etanol 80% sampai kadar yang sesuai untuk kolorimetri.
Larutan pembanding, ditimbang saksama pembanding lebih kurang 10 mg, dilarutkan dalam etanol pa, diencerkan secara kuantitatif dan jika perlu bertahap dengan etanol pa hingga kadar 25, 50 dan 100 ug/ml.
Pengukuran, dipipet secara terpisah 0,5 ml larutan uji dan larutan pembanding, ditambahkan pada masing-masing 1,5 ml etanol P, 0,1 ml aluminium klorida P 10%, 0,1 ml natrium asetat 1M dan 2,8 air suling. Dikocok dan didiamkan selama 30 menit pada suhu ruang. Diukur serapan pada panjang gelombang serapan maksimum. Dilakukan pengukuran blangko dengan cara yang sama, tanpa penambahan aluminium klorida (Anonim, 2009; Chang 2002).
HASIL DAN PEMBAHASAN
Determinasi Tanaman. Tanaman kepel (S. burahol) yang digunakan dalam penelitian dideterminasi di laboratorium Biologi Farmasi Fakultas Farmasi Universitas Gadjah Mada. Tujuan determinasi untuk mendapatkan kebenaran identitas dengan jelas dari tanaman yang diteliti dan menghindari kesalahan dalam pengumpulan bahan utama penelitian. Hasil determinasi menyatakan bahwa spesimen tumbuhan tersebut adalah benar – benar tanaman Stelecocharpus burahol, (Bl.) Hook f. & Th. dari famili Annonaceae. Hasil determinasi tersebut berdasarkan buku Flora of Java Vol II (Backer and Van Den Brink, 1965).
Diniatik, dkk
Pengumpulan Bahan dan
Pembuatan Simplisia Daun Kepel (S. burahol). Pada penelitian ini digunakan tanaman kepel (gambar 1) yang diambil di Kecamatan Mlati, Kabupaten Sleman Yogyakarta. Daun segar tanaman kepel diambil pada bulan Mei pada pagi hari. Daun yang dipetik adalah daun kepel segar diambil dari pohonnya yang berumur 10 tahun sejak penanaman, daun diambil pada saat tidak berbunga dan tidak berbuah (Anonim, 1985). Pengambilan dilakukan pada tempat dan waktu tertentu untuk menghindari bermacam – macam kandungan kimia dikarenakan perbedaan kondisi lingkungan, keadan tanah, dan iklim.
Gambar 1. Tanaman kepel (S. burahol)
Daun kepel segar yang didapatkan, dicuci dengan air yang mengalir untuk membersihkan kotoran atau kontaminan yang yang berupa tanah, atau materi lain pada daun tersebut. Dipilih daun (3 kg) yang bagus untuk selanjutnya dianginkan. Daun kepel dikeringkan di bawah sinar matahari yang ditutupi kain hitam. Selama pengeringan, bahan ditata tidak bertumpuk dan dibolak-balik agar pemanasan merata serta proses pengeringan berlangsung cepat. Daun kepel sudah kering di hari ke tujuh(Anonim, 1985).
Pengeringan dilakukan hingga kadar air kurang dari 10% atau sampai daun mudah untuk dihancurkan ketika diremas. Tujuan dari pengeringan adalah mencegah pertumbuhan jamur atau mikroorganisme dan penguraian senyawa aktif oleh reaksi
enzimatik dan proses hidrolisis karena kandungan air yang tinggi, agar simplisia yang dihasilkan tidak mudah rusak sehingga dapat disimpan dalam waktu yang relatif lama. Simplisia kering yang diperoleh selanjutnya diserbuk dengan menggunakan blender untuk memperkecil luas permukaan sehingga kontak permukaan partikel simplisia dengan penyari semakin besar dan penyarian lebih optimal. Simplisia selanjutnya diayak menggunakan ayakan mesh 20/40 yang berarti sebanyak 100% simplisia kering lolos pada ayakan mesh 20, kemudian sebanyak 40% dari 100% simplisia kering lolos ayakan mesh 40, sehingga dari 750 gram simplisia kering daun kepel sebanyak 450 gram lolos ayakan mesh 20 dan sebanyak 300 gram lolos ayakan mesh 40. Pada umumnya proses penyaringan ini penting dalam proses ekstraksi, karena dengan adanya pengecilan ukuran partikel akan memperluas permukaan kontak serbuk dengan penyari sehingga ekstraksi menjadi lebih maksimal dan kandungan zat aktif dapat tersari secara optimal.
Pembuatan Ekstrak Etanol Daun Kepel. Metode penyarian yang digunakan adalah maserasi. Metode ini merupakan metode yang paling sederhana karena mudah dilakukan, murah, tidak memerlukan peralatan yang canggih. Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari. Pada penelitian ini untuk meningkatkan efektivitas ekstraksi dilakukan pengadukan dan remaserasi, yaitu dimaserasi selama 2 x 24 jam dengan perbandingan antara simplisia dengan etanol 70% adalah 1:10 untuk hari pertama, dan 1:4 untuk hari kedua. Caranya yaitu serbuk simplisia sebanyak 750 gram dimaserasi dengan etanol 70% sebanyak 7,5 Liter, kemudian dienaptuangkan dan diperas. Ampas yang diperoleh dimaserasi lagi dengan etanol 70% sebanyak 3 Liter. Pada penelitian ini penyari yang digunakan yaitu
Diniatik, dkk
etanol 70%. Penyari etanol 70% dapat menarik senyawa – senyawa relatif polar seperti senyawa fenol, flavonoid, saponin, dan senyawa polar lain yang terkandung dalam daun kepel, sedangkan etanol yang digunakan merupakan etanol teknis yang ada di pasaran yang memungkikan diperoleh kembali saat diuapkan dengan rotary evaporator. Dipilih etanol karena sesuai dengan polaritas senyawa, tidak beracun, netral, dapat mencegah pertumbuhan kapang dan kuman, panas yang diperlukan untuk pemekatan lebih sedikit. Maserat yang diperoleh diuapkan di atas penangas air hingga konsistensi kental. Penguapan dilakukan untuk menghilangkan larutan penyari agar tidak mempengaruhi uji selanjutnya seperti yang tertera pada tabel 1 berikut.
Tabel 1. Rendemen ekstrak etanol
Jenis Bobot simplisia basah Bobot simplisia kering Berat ekstrak Rendemen (%) Ekstrak etanol 70% 3 kg 750 g 150,23 g 20,03
Dari serbuk simplisia sebesar 750 g diperoleh ekstrak 150,23 g. Ektrak kental ini dihidrolisis hingga diperoleh 31,09 g fraksi kloroform dan 26,58 g fraksi etil asetat. Kemudian ekstrak etanol, fraksi kloroform dan fraksi etil asetat dilakukan penetapan kadar flavonoid total dengan menggunakan metode Chang.
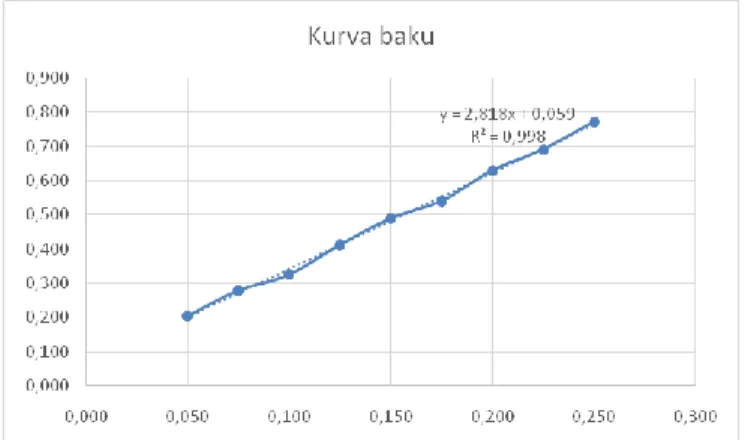
Pembuatan kurva baku rutin. Dibuat kurva baku dengan menimbang 10,0 mg standar rutin yang dilarutkan dalam 5 ml etanol 80%. Panjang gelombang maksimal yang diperoleh adalah 415,5 nm. Data kurva baku bisa dilihat pada gambar 2 berikut.
Gambar 2. Gambar regresi linier kurva bau rutin
Tabel 1. Data kurva baku rutin
Konsentrasi (mg/ml) Absorbansi 0,050 0,205 0,075 0,279 0,100 0,326 0,125 0,412 0,150 0,489 0,175 0,540 0,200 0,629 0,225 0,690 0,250 0,770
Penetapan Kadar Flavonoid Total Pada Ektrak Etanol Daun Kepel
Sebelum ditentukan kadar flavonoidnya dilakukan dulu uji kualitatif adanya flavonoid, dengan menggunakan pengamatan dibawah sinar UV 366. Pada gambar 3 dibawah terdapat pada ekstrak etanol fluoresensi hijau (rf 0,05), hijau kekuningan (rf 0,2), kuning (rf 0,5), lembayung (rf 0,65), kuning (rf 0,7), lembayung (rf 0,75). Dugaan flavonoid ada pada bercak no 2 sampai 6.
Diniatik, dkk
Gambar 3. Analisis kualitatif adanya flavonoid dari ekstrak etanol, fraksi kloroform dan fraksi etil asetat, A. fase gerak asam asetat 30%, dilihat di sinar UV 366, dan diuapi amoniak dilihat di sinar UV 366
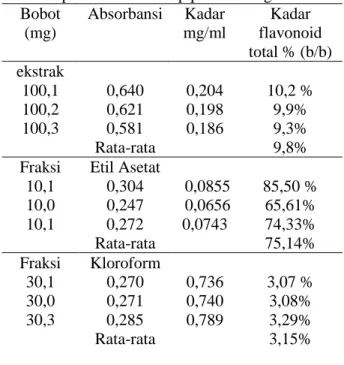
Selanjutnya dilanjutkan penetapan kadar dengan menggunakan kurva baku yang sudah dibuat diatas, yaitu y=2,818x+0,059, dapat ditentukan kadar flavonoid total dari ekstrak etanol daun kepel. Pada table 2 dibawah diperoleh kadar flavonoid total ekstrak etanol daun kepel relatif terhadap rutin yaitu rata-rata 9,8% b/b. Metode penetapan kadar ini tidak melalui metode hidrolisis, sehingga proses kerjanya jauh lebih singkat dan mudah (Diniatik dkk, 2013). Metode ini juga pernah digunakan untuk penetapan kadar flavonoid total pada tanaman yang satu famili dengan S. burahol, Annonaceae, yaitu tanaman Annona dioca St. Hill, dengan kadar flavonoid 73,32 % (b/b) (Formagio et al, 2013). Kadar flavonoid total yang cukup besar pada ekstrak etanol (9,8 % b/b)sangat bisa dikaitkan dengan beberapa uji aktivitas untuk melengkapi penelitian terkait daun kepel. Beberapa penelitian seperti uji pelarutan batu kalsium dari fraksi air dan fraksi etanol daun kepel sudah dilakukan dan berkorelasi positif dengan kadar
flavonoid yang cukup signifikan pada penelitian ini (Hidayati, 2004). Pada penetapan kadar flavonoid total pada fraksi kloroform dan fraksi etil asetat diperoleh kadar rata-rata 3,15% dan 75,14% (b/b). hal ini menunjukkan bahwa flavonoid yang sudah terhidrolisis, menjadi aglikon flavonoid, terdapat di fraksi kloroform dalam jumlah yang sangat kecil, sedangkan sebagian besar masuk di dalam fraksi etil asetat. Hidrolisis sebelum fraksinasi bertujuan untuk memisahkan aglikon flavonoidnya yang masuk dalam pelarut organik, sedangkan glikonnya masuk pada air asam.
Tabel 2. Kadar flavonoid total ekstrak etanol daun kepel relatif terhadap pembanding rutin
Bobot (mg) Absorbansi Kadar mg/ml Kadar flavonoid total % (b/b) ekstrak 100,1 0,640 0,204 10,2 % 100,2 0,621 0,198 9,9% 100,3 0,581 Rata-rata 0,186 9,3% 9,8% Fraksi 10,1 Etil Asetat 0,304 0,0855 85,50 % 10,0 0,247 0,0656 65,61% 10,1 0,272 Rata-rata 0,0743 74,33% 75,14% Fraksi 30,1 Kloroform 0,270 0,736 3,07 % 30,0 0,271 0,740 3,08% 30,3 0,285 Rata-rata 0,789 3,29% 3,15% KESIMPULAN
1. Rendemen ekstrak etanol daun kepel sebesar 20,03%
2. Kadar rata-rata flavonoid total dalam ekstrak etanol daun kepel adalah 9,8 %(b/b), fraksi etil asetat 75,14%(b/b) dan fraksi kloroform 3,15 %(b/b)
DAFTAR PUSTAKA
Diniatik, dkk
Anonim, 1985, Cara Pembuatan Simplisia, 4-10, Departemen Kesehatan RI, Jakarta.
Backer, C.A. dan Bakhuizen van den Brink, R.B.C., 1963, Flora of Java: Spermatophytes only, pp. 3-51, 100-102, Vol. I, Netherlands.
Diniatik, Hapsari, I., Tiara, M., Meidyawati, A., Nurhidayat, S., 2013, Determination and Validation Method of Total Flavonoid Content and Total Phenolic Content of Ethanolic Extract of Mangosteen (Garcinia mangostana L.) Leaves as Natural Preservatives Candidate by using Spectrophotometric Method, Prosiding International Seminar NETS, Universitas Muhammadiyah Purwokerto
Chang CC, MH Yang, HM Wen, and JC Chern. 2002. Estimation of total flavonoid content in propolis by two complementery colorimetric methods. J Food Drug Anal., 10 (3), 178-182.
Formagio, A.S.N., Kassuya, C.A.L., Neto, F.F., Volobuff, C.R.F., Iriguchi, E.K.K, Vieira, M.C., Foglio, M.A., 2013, The Flavonoid Content and Antiproliferative, Hypoglycaemic, Antiinflamatory and Free Radical Scavenging Activities on Annona dioca, St. Hill, BMC Complementary and Alternative Medicine, 13:14, page 1-8.
Hasan, A., & Tahir, M.N., 2005, Flavonoids from the Leaves of Impatiens bicolor, Turk J Chem, 29 (2005), 65-70.
Hidayati, 2004, Uji Daya Melarutkan Fraksi Air dan Fraksi Etanol Infusa Daun Kepel (Stelecocharpus burahol, Hook) Terhadap Batu Ginjal Kalsium
Iwashina, T. & Kokubugata, G., 2012, Flavone and Flavonol Glycosides
from the Leaves of Triumfetta procumbens in Ryukyu Islands, Bull. Natl. Mus. Nat. Sci., Ser. B, 38(2), pp. 63–67, May 22.
Purwantiningsih, Hakim, A.R., Purwatini, I., 2010, Antiihyperuricemic Activity Of The Kepel Stelechocarpus burahol (Bl.)Hook.F.&Th.] Leaves Extract And Xantine Oksidase Inhibitory Study, International Journal of Pharmacy and Pharmaceutical Sciences,Vol. 2, Issue. 2,hal 122-127 Matlawska, I. & Sikorska, M., 2005,
Flavonoids FromAbutilon Theophrasti Flowers, Acta Poloniae Pharmaceutica N Drug Research, Vol. 62 No. 2 Pp. 135n139, Issn 0001-6837 Polish Pharmaceutical Society
Nazaruk, J., & Golden, J., 2003, Flavonoid Compounds From The Flowers of Circum rivulare Jacq. All, Acta Poloniae Pharmaceutica-Drug Research, Vol 60, No 1, 87-89
Sunarni, 2007, Flavonoid antioksidan penangkap radikal dari daun kepel (Stelechocarpus burahol (Bl.) Hook f. & Th.), Majalah Farmasi Indonesia, 18(3), 111 – 116
Syukri, M., 2007, Asam Urat dan Hiperuresemia, Majalah Kedokteran Nusantara, Volume 40 No. 1.
Tisnadjaja, D., Saliman, E., Silvia, Simanjuntak, P., 2006, Pengkajian Burahol (Stelechocarpus burahol (Blume) Hook & Thomson) sebagai Buah yang Memiliki Kandungan Senyawa Antioksidan, Biodiversitas, ISSN: 1412-033X, Volume 7, Nomor 2 April 2006, Halaman: 199-202