UJI AKTIVITAS BIOLOGI SECARA BSLT DAN UJI SITOTOKSIK DENGAN METODE MTT DARI EKSTRAK n-HEKSANA DAN EKSTRAK METANOL
DAUN KELADI TIKUS (Typhonium divaricatum (L) Decne)
Yunahara Farida1, Titiek Martati1, Bernard Edward1
1
Fakultas Farmasi Universitas Pancasila, Jagakarsa Jakarta 12640 Email : yunahara_farida@yahoo.com
ABSTRAK
Tanaman keladi tikus (Typhonium divaricatum (L) Decne), familia Araceae. merupakan jenis tanaman liar yang belum banyak dikenal oleh masyarakat. Beberapa hasil penelitian menyebutkan bahwa ekstraknya telah dibuktikan dapat menyembuhkan beberapa kasus penyakit antara lain kanker. Penelitian ini bertujuan untuk mengetahui apakah ekstrak n-heksana dan metanol dari daun keladi tikus mempunyai aktivitas sitotoksik terhadap sel kanker payudara T-47D. Penelitian yang dilakukan meliputi penapisan fitokimia, uji aktivitas biologi secara Brine Shrimp Lethality Test (BSLT) dan uji aktivitas sitotoksik dengan metode MTT. Hasil penapisan fitokimia terhadap serbuk dan ekstrak daun menunjukkan adanya flavonoid dan steroid/triterpenoid. Hasil penelitian uji aktivitas biologi secara BSLT menunjukkan bahwa ekstrak metanol yang paling aktif dengan nilai IC50 = 32,91 g/mL sedangkan n-heksana =126,21 g/mL.
Hasil uji aktivitas sitotoksik secara MTT, ekstrak n-heksana memiliki aktivitas terhadap sel kanker payudara T-47D yang lebih tinggi dibandingkan ekstrak metanol.dengan nilai IC50 = 32,50 g/mL dan ekstrak metanol = 345,40 g/mL. Apabila dibandingkan
dengan cisplatin (IC50 3,07 g/mL) maka aktivitas sitotoksik cisplatin terhadap sel
kanker payudara T-47 D masih jauh lebih tinggi.
Kata kunci: Keladi tikus, Typhonium divaricatum (L) Decne), BSLT, sel kanker
payudara T-47 D, MTT .
PENDAHULUAN
Saat ini pemanfaatan tumbuhan obat
untuk mengobati berbagai jenis
penyakit semakin disukai masyarakat
karena jarang menimbulkan efek
samping yang tidak diinginkan, salah satunya adalah untuk terapi kanker.
Penyakit kanker dikenal sebagai
penyakit yang sukar disembuhkan dan dapat menyebabkan kematian, sehingga hal mi merupakan masalah yang sulit dalam bidang pengobatan. Walaupun telah cukup banyak ditemukan obat kemoterapi untuk terapi kanker. namun hasilnya belum memuaskan, disamping kurang selektif dalam penggunaan obat yang ada, juga ditemukan efek samping yang cukup besar dan obat tersebut.
Akibatnya mendorong masyarakat
banyak melakukan pengobatan dengan menggunakan bahan alam atau obat tradisional. salah satunya adalah
tanaman keladi tikus (Typhonium
divaricatum (L) Decne).
Tanaman keladi tikus (Typhonium
divaricatum (L) Decne), familia Araceae. merupakan salah satu jenis tanaman liar yang belum banyak
dikenal oleh masyarakat. Secara
empiris, masyarakat Indonesia
menggunakannya untuk mengobati
penyakit kanker/tumor. Beberapa hasil
penelitian menyebutkan bahwa
ekstraknya telah dibuktikan dapat
menyembuhkan beberapa kasus
penyakit antara lain kanker. Selain itu ekstrak etanol dan kloroform dan daun
dan umbi keladi tikus ternyata
mempunvai aktivitas penghambatan
pertumbuhan sel lestari tumor.
Mengingat potensi tanaman obat asli Indonesia yang cukup besar maka penelitian terhddap tanaman keladi tikus (Typhonium divaricatum (L) Decne)
perlu dikembangkan dengan cara
melakukan ekstraksi dan diuji toksisitas, dan aktivitas sitotoksik terhadap sel kanker payudara.
BAHAN DAN METODE BAHAN. Bahan yang digunakan dalam
penelitian ini adalah daun keladi tikus yang diperoleh dari Balittro, Bogor dan dideterminasi di Herbarium Bogoriense, Pusat Penelitian Biologi, LIPI, Bogor. Bahan kimia: n-heksana, metanol, HCl, amil alkohol, eter, asam asetat anhidrat, H2SO4, telur Artemia salina Leach,
garam tanpa iodium, DMSO, Sel kanker
payudara T-47D, cisplatin, RPMI
(Roswell Park Memorial Institute) 1640, FBS (Fetal Bovine Serum), penisilin-streptomisin, MTT (3-(4,5- dimethylthiazol-2-yl)-2,5diphenyl-tetrazolium bromide), PBS (Phosphat
Bufferd Salina), SDS (Sodium Dodesil Sulfat), biru tripan, tripsin, air suling
steril, etanol.
Rotary evaporator, Orbital shaker,
tempat penetasan telur artemia, Lampu TL, Labu kultur jaringan 25 mL, pelat kultur jaringan 96 sumuran, LAF cabinet (Laminar Air Flow Biological
Safety Cabinet), inkubator sel dengan
aliran CO2 5%, tangki nitrogen cair, alat
sentrifuge, mikropipet (Eppendorf),
timbangan analitik, mikroskop,
hemositometer, ELISA plate reader, alat-alat gelas.
METODE. Daun keladi tikus dibuat
serbuk, kemudian di maserasi
menggunakan metanol dan di partisi menggunakan n-heksana sehingga di dapat ekstrak n-heksana. Sisa hasil partisi diuapkan dan didapatkan ekstrak metanol. Penapisan fitokimia dilakukan dengan cara mengidentifikasi senyawa
kimia yang terdapat dalam serbuk dan ekstrak.
Pengujian aktivitas biologi secara BSLT (Brine Shrimp Lethality Test).
Terhadap ekstrak n-heksana dan
metanol dilakukan uji toksisitas
berdasarkan metode Meyer et.al. (1982) menggunakan telur Artemia salina Leach. Mula-mula telur Artemia salina ditetaskan didalam air laut buatan (38 g garam tanpa iodium dalam 1000 mL air biasa) di bawah lampu TL 18 watt. Media penetasan telur diberi aerasi udara. Setelah 48 jam larva menetas
menjadi nauplii dan siap untuk
digunakan. Nauplii dimasukkan ke dalam vial yang berisi larutan ekstrak sampel dengan konsentrasi 10,100 dan 1000 bpj dengan 3 kali ulangan. Semua vial di inkubasi pada suhu kamar selama 24 jam di bawah penerangan lampu TL 18 watt. Pengamatan dilakukan setelah 24 jam dengan melihat jumlah Artemia
salina yang mati pada setiap konsentrasi. Penentuan harga LC50
dalam g/mL dilakukan menggunakan analisis probit. Hasil uji lethalitas LC50
selanjutnya digunakan sebagai dasar penentuan konsentrasi untuk pengujian terhadap sel kanker payudara T-47D.
Pengujian aktivitas sitotoksik.
Pembuatan larutan uji. Ekstrak bahan
uji ditimbang sebanyak 10 mg,
kemudian dilarutkan dalam 20 µL DMSO dan 80 µL medium RPMI 1640 sehingga diperoleh konsentrasi larutan induk 100000 bpj. Dari larutan induk diencerkan hingga diperoleh satu seri konsentrasi 10, 25, 50, 100, 250 dan 500 bpj.
Pembuatan larutan kontrol positif.
Larutan induk cisplatin ditimbang sebanyak 10 mg, kemudian dilarutkan dalam 20mL medium RPMI 1640
sehingga diperoleh konsentrasi larutan induk 500 bpj. Dari larutan tersebut diencerkan hingga diperoleh satu seri konsentrasi 3, 6, 9, 12, 15 dan 18 bpj,
sedangkan kontrol negatif adalah
medium RPMI 1640.
Pembuatan media kultur. media
kultur yang digunakan adalah medium RPMI cair untuk sel T-47D yang ditambahkan 10% FBS dan antibiotik penisilin-streptomisin 0,1%. Medium disterilkan secara filtrasi dan disimpan pada suhu 2-80 C.
Pencairan sel kanker (cell thawing).
Tabung berisi sel dikeluarkan dari tangki nitrogen cair dan dibenamkan dalam pemanas air bersuhu 370 C selama 3 menit. Seluruh cairan sel dipipet dan dimasukkan ke dalam tabung sentrifugasi dan ditambahkan 5
mL medium RPMI 1640 lalu
disentrifugasi dengan kecepatan 1000 rpm selama 3-5 menit. setelah itu supernatant dibuang dan pelet yang diperoleh disuspensikan dalam 6 mL yang mengandung 20% FBS. suspensi sel dipipet dan dimasukkan kedalam labu kultur lalu diinkubasi pada suhu 370 C dalam inkubator sel 5% CO2
sampai 80% di inkubasi selama 3 hari yaitu sampai sel tumbuh di hampir seluruh permukaan labu kultur.
Sub kultur. Labu kultur berisi sel yang
telah diinkubasi selama 3 hari
dikeluarkan dari inkubator sel. Seluruh medium dalam labu kultur dipipet dan dibuang, kultur sel dicuci sebanyak 2 kali, dengan 5 mL PBS. Ke dalam labu kultur ditambahkan 2 mL tripsin, kemudian sel didiamkan selama 5 menit dalam inkubator, Ditambahkan 3 mL RPMI 1640 yang mengandung 10% FBS, cairan sel dipipet dan dipindahkan ke dalam tabung sentrifugasi lalu disentrifugasi pada kecepatan 1000 rpm
selama 5 menit. Supernatan dibuang dan pelet yang diperoleh disuspensikan dalam 12 mL RPMI 1640 yang mengandung 10% FBS. Suspensi sel dibagi menjadi dua bagian, masing-masing dipipet sebanyak 6 mL dan dimasukkan ke dalam 2 buah labu kultur baru kemudian diinkubasi pada 370 C dalam inkubator sel. Sel diperiksa setiap hari dibawah mikroskop untuk memeriksa kemungkinan pencemaran oleh jamur atau bakteri. Apabila medium kultur telah berubah warna maka diganti dengan medium RPMI yang mengandung serum baru.
Perhitungan kepadatan sel T-47D.
Kultur yang telah diinkubasi selama 3 hari diamati dengan mikroskop untuk mengetahui tingkat kepadatannya. Jika tumbuh baik maka sel dapat digunakan dan jika tidak maka sel harus diinkubasi kembali hingga kepadatannya optimal. Medium dalam labu kultur dipipet dan dibuang, kultur sel dicuci sebanyak 2 kali, masing-masing dengan 5 mL PBS. Ke dalam labu kultur ditambahkan 2 mL tripsin dan sel didiamkan selama 5 menit dalam inkubator, kemudian dikeluarkan dari inkubator dan dilihat dibawah mikroskop untuk memastikan sel sudah tidak melekat pada dasar labu. Ditambahkan 1 mL RPMI, dipipet cairan sel dan dipindahkan ke dalam
tabung sentrifugasi kemudian
disentrifugasi dengan kecepatan 1000 rpm selama 5 menit. Supernatan dibuang dan pelet yang diperoleh disuspensikan dalam 1 mL RPMI. Suspensi dipipet sebanyak 10 µL dan ditambahkan 90 µL biru tripan 0,4%. Kepadatan sel dihitung menggunakan hemositometer yaitu lebih kurang 20 µL dari suspensi sel dalam larutan biru
tripan dipipet lalu ujung pipet
disentuhkan dengan sudut 300 pada permukaan hemositometer dibiarkan
terisi perlahan dengan daya kapilaritas. Kepadatan sel dihitung dari jumlah sel rata-rata dalam keempat bidang besar dikalikan faktor pengenceran dan dibagi dengan volume satu bidang besar
Kepadatan sel atau jumlah sel per ml = n/4 x 2 x 104
n = jumlah rata-rata sel dalam keempat bidang besar
Penyiapan kultur kanker (T-47D).
Setelah kepadatan sel diketahui, sisa suspensi sel yang tidak digunakan dalam perhitungan kepadatan sel, yaitu sebanyak 990 µl digunakan untuk pengujian sitotoksisitas dan diencerkan dengan medium RPMI 1640 yang
mengandung 10% FBS dengan
perhitungan sebagai berikut : P1 V1 = P2 V2
P1adalah kepadatan hasil penghitungan,
V1 adalah volume suspensi sel yang
dibutuhkan untuk pengenceran, P2
adalah kepadatan sel yang dikehendaki dalam sumur uji dan V2 adalah total
suspensi sel yang akan diisikan kedalam sumur uji.
Pengujian sitotoksisitas ekstrak terhadap sel T-47D. Kedalam pelat
kultur jaringan 96 sumuran dimasukkan suspensi sel sebanyak 100 µl kemudian diinkubasi selama 24 jam dalam inkubator sel pada suhu 370C. Setelah 24 jam, ke dalam masing-masing sumur ditambahkan 100 µl masing-masing ekstrak dengan berbagai konsentrasi untuk kontrol negatif ditambah 100 µl
medium kultur sel RPMI 1640.
Kemudian pelat kultur jaringan
diinkubasi selama 24 jam pada suhu 370C dalam inkubator sel. Pada akhir periode inkubasi, ke dalam setiap sumur ditambahkan 100 µl MTT (50mg MTT
dalam 10ml PBS steril), kemudian diinkubasi kembali dalam inkubator
CO2 selama 4 jam pada 370C.
Kemudian ditambahkan 100 µl SDS dicampur secara merata, kemudian isi tiap-tiap sumur dan ukur serapannya menggunakan ELISA plate reader pada 570 nm.
Perhitungan persentase kematian sel.
Untuk mengetahui berapa besar
persentase penghambatan proliferasi sel T-47D, dihitung menggunakan rumus berikut :
Serapan perlakuan
Persen Proliferasi Sel = x 100% Serapan kontrol
Persen penghambatan prolifersi = 100 – persen proliferasi sel
Data persentase penghambatan
proliferasi sel diolah menggunakan
analisis regresi linier untuk
mendapatkan nilai IC50. Suatu ekstrak
dinyatakan aktif atau memiliki potensi sebagai anti kanker bila nilai IC5500≤ 20
µg/mL.
HASIL DAN PEMBAHASAN
Hasil penapisan fitokimia menunjukkan bahwa serbuk dan ekstrak metanol mengandung flavonoid dan steroid/
triterpenoid sedangkan ekstrak
n-heksana mengandung steroid/
triterpenoid. Golongan senyawa ini
berpotensi mempunyai aktivitas
farmakologi. Oleh karena itu
dilanjutkan dengan uji toksisitas secara BSLT sebagai uji pendahuluan. Hasil uji toksisitas secara BSLT menunjukkan
bahwa ekstrak metanol 1 (hasil
maserasi) memberikan nilai LC50 32,91
g/mL dan ekstrak metanol 2 (hasil
partisi) 38,91 g/mL sedangkan n-heksana 126,21 g/mL (Tabel 1).
Berdasarkan Tabel 1, suatu senyawa termasuk dalam kategori sangat aktif apabila memiliki nilai LC50 < 30 bpj
(McLaughlin & Roger, 1998). Ekstrak suatu tanaman dikatakan toksik apabila nilai LC50-nya lebih kecil dari 1000 bpj
(Meyer, 1982). Dari hasil uji
menunjukkan bahwa ekstrak daun keladi tikus berpotensi sebagai anti tumor atau anti kanker. Ekstrak metanol dalam uji BSLT ternyata lebih aktif
dibandingkan dengan ekstrak
n-heksana.
Tabel 1.Hasil uji toksisitas dari ekstrak n-heksana dan ekstrak metanol secara BSLT
Sampel Log konsent % kematian Probit LC50 ( g/mL) Ekstrak metanol 1 3,003 2,003 1,003 96,66 60,0 33,33 6,88 5,25 4,56 32,91 Ekstrak n-heksana 3,002 2,002 1,002 93,33 33,33 6,66 6,48 4,56 3,52 126,21 Ekstrak metanol 2 3,004 2,004 1,004 96,66 50,00 33,33 6,88 5,00 4,56 38,91
Hasil pengamatan terhadap aktivitas sel kanker payudara T-47D adalah dengan melihat aktivitas ekstrak n-heksana maupun metanol terhadap sel kanker T-47 D diperlihatkan dengan nilai IC50,
dimana penetapan nilai IC50 dilakukan
menggunakan regresi linier. Dari data nilai IC50 (Tabel 2) terlihat bahwa
ekstrak n-heksana menunjukkan
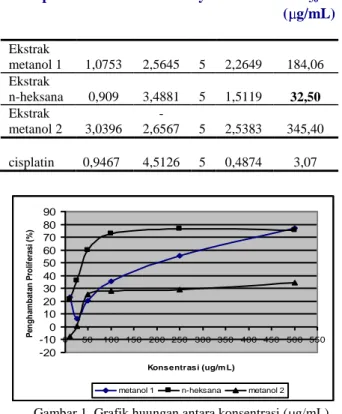
aktivitas penghambatan proliferasi galur sel kanker payudara T-47D lebih tinggi dibandingkan dengan ekstrak metanol. Grafik hubungan antara konsentrasi dan penghambatan proliferasi dapat dilihat pada Gambar 1.
Tabel 2. Aktivitas inhibisi ekstrak daun keladi tikus terhadap strain sel T-47D
Sampel b a y x IC50 ( g/mL) Ekstrak metanol 1 1,0753 2,5645 5 2,2649 184,06 Ekstrak n-heksana 0,909 3,4881 5 1,5119 32,50 Ekstrak metanol 2 3,0396 -2,6567 5 2,5383 345,40 cisplatin 0,9467 4,5126 5 0,4874 3,07 -20 -10 0 10 20 30 40 50 60 70 80 90 0 50 100 150 200 250 300 350 400 450 500 550 Konsentrasi (ug/m L) P e n g h a m b a ta n P ro li fe ra s i (% )
metanol 1 n-heksana metanol 2
Gambar 1. Grafik huungan antara konsentrasi ( g/mL) dan penghambatan proliferasi (%) dari ekstrak metanol dan ekstrak n-heksana
KESIMPULAN
Dari penapisan fitokimia menunjukkan di dalam serbuk dan ekstrak daun keladi tikus mengandung flavonoid dan steroid triterpenoid. Ekstrak metanol dan n-heksana daun keladi tikus memiliki toksisitas terhadap larva udang
Artemia salina Leach. Dari hasil uji
sitotoksik, ekstrak n-heksana memiliki aktivitas terhadap sel kanker payudara T-47D yang lebih tinggi dibandingkan ekstrak metanol dengan nilai IC50
32,50 g/mL.
Ucapan Terima kasih
Terima kasih kepada DP2M, Direktorat Jenderal Pendidikan Tinggi, Depdiknas, yang telah mendanai penelitian ini.
DAFTAR PUSTAKA
1. McLaughlin, J.L.and Rogers, L.L. The use of biological assay to evaluate botanicals.Drug Information Journal, 1998, 32:513-524.
2. Meyer BN. Brine shrimp: a
convinient general bioassay for active plant constituent. Planta Medica. 1982., 45: 31-4
3. Aryanti. Isolasi senyawa anti kanker
dari tanaman keladi tikus
(Typhonium divaricatum (L).
Decne). Jurnal Bahan Alam
Indonesia 2002;1(1):188
4. Zheng G.Q. Cytotxic terpenoid and flavonoids Artemisia annua. Planta Medica (1994) 60: 54-57.
5. Kamuhabwa,A, Nshima, C. & de Witte, P. Cytotoxicity of some medicinal plant extracts used in Tanzanian traditional medicine. J.Ethnopharmacol. 2000. 70: 143-149.
6. Wilson, AP. Cytotoxicity and
viability assays. In: Masters JRW, Editor. Animal cell culture: A Parctical Approach. 3rd ed. Oxford University Press, New York. 2000, 263-4; 272.
7. MTT cell proliferation assay
instruction catalog number 30-1010k, ATCC[serial online] 2001; diambil dari http//www.atcc.org. 8. McLaughlin, JL, Anderson JE. A
blind comparation of single benzsch-top bioassay and human tumor cell. Cytotoxicities studies as Anti tumor prescreens. Phytochemical Analysis. Volume 2; 1991. 107-11
9. Sugianto. Aktivitas antikarsinogenik
senyawa yang berasal dari
tumbuhan. Majalah Farmasi
Indonesia 2003;14(3):132.
10. Harborne JB. Metode Fitokimia. Penuntun cara modern menganalisis
tumbuhan. Terbitan kedua.
Terjemahan Padmawinata K,
Soediro I. Bandung: ITB; 1987. hal. 47-61
11. Sugianto. Aktivitas antikarsinogenik
senyawa yang berasal dari
tumbuhan. Majalah Farmasi
Indonesia, 2003;14(3):132.
12. Orech, et.al. Potential toxicity of some traditional lefy vegetables consumed in nyah’oma division, western Kenya. African Journal of Food and Nutritional Sciences: 2005, Volume 5 No 1.
13. Tri Dewi, Yuliyanah. Uji aktivitas
penghambatan pertumbuhan sel
lestari tumor dari ekstrak etanol
keladi tikus (Typhonium
flagelliforme (Lodd.) Bl.) secara in vitro. 2003
14. Krishnaraju, A.V. et.al. Assestment of bioactivity of Inddian medicinal plants using brine shrimps (Artemia salina) lethality assay, International Journal of Applied Science and Engineering, 2005.3,2: 125-134.
15. Ayo, R.G, Audu, O.T, and
Amupitan, J.O, Physico-chemical characterization and cytotoxicity studies of seed extracts Khaya
senegalensis (Desr.) AJuss. African
Journal of Biotechnology, 2007, Vol. 6 (7), pp. 894-896.
16. Krishnaraju, A.V. et.al. Biological
Screening of Medicinal Plants
Collected from Eastern Ghats of India Using Artemia salina(Brine Shrimp Test), Int. J. Appl. Sci. Eng., 2006. 4, 2: 115-125
17. Choo, C.Y., Chan, K.L., Tayeka,K., Itokawa, H., Cytotoxic Activity of
Typhonium flagelliforme (Araceae).
Phytother.Rea.2001;15(3):260-2