Peran Endotel dalam Sepsis Berat dan Sindrom Difungsi
Peran Endotel dalam Sepsis Berat dan Sindrom Difungsi
Organ Multipel
Organ Multipel
Patofisiologi Patofisiologi
Terdapat beberapa hal yang penting dalam patofisiologi sepsis. Yang pertama, Terdapat beberapa hal yang penting dalam patofisiologi sepsis. Yang pertama, adalah respon pejamu, dibandingkan dengan sifat alami patogen, hal ini lebih adalah respon pejamu, dibandingkan dengan sifat alami patogen, hal ini lebih mempengaruhi hasil akhir pasien. Kedua, monosit dan sel endotel memiliki peran mempengaruhi hasil akhir pasien. Kedua, monosit dan sel endotel memiliki peran utama dalam mengawali dan mempertahankan respon pejamu. Ketiga, sepsis utama dalam mengawali dan mempertahankan respon pejamu. Ketiga, sepsis dihubungkan dengan keterlibatan aktivasi kaskade inflamasi dan koagulasi. Pada dihubungkan dengan keterlibatan aktivasi kaskade inflamasi dan koagulasi. Pada akhirnya, dalam upaya yang dilakukan untuk melawan dan mengeliminasi akhirnya, dalam upaya yang dilakukan untuk melawan dan mengeliminasi pathogen,
pathogen, respon respon pejamu pejamu dapat dapat menimbulkan menimbulkan kerusakan kerusakan yang yang sejalan sejalan padapada jaringan
jaringan normal, normal, mengakibatkan mengakibatkan suatu suatu keadaan keadaan patologi patologi yang yang tidak tidak difus, difus, tetapitetapi lebih dapat dikenali
lebih dapat dikenali distribusinya secara fokal. distribusinya secara fokal. Setiap hal-hal tersebut di atas Setiap hal-hal tersebut di atas akanakan dibahas satu persatu.
dibahas satu persatu.
Pentingnya respon pejamu
Pentingnya respon pejamu. Beberapa temuan menunjukkan tentang. Beberapa temuan menunjukkan tentang pentingnya faktor
pentingnya faktor pejamu pejamu dalam dalam mempengaruhi mempengaruhi hasil hasil akhir akhir pasien pasien dengan dengan sepsissepsis berat.
berat. Pertama, Pertama, meskipun meskipun cepatnya cepatnya implementasi implementasi terapi terapi antibiotik antibiotik yang yang tepat,tepat, angka kematian sepsis masih cukup tinggi, antara 28% hingga 50%. Kedua, angka kematian sepsis masih cukup tinggi, antara 28% hingga 50%. Kedua, pasien
pasien sepsis sepsis dengan dengan kultur kultur positif positif dan dan kultur kultur negatif negatif atau atau dengan dengan syok syok septik septik memiliki angka kematian yang sebanding. Ketiga, pemberian antibodi memiliki angka kematian yang sebanding. Ketiga, pemberian antibodi anti-endotoksin dalam jumlah besar, secara klinis tidak memberikan peningkatan endotoksin dalam jumlah besar, secara klinis tidak memberikan peningkatan angka kelangsungan hidup. Dan yang terakhir, terdapat hubungan langsung antara angka kelangsungan hidup. Dan yang terakhir, terdapat hubungan langsung antara jumlah
jumlah kriteria kriteria SIRS SIRS dan dan angka angka kematian, kematian, dan dan terdapat terdapat peningkatan peningkatan lebih lebih lanjutlanjut dalam angka kematian pada spectrum SIRS, sepsis, sepsis berat, dan syok septik. dalam angka kematian pada spectrum SIRS, sepsis, sepsis berat, dan syok septik. Yang jelas, kesuksesan terapi masa depan akan berdasarkan pada kemampuan Yang jelas, kesuksesan terapi masa depan akan berdasarkan pada kemampuan respon pejamu yang adekuat.
respon pejamu yang adekuat.
Peran monosit dan sel endotel dalam memediasi respon pejamu
Peran monosit dan sel endotel dalam memediasi respon pejamu. Monosit,. Monosit, makrofag jaringan, berbagai derivat sel myeloid lainnya, dan beberapa perluasan makrofag jaringan, berbagai derivat sel myeloid lainnya, dan beberapa perluasan sel endotel, merupakan penjuru utama dari respon imun bawaan. Sebagai lini sel endotel, merupakan penjuru utama dari respon imun bawaan. Sebagai lini pertama
melalui reseptor yang berinteraksi dengan struktur mikroba yang diawetkan. melalui reseptor yang berinteraksi dengan struktur mikroba yang diawetkan. Interaksi antara pathogen dan sel pejamu menghasilkan inisiasi kaskade inflamasi Interaksi antara pathogen dan sel pejamu menghasilkan inisiasi kaskade inflamasi dan koagulasi (Gambar 1). Jalur ini menghasilkan mediator yang dapat larut yang dan koagulasi (Gambar 1). Jalur ini menghasilkan mediator yang dapat larut yang berfungsi
berfungsi dalam dalam siklus siklus autokrin autokrin dan dan parakrin parakrin untuk untuk mengaktifkan mengaktifkan monosit/monosit/ makrofag jaringan dan/atau endotel lebih lanjut.
makrofag jaringan dan/atau endotel lebih lanjut.
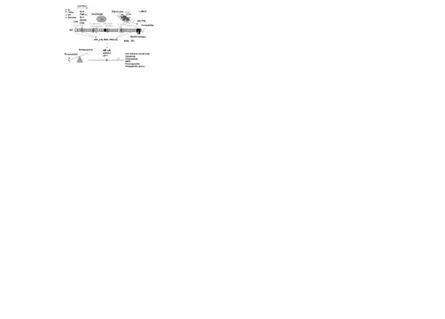
Gambar 1. Peran monosit dan endotel dalam memediasi respon pejamu terhadap Gambar 1. Peran monosit dan endotel dalam memediasi respon pejamu terhadap infeksi
infeksi. LPS dan/atau sel yang berkaitan dengan pathogen lainnya, mengaktifkan reseptor . LPS dan/atau sel yang berkaitan dengan pathogen lainnya, mengaktifkan reseptor pengenal pathogen (atau
pengenal pathogen (atautoll-like receptorstoll-like receptors) pada monosit, makrofag jaringan dan sel) pada monosit, makrofag jaringan dan sel endotel, menghasilkan pelepasan mediator inflamasi dan faktor
endotel, menghasilkan pelepasan mediator inflamasi dan faktor jaringan (dengan aktivasijaringan (dengan aktivasi berurutan dari jalur koagulasi). Bersama
berurutan dari jalur koagulasi). Bersamaan dengan produk sistem kontak (misal, kinin)an dengan produk sistem kontak (misal, kinin) dan kaskade komplemen (misal, C5a) (tidak ditunjukkan), mediator inflamasi berfungsi dan kaskade komplemen (misal, C5a) (tidak ditunjukkan), mediator inflamasi berfungsi dalam siklus autokrin dan parakrin untuk mengaktifkan monosit dan endotel lokal lebih dalam siklus autokrin dan parakrin untuk mengaktifkan monosit dan endotel lokal lebih
lanjut (garis putus-putus, kiri, menunjukkan jalur parakrin). Komponen kaskade lanjut (garis putus-putus, kiri, menunjukkan jalur parakrin). Komponen kaskade koagulasi yang bervariasi tidak hanya mengaktifkan substrat
koagulasi yang bervariasi tidak hanya mengaktifkan substrat berikutnya (menghasilkanberikutnya (menghasilkan pembentukan fibrin), tetapi juga m
pembentukan fibrin), tetapi juga memicu reseptor yang diaktifkan protease padaemicu reseptor yang diaktifkan protease pada permukaan beberapa sel, termasuk e
permukaan beberapa sel, termasuk endotel (garis putus-putus, kanan). Efek gabungan darindotel (garis putus-putus, kanan). Efek gabungan dari LPS, mediator inflamasi, dan
LPS, mediator inflamasi, dan serine protease pada endotel dapat menghasilkan modulasiserine protease pada endotel dapat menghasilkan modulasi fenotipe yang signifikan (tidak ditunjukkan). CAM
fenotipe yang signifikan (tidak ditunjukkan). CAM adalahadalah cell adhesion moleculescell adhesion molecules; PAF,; PAF,
platelet activating factor
platelet activating factor ; NO,; NO,nitric oxidenitric oxide; ROS,; ROS,reactive oxygen speciesreactive oxygen species; MIP-2,; MIP-2,
macrophage inflammatory protein 2 macrophage inflammatory protein 2..
Aktivasi jalur inflamasi dan koagulasi
Aktivasi jalur inflamasi dan koagulasi. Hal ini telah diakui secara luas bahwa. Hal ini telah diakui secara luas bahwa respon inflamasi memiliki peran yang penting dalam memediasi fenotipe sepsis. respon inflamasi memiliki peran yang penting dalam memediasi fenotipe sepsis. Patogen memicu aktivasi awal dari sistem kontak (faktor XII, prekalikrein, dan Patogen memicu aktivasi awal dari sistem kontak (faktor XII, prekalikrein, dan kininogen dengan berat molekul tinggi) dan kaskade komplemen, dan kininogen dengan berat molekul tinggi) dan kaskade komplemen, dan meningkatkan pelepasan mediator inflamasi secara cepat dari beberapa tipe sel meningkatkan pelepasan mediator inflamasi secara cepat dari beberapa tipe sel
(contoh monosit, dan sel endotel), perubahan yang bersamaan dengan manifestasi klinis SIRS. Secara serentak, jalur inflamasi endogen teraktivasi, yang akan mengurangi respon inflamasi. Proses berikutnya disebut sebagai sindrom respon kompensasi anti-inflamasi. Idealnya, kedua fase ini dikoordinasikan untuk membantu host melawan invasi oleh pathogen. Meskipun demikian, respon inflamasi yang berlebihan atau terus-menerus, respon anti-inflamasi yang tidak adekuat, atau mungkin tidak serentaknya kedua fase ini dapat mengakibatkan kerusakan jaringan dan kematian.
Di samping mengaktifkan sistem inflamasi, pathogen juga memicu kaskade pembekuan darah. Selama terjadinya sepsis, ekspresi faktor jaringan (TF) pada permukaan monosit dan makrofag jaringan yang beredar akan meningkat jumlahnya, mengakibatkan aktivasi jalur ekstrinsik, peningkatan thrombin dan pembentukan fibrin. Fibrin tidak hanya menstabilkan perlekatan platelet, tetapi juga berperan dalam menghambat pergerakan pathogen pada permukaan leukosit, mempermudah untuk memakan dan menghilangkan pathogen. Pembekuan darah diawali melalui jalur ekstrinsik dan dilanjutkan melalui jalur intrinsik oleh mekanisme yang melibatkan umpan silang dan umpan balik. Kaskade pembekuan darah disusun oleh serangkaian reaksi yang saling berhubungan dimana serine protease, bila teraktivasi, akan terbebas untuk mengaktifkan substrat berikutnya. Reaksi ini terjadi pada membran fosfolipid yang teraktivasi dan pada beberapa kasus dipercepat dengan munculnya kofaktor (faktor VIIIa dan Va). Dalam setiap respon prokoagulan, terdapat reaksi antikoagulan yang alami. Tissue factor pathway inhibitor (TFPI) mengontrol jalur ekstrinsik, antitrombin III (ATIII) — heparan menetralisir serin protease dalam kaskade tersebut, meekanisme trombomodulin (TM)/protein C/protein S akan menonaktifkan kofaktor Va dan VIIIa, dan plasmin mengurangi pembentukan fibrin. Hemostasis merepresentasikan keseimbangan yang sangat baik antara pembentukan prokoagulan dan antikoagulan. Bukan hanya aktivasi jalur ekstrinsik pada sepsis, tetapi juga terdapat penurunan respon antikoagulan alami (misal pengurangan kadar protein C dan ATIII yang beredar, penurunan ekspresi TM pada permukaan sel endotel, fibrinolisis yang dihambat). Pergeseran hasil ke arah status
prokoagulan akan mengakibatkan peningkatan thrombin, pembentukan fibrin, dan pemakaian faktor pembekuan yang berlebihan.
Sekali teraktivasi, interaksi jalur inflamasi dan koagulasi satu sama lain akan memperkuat respon pejamu lebih lanjut (Gambar 1). Misalnya, mediator inflamasi meningkatkan ekspresi TF pada permukaan monosit, makrofag jaringan, netrofil, dan mungkin beberapa bagian sel endotel yang beredar. Sebaliknya, serine protease mampu berinteraksi dengan reseptor yang diaktifkan protease pada permukaan monosit dan sel endotel, mengakibatkan aktivasi dan inflamasi tambahan. Contohnya, adanya sinyal trombin dalam sel endotel akan menghasilkan perubahan bentuk sel, permeabilitas sel, respon proliferasi, dan adhesi leukosit. Perubahan selanjutnya dimediasi terutama oleh kemampuan trombin untuk mempengaruhi ekspresi E-selectin, P-selectin, Molekul Adhesi Interseluler 1 (ICAM-1) dan Molekul Adhesi Sel Vaskuler 1 (VCAM-1). Selain itu, adanya sinyal trombin dalam sel endotel telah terbukti dapat mempengaruhi sekresi faktor von Willebrand (VWF), meningkatkan ekspresi reseptor mRNA yang diaktifkan protease 1 (PAR-1), IL-8, monocyte chemoattractant protein 1 (MCP-1), faktor pertumbuhan, dan matriks metalloproteinase. Kompleks TF/VIIa dan faktor Xa juga dapat berikatan dengan reseptor yang diaktifkan protease dan memicu respon proinflamasi. Yang terakhir, fibrin(ogen) telah terbukti akan berinteraksi dengan sel endotel, menghasilkan sejumlah perubahan fenotip termasuk peningkatan ekspresi IL-8. Umpan silang antara jalur inflamasi dan koagulasi berperan dalam respon pejamu yang kuat terhadap sepsis.
Ekspresi fokal terhadap fenotip sepsis. Sifat konsisten dari lesi patologis dalam sepsis berat dan MODS adalah distribusinya yang bersifat fokal. Khususnya, pasien hanya mengalami disfungsi pada beberapa organ yang terbatas. Endotel merupakan faktor yang penting pada respon fokal dalam kasus sepsis. Seperti yang akan didiskusikan berikut, endotel menunjukkan heterogenitas yang sangat baik dalam status kesehatan dan penyakit, memadukan perubahan sistemik dalam inflamasi dan koagulasi dalam jalur yang berbeda dari organ satu ke organ lainnya.
Peran endotel dalam menyusun respon pejamu pada sepsis
Aktivasi dan disfungsi sel endotelEndotel merupakan organ yang sangat pervasif; Tubuh manusia mengandung sekitar 1013 sel endotel, dengan berat 1 kg dan mencakup luas permukaan 4000 m2 hingga 7000 m2. Di antara fungsi-fungsi lainnya, endotel memediasi tonus vasomotor, mengatur peredaran seluler dan nutrisi, memelihara kekentalan darah, berperan atas keseimbangan lokal dalam mediator proinflamasi dan anti-inflamasi, berpartisipasi dalam pembentukan pembuluh darah baru, dan menjalankan kematian sel yang direncanakan. Yang penting, tiap-tiap aktivitas tersebut diatur dalam waktu dan tempat yang berbeda (sebuah fenomena yang disebut sebagai heterogenitas sel endotel atau keragaman vaskuler).
Dalam kondisi normal, sel endotel sangatlah aktif, secara terus-menerus mengartikan dan bereaksi terhadap perubahan dalam lingkungan ekstraseluler setempat, yang mungkin muncul dalam kondisi transient bacteremia, trauma kecil, dan beberapa stress harian lainnya. Dengan kata lain, aktivasi sel endotel muncul sebagai respon adaptasi normal, keberadaan dan durasinya tidak hanya tergantung pada tipe stimulus, tetapi juga pada dinamika ruang dan waktu dari sistem tersebut. Contohnya, pada setiap waktu, sel endotel vena dan arteri dapat memiliki respon yang berbeda terhadap setiap sinyal sistemik, sedangkan di setiap lokasi, respon akan bervariasi dari satu waktu ke waktu, bergantung pada kesehatan dan status keseluruhan organisme. Oleh karena itu, aktivasi sel endotel bukanlah suatu respon menyeluruh atau respon yang tidak berarti, dan apakah respon ini perlu dikaitkan dengan penyakit. Aktivasi sel endotel justru merepresentasikan sebuah spektrum dari respon dan muncul dibawah pengaruh kondisi fisiologis dan patofisiologis.
Berbagai respon endotel yang bermanfaat bagi pejamu dapat dipertimbangkan sebagai fungsional, fisiologis atau adaptasi. Misalnya, ketika patogen menginvasi suatu jaringan, sel endotel dipengaruhi secara lokal untuk melepaskan mediator-mediator inflamasi, untuk menarik leukosit, dan untuk meningkatkan pembekuan darah untuk mendirikan pertahanan terhadap infeksi. Selama proses ini, sel endotel dapat mengalami nekrosis atau apoptosis seiring dengan jaringan yang
direabsorbsi dan diperbaiki. Bila kita melihat pada tingkat seluler, nekrosis dan/atau apoptosis merupakan ekspresi akhir dari suatu disfungsi. Meskipun demikian, bila dipertimbangkan pada konteks pertahanan pejamu yang lebih luas, kehilangan endotel lokal merupakan bagian dari sebuah respon adaptasi yang telah dikoordinasikan lebih luas. Mungkin analogy yang pas adalah altruism kelompok atau pemilihan kelompok, sebuah mekanisme kerjasama yang evolusioner pada hewan, dimana efek positif pada tingkat kelompok lebih berarti daripada efek negatif pada tingkat individu. Istilah disfungsi sel endotel lebih dipilih untuk kasus dimana respon sel endotel, baik lokal maupun sistemik, menggambarkan suatu kewajiban terhadap pejamu. Misalnya, dalam kasus sepsis berat, terdapat aktivasi endotel yang berlebih, terus-menerus dan menyeluruh. Tanpa adanya dukungan buatan terhadap organ, sebenarnya semua pasien dengan sepsis berat akan meninggal. Dengan kata lain, sebagian besar manusia tersebut telah melewati ambang dari respon adaptif menjadi respon maladaptif. Sepanjang endotel berperan dalam fenotip sepsis berat, perjalanannya dapat ditandai dengan suatu gangguan fungsi.
Respon endotel dalam sepsis berat
Sepsis dapat meningkatkan modulasi fenotip endotel dengan berbagai mekanisme yang berbeda. Dalam beberapa kasus, patogen secara langsung menginfeksi sel endotel yang intak. Pada umumnya, komponen dinding sel bakteri (seperti lipopolisakarida [LPS]) akan mengaktivasi reseptor pengenal pola pada permukaan endotel. Akhirnya, ada banyak sekali faktor turunan pejamu yang mengaktifkan sel endotel, termasuk komplemen, sitokin, kemokin, serin protease, fibrin, leukosit dan trombosit yang teraktivasi, hiperglikemia, dan/atau perubahan dalam oksigenasi atau aliran darah (lihat Tabel 1 dan Gambar 2 untuk daftar mediator turunan pejamu)
Reaksi endotel dapat berbeda-beda tergantung pada sifat alami patogen, genetic pejamu, komorbiditas yang mendasari, usia, jenis kelamin, dan lokasi pembuluh darah utama. Sel endotel dapat mengalami perubahan struktural, termasuk vakuolisasi nucleus, pembengkakan sitoplasma, fragmentasi sitoplasma, pelepasan dan/atau pemisahan. Perubahan fungsional lebih umum terjadi dan
mencakup pergeseran keseimbangan hemostatis, peningkatan peredaran dan adhesi leukosit, perubahan tonus vasomotor, penurunan fungsi pertahanan dan kematian sel yang terprogram.
Tabel 1. Pengobatan menurut target.
Referensi tidak seluruhnya dimasukkan; tetapi disusun berdasarkan fase pemilihan dasar,fase preklinis, fase klinis awal dan/atau fase 3 percobaan klinis, sebagaimana tinjauan yang terpilih.
*Penetapan cepat dari terapi antibiotik yang tepat memberikan jalan utama dalam terapi pasien dengan sepsis berat.
†Fase 3 percobaan klinis telah menunjukkan tidak ada manfaat bagi angka kelangsungan hidup.
‡ Peran fisiologis utama Faktor XII bukan untuk memediasi aktivasi koagulasi, tetapi lebih
untuk meningkatkan angka dan luas aktivasi prekalikrein, menghasilkan pembentukakn bradikinin, meningkatkan aktivitas profibrinolitik dan menghambat aktivasi trombosit yang
dimediasi trombin.
§ Fase 3 percobaan klinis telah dilakukan dan terbukti mampu meningkatkan angka
kelangsungan hidup. Derajat dimana penurunan aktivasi sel endotel terkait pengobatan yang memiliki peran dalam manfaat keseluruhan masih belu m diketahui.
Keberadaan prokoagulan. Mediator inflamasi dapat berinteraksi dengan sel endotel untuk meningkatkan fenotipe prokoagulan sesungguhnya. Dalam kondisi in vitro, penambahan LPS dan/atau sitokin pada sel endotel telah terbukti dapat menurunkan sintesis TM, aktivator plasminogen tipe jaringan dan heparan, untuk meningkatkan ekspresi TF dan penghambat aktivator plasminogen 1 (PAI-1), dan untuk membentuk mikropartikel prokoagulan. Perluasan terhadap perubahan yang terjadi pada endotel yang intak masih belum dimengerti dengan jelas. Dalam penelitian terkini pada pasien dengan meningococcemia, kadar TM berkurang dalam pembuluh darah mikro di kulit, sebuah efek yang akan diprediksikan untuk menghasilkan penurunan kadar protein C aktif. Dalam percobaan tikus dengan endotoksemia, pemberian LPS menghasilkan penurunan jumlah total antigen TM jaringan di paru dan otak, tetapi tidak di ginjal, menunjukkan bahwa perubahan ekspresi TM akibat sepsis dapat bervariasi pada masing-masing organ. Ketika sepsis dihubungkan dengan peningkatan kadar PAI-1, sumber endotel PAI-1 masih belum ditentukan. Dengan beberapa pengecualian, penelitian sepsis secara konsisten telah gagal dalam menunjukkan TF pada endotel yang intak.
Bila endotel dilihat dalam konteks lingkungan alaminya, kepemilikan tambahan muncul yang dapat melibatkan status prokoagulan. Contohnya, sel endotel yang teraktivasi akan menarik trombosit, monosit, dan netrofil — sel yang mampu menginisiasi dan memperkuat koagulasi. Aktivasi endotel dapat menghasilkan translokasi fosfolipid permukaan sel yang meningkatkan ikatan kompleks koagulasi. Sel endotel yang mengalami apoptosis dapat mengekspresikan sebuah fenotipe prokoagulan yang meningkat. Perkembangan status aliran dalah yang lambat pada sepsis, yang dapat mengurangi curah jantung secara sekunder, vasokonstriksi, atau lesi oklusif, dapat mengurangi pembersihan serin protease yang teraktivasi, sehingga mengakibatkan pembekuan darah tambahan.
Sebagaimana kekayaan endotel lainnya, keseimbangan hemostatis diatur secara berbeda antar anyaman pembuluh darah. Dalam percobaan tikus dengan endotoksemia, pemberian LPS sistemik menghasilkan pengendapan fibrin yang spesifik organ pada ginjal dan kelenjar adrenal. Dalam penelitian lain, pemberian
LPS menghasilkan kadar fibrin yang dapat ditemukan di paru, tetapi tidak di otak, dari seekor mencit liar. Penelitian lainnya membuktikan bahwa injeksi LPS pada mencit liar berhasil meningkatkan kadar fibrin di ginjal, hepar, dan miokardium, tetapi tidak di paru. Pada percobaan baboon dengan model sepsis, pemberian E. coli dengan dosis lethal menghasilkan peningkatan endapan fibrin pada area marginal dan sinusoid limpa, sinusoid hepar, glomerulus, dan pembuluh darah peritubular ginjal, tetapi sedikit atau bahkan tidak ditemukan fibrin pada vena porta hepar, korteks cerebrii, kulit, miokardium, atau aorta. Ketidaksesuaian pola endapan fibrin dalam beberapa penelitian di atas mungkin berkaitan dengan perbedaan spesies/keturunan yang diteliti, tipe model sepsis, dan/atau sifat alami dari uji fibrin. Meskipun demikian, bila data tersebut dikumpulkan, terdapat data yang konsisten dalam membuktikan hubungan antara sepsis dan koagulasi yang spesifik organ.
Pada percobaan genetic tikus dengan hiperkoagulabilitas, sepsis menghasilkan pergeseran yang menonjol dalam keseimbangan hemostasis. Contohnya, pada mencit yang membawa mutasi gen TM yang akan mengacaukan aktivasi protein C dependen TM, pemberian LPS mengakibatkan kadar endapan fibrin yang lebih tinggi di paru dan ginjal tetapi tidak di otak, dibandingkan dengan mencit liar. Pada mencit dengan defisiensi ATIII heterozigot, tantangan LPS menghasilkan peningkatan endapan fibrin di dalam ginjal, hepar, dan jantung. Beberapa penelitian tersebut menunjukkan pentingnya genetic yang mendasari dalam
memodulasi fenotip sepsis.
Keberadaan proadhesif. Reaksi endotel terhadap mediator inflamasi dengan mengekspresikan adhesi molekul pada permukaan sel, termasuk P-selectin, E-selectin, ICAM-1 dan VCAM-1. Secara bersamaan, perubahan ini mengakibatkan peningkatan pergiliran, perlekatan yang kuat, dan perpindahan leukosit menuju jaringan yang mendasari. Perubahan ini tidaklah menyeluruh, tetapi lebih cenderung terjadi secara lokal di organ dan segmen anyaman pembuluh darah tertentu. Sel endotel yang teraktivasi juga akan menarik jumlah trombosit yang lebih banyak ke dinding pembuluh darah. Pentingnya adhesi molekul dalam memediasi fenotip sepsis didukung oleh penelitian pada mencit mati.
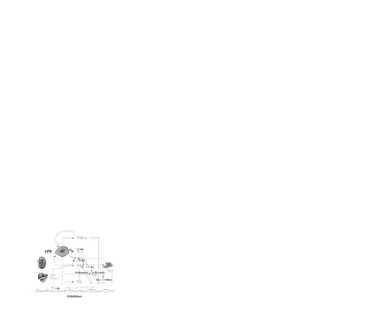
Gambar 2. Endotel sebagai target terapi.
Pemahaman respon endotel terhadap patogen memberikan dasar untuk desain terapi. Untuk tujuan ilustrasi dan diskusi, urutan waktu kejadian digambarkan dari kiri ke kanan. Dalam sepsis, endotel
diaktifkan oleh ikatan toll-like receptor (TLR4) yang dimediasi LPS, atau dengan interaksi mediator inflamasi (IL-6, TNF-α, IL-1, kinin, dan C5a ditampilkan) dengan reseptornya yang berurutan (digambarkan sebagai reseptor tunggal yang mewakilinya). Pada waktu yang sama (atau
selanjutnya dalam kaskade sepsis), endotel dapat dipengaruhi oleh faktor lingkungan lainnya, seperti hipoksi, aliran darah yang lambat, perubahan suhu, gangguan elektroli/asam-basa, dan/atau
hiperglikemia. Interaksi mediator ekstraseluler dengan reseptornya mengakibatkan aktivasi jalur pemberian isyarat berikutnya (termasuk MAPK dan PKC), yang menghasilkan perubahan
posttranskripsi dari fungsi sel atau perubahan profil ekspresi gen melalui sejumlah faktor transkripsi, termasuk NF-кB, GATA-2, dan AP-1. Peningkatan adhesi molekul sel pada permukaan endotel (P-selectin, E-selectin, VCAM-1 dan ICAM-1 ditunjukkan) menimbulkan peningkatan adhesi, pergiliran, dan perpindahan leukosit yang beredar. Interaksi leukosit-endotel
lebih lanjut akan memodulasi fenotip sel-sel tersebut. Pelepasan sitokin dari endotel mengakibatkan aktivasi tambahan monosit dan sel endotel. Peningkatan ekspresi prokoagulan
(seperti TF) dan/atau berkurangnya ekspresi antikoagulan (contoh TM, EPCR) menimbulkan peningkatan produksi trombin dan pembentukan fibrin. Berbagai komponen jalur koagulasi (termasuk serin protease, fibrin, dan trombosit) dapat memberikan isyarat langsung pada endotel
melalui reseptor yang diaktifkan protease (PAR-1 ditunjukkan). Perubahan ekspresi gen proapoptosis dan antiapoptosis (bersama dengan banyaknya perubahan posttranskripsi) dapat
mengakibatkan pergeseran keseimbangan kematian sel terprogram. Selama proses aktivasi , NADPH oksidase dapat mempengaruhi pembentukan reactive oxygen species (ROS), nitric oksida
(NO) dilepaskan, dan permeabilitas sel meningkat. Untuk menjaga dinamika tempat dan waktu, aktivitas relatif berbagai jalur akan bervariasi antar sel endotel yang berbeda dari satu waktu ke waktu lainnya. Hal yang tidak digambarkan adalah interaksi kuat antara endotel dengan matriks
molekul intraseluler 1; VCAM-1, adhesi molekul sel pembuluh darah; EC, sel endotel; T F, faktor jaringan; TM, trombomodulin; EPCR, reseptor protein C endotel; NO, nitricoksida; PGI2,
prostasiklin. Reseptor dinamai dengan huruf tipis.
Keberadaan vasomotor. Tonus vasomotor diatur oleh kombinasi mekanisme yang tergantung endotel dan yang tidak tergantung endotel. Sel endotel memproduksi molekul vasoaktif yang mengatur tonus arteriol dan berperan dalam pengaturan tekanan darah. Hal ini mencakup vasodilator (nitrit oksida [NO] dan prostasiklin) dan vasokonstriktor (endothelin, tromboksan A2 dan platelet
activating factor ). Pada sepsis, endotel yang teraktivasi akan mengalami perubahan spesifik lokasi yang dapat mempengaruhi keseimbangan
vasokonstriktor dan vasodilator.
Peningkatan permeabilitas. Dalam pembuluh darah yang intak, endotel membentuk pertahanan yang bersifat terus-menerus, semipermeabel yang bervariasi kesatuan dan pengaturannya pada setiap anyaman pembuluh darah yang berbeda. Sifat utama endotel dalam sepsis adalah peningkatan permeabilitas atau hilangnya fungsi pertahanan, yang mengakibatkan pergeseran komponen sirkulasi dan edema jaringan. TNF-α mempengaruhi peningkatan permeabilitas sel endotel baik in vitro maupun in vivo. Dalam kondisi in vitro, trombin juga meningkatkan permeabilitas sel endotel, sedangkan TNF-α dan trombin bekerja secara sinergis untuk mempengaruhi disfungsi pertahanan in vitro. Distribusi ulang cairan dari ruang intravaskular ke ekstravaskular dapat berperan dalam hipovolemia, hemokonsentrasi, dan stasis aliran darah.
Apoptosis sel endotel. Apoptosis sel endotel merupakan proses yang diatur dengan sangat baik. Normalnya, hanya sedikit sekali persentase (< 0.1%) sel endotel yang mengalami apoptosis. Dalam kondisi in vitro, patogen tertentu mampu mempengaruhi apoptosis sel endotel. Inkubasi sel endotel biakan dengan LPS telah dilaporkan dapat mempengaruhi apoptosis pada beberapa tetapi tidak semuanya. LPS telah terbukti mampu meningkatkan regulasi Bc1-2 homolog, A1, dan zinc finger protein, A20, dalam sel endotel biakan. Kaskade sepsis melibatkan banyak mediator inflamasi lainnya yang dapat mempengaruhi apoptosis sel
endotel, termasuk TNF-α, IL-1, interferom, radikal bebas oksigen, dan hipoksia. Interaksi antara sel yang beredar dan endotel dapat memperbesar sinyal proapoptosis lebih lanjut. Misalnya, monosit yang diaktifkan LPS menimbulkan kematian sel terprogram pada sel endotel melalui kombinasi mekanisme yang tergantung dan tidak tergantung TNF-α.
Apoptosis sel endotel mengakibatkan respon proinflamasi yang berarti. Contohnya, dalam kondisi in vitro, sel endotel yang apoptosis akan memediasi induksi parakrin ICAM-1 dan VCAM-1 yang dependen IL-1, meningkatkan produksi reactive oxygen species (ROS), meningkatkan aktivitas prokoagulan, menurunkan produksi prostasiklin, dan aktivasi komplemen. Selain itu, sel endotel yang mengalami apoptosis terbukti dapat meningkatkan ikatan terhadap platelet yang nonaktif.
Dalam percobaan tikus dengan endotoksemia, LPS yang diberikan secara intraperitoneal mengakibatkan apoptosis endotel yang luas. Dalam penelitian lainnya, pemberian LPS melalui intravena pada mencit telah terbukti mampu mempengaruhi apoptosis sel endotel di paru, tetapi tidak di hepar, menunjukkan adanya kematian sel yang terprogram yang spesifik pada organ tertentu.
Aktivasi endotel lokal versussistemik
Respon pejamu bawaan berkembang sebagai mekanisme kerja lokal untuk merngeradikasi patogen dan jaringan nekrotik. Endotel menyusun respon lokal dengan memicu adhesi dan transmigrasi leukosit, mempengaruhi produksi trombin dan pembentukan fibrin, mengubah tonus vasomotor lokal, meningkatkan permeabilitas, dan memicu kematian sel yang terprogram. Aktivasi koagulasi
memberikan sejumlah peran yang potensial, termasuk pertahanan terhadap patogen, aktivasi reseptor yang diaktifkan protease, dan stimulasi ekspresi chemokin makrofag ekstravaskuler. Normalnya, mekanisme umpan balik negatif lokal dan sistemik akan teraktivasi, mengurangi respon pada lokasi distal. Penggolongan respon imun bawaan membatasi kerusakan kolateral pejamu dan melindungi integritas dan kemampuan adaptasi terhadap endotel yang tidak terlibat. Oleh karenanya, endotel secara keseluruhan tidak terkunci ke dalam respon tunggal tetapi juga menjaga keseimbangan untuk berhubungan dengan
serangan lain. Ketika respon pejamu menyeluruh, hal ini akan melepaskan keseimbangan dan kesesuaian lokal yang berkembang baik dan mengakibatkan gangguan regulasi, respon inflamasi yang tidak tepat. Dalam kondisi ini, keterlibatan endotel yang luas dan monosit/makrofag jaringan, bersama dengan aktivasi inflamasi dan koagulasi yang lebih menyeluruh, dapat mengakibatkan SIRS dan MODS.
Hubungan antara disfungsi sel endotel dan MODS
Selain meningkatnya pengetahuan bahwa kaskade inflamasi dan koagulasi akan teraktivasi dalam kondisi sepsis berat, sedikit yang tahu tentang mekanisme bahwa hal itu dapat mengakibatkan disfungsi organ dan kematian. Jalur inflamasi dan koagulasi dan tipe sel yang bervariasi sangatlah erat kaitannya bahwa mereka tidak dapat dan tidak seharusnya dipandang sebagai sesuatu yang berdiri sendiri-sendiri dalam sepsis berat. Aktivasi kaskade inflamasi memberi pengaruh yang kuat bagi jalur koagulasi, dan juga sebaliknya. Monosit yang teraktivasi mempengaruhi endotel, dan begitu pula sebaliknya. Adanya disfungsi dari satu organ manapun memiliki efek beruntun terhadap semua organ lainnya. Sehingga, respon pejamu terhadap sepsis sangatlah terintegrasi dengan baik, dan secara keseluruhan jauh lebih besar daripada total unsur utamanya (Gambar 3).
Berdasarkan pertimbangan tersebut, bagaimana bisa kita menilai dengan baik peran endotel dalam memediasi fenotip sepsis? Bukti yang ada menunjukkan bahwa fungsi endotel berubah dalam kondisi sepsis berat yang akan berbeda dari
satu lokasi anyaman pembuluh darah dengan yang lainnya. Perubahan ini, pada bagian yang lebih besar, respon pejamu yang terintegrasi, dapat membantu
mengawali dan mempertahankan siklus inflamasi, koagulasi, dan interaksi seluler yang spesifik lokasi yang pada akhirnya dapat mengakibatkan oklusi, hipoksia, dan disfungsi organ. Untuk mendukung bahwa endotel memiliki peran utama yang lebih atau kutang dibandingkan dengan monosit, atau bahwa kaskade inflamasi lebih atau kurang penting dibandingkan kaskade koagulasi dalam pathogenesis sepsis masih belum diketahui pasti. Mungkin sebuah jalan pemikiran yang lebih produktif adalah sebagai berikut: endotel sangatlah penting, tetapi tidak tunggal, sebagai komponen respon pejamu terhadap sepsis; endotel secara
strategis terletak di antara darah dan jaringan yang mendasarinya; endotel merupakan lapisan sel yang sangat lunak dan fleksibel; sehingga, endotel berpotensi sebagai target yang berharga bagi terapi sepsis.
Endotel sebagai target terapi
Perspektif terapiSelama satu dekade terakhir, sejumlah penelitian telah dicurahkan pada percobaan sepsis, dengan lebih dari 10000 pasien terdaftar dalam lebih dari 20 percobaan dengan kontrol placebo, fase 3 percobaan klinis acak. Kebanyakan pengobatan ini telah gagal dalam mengurangi angka kematian pasien dengan sepsis berat, termasuk strategi antiendotoksin, antisitokin, antiprostaglandin, antibradikinin, dan anti-PAF, ATIII serta TFPI. Selama penulisan jurnal ini, sejumlah 5 fase 3 percobaan klinis telah membuktikan peningkatan angka kelangsungan hidup pada pasien yang sakit kritis atau pasien dengan sepsis berat. Hal ini meliputi penggunaan ventilasi volume tidal yang rendah, protein C aktif, glukokortikoid dosis rendah, terapi insulin intensif, dan terapi dengan tujuan terarah segera.
Gambar 3. Gambaran kompleks respon pejamu terhadap infeksi
Respon pejamu terhadap infeksi melibatkan serangkaian sel dan mediator larut yang sangat luas, dimana meliputi tetapi tidak terbatas pada monosit, sel endotel, dan trombosit dan komponen komplemen, kaskade inflamasi dan koagulasi. Dibandingkan menunjukkan hubungan yang detil,
gambar ini bermaksud untuk menyampaikan sifat r espon pejamu yang saling ketergantungan, berlebihan, dan pleiotropik. Beberapa faktor memodulasi fenotip, termasuk tipe patogen, dan
faktor pejamu, seperti genetik, make up, usia, jenis kelamin, status kesehatan dan siste m organ lainnya (contohnya ginjal dan hepar). Normalnya, mekanisme pejamu terkoordinasi dengan baik,
baik dalam tempat dan waktu, untuk membantu pejamu melawan patogen. Meskipun demikian, ketika respon pejamu tidaklah proporsional dengan pengobatan (misal, berlebihan, terus-menerus,
terlokalisasi buruk), maka keseimbangan kekuatan akan bergeser menyerupai patogen, mengakibatkan fenotip sepsis. Dengan adanya respon dengan integrasi tinggi dan sifat alami yang
nonlinear, akan cukup sulit untuk mengidentifikasi komponen tunggal dari modulasi terapi manakah yang akan mempersingkat kaskade dan meningkatkan hasilnya. Seiring dengan kompleksitas respon sepsis yang menyisakan hal di luar kendali kita, harapan terbaik bagi kemajuan terapi akan berdasar pada sasaran yang luas, dimana komponen multipel ditargetkan
pada waktu yang sama.
Strategi untuk mencapai target endotel
Pada prinsipnya, terdapat 2 strategi untuk mengurangi respon endotel pada sepsis. Pertama adalah untuk menargetkan komponen nonendotel respon pejamu, termasuk mediator yang larut atau tipe sel lainnya (seperti leukosit, trombosit), yang tidak memodulasi fungsi sel endotel. Strategi lainnya adalah dengan menargetkan komponen endotel (misal, reseptor permukaan sel, jalur pemberi tanda, jaringan transkripsi, atau produk gen sel endotel) yang terlibat dalam memediasi fenotip sepsis (Gambar 2; Tabel 1). Target yang terdaftar dalam Tabel 1 diturunkan dari kombinasi penelitian dasar dan klinis. Sementara sejumlah terapi ini telah mencapai fase 3 percobaan klinis, yang lain masih dalam fase preklinis atau fase klinis awal. Perluasan terhadap target selanjutnya akan
menerjemahkan ke dalam efektivitas klinis masih harus diperhatikan.
Terapi antimediator. Beberapa upaya telah dibuat untuk mencapai target LPS atau mediator inflamasi yang secara langsung mengaktifkan sel endotel baik pada tingkat faktor ekstraseluler maupun reseptornya sendiri. Pada fase besar 3 percobaan klinis, penggunaan terapi antimediator spesifik telah gagal dalam
meningkatkan angka kelangsungan hidup pada pasien dengan sepsis berat.
Terapi antiadhesi. Interaksi sel yang beredar dengan endotel sepertinya memiliki peran yang penting dalam respon pejamu terhadap infeksi. Beberapa strategi telah digunakan untuk menghambat interaksi leukosit-sel endotel dalam percobaan hewan dengan sepsis, termasuk penggunaan antibody monoclonal.
Selain itu, trombosit yang nonaktif mendorong endotel yang terstimulasi, dalam sebuah proses yang melibatkan P-selectin dan E-selectin, menunjukkan bahwa terapi yang ditujukan pada adhesi molekul sel ini juga dapat mengurangi interaksi trombosit-endotel. Trombosit yang teraktivasi telah terbukti dapat melekat pada endotel melalui mekanisme dependen GPIIbIIIa, menunjukkan peran yang potensial bagi penghambat GPIIbIIIa dalam sepsis. Hingga saat ini, terapi
antiadhesi dalam sepsis masih diselidiki.
Terapi antikoagulan. Beberapa molekul antikoagulan telah diteliti dalam percobaan hewan primata dengan sepsis. Heparin dan active-site-blocked factor Xa menghambat aktivasi koagulasi, tetapi tidak melindungi terhadap disfungsi
organ atau kematian. Hasil ini menunjukkan bahwa aktivasi kaskade koagulasi tidaklah cukup untuk mempengaruhi angka kematian dalam sindrom ini. Berlawanan dengan agen yang menghambat aktivitas trombin atau penghasil trombin, pemberian active-site-blocked factor Xa, ATIII, dan protein C aktif, atau TFPI akan memblok aktivasi jalur koagulasi dan inflamasi, mengurangi kerusakan organ, dan mencegah kematian pada percobaan baboon dengan sepsis. Efek anti-inflamasi dari agen ini terkait, setidaknya sebagian, dengan kemampuan mereka untuk memblok protease-activated receptor
–
mediated signaling dan/atau untuk mengaktifkan jalur perlindungan dalam endotel. Bersama dengan kegagalan hasil percobaan antisitokin/antimediator, data ini menunjukkan, tetapi tanpa bukti berarti, bahwa angka kematian pada sepsis berat berkaitan dengan aktivasigabungan dari jalur proinflamasi dan koagulasi.
Potensi terapi protein C aktif dibuktikan dalam fase 3 terbaru percobaan Protein C Worldwide Evaluation in Severe Sepsis (PROWESS), dimana pemberian rekombinasi protein C aktif manusia (drotrecogin alfa [aktif]) kepada pasien dengan sepsis berat menghasilkan penurunan angka kematian. Sejumlah 1690 pasien dengan diagnosis sepsis berat diacak untuk menerima terapi drotrecogin alfa (aktif) atau placebo. Terdapat penurunan yang signifikan dalam waktu 28 hari yang menyebabkan kematian (24.7% vs. 30.8% dalam kelompok pengobatan dan placebo, P < 0.005). Percobaan PROWESS merupakan percobaan
klinis yang pertama kali dipublikasikan untuk membuktikan adanya keuntungan angka kelangsungan hidup pada pasien dengan sepsis berat.
Berlawanan dengan hasil penelitian preklinis dan fase awal 1/2 yang menjanjikan, fase 3 percobaan klinis dengan ATIII atau TFPI gagal membuktikan peningkatan angka kelangsungan hidup pada pasien dengan sepsis berat. Satu penjelasan yang memungkinkan atas temuan ini adalah terkait dengan desain penelitian. Misalnya, pasien dalam fase 3 percobaan klinis mungkin telah mendapatkan dosis ATIII dan/atau TFPI yang kurang optimal. Selain itu, dalam penelitian ATIII, manfaat potensial dari obat tersebut dapat dikaburkan dengan pemberian heparin yang bersamaan. Penjelasan lain adalah bahwa protein C aktif
memiliki efek biologis unik yang menjadikannya terlepas dari ATIII dan TFPI pada manusia dengan sepsis berat (berbeda dengan percobaan baboon dengan sepsis). Sesungguhnya, saat TFPI dan ATIII mungkin menggunakan efek anti inflamasinya secara tidak langsung melalui reseptor yang diaktifkan protease (hingga saat ini, belum ada bukti tentang reseptor ATIII), protein C aktif mengikat dan mengaktifkan reseptor unik, reseptor protein C endotel (EPCR), yang diekspresikan pada permukaan sel endotel dan beberapa monosit. Interaksi antara protein C aktif dengan reseptornya telah diterapkan dalam fungsi anti-inflamasi
dan antiapoptosis nya yang sangat besar.
Terapi antiapoptosis. Seperti yang telah didiskusikan sebelumnya, apoptosis memiliki peran yang sangat penting dalam memediasi fenotip sepsis. Yang menarik, adanya inhibisi apoptosis akan merepresentasikan suatu alur umum dalam terapi sepsis yang ditetapkan. Contohnya, protein C aktif telah terbukti mampu menghambat apoptosis dalam sel endotel biakan dengan mekanisme yang mungkin mencakup penurunan transkripsi dari gen proapoptosis calreticulin dan TRMP-2, dan mempengaruhi gen antiapoptosis A1 Bc1-2 homolog dan penghambat apoptosis (IAP) homolog B. Pemeliharaan aliran darah dan oleh
karenanya mengurangi stress dapat menjadi penghambat apoptosis sel endotel yang penting, dan manfaat terapi yang direncanakan dengan segera dapat menggambarkan, sedikitnya sebagian, efek perlindungan hemodinamik pada fungsi sel endotel. Selain itu, insulin menimbulkan kelangsungan sel endotel yang
dependen Akt. Untuk menyoroti temuan ini, sangatlah menarik untuk menspekulasikan bahwa terapi insulin yang intensif dan kontrol gula darah yang ketat pada pasien dengan sakit kritis memiliki efek perlindungan ( prosurvival ) terhadap endotel.
Hipoksia telah terbukti mampu mempengaruhi kematian sel yang terprogram pada sel endotel, sehingga menegaskan pentingnya memelihara oksigenasi yang
adekuat. Strategi antiapoptosis lainnya yang dapat dipertimbangkan mencakup statin, antioksidan, faktor pertumbuhan dan penghambat caspase.
Faktor transkripsi sebagai target. Beberapa faktor transkripsi dalam endotel
telah terlibat dakam respons pejamu terhadap infeksi, termasuk NF-кB, epithelium-specific Ets factor-1 (ESE-1), activator protein-1 (AP-1), GATA-2, dan Egr-1. Selain itu, pemberian LPS pada hewan pengerat telah terbukti mampu menurunkan aktivitas ikatan DNA dengan Sp1 dan AP-2.
Dari berbagai faktor transkripsi yang terlibat dalam mediasi fenotip sepsis, NF-кB telah mendapatkan perhatian khusus sebagai target terapi yang potensial. Pada percobaan tikus dengan endotoksemia, transfer gen somatic secara intravena dengan IкBα menghasilkan peningkatan angka kelangsungan hidup. Dalam percobaan tikus dengan sepsis, pemberian pyrrolidine dithiocarbamate sistemik
menghambat ekspresi gen TNF-α, siklooksigenase-2 (COX-2) dan ICAM-1 yang dimediasi oleh NF-кB. Penghambat NF-кB yang lebih selektif, seperti peptida antibacterial PR39, dapat mempertahankan hasil yang lebih menjanjikan.
ATIII dan protein C aktif, masing-masing telah terbukti dapat menghambat aktivasi NF-кB pada sel endotel. Penelitian terbaru menunjukkan bahwa penggunaan glukokortikoid dosis rendah mengurangi angka kematian pada pasien dengan sepsis berat. Efek steroid yang menguntungkan juga mungkin berhubungan, sebagian, dengan melemahnya aktivitas NF-кB.
Sebagai hal yang penting, NF-кB telah terbukti mampu mengurangi apoptosis sel endotel yang dimediasi TNF-α, mungkin melalui induksi protein sitoprotektif seperti IAPs, Bc1-2-like factors, dan A20. Selain itu, blokade selektif NF-кB dapat mensensitisasi sel endotel terhadap efek proapoptosis TNF-α. Pengamatan ini menunjukkan bahwa NF-кB memiliki peran protektif selama perjalanan sepsis
dan menggarisbawahi perlunya kewaspadaan dalam pengembangan terapi anti- NF-кB.
J alur pemberian isyarat sebagai target. Jalur pemberian isyarat p38 mitogen-activated protein kinase (MAPK) dipercaya memiliki peran penting dalam memediasi respon proinflamasi dan apoptosis sel endotel. Mencit yang tidak memiliki MAPKAP kinase 2, sebuah target akhir p38 MAPK, menunjukkan peningkatan resistensi terhadap LPS, sebuah efek yang diperjelas dengan
berkurangnya produksi TNF-α. Beberapa penelitian telah menjadikan isyarat p38
MAPK sebagai target dalam percobaan menggunakan hewan, dengan hasil yang beragam. Yang menarik, dalam percobaan seorang manusia dengan endotoksemia, pemberian per oral penghambat p38 MAPK terbaru mengurangi produksi sitokin dan respon leukosit. Suatu perluasan dimana pengobatan tidak berdampak pada disfungsi sel endotel.
Isoform protein kinase C (PKC) yang baru dan atipikal juga terlibat dalam aktivasi sel endotel. Dalam kondisi in vitro, induksi ICAM-1 yang dimediasi trombin dalam sel endotel akan tergantung pada jalur pemberian isyarat PKC-δ
- NF-кB, dimana stimulasi ICAM-1 oleh TNF-α melibatkan PKC-ζ-NF-кB.
Stimulasi trombin VCAM-1 dalam sel endotel dimediasi oleh PKC-δ-NF-кB dan
jalur isyarat PKC-ζ-GATA-2. PKC-ζ juga terbukti memediasi stimulasi TNF-α
terhadap NADPH oxidase
–
derived ROS dalam sel endotel. Dibandingkan denganmencit liar, pemberian LPS terhadap PKC-ζ -/- mencit menghasilkan aktivasi
NF-кB yang lebih sedikit dan signifikan di paru, tetapi tidak di hepar. Hasil ini
menunjukkan bahwa isoform PKC-ζ memiliki peran yang penting dalam
memediasi respon pejamu pada organ tertentu dan dapat menunjukkan target terapi spesifik lokasi yang berharga pada kasus sepsis berat.
Pengambat Nitric oxide synthase (NOS). Sepsis dikaitkan dengan peningkatan aktivitas inducible NOS (iNOS) dan menurunkan aktivitas endotel NOS (eNOS). Meskipun demikian, peran relatif iNOS dan eNOS dalam memediasi fenotip sepsis masih belum jelas. Pada percobaan genetic tikus, tidak adanya iNOS dan eNOS tidak mengubah fenotipe sepsis secara signifikan. Sesungguhnya, ekspresi eNOS yang berlebih dan kronik dalam endotel mencit
berakibat peningkatan resistensi terhadap hipotensi yang dipengaruhi LPS dan kematian. Dalam beberapa penelitian, penggunaan penghambat NOS memberikan hasil yang menguntungkan, dimana beberapa penelitian lain melaporkan temuan yang berlawanan. Pada percobaan kelinci dengan sepsis, pemberian L-arginin, tetapi tanpa L-NAME ( N(G)-nitro-L-arginine methyl ester ), dapat menurangi kerusakan sel endotel oleh LPS. Induksi interaksi trombosit-endotel oleh LPS pada mencit yang telah terbukti dapat dikurangi dengan donor NO dan diperburuk
dengan penghambat NOS atau defisiensi eNOS, menunjukkan efek menguntungkan dari NO turunan eNOS. Penelitian lebih lanjut masih dibutuhkan untuk mempertimbangkan terapi penghambat NOS pada sepsis.
Tantangan terapi
Banyak alasan yang diungkapkan untuk menjelaskan sejarah kegagalan percobaan klinis pada sepsis. Hal ini meliputi tidak dapat digunakannya hasil percobaan dari hewan dengan sepsis, ketidakseragaman pengobatan suportif, heterogenitas populasi pasien, keterlibatan efek perancu, pemilihan waktu yang tidak tepat, dan pilihan pengujian hasil yang buruk. Penjelasan yang berhubungan dengan rumitnya respon pejamu. Hal ini sangat penting untuk dipertimbangkan ketika memilih endotel sebagai target terapi.
Pemilihan waktu. Sepsis menggambarkan serangkaian gejala klinis dan patologis yang berat. Dalam percobaan sepsis, pilihan criteria inklusi dan eksklusi akan sangat mempengaruhi hasilnya. Contohnya, pada satu akhir spectrum, inklusi pasien berisiko rendah dapat menyembunyikan respon menguntungkan yang sebaliknya. Pada individu ini, efek berlawanan dari pengobatan (seperti perdarahan akibat antikoagulan) dapat lebih banyak dari keuntungan kecil lainnya. Pertimbangan lain yang penting adalah sifat adaptasi alami respon pejamu. Selama respon menyeluruh adalah protektif (misal selama stadium awal perjalanan sepsis), terapi yang ditargetkan mungkin tidak memiliki pengaruh, atau bahkan memberikan dampak negative terhadap kelangsungan hidup. Pada keadaan lain, pasien dengan penyakit stadium akhir dapat relatif resisten terhadap terapi. Kaskade yang dipengaruhi sepsis yang telah mendapatkan intervensi terapi, mungkin tidak lagi responsif. Ketika merencanakan terapi dengan target endotel,
akan sangatlah penting untuk menentukan pemilihan waktu yang optimal dan spectrum beratnya suatu penyakit.
Kerumitan respon pejamu. Secara tradisional, berbagai pendekatan telah dilakukan untuk memahami patofisiologi sepsis. Sesungguhnya, sebagian besar penelitian dasar dalam bidang ini telah terfokus pada mekanisme isolasi dan
spesifik tentang respon pejamu. Data ini telah memunculkan model patofisiologi linear, yang telah memandu pada pilihan target terapi. Dugaan bahwa berbagai komponen respon pejamu terlibat dalam serangkaian prediksi dimana berkurangnya satu saja komponen tersebut (contoh TNF-α) akan mengganggu kaskade sepsis. “Model tipe domino” ini memberikan cara untuk paradigma kerumitan nonlinear yang lebih realistis, dimana berbagai tipe sel, mediator inflamasi, faktor koagulasi, reseptor permukaan sel, jalur isyarat intraseluler, faktor transkripsi, dan gen berinteraksi sebagai bagian dari jaringan yang saling berpasangan lokasi dan waktunya.
Satu cara untuk memahami kerumitan respon pejamu yang tak terpisahkan adalah untuk mengembangkan rencana target dasar yang luas, dimana berbagai komponen dikurangi secara bersamaan, misalnya kaskade inflamasi dan koagulasi. Hal ini mungkin dengan memilih terapi yang lebih luas yang menggantikan protein C aktif, dimana banyak agen lainnya sebelum ia gagal. Meskipun mekanisme yang tepat dimana drotrecogin alfa (aktif) yang meningkatkan angka kelangsungan hidup pada pasien ini belum diketahui, beberapa bukti mengarah pada peran beraneka ragam komponen ini dalam
menghambat respon proinflamasi dan prokoagulan, memicu fibrinolisis, dan mengurangi aktivasi sel endotel dan leukosit.
Pendekatan alternative adalah untuk menargetkan komponen respon pejamu yang tidak berlebihan yang menjadi pusat inisiasi dan bertahannya fenotip sepsis. Beberapa contoh dapat meliputi fungsi tunggal endotel (misal apoptosis), atau faktor transkripsi tunggal (misal NF-кB). Meskipun demikian, dalam merencanakan strategi semacam itu, sangatlah penting bila kita memahami perilaku sistem kompleks linear yang tak terprediksi dan mengatur kembali harapan kita sesuai kondisi tersebut. Bila dalam teori, respon pejamu terhadap
infeksi (dalam setiap pasien pada setiap waktu) dapat dibentuk dengan serangkaian kompleks persamaan nonlinear yang sangat rumit, formula ini tidak hanya sulit untuk dipahami, tetapi juga mungkin sangat sensitive pada kondisi awal. Hasilnya, menjadikan target komponen tunggal tidak hanya dapat gagal dalam memodulasi respon pejamu, tetapi dapat memiliki konsekuensi yang tidak diharapkan dan mengganggu. Tantangan ilmiah yang penting untuk abad 21 adalah untuk mempelajari bagaimana mempengaruhi interaksi nonlinear bagi pendekatan mekanistik dan terapetik. Perkembangan lebih lanjut dalam memahami jaringan yang rumit akan mendasari peningkatan hasil dan sarana matematis dan statistik yang lebih lengkap, termasuk kemajuan teknik pengelompokan, pengumpulan data dan strategi pengenalan pola, teknik Bayesian, persamaan diferensial, serta sarana simulasi. Dengan mempelajari dan melingkupi
model biologis yang lebih realistis yang melibatkan jaringan yang rumit, kita dapat meningkatkan kapasitas kita untuk menyusun kembali respon pejamu dalam pemahaman kita.
Implikasi bagi percobaan klinis. Dalam percobaan klinis, pasien mungkin serupa, tetapi mereka tidak pernah identik. Dari titik awal terapi, apa yang dapat menyelamatkan seorang pasien, mungkin berbahaya bagi yang lainyya. Selain itu, intervensi terapi yang menguntungkan pasien pada suatu waktu dapat mengganggu titik lain pada saat bersamaan. Sehingga, terapi yang optimal bagi sepsis sangat tergantung pada masing-masing pasien dan waktu. Meskipun demikian, sampai saat kita dapat menandai perilaku yang rumit dari respon pejamu, kita akan terbatas pada desain klasik randomized control trial , dimana intervensi tunggal diuji dalam kelompok pasien yang heterogen. Tujuan yang penting, yang hanya dapat dicapai melalui percobaan klinis besar, adalah untuk
mengidentifikasi sejumlah pasien yang mendapatkan manfaat pengobatan. Informasi ini kemudian dapat digunakan untuk merancang penelitian preklinis/klinis yang baru. Beberapa pendekatan akan membantu mengurangi heterogenitas pasien dan dapat mengembangkan terapi yang lebih sesuai, misalnya, terhadap salah satu komponen respon endotel atau komponen lainnya atau terhadap anyaman pembuluh darah yang spesifik.
Simpulan
Selain informasi baru tentang patofisiologi dan pengobatan sepsis berat, kelainan ini juga berhubungan dengan tingginya angka kematian yang tidak dapat diterima. Pemecahan selanjutnya akan membutuhkan pergeseran konsep yang menegaskan hubungan antara mediator yang bervariasi dan sel yang terlibat dalam respon pejamu. Endotel merupakan kunci dalam mengawali, mempertahankan dan memodulasi respon pejamu terhadap infeksi. Penelitian tambahan menjanjikan untuk memberikan pandangan yang baru tentang endotel, bukan sebagai mekanisme isolasi dari patofisiologi sepsis, tetapi lebih sebagai koordinator dalam respon yang tersusun jauh lebih luas, secara lokasi dan waktu.
Catatan tambahan untuk dibuktikan. Penelitian terkini menunjukkan bahwa protein C aktif memberi isyarat melalui PAR-1 dalam sel endotel biakan, oleh suatu mekanisme dependen EPCR. Konsisten dengan hasil ini, baik EPCR dan PAR-1 terbukti memang dibutuhkan untuk memediasi fungsi sitoprotektif dari protein C aktif dalam biakan sel endotel otak manusia yang hipoksia dan dalam mencit dengan model stroke. Secara bersamaan, temuan ini menunjukkan bahwa protein C aktif memberi isyarat melalui reseptor PAR-1 baik in vitro maupun in
vivo. Oleh karena PAR-1 juga merupakan reseptor bagi trombin, penelitian ini menimbulkan pertanyaan menarik tentang bagaimana dua ligan yang berbeda, yaitu protein C aktif dan trombin, memediasi respon PAR-1 yang berbeda (misal, respon perlindungan dan proinflamasi, secara berurutan).