PENGARUH PERLAKUAN ASAM DAN WAKTU
FERMENTASI TERHADAP PEMBENTUKAN
BIOETANOL DENGAN BAHAN BAKU SABUT KELAPA
Faisol Asip*, Bella Febrianti, Siti Gibreallah
*Jurusan Teknik Kimia, Fakultas Teknik, Universitas Sriwijaya Jl. Raya Indralaya – Prabumulih KM. 32 Indralaya Ogan Ilir (OI) 30662
Email: [email protected]
Abstrak
Sabut kelapa merupakan salah satu bahan limbah yang memiliki kandungan lignoselulosa yang cukup tinggi namun belum dimanfaatkan secara optimal. Pada umumnya sabut kelapa digunakan sebagai kerajinan tangan atau hanya dibuang dan dibakar begitu saja. Dengan kadar selulosa sebesar 44,4433% sabut kelapa dapat dikonversi menjadi bioetanol yang merupakan bentuk pemanfaatan yang lebih berguna dan memiliki nilai yang jauh lebih tinggi. Penelitian ini bertujuan untuk mengetahui pengaruh asam kuat (H2SO4) dan asam lemah (CH3COOH) pada delignifikasi untuk menurunkan kadar lignin pada sabut kelapa dengan variasi konsentrasi 1, 3, 5%. Setelah itu dilakukan proses hidrolisis dengan larutan basa (KOH 5%) yang selanjutnya dilakukan proses fermentasi dengan waktu 3, 5, 7 hari menggunakan ragi Saccharomyces cerevisiae. Dari hasil penelitian yang didapat kadar lignin terendah didapatkan pada sampel H2SO4 5%, sedangkan dari hasil hidrolisis didapat kadar glukosa tertinggi didapatkan oleh sampel H2SO4 5%, dan kadar bioetanol terbesar adalah 5,7768 %v/v yang didapatkan dari sampel H2SO4 5% dengan waktu fermentasi optimal selama 5 hari.
Kata Kunci: Bioetanol, delignifikasi, fermentasi, hidrolisis, sabut kelapa.
Abstract
Coconut coir is a waste material that containS high lignocellulose but has not been used optimally. In general, coconut fiber used as crafts or simply thrown away or just burned away. With a cellulose content of 44.4433% coconut coir can be converted into bioethanol, which is a more useful and have a much higher value. This study aims to determine the influence of strong acid (H2SO4) and weak acid (CH3COOH) on delignification to reduce the lignin content in coconut coir with various concentration of 1, 3, 5%. Ater that, hydrolysis process done by alkaline solution (KOH 5%) and the fermentation process with a time of 3, 5, 7 days using a yeast of Saccharomyces cerevisiae. From the research results obtained low lignin content was found in samples of using H2SO4 5% on delignifiacation process, whereas of hydrolysis obtained the highest glucose levels obtained by the sample H2SO4 5%, and the best concentration of bioethanol is 5.7768%v/v obtained from the sample H2SO4 5% at with optimal fermentation time for 5 days.
Keywords: Bioethanol,delignification, fermentation, hydrolysis, coconut coir.
1. PENDAHULUAN
Meningkatnya jumlah populasi manusia di Indonesia menyebabkan kebutuhan akan energi minyak bumi juga semakin meningkat. Hal ini dilihat dari banyaknya konsumsi bahan bakar minyak dan jumlah impor yang dilakukan di negara Indonesia. Berdasarkan data Badan Pusat Statistik (BPS) pada bulan Februari 2015, impor migas mencapai 11,558 miliar dollar AS atau naik 6,34% dibandingkan dengan data yang diperoleh pada Januari 2015.
mempunyai beberapa keunggulan dibanding dengan bahan bakar minyak, yaitu kandungan oksigen yang tinggi sebesar 35%, sehingga jika dibakar sangat ramah lingkungan karena emisi gas karbon monoksida yang dihasilkan lebih rendah yaitu 19-25% dibandingkan dengan bahan bakar minyak, sehingga tidak memberikan kontribusi pada akumulasi karbon dioksida di atmosfer dan bioetanol bersifat dapat diperbaharui, sedangkan bahan bakar minyak akan habis karena bahan bakunya adalah fosil (Aisyah, S. N; Sembiring, K. C, 2010).
Sumber bahan baku bioetanol umumnya dapat ditemukan dari tanaman yang mengandung pati, seperti singkong, kelapa, kapuk, kelapa sawit, jarak pagar, rambutan, sirsak, atau tengkawang, tanaman yang mengandung gula seperti tetes tebu atau molase, nira tebu, nira aren, dan nira surgum manis, dan juga mengandung serat selulosa seperti jerami padi, serbuk kayu, batang sorgum, batang pisang, dan sabut kelapa. Bioetanol sendiri sebenarnya lebih mudah dihasilkan dari bahan baku yang mengandung glukosa karena proses pembentukan nya lebih sederhana, namun bahan baku yang mengandung glukosa lebih banyak dimanfaatkan dalam produk lain seperti di bidang pangan, maka dari itu pembuatan bioetanol lebih di kembangkan dengan bahan baku yang mengandung selulosa. Selulosa merupakan sumber daya alam yang banyak ditemukan di alam, serta memiliki potensi dalam menghasilkan produk yang bermanfaat seperti glukosa, etanol, dan juga bahan bakar (Gunam, ddk, 2011). Salah satu bahan baku yang mengandung selulosa yang dapat dimanfaatkan untuk pembuatan bioetanol yaitu sabut kelapa, karena sabut kelapa merupakan salah satu bahan baku yang mengandung kadar selulosa yang cukup tinggi.
Tabel 1. Komposisi Sabut Kelapa
Senyawa Persentase (%)
Selulosa 43,44
Dilihat dari komposisi kimia sabut kelapa yang terdiri dari selulosa, maka sabut kelapa
dapat dimanfaatkan sebagai bahan baku pembuatan bioetanol.
Sabut kelapa adalah salah satu limbah yang jumlahnya banyak dan dapat dimanfaatkan kembali. Setiap butir sabut kelapa, bisa menghasilkan serat (coco fiber) sekitar 0,15 Kg dan serbuk (coco peat) sekitar 0,39 Kg, Menurut data BPS Provinsi Sumatera Selatan tahun 2013, luas area kebun kelapa di Sumatera Selatan sekitar 7 1.441 ha yang tersebar di 14 wilayah yang ada di Sumatera Selatan, dengan melihat jumlah sebesar ini maka dapat dikatakan bahwa limbah sabut kelapa di Sumatera Selatan merupakan salah satu jenis limbah yang banyak dihasilkan, dan dapat menjadi salah satu komoditi limbah yang memiliki potensi bisnis yang tinggi jika dimanfaatkan dengan baik Sabut kelapa merupakan bagian terluar yang membungkus buah kelapa, sabut kelapa yang dimiliki oleh setiap buah kelapa berkisar hampir 35% atau sekitar 2/3 bagian dari volume buah kelapa, ketebalan sabut kelapa berkisar 5-6 cm yang terdiri dari lapisan terluar (exocarpium) dan lapisan dalam (endocarpium).
Pemanfaatan sabut kelapa kebanyakan hanya untuk dibakar ataupun dijadikan kerajinan tangan. Pembakaran sabut kelapa dapat mengakibatkan polusi udara dan emisi gas dilingkungan dan rendahnya nilai kebermanfaatan sabut kelapa tersebut. Sehingga jika dikonversi menjadi bioetanol selain akan mengurangi limbah dari perkebunan kelapa, mengurangi polusi dari efek pembakaran langsung serta meningkatkan nilai kebermanfaatan sabut kelapa itu sendiri, selain itu hal ini juga dapat mengurangi kebutuhan impor migas jika dilakukan produksi secara massal dan secara berkelanjutan.
2. METODOLOGI PENELITIAN Waktu dan Tempat Penelitian
Penelitian ini telah dilakukan pada bulan Oktober 2015 sampai Februari 2016, di Laboratorium Bioproses Jurusan Teknik Kimia Fakultas Teknik, Universitas Sriwijaya.
Alat-alat yang digunakan pada penelitian ini adalah neraca analitik, gelas ukur, labu ukur 500mL dan 1 L, pipet tetes, erlenmeyer 1000 mL, erlenmeyer 500mL, batang pengaduk, autoclave, beaker gelas 500mL, saringan, corong gelas, oven, Ph kertas, aluminium foil, seperangkat alat distilasi, hotplate, piknometer 5mL, blender.
pekat, larutan luff, larutan KI, Na2CO3, larutan amylum, dan HCl.
Variabel tetap dari penelitian ini adalah bahan baku berupa sabut kelapa 30 g, larutan hidrolisa KOH 5%, berat ragi (Saccharomyces cerevisiae) 1% dari massa fermentasi. Dan yang merupakan variabel bebas pada penelitian ini merliputi larutan yang dihgunakan untuk pretreatment yaitu H2SO4 dan CH3COOH (1,3,5) % dan waktu fermentasi (3, 5, 7) hari.
Prosedur Penelitian A. Pretreatment
Bahan baku (sabut kelapa) dikeringkan di panas matahari. Kemudian sabut kelapa digiling dengan menggunakan blender sampai ukuran berukuran ±1mm. Setelah itu sebanyak 30 g sabut kelapa dimasukkan dalam erlenmeyer 1000mL dan ditambahkan masing-masing H2SO4 dan CH3COOH (1, 3, 5) %. Proses selanjutnya, tutup rapat erlenmeyer dengan tutup gabus, dan sampel dipanaskan selama 60 menit pada suhu 121oC di autoclave. Setelah dipanaskan, sampel kemudian disaring dan residu dicuci dengan aquadest hingga pH netral (pH 7). Filtrat kemudian dikeringkan di dalam oven selama 4 jam pada suhu 105oC, hingga kering.
B. Tahap Hidrolisa
Hasil pretreatment yang telah kering, dimasukkan kedalam erlenmeyer 1000mL kemudian ditambahkan sebanyak 500mL larutan KOH 5%. Setelah itu tutup rapat erlenmeyer dengan tutup gabus dan dipanaskan selama 1 jam pada suhu 121oC di autoclave.
C. Tahap Fermentasi
Filtrat hasil hidrolisis (hidrolisat) selanjutnya didinginkan dan disaring dan diambil filtrate berupa larutan kemudian pH larutan diatur dengan ditambahkan sejumlah larutan NaOH hingga mencapai Ph 5. Hidrolisat kemudian ditambahkan ragi (Saccharomyces cerevisiae) sebanyak 1% dari massa larutan yang akan difermentasi. Hidrolisat berisi sampel yang akan difermentasi, ditutup rapat dengan tutup gabus yang kemudian corong erlenmeyer dihubungkan selang karet, ujung selang dimasukkan ke dalam botol berisi air agar tidak terjadi kontak langsung dengan udara dilingkungan sekitar. Setelah itu dilakukan inkubasi selama selang waktu tertentu sesuai dengan variasi yang ditentukan (3, 5, 7) hari. Setelah proses fermentasi, larutan di murnikan menggunakan rotary vakum evaporator.
D. Tahap Pemurnian Bioetanol
Siapkan 1 set peralatan rotary vakum evaporator. Ambil larutan dari hasil fermentasi kemudian masukkan dalam labu, pasang labu pada alat evaporator. Pertahan temperatur 78oC selama 10 menit untuk mendapatkan hasil bioetanol yang bervariasi. Simpan bioetanol dalam wadah yang tertutup rapat, simpan dalam lemari pendingin dengan suhu <5oC. Analisa bioetanol dilakukan degan metode pengukuran densitas dan juga dengan Gas Chromatography.
Prosedur Analisa Penentuan kadar selulosa dan lignin menggunakan metode Chesson
Sampel kering sebanyak 1 g (berat a) ditambahkan 150 ml aquadest direfluk pada suhu 100oC menggunakan waterbath selama 1 jam. Hasilnya kemudian disaring, residu dicuci dengan air panas 300mL, kemudian residu dikeringkan dengan oven sampai beratnya konsntan dan kemudian ditimbang (berat b). Selanjutnya, residu ditambah 150 mL H2SO4 1N, kemudian direfluk dengan waterbath selama 1 jam pada suhu 100oC. Hasilnya dikeringkan kemudian dicuci hingga pH netral, dan residu dikeringkan hingga berat konstan, kemudian ditimbang (berat c). Residu kering sampai beratnya konstan dan ditimbang (berat d). Selanjutnya residu diabukan dengan furnace pada suhu 575oC dan kemudian ditimbang (berat e).
Perhitungan kadar selulosa dan kadar lignin menggunakan rumus berikut ini:
Kadar Selulosa =
Kadar Lignin =
Penentuan Kadar Glukosa dengan Metode
Luff Schoorl
Analisa Titrasi Luff-Schoorl
Sebanyak 25 ml larutan yang akan diuji ditambahkan 25 ml larutan luff schoorl dan dimasukkan ke dalam erlenmeyer. Sampel didihkan selama 10 menit dalam Erlenmeyer yang dilengkapi dengan pendingin balik. Hasil pendidihan didinginkan dengan cepat, setelah dingin ditambahkan dengan hati-hati 15 ml larutan KI 20% dan 25ml larutan H2SO4 26,5%. Ditambahkan indicator amilum 1% sebanyak 2 ml. Larutan dititrasi dengan larutan Na2S2O3 (Natrium Tiosulfat) 0,1 N secara hati-hati sampai larutan berwarna putih susu. Catat jumlah larutan Na2S2O3 yang digunakan. Dilakukan titrasi terhadap blanko (25 ml aquadest), volum masing-masing dicatat. Kadar gula dihitung berdasarkan selisih titrasi blanko dan titran sampel dengan menggunakan tabel gula menurut Luff-Schoorl (terlampir). Adapun perhitungan kadar blanko adalah sebagai berikut :
ml Na2S2O3 = ml Na2S2O(Blanko-sampel) x N. Na2S2O3 X 10
P = Pengenceran sampel : volume yang diambil untuk analisis
Penentuan Densitas dengan Piknometer
Untuk menganalisa kadar alkohol (bioetanol) yang didapat digunakan analisa densitas. Analisa densitas ini dilakukan dengan menggunakan alat piknometer, piknometer yang digunakan adalah piknometer 5 mL pada suhu kamar.
Prosedur perhitungan densitas dengan menggunakan piknometer, yaitu :
1. Menimbang berat piknometer kosong pada suhu kamar diperoleh a gram.
2. Menimbang berat piknometer yang telah berisi aquadest penuh pada suhu kamar diperoleh b gram.
3. Menghitung volume piknometer dengan menggunakan rumus
Volume piknometer = = c mL 4. Menimbang berat piknometer yang telah
diisi penuh dengan zat (bioetanol) yang akan ditentukan densitasnya pada suhu kamar diperoleh d gram.
Densitas =
Densitas =
Dari densitas yang diperoleh dapat ditentukan kadar alkohol (bioetanol) yang terkandung dengan melihat tabel densitas standar bioetanol pada suhu kamar (terlampir). Analisa ini dilakukan terhadap hasil fermentasi yang telah di destilasi, gunanya untuk mengetahui kadar alkohol (bioetanol) yang terdapat dalam hasil fermentasi.
3. HASIL DAN PEMBAHASAN
Pengaruh Konsentrasi H2SO4 dan
CH3COOH terhadap Delignifikasi
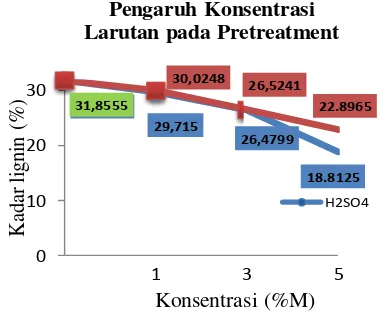
Penelitian pengaruh variabel konsentrasi H2SO4 dan CH3COOH terhadap kadar lignin yang hilang dari proses delignifikasi berbahan baku sabut kelapa, menggunakan variasi konsentrasi H2SO4 dan CH3COOH sebesar (1, 3, 5)%. Penurunan kadar lignin pada sampel setelah proses delignifikasi diuji dengan menggunakan metode Chesson.
Grafik dibawah ini menggambarkan kadar penurunan lignin yang terjadi setelah dilakukan proses delignifikasi. terhadap Penurunan kadar Lignin
tinggi dialami pada penggunaan senyawa asam kuat, hal ini terjadi karena asam kuat lebih reaktif untuk memecah lapisan lignin dan melarutkannya dibandingkan dengan asam lemah dan juga semakin besar konsentrasi dari suatu larutan maka akan semakin banyak molekul dari larutan itu yang dapat memecah struktur lignin. Menurut Sahare et al. (2012) dalam Mardina et al. (2013).Pengurangan kadar lignin yang semakin besar menyebabkan semakin banyak selulosa yang reaktif untuk proses hidrolisis.
Pengaruh Konsentrasi H2SO4 dan
CH3COOH Delignifikasi Terhadap Glukosa
yang Dihasilkan
Gambar 2. Hasil Analisis Kadar Glukosa
terhadap konsentrasi Delignifikasi H2SO4 dan CH3COOH
Proses hidrolisis pada penelitian ini dilakukan dengan menggunakan variabel tetap berupa jenis larutan KOH 5%, suhu 1210C, dan waktu 1 jam. Pemilihan penggunaan KOH pada proses hidrolisis dikarenakan pada proses pretreatment telah dilakukan menggunakan asam, sehingga untuk melanjutkan ke proses hidrolisa di perlukan larutan basa sebagai katalis dalam proses hidrolisa. Pada tahapan ini tidak terdapat variable bebas. Metode Luff-schrool dilakukan untuk menganalisis kadar glukosa pada sampel. Gambar 2. menunjukkan konsentrasi delignifikasi H2SO4 dan CH3COOH terhadap analisis pembentukan kadar glukosa. Pada gambar terlihat jelas bahwa semakin kuat asam serta semakin besar konsentrasi larutan yang digunakan ketika proses delignifikasi semakin besar pula kadar glukosa yang dihasilkan hal tersebut telah dijelaskan sebelumnya pada hasil analisis uji lignin dimana
semakin banyak lignin yang terdegradasi maka akan semakin banyak selulosa yang terbentuk dan akan menghasilkan konversi selulosa ke glukosa yang juga akan semakin tinggi. Kadar glukosa paling besar ditunjukkan pada sampel dengan delignifikasi H2SO4 5%, yaitu 6,2446%.
Pengaruh Waktu Fermentasi Terhadap Kadar Bioetanol
Proses fermentasi pada penelitian ini dilakukan dengan menggunakan variable tetap berupa khamir Saccharomyces Cerevisiae (ragi roti) sebanyak 3 gr (1% dari massa larutan fermentasi), dan pH 5.
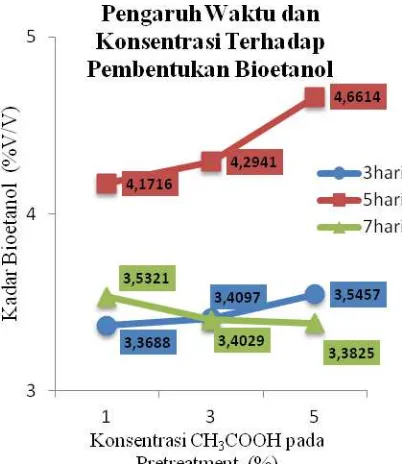
Gambar 3. Hasil Analisis Density pengaruh waktu fermentasi terhadap kadar Bioetanol dengan konsentrasi Delignifikasi H2SO4
Gambar 4. Hasil Analisis Density pengaruh waktu fermentasi terhadap kadar Bioetanol dengan konsentrasi Delignifikasi CH3COOH.
Dari Gambar 3. dan Gambar 4. menunjukkan pengaruh dari waktu fermentasi terhadap hasil analisis kadar bioetanol yang menggunakan asam kuat dan asam lemah saat proses delignifikasi. Dapat dilihat, bahwa produksi bioetanol pada hari ketiga memiliki hasil yang cukup signifikan, selanjutnya memasuki hari kelima bioetanol yang diproduksi masih mengalami peningkatan, namun pada saat memasuki hari ketujuh bioetanol yang dihasilkan mengalami penurunan. Hal ini menunjukkan waktu optimal fermentasi adalah 5 hari. Pada tabel 4.3 dapat pula dilihat kadar bioetanol tertinggi yang diukur menggunakan metode density dimiliki oleh sampel yang menggunakan asam kuat 5% pada saat proses delignifikasi hal ini disebabkan karena sampel dengan delignifikasi H2SO4 5% menghasilkan glukosa dengan kadar tertinggi sehingga konversi glukosa ke bioetanol juga memiliki hasil yang paling tinggi.
Kadar bioetanol yang dihasilkan pada sampel dengan delignifikasi H2SO4 5%, serta waktu fermentasi optimum (5 Hari) adalah 5,7768%. Berdasarkan hal tersebut, 2 sampel terbaik bioetanol yang telah dihitung kadarnya menggunakan metode density dari masing-masing asam kuat dan asam lemah dilakukan pengujian gas chromatography untuk dilakukan pengujian kadar bioetanol secara akurat.
Pengujian bioetanol menggunakan GC (gas chromatography) pada sampel yang di pretreatment menggunakan asam kuat (H2SO4) 5% dan waktu fermentasi selama 5 hari menunjukkan jumlah bioetanol yang terkadung memiliki konsentrasi sebesar 5,075 %v/v sedangkan pada sampel yang dilakukan pretreatment menggunakan asam lemah (CH3COOH) dan waktu fermentasi selama 5 hari menunjukkan kadar bioetanol yang terbentuk sebesar 3,968 %v/v.
Gambar 5. Kadar pertumbuhan bioetanol
terhadap kurva pertumbuhan Saccaromyces cerevisiae
ini mengakibatkan bioetanol yang dihasilkan oleh ragi semakin sedikit.
Waktu fermentasi juga mempengaruhi jumlah gas CO2 yang dihasilkan. Semakin lama proses fermentasi maka gas CO2 yang dihasilkan akan semakin banyak juga (Hambali,et,al.2008). Peningkatan produksi gas ini menyebabkan penurunan nilai pH, karena gas CO2 sering disebut gas asam atau memiliki sifat asam sehingga CO2 berkontribusi terhadap nilai PH (Kartohardjono,et,al.2007), Kondisi ini menyebabkan pertumbuhan Saccharomyces cerevisiae terganggu dan menyebabkan semakin sedikit bioetanol yang akan dihasilkan (Datar,et,al.2004 dalam Azizah,et,al.(2012). Menurut Roukas (1994) dalam Azizah,et,al.(2012), kisaran pertumbuhan Saccharomyces cerevisiae adalah pada pH 3,5-6,5. Ditambahkan oleh Elevri dan Putra (2006) produksi optimal bioetanol oleh Saccharomyces cerevisiae terjadi pada pH 4,5.
Pada gambar diatas juga ditunjukkan kadar bioetanol yang terbentuk yang dihubungkan dengan kurva pertumbuhan bakteri Saccaromyces cerevisiae, dapat dilihat bahwa, pada sampai hari ke-3, Saccaromyces cerevisiae berada pada lag phase, dimana pada fase ini kadar bietanol yang dihasilkan masi sedikit yakni kurang dari 4%, pada hari ke-5, Saccaromyces cerevisiae memasuki fase stasioner (stationary phase), dan kadar bietanol yang dihasilkan mencapai hasil yang tertinggi yakni 5,7768%, selanjutnya pada hari ke-7, Saccaromyces cerevisiae memasuki fase kematian (death phase) dimana hal ini menyebabkan kadar bietanol yang dihasilkan mengalami penurunan hingga 38%. Hal ini menunjukkan bahwa waktu optimum fermentasi terjadi pada hari ke-5.
4. KESIMPULAN
Kadar bioetanol paling tinggi dihasilkan oleh sampel dengan konsentrasi asam sulfat saat delignifikasi sebesar 5% serta fermentasi dihari kelima yaitu sebesar 5,7768%. Kadar penurunan lignin paling tinggi ditunjukkan pada pretreatment menggunakan asam kuat dengan konsentrasi tertinggi (5%) dan semakin tinggi konsentrasi asam kuat (H2SO4) maka kadar glukosa yang dihasilkan semakin besar, kadar glukosa tertinggi dihasilkan pada konsentrasi 5% asam sulfat. Semakin lama waktu fermentasi, kadar bioetanol yang dihasilkan semakin besar, waktu optimum pembentukan bioetanol yaitu pada hari kelima. Melewati waktu optimum tersebut kadar bioetanol yang dihasilkan mengalami penurunan.
DAFTAR PUSTAKA
Alex. 2015. Rotary Evaporator. (online). (http://research. fk.ui.ac .id/ sistem informasi/). Diakses 4 Januari 2016. Anindyawati, T. 2009. Prospek Enzim dan
Limbah Lignoselulosa untuk Produksi Bioetanol. BS 1(44) : 49-56.
Anonim. 2015. Perkebunan Kelapa. (Online). (http://www.bps.go.id). Diakses 4 Januari 2016.
Anonim. 2014. skema tujuan pretreatment biomassa lignoselulosa. (Online). (http://syifarobbani.wordpress.com). Diakses 10 Februari 2016.
Anonim. 2014. Molekul Selulosa. (online). (http://www.scientificpsychic.com/). Diakses 10 Februari 2016.
Anonim. 2015. Struktur molekul etanol. (Online). (http://id.wikimedia.org/). Diakses 10 Februari 2016.
Axelsson, Josefin. 2011. Separate Hydrolysis and Fermentation of Pretreated Spruce. Department of Physics, Chemistry and Biology Linkoping University : Sweden. Azizah,N.et.al. 2012. Pengaruh Lama
Fermentasi Terhadap Kadar Alkohol, pH, Dan Produksi Gas Pada Proses Fermentasi Bioetanol Dari Whey Dengan Subtitusi Kulit Nanas. Jurnal Aplikasi Teknologi Pangan 1(3):72-77.
Badan Standarisasi Nasional. 1992. Cara Uji Makanan dan Minuman. SNI : 01-2891-1992.
Badan Standarisasi Nasional. 2012.Bioetanol Terdenaturasi Untuk Gasohol. SNI : 7390-2012
Fitriani, S. Bahri, Nurhaeni, 2013. Produksi Bioetanol Tongkol Jagung (Zea Mays) dari Hasil Proses Delignifikasi. Online Jurnal of Natural Science. 2(3) : 66-74.
Hargono, N.B.Samodra, N.Z.Firdausi. 2013. Rancang Bangun Alat Destilasi Pemurnian Bioetanol Grade Teknis Berskala UKM : Kajian Kinerja Alat Tentang Derajad Pemurniannya. TEKNIK. 3(34) : 0852-1697
Hasanah, Hafidatul. 2008. Pengaruh Lama Fermentasi Terhadap Kadar Alkohol Tape Ketan Hitam (Oryza sativa L var forma glutinosa) dan Tape Singkong (Manihot utilissima Pohl). [Skripsi]. Malang : Fakultas Sains dan Teknologi. Universitas Islam Negeri (UIN) Malang.
Muryanto.2012. Enkapsulasi Rhizopus oryzae dalam Kalsium-alginat untuk Produksi Bioetanol dari Tandan Kosong Kelapa Sawit dengan Sakarifikasi dan Fermentasi Serentak. [Tesis]. Depok: Fakultas Teknik. Universitas Indonesia.
Pangestu. 2011. Teknologi Pengolahan Hasil Pertanian. Bina Ilmu, Surabaya.
Perry, J. H. 1984. Chemical Engineering Handbook, 6th edition Mc Graw Hill,. Inc, New York.
Prawitwong,P.et.al. 2012. Efficient Ethanol Production from Separated Parenchyma and Vascular Bundle of Oil Palm Trunk. BioresourceTechnology 125(2012):37-42. Purnomo,F. 2012. Proses Delignifikasi Tongkol
Jagung Menggunakan Ammonium Hidroksida Sebagai BAhan Baku Pembuatan BIoetanol [Skripsi]. Purwokerto : Fakultas Teknik Jurusan Teknik Kimia. Universitas Muhammadiyah Purwokerto.
Rusdi, P. Akbar. 2014. Sistem Pengendalian Suhu Pada Proses Distilasi Vakum Bioetanol Menggunakan Kontrol Logika Fuzzy. [Skripsi]. : Fakultas Teknik. Teknik elektro
Saifuddin,F. 2007. Pemodelan Matematika Digester Pulp Kontinyu. [Tesis]. Bandung : Fakultas Teknologi Industri. Institut Teknologi Bandung.
Sari, Niketut. 2014. Proses Kimia dan Biologi Pembuatan Bioetanol Dari Rumput Gajah. (Online). (http://niketut.wordpress.com). Diakses 10 Februari 2016.
Sukadarti, S, dkk. 2010. Produksi Gula Reduksi dari Sabut Kelapa Menggunakan Trichoderma reesei. Prosiding Seminar Nasional Teknik Kimia Kejuangan, Universitas Pembangunan Nasional Veteran. Yogyakarta.
Taherzadeh, M.J., and K. Karimi. 2008. Pretreatment of Lignocellulosic Waste to Improve Ethanol and Biogas Production : A review. International Journal of Molecular Sciences. 9: 1621-1651.
Wiratmaja,I.G. 2010. Analisa Unjuk Kerja Motor Bensin Akibat Pemakaian Biogasoline. Jurnal Ilmiah Teknik Mesin CakraM. 1(4): 16-25.
Wiratmaja, I. G., Kusuma, I.G. dan Winaya, I.N., 2011. Pembuatan Etanol Generasi Kedua Dengan Memanfaatkan Limbah Rumput Laut Eucheuma Cottonii sebagai Bahan Baku. Universitas Udayana. Jurnal Ilmiah Teknik Mesin, 5 (1): 75-84.
Yuanisa, A., K. Ulum, A.K. Wardani. 2015. Pretreatment Lignoselulosa Batang Kelapa Sawit Sebagai Langkah Awal