Bank Soal UN Sistem Periodik Unsur
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia tahun dari 2002 un hingga 2011, 2012, 2013 dan 2014 berkaitan dengan sistem periodik unsur / SPU dan konfigurasi elektron.
Sistem Periodik Unsur
(1) Soal Ebtanas Tahun 2001
Diantara sifat periodik berikut, yang benar dalam satu golongan dari atas ke bawah adalah... A. jari-jari elektron makin pendek
B. elektronegativitas makin kecil C. energi ionisasi makin besar D. afinitas elektron makin besar E. sifat logam berkurang
(2) Soal Ebtanas Tahun 2001
Suatu unsur X mempunyai konfigurasi elektron [54Xe] 6s2 4f2. Unsur X dalam sistem periodik
termasuk dalam.... A. blok s B. blok p C. blok d D. blok f E. blog g
(3) Soal Ebtanas Tahun 2002
Unsur V, W, X, Y, Z berturut-turut mempunyai nomor atom 2, 3, 8, 13, 16, Pasangan unsur yang berada dalam satu golongan adalah....
A. A dan C B. C dan E C. B dan E D. D dan C E. E dan B
(4) Soal Ebtanas Tahun 2003
Unsur tembaga, Cu, dengan nomor atom 29, terletak pada golongan dan periode.... A. IA / 5
B. IIA / 3 C. IB / 4 D. VB / 7 E. VII / 5
(5) Soal Ebtanas Tahun 2003
Berdasarkan sifat reduktornya, urutan yang benar dari unsur periode ke-3 dari yang terendah ke yang terbesar sifat reduktornya adalah...
B. Ar – Cl – S – P – Si – Al – Mg – Na C. Mg – Al – Na – P – Si – S – Ar – Cl D. Na – Mg – Al – Si – Ar – Cl – S – P E. Ar – Cl – S– P – Si – Na – Mg – Al (6) Soal Ujian Nasional Tahun 2004
Nomor atom unsur-unsur P, Q, R dan S berturut-turut adalah 20, 19, 18 dan 12. Unsur-unsur yang terletak pada golongan yang sama adalah....
A. P dan Q B. Q dan R C. R dan S D. P dan S E. Q dan S
(7) Soal Ujian Nasional Tahun 2008 Dua buah unsur memiliki notasi 27
13X dan 35,517Y
Unsur Y dalam sistem periodik terletak pada ... A. golongan IV B, periode 5
B. golongan VIII B, periode 4 C. golongan IV A, periode 3 D. golongan VII A, periode 3 E. golongan VIII A, periode 3
(8) Soal Ujian Nasional Tahun 2009 Unsur 32
16T dalam sistem periodik terletak pada golongan dan periode berturut-turut...
A. IVA, 3 B. VA, 2 C. VIA, 3 D. VIIA, 3 E. IVB, 2
(9) Soal Ujian Nasional Tahun 2010
Diagram orbital 2 buah unsur sebagai berikut:
Letak unsur Y dalam tabel periodik terdapat pada golongan dan periode secara berurutan.... A. VIIA, 3
B. VIIA, 7 C. VA, 3 D. IIIA, 5 E. IIIA, 7
(10) Soal Ujian Nasional Tahun 2011
Letak unsur X dengan nomor atom 26 dan nomor massa 56, dalam sistem periodik pada golongan dan periode....
B. VI B dan 3 C. VI B dan 4 D. VIII B dan 3 E. VIII B dan 4
(11) Soal Ujian Nasional Tahun 2012 Perhatikan tabel sistem periodik berikut!
Konfigurasi elektron unsur Q yang paling sesuai adalah.... A. 1s2 2s2 2p6 3s2 3p6
B. 1s2 2s2 2p6 3s2 3p4
C. 1s2 2s2 2p6 3s2 3p5
D. 1s2 2s2 2p6 3s2 3p6 4s2
E. 1s2 2s2 2p6 3s2 3p4 4s2 3d2
(12) Soal Ujian Nasional Tahun 2012
Dua buah unsur mempunyai diagram orbital sebagai berikut: dan
Nomor atom dari unsur X adalah.... A. 17
B. 18 C. 21 D. 26 E. 30
(13) Soal Ujian Nasional Tahun 2012
Unsur Y dalam sisitem periodik terletak pada golongan dan periode berturut-turut.... A. IIIA, 3 B. IIIB, 4 C. VA, 3 D. VIIA, 3 E. VIIB, 4 (14) Soal UN Kimia 2013
Perhatikan notasi unsur berikut!
Konfigurasi elektron dan letak unsur X tersebut dalam sistem periodik adalah….(Nomor atom Ne = 10)
(15) Soal Ujian Nasional Tahun 2014
Notasi unsur M dilambangkan sebagai berikut:
2248M
Konfigurasi elektron dan letak unsur M pada tabel periodik modern secara berturut-turut adalah….
Bank Soal UN Perubahan Kimia Fisika
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia un tahun 2002 - 2011 tentang perubahan fisika dan perubahan kimia.
Perubahan Fisika dan Kimia
(1) Soal Ebtanas Tahun 1996
1. Lilin di dalam tabung reaksi dipanaskan 2. Gula pasir dilarutkan dalam air
3. pita magnesium dibakar
4. Larutan KI 0,1 M dan Pb(NO3)2 0,1 M dicampur
5. Pita magnesium dimasukkan ke asam klorida dan gas yang dihasilkan dibakar Dari percobaan di atas, yang menunjukkan perubahan kimia adalah...
A. 1 B. 2 C. 3 D. 3 dan 4 E. 3, 4 dan 5
(2) Soal Ebtanas Tahun 1998 Diantara perubahan berikut: 1. besi berkarat
2. lilin menyala 3. iodium menyublim 4. bensin terbakar 5. emas melebur
yang termasuk perubahan kimia adalah... A. 1, 2, 4
B. 1, 3, 5 C. 1, 4, 5 D. 2, 3, 4 E. 2, 3, 5
(3) Soal Ebtanas Tahun 1999
Perhatikan perubahan materi yang terjadi di bawah ini: (1) pembuatan gula dari tebu
(2) penyulingan minyak bumi (3) pembuatan tape dari singkong (4) pembuatan garam dapur dari air laut (5) air susu jadi masam
(6) minyak kelapa menjadi tengik
Perubahan materi yang merupakan perubahan kimia adalah... A. (1), (3), (5)
B. (2), (4), (6) C. (3), (4), (5) D. (3), (5), (6) E. (4), (5), (6)
(4) Soal Ebtanas Tahun 2000
Seorang siswa mencampurkan dua zat kimia. Diantara pernyataan di bawah ini yang tidak menunjukkan telah terjadi reaksi kimia adalah....
A. timbul gas B. terjadi endapan C. perubahan suhu D. perubahan massa E. perubahan warna
(5) Soal Ebtanas Tahun 2001
Di antara peristiwa berikut, yang termasuk perubahan kimia adalah... A. kapur barus menyublim
B. bensin menguap C. besi berkarat D. lilin melebur E. es mencair
(6) Soal Ebtanas Tahun 2002 Diantara perubahan materi berikut : (1) pembuatan tape
(2) penguapan air (3) susu menjadi masam (4) penyepuhan logam
(5) beras digiling menjadi tepung (6) garam dapur larut dalam air
Kelompok yang tergolong perubahan kimia adalah... A. (1), (2) dan (3)
B. (1), (2) dan (4) C. (1), (3) dan (4) D. (2), (3) dan (5) E. (3), (4) dan (6)
(7) Soal Ebtanas Tahun 2003
Diantara perubahan berikut yang termasuk kimia adalah... A. tebu menjadi gula
B. beras menjadi tepung C. minyak wangi menguap D. singkong menjadi tape E. air laut menjadi garam
(8) Soal Ujian Nasional Tahun 2004
Perhatikan perubahan-perubahan materi berikut : 1. singkong jadi tape
2. lilin mencair 3. susu menjadi basi
perubahan yang berlangsung secara kimiawi adalah... A. 1, 2, 3 B. 1, 2 C. 1, 3 D. 2, 3 E. 3
Bank Soal UN Struktur Atom
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia tahun 2002 - 2011, 2012, 2013 dan 2014 tentang struktur Atom dan Konfigurasi elektron.
Struktur Atom dan Konfigurasi Elektron
(1) Soal Ebtanas Tahun 2001
Pasangan unsur - unsur berikut ini yang memiliki elektron valensi sama yaitu... A. 3Li dan 13Al
B. 11Na dan 19K
C. 12Mg dan 30Zn
D. 5B dan 21Sc
(2) Soal Ebtanas Tahun 2002 Unsur klor dengan lambang 35
17Cl mengandung.... A. 17 n, 18 p B. 17 n, 35 p C. 18 n, 17 p D. 18 n, 35 p E. 35 n, 17 p
(3) Soal Ebtanas Tahun 2003 Jika diketahui nuklida 23
11Na, maka jumlah elektron, proton dan neutron adalah....
A. 23 proton, 12 elektron, 11 neutron B. 11 proton, 12 elektron, 23 neutron C. 11 proton, 11 elektron, 12 neutron D. 11 proton, 12 elektron, 11 neutron E. 12 proton, 11 elektron, 11 neutron (4) Soal Ebtanas Tahun 2003
Konfigurasi elektron yang benar untuk 24Cr adalah...
A. 1s2 2s2 3p2 3s2 3p6 4s2 3d4
B. 1s2 2s2 3p2 3s6 3p6 3d4 4s2
C. 1s2 2s2 3p2 3s2 3p6 4s2 4p4
D. 1s2 2s2 3p2 3s2 3p6 4s1 3d5
E. 1s2 2s2 3p2 3s2 3p6 3d2 4f6
(5) Soal Ebtanas Tahun 2003
Bilangan kuantum elektron terakhir dari unsur X dengan nomor atom 11 adalah.... A. n = 4, l = 0, m = -1, s = - 1/2
B. n = 4, l = 1, m = 0, s = + 1/2 C. n = 3, l = 0, m = 0, s = + 1/2 D. n = 3, l = 1, m = 0, s = - 1/2 E. n = 2, l = 0, m = 0, s = + 1/2 (6) Soal UN Kimia Tahun 2004
Konfigurasi elektron dari unsur dengan nomor atom 24 adalah... A. (Ar) 3d4 4s2
B. (Ar) 3d5 4s1
C. (Ar) 3d3 4s2 4p1
D. (Ar) 3d3 4s1 4p2
E. (Ar) 3d4 4p2
(7) Soal UN Kimia Tahun 2008 Dua buah unsur memiliki notasi 27
13X dan 35,517Y
Diagram orbital yang paling tepat untuk elektron terakhir dari unsur X adalah.... (Nomor atom Ar = 18, Kr = 36, Ne = 10)
(8) Soal UN Kimia Tahun 2009
Tiga buah unsur dengan notasi sebagai berikut :
23
11P, 2412Q, 35,517R
Konfigurasi elektron unsur P adalah .... (Nomor atom Ne = 10, Ar = 18) A. [Ne] 3s1
B. [Ne] 4s1
C. [Ar] 3s1
D. [Ar] 4s1
E. [Ar] 4s2 3d3
(9) Soal UN Kimia Tahun 2010
Diagram orbital 2 buah unsur sebagai berikut:
Nomor atom unsur X adalah.... A. 6
B. 16 C. 17 D. 24 E. 25
(10) Soal UN Kimia Tahun 2011
Konfigurasi elektron X2− dari suatu ion unsur 32
16X adalah.... A. 1s22s22p63s23p2 B. 1s22s22p63s23p4 C. 1s22s22p63s23p6 D. 1s22s22p63s23p63d2 E. 1s22s22p63s23p23d2
(11) Soal UN Kimia Tahun 2012
Konfigurasi elektron unsur Q yang paling sesuai adalah.... A. 1s2 2s2 2p6 3s2 3p6 B. 1s2 2s2 2p6 3s2 3p4 C. 1s2 2s2 2p6 3s2 3p5 D. 1s2 2s2 2p6 3s2 3p6 4s2 E. 1s2 2s2 2p6 3s2 3p4 4s2 3d2
(12) Soal UN Kimia Tahun 2013
Harga keempat bilangan kuantum elektron terakhir dari atom 32
16S adalah.... A. n = 2; l = 0; m = 0; s = − 1/ 2 B. n = 3; l = 1; m = −1; s = − 1/ 2 C. n = 3; l = 1; m = 0; s = − 1/ 2 D. n = 3; l = 1; m = 0 s = + 1/ 2 E. n = 3; l = 1; m = +1; s = + 1/ 2 (13) Soal UN Kimia 2013
Harga keempat bilangan kuantum untuk elektron terakhir dari 17Cl adalah…
A. n= 3, l = 1, m = +1, dan s = -1/2 B. n = 3, l = 1, m = 0, dan s = +1/2 C. n = 3, l = 1, m = 0, dan s = -1/2 D. n = 3, l = 2, m = 0, dan s = +1/2 E. n = 2, l = 1, m = 0, dan s = -1/2 (14) Soal UN Kimia 2014
Notasi unsur M dilambangkan sebagai berikut:
2248M
adalah….
Bank Soal UN Ikatan Kimia
Category: Bank Soal UN Kimia SMA2012 dan 2013, 2014 tentang ikatan kimia.
Ikatan Kimia
(1) Soal Ebtanas Tahun 2001
Senyawa dengan rumus molekul N2O, NO, NO2 berturut-turut mempunyai nama....
A. Nitrogen (IV) oksida, Nitrogen (II) oksida, Nitrogen (I) oksida B. Nitrogen (II) oksida, Nitrogen (I) oksida, Nitrogen (IV) oksida C. Nitrogen (II) oksida, Nitrogen (IV) oksida, Nitrogen (I) oksida D. Nitrogen (I) oksida, Nitrogen (II) oksida, Nitrogen (IV) oksida E. Nitrogen (I) oksida, Nitrogen (IV) oksida, Nitrogen (II) oksida (2) Soal Ebtanas Tahun 2001
Rumus struktur Lewis asam nitrat adalah seperti disamping ini.
Ikatan kovalen koordinasi ditunjukkan oleh anak panah nomor.... A. 1
B. 2 C. 3 D. 4 E. 5
(3) Soal Ebtanas Tahun 2001
Diberikan pasangan kelompok senyawa berikut : 1. H2O dengan HCl
2. NH3 dengan HBr
3. NH3 dengan H2S
4. HF dengan H2O
5. NH3 dengan HF
Kelompok senyawa yang mempunyai ikatan hidrogen adalah... A. 1 dan 2
B. 2 dan 3 C. 3 dan 4 D. 4 dan 5
E. 5 dan 1
(4) Soal Ebtanas Tahun 2002
Nomor atom unsur A, B, C, D dan E berturut-turut 6, 8, 9, 16, 19. Pasangan unsur yang dapat membentuk ikatan ion adalah pasangan antara unsur....
A. A dan C B. C dan E C. B dan B D. D dan C E. E dan B
(5) Soal Ebtanas Tahun 2003
Pasangan senyawa berikut yang mempunyai ikatan hidrogen adalah... A. HCl dengan NaOH
B. H2O dengan H2S C. KOH dengan H3PO4 D. HF dengan NH3
E. CH3COOH dengan H2SO4 (6) Soal Ebtanas Tahun 2003
Diantara senyawa berikut ini yang merupakan senyawa berikatan kovalen adalah.... A. NaCl, KI, Mg(OH)2
B. ZnSO4, HgO, CH3COOH C. Cl2, CaO, O3
D. H2O, HCl, LiOH E. H3PO4, CH3OH, CO2 (7) Soal Ebtanas Tahun 2004
Empat unsur A, B, C, D masing-masing mempunyai nomor atom 16, 17, 18, 19. Pasangan yang dapat membentuk ikatan ion adalah...
A. A dan B B. A dan C C. B dan D D. B dan C E. C dan D
(8) Soal UN Kimia Tahun 2008 Dua buah unsur memiliki notasi 27
13X dan 35,517Y
Bila kedua unsur tersebut berikatan, maka rumus senyawa yang dihasilkan adalah.... A. XY2
B. XY3 C. X2Y D. X3Y E. X2Y3
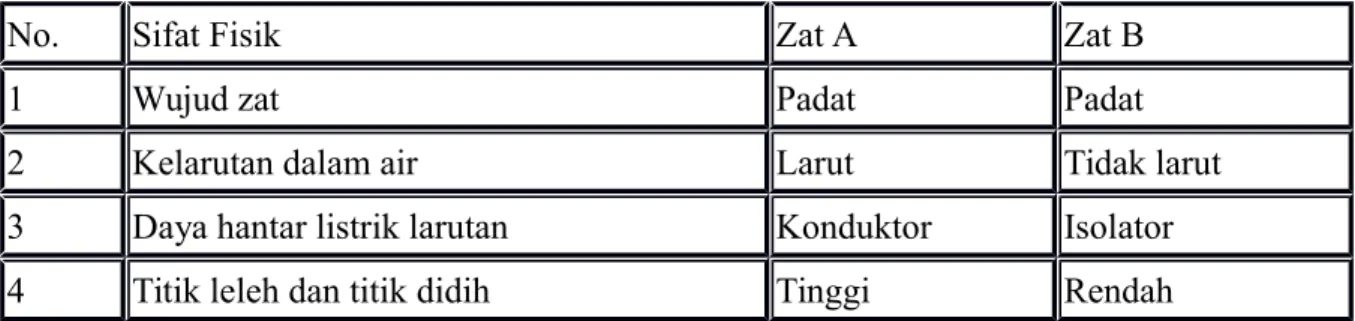
(9) Soal UN Kimia Tahun 2008
No. Sifat Fisik Zat A Zat B
1 Wujud zat Padat Padat
2 Kelarutan dalam air Larut Tidak larut
3 Daya hantar listrik larutan Konduktor Isolator
4 Titik leleh dan titik didih Tinggi Rendah
Berdasarkan data tersebut, maka dapat disimpulkan bahwa jenis ikatan yang terdapat pada zat A dan zat B berturut-turut adalah ...
A. ionik dan kovalen non polar B. kovalen polar dan ionik C. kovalen non polar dan ionik D. kovalen koordinasi dan logam E. hidrogen dan kovalen
(10) Soal UN Kimia Tahun 2009
Unsur R dan unsur 19K dapat membentuk senyawa dengan rumus dan jenis ikatan
berturut-turut... A. R2K, ion B. K2R, ion C. KR2, kovalen D. RK2, kovalen E. KR, ion
(11) Soal UN Kimia Tahun 2009
Perhatikan data beberapa senyawa berikut :
Simbol Senyawa Titik leleh (°C) Daya Hantar Listrik Larutannya
Y 870 Menghantarkan
X −25 Tidak Menghantarkan
Berdasarkan data maka jenis ikatan yang terdapat pada senyawa Y dan Z adalah... A. ionik dan kovalen polar
B. ionik dan kovalen non polar C. kovalen polar dan ionik D. kovalen non polar dan ionik
E. kovalen non polar dan kovalen polar (12) Soal UN Kimia Tahun 2010
Dari data tersebut, ikatan yang terdapat dalam senyawa Q dan R berturut-turut adalah.... A. kovalen polar dan ion
B. kovalen non polar dan ion
C. kovalen non polar dan kovalen polar D. kovalen koordinasi dan ion
E. kovalen non polar dan hidrogen (13) Soal UN Kimia Tahun 2011
Senyawa M mempunyai sifat sebagai berikut: 1. mudah larut dalam air;
2. dapat menghantar listrik dalam fase cair; dan 3. titik didihnya dan titik lelehnya tinggi.
Jenis ikatan dalam senyawa M tersebut adalah.... A. kovalen polar
B. kovalen non polar C. hidrogen
D. logam E. Ion
(14) Soal UN Kimia Tahun 2012
Berikut ini data sifat fisik dari dua zat yang tak dikenal.
Senyawa Titik leleh (°C) Daya Hantar Listrik Larutan
Y 32 Tidak Menghantarkan
Z 804 Menghantarkan
Berdasarkan data tersebut, jenis ikatan yang terdapat dalam senyawa Y dan Z berturut-turut adalah....
A. ion dan kovalen polar B. ion dan ion
C. kovalen nonpolar dan ion D. ion dan kovalen nonpolar
E. kovalen polar dan kovalen nonpolar
Perhatikan data sifat fisik dari 2 buah zat yang berikut.
No Sifat fisik Zat A Zat B
1. Daya hantar listrik lelehan Menghantar Listrik Tidak menghantar listrik 2. Daya hantar listrik larutan Menghantar listrik Tidak menghantar listrik
3. Titik didih dan titik leleh Tinggi Rendah
Berdasarkan data tersebut, jenis ikatan yang terdapat pada zat A dan zat B berturut-turut adalah....
A. ion dan kovalen non polar
B. kovalen polar dan kovalen non polar C. kovalen polar dan koordinasi
D. kovalen polar dan ion E. hidrogen dan ion
(16) Soal UN Kimia Tahun 2013
Unsur X dan Y berturut-turut memiliki konfigurasi elektron 1s2 2s2 2p6 3s2 3p3 dan 1s2 2s2 2p6
3s2 3p5. Bentuk molekul yang terjadi jika kedua unsur tersebut berikatan sesuai aturan oktet
adalah…. A. segitiga datar B. tetrahedral C. segitiga piramida D. bentuk V E. oktahedral (17) Soal UN Kimia 2013
Perhatikan data sifat fisik dari 2 zat berikut!
Jenis ikatan yang terdapat pada zat X dan zat Y berturut-turut adalah…. A. ionik dan kovalen non polar
B. kovalen non polar dan ionik
C. kovalen polar dan kovalen non polar D. kovalen polar dan ionik
E. hidrogen dan ionik
Perhatikan gambar struktur Lewis senyawa HNO3 berikut!
Pasangan elektron yang terbentuk secara kovalen koordinasi ditunjukkan pada nomor…. A. 1 B. 2 C. 3 D. 4 E. 5 (20) Soal UN Kimia 2013
Perhatikan grafik titik didih beberapa senyawa hidrida golongan IV A, V A, dan VIA!
Senyawa yang mengandung ikatan hidrogen antar molekulnya adalah nomor…. A. (1) dan (2) B. (1) dan (3) C. (2) dan (3) D. (3) dan (4) E. (5) dan (6) (21) Soal UN Kimia 2014
Jika 4X dan 17Y berikatan, bentuk molekul dan sifat kepolaran yang terbentuk adalah…
A. segiempat planar dan polar B. linear dan polar
C. tetrahedral dan non polar D. oktahedral dan non polar E. linear dan non polar
(22) Soal UN Kimia 2014
Perhatikan senyawa kovalen berikut! (1) CH4
(2) PCl5
(3) NH3
(4) CHCl3
(5) H2O
Jika diketahui nomor atom H = 1, C = 6, N = 7, O = 8, P = 15, Cl = 17, senyawa yang tidak mengikuti aturan oktet adalah….
A. (1) B. (2) C. (3) D. (4) E. (5) (23) Soal UN Kimia 2014
Perhatikan ilustrasi tentang gaya intra dan antarmolekul berikut!
Ikatan hidrogen ditunjukkan oleh nomor…. A. (1)
B. (2) C. (3) D. (4) E. (5)
Bank Soal UN Laju Reaksi Kimia
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia un tahun 2002 - 2011, 2012, 2013, 2014 tentang laju reaksi kimia.
Laju Reaksi
(1) Soal Ebtanas Tahun 2001
Data percobaan laju reaksi diperoleh dari reaksi: A + B → C
sebagai berikut:
Nomor Percobaan 0,20 [B] molar Laju reaksi molar/detik
1 0,01 0,20 0,02
2 0,02 0,20 0,08
3 0,03 0,20 0,18
4 0,03 0,40 0,36
Rumus laju reaksinya adalah.... A. V = k [A]2 [B]
B. V = k [A] [B]2
C. V = k [A] [B] D. V = k [A]2 [B]2
E. V = k [A]3 [B]
(2) Soal Ebtanas Tahun 2002 Dari reaksi:
2 NO(g) + 2H2(g) → N2(g) + 2H2O(g)
diperoleh data percobaan sebagai berikut:
Nomor Percobaan Konsentrasi (M) Laju reaksi (M.det-1)
NO H2
1 2 × 10−3 2 × 10−3 4 × 10−6
2 4 × 10−3 2 × 10−3 8 × 10−6
4 4 × 10−3 6 × 10−3 24 × 10−6
5 4 × 10−3 8 × 10−3 32 × 10−6
Persamaan laju reaksi tersebut adalah... A. V = k [NO] [H2] B. V = k [NO]2 [H 2] C. V = k [NO] [H2]2 D. V = k [NO]2 [H 2]2 E. V = k [H2]2
(3) Soal Ebtanas Tahun 2003 Data eksperimen untuk reaksi : N2 (g) + 3 H2 (g) → 2 NH3 (g)
Terdapat tabel berikut ini
No. [N2] [H2] Laju reaksi
1 0,002 0,002 4 × 10−4
2 0,004 0,002 8 × 10−4
3 0,004 0,008 32 × 10−4
Persamaan laju reaksinya adalah.... A. V = k[N2][H2]
B. V = k[N2][H2]2
C. V = k[N2]2[H2]2
D. V = k[N2]
E. V = k[H2]
(4) Soal Ujian Nasional Tahun 2004
Berikut adalah data hasil percobaan pada suhu tertentu untuk reaksi: A2 (g) + 2C (g) → 2 AC
(g)
Percobaan [A2](g) awal [C](g) awal Laju awal reaksi
1 0,1 M 0,1 M 2 M/detik
2 0,1 M 0,2 M 8 M/detik
3 0,1 M 0,2 M 16 M/detik
Persamaan laju reaksi untuk reaksi tersebut adalah.... A. v = k [A2] [ C]2
C. v = k [A2]2 [ C]
D. v = k [A2] [ C]
E. v = k [A2] [ C]2
(5) Soal Ujian Nasional Tahun 2008
Pada percobaan logam magnesium yang direaksikan dengan larutan asam klorida : Mg(s)+2 HCl(aq) → MgCl2(aq)+H2(g)
diperoleh data sebagai berikut :
Suhu (°C) Volume H2 Waktu (detik)
1 0,1 M 0,1 M
2 0,1 M 0,2 M
3 0,1 M 0,2 M
Laju reaksi pada pembentukan gas H2 adalah ... mL/detik.
A. 25/10 B. 50/25 C. 75/10 D. 50/5 E. 25/5
(6) Soal Ujian Nasional Tahun 2009 Data hasil eksperimen dari reaksi : A (aq)+2B (aq) → C (aq)
A (M) B (M) Laju Reaksi
0,1 0,01 x
0,1 0,03 3x
0,3 0,01 9x
Laju reaksi yang terjadi jika konsentrasi A = 0,2 M dan B = 0,3 M adalah.... A. k (0,2) (0,3)
B. k (0,2) (0,3)2
C. k (0,2)2 (0,3)
D. k (0,2)2
E. k (0,3)
(7) Soal Ujian Nasional Tahun 2010
persamaan reaksi:
2NO(aq) + Br2(g) → 2NOBr(g)
Berdasarkan reaksi tersebut diperoleh data berikut:
Percobaan Konsentrasi Awal (M) Laju reaksi Awal (Ms-1)
NO Br2
1 0,1 0,05 6
2 0,1 0,10 12
3 0,2 0,10 24
Laju reaksi bila konsentrasi gas NO = 0,01 M dan gas Br2 = 0,03 M adalah....
A. 0,012 B. 0,36 C. 1,200 D. 3,600 E. 12,00
(8) Soal Ujian Nasional Tahun 2011
Berikut ini diberikan data percobaan laju reaksi : Q(g) + 2T(g) → T2Q(g)
pada beberapa kondisi:
No. [Q] [T] V(M/det)
1 0,1 0,1 1,25 . 10−2
2 0,2 0,1 5 . 10−2
3 0,1 0,2 10−1
Jika [Q] dan [T] masing-masing diubah menjadi 0,5 M, maka harga laju (V) reaksi saat itu adalah....M/det A. 5,0 B. 7,5 C. 10,5 D. 12,5 E. 39,0
(9) Soal Ujian Nasional Tahun 2012 Data hasil percobaan laju reaksi:
Berdasarkan data tersebut orde reaksi total adalah... A. 1 B. 2 C. 3 D. 4 E. 5
(10) Soal UN Kimia Tahun 2013
Perhatikan tabel hasil reaksi logam seng dengan asam sulfat berikut: Zn (s) + H2 SO4 (aq)→ ZnSO4 (aq) + H2 (g)
Laju reaksi pada pembentukan gas H2 adalah….
A. 0,5 mL/detik B. 1,5 mL/detik C. 3,0 mL/detik D. 4,5 mL/detik E. 6,0 mL/detik
(11) Soal UN Kimia Tahun 2013
Perhatikan bagan reaksi 4 gram pualam CaCO3 dengan larutan HCl pada masing-masing
Laju reaksi yang hanya dipengaruhi oleh suhu terdapat pada gambar nomor….. A. (1) terhadap (2) B. (1) terhadap (3) C. (2) terhadap (4) D. (3) terhadap (4) E. (4) terhadap (5)
(12) Soal UN Kimia Tahun 2014
Perhatikan data pada tabel percobaan dari reaksi berikut! Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
No. Suhu(°) Volume H2 (mL) Waktu (detik)
(1) 25 5 10
(2) 25 10 20
(3) 25 15 30
Laju reaksi pembentukan gas H2 adalah...
A. 0,02 mL.det-1
B. 0,05 mL.det-1
C. 0,10 mL.det-1
D. 0,15 mL.det-1
E. 0,50 mL.det-1
Bank Soal UN Stoikiometri
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia un tahun 2002 - 2011, 2012, 2013 dan 2014 tentang stoikiometri dasar.
STOIKIOMETRI
(1) Soal Ebtanas Tahun 2001
Jika diketahui massa atom relatif Ar : N = 14; H = 1 dan tetapan Avogadro = 6 × 1023, dalam
8 gram N2H4 terdapat atom nitrogen sebanyak...
A. 3 × 1023 atom
C. 9× 1023 atom
D. 12× 1023 atom
E. 15× 1023 atom
(2) Soal Ebtanas Tahun 2002
Di antara reaksi berikut ini, yang tidak mengikuti hukum kekekalan massa adalah.... (Ar : S = 32; Cu = 63,5; O = 16; C = 12; Fe = 56; H = 1)
A. 5 g belerang + 10 g tembaga → 15 g tembaga (II) sulfida B. 2 g belerang + 3,5 g besi → 5,5 g besi (II) sulfida
C. 5 g belerang + 10 g oksigen → 10 g belerang dioksida D. 3 g karbon + 8 g oksigen → 11 g karbondioksida E. 1 g oksigen + 8 g hidrogen → 9 g air
(3) Soal Ebtanas Tahun 2002
Massa molekul relatif : Na = 23; O = 16; S = 32. Massa molekul relatif dari senyawa Na2SO4
adalah... A. 23 + 2 + 32 + 16 + 4 → 77 B. 2(23) + (32) + 4(16) → 142 C. 23 + 2(32) + 16 + 4 → 107 D. 4(23) + 1(32) + 2(16) → 156 E. 23 + 32 + 16 → 71
(4) Soal Ebtanas Tahun 2003
Massa CaCO3 yang terjadi dari 0,1 mol CaCO3 adalah...
(Ar Ca = 40, O = 16, C = 12) A. 8 gram B. 10 gram C. 12 gram D. 14 gram E. 16 gram
(5) Soal Ujian Nasional 2004
Dalam 100 kg air laut terdapat 0,001 gram raksa. Kandungan air raksa dalam air laut tersebut adalah... A. 0,001 bpj
B. 0,01 bpj C. 0,10 bpj D. 1,00 bpj E. 10,00 bpj
(6) Soal Ujian Nasional 2004 Diketahui reaksi :
a C3H8 + b O2 → c CO2 + d H2O
Jika reaksi tersebut disetarakan maka harga a, b, c dan d berturut-turut adalah...
A. 2, 5, 6, 2 B. 1, 3, 3, 4
C. 2, 10, 4, 4 D. 1, 4, 3, 2 E. 1, 5, 3, 4
(7) Soal UN Kimia 2008
Sebanyak 10 gram padatan kalium klorat dipanaskan dalam wadah tertutup, sehingga terjadi reaksi sesuai persamaan :
2 KClO3(s) → 2 KCl(s)+3 O2(g)
Massa zat yang dihasilkan adalah.... A. lebih besar dari 25 gram
B. lebih besar dari 10 gram C. sama dengan 10 gram D. lebih kecil dari 25 gram E. lebih kecil dari 10 gram (8) Soal UN Kimia 2009
Pembakaran sempurna gas asetilen dapat ditulis seperti berikut : C2H2 (g)+O2 (g) → CO2 (q)+H2O (g)(belum setara)
Jika reaksi dilakukan pada tekanan yang sama maka perbandingan volume C2H2 : O2
adalah.... A. 1 : 2 B. 1 : 4 C. 1 : 5 D. 2 : 2 E. 2 : 5
(9) Soal UN Kimia 2009 dan UN 2010
Dalam kehidupan sehari-hari, karbit sering digunakan untuk pengelasan logam karena gas yang dihasilkan dari reaksi karbit dengan air mempunyai sifat mudah terbakar, nyala terang dan berkalor tinggi. Reaksi selengkapnya sebagai berikut:
CaC2 (s)+2H2O (l) → Ca(OH)2 (aq) + C2H2 (g)
Nama IUPAC senyawa karbit pada reaksi tersebut adalah... A. kalsium hidroksida B. kalsium dikarbida C. kalsium dikarbonat D. kalsium karbida E. kalsium oksida (10) Soal UN Kimia 2011
Tahap awal pembuatan asam nitrat dalam industri melibatkan reaksi oksidasi amonia yang menghasilkan nitrogen monoksida dan uap air menurut reaksi berikut ini:
Volume nitrogen monoksida yang dihasilkan pada reaksi 6 liter gas amonia (P.T) adalah.... A. 4 liter B. 6 liter C. 10 liter D. 12 liter E. 14 liter (11) Soal UN Kimia 2012
Perhatikan grafik titrasi asam-basa berikut!
Jika volume larutan yang dititrasi sebanyak 10 mL maka konsentrasi larutan basa LOH itu adalah... A. 0,25 M B. 0,125 M C. 0,1 M D. 0,075 M E. 0,025 M (12) Soal UN Kimia 2012
Perhatikan persamaan reaksi berikut! Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2 (g)
Apabila 4 gram logam Mg dimasukkan ke dalam 10 mL larutan HCl 2 M, maka volume gas H2 yang terbentuk dalam keadaan standar adalah....
(Ar Mg = 24; H = 1; Cl = 35,5) A. 0,224 L B. 0,448 L C. 1,904 L D. 2,240 L E. 3,808 L
(13) Soal UN Kimia Tahun 2013
Sebanyak 12,8 gram sulfur dioksida dibakar dengan 3,2 gram gas oksigen dalam ruang tertutup menghasilkan gas sulfur trioksida menurut reaksi:
Gas sulfur trioksida yang terbentuk sebanyak…..(Ar S = 32; O = 16) A. 8 gram
B. 9 gram C. 10 gram
D. 11 gram E. 16 gram
(14) Soal UN Kimia Tahun 2014
Direaksikan gas nitrogen dan gas oksigen dengan perbandingan massa sebagai berikut:
Berdasarkan tabel tersebut perbandingan massa N : O dalam oksida nitrogen yang dihasilkan adalah…. A. 3 : 6 B. 4 : 8 C. 7 : 9 D. 7 : 12 E. 12 : 7
(15) Soal UN Kimia Tahun 2014
Logam besi dalam industri diperoleh melalui reaksi: Fe2O3(s) + C(s) → Fe(s) + CO2(g) (belum setara).
(Ar Fe = 56; O = 16) Volume gas CO2 (STP) yang dihasilkan jika massa besi (III) oksida
yang bereaksi sebanyak 32 gram adalah….. A. 1,12 L
B. 6,72 L C. 11,20 L D. 22,40 L E. 36,60 L
(16) Soal UN Kimia Tahun 2014
Karbit (kalsium karbida) adalah zat padat berwarna putih yang pada umumnya digunakan untuk mengelas. Karbit dihasilkan dari pemanasan kalsium oksida dan karbon dalam tanur listrik dengan hasil samping gas karbon dioksida. Persamaan reaksi setara yang
menggambarkan reaksi pembuatan karbit adalah…. A. Ca(s) + C(s) → CaC2(s)
B. CaO(s) + 2C(s) → CaC2(s)
C. 2CaO(s) + 5C(s) → 2CaC2(s) + CO2(g)
D. CaC2(s) + H2O(l) → CaH2(g) + CO2(g)
Bank Soal UN Senyawa Benzena dan Turunannya
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional un kimia tahun 2002 - 2011, 2012, 2013, 2014 tentang senyawa benzena dan turunannya.
Benzena dan Turunannya
(1) Soal Ebtanas Tahun 2001
A. aspirin B. zat warna C. pengawet D. anti septik
E. bahan-bahan nilon 66 (2) Soal Ebtanas Tahun 2002
Nama dari senyawa turunan benzena dengan rumus struktur berikut ini adalah....
A. 3,5 - dikloro fenol B. 1,3 - dikloro fenol C. 3,5 - dikloro toluena D. 1,3 dikloro benzena E. 3,5 - dikloro benzoat
(3) Soal Ujian Nasional Tahun 2004
Nama molekul turunan benzena di bawah ini adalah....
A. Ortho hidroksi toluen B. Ortho toluen fenol C. Ortho hidro toluen
D. Ortho hidro metil benzena E. Ortho metil hidrokso benzena (4) Soal UN Kimia 2008
Berikut adalah persamaan reaksi pembuatan turunan benzena
Jenis reaksi tersebut adalah... A. sulfonasi
B. adisi C. alkilasi D. halogenasi
E. oksidasi
(5) Soal UN Kimia 2008
Nama senyawa turunan benzena dengan rumus struktur adalah....
A. toluena B. nitrobenzena C. klorobenzena D. anilin E. asam benzoat (6) Soal UN Kimia 2009
Berikut ini adalah kegunaan senyawa turunan benzena : 1. pengawet makanan;
2. bahan peledak; 3. zat disinfektan;
4. pembuatan zat warna; dan 5. bahan bakar roket.
Kegunaan yang tepat untuk senyawa turunan benzena dengan rumus
adalah.... A. 1 B. 2 C. 3 D. 4 E. 5 (7) Soal UN Kimia 2010
Beberapa kegunaan turunan benzena antara lain: 1. pengawet makanan;
2. desinfektan; 3. antioksidan; 4. obat-obatan; dan 5. minyak wangi.
adalah... A. 1 B. 2 C. 3 D. 4 E. 5 (8) Soal UN Kimia 2010
Nama yang tepat untuk senyawa turunan benzena dengan rumus struktur
adalah...
A. 1,4 − dimetil benzena B. 1,3 − dimetil benzena C. meta − dimetil benzena D. meta - xilena
E. 3 − metil toluena (9) Soal UN Kimia 2012
Perhatikan persamaan reaksi benzena berikut!
Nama senyawa X yang dihasilkan dan jenis reaksi yang terjadi adalah... A. anilina, alkilasi B. toluena, alkilasi C. anilina, halogenasi D. klorobenzena, halogenasi E. klorobenzena, alkilasi (10) Soal UN Kimia 2013
Beberapa senyawa turunan benzena berikut: (1) fenol;
(2) trinitrotoluena; (3) stirena;dan (4) asam benzoat.
Senyawa yang digunakan sebagai bahan baku pembuatan bahan peledak dan sebagai pengawet makanan atau minuman berturut-turut adalah nomor….
A. (1) dan (2) B. (1) dan (3) C. (2) dan (3) D. (2) dan (4) E. (3) dan (4) (11) Soal UN Kimia 2014
Berikut beberapa kegunaan senyawa benzena: (1) bahan pembuat anilina;
(2) pengawet kayu;
(3) bahan pembuatan semir sepatu; (4) pengawet makanan; dan
(5) bahan baku pembuatan peledak. Kegunaan dari nitrobenzena adalah… A. (1) dan (2)
B. (1) dan (3) C. (3) dan (4) D. (3) dan (5) E. (4) dan (5)
Bank Soal UN Koloid
Category: Bank Soal UN Kimia SMA
Kimia Study Center - Kumpulan contoh soal UN ujian nasional kimia tahun 2001 - 2002 - 2011 dan 2012, 2013, 2014 tentang sistem koloid.
Koloid
Contoh koloid yang medium pendispersinya padat dan fase terdispersinya cair adalah... A. asap B. awan C. agar-agar D. mutiara E. batu apung
(2) Soal Ebtanas Tahun 2001 Peristiwa berikut:
1. Pembentukan delta pada muara sungai 2. Pemurnian gula pasir (kotor)
3. Penyembuhan sakit perut oleh norit 4. Penjernihan air
Yang merupakan contoh peristiwa koagulasi koloid, kecuali.... A. 1 dan 2
B. 1 dan 3 C. 1 dan 4 D. 2 dan 3 E. 2 dan 4
(3) Soal Ebtanas Tahun 2001
Pembuatan sol Fe(OH)3 dapat dilakukan dengan cara....
A. mekanik B. peptisasi C. reaksi redoks D. hidrolisis
E. dekomposisi rangkap (4) Soal Ebtanas Tahun 2002
Proses pembuatan koloid berikut ini yang tergolong cara kondensasi adalah... A. menambahkan larutan AlCl3 ke dalam endapan Al(OH)3
B. menambahkan larutan jenuh jenuh FeCl3 ke dalam air panas
C. mengalirkan arus listrik tegangan tinggi ke larutan AuCl3
D. memasukkan serbuk belerang yang sudah digerus ke dalam air E. menambahkan alkohol 95 % ke dalam larutan jenuh kalsium asetat (5) Soal Ebtanas Tahun 2003
Pembuatan koloid berikut ini yang termasuk pembuatan koloid dengan cara kondensasi adalah...
A. menggiling serbuk belerang lalu mencampur dengan air
B. sol emas dibuat dengan melompatkan bunga api listrik ke dalam elektroda Au dalam air C. mereaksikan CuSO4 dengan Na2S dalam air
D. mengalirkan gas SO2 ke dalam larutan H2S
E. pembuatan sol dengan memanaskan suspensi amilum (6) Soal Ujian Nasional 2004
Koloid yang dibuat dengan cara kondensasi (hidrolisa) yaitu …
B. peptisasi As2S3 dalam air dengan menambahkan gas H2S
C. membuat sol logam dengan cara busur Bredig
D. pembuatan sol Fe(OH)3 dengan cara mereaksikan FeCl3 dengan air panas
E. membuat sol belerang dengan cara menggerus butir-butir belerang yang dicampur butir gula lalu dilarutkan dalam air
(7) Soal UN Kimia 2008
Berikut ini beberapa fenomena sehari-hari yang menunjukkan sifat koloid dalam kehidupan : 1. proses cuci darah
2. kabut di pegunungan
3. pembentukan delta di muara sungai 4. pemutihan gula
5. proses kerja obat diare
Sifat koagulasi koloid dapat ditunjukkan dalam contoh kejadian nomor.... A. 1 B. 2 C. 3 D. 4 E. 5 (8) Soal UN Kimia 2009
Berikut ini adalah beberapa sifat koloid: 1. efek Tyndall;
2. gerak Brown; 3. koagulasi;
4. elektroforensi; dan 5. dialisis.
Aspek sifat koloid pada proses pengolahan air untuk memperoleh air bersih adalah... A. 1 B. 2 C. 3 D. 4 E. 5 (9) Soal UN Kimia 2010
Berikut ini beberapa sifat koloid: 1. dialisis;
2. koagulasi; 3. adsorbsi;
4. efek Tyndall; dan 5. koloid pelindung.
Proses menghilangkan bau badan dengan deodorant dan memanaskan putih telur merupakan penerapan sifat koloid, berturut-turut....
A. 1 dan 3 B. 2 dan 4 C. 3 dan 2 D. 3 dan 4
E. 4 dan 5
(10) Soal UN Kimia 2011
Perhatikan contoh penerapan sifat koloid berikut! (1) Sorot lampu mobil pada saat kabut
(2) Pembentukan delta di muara sungai (3) Proses cuci darah
(4) Gelatin dalam es krim (5) Pemutihan gula tebu
Contoh yang merupakan penerapan sifat adsorbsi adalah... A. (1) B. (2) C. (3) D. (4) E. (5) (11) Soal UN Kimia 2011
Perhatikan beberapa proses pembuatan koloid berikut: (1) H2S ditambahkan ke dalam endapan NiS;
(2) sol logam dibuat dengan cara busur Bredig; (3) larutan AgNO3 diteteskan ke dalam larutan HCl;
(4) larutan FeCl3 diteteskan ke dalam air mendidih; dan
(5) agar-agar dipeptisasi dalam air
Contoh pembuatan koloid dengan cara kondensasi adalah... A. (1) dan (2) B. (1) dan (3) C. (3) dan (4) D. (3) dan (5) E. (4) dan (5) (12) Soal UN Kimia 2012
Sifat koloid dan penerapannya yang tepat adalah....
. Sifat-Sifat Koloid Penerapan dalam
Kehidupan Sehari-hari
A. Adsorbsi Penggunaan norit
B. Koagulasi Menghilangkan bau badan C. Dialisis Gelatin pada es krim D. Efek Tyndall Penyaringan asap pabrik E. Gerak Brown Sorot lampu di malam hari
Perhatikan penerapan sifat koloid berikut! (1) Penyaringan asap pabrik dengan alat Cottrel. (2) Pemutihan gula dengan karbon aktif.
(3) Penjernihan air dengan tawas. (4) Sorot lampu di malam hari berkabut. (5) Cuci darah pada penderita ginjal. Sifat adsorpsi ditunjukkan pada nomor…. A. (1) dan (2)
B. (2) dan (3) C. (2) dan (4) D. (3) dan (5) E. (4) dan (5)
(14) Soal Ebtanas Tahun 2014
Beberapa contoh penerapan sifat koloid dalam kehidupan sehari-hari: (1) Sinar matahari kelihatan saat masuk ruangan melalui celah
(2) Pembentukan delta di muara sungai (3) Penjernihan air
(4) Menggunakan alat cottrel dalam industri (5) Proses cuci darah
Penerapan sifat koloid dari elektroforesis dan dialisis secara berturut-turut adalah…. A. (1) dan (2)
B. (2) dan (3) C. (3) dan (4) D. (4) dan (5) E. (5) dan (1)
Bank Soal UN Kesetimbangan Kimia
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional UN kimia tahun 2002 - 2011, 2012, 2013, 2014 tentang kesetimbangan pada reaksi kimia dan pergeserannya.
Kesetimbangan Kimia dan Pergeseran
(1) Soal Ebtanas Tahun 2001 Diketahui reaksi :
A (g) + 2 B (g) → AB2 (g)
Kesetimbangan bergeser ke kanan jika... A. suhu dinaikkan
B. suhu diturunkan C. tekanan diperbesar D. tekanan diperkecil E. konsentrasi B dikurangi (2) Soal Ebtanas Tahun 2001
Dalam ruang 5 liter direaksikan 0,5 mol N2 dengan 0,4 mol gas O2 menurut reaksi :
N2 (g) + O2 (g) ↔ 2 NO (g)
Setelah tercapai keadaan setimbang terbentuk 0,2 mol gas NO. Harga Kc adalah... A. 1/2
B. 1/3 C. 1/4 D. 1/5 E. 2/5
(3) Soal Ebtanas Tahun 2002
Dalam bejana 3 liter, 5 mol amoniak terurai dengan derajat disosiasi 0,4 menurut reaksi : 2NH3 (g) ↔ N2(g) + 3H2 (g)
Tekanan pada kesetimbangan adalah 3,5 atm. Harga Kp adalah.... A. 1/3
B. 1/2 C. 3/4 D. 1 E. 1,5
(4) Soal Ebtanas Tahun 2003 Perhatikan reaksi :
2 CO (g) + O2 (g) ↔ 2 CO2 (g) Δ H = + X kJ
Reaksi akan bergeser ke kanan jika... A. tekanan diperkecil
B. tekanan diperbesar C. diberi katalis D. suhu dinaikkan E. suhu diturunkan
(5) Soal Ebtanas Tahun 2004
persamaan
2NH3 (g) ↔ N2 (g) + 3H2 (g)
Jika harga Kc reaksi tersebut = 1/3 maka konsentrasi N2 dalam kesetimbangan adalah....
A. 1 M B. 3 M C. 1/3 M D. 2/3 M E. 1/2 M
(6) Soal Ujian Nasional Tahun 2004 Pada reaksi kesetimbangan :
A + B ↔ C + O
Kesetimbangan akan lebih cepat tercapai apabila.... A. zat A ditambah B. tekanan diperbesar C. volume diperbesar D. digunakan katalis E. suhu dinaikkan (7) Soal UN Tahun 2008
Data percobaan reaksi kesetimbangan 2 SO2(g)+O2(g)⇔2 SO3(g) sebagai berikut :
. Volume Konsentrasi pada Kesetimbangan
SO2 1 L 0,4
O2 1 L 0,7
SO3 1 L 0,6
(8) Soal UN Tahun 2009
Dalam suatu ruang 1 liter pada suhu T°C terdapat dalam keadaan setimbang 2 mol NH3, 1
mol O2, 1 mol N2 dan 2 mol H2O menurut persamaan reaksi
4 NH3 (g)+3 O2 (g)⇔2 N2 (g)+6 H2O (g)
Harga tetapan kesetimbangan reaksi (Kc) pada suhu tersebut adalah.... A. 1 B. 2 C. 3 D. 4 E. 8 (9) Soal UN Tahun 2010 Pada reaksi kesetimbangan : 2NH3(g) ⇔ N2(g) + 3 H2 (g)
pada suhu 27°C mempunyai Kp = 2,46 atm. Maka harga Kc reaksi tersebut adalah....(R = 0,082 L.atm.mol−1)
(10) Soal UN Tahun 2011
Pada reaksi kesetimbangan berikut:
6 NO (g) + 4NH3 (g) ⇔ 5 N2 (g) + 6 H2O (g) ΔH = −x kJ
Jika suhu diturunkan pada volume tetap, maka kesetimbangan akan bergeser ke... A. kanan, konsentrasi N2 berkurang
B. kanan, konsentrasi N2 bertambah
C. kanan, konsentrasi N2 tetap
D. kiri, konsentrasi NO bertambah E. kiri, konsentrasi NO berkurang (11) Soal UN Tahun 2012
Perhatikan data reaksi kesetimbangan di bawah ini! (1) N2 (g) + 3H2 (g) ↔ 2NH3 (g) ΔH = −92 kJ
(2) N2O4 (g) ↔ 2NO2 (g) ΔH = +59,2 kJ
(4) 2SO2 (g) + O2 (g) ↔ 2SO3 (g) ΔH = −190 kJ
Pasangan reaksi yang menghasilkan produk lebih banyak jika suhu dinaikkan adalah... A. (1) dan (2)
B. (1) dan (3) C. (1) dan (4) D. (2) dan (3) E. (3) dan (4)
(12) Soal UN Kimia Tahun 2013
Perhatikan reaksi kesetimbangan berikut!
Jika suhu tetap, tekanan sistem diperbesar maka kesetimbangan bergeser ke arah…. A. kiri, karena kesetimbangan bergeser ke jumlah mol terkecil
B. kiri, karena kesetimbangan bergeser ke jumlah mol terbesar C. kanan, karena kesetimbangan bergeser ke jumlah mol terbesar D. kanan, karena konsentrasi N2 bertambah
E. tetap, karena perubahan tekanan dan volume tidak menggeser kesetimbangan (13) Soal UN Kimia Tahun 2013
Dalam volume 1 liter dipanaskan gas NH3 hingga terjadi reaksi:
Data yang diperoleh sebagai berikut:
Harga Kc kesetimbangan tersebut adalah…. A.
B.
D.
E.
(14) Soal UN Kimia Tahun 2014
Suatu reaksi kesetimbangan gas ditunjukkan pada persamaan berikut: CO(g) + H2O(g) ↔ CO2(g) + H2(g)
Jika saat setimbang, perbandingan konsentrasi zat-zat yang bereaksi sebagai berikut:
Konsentrasi Zat Saat Setimbang (M)
CO(g) H2O(g) CO2(g) H2(g)
2 1 1 1
Harga tetapan kesetimbangan reaksi tersebut adalah.... A. ½
B. 1 C. 2 D. 4 E. 8
(15) Soal UN Kimia Tahun 2014 Reaksi kesetimbangan:
2H2S (g) + 3O2(g) ↔ 2H2O(g) + 2SO2 (g)
Jika tekanan diperbesar, pernyataan yang tepat adalah…. A. bergeser ke kanan, gas SO2 bertambah
B. bergeser ke kanan, gas SO2 berkurang
C. bergeser ke kanan, gas H2O berkurang
D. bergeser ke kiri, gas H2S bertambah
Bank Soal UN Reaksi Redoks
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia un tahun 2002 - 2011, 2012, 2013, 2014 tentang reaksi reduksi dan oksidasi - reaksi redoks.
Reaksi Redoks
(1) Soal Ebtanas Tahun 2001 Reaksi redoks
a Cr2O7 (aq) + b C2O42- (aq) + c H+ → d Cr3+ (aq) + e CO2 (g) + f H2O (l)
setelah disetarakan mempunyai harga a, b, d, e berturut-turut.... A. 1, 3, 1, 6
B. 1, 3, 2, 6 C. 2, 3, 2, 6 D. 2, 3, 2, 3 E. 6, 2, 3, 1
(2) Soal Ebtanas Tahun 2002
Di antara persamaan reaksi berikut, yang merupakan reaksi redoks adalah.... A. NaOH (s) + HCl (aq) → NaCl (aq) + H2O (l)
B. CaSO4 (aq) + 2 LiOH (aq) → Ca(OH)2 (s) + Li2SO4 (aq)
C. Mg(OH)2 (s) + 2 HCl (aq) → MgCl2 (aq) + 2 H2O (l)
E. MnO2 (s) + HCl (aq) → MnCl2 (aq) + 2 H2O (l) + Cl2 (g)
(3) Soal Ebtanas Tahun 2003 Persamaan reaksi redoks berikut :
a KOH + b Al + 18 H2 + 5 KOH → c NH3 + d KAl(OH)4
Harga a, b, c dan d berturut-turut adalah... A. 3, 8, 3, 8
B. 2, 6, 2, 6 C. 2, 7, 2, 7 D. 3, 7, 3, 7 E. 3, 6, 3, 6
(4) Soal Unas Tahun 2004 Pada reaksi :
Cl2 (aq) + 2 KOH (aq) → KCl (aq) + KClO (aq) + H2O (l)
bilangan oksidasi klor berubah dari : A. –1 menjadi +1 dan 0 B. +1 menjadi -1 dan 0 C. 0 menjadi –1 dan -2 D. –2 menjadi 0 dan +1 E. 0 menjadi –1 dan +1 (5) Soal UN Tahun 2008
Gas nitrogen monoksida merupakan gas yang tidak berwarna dan beracun. Gas tersebut dapat dihasilkan dari reaksi asam sulfida dengan asam nitrat, dengan persamaan reaksi :
3 H2S(g) + 2 HNO3(aq) + 6 H+(aq) → 2 NO(g) + 2 S(s) + 4 H2O(l)
Spesi yang merupakan oksidator adalah ... A. H2S B. HNO3 C. NO D. S E. H2O (6) Soal UN Tahun 2009
Koefisien reaksi atau nilai a, b, c, dan d dari persamaan reaksi: a SO2 (g) + b H2S (g) → c H2O (l) + d S(s) berturut-turut adalah... A. 1, 2, 2, 3 B. 1, 2, 1, 3 C. 1, 3, 1, 2 D. 2, 1, 2, 1 E. 2, 1, 1, 3
(7) Soal UN Tahun 2010
Gas klor dapat dibuat melalui reaksi redoks berikut:
a K2Cr2O7 (aq) + 14 HCl (aq) → 2 KCl (aq) + b CrCl3 (aq) + c Cl2 (aq) + d H2O(l)
Setelah disetarakan, nilai koefisien reaksi a, b, c, dan d secara berurutan adalah.... A. 1, 2, 2, 7 B. 1, 2, 3, 7 C. 1, 2, 1, 7 D. 2, 1, 2, 7 E. 2, 2, 3, 7 (8) Soal UN Tahun 2011
Perhatikan reaksi redoks berikut! 2 HBr + H2SO4 → Br2 + SO2 + 2 H2O
Zat yang merupakan oksidator adalah... A. HBr B. H2SO4 C. Br2 D. SO4 E. H2O (9) Soal UN Tahun 2011
Pada persamaan reaksi redoks berikut:
a MnO4− (aq) + b H+ (aq) + c C2O42− (aq) → 2 Mn 2+ (aq) + 8 H2O (l) + 10 CO2 (g)
Harga koefisien a, b, dan c adalah... A. 1, 4, dan 2 B. 1, 8, dan 3 C. 2, 6, dan 5 D. 2, 8, dan 5 E. 2, 16, dan 5 (10) Soal UN Tahun 2012 Pada reaksi redoks:
a Cu (s) + b NO3− (aq) + H+ (aq) → c Cu2+ (aq) + NO (g) + d H2O (l)
Harga koefisien a, b, c, dan d berturut-turut adalah.... A. 2, 1, 2, dan 2
B. 2, 1, 2, dan 4 C. 3, 2, 3, dan 4 D. 4, 1, 2, dan 3 E. 4, 1, 2, dan 4
(11) Soal UN Tahun 2013
Diketahui persamaan reaksi redoks:
a C2 O42− + Cr2 O72− + b H+ → c CO2 + d Cr3+ + H2 O
Setelah reaksi disetarakan, harga a, b, dan d yang paling tepat adalah… A. 3, 1, dan 2 B. 3, 1, dan 6 C. 3, 1, dan 7 D. 3, 14, dan 2 E. 3, 14, dan 7 (12) Soal UN Tahun 2013
Perhatikan beberapa persamaan reaksi berikut ini!
Persamaan reaksi yang merupakan reaksi oksidasi terdapat pada nomor… (1) dan (2) (1) dan (3) (2) dan (3) (2) dan (4) (3) dan (4) (13) Soal UN Tahun 2014
Gas klorin dan larutan NaOH dingin apabila dicampurkan menghasilkan natrium klorida dan natrium hipoklorit yang dapat dijadikan sebagai pemutih pakaian menurut persamaan reaksi: Cl2 + 2 OH− → Cl− + ClO− + H2O
Zat yang mengalami autoredoks berikut perubahan bilangan oksidasinya adalah….. A. Cl2 dari bilangan oksidasi – 1 menjadi 0 dan +1
B. Cl2 dari bilangan oksidasi 0 menjadi – 1 dan +1
C. H dari bilangan oksidasi +1 menjadi 0 dan +2 D. O dari bilangan oksidasi – 2 menjadi – 3 dan – 1 E. O dari bilangan oksidasi – 1 menjadi 0 dan – 2
Bank Soal UN Sel Volta
Category: Bank Soal UN Kimia SMA
Kimia Study Center - Kumpulan contoh soal ujian nasional kimia un tahun 2002 - 2011, 2012, 2013, 2014 tentang sel volta dan potensial sel standar.
Sel Volta dan Potensial Sel Standar
(1) Soal Ebtanas Tahun 2002 no. 45 Diketahui potensial elektroda dari : Al3+ + 3e → Al Eo = –1,66 volt
Fe3+ + 3e → Fe Eo = − 0,44 volt
Reaksi redoks:
2 Al (aq) + 3 Fe2+ (aq) ↔ 2 Al3+(aq) + 3 Fe (s)
menghasilkan potensial standar sebesar... A. + 2,10 volt
B. + 2,00 volt C. + 1,22 volt D. − 1,22 volt E. − 2,10 volt
(2) Soal Ebtanas Tahun 2003
F2 (g) + 2e → 2F −(aq) Eo = + 2,87 volt
Cl2 (g) + 2e → 2Cl−(aq) Eo = + 1,36 volt
Br2 (l) + 2e → 2Br −(aq) Eo = + 1,06 volt
I2 (g) + 2e → 2I−(aq) Eo = + 0,54 volt
Harga potensial sel untuk reaksi : F2 (g) + 2I− (aq) → I2 (s) + 2 F −(aq) adalah.... A. 2,33 volt B. 2,87 volt C. 2,90 volt D. 3,41 volt E. 3,93 volt
(3) Soal Ujian Nasional Tahun 2004
Tegangan suatu sel, yang setengah sel-selnya diberikan di bawah ini : Mg2+ + 2 e → Mg (s) E = –2,37 V Cu2+ + 2 e → Cu (s) E = +0,3 V ialah... A. − 2,03 volt B. +1,35 volt C. +2,71 volt D. +2,03 volt E. −1,02 volt
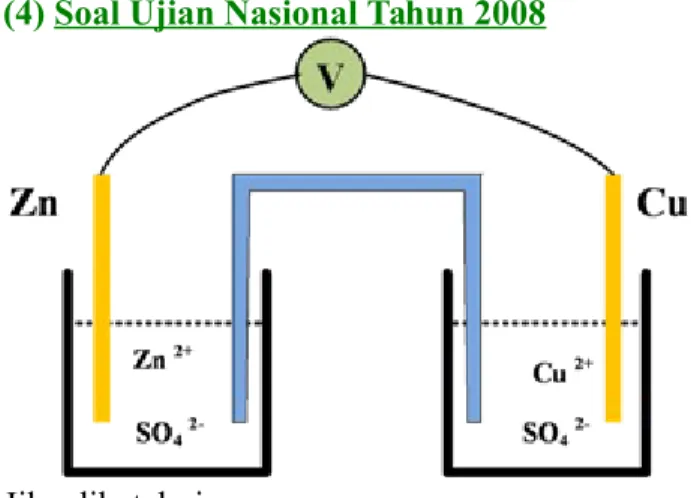
(4) Soal Ujian Nasional Tahun 2008
Jika diketahui :
Zn+2 / Zn Eo = –0, 76 Volt
Cu+2 / Cu Eo = +0,34 Volt
Diagram sel yang paling tepat untuk menggambarkan proses tersebut adalah... A. ZnSO4 / Zn // CuSO4 / Cu
B. Zn / Zn+2 // Cu+2 / SO4
2-C. Zn+2 / SO
2-D. Cu / CuSO4 // ZnSO4 / Zn
E. Cu / Cu+2 // Zn+2 / Zn
(5) Soal Ujian Nasional Tahun 2008
Maka besarnya potensial sel (Eo sel) Volta tersebut adalah ...
A. –0,42 Volt B. –1,10 Volt C. +0,42 Volt D. +1,10 Volt E. +11,0 Volt
(6) Soal UN Kimia Tahun 2009 Perhatikan rangkaian sel volta berikut!
Maka diagram sel dari rangkaian tersebut adalah ... A. Pb2+ | Pb || Ag | Ag+
B. Ag | Ag+ || Pb2+ | Pb
C. Ag+ | Ag || Pb2+ | Pb
D. Pb | Pb2+ || Ag | Ag+
E. Pb | Pb2+ || Ag+ | Ag
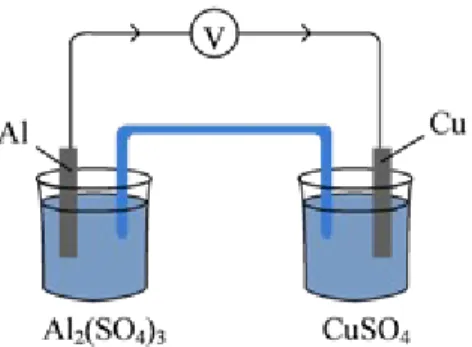
(7) Soal UN Kimia 2010 No. 34
Diagram sel volta yang benar adalah.... A. Al(s)/Al3+(aq) // Cu2+ (aq)/Cu(s)
B. Al3+ (aq)/Al(s) // Cu(s)/Cu2+(aq)
C. Cu2+(aq)/Cu(s) // Al(s)/Al3+(aq)
D. Cu(s)/Cu2+(aq) //Al3+(aq)/Al(s)
E. Al(s)/Cu2+(aq) // Al3+(aq)/Cu(s)
(8) Soal UN Kimia 2011 No. 32
Dalam suatu sel volta terjadi reaksi Sn + 2 Ag+ → Sn2+ + 2 Ag
Eo Sn2+ | Sn = − 0,14 volt dan Eo Ag+ |Ag = + 0,080 volt, harga potensial sel reaksi tersebut
adalah.... A. 1,88 volt B. 1,74 volt C. 0,94 volt D. 0,36 volt E. − 0,94 volt (9) Soal UN Kimia 2012 Mg2+ (aq) + 2e → Mg (s) E o = −2,38 volt Al3+ (aq) + 3e → Al (s) E o = −1,66 volt
Notasi sel reaksi yang dapat berlangsung adalah.... A. Mg | Mg2+ || Al3+ | Al B. Al | Al3+ || Mg2+ | Mg C. Mg2+ | Mg || Al | AlMg3+ D. Al3+ | Al || Mg2+ | Mg E. Mg | Mg2+ || Al | Al3+ (10) Soal UN Kimia 2012 Mg2+ (aq) + 2e → Mg (s) E o = −2,38 volt Al3+ (aq) + 3e → Al (s) E o = −1,66 volt
Harga Eo sel persamaan reaksi tersebut adalah...
B. +0,76 volt C. +0,72 volt D. −0,72 volt E. −4,04 volt
(11) Soal UN Kimia 2013 Berdasarkan data berikut: Fe2+ + 2e → Fe, E° = -0,44 V
Pb2+ + 2e → Pb, E° = -0,13 V
Zn2+ + 2e → Zn, E° = -0,76 V
Sn2+ + 2e → Sn, E° = -0,14 V
Reaksi yang tidak dapat berlangsung spontan adalah…. A. Sn / Sn2+ // Pb2+ / Pb B. Zn / Zn2+ // Sn2+ / Sn C. Pb / Pb2+ // Zn2+ / Zn D. Fe / Fe2+ // Pb2+ / Pb E. Zn / Zn2+ // Fe2+ / Fe (12) Soal UN Kimia 2014 Data potensial elektroda standar: Pb2+ (aq) + 2e → Pb E° = - 0,13 V
Ag+ (aq) + e → Ag E° = +0,80 V
Zn2+ (aq) + 2e → Zn E° = - 0,76 V
Mg2+ (aq) + 2e → Mg E° = - 2,37 V
Notasi sel berikut yang berlangsung spontan adalah... A. Pb/Pb2+ // Ag+/Ag
B. Pb/Pb2+ // Mg2+ / Mg
C. Zn/Zn2+ // Mg2+ /Mg
D. Ag/Ag+ // Zn2+ / Zn
Bank Soal UN Elektrolisis
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional UN kimia tahun 2002 - 2011, 2012, 2013, 2014 materi elektrolisis dan hukum faraday.
Elektrolisis
(1) Soal Ebtanas Tahun 2001
Arus listrik sebesar 10 ampere dialirkan selama 16 menit ke dalam larutan CuSO4 (Ar : Cu = 63,5; S = 32; O = 16) dengan elektroda karbon. Massa tembaga yang dapat diendapkan di katoda adalah.... A. 1,58 gram B. 2,39 gram C. 3,16 gram D. 6,32 gram E. 8,23 gram
(2) Soal Ebtanas Tahun 2002
Pada reaksi elektrolisa larutan NiSO4 dengan elektroda Ag, reaksi yang terjadi pada anoda adalah....
A. Ni2+ (aq) + 2e → Ni (s)
C. Ni (s) → Ni2+ (aq) + 2e
D. 2H2O (l) + 2e → H2 (g) + 2OH− (aq)
E. 2H2O (l) → 4H+ (aq) + O2 (g) + 4e
(3) Soal Ebtanas Tahun 2003
Zat yang terbentuk di kutub negatif dari elektrolisis larutan NaCl dengan elektroda grafit adalah... A. logam Na B. gas Cl2 C. OH− dan H 2 D. H2O E. H+ dan O 2
(4) Soal Ujian Nasional Tahun 2004
Perhatikan gambar elektrosis larutan KI dengan elektroda karbon.
Zat yang terjadi pada elektrode B adalah... A. I2
B. gas H2
C. gas O2
D. H2O
E. logam K
(5) Soal Ujian Nasional Tahun 2008
Sejumlah arus listrik yang sama dialirkan ke dalam dua sel elektrolisis yang berbeda sesuai gambar berikut :
Jika dalam larutan ZnSO4 akan mengendap 13 gram Zn (Ar = 65), maka pada larutan SnCl4
A. 0,9 gram B. 11,9 gram C. 18,3 gram D. 71,0 gram E. 595 gram
(6) Soal UN Kimia Tahun 2009 dan UN Kimia Tahun 2010
Sebanyak 1 liter larutan CrCl3 1M dielektrolisis dengan arus 6 Ampere. Jika diketahui Ar Cr
= 52; 1 F = 96.500 maka waktu yang diperlukan untuk mengendapkan logam krom sebanyak 3,88 gram tersebut adalah....detik.
(7) Soal UN Kimia Tahun 2011
Proses elektrolisis lelehan NaCl dengan elektroda karbon, digunakan arus sebesar 10 ampere selama 30 menit. Massa logam natrium yang diperoleh adalah....
(Ar Na= 23, Cl = 35,5)
(8) Soal UN Kimia Tahun 2012
Pada penyepuhan logam besi dengan tembaga digunakan larutan CuSO4 dengan arus 2A
selama 30 menit. Massa tembaga yang mengendap di katoda adalah...(Ar Cu = 63,5) A. (63,5 × 30 × 60) / (96.500)
B. (63,5 × 96.500 × 2) / (2 × 30 × 60) C. (2 × 96.500 × 2) / (2 × 63,5) D. (63,5 × 2 × 30 × 2) / (60 × 96.500) E. (63,5 × 60 × 30 × 2) / (96.500)
(9) Soal UN Kimia Tahun 2013
Poses elektrolisis lelehan NaCl dengan elektrode karbon, digunakan arus sebesar 10 ampere selama 30 menit. Massa logam natrium yang diperoleh adalah….
(10) Soal UN Kimia Tahun 2014
Dalam elektrolisis larutan LSO4 dengan elektroda inert dihasilkan 448 ml gas di anoda (STP) dan 2,56 gram endapan logam L di katoda. Ar L adalah….
A. 32,0 B. 63,5 C. 64,0 D. 65,0 E. 127,0
Bank Soal UN Hasil Kali Kelarutan
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional UN kimia tahun 2002 - 2011, 2012, 2013, 2014 tentang hasil kali kelarutan.
Kelarutan dan Hasil Kali Kelarutan
(1) Soal Ebtanas Tahun 2001
Dalam 100 cm3 air dapat larut 1,16 mg Mg(OH)
2 (Mr = 58). Harga Ksp dari Mg(OH)2
adalah.... A. 16,0 × 10-12 B. 3,2× 10-11 C. 8,0× 10-10 D. 4,0× 10-10 E. 8,0× 10-8
(2) Soal Ebtanas Tahun 2001
Kelarutan AgCl dalam air pada 25o C adalah 1,435 mg per liter. Kelarutan AgCl dalam
larutan yang mengandung 0,1 M NaCl adalah … (massa molar AgCl = 143,5 gram mol-1)
A. 1 × 10-4 mol per liter
B. 1 × 10-5 mol per liter
D. 1 × 10-10 mol per liter
E. 1 × 10-14 mol per liter
(3) Soal Ebtanas Tahun 2002
Larutan jenuh dari L(OH)2 mempunyai pH = 10, Ksp dari L(OH)2 tersebut adalah....
A. 5 × 10-13
B. 2 × 10-12
C. 5 × 10-10
D. 2 × 10-10
E. 2 × 10-8
(4) Soal Ebtanas Tahun 2003
Tentukan Ksp Mg(OH)2, jika sebanyak 0,58 gram Mg(OH)2 dilarutkan dalam 200 mL air. (Mr
Mg(OH)2 = 58). A. 10-4 B. 10-2 C. 5 × 10-4 D. 5 × 10-2 E. 10-3 (5) Soal UN 2008
Kelarutan Mg(OH2) dalam NaOH 0,1 M dengan Ksp Mg(OH)2 = 1,8×10−11 mol3 L-3 adalah ...
A. 1,8×10−13 mol/L B. 1,8×10−10 mol/L C. 4,5×10−10 mol/L D. 1,8×10−9 mol/L E. 6,7×10−6 mol/L (6) Soal UN 2009
Ke dalam 5 wadah yang berbeda dimasukkan masing-masing 100 mL; 0,001 M larutan yang mengandung Ca(NO3)2, Ba(NO3)2, Mg(NO3)2, Fe(NO3)2, dan Pb(NO3)2
Diketahui: Ksp : Ba(OH)2 : 4⋅10−3
Mg(OH)2 : 3⋅10−12
Ca(OH)2 : 5⋅10−6
Pb(OH)2 : 3⋅10−16
Fe(OH)2 : 5⋅10−16
Jika ke dalam tiap wadah ditetesi KOH 0,001 M, maka campuran yang tidak menghasilkan endapan adalah ...
A. Fe(OH)2 dan Mg(OH)2
B. Mg(OH)2 dan Pb(OH)2
C. Ca(OH)2 dan Ba(OH)2
D. Ba(OH)2 dan Mg(OH)2
(7) Soal UN 2012
Berikut ini beberapa garam dan Ksp nya: (1) Cu(OH)2, Ksp = 2,6 × 10−19
(2) Fe(OH)2, Ksp = 8,0 × 10−16
(3) Pb(OH)2, Ksp = 1,4 × 10−20; dan
(4) Mg(OH)2, Ksp = 1,8 × 10−11
Urutan kelarutan senyawa tersebut dari yang kecil ke besar adalah... A. (1), (2), (3), (4)
B. (2), (4), (1), (3) C. (3), (1), (2), (4) D. (3), (2), (4), (1) E. (4), (2), (1), (3)
(8) Soal Ebtanas Tahun 2013
Sebanyak 50 mL larutan Ca(NO3)2 10−2 M dicampurkan dengan 50 mL larutan Na2CO3 10−2
M dengan reaksi:
Ca(NO3)2 (aq) + Na2CO3 (aq) → CaCO3 (s) + 2NaNO3 (aq)
Jika Ksp CaCO3 = 9 × 10−9, massa yang mengendap sebanyak…
(Ar Ca = 40; C = 12; O = 16; Na = 23; N = 14) A. 100 gram B. 0,100 gram C. 0,050 gram D. 0,025 gram E. 0,0025 gram (9) Soal UN 2014
100 mL NaOH 1,8 M + 100 mL CH3COOH 1,8 M ke dalam larutan garam uji terbentuk
ditetesi larutan Ni(OH3)2 sampai keadaan tepat jenuh Ni(OH)2. Kalau Kw = 10 – 14, Ka = 10 – 5
KSp Ni(OH)2 = 1,8 × 10 – 14, maka (Ni2+) pada saat tepat jenuh (tepat saat terjadi pengendapan)
adalah…. A. 2 × 10 – 2 M B. 2 × 10 – 3 M C. 2 × 10 – 4 M D. 2 × 10 – 5 M E. 2 × 10 – 6 M
Bank Soal UN Senyawa Unsur Pembuatan dan Manfaat
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia tahun 2002 - 2011 dan 2012, 2013, 2014 tentang cara pembuatan atau memperoleh unsur dan senyawa serta kegunaan, sifat atau manfaatnya dalam kehidupan sehari-hari serta kimia unsur.
Unsur dan Senyawa Kimia, Sifat, Reaksi, Kegunaan dan Pembuatan
(1) Soal Ebtanas Kimia Tahun 2001
Unsur-unsur yang sangat penting diperlukan oleh tumbuh-tumbuhan adalah... A. N, P, K
B. N, P, Ca C. N, P, C D. Zn, K, P E. Mn, Cu, Pb
(2) Soal Ebtanas Kimia Tahun 2001
Senyawa magnesium yang digunakan untuk menetralkan kelebihan asam lambung adalah... A. magnesium klorida
B. magnesium sulfat C. magnesium karbonat D. magnesium kromat E. magnesium hidroksida
Diantara senyawa berikut ini yang dapat dipakai sebagai obat pencuci perut adalah … A. KNO3 B. NaHCO3 C. Na2HCO3 D. MgSO4. 7H2O E. CaSO4 .7H2O
(4) Soal Ebtanas Kimia Tahun 2003
Senyawa berikut yang digunakan untuk membersihkan kutek adalah … A. alkohol
B. eter C. aseton D. asam asetat E. formalin
(5) Soal Ebtanas Kimia Tahun 2003
Senyawa yang digunakan untuk pendingin AC adalah... A. Freon
B. Formalin C. Alkohol D. CO2 E. Aseton
(6) Soal Ebtanas Kimia Tahun 2003
Natrium siklamat dalam pembuatan sirup sering digunakan, karena berfungsi untuk.... A. zat pewarma
B. zat pengawet C. anti oksidan D. pemutih E. pemanis
(7) Soal Ujian Nasional Kimia Tahun 2004
Unsur-unsur yang diperlukan oleh tanaman di antaranya adalah unsur N, P dan K yang berturut-turut terdapat dalam pupuk....
A. ES, Urea, Kalium Klorida B. Urea, TSP, Kalium Klorida C. Kalium Klorida, Urea, TSP D. TSP, Urea, Kalium Klorida E. ES, TSP, Urea
(8) Soal UN Kimia Tahun 2009
Berikut data batuan/mineral serta kandungan unsur:
No Unsur Mineral
1 K Sendawa Chili
3 Si Kuarsa
4 Mg Kalkopirit
5 Al Bauksit
Pasangan data yang berhubungan secara tepat adalah.... A. 1 dan 2
B. 1 dan 5 C. 2 dan 3 D. 3 dan 4 E. 4 dan 5
(9) Soal UN Kimia Tahun 2009
Logam alumunium diperoleh dari pengolahan biji bauksit (Al2O3.xH2O).
Leburannya dielektrolisis dengan elektroda grafit melalui reaksi berikut : Al2O3 (l) → 2 Al3+ (l)+3 O2− (l) di katoda Al3+ (l)+3e→ Al (l) di anoda 2 O2- (l) → O 2 (g) + 4e __________________________ Reaksi keseluruhan : 2 Al2 O3 (l) → 4 Al (l)+3 O2 (g)
Nama proses pengolahan logam tersebut dikenal dengan... A. Hall – Herault
B. Frasch
C. Haber – Bosh D. Oswalt E. Kontak
(10) Soal UN Kimia Tahun 2009
Unsur yang dihasilkan dari proses tersebut dapat membentuk senyawa yang sering digunakan untuk...
A. melarutkan bauksit agar berfase cair B. pengawet warna merah pada daging C. pengeyal produk daging olahan D. pemutih tepung beras dan jagung
E. mengendapkan kotoran air hingga jernih (11) Soal UN Kimia Tahun 2010
Perhatikan tabel tentang batuan/mineral dan unsur yang dikandungnya:
No Nama Mineral Unsur yang Dikandung
1 Siderit Besi
2 Kriolit Aluminium
4 Selestit Selenium
5 Kalkosit Tembaga
Pasangan data yang keduanya berhubungan secara tepat adalah... A. 1 dan 2
B. 1 dan 3 C. 2 dan 3 D. 3 dan 4 E. 3 dan 5
(12) Soal UN Kimia Tahun 2010
Berikut ini beberapa proses pengolahan logam: 1. Proses Down.
2. Tanur tiup 3. Ekstraksi. 4. Bessemer. 5. Hall-Heroult.
Nama yang paling tepat untuk pembuatan unsur besi adalah... A. 1
B. 2 C. 3 D. 4 E. 5
(13) Soal UN Kimia Tahun 2010
Perhatikan data nama unsur dan kegunaannya berikut ini:
No Nama Unsur Kegunaan
1 2 3 4 5 Klorin Kalsium Kalium Belerang Fosforus
Campuran pemadam kebakaran Bahan kembang api
Pupuk Fotografi Korek api
Pasangan data yang keduanya berhubungan dengan benar adalah.... A. 1 dan 2
B. 1 dan 3 C. 2 dan 4 D. 3 dan 4 E. 3 dan 5
(14) Soal UN Kimia Tahun 2011
1 2 3 4 5 Barium Stronsium Kalium Mangan Magnesium Wiserit Selestit Dolomit Pirolusit Karnalit Penyamak kulit
Nyala merah kembang api Campuran asbes
Zat aktif dalam baterai Antasida
Pasangan data yang ketiganya berhubungan dengan tepat adalah.... A. 1 dan 2
B. 2 dan 3 C. 3 dan 4 D. 3 dan 5 E. 4 dan 5
(15) Soal UN Kimia Tahun 2012
Tabel berikut berisi data nama unsur berikut proses mendapatkannya
Pasangan data yang keduanya berhubungan dengan tepat adalah... A. 1 dan 2
B. 1 dan 3 C. 2 dan 3 D. 2 dan 4 E. 3 dan 4
(16) Soal UN Kimia Tahun 2012
Dari beberapa kegunaan unsur/senyawa berikut ini: (1) pengisi balon udara;
(2) lampu reklame;
(3) pencampur oksigen dalam tabung penyelam; (4) film fotografi;
(5) antiseptik pada luka;
Kegunaan gas helium/senyawanya terdapat pada nomor... A. 1 dan 2 B. 1 dan 3 C. 2 dan 4 D. 3 an 5 E. 4 dan 5 (17) Soal UN Kimia 2013 Berikut ini beberapa sifat unsur:
(2) titik leleh tinggi;
(3) membentuk molekul diatomik;dan (4) oksidator kuat.
Sifat unsur halogen terdapat pada nomor…. A. (1) dan (2) B. (1) dan (3) C. (2) dan (3) D. (2) dan (4) E. (3) dan (4) (18) Soal UN Kimia 2013
Berikut ini beberapa senyawa yang mengandung unsur golongan alkali tanah: (1) BaSO4;
(2) MgSO4;
(3) Ca(OCl)2
(4) MgSO4;dan
(5) CaSO4.
Senyawa yang digunakan untuk obat cuci perut adalah nomor…. A. (1) B. (2) C. (3) D. (4) E. (5) (19) Soal UN Kimia 2013
Berikut ini adalah beberapa proses pengolahan unsur: (1) Goldschmit;
(2) Wohler; (3) Haber-Bosch; (4) Frasch;dan (5) Dow.
Proses pengolahan magnesium ditunjukkan oleh nomor…. A. (5) B. (4) C. (3) D. (2) E. (1) (20) Soal UN Kimia 2013
Logam natrium bila dimasukkan dalam air akan bereaksi membentuk larutan natrium hidroksida dan gas hidrogen. Persamaan reaksi yang tepat dan setara adalah….. A. Na(s) + H2 O(l) → NaOH (aq) + H2 (g)
B. 2Na(s) + 2H2 O(l) → 2NaOH (aq) + H2 (g)
C. Na(s) + 2H2 O(l) → NaOH (aq) + H2 (g)
E. 3Na(s) + 2H2O(l) → 3NaOH (aq) + H2 (g)
(21) Soal UN Kimia 2014
Sifat-sifat suatu senyawa sebagai berikut: (1) Titik didih tinggi
(2) Senyawanya berwarna (3) Membentuk ion kompleks (4) Menghantarkan arus listrik
Contoh senyawa yang memiliki sifat tersebut adalah…. A. CuSO4 B. SrSO4 C. MgSO4 D. Na2SO4 E. CaSO4 (22) Soal UN Kimia 2014
Berikut ini merupakan salah satu tahap reaksi pengolahan logam dari bijihnya
Fe2O3(s) + 3CO(g) → 2Fe(s) + 3 CO2(g)
Nama pengolahan unsur tersebut adalah…. A. Dow B. Deacon C. Frasch D. Hall Herault E. Tanur Tinggi (23) Soal UN Kimia 2014
Berikut senyawa yang mengandung unsur golongan IA dan IIA: (1) CaCOCl2 (2) SrSO4 (3) Na2SO4 (4) Na2B4O7 (5) KIO3 (6) CaC3
Senyawa yang diperlukan pada pabrik kertas dan pengempal berturut-turut adalah…. A. (1) dan (2)
B. (1) dan (4) C. (2) dan (3) D. (3) dan (4) E. (5) dan (6)
Bank Soal UN Energitika Kalor Reaksi
Category: Bank Soal UN Kimia SMAKimia Study Center - Kumpulan contoh soal ujian nasional kimia UN tahun 2002 - 2011, 2012, 2013, 2014 tentang menentukan kalor pada reaksi kimia.
Kalor Reaksi
(1) Soal Ebtanas Kimia Tahun 2001 Diketahui reaksi : S (s) + O2 (g) → SO2 (g) ∆H1 = –299 kJ mol-1 SO2 (g) + 1/2 O2 (g) → SO3 (g) ∆H2 = X kJ mol-1 S (s) + 3/ 2 O2 (g) → SO3 (g) ∆H3 = –396 kJ mol-1 Besarnya X adalah... A. –49,9 kJ mol-1 B. –97 kJ mol-1 C. –194 kJ mol-1 D. +49,9 kJ mol-1 E. +97 kJ mol-1
(2) Soal Ebtanas Kimia Tahun 2001 Diketahui energi ikatan dari
O – H = 464 kJ O = O = 500 kJ H – H = 436 kJ
Kalor yang diperlukan untuk menguraikan 9 gram air (Mr = 18) adalah... A. 8 kJ
B. 121 kJ C. 222 kJ D. 242 kJ E. 472 kJ
(3) Soal Ebtanas Kimia Tahun 2002
Jika diketahui perubahan entalpi untuk reaksi berikut : 2 Fe (s) + 3/
2 O2 (g) → Fe2O3 (s) ∆H = – 822 kJ/mol
C (s) + 1/
2 O2 (g) → CO (g) ∆H = – 110 kJ/mol
Perubahan untuk reaksi
3 C (s) + Fe2O3 (s) → 2 Fe (s) + 3 CO (g) adalah... A. –932 kJ/mol B. –712 kJ/mol C. –492 kJ/mol D. +492 kJ/mol E. +712 kJ/mol
(4) Soal Ebtanas Kimia Tahun 2002 Berdasarkan diagram :
Perubahan entalpi untuk A2B → CD2 adalah...
A. ΔH1 + ΔH2 + ΔH3
B. − ΔH1 + ΔH2 + ΔH3
C. − ΔH1 − ΔH2 − ΔH3
D. ΔH1 − ΔH2 − ΔH3
E. − ΔH1 + ΔH2 − ΔH3
(5) Soal Ebtanas Kimia Tahun 2002
Berdasarkan diagram tersebut harga ΔH2 adalah.... A. 790,4 kJ B. 593,8 kJ C. 196,6 kJ D. − 196,6 kJ E. − 593,8 kJ
(6) Soal Unas Kimia Tahun 2004
Diketahui perubahan entalpi pembentukan H2S, SO2 dan H2O berturut-turut –20 kJ/mol, –298
kJ/mol dan –286 kJ/mol. Harga perubahan entalpi reaksi : 2H2S (g) + 1 1/2 O2 (g) → SO2 (g) + H2O (g) A. –446 kJ B. –564 kJ C. –604 kJ D. –645 kJ E. –654 kJ
(7) Soal Unas Kimia Tahun 2008 Diketahui energi ikatan rata-rata : C ≡ C : 839 kJ/mol
C − C : 343 kJ/mol H − H : 436 kJ/mol C − H : 410 kJ/mol
Perubahan entalpi yang terjadi pada reaksi :
CH3 − C ≡ CH + 2 H2 → CH3 −CH2 −CH3 sebesar ... A. +272 kJ/mol B. – 272 kJ/mol C. – 1.711 kj/mol D. – 1.983 kJ/mol E. – 3.694 kJ/mol
(8) Soal Unas Kimia Tahun 2010
Seorang siswa mengukur perubahan entalpi dari reaksi HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l)
Suhu awal larutan HCl dan NaOH masing-masing 25°C dan setelah dicampurkan menjadi 30°C. Jika banyaknya zat yang dicampurkan 50 mL HCl 0,2 M dan 50 mL NaOh 0,4 M kapasitas kalor bejana diabaikan dan kalor jenis air 4,2 J g−1.K−1, maka perubahan entalpi (ΔH
A. 4,2 kJ B. 16,8 kJ C. −21.0 kJ D. −84,0 kJ E. 210 kJ
(9) Soal Unas Kimia Tahun 2011 Data energi ikatan rata-rata: C = C : 609 kJ/mol;
C – Cl : 326 kJ/mol; C – H : 412 kJ/mol; C – C : 345 kJ/mol; H – Cl : 426 kJ/mol;
Besar entalpi reaksi CH2 = CH2 + HCl → CH3CH2Cl adalah....
A. − 312 kJ/mol B. −48 kJ/mol C. +48 kJ/mol D. +100 kJ/mol E. +312 kJ/mol (10) Soal UN Tahun 2012
Perhatikan data persamaan reaksi termokimia di bawah ini!
(1) C3H8 (g) + 5O2(g) → 3CO2(g) + 4H2O (l) ΔH = − kJ.mol−1
(2) CH3OH (l) + 3/2 O2(g) → CO2(g) + 2H2O (l) ΔH = − kJ.mol−1
(3) NaCl (s) + → Na (s) + 1/2 Cl2 (g) ΔH = + kJ.mol−1
(4) NO (g) → 1/2 N2 (g) + 1/2 O2 (g) ΔH = − kJ.mol−1
(5) H2 (g) + 1/2 O2 (g) → H2O (g) ΔH = − kJ.mol−1
Persamaan reaksi yang merupakan ΔH°f, ΔH°d dan ΔH°c adalah...
A. 1, 2, dan 3 B. 1, 3, dan 4 C. 2, 3, dan 4 D. 3, 4, dan 5 E. 5, 3, dan 2
(11) Soal UN Kimia Tahun 2013
Berdasarkan diagram tersebut , harga ΔH sebesar…. A. + 526 kJ B. – 42 kJ C. – 242 kJ D. – 256 kJ E. – 284 kJ
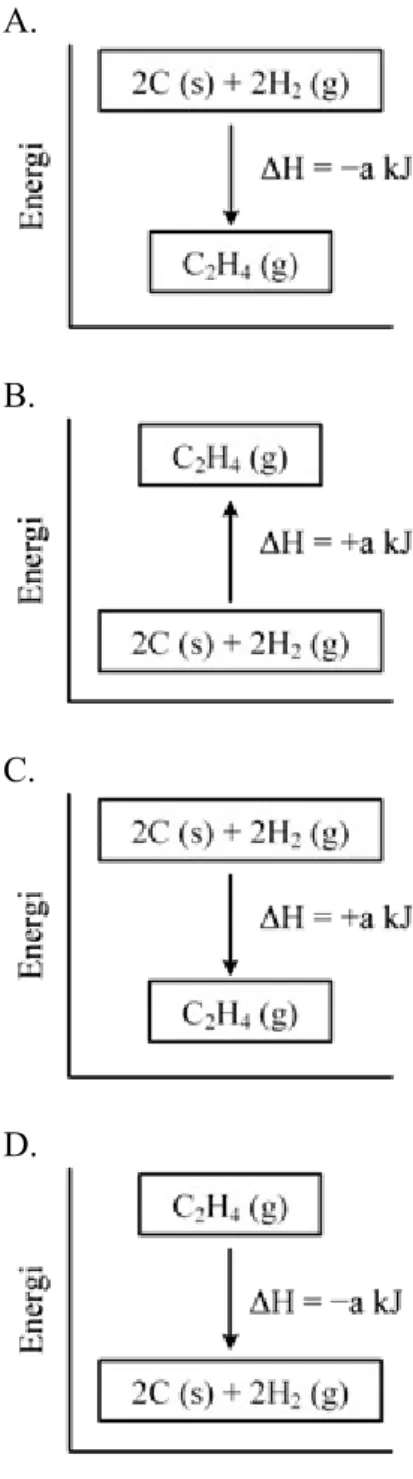
(12) Soal UN Kimia Tahun 2013 Diketahui reaksi:
2C (s) + 2H2 → C2 H4 (g) ΔH = +a kJ
Grafik yang menunjukkan proses reaksi tersebut adalah….. A.
B.
C.