152
APLIKASI FTIR DAN KEMOMETRIKA PLSR (Partial Least Square
Regression) PADA PREDIKSI KADAR FLAVONOID TOTAL
BUNGUR (Lagerstroemia speciosa Pers.) KHAS KALIMANTAN
{Application of FTIR And Chemometric PLSR (Partial Least Square Regression) on
the Prediction of the total Flavonoid of Kalimantan’s Bungur (Lagerstroemia
speciosa Pers.)}
Liling Triyasmono*, Noor Cahaya, Yuniar Novita Sari
Prodi Farmasi, FMIPA, Universitas Lambung Mangkurat
ABSTRAKFTIR memiliki potensi sebagai salah satu andalan analisis kuantitatif pada penetapan kadar flavonoid total dari bungur yang dikombinasikan dengan Kemometrika. PLSR dipilih untuk membuat model prediksi yang menghubungkan antara kadar flavonoid total yang diperoleh dengan metode standar (metode AlCl3) dan spektrum FTIR. Aplikasi PLSR dalam penentuan kadar flavonoid total bungur
menghasilkan nilai koefisien determinasi R2 kalibrasi = 0,998 dan R2 validasi = 0,995, RMSEC =0,205,
RMSEP =0,831, Berdasarkan hasil tersebut dapat disimpulkan bahwa spektrum FTIR bungur dapat digunakan untuk memprediksi kadar flavonoid total dalam bungur dengan persamaan regresi y = 0,979 TF (Bungur) + 0,065 secara akurat dan presisi.
Kata Kunci: FTIR, PLSR, Kasturi, Flavonoid Total, R2, RMSEC, RMSEP PENDAHULUAN
Pengobatan di Indonesia saat ini semakin berkembang ke arah pengobatan tradisional. Salah satu jenis Tumbuhan yang digunakan secara empiris dan tradisional di Kalimantan Selatan adalah Bungur untuk mengobati tekanan darah tinggi dan kencing manis. Daun Bungur memiliki kandungan kimia, seperti saponin, flavonoid dan tanin, sedangkan pada kulit batang bungur mengandung flavonoid dan tanin (Dalimartha, 2003).
Ekstrak polar dari tumbuhan Lythrum salicaria L yang memiliki famili sama dengan bungur yaitu Lythraceae mengandung senyawa golongan flavonoid yang memiliki aktivitas sebagai antioksidan dan antiradang (Tunalier, 2007). Kemudian ekstrak air dari daun Bungur
memiliki aktivitas antidiabetes dan antioksidan (Saumya & Basha, 2011). Asih & Setiawan (2008) menyatakan bahwa dalam fraksi n-butanol kulit batang Bungur ditemukan adanya senyawa flavonoid
Metode analisis kuantitatif senyawa aktif tumbuhan memiliki peranan penting dalam pengembangan produk kesehatan berbasis tumbuhan obat. Analisis total flavonoid dengan metode standar saat ini adalah dengan metode AlCl3 (Desmiaty, 2009).
Spektrofotometri FTIR merupakan salah satu instrumentasi yang cukup handal dalam analisis kualitatif suatu senyawa aktif yang berasal dari tumbuhan (Stuart, 2004). Kemometrika pada spektroskopi FTIR akan memberikan cara untuk pengembangan kalibrasi
153
multivariat dari spektra yang sederhana sampai spektra yang kompleks (Ma, 2000). Ketersedian perangkat lunak yang lebih modern pada kemometrika dapat menghasilkan model data yang tepat dan model kalibrasi yang lebih kuat (Ma, 2000).
Aplikasi kombinasi spektrum FTIR dengan kemometrika telah berhasil digunakan dalam autentikasi minyak buah merah (Rohman
et al, 2010), klasifikasi meniran (Dharmaraj et al., 2006), kadar antioksidan total (Versari et al., 2010), penetapan kadar flavonoid total tempuyung (Rohaeti dkk, 2011).
Penelitian ini akan mengaplikasikan FTIR yang dikombinasikan dengan kemometrika yang menghubungkan secara statistika antara spektrum FTIR kajajahi dan kadar total flavonoid yang ditentukan dengan metode AlCl3 (metode
standar) Keberhasilan model prediksi kadar flavonoid total akan dievaluasi menggunakan nilai koefisien determinasi (R2), RMSEC dan
RMSEP.
METODE PENELITIAN Alat
Alat yang digunakan adalah perangkat maserasi, rotary evaporator, FTIR ABB Horizon MB 2000, Software ABB Horizon MB, Komputer pengolah data, dan peralatan gelas.
Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah simplisia bungur, etanol 70%, KBr for IR, AlCl3, kuersetin, pelarut organik
untuk proses ekstraksi dan pengukuran kadar flavonoid total.
Cara Kerja Ekstraksi
Simplisia dimaserasi dengan etanol 70% selama 6 jam. Selanjutnya di rotary evaporator
untuk mendapatkan ekstrak kering. Ekstrak kering yang diperoleh kemudian dibuat dalam tiga konsentrasi 30%, 50% dan 70%.
Penetapan kadar flavonoid total
Masing-masing ekstrak 1000 ppm (10 mg ekstrak dilarutkan ke dalam 10 ml etanol p.a). Sebanyak 1 mL larutan ekstrak dimasukkan dalam tabung reaksi, lalu direaksikan dengan 1
mL AlCl3 2%. Kemudian ditambahkan 8 mL asam
asetat 5% ke dalam larutan, kemudian
didiamkan kembali selama 12 menit.
Selanjutnya, absorbansi dari larutan uji diukur pada panjang gelombang maksimum yang diperoleh menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum 415 nm. Blanko yang digunakan adalah campuran antara pelarut dan pereaksi namun tanpa sampel. Dilakukan sebanyak tiga kali replikasi (Rohaeti et al., 2011).
Pembuatan Spektrum FTIR
Sebanyak 50,0 mg masing-masing serbuk ekstrak dicampur dan dihomogenkan dengan 950 mg KBr for IR, lalu dilakukan pengukurun pada FTIR ABB Horizon MB 2000 pada daerah IR tengah dengan software Horizon MB 2000. Spektrum yang dihasilkan dengan kecepatan 32 detik dan resolusi 4 cm-1.
Selanjutnya spektrum FTIR masing-masing ekstrak diolah dengan Horizon MB 2000 program kemometrika PLSR tanpa derivatisasi.
Pembuatan Model Prediksi Flavonoid Total
Model Kalibrasi multivariat menggunakan metode regresi PLSR. Pembentukan model prediksi flavonoid total dilakukan oleh PLS dengan melibatkan variabel x (hasil pengukuran FTIR) dan variabel y (hasil pengukuran metode standar). Kalibrasi dan validasi model dievaluasi
154
dengan teknik validasi silang. Akurasi model dilihat berdasarkan nilai koefisien determinasi (R2) dan presisi dievaluasi berdasarkan nilai
RMSEC dan RMSEP. Keberterimaan model ditentukan dengan nilai RMSEC dan RMSEP yang rendah dan koefisien determinasi yang tinggi (Miller and Miller, 2010)
HASIL DAN DISKUSI
Kadar Flavonoid Total Bungur dengan metode standar (AlCl3)
Penentuan kandungan flavonoid total dilakukan dengan metode AlCl3. Prinsip dari
penentuan flavonoid dengan metode AlCl3 adalah
pembentukan kompleks antara AlCl3 dengan
gugus keto C-4 dan C-3 atau C-5 dari gugus hidroksil yang dimiliki senyawa flavonoid (Desmiaty, 2009). Pada penentuan flavonoid total ini dibuat kurva baku menggunakan kuersetin karena kuersetin merupakan flavonoid golongan flavonol yang mempunyai gugus keto pada C-4 dan memiliki gugus hidroksi pada atom C-3 atau C-5 (Desmiaty, 2009). Berikut merupakan reaksi pembentukan kompleks antara senyawa kuersetin dengan AlCl3.
Gambar 1. Proses pembentukan Komplek
Flavonoid-AlCl3
Flavonoid total dapat ditentukan dengan terlebih dahulu menentukan kurva baku kuersetin. Kurva baku kuersetin dibuat dalam konsentrasi 50, 60, 70, 80, 90, 110, 120, 130 dan
140 ppm. Kurva baku ini dibuat sebagai
pembanding ekuivalen senyawa flavonoid yang terdapat dalam ekstrak bungur sehingga dapat menentukan kadar flavonoid totalnya. Berikut adalah grafik kurva baku kuersetin.
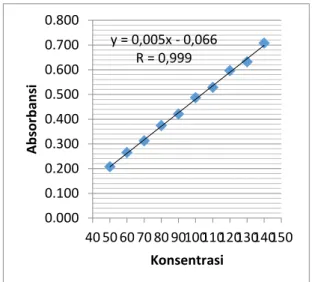
Gambar 2. Kurva Baku Kuersetin
Persamaan regresi yang diperoleh dari kurva baku kuersetin yaitu y=0,005x + (-0,066) dengan nilai koefisien korelasi (r) sebesar 0,999. Nilai ini menyatakan bahwa 99,9% terdapat korelasi antara konsentrasi dengan absorbansi. Hasil tersebut sejalan dengan Penelitian yang dilakukan oleh Widyastuti (2010) yang juga
menentukan flavonoid total dengan
menggunakan kurva baku kuersetin
memperoleh nilai koefisien korelasi (r) sebesar 0,999. Data hasil %RSD yang diperoleh untuk penelitian ini yaitu 2-7%, yang mana hasil ini sudah memenuhi syarat %RSD menurut
Gonzales et.al (2010) sehingga dapat
disimpulkan bahwa syarat validitas telah terpenuhi. Selanjutnya persamaan regresi tersebut digunakan untuk penentuan.
Kadar falvonoid total yang terukur dari ekstrak kasturi dengan 3 variasi konsentrasi yang berbeda sebagaimana pada Tabel 1.
y = 0,005x - 0,066 R = 0,999 0.000 0.100 0.200 0.300 0.400 0.500 0.600 0.700 0.800 40 50 60 70 80 90100110120130140150 A b sor b an si Konsentrasi
155 Tabel 1. Hasil pengukuran kadar flavonoid total
Kasturi Ekstrak
Kasturi
Rerata Kadar Flavonoid Total (% b/b)
30 % 1,64
50 % 2,60
70 % 3,50
Spektrum FTIR Ekstrak Bungur
Pola spektrum FTIR bungur merupakan pola spektrum sidik jari yang dihasilkan dari serapan vibrasi dari seluruh konstituen yang ada
dengan beragam metabolit sekundernya
(Nauman, 1998). Berikut spektrum FTIR Kasturi yang dihasilkan dari pengukuran menggunakan FTIR ABB Horizon MB 2000
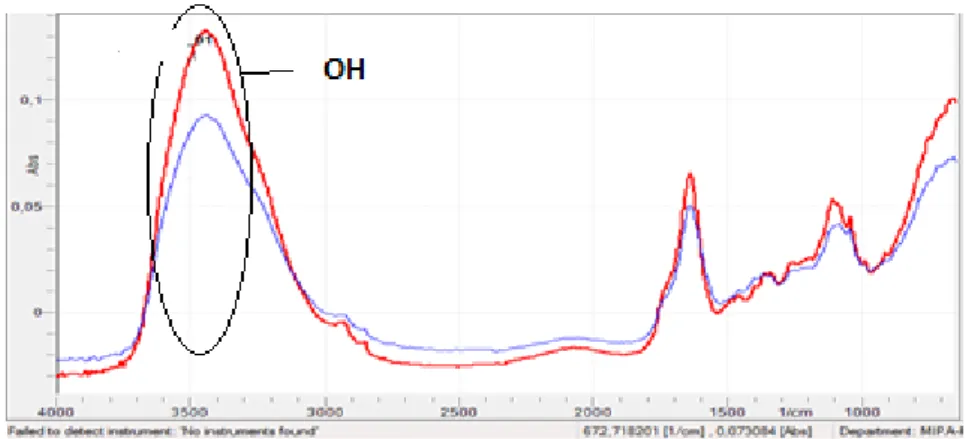
Berdasarkan hasil spektra FTIR
menunjukkan bahwa masing-masing ekstrak memiliki profil spektra FTIR yang hampir sama pada bilangan gelombang 3300 dengan adanya gugus –OH, C=O sebagai karbonil, yang merupakan gugus utama flavonoid. (Molyneux, 2010). Puncak serapan yang cukup berbeda sangat dipengaruhi oleh konsentrasi masing-masing flavonoid hal ini juga sangat nampak khususnya di daerah sidik jari, namun perbedaan absorbansi dan kekhasan srapan konstituen yang sangat halus hanya dapat diamati dengan kemometrika (Rohman et al., 2010)
Model Prediksi Flavonoid Total Ekstrak Bungur
Kalibrasi multivariat dengan metode PLS secara otomatis akan memberikan informasi spektrum yang khusus dan relevan dengan suatu sifat kimia dari model kalibrasi pada bilangan gelombang tertentu (Van der Vort et al., 1992). Berdasarkan hal tersebut maka pemilihan bilangan gelombang didasarkan pada hasil optimasi yang memberikan hubungan yang linier
pada perubahan serapan di setiap bilangan gelombang tertentu (Triyasmono et al., 2013) Penentuan flavonoid total ekstrak bungur dengan 3 variasi konsentrasi dipilih bilangan gelombang sekitar 3300 cm-1 yang merupakan
bilangan gelombang dari serapan gugus fungsi – OH yang terikat pada senyawa flavonoid (Rohaeti dkk., 2011; Molyneux, 2010; Desmiaty, 2009). Varibel x merupakan kadar flavonoid total bungur hasil analisis dengan metode AlCl3,
sedangkan variabel y merupakan nilai absorbans pada bilangan gelombang 3300 – 3700 cm-1
spektrum FTIR bungur yang dihasilkan. Hasil prediksi PLS menunjukkan nilai koefisien determinasi R2 = 0,998 dan RMSEC = 0, 20. Hal ini
menunjukkan bahwa model kalibrasi dapat diterima dikarenakan memenuhi syarat dengan nilai koefisian determinasi yang tinggi dan galat yang rendah (Miller and Miller, 2010; Baranska et al., 2005). Plot regersi dapat dilhat pada Gambar 4.
Kesahihan model yang terbentuk diuji dengan metode validasi silang. Teknik sangat
bermanfaat untuk menentukan jumlah
komponen yang optimum dari jumlah contoh yang sedikit secara independen (Stchur et al., 2002). Berdasarkan hasil validasi silang dalam menentukan keakuratan dan ketilitian model yang terbentuk dihasilkan nilai R2 = 0,995
dengan RMSEP = 0,831 seperti halnya pada plot validasi pada Gambar 5.
Plot regresi validasi menunjukkan mutu model yang dikembangkan berhasil dengan baik. Model yang baik akan menghasilkan titik-titik yang berdekatan sepanjang garis regresi dengan nilai slope mendekati 1 serta nilai kalibrasi dan nilai validasi yang saling berdekatan (Naes et al., 2002) selain itu nilai R2 yang besar dan RMSEP
156
model yang dikembangkan dapat diterima (Miller and Miller., 2010)
Pengembangan metode analisis
flavonoid total menghasilkan simpulan bahwa aplikasi metode FTIR yang dikombinasikan
dengan kemometrika PLS dapat memberikan alternativ kecepatan dalam analisis, yang mana saat ini perkembangan obat berbasis bahan alam semakin pesat.
Gambar 3. Spektra FTIR Ekstrak Bungur
Gambar 4. Plot regresi PLS total flavonoid bungur
Gambar 5. Plot validasi prediksi total flavonoid Bungur
KESIMPULAN
Metode Spektrum FTIR yang dikombinasikan dengan Kemometrika PLSR dapat digunakan sebagai alternatif penentuan flavonoid total
dengan suatu model prediksi kadar flavonoid total y = 0,979 TF (Kasturi) + 0,065, R2 kalibrasi
= 0,998, RMSEC = 0, 20, R2 validasi = 0,995, RMSEP = 0,831. R² = 0.9958 0 1 2 3 4 0 1 2 3 4
157 DAFTAR PUSTAKA
Baranska, M., Schulz., Siuda, R., Strehle, M.H Rosch, P., Popp, J., Jouber and E., Manly, M., 2005, Quality Qontrol of Harpagophytum procumbens and Its Related Phtyopharmaceutical Products by Means of NIR-FT Raman Spectroscopy, Biopolymers, 77: 1-8. Davies, A. M. C., 1998, Cross Validation: Do We Love It
Too Much?, Spectrosc. Eur., 10: 24-25.
Desmiaty, Y., J. Ratnawati, & P. Andini. 2009. Penentuan Jumlah Flavonoid Total Ekstrak Etanol Daun Buah Merah (Pandanus conoideus Lamk.) Secara
Kolorimetri Komplementer. Dipresentasikan Pada
Seminar Nasional POKJANAS TOI XXXVI 13 & 14 Mei 2009, Universitas Sanata Dharma, Yogyakarta. Devika, Mohandass, Nusrath. 2013. Fourier Transform
Infra Red (FT-IR) Spectral Studies Of Foeniculum Vulgare. Int. Res. J. Pharm. 4(3) 203-206.
Dharmaraj, S., Jamaludin, A.M., Razak, H.M., Valliapan, R., Ahmad, N.A., and Ismail, Z.A., 2006, The clasification of Phylantus niruri Linn, According to Location by Infrared Spectroscopy, Vibrational
Spectroscopy, 41: 68-72
Diaz, T.G., Meras, I.D., Casas, J.S., Franco, M.F.A. 2005. Characterization of virgin olive oils according to its triglycerides and sterols composition by chemometric methods. Food Control 16: 339-347.
Ma, K, 2000. Peroxide value and Trans analyses by Fourier Transform Infra red (FTIR) Spectroscopy,
Disertation, Ph.D, Department of Food Science and
agriculture Chemistry, MacDonald Campus of MacGill University, Montreal, Canada : 9-10, 19-20 Miller, J.N., and Miller, J.C., 2010. Statistic ad
Chemometrics for Analytical Chemistry, 6th edition,
Prentice Hall, England, p 110-111, 243-244. Pavia DL, Lampman GM, Kris GS. 2009. Introduction to
Spectroscopy. 4th edition. Washington DC: Thomson
Learning Brooks/Cole.
Rohman, A., Che Man, Y,B., and Riyanto, S. 2011,
Authentication analysis of red fruit (Pandanus
Conoideus,Lam) oil using FTIR spectroscopy in
combination with chemometrics, Phytochem Anal 22 (5):462-467
Stuart, B. 2004, Infra Red Spectroscopy: Fundamental and Aplication, p.18-34. John Wiley & Sons, Ltd. Triyasmono, L., Riyanto, s., Rohman, A., 2013,
Determination of Iodine value and Acid Value of Red Fruit Oil by Infrared Spectroscopy and Multivariate Calibration, Int. Food and Reseacrh J, 20(6): 3259-3263
Van de Voort,F.R., Sedman,J., Emo, G., and Ismail, A.A. 1992. Rapid and Direct Iodine Value and Saponofication Number Determination of Fats and Oils by Attenuated Total Reflactance/Fourier Transform Infrared Spectroscopy, Journal of the