LAPORAN BIOKIMIA KI 3161
Percobaan 7
PENENTUAN ANGKA PENYABUNAN, NETRALISASI EKIVALEN DAN
GLISEROL DALAM MINYAK
Nama
: Ade Tria
NIM
: 10511094
Kelompok
: 4
Tanggal Percobaan : 19 November 2013
Tanggal Pengumpulan : 26 November 2013
Nama Asisten : Ayra Ulpiyana (20511307)
LABORATORIUM BIOKIMIA
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT TEKNOLOGI BANDUNG
PENENTUAN ANGKA PENYABUNAN, NETRALISASI EKIVALEN
DAN GLISEROL DALAM MINYAK
I. Tujuan
Menentukan angka penyabunan trigliserida dan netralisasi ekivalen dari asam lemak minyak kelapa sawit, serta menentukan gliserol melalui uji kualitatif (uji akrolein dan uji kalorimetri) pada hasil reaksi penyabunan.
II. Teori Dasar
Lipid merupakan senyawa ester antara asam lemak dan gliserol yang bersifat tidak larut dalam air, dapat diekstrak dari sel dan jaringan oleh pelarut nonpolar, seperti kloroform dan eter. Asam lemak adalah komponen unit pembangun pada hampir semua lipid. Asam lemak adalah asam organik berantai panjang yang mempunyai atom karbon dari 4 sampai 24. Asam lemak memiliki gugus karboksil tunggal dan ekor hidrokarbon nonpolar yang panjang. Hal ini membuat kebanyakan lipid bersifat tidak larut dalam air dan tampak berminyak atau berlemak (Lehninger, 1982).
Analisis lipid dalam makanan memerlukan hidrolisa, isolasi, dan karakterisasi produk. Hidrolisa lipid sederhana biasanya dilakukan dengan alkali panas (penyabunan). Konsumsi atau pemakaian alkali oleh lipid tertentu umumnya dinyatakan dalam istilah angka penyabunan yang didefinisikan sebagai banyaknya miligram KOH yang dipakai untuk penyabunan sempurna 1 gram lemak/ minyak. Hasil reaksi penyabunan suatu lemak/ minyak netral adalah gliserol dan campuran garam dari asam lemak. Asam lemak dengan berat molekul tinggi berbeda dengan garamnya tidak larut dalam air, tetapi larut dalam pelarut non-polar seperti eter.
Gambar 2.1 Reaksi Penyabunan
Perhitungan berat molekul rata-rata dari fraksi asam lemak dapat dilakukan dengan menggunakan netralisasi ekivalen sampelnya. Dalam reaksi netralisasi, setiap senyawa akan melepaskan atau menerima atom hidrogen sehingga berat ekivalen dapat ditentukan dari perbandingan massa molekul relatif (Mr) dengan banyaknya atom H yang dilepas atau diterima. Netralisasi ekivalen didefinisikan sebagai jumlah garam asam yang diperlukan untuk menetralkan satu ekivalen alkali dan dapat ditentukan sebagai berikut.
( )
III. Data Pengamatan
a) Penentuan Angka Penyabunan Massa minyak = 2,5105 gram NHCl = 0,1 N
Tabel 3.1 Hasil Titrasi Penentuan Angka Penyabunan Larutan Volume HCl (mL)
Sampel Blanko
104,2 200,2
b) Penentuan Netralisasi Ekivalen NNaOH = 0,992 N
Tabel 3.2 Hasil Titrasi Penentuan Netralisasi Ekivalen Larutan Volume NaOH (mL)
Sampel Blanko
67,2 0,4
Massa residu + erlenmeyer = 64,1265 gram Massa erlenmeyer = 62,1265 gram
Massa residu = (64,1265-62,1265) gram = 2,0000 gram
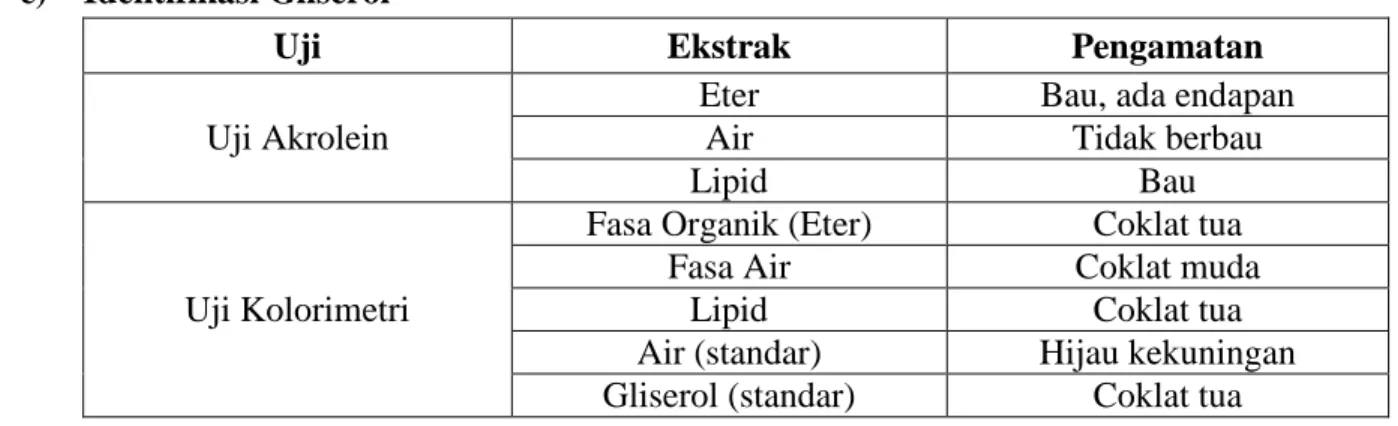
c) Identifikasi Gliserol
Uji Ekstrak Pengamatan Uji Akrolein
Eter Bau, ada endapan Air Tidak berbau
Lipid Bau
Uji Kolorimetri
Fasa Organik (Eter) Coklat tua Fasa Air Coklat muda
Lipid Coklat tua Air (standar) Hijau kekuningan Gliserol (standar) Coklat tua
IV. Pengolahan Data
a) Penentuan Bilangan Penyabunan ( ) ( ) ( ) ( ) ( ) ⁄ b) Penentuan Netralisasi Ekivalen
( ) ( ) ( )
c) Identifikasi Gliserol
Uji Ekstrak Pengamatan Hasil Uji Akrolein
Eter Bau, ada endapan + Air Tidak berbau -
Lipid Bau +
Uji Kolorimetri
Fasa Organik (Eter) Coklat tua + Fasa Air Coklat muda + Lipid Coklat tua - Air (standar) Hijau kekuningan + Gliserol (standar) Coklat tua + Keterangan : + = hasil positif (terdapat gliserol)
- = hasil negatif (tidak terdapat gliserol) V. Pembahasan
Pada percobaan dilakukan penentuan angka penyabunan minyak, penentuan netralisasi ekivalen asam lemak dari minyak kelapa sawit, serta pengujian kualitatif untuk menentukan keberadaan gliserol. Angka penyabunan diperoleh dengan menggunakan metode titrasi balik. Dari metode ini diperoleh jumlah KOH yang dikonsumsi oleh lemak dengan mentitrasi KOH berlebih (sisa dari reaksi penyabunan). Jumlah KOH total ditentukan dengan titrasi blanko sehingga jumlah KOH yang digunakan untuk proses penyabunan adalah selisih dari jumlah KOH hasil titrasi tersebut. Besar kecilnya angka penyabunan tergantung pada panjang pendeknya rantai karbon asam lemak atau dapat juga dikatakan bahwa besarnya angka penyabunan tergantung pada massa molekul lemak tersebut. Reaksi pada metode titrasi balik dituliskan sebagai berikut.
KOHsisa (aq) + HCl (aq) KCl (aq) + H2O (aq)
Pada titrasi diperoleh volume titran HCl yang digunakan adalah 104,2 mL untuk sampel dan 200,2 mL untuk blanko. Dan angka penyabunan yang diperoleh adalah 214,56mg/g lemak. Jumlah titran yang digunakan sangat banyak sehingga diperlukan pengisian titran berulang kali pada buret (50 mL). Hal ini dikarenakan besarnya konsentrasi HCl yang digunakan adalah 0,1 N. Nilai konsentrasi ini sangat kecil sehingga diperlukan jumlah HCl yang lebih banyak untuk bereaksi dengan KOH yang berlebih. Dari literatur, angka penyabunan dari minyak kelapa sawit adalah sekitar 196-205 mg/g. Bila dibandingkan dengan angka penyabunan pada percobaan diperoleh galat sekitar 5 - 9 %.
Perbedaan nilai dari angka penyabunan tersebut dapat disebabkan karena kesalahan pada proses refluks. Refluks dilakukan selama sekitar 30 menit dan waktu dihitung mulai labu bundar diletakkan di atas penangas uap. Seharusnya waktu dihitung saat air pada penangas uap mulai mendidih. Kesalahan ini membuat reaksi pada proses refluks menjadi kurang sempurna dan mempengaruhi besar angka penyabunan yang diperoleh pada percobaan.
Hasil titrasi pada penentuan angka penyabunan minyak digunakan untuk menentukan netralisasi ekivalen dari asam lemak. Proses netralisasi ekivalen dilakukan dengan mengubah sabun (garam asam lemak) menjadi asam lemak dengan menambahkan HCl pekat. Kelebihan HCl ini kemudian dititrasi dengan NaOH. Pada percobaan diperoleh volume titran NaOH yang digunakan adalah 67,2 mL untuk sampel dan 0,4 mL untuk
blanko. Dan diperoleh residu dari asam lemak adalah 1,96 gram. Hasil residu yang diperoleh ini jauh lebih kecil dari yang diharapkan. Hal ini dapat disebabkan pada proses pemisahan dengan ekstraksi. Siklus ekstraksi yang dilakukan hanya tiga kali sehingga kemungkinan pemisahan antara fasa organik (eter) dan fasa air belum sempurna.
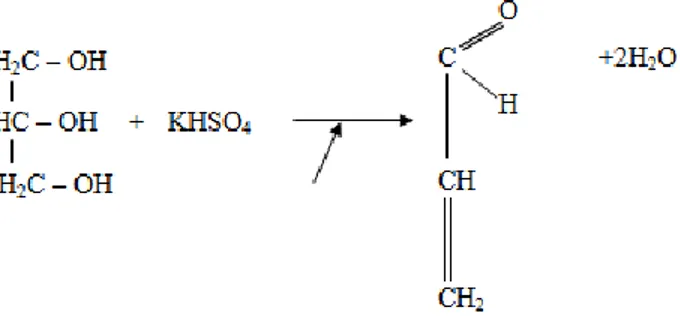
Untuk menguji keberadaan gliserol pada residu, fasa organik (eter), serta fasa air yang diperoleh dilakukan uji kualitatif yaitu uji akrolein dan uji kolorimetri. Hasil positif pada uji akrolein didasarkan pada timbulnya bau yang khas dari gliserol yang dicampurkan dengan KHSO4 kemudian dipanaskan. Pada percobaan diperoleh hasil positif pada eter dan
lipid. Hasil ini tidak sesuai dengan yang seharusnya bahwa fasa air yang menunjukkan hasil positif. Kesalahan ini dapat dikarenakan proses pemisahan dengan ekstraksi yang tidak sempurna sehingga gliserol yang seharusnya berada pada fasa air terikut ke fasa organik (eter) sehingga bau khas timbul pada eter dan lipid. Reaksi yang terjadi pada uji akrolein adalah sebagai berikut.
Uji lainnya untuk menentukan keberadaan gliserol adalah uji kolorimetri. Uji ini didasarkan pada perubahan warna dari larutan. Penambahan NaOCl pada larutan mampu mereduksi kelebihan lemak kemudian terbentuk gliseril. HCl merupakan katalis yang nantinya akan mempercepat reaksi. Pemanasan dilakukan untuk membuang kelebihan asam akibat penambahan HCl tadi. Terakhir yaitu penambahan H2SO4, penambahan ini
mampu memisahkan gugus yang terikat pada –OH sehingga gugus benzena yang terikat pada α-naftol dapat berikatan dengan gugus –OH yang ada pada gliserol. Uji dilakukan pada 5 larutan, yaitu fasa organik (eter), fasa air, lipid, air (standar), dan gliserol (standar).
Pada uji kolorimeteri, hasil positif ditandai dengan terebentuknya warna hijau zamrud. Namun pada percobaan, uji kolorimetri terhadap gliserol (standar) diperoleh larutan berwarna coklat tua sehingga warna coklat tua digunakan sebagai warna penentu hasil positif keberadaan gliserol. Pada fasa organik (eter), lipid, dan fasa air juga diperoleh hasil positif terbentuk larutan warna coklat tua pada eter dan lipid, sedangkan fasa air coklat muda. Sementara pada air (standar) diperoleh larutan berwarna hijau kekuningan. Pada uji ini seharusnya hanya fasa air dan gliserol (standar) yang menunjukkan hasil positif. Hal ini juga disebabkan dari kesalahan pada proses pemisahan dengan ekstraksi sehingga hasil yang diperoleh tidak jauh berbeda dengan hasil uji akrolein. Pada percobaan ini fasa air menunjukkan hasil positif dengan warna coklat muda sehingga dapat diartikan bahwa hanya sedikit gliserol yang berada pada fasa air. Hasil negatif diperoleh pada air (standar) karena gliserol tidak dapat larut dalam larutan polar, tetapi larut dalam senyawa nonpolar. Reaksi yang terjadi pada uji kolorimetri adalah sebagai berikut.
VI. Simpulan
Dari hasil perhitungan dan pengolahan data diperoleh bilangan penyabunan dari reaksi penyabunan adalah 214,56 mg KOH/g lemak dengan galat 5-9% dan nilai dari netralisasi ekivalen adalah 30,181 gram ekivalen. Sementara itu, untuk uji keberadaan gliserol diperoleh hasil positif pada fasa organik (eter) dan lipid dengan uji akrolein dan dengan uji kolorimetri diperoleh hasil positif pada fasa organik (eter), fasa air, lipid, dan gliserol (standar).
VII. Daftar Pustaka
Belitz, H. D. dan Grosch. 1987. Food Chemistry. Berlin: Springer-Verlag. Hlm. 129. Fessenden dan Fessenden. 1997. Dasar-Dasar Kimia Organik. Jakarta: Binarupa Aksara.
Lehninger, D. dan Michael M. Cox. 1998. Principles of Biochemistry. New York: W. H. Freeman and Company.
http://www.chem-is-try.org/materi_kimia/instrumen_analisis/titrasi-volumetri/konsentrasi-larutan-4/, diakses tanggal 23 November 2013 pukul 20.10 WIB.