Lampiran 2. Tumbuhan segar, daun segar, simplisia dan serbuk simplisia
daun bangun-bangun
Plectranhus amboinicus
(Lour.)
Tumbuhan Daun Bangun-Bangun (
Plectranthus amboinicus
(Lour.) Spreng)
Lampiran 2. (lanjutan)
Simplisia Daun Bangun-Bangun
Lampiran 3. Mikroskopik Serbuk Daun Bangun-Bangun (
Plectranthus
amboinicus
(Lour.) Spreang) Perbesaran 10x40
Keterangan:
a.
Kristal kalsium oksalat berbentuk prisma
b.
Rambut penutup uniseluler
c.
Rambut kelenjar berbentuk glandular
d.
Pembuluh kayu berbentuk spiral
e.
Stomata berbentuk diasitik
A
B
D C
Lampiran 4. Bagan Kerja Pembuatan Simplisia Daun Bangun-Bangun
Dibersihkan dari pengotor
Dicuci dengan air mengalir
Ditiriskan
Ditimbang
Dikeringkan didalam lemari pengering dengan
suhu 40-50
0C
Ditimbang
Dihaluskan dengan menggunakan blender
Daun Bangun-bangun
Berat Basah 9000 g
Berat Kering 900 g
Lampiran 5. Perhitungan Hasil Karakteristik Simplisia
Perhitungan Kadar Air Simplisia Daun Bangun-Bangun (
Plectranthus amboinicus
(Lour.) Spreng)
% kadar air
=
Volumeair (mL)Beratsampel (g)
x 100%
No.
Berat sampel (g)
Volume awal (mL)
Volume akhir (mL)
1.
5,011
1,7
2,1
2.
5,007
2,1
2,5
3.
5,025
2,5
2,9
1.
% kadar air =
2,10-1,70 (mL)5,011 (g)
x 100% = 7,98%
2.
% kadar air =
2,50-2,10 (mL)5,007 (g)
x 100% = 7,98%
3.
% kadar air =
2,90-2,50 (mL)5,025 (g)
x 100% = 6,96%
% rata-rata kadar air
=
7,98% + 7,98% + 6,96%Lampiran 6. Bagan Ekstraksi Serbuk Simplisia Secara Maserasi
900 g serbuk simplisia daun bangun-bangun
Maserat
Ditambahkan etilasetat
hingga diperoleh 100 bagian
Dibiarkan selama 2 hari
terlindung dari cahaya
Dienaptuangkan dan disaring
Dimaserasi dengan 75 bagian
n
-heksana
Dibiarkan selama 5 hari terlindungi dari cahaya sambil
sesekali diaduk
Disaring
Ampas
Ditambahkan
n
-heksana hingga diperoleh
100 bagian
Dibiarkan selama 2 hari terlindung dari cahaya
Dienaptuangkan dan di saring
Maserat
Ampas
Dimaserasi dengan 75 bagian
etilasetat
Dibiarkan selama 5 hari terlindung
dari cahaya sambil sesekali diaduk
Disaring
Maserat
Ampas
Maserat
Ampas
Dikumpulkan maserat
Dipekatkan dengan
rotary
evaporatory
Lampiran 7. Bagan Pembuatan Fraksinasi Etilasetat Daun Bangun-Bangun
Plectranthus amboinicus
(Lour.) Spreang Dengan Metode
Kromatografi Cair Vakum (KCV)
Ditambahkan dengan silikagel 10 g sedikit demi
sedikit
Diaduk hingga homogen
Dimasukkan ke dalam kolom dan di bagian atasnya
di tutup dengan kertas saring
Difraksinasi dengan KCV dengan fase diam silikagel
60H dan fase gerak dengan gradien kepolaran yang meningkat yaitu berturut-turut
n-
heksana: etilasetat (100:0), (90:10), (80:20), (70:30), (60:40), (50:50), (40:60),
(30:70), (20:80), (10:90), (0:100) dan etilasetat : metanol (80:20), (60:40),
(40:60), (20:80) dan (0:100).
Masing-masing fraksi dimonitor komponen kimianya
dengan KLT menggunakan fase diam silikagel GF
254dan fase gerak
n
-heksana :
etilasetat (7:3)
Fraksi yang memiliki profil KLT yang sama
digabung
Keterangan : * uji BSLT
Lampiran 8. Bangan Pembuatan Air Laut Buatan
2 g ekstrak etilasetat
Dilarutkan
terlebih dahulu dalam
beakerglass
Dimasukkan dalam labu tentukur 1000 mL
Ditambahkan air suling sampai 1000 mL
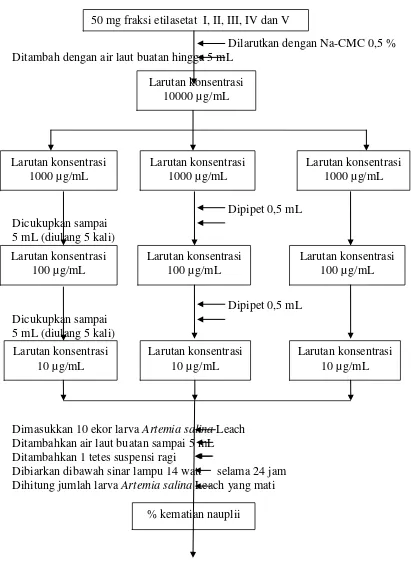
Lampiran 9. Bagan Pengujian Sitotoksik
38 gram garam
non-yodium
Dilarutkan dengan Na-CMC 0,5 %
Ditambah dengan air laut buatan hingga 5 mL
Dipipet 0,5 mL
Dicukupkan sampai
5 mL (diulang 5 kali)
Dipipet 0,5 mL
Dicukupkan sampai
5 mL (diulang 5 kali)
Dimasukkan 10 ekor larva
Artemia salina
Leach
Ditambahkan air laut buatan sampai 5 mL
Ditambahkan 1 tetes suspensi ragi
Dibiarkan dibawah sinar lampu 14 watt selama 24 jam
Dihitung jumlah larva
Artemia salina
Leach yang mati
Lampiran 10. Perhitungan Persentase Kematian
Nauplii
Perhitungan LC
50fraksi etilasetat I
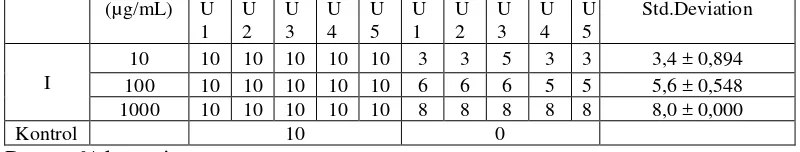
Tabel 1. Hasil pengujian BSLT fraksi etilasetat I
Fraksi Kons. Hidup awal Jumlah mati Rata-rata ±
50 mg fraksi etilasetat I, II, III, IV dan V
Larutan konsentrasi
10000 µg/mL
Larutan konsentrasi
1000 µg/mL
Larutan konsentrasi
1000 µg/mL
Larutan konsentrasi
1000 µg/mL
Larutan konsentrasi
100 µg/mL
Larutan konsentrasi
100 µg/mL
Larutan konsentrasi
100 µg/mL
Larutan konsentrasi
10 µg/mL
Larutan konsentrasi
10 µg/mL
Larutan konsentrasi
10 µg/mL
(µg/mL) U
Tes
= Jumlah kematian nauplii larutan uji
Kontrol
= Jumlah kematian nauplii larutan kontrol
Total
= Jumlah nauplii yang digunakan
% kematian (10 µg/mL) =
3,4−0Tabel 2. Perhitungan persamaan garis linier.
X
(Log konsentrasi)
Y
Perhitungan LC50 dengan nilai Y adalah 50
Y = ax + b
50 = 23 X + 10,667
X = 1,71013
Lampiran 10. (lanjutan)
Perhitungan LC
50fraksi etilasetat II
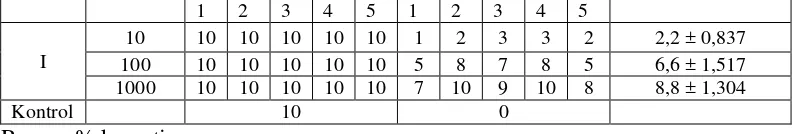
Tabel 3. Hasil pengujian BSLT fraksi etilasetat II
Fraksi Kons. (µg/mL)
Hidup awal Jumlah mati Rata-rata ±
I
Tes
= Jumlah kematian nauplii larutan uji
Kontrol
= Jumlah kematian nauplii larutan kontrol
Total
= Jumlah nauplii yang digunakan
% kematian (10 µg/mL) =
1,8−0Tabel 4. Perhitungan persamaan garis linier.
X
(Log konsentrasi)
Y
Y = ax + b
50 = 38 X - 14
X = 1,68421
Lampiran 10. (lanjutan)
Perhitungan LC
50fraksi etilasetat III
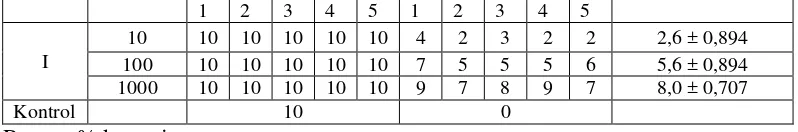
Tabel 5. Hasil pengujian BSLT fraksi etilasetat III
Fraksi Kons. (µg/mL)
Hidup awal Jumlah mati Rata-rata ±
Std.Deviation
1 2 3 4 5 1 2 3 4 5
Tes
= Jumlah kematian nauplii larutan uji
Kontrol
= Jumlah kematian nauplii larutan kontrol
Total
= Jumlah nauplii yang digunakan
% kematian (10 µg/mL) =
2,2−0Tabel 6. Perhitungan persamaan garis linier.
X
(Log konsentrasi)
Y
Perhitungan LC50 dengan nilai Y adalah 50 :
Y = ax + b
50 = 33 X -7,33
X = 1,73736
Lampiran 10. (lanjutan)
Perhitungan LC
50fraksi etilasetat IV
Tabel 7. Hasil pengujian BSLT fraksi etilasetat IV
Fraksi Kons. (µg/mL)
Hidup awal Jumlah mati Rata-rata ±
Std.Deviation
1 2 3 4 5 1 2 3 4 5
Tes
= Jumlah kematian nauplii larutan uji
Kontrol
= Jumlah kematian nauplii larutan kontrol
Total
= Jumlah nauplii yang digunakan
% kematian (10 µg/mL) =
2,6−0Tabel 8. Perhitungan persamaan garis linier.
X
(Log konsentrasi)
Perhitungan LC50 dengan nilai Y adalah 50 :
Y = ax + b
50 = 26 X + 1,33
X = 1,87192
Lampiran 10. (lanjutan)
Perhitungan LC
50fraksi etilasetat V
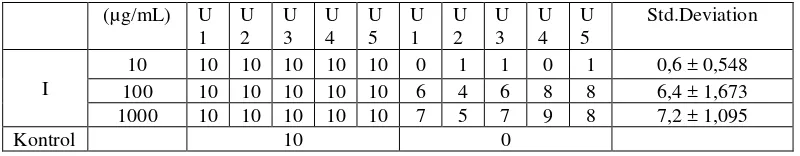
Tabel 9. Hasil pengujian BSLT fraksi etilasetat V
(µg/mL) U
Tes
= Jumlah kematian nauplii larutan uji
Kontrol
= Jumlah kematian nauplii larutan kontrol
Total
= Jumlah nauplii yang digunakan
% kematian (10 µg/mL) =
0,6−0Tabel 10. Perhitungan persamaan garis linier.
X
(Log konsentrasi)
Y
Perhitungan LC50 dengan nilai Y adalah 50 :
Y = ax + b
Lampiran 11 Perhitungan Statistik Fraksi Etilasetat I
Descriptives
JumlahKematianNauplii
N Mean
Std. Deviation
Std. Error
95% Confidence Interval for Mean
Minimum Maximum Lower
Test of Homogeneity of Variances
Post Hoc Tests
Multiple Comparisons
Dependent Variable:JumlahKematianNauplii
(I)
95% Confidence Interval
*. The mean difference is significant at the 0.05 level.
JumlahKematianNauplii
Konsentrasi N
Subset for alpha = 0.05
Means for groups in homogeneous subsets are displayed.
Perhitungan Statistik Fraksi Etilasetat II
95% Confidence Interval for Mean
Minimum Maximum Lower
Post Hoc Tests
Multiple Comparisons
Dependent Variable: Jumlah Kematian Nauplii
(I) konsentrasi (J)
*. The mean difference is significant at the 0.05level.
Homogeneous Subsets
JumlahKematianNauplii
konsentrasi N
Subset for alpha = 0.05
Means for groups in homogeneous subsets are displayed.
Perhitungan Statistik Fraksi Etilasetat III
Descriptives
JumlahKematianNauplii
N Mean
Std. Deviation
Std. Error
95% Confidence Interval for Mean
Minim
Test of Homogeneity of Variances Jumlah Kematian Nauplii
Levene
Statistic df1 df2 Sig.
1.555 2 12 .251
ANOVA Jumlah Kematian Nauplii
Post Hoc Tests
Multiple Comparisons Dependent Variable: Jumlah Kematian Nauplii
(I)
95% Confidence Interval
*. The mean difference is significant at the 0.05 level.
Homogeneous Subsets Jumlah Kematian Nauplii
Konsentrasi N
Subset for alpha = 0.05
Means for groups in homogeneous subsets are displayed.
Perhitungan Statistik Fraksi Etilasetat IV
95% Confidence Interval for Mean
Minimum Maximum Lower
Test of Homogeneity of Variances Jumlah Kematian Nauplii
Levene
Statistic df1 df2 Sig.
.848 2 12 .453
ANOVA Jumlah Kematian Nauplii
Sum of
Squares df Mean Square F Sig.
Between Groups 73.200 2 36.600 52.286 .000
Within Groups 8.400 12 .700
Post Hoc Tests
Multiple Comparisons Dependent Variable:Jumlah Kematian Nauplii
(I)
95% Confidence Interval
*. The mean difference is significant at the 0.05 level.
Homogeneous Subsets Jumlah Kematian Nauplii
Konsentrasi N
Subset for alpha = 0.05
Means for groups in homogeneous subsets are displayed.
Perhitungan Statistik Fraksi Etilasetat V
Descriptives
Jumlah Kematian Nauplii
N Mean
Std. Deviation
Std. Error
95% Confidence Interval for Mean
Minimum Maximum Lower
Bound
Upper Bound
10 µg/ml 5 .60 .548 .245 -.08 1.28 0 1
100 µg/ml 5 6.40 1.673 .748 4.32 8.48 4 8 1000 µg/ml 5 7.20 1.095 .490 5.84 8.56 6 9
Total 15 4.73 3.240 .836 2.94 6.53 0 9
Test of Homogeneity of Variances
Jumlah Kematian Nauplii
Levene
Statistic df1 df2 Sig.
Post Hoc Tests
Multiple Comparisons
Dependent Variable:Jumlah Kematian Nauplii
(I)
95% Confidence Interval *. The mean difference is significant at the 0.05 level.
Homogeneous Subsets Jumlah Kematian Nauplii
konsentrasi N
Subset for alpha = 0.05
Data Statistik
Fraksi Etilasetat Daun Bangun-Bangun I
Confidence LimitsProbabil ity
95% Confidence Limits for Konsentrasi
95% Confidence Limits for log(Konsentrasi)a
Estimate
Lower Bound
Upper
Bound Estimate
Data Statistik
Fraksi Etilasetat Daun Bangun-Bangun II
Confidence LimitsProbabil ity
95% Confidence Limits for konsentrasi
95% Confidence Limits for log(konsentrasi)a
Estimate
Lower Bound
Upper
Bound Estimate
Data Statistik
Fraksi Etilasetat Daun Bangun-Bangun III
Confidence Limits
Probabil ity
95% Confidence Limits for konsentrasi
95% Confidence Limits for log(konsentrasi)a
Estimate
Lower Bound
Upper
Bound Estimate
Data Statistik
Fraksi Etilasetat Daun Bangun-Bangun IV
Confidence Limits
Proba
bility
95% Confidence Limits for konsentrasi
95% Confidence Limits for
log(konsentrasi)a
Estimate
Lower
Bound
Upper
Bound Estimate
Data Statistik
Fraksi Etilasetat Daun Bangun-Bangun V
Confidence LimitsProba bility
95% Confidence Limits for konsentrasi
95% Confidence Limits for log(konsentrasi)a
Estimate
Lower Bound
Upper
Bound Estimate