SCREENING FITOKIMIA DAN PEMBUATAN SEDIAAN KAPSUL DAUN KATUK (Sauropus andrygynus)
Hilda Amalia (13.069), Ribut Dina Makela Juba, Ingrid Emilia Ranggajawa, Adi Suprayitno, Kharisma Aulia, Agnesia Cini, Heribertus Kurniawan Janggur
Ringkasan
Beberapa penelitian sebelumnya menyatakan adanya suatu senyawa steroid yang terdapat di dalam daun katuk yang dapat dijadikan obat kontrasepsi pria. Praktikum ini bertujuan
untuk memastikan adanya senyawa steroid melalui screening fitokimia dan membuatnya sebagai suatu sediaan obat. Metode ekstraksi yang digunakan adalah ekstraksi soxhletasi.
Hasil ekstrak cair yang diperoleh adalah 200 ml dan ekstrak kental 9,75 g. Dari hasil screening yang dilakukan dinyatakan bahwa daun katuk positif mengandung alkaloid, flavonoid, saponin, dan steroid. Hasil uji mutu sediaan yang dilakukan menyatakan bahwa sediaan kapsul yang telah dibuat memenuhi standar keseragaman bobot.
PENDAHULUAN
Indonesia merupakan suatu Negara berkembang dengan jumlah penduduk yang cukup tinggi. Tingkat jumlah penduduk yang besar merupakan salah satu penyebab timbulnya banyak masalah. Gejala nyata yang sedang dihadapi adalah angka kelahiran yang tidak bisa terkendali, yang mana angka kelahiran lebih besar dibandingkan angka kematian setiap tahunnya. Hal ini merupakan salah satu pemicu meningkatnya angka kemiskinan dan kriminalitas di Indonesia. Dalam mengatasi masalah ini pemerintah telah mencanangkan program keluarga berencana (KB). Dalam program ini yang lebih ambil alih adalah kaum wanita. Kaum wanita melakukan program KB tersebut dengan beberapa cara seperti meminum obat KB, melakukan spiral, dan beberapa hal lainnya yang dapat menghambat terjadinya ovulasi. Sedangkan partisipasi kaum pria dalam program KB masih sangat kurang sekali, yang dikarenakan karena alat kontasepsi bagi para pria masih kurang. Sejauh ini alat kontrasepsi laki – laki yang telah dikembangkan adalah kondom
dan beberapa obat yang berfungsi sebagai penghambat aktivitas spermatozoa dan menghentikan proses spermatogenesis pada pria tanpa menghilangkan libido dan tingkah laku seksual. Namun jumlah obat kontrasepsi yang ada masih sedikit selain itu masih kurangnnya sosialisasi program KB bagi kaum pria.
spermatozoa dan menghentikan proses spermatogenesis. Hal ini diperkuat dengan percoban yang telah dilakukan pada tikus. Jika jumlah steroid di dalam tubuh tikus meningkat dapat menghambat aktivitas kelenjar hipotalamus dan aktivitas kelenjar hipofise, sehingga menimbulkan efek umpan balik negative terhadap hipotalamus dan akhirnya dapat mempengaruhi mutu spermatozoa. Hal ini akan menyebabkan terganggunya hubungan antara hipotalamus, hipofise dan testis yang menyebabkan terjadinya hambatan pada sekresi hormone Follicle Stimulating Hormon (FSH) dan Luteinizing Hormon (LH) dari hipofise sehingga menyebabkan terjadinya gangguan proses
spermatogenesis.
Daun katuk adalah salah satu tanaman yang sering kita jumpai di sekitar kita
bahkan ada beberapa orang yang menanamnya di pekarangan rumah. Tanaman ini biasa dimakan sebagai pelengkap lalapan. Daun katuk telah banyak dikenal masyarakat sebagai pelancar ASI. Dan juga daun katuk telah dibuat menjadi beberapa obat herbal. Tapi selain itu menurut beberapa penelitian sebelumnya menyebutkan bahwa infusa daun katuk dapat menurunkan kualitas spermatozoa pada mencit/tikus. Hal ini kemungkinan karena daun katuk mengandung diantaranya Androstan-17-one, 3-ethyl-3hydroxy-5-alpha (Steroid). Sehingga kandungan steroid dalam daun katuk dan juga berdasarkan penelitian diatas maka daun katuk dapat berpotensi sebagai obat kontrasepsi bagi laki – laki.
Tujuan
1) Untuk menguji adanya senyawa steroid di dalam tanaman daun katuk dengan cara melakukan skrining fitokimia dan kromatografi lapis tipis
2) Untuk mengolah hasil ekstrak daun katuk menjadi sediaan obat
Manfaat
1) Agar mahasiswa mampu melakukan skrining fitokimia pada simplisia daun katuk 2) Agar mahasiswa mampu melakukan uji spesifik fitokimia secara KLT pada simplisia
daun katuk
3) Agar mahasiswa mampu melakukan ekstraksi soxhletasi steroid pada simplisia daun katuk
TINJAUAN PUSTAKA
Ekstraksi
Ekstraksi adalah proses pemisahan substansi dari campurannya dengan menggunakan pelarut yang sesuai. Jadi, ekstraksi adalah sediaan yang diperoleh dengan cara ekstraksi tanaman obat dengan ukuran partikel tertentu dan menggunakan medium pengekstraksi yang tertentu pula.
Ada beberapa factor yang harus diperhatikan dalam proses ekstraksi yaitu:
1) Sebelum simplisia diproses harus diyakini betul bahwa simplisia yang akan diekstraksi adalah simplisia yang benar dan sesuai serta telah disetujui oleh bagian jaminan mutu.
2) Selanjutnya simplisia dihaluskan ukurannya sesuai dengan ketentuan buku acuan atau spesifikasi produk untuk ekstraksi
3) Untuk ekstraksi ini ada 3 kelompok serbuk, yaitu serbuk berukuran kasar, serbuk berukuran sedang, dan serbuk berukuran halus
4) Persiapan ekstraksi, biasanya simplisia direndam dengan pelarut yang akan digunakan untuk penyarian selama 8 – 48 jam. Semakin keras simplisia, semakin lama waktu yang diperlukan.
Tipe – tipe ekstraksi ada beberapa, yaitu: 1) Ekstraksi padat-cair
Ekstraksi padat-cair ini biasa digunakan untuk melarutkan zat yang dapat larut dari campurannya dengan zat padat yang tidak dapat larut.
2) Ekstraksi cair-cair
Ekstraksi cair-cair ini biasa digunakan untuk memisahkan dua zat cair yang saling bercampur, dengan menggunakan pelarut yang dapat melarutkan salah satu zat.
Soxhletasi
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ektraksi kontiniu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
Prinsip :ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontiyu dengan jumlah pelarut konstan dengan adanya pendingin balik.
Kerugian : karena pelarut didaur ulang ekstrak yang terkumpul pada wadah di sebelah bawah terus-menerus dipanaskan sehingga dapat menyebabkan reaksi peruraian oleh panas, jumlah total senyawa-senyawa yang diekstraksi akan melampaui kelarutannya dalam pelarut tertentu sehingga dapat mengendap dalam wadah dan membutuhkan volume pelarut yang lebih banyak untuk melarutkannya, bila dilakukan dalam skala besar, mungkin tidak cocok untuk menggunakan pelarut dengan titik didih yang terlalu tinggi.
Ekstraksi steroid secara umum
Steroid merupakan golongan senyawa yang sebagian besar bersifat nonpolar, maka ekstrasinya biasanya juga menggunakan pelarut nonpolar misalnya n-heksana atau
petroleum eter. Dapat juga digunakan pelarut methanol atau etanol terlebih dahulu sebagai pelarut universal kemudian setelah diperoleh ekstrak dilanjutkan dengan ekstraksi partisi menggunakan pelarut nonpolar. Jika yang akan diisolasi adalah senyawa steroid yang terikat dengan gugus gula, maka ekstrak dilakukan dengan menggunakan pelarut semipolar atau bahkan pelarut polar tergantung dari gugus gula yang terikat. Ekstraksi steroid dapat dilakukan baik dengan pemanasan (soxhletasi) maupun tanpa pemanasan (maserasi pada suhu kamar). (Alfinda Novi kristati, 2008)
Kromatografi
Kromatografi adalah suatu nama yang diberikan untuk teknik pemisahan tertentu. Ada banyak teknik pemisahan tetapi kromatgrafi merupakan teknik paling banyak digunakan. Kebanyakan pemisahan kromatografi rutin dari suatu campuran dikerjakan dalam beberapa menit dengan peralatan yang relatif sederhana ( Nirwana, 1995 ).
Pada dasarnya semua cara kromatografi menggunakan 2 fase, yaitu fase diam (stationary) dan fase gerak (mobile). Pemisahan-pemisahan tergantung pada gerakan relative pada 2 fase tersebut. Gerakan fase gerak menyebabkan perbedaan migrasi dari penyusun cuplikan. Inilah yang dipakai sebagai dasar pemisahan kromatografi. Tanpa perbedaan dalam kecepatan migrasi dari dua senyawa tidak mungkin terjadi pemisahan.
Keuntungan Kromatografi
Kromatografi Lapis Tipis
Kromatografi Lapis Tipis (KLT) merupakan cara pemisahan campuran senyawa menjadi senyawa murninya dan mengetahui kuantitasnya yang menggunakan. Kromatografi juga merupakan analisis cepat yang memerlukan bahan sangat sedikit, baik penyerap maupun cuplikannya.
KLT dapat dipakai dengan dua tujuan. Pertama, dipakai selayaknya sebagai metode untuk mencapai hasil kualitatif, kuantitatif atau preparatif. Kedua, dipakai untuk menjajaki sistem pelarut dan sistem penyangga yang akan dipakai dalam kromatografi kolom atau
kromatografi cair kinerja tinggi (Gritter et al, 1991).
KLT dapat digunakan untuk memisahkan senyawa – senyawa yang sifatnya hidrofobik
seperti lipida – lipida dan hidrokarbon yang sukar dikerjakan dengan kromatografi kertas. KLT juga dapat berguna untuk mencari eluen untuk kromatografi kolom, analisis fraksi yang diperoleh dari kromatografi kolom, identifikasi senyawa secara kromatografi dan isolasi senyawa murni skala kecil. Pelarut yang dipilih untuk pengembang disesuaikan dengan sifat kelarutan senyawa yang dianalisis. Bahan lapisan tipis seperti silika gel adalah senyawa yang tidak bereaksi dengan pereaksi – pereaksi yang lebih reaktif seperti asam sulfat. Data yang diperoleh dari KLT adalah nilai Rf yang berguna untuk identifikasi senyawa. Nilai Rf untuk senyawa murni dapat dibandingkan dengan nilai Rf dari senyawa standar. Nilai Rf dapat didefinisikan sebagai jarak yang ditempuh oleh senyawa dari titik asal dibagi dengan jarak yang ditempuh oleh pelarut dari titik asal. Oleh karena itu bilangan Rf selalu lebih kecil dari 1,0.
Pelaksanaan KLT Fase Diam
Fase diam yang digunakan dalam KLT merupakan penjerap berukuran kecil dengan diameter partikel antara 10-30 μm. Semakin kecil ukuran rata-rata partikel fase diam dan semakin sempit kisaran ukuran fase diam, maka semakin baik kinerja KLT dalam hal efisiensi dan resolusinya.
Penjerap yang paling sering digunakan adalah silika dan serbuk selulosa, sementara
mekanisme sorpsi yang utama pada KLT adalah adsorpsi dan partisi (Gandjar & Rohman, 2007).
Fase Gerak
diatur sedemikian rupa sehingga pemisahan dapat terjadi secara optimal. Berikut adalah beberapa petunjuk dalam memilih dan mengoptimasi fase gerak :
1. Fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT merupakan teknik yang sensitif.
2. Daya elusi fase gerak harus diatur sedemikian rupa sehingga harga Rf terletak antara 0,2-0,8 untuk memaksimalkan pemisahan.
3. Untuk pemisahan dengan menggunakan fase diam polar seperti silika gel, polaritas fase gerak akan menentukan kecepatan migrasi solut yang berarti juga menentukan
nilai Rf. Penambahan pelarut yang bersifat sedikit polar seperti dietil eter ke dalam pelarut non polar seperti metil benzene akan meningkatkan harga Rf secara signifikan
(Gandjar & Rohman, 2007).
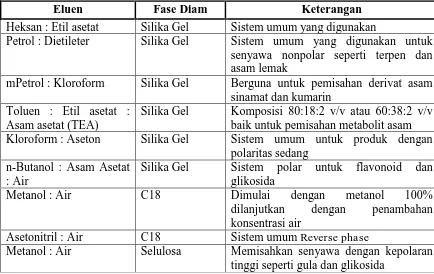
Tabel 1. Beberapa Jenis eluen dan fase diam untuk KLT
Penotolan Sampel
Untuk memperoleh roprodusibilitas, volume sampel yang ditotolkan paling sedikit 0,5 μl. Jika volume sampel yang ditotolkan lebih besar dari 2-10 μl, maka penotolan harus dilakukan secara bertahap dengan dilakukan pengeringan antar totolan (Gandjar & Rohman, 2007).
Pengembangan
Eluen Fase Diam Keterangan
Heksan : Etil asetat Silika Gel Sistem umum yang digunakan
Petrol : Dietileter Silika Gel Sistem umum yang digunakan untuk senyawa nonpolar seperti terpen dan asam lemak
mPetrol : Kloroform Silika Gel Berguna untuk pemisahan derivat asam sinamat dan kumarin
Toluen : Etil asetat : Asam asetat (TEA)
Silika Gel Komposisi 80:18:2 v/v atau 60:38:2 v/v baik untuk pemisahan metabolit asam Kloroform : Aseton Silika Gel Sistem umum untuk produk dengan
polaritas sedang
Asetonitril : Air C18 Sistem umum Reverse phase
Bila sampel telah ditotolkan maka tahap selanjutnya adalah mengembangkan sampel dalam bejana kromatografi yang sebelumnya telah dijenuhi dengan uap fase gerak. Tepi bagian bawah lempeng tipis yang telah ditotoli sampel dicelupkan kedalam fase gerak kurang lebih 0,5-1 cm. Tinggi fase gerak dalam bejana harus dibawah lempeng yang telah berisi totolan sampel.
Bejana kromatografi harus tertutup rapat dan sedapat mungkin volume fase gerak sedikit mungkin, akan tetapi harus mampu mengelusi lempeng sampai ketinggian lempeng yang telah ditentukan. Untuk melakukan penjenuhan fase gerak, biasanya bejana dilapisi dengan
kertas saring. Jika fase gerak telah mencapai ujung dari kertas saring, maka dapat dikatakan bahwa fase gerak telah jenuh (Gandjar & Rohman, 2007).
Deteksi Bercak
Deteksi bercak pada KLT dapat dilakukan secara kimia dan fisika. Cara kimia yang biasa digunakan adalah dengan mereaksikan bercak dengan suatu pereaksi melalui cara penyemprotan sehingga bercak menjadi jelas. Cara fisika yang dapat digunakan untuk menampakkan bercak adalah dengan cara pencacahan radioaktif dan fluorosensi sinar ultraviolet. Fluorosensi sinar ultraviolet terutama untuk senyawa yang dapat berfluorosensi, membuat bercak akan terlihat jelas (Gandjar & Rohman, 2007).
Deteksi senyawa dilakukan dengan menggunakan detektor UV di bawah sinar UV 254 nm, indikator pada plat KLT akan memancarkan warna hijau dan pada UV 366 nm akan memancarkan warna ungu. Komponen yang menyerap cahaya pada 254 atau 366 nm akan tampak sebagai bercak gelap pada plat yang bercahaya (Gibbons, 2006). Metode deteksi lain adalah dengan menggunakan pereaksi semprot. Pereaksi semprot yang umum digunakan dapat dilihat pada tabel 2
Tabel 2. Beberapa Jenis Pereaksi Semprot untuk KLT (Gibbons, 2006)
Pereaksi semprot Komposisi Perlakuan Keterangan
bismuth subnitrat dalam 10 mL asam asetat dan 50 mL air. Larutan tersebut diencerkan dalam 10 mL asam asetat dan 50 mL air
Screening
Skrining fitokimia merupakan analisis kualitatif terhadap senyawa – senyawa metabolit sekunder. Suatu ekstrak dari bahan alam terdiri atas berbagai macam metabolit sekunder yang berperan dalam aktivitas biologinya. Senyawa – senyawa tersebut dapat diidentifikasi dengan pereaksi – pereaksi yang mampu memberikan ciri khas dari setiap golongan metabolit sekunder (Harborne, 1987).
a. Senyawa metabolit sekunder
Menurut Judoamdjojo (1990), metabolik sekunder adalah hasil metabolisme yang disintesis oleh beberapa organisme tertentu yang tidak merupakan kebutuhan pokok untuk hidup dan tumbuh. Meskipun demikian, metabolik sekunder dapat berfungsi sebagai nutrien darurat untuk pertahanan hidup. Sedangkan menurut Herbert (1981), metabolisme sekunder merupakan senyawa yang dihasilkan organisme untuk aktivitas tertentu dan sifatnya tidak esensial untuk kehidupannya. Menurut Sastrohamidjojo (1996), bahwa metabolik sekunder adalah bahan kimia non-nutrisi yang mengontrol spesies biologi dalam lingkungan atau memainkan peranan penting dalam koeksistensi dan koevolusi spesies. Fungsi metabolit sekunder adalah untuk mempertahankan diri dari kondisi lingkungan yang kurang menguntungkan,
Menutu Harborne (1987), senyawa metabolit sekunder yang umum terdapat pada tanaman adalah : alkaloid, flavanoid, steroid, saponin, terpenoid dan tannin.
b. Identifikasi senyawa – senyawa metabolit sekunder Alkaloid
Alkaloid adalah suatu golongan senyawa yang tersebar luas hampir pada semua jenis tumbuhan. Semua alkaloid mengandung paling sedikit satu atom nitrogen yang biasanya bersifat basa dan membentuk cincin heterosiklik (Harborne, 1984).
hanya sedikit yang berupa cairan (misalnya nikotin) pada suhu kamar (Sabirin, et al.,1994).
Sifat kimia
1) Umumnya bersifat basa tergantung adanya PEB pada nitrogen
2) Alkaloid mudah terdekomposisi oleh panas dan sinar denga adanya oksigen
3) Pembentukan garamnya dengan senyawa organic maupun non dapat mencegah proses terdekomposisi
Sifat fisika
1) Isolasi alkaloid dapat membentuk Kristal dengan TL tertentu, sehingga sedikit yang berbentuk amorf dan beberapa cairan seperti nikotin dan kaniin
2) Kebanyakan alkaloid tidak berwarna kecuali, berberin (kuning) dan betanin ( merah) 3) Alkaloid dalam bentuk bebasnya mudah larut dalam pelarut organic, sedang dalam
bentuk garamnya mudah larut dalam air Cara identifikasi Alkaloid
Alkaloid dalam larutan netral atau sedikit asam jika ditambah pereaksi terbentuk endapan kristal atau amorf.
1) Dengan pereaksi Mayer (larutan Merkuri Iodida) => endapan krem
Pereaksi Mayer dibuat dengan cara senyawa HgCl2 sebanyak 1.5 gram dilarutkan dengan 60 ml aquadest. Di tempat lain dilarutkan KI sebanyak 5 gram dalam 10 ml aquadest. Kedua larutan yang telah dibuat tersebut kemudian dicampur dan diencerkan dengan aquadest sampai volume 100 ml. Pereaksi Mayer yang diperoleh selanjutnya disimpan dalam botol gelap
2) Dengan pereaksi Wagner (larutan Yodin dalam Kl) => endapan merah coklat
Pereaksi Wagner dibuat dengan cara senyawa KI sebanyak 2 gram dan iodin sebanyak 1.3 gram dilarutkan dengan aquadest sampai volumenya 100 ml kemudiaan disaring. Pereaksi Wagner ini juga harus disimpan dalam botol gelap.
3) Dengan pereaksi Dragendorf => endapan coklat kemerahan
Pereaksi Dragendorf dibuat dengan cara bismuth subnitrat sebanyak 1 gram dilarutkan
dalam campuran asam asetat glasial dan 40 ml aquadest. Di tempat lain 8 gram KI dilarutkan dalam 20 ml aquadest. Kedua larutan yang telah dibuat, dicampur kemudian diencerkan dengan aquadest sampai volumenya 100 ml.
Senyawa golongan saponin
darah merah. Saponin mempunyai toksisitas yang tinggi. Berdasarkan strukturnya saponin dapat dibedakan menjadi dua macam yaitu saponin yang mempunyai rangka steroid dan saponin yang mempunyai rangka triterpenoid. Berdasarkan pada strukturnya saponin akan memberikan reaksi warna yang karakteristik dengan pereaksi Liebermann-Buchard (LB). (Harborne, 1987)
Steroid
Steroid merupakan suatu golongan terpenoid yang mengandung inti siklopentana perhidrofenantren, yaitu 3 cincin sikloheksana dan sebuah cincin siklopentana. Contoh
steroid antara lain zoosterol, fitosterol, mikosterol, dan marinesterol. Senyawa steroid memiliki kerangka dasar triterpena asiklik.
Sifat kimia steroid
1) senyawa yang memiliki kerangka dasar triterpena asiklik 2) sistem empat cincin yang tergabung
3) Cincin A, B, dan C beranggotakan enam atom karbon dan cincin D beranggotakan lima.
4) Senyawa tidak jenuh (rantai terbuka ataupun siklik)
5) Isoprenoid kebanyakan berbentuk kiral dan terjadi dalam dua bentuk enantiomer Sifat fisika steroid
1) Dalam keadaan segar merupakan cairan tak berwarna, tetapi jika teroksidasi warnanya akan menjadi gelap
2) Mempunyai bau khas 3) Indeks bias tinggi
4) Sebagian besar bersifat optis aktif
5) Kerapatan umumnya lebih rendah daripada air 6) Tahan pada suhu 140°C - 180°C
Identifikasi senyawa golongan terpenoid dan steroid dilakukan dengan menggunakan pereaksi Liebermann-Burchard. Jika positif steroid makan akan memberikan warna hijau – biru. (Harboene, 1987)
Pereaksi Lieberman – burchard dengan 5 ml anhidrida asam asetat dicampur secara hati-hati dengan 5 ml asam sulfat pekat, kemudian campuran ini ditambahkan juga secara hati-hati ke dalam 50 ml etanol absolut. Setiap campuran zat dilakukan dengan pendinginan .
Identifikasi senyawa golongan antraquinon
Antraquinon merupakan suatu glikosida yang di dalam tumbuhan biasanya terdapat sebagai turunan antrakuinolon terhidloksilasi, termitilasi, atau terkarboksilasi.
Antraquinolon berikatan dengan gula sebagai O-glikosida atau sebagai C-glikosida. Turunan antraquinolon umumnya larut dalam air panas atau dalam alcohol encer. Senyawa Antraquinolon dapat bereaksi dengan basa memberikan warna ungu atau hijau. (Harborne, 1987).
Flavonoid
Sifat kimia flavonoid
1) Flavonoid adalah senyawa yang terdiri dari C6– C3– C6
2) Gugus gula besenyawa pada satu atau lebih grup hidroksil fenolik
3) Gugus hidroksil selalu terdapat pada karbon nomor 5 dan nomor 7 pada cincin A 4) Pada cincin B gugusan hidroksil atau alkoksil terdapat pada karbon nomor 3 dan
nomor 4.
5) Mengandung system aromatic yang terkonyugasi 6) Senyawa polar
Sifat fisika flavonoid 1) larut dalam air.
2) Memiliki warna yang berubah bila ditambahkan basa atau ammonia.
Cara identifikasi flavonoid
Identifikasi senyawa flavonoid dilakukan dengan menggunakan pereaksi Willstater/Sianidin. Adanya flavonoid ditandai dengan warna merah, orange dan hijau tergantung pada struktur flavonoid yang terkandung dalam sampel. (Fitokimia, 2008) Tanin
astringent dari tannin menyebabkan rasa kering dan puckery (kerutan) di dalam mulut setelah mengkonsumsi teh pekat, anggur merah atau buah yang mentah. Dekstruksi atau modifikasi tannin selama ini berperan penting dalam pengawet kayu, adsorben logam berat, obat-obatan, antimikroba dll. Tannin merupakan senyawa phenol yang larut dalam air dan memiliki berat molekul antara 500 dan 3000 Da. Tannin diklasifikasikan menjadi hydrolyzable tannin dan condensed tannins (proanthocyanidins). Tanin dapat dimanfaatkan sebagai adsorbent logam berat, antimikroba, dan Plywood Adhesive.
Sifat-sifat Tannin Tumbuhan
Menurut Browning (1966) sifat utama tannin tumbuh-tumbuhan tergantung pada
gugusan phenolik-OH yang terkandung dalam tannin, dan sifat tersebut secara garis besar dapat diuraikan sebagai berikut:
Sifat Kimia Tannin
1) Tannin memiliki sifat umum, yaitu memiliki gugus phenol dan bersifat koloid, sehingga jika terlarut dalam air bersifat koloid dan asam lemah.
2) Umumnya tannin dapat larut dalam air. Kelarutannya besar dan akan meningkat apabila dilarutkan dalam air panas. Begitu juga tannin akan larut dalam pelarut organik seperti metanol, etanol, aseton dan pelarut organik lainnya.
3) Tannin akan terurai menjadi pyrogallol, pyrocatechol dan phloroglucinol bila dipanaskan sampai suhu 210oF-215oF (98,89oC-101,67oC)
4) Tannin dapat dihidrolisa oleh asam, basa, dan enzim.
5) Ikatan kimia yang terjadi antara tannin-protein atau polimer-polimer lainnya terdiri dari ikatan hidrogen, ikatan ionik, dan ikatan kovalen.
Sifat Fisik Tannin
1) Umumnya tannin mempunyai berat molekul tinggi dan cenderung mudah dioksidasi menjadi suatu polimer, sebagian besar tannin bentuknya amorf dan tidak mempunyai titik leleh.
2) Tannin berwarna putih kekuning-kuningan sampai coklat terang, tergantung dari
sumber tannin tersebut.
3) Tannin berbentuk serbuk atau berlapis-lapis seperti kulit kerang, berbau khas dan mempunyai rasa sepat (astrigent).
4) Warna tannin akan menjadi gelap apabila terkena cahaya langsung atau dibiarkan di udara terbuka.
Cara identifikasi tanin
1) Sampel ditambahkan air panas dan didihkan selama 5 menit
2) Setelah dingin disaring, filtrate dibagi 2, masing-masing ditambahkan FeCl3 1% dan gelatin 10%
3) Bila positif akan berwarna hijau/biru
Kapsul
Kapsul dapat didefinisikan sebagai bentuk sediaan padat, dimana satu macam bahan obat atau lebih dan/atau bahan inert lainnya yang dimasukkan ke dalam cangkang atau wadah
kecil yang umumnya dibuat dari gelatin yang sesuai. Tergantung pada formulasinya kapsul dari gelatin bisa lunak dan bisa juga keras. Kebanyakan kapsul – kapsul yang diedarkan di
pasaran adalah kapsul yang semuanya dapat ditelan oleh pasien, untung keuntungan dalam pengobatan. Begitu pula, kapsul dapat dibuat untuk disisipkan ke dalam rectum sehingga obat dilepaskan dan diabsorbsi di tempat tersebut, atau isi kapsul dapat dipindahkan dari cangkang gelatin dan digunakan sebagai pengukur yang dini dari obat – obat bentuk serbuk. (Ansel, 1989)
METODE PENGUJIAN Alat dan Bahan
Alat – alat yang dibutuhkan adalah gunting, oven, tabung reaksi, botol, Bunsen, kaki tiga, batang pengaduk, alat soxhletasi, bejana kromatografi, kertas saring, silica gel, pinset, pensil, cawan penguap, lampu spiritus, kawat kasa, kertas perkamen, timbangan, gelas ukur, Erlenmeyer, kertas saring, water bath
Bahan-bahan yang dibutuhkan adalah simplisia daun katuk, etanol, pereaksi Mayer, pereaksi Dragendorf, pereaksi Lieberman burchard, pereaksi Wagner, n-heksan, logam Mg, asam klorida 2%, NaOH 1%, FeCl3 1%, Gelatin 10%, Asam sulfat 2 N, Kloroform berammonia, dan kloroform.
Pembuatan Simplisia
1) Dilakukan pemanenan daun katuk dari tanaman liar dipekarangan rumah.
2) Diambil daun katuk yang tidak terlalu tua dengan menggunakan tangan atau gunting
3) Dilakukan penyortiran basah (dipilih yang layak untuk dibuat simplisia) 4) Dicuci menggunakan air mengalir menggunakan teknik pencucian bertingkat 5) Dikeringkan menggunakan sinar matahari atau di oven dengan suhu 25°C-30° 6) Setelah kering dilakukan penyortiran kering (dipilih simplisia yang bebas dari
benda-benda asing atau kotoran-kotoran)
8) Diayak agar dihasilkan serbuk simplisia halus Pengujian Simplisia
Uji kadar abu
1) Ditimbang 3 g gram serbuk daun katuk 2) Dimasukkan ke dalam krus platina
3) Dibakar diatas api bunsen sampai berubah warna menjadi abu-abu 4) Dihitung kadar abunya.
Uji kadar air menggunakan metode gravimetri 1) Ditimbang bobot awal daun katuk, dicatat hasilnya
2) Ditimbang bobot daun yang telah kering atau sudah menjadi simplisia, dicatat
hasilnya
3) Dihitung kadar air dengan menggunakan rumus: � �� � − � �� ℎ��
� �� � x 100%
Screening Fitokimia a. Alkaloid
500 mg sampel dibasakan dengan kloroform berammonia, lalu disaring. Ditambahkan
0,5 – 1 ml asam sulfat 2N pada hasil filtrate, dikocok sampai terbentuk 2 lapisan. Lapisan asam (atas) dipipet dan dibagi dalam 3 tabung reaksi. Masing – masing tabung reaksi ditambahkan 2 tetes pereaksi Mayer, pereaksi Wagner, dan pereaksi Dragendorf. Kemudian diamati perubahan yang terjadi.
b. Flavonoid
5 gram sampel diekstraksi dengan pelarut n-heksana atau petrolatum eter sebanyak 15 ml, lalu disaring. Ekstrak yang diperoleh selanjutnya diekstraksi lebih lanjut menggunakan methanol atau etanol sebanyak 30 ml. 2 ml ekstrak methanol/etanol yang diperoleh dimasukkan dalam tabung reaksi dan ditambahkan dengan 0,5 HCl pekat dan 3-4 pita logam Mg. Adanya flavonoid dengan warna merah, orange dan hijau tergantung pada struktur flavonoid yang terkandung dalam sampel tersebut. (Fitokimia, 2008)
c. Antarkuinolon
asam, kemudian diekstraksi dengan benzene. Ekstrak benzene yang diperoleh diambil 5 ml dan ditambahkan dengan 5 ml ammonia, lalu dikocok. Jika terbentuk warna merah pada lapisan ammonia, maka sampel mengandung senyawa golongan Antarkuinon.
d. Tanin
Sejumlah kecil sampel dalam tabung reaksi dipanaskan di atas tangas air, kemudian disaring. Filtrate kemudian dibagi menjadi 2. Kepada filtrate 1 ditambahkan larutan gelatin 1%. Adanya senyawa tanin ditandai dengan terjadinya endapan berwarna
putih. Kepada filtrate 2 ditambahkan larutan besi (III) klorida 1%. Adanya senyawa tanin ditandai dengan terjadinya endapan berwarna hijau.
e. Saponin
Ditimbang 500 mg dimasukkan dalam tabung reaksi. Ditambahkan 10 ml air panas, dinginkan dan kemudian dikocok kuat-kuat selama 10 detik. Bila positif akan keluar busa/buih yang mantap selama 10 menit, setinggi 1 cm-10 cm. Jika ditambahkan 1 asam klorida 2 N, buih tidak hilang (MMI IV)
f. Steroid dan terpenoid
Bahan sampel tanaman sebanyak 1 gram dilarutkan dengan pelarut n-heksana atau petroleum eter (kurang lebih 2 ml), kemudian disaring. Ekstrak yang diperoleh diambil sedikit dan dikeringkan diatas papan spot test, kemudian disaring. Ditambahkan 3 tetes anhidrida asetat ( Ac2O ) dan kemudian satu tetes asam sulfat pekat (H2SO4 pekat). Adanya senyawa golongan terpenoid akan ditandai dengan timbulnya warna merah sedangkan adanya senyawa golongan steoroid ditandai dengan munculnya warna biru. (Fitokimia,2008)
Kromatografi Lapis Tipis
Dibuat ekstrak sampel dengan methanol. Dibuat eluen n-heksana:kloroform dengan perbandingan 70:30. Dimasukkan kertas saring ke dalam chamber. Eluen dimasukkan ke dalam chamber. Chamber dijenuhkan dengan eluen tersebut. Disiapkan fase diam silica gel. Ekstrak daun katuk ditotolkan pada silica gel. Setelah chamber jenuh, silica gel
dimasukkan ke dalam chamber dan kertas saring dikeluarkan dari chamber. Diamati sampai menghasilkan totolan berwarna sampai tanda batas atas silica gel. Diamati warna totolan, lalu dilihat disinar UV. Bila totolan tidak terlihat jelas maka dilakukan penyemprotan.
Ekstraksi
Simplisia daun katuk 55 g dimasukkan dalam selonsong soxhlet. Ditambahkan etanol 70% sampai bisa terjadi sirkulasi. Dilakukan ekstraksi sebanyak 16 sirkulasi. Hasil ekstrak dikumpulkan dan diupkan sampai diperoleh ekstrak kental.
Pembuatan Sediaan
Ekstrak kental dimasukkan dalam mortar hangat. Ditambahkan saccharum lactis dan digerus sampai ekstrak berubah menjadi serbuk. Setelah menjadi serbuk dimasukkan ke dalam cangkang kapsul.
Pengujian Sediaan Keseragam bobot
Ditimbang 20 kapsul daun katuk dan dicatat. Lalu ditimbang satu per satu kapsul daun katuk dan dicatat. Dikeluarkan isi tiap kapsul dan ditimbang cangkang kapsul satu persatu dan dicatat. Ditimbang serbuk/isi kapsul satu per satu dan dicatat. Diulangi sampai kapsul ke – 20. Dihitung berapa bobot isi, rata-rata, dan penyimpangannya.
HASIL DAN PEMBAHASAN Hasil Pengujian Simplisia Screening Fitokimia
Metabolit Sekunder Hasil
Alkaloid +
Flavonoid +
Antarkuinon -
Tanin -
Saponin +
Steroid +
Terpenoid -
a. Alkaloid
tanin akan terikat semakin banyak dengan kloroform dan alkaloid yang bebas semakin banyak saat diekstraksi. Hasil filtratnya ditambahkan 5 ml asam sulfat 2 N, lalu dikocok maka akan terbentuk 2 lapisan. Penambahan asam sulfat 2 N berfungsi untuk mengikat kembali alkaloid menjadi garam alkaloid dan dapat bereaksi dengan logam – logam berat, yaitu spesifik dengan alkaloid yang menghasilkan kompleks garam anorganik yang tidak larut sehingga terpisah dengan metabolic sekunder. Penambahan asam sulfat 2 N mengakibatkan larutan terbentuk menjadi 2 fase karena adanya perbedaan tingkat kepolaran antara fase aqueus yang polar dengan kloroform yang
relative kurang polar. Garam alkaloid akan larut pada lapisan atas sedangkan lapisan kloroform berada pada lapisan paling bawah karena memiliki massa jenis yang lebih
besar. Lapisan atas merupakan bagian asam. Lapisan asam ini lalu dipipet dan dibagi dalam 3 tabung reaksi. Pada tabung reaksi 1 ditambahkan 2 tetes pereaksi mayer, tabung reaksi 2 ditambahkan 2 tetes pereaksi Wagner, dan tabung reaksi 3 ditambahkan 2 tetes pereaksi Dragendorf.
Pada praktikum diperoleh hasil bahwa daun katuk positif mengandung alkaloid yang ditandai dengan adanya endapan putih saat sampel direaksikan dengan pereaksi Mayer. Diperkirakan endapan tersebut adalah kompleks kalium-alkaloid. Pada pembuatan pereaksi Mayer, larutan merkurium(II) klorida ditambah kalium iodida akan bereaksi membentuk endapan merah merkurium(II) iodida. Jika kalium iodida yang ditambahkan berlebih maka akan terbentuk kalium tetraiodomerkurat(II) (Svehla, 1990). Alkaloid mengandung atom nitrogen yang mempunyai pasangan elektron bebas sehingga dapat digunakan untuk membentuk ikatan kovalen koordinat dengan ion logam (McMurry, 2004). Pada uji alkaloid dengan pereaksi Mayer, diperkirakan nitrogen pada alkaloid akan bereaksi dengan ion logam K+ dari kalium tetraiodomerkurat(II) membentuk kompleks kalium-alkaloid yang mengendap.
Hasil positif alkaloid pada uji Wagner ditandai dengan terbentuknya endapan coklat muda sampai kuning. Diperkirakan endapan tersebut adalah kalium-alkaloid. Pada pembuatan pereaksi Wagner, iodin bereaksi dengan ion I- dari kalium iodida
menghasilkan ion I3- yang berwarna coklat. Pada uji Wagner, ion logam K+ akan membentuk ikatan kovalen koordinat dengan nitrogen pada alkaloid membentuk kompleks kalium-alkaloid yang mengendap.
reaksi hidrolisis karena garam-garam bismut mudah terhidrolisis membentuk ion bismutil (BiO+). Agar ion Bi3+ tetap berada dalam larutan, maka larutan itu ditambah asam sehingga kesetimbangan akan bergeser ke arah kiri. Selanjutnya ion Bi3+ dari bismut nitrat bereaksi dengan kalium iodida membentuk endapan hitam Bismut(III) iodida yang kemudian melarut dalam kalium iodida berlebih membentuk kalium tetraiodobismutat (Svehla, 1990). Pada uji alkaloid dengan pereaksi Dragendorff, nitrogen digunakan untuk membentuk ikatan kovalen koordinat dengan K+ yang merupakan ion logam.
b. Flavonoid
Pada uji flavonoid diperoleh hasil bahwa daun katuk positif mengandung flavonoid.
Hal ini ditandai adanya warna hijau pada saat daun katuk yang telah diekstrak dengan petrolatum eter dan methanol direaksikan dengan HCl pekat dan pita logam.
Flavonoid umumnya lebih mudah larut dalam air atau pelarut polar dikarenakan memiliki ikatan dengan gugus gula (Markham, 1988). Flavonoid terutama berupa senyawa yang larut dalam air dan senyawa aktifnya dapat diektraksi dengan etanol 70% (Harbone 1987).
Flavonoid adalah senyawa yang mengandung karbon C15 atas dua inti fenolat yang dihubungkan tiga satuan karbon cincin A yang memiliki karakteristik bentuk hidroksilasi phloroglusinal dan cincin B biasanya 4,3,4 atau 3,4,5 terhidroksilasi (Sastrohamidjojo, 1995). Sampel daun katuk sebanyak 10 gram yang telah dihaluskan diekstraksi dengan methanol. Hal ini bertujuan untuk dapat melarutkan senyawa ini, dan selanjutnya di saring untuk memisahkan filtrat dan residu. Filtrat diuapkan dan diekstraksi dengan n-heksan. Setelah itu ekstrak daun katuk dalam n-heksana diekstraksi kembali dengan etanol untuk melarutkan flavanoid dan ditambahkan dengan 0,5 g Mg. Penambahan logam Mg dan HCl untuk mendeteksi adanya senyawa flavanoid dimana flavanoid akan bereaksi dengan Mg setelah penambahan asam klorida pekat dengan terjadinya perubahan warna merah muda/ungu sebab flavanoid mengalami perubahan serapan cahaya ke arah panjang gelombang yang lebih besar
akibat adanya reaksi reduksi oleh HCl. c. Antarkuinon
menghidrolisis glikosida dan mengoksidasi antron atau antranol menjadi antrakinon. Sedangkan H2O2 3% berfungsi sebagai pemberi suasana asam. Sehingga didapatka senyawa dengan suasana netral dengan adanya penmbahan H2O2 3%. Kemudian larutan tersebut dipanaskan dan disaring. Filtrat kemudian ditambahkan asam asetat glasial 1 – 2 tetes, kemudian di ekstraksi dengan benzene. Ekstraksi bertujuan untuk menghidrolisis antrakuinon, yaitu memisahkan antara glikon dan aglikonnya. Ekstrak benzen diambil dan dibagi menjadi dua bagian, yaitu larutan 1 dan 2. Larutan 1 digunakan sebagai blanko. Larutan 2 ditambahkan ammoniak. Ammoniak berfungsi
untuk memberikan suasana basa. Warna merah atau merah muda pada lapisan alkalis menunjukkan adanaya antrakinon. Tetapi pada hasil praktikum ini tidak terjadi
perubahan warna menjadi warna merah. Hal ini menunjukkan bahwa ekstrak tidak mengandung senyawa antrakinon.
d. Tanin
Pada uji tanin menyatakan bahwa daun katuk tidak mengandung tanin. Hal ini karena pada saat filtrate simplisia daun katuk ditambahkan gelatin tidak terjadi reaksi atau perubahan apapun. Begitu juga halnya ketika filtrate ditambahkan dengan larutan besi (III) klorida 1% tidak terjadi endapan berwarna hijau pada filtrate tersebut. Pada uji tanin diperoleh hasil negative, adanya tanin akan mengendapkan protein pada gelatin. Tanin bereaksi dengan gelatin membentuk kopolimer mantap yang tidak larut dalam air (Harborne, 1996). Reaksi ini lebih sensitif dengan penambahan NaCl untuk mempertinggi penggaraman dari tanin-gelatin.
e. Saponin
Pada uji saponin menyatakan bahwa daun katuk memiliki jumlah saponin yang cukup besar. Hal ini karena pada saat sampel ditambahkan dengan air panas lalu dikocok kuat-kuat terbentuk busa yang cukup banyak setinggi ± 5 cm dan bertahan selama beberapa menit. Jika ditambahkan asam klorida 2 N, buih tersebut tidak hilang. Saponin merupakan suatu glikosida dengan gugus hidroksil pada molekulnya. Saponin mempunyai sifat seperti sabun ketika dilarutkan ke dalam air yaitu akan
Saponin adalah senyawa aktif permukaan yang dapat menimbulkan busa jika dikocok dalam air. Hal tersebut terjadi karena saponin memiliki gugus polar dan non polar yang akan membentuk misel. Pada saat misel terbentuk maka gugus polar akan menghadap ke luar dan gugus nonpolar menghadap ke dalam dan keadaan inilah yang tampak seperti busa (Robinson, 1991; Sangi dkk., 2008) f) Steroid dan terpenoid
Hasil positif steroid ditunjukkan dengan terjadinya perubahan warna menjadi hijau biru sesuai dengan pernyataan Harborne tahun 1987. Pereaksi Lieberman Burchard
asam asetat anhidrida dan asam sulfat pekat bereaksi dan menghasilkan warna hijau biru (Gambar 18). Reaksi yang terjadi antara steroid dengan asam asetat anhidrat
adalah reaksi asetilasi gugus –OH pada steroid yang akan menghasilkan kompleks asetil steroid. Penambahan asam sulfat pekat bertujuan untuk mendestruksi kompleks asetil steroid.
Kromatografi Lapis Tipis
Kromatografi lapis tipis merupakan suatu jenis kromatografi yang menggunakan fase diam dan fase gerak dalam prinsip kerjanya. Pada praktikum uji KLT simplisia daun katuk digunakan silica gel sebagai fase diam dan n-heksan dan kloroform (70:30) sebagai eluen atau fase gerak. N-heksan sebagai eluen utama karena n-heksan merupakan suatu pelarut yang dapat mengidentifikasi steroid secara spesifik karena sifatnya yang nonpolar. Sifat steroid yang nonpolar sehingga membutuhkan pelarut yang nonpolar juga agar dapat memisahkan atau mengidentifikasikan senyawa steroid dalam sampel ekstrak. Pada praktikum KLT ini diperoleh bercak berwarna kuning. Saat dilihat di sinar UV, tidak dihasilkan warna atau tanda yang jelas dan spesifik. Karena hasil yang tidak spesifik lalu hasil bercak pada silica gel disemprot dengan pereaksi warna Lieberman – Burchard yang merupakan pereaksi yang dapat mengidentifikasi adanya steroid, lalu di oven pada suhu 100°C selama 10 menit. Proses pengovenan ini untuk memperlebar pori-pori bercak pada silica gel sehingga cepat bereaksi dengan pelarut Lieberman burchaerd. Setelah dioven tidak dihasilkan warna bercak yang diinginkan, warna bercak pada silica gel menjadi rusak
dan tak teridentifikasi. Hal ini diduga karena proses semprot yang dilakukan kurang baik dan maksimal sehingga membuat warna bercak menjadi rusak bahkan hilang. Selain itu bisa juga karena kandungan steroid yang jumlahnya sedikit pada tanaman daun katuk. Ekstraksi
Ekstrak kental = 9,75 g
Ekstraksi merupakan proses penarikan suatu zat dengan pelarut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Pada praktikum ekstraksi simplisia daun katuk digunakan ekstraksi soxhletasi. Penggunaan ekstraksi sochletasi karena senyawa steroid yang diinginkan tahan terhadap suhu tinggi yaitu 140°C - 180°C, sehingga ekstraksi soxhletasi dianggap paling baik dan efektif. Pada proses ekstraksi steroid ini pelarut yang digunakan adalah etanol 70%, karena senyawa steroid dapat larut dalam pelarut etanol. Proses ekstraksi soxhletasi hanya sampai 7 sirkulasi. Hal ini seharusnya
dilakukan sebanyak 16 sirkulasi, namun karena keterbatasan waktu dan beberapa kendala maka pada sirkulasi ke 7, proses ekstraksi dihentikan.
Hasil ekstraksi Soxhlet 355 gram serbuk daun katuk dengan 480 ml etanol 70% diperoleh ekstrak encer berwarna hijau muda sebanyak 200 ml. Hasil ekstraksi ini kemudian dievaporasi diatas waterbath dengan suhu sampai 90°C dengan maksud agar senyawa etanol yang memiliki titik didih ±78°C yang terdapat pada ekstraksi menguap dan hilang, sehingga diperoleh hasil ekstraksi kental. Hasil ekstraksi kental yang diperoleh adalah sebanyak 9,76 gram, yang akan dioleh menjadi sediaan kapsul.
Mutu Fisik Sediaan No Berat
Kapsul
Berat
Cangkan g
Berat Isi Penyimpangan
1 1,1122 g 0,1198 g 0,9924 g 0,54%
2 1,1756 g 0,1197 g 1,0559 g 5,82%
3 1,0751 g 0,1192 g 0,9559 g 4,19%
4 1,1656 g 0,1208 g 1,0448 g 4,71%
5 1,0608 g 0,1192 g 0,9416 g 5,63%
6 1,1584 g 0,1193 g 1,0391 g 4,13%
7 1,1563 g 0,1193 g 1,0370 g 3,92%
8 1,1019 g 0,1195 g 0,9824 g 1,54%
10 1,1088 g 0,1193 g 0,9895 g 0,83%
No Berat Kapsul Berat Cangkang Berat Isi Penyimpangan
11 1,1388 g 0,1194 g 1,0194 g 2,16%
12 1,1437 g 0,1195 g 1,0242 g 2,64%
13 1,1618 g 0,1192 g 1,0426 g 4,48%
14 1,1137 g 0,1192 g 0,9945 g 0,33%
15 1,1354 g 0,1193 g 1,0161 g 1,83%
16 1,0772 g 0,1194 g 0,9578 g 4,01%
17 1,1030 g 0,1195 g 0,9835 g 1,43%
18 1,1287 g 0,1194 g 1,0093 g 1,15%
19 1,1102 g 0,1197 g 0,9905 g 0,73%
20 1,1462g 0,1195 g 1,0267 g 2,89%
Untuk evaluasi fisik dari sediaan kapsul daun katuk ini yaitu keseragaman bobot. Uji ini
dilakukan untuk 20 kapsul. Pertama-tama, ditimbang bobot kapsul kemudian kapsul dikeluarkan isinya dan ditimbang bobot cangkang kapsul. Penimbangan ini dilakukan hingga kapsul yang ke 20. Dari hasil uji Keseragaman bobot ini diketahui bobot 20 kapsul = 22,4653 gram, bobot 20 cangkang = 2,8057 gram. Bobot isi 20 kapsul = 19,9566 gram dan rata-rata bobot isi tiap kapsul = 0,9978 gram. Kapsul no 1-20 telah memenuhi syarat kolom A karena penyimpangan di bawah 7,5%.
Kesimpulan
dihasilkan kemudian dimasukkan dalam cangkang kapsul. Kemudian dilakukan uji keseragaman bobot kapsul dan hasil uji tersebut menyatakan bahwa sedian kapsul ini memenuhi syarat keseragaman bobot.
DAFTAR PUSTAKA
Agoes, G. (2007). Teknologi Bahan Alam. Bandung: ITB.
Alfinda Novi Kristanti, N. S. (2008). Buku Ajar Fitokimia. Surabaya: Airlangga Univercity press.
Anonim. (1985). Cara Pembuatan Simplisia. Jakarta: Departemen Kesehatan RI.
Anonim. (1986). Sediaan Galenik. Jakarta: Departemen Kesehatan Republik Indonesia.
Anonim. (1987). Analisis Obat Tradisional. Jakarta: Departemen Kesehatan RI.
Anonim. (1997). Materia Medica Indonesia jilid V. Jakarta: Departemen Kesehatan RI.
Anonim. (1997). Materia Medica Indonesia jilid VI. Jakarta: Departemen Kesehatan RI.
Fajriyah, S. (n.d.). Pembuatan Simplisia dan Standarisasi Mutu Simplisia Rimpang Temulawak
(Curcuma xanthorriza rhizoma) dengan Pengeringan Sinar Matahari.
J.B.Harborne. (1987). Metode Fitokimia: Penuntun cara modern menganalisis tumbuhan.
Bandung: ITB.
robinson, t. (1995). kandungan organik tumbuhan tinggi. bandung: ITB.
Wargono, F. E. (2013). uji efek daun katuk terhadap kualitas spermatozoa tikus putih jantan