Informasi Dokumen
- Penulis:
- Taufik Budi Prabawa
- Pengajar:
- Bapak Drs. Allwar M.Sc., Ph.D.
- Bapak Thorikul Huda, S.Si., M.Sc.
- Ibu Reni Banowati I, S.Si., M.Sc.
- Sekolah: Universitas Islam Indonesia
- Mata Pelajaran: Analisis Kimia
- Topik: Verifikasi Metode Penentuan Kadar Total Sugar As Invert Dalam Tetes Tebu Dengan Metode Lane Eynon
- Tipe: laporan praktik kerja lapangan
- Tahun: 2018
- Kota: Yogyakarta
Ringkasan Dokumen
I. PENDAHULUAN
Bagian pendahuluan ini menjelaskan latar belakang penelitian mengenai penentuan kadar Total Sugar As Invert (TSAI) dalam tetes tebu menggunakan metode Lane Eynon. Tetes tebu merupakan produk sampingan dari pengolahan gula yang memiliki kadar gula tinggi. Penelitian ini dilakukan untuk memastikan bahwa laboratorium PT. Miwon Indonesia dapat menerapkan prosedur operasi standar dan menjamin mutu hasil pengujian. Penelitian ini bertujuan untuk memverifikasi metode pengujian yang digunakan dalam penentuan TSAI.
1.1 Latar Belakang
Latar belakang penelitian ini mencakup pentingnya penentuan kadar Total Sugar As Invert dalam tetes tebu, yang merupakan produk sampingan dari industri gula tebu. Tetes tebu memiliki kandungan gula yang tinggi dan digunakan sebagai bahan baku untuk berbagai produk. Metode Lane Eynon dipilih karena kesederhanaan dan akurasinya dalam menentukan kadar gula, yang penting bagi industri seperti PT. Miwon Indonesia.
1.2 Rumusan Masalah
Rumusan masalah dalam penelitian ini mencakup dua pertanyaan utama: bagaimana hasil penentuan kadar TSAI dalam tetes tebu menggunakan metode Lane Eynon, dan bagaimana hasil verifikasi metode tersebut dalam hal presisi, akurasi, dan estimasi ketidakpastian. Pertanyaan-pertanyaan ini menjadi fokus utama dalam analisis yang dilakukan.
1.3 Tujuan
Tujuan dari penelitian ini adalah untuk mengetahui kadar TSAI dalam tetes tebu secara kuantitatif dan untuk menentukan nilai parameter verifikasi dari metode uji yang digunakan. Dengan mencapai tujuan ini, diharapkan dapat memberikan data yang valid dan dapat diandalkan untuk analisis rutin di laboratorium.
1.4 Manfaat
Manfaat dari penelitian ini adalah untuk memberikan pemahaman yang lebih baik tentang kadar TSAI dalam tetes tebu dan untuk memastikan bahwa metode yang digunakan dapat menghasilkan data yang valid. Ini sangat penting untuk menjamin kualitas bahan baku yang digunakan dalam proses produksi di PT. Miwon Indonesia.
II. DASAR TEORI
Bagian ini membahas teori dasar yang mendasari penelitian, termasuk gambaran umum PT. Miwon Indonesia, karakteristik tetes tebu, konsep total sugar as invert, metode Lane Eynon, dan pentingnya verifikasi metode. Teori-teori ini memberikan landasan untuk memahami proses analisis yang dilakukan.
2.1 Gambaran Umum PT. Miwon Indonesia
PT. Miwon Indonesia adalah perusahaan yang bergerak di bidang industri bahan tambahan makanan, khususnya monosodium glutamat (MSG). Didirikan pada tahun 1974, perusahaan ini telah berkembang pesat dan menjadi salah satu produsen MSG terkemuka di Indonesia. Lokasi pabrik berada di Gresik, Jawa Timur, dan memiliki standar tinggi dalam pengujian bahan baku.
2.2 Tetes Tebu
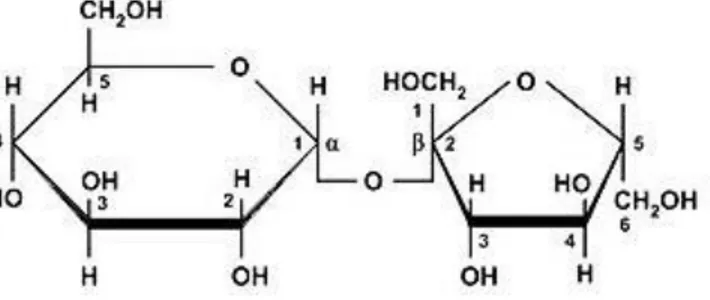
Tetes tebu adalah produk sampingan dari pengolahan gula tebu yang mengandung kadar gula tinggi. Proses pengolahan tetes tebu dimulai dengan penggilingan tebu untuk mendapatkan nira, yang kemudian dimurnikan dan dikristalisasi. Tetes tebu memiliki berbagai manfaat, termasuk sebagai bahan baku untuk etanol dan MSG. Kandungannya bervariasi, dengan sukrosa sebagai komponen utama.
2.3 Total Sugar as Invert
Total Sugar As Invert (TSAI) merupakan jumlah gula yang dihitung sebagai gula reduksi setelah proses hidrolisis. Gula pereduksi berperan penting dalam berbagai reaksi kimia, termasuk reaksi Maillard. Penentuan kadar gula pereduksi dilakukan menggunakan metode Lane Eynon, yang melibatkan titrasi dengan larutan Fehling.
2.4 Metode Lane Eynon
Metode Lane Eynon adalah metode titrasi untuk menentukan kadar gula pereduksi dalam larutan. Metode ini menggunakan larutan Fehling yang terdiri dari dua komponen, yaitu Fehling A dan B. Titrasi dilakukan hingga perubahan warna menunjukkan bahwa semua gula telah direduksi. Metode ini sederhana dan efektif untuk analisis rutin di laboratorium.
2.5 Verifikasi Metode
Verifikasi metode pengujian penting untuk memastikan bahwa metode yang digunakan dapat menghasilkan data yang valid. Proses ini melibatkan evaluasi terhadap presisi, akurasi, dan ketidakpastian pengukuran. Validasi metode merupakan elemen penting dalam kontrol kualitas dan diperlukan untuk memenuhi standar internasional.
2.5.1 Presisi
Presisi mengacu pada kedekatan hasil pengukuran dari serangkaian pengujian yang dilakukan dalam kondisi yang sama. Parameter ini dinyatakan dalam bentuk persentase relative standard deviation (%RSD). Uji presisi penting untuk mengetahui konsistensi dan keandalan metode yang digunakan dalam analisis.
2.5.2 Akurasi
Akurasi mengukur seberapa dekat hasil analisis dengan nilai yang sebenarnya. Uji akurasi dilakukan dengan menambahkan standar ke dalam sampel dan membandingkan hasilnya dengan nilai yang diharapkan. Hasil yang mendekati 100% menunjukkan bahwa metode tersebut akurat dan dapat diandalkan.
2.6 Ketidakpastian Pengukuran
Ketidakpastian pengukuran mencerminkan rentang nilai yang mungkin mencakup nilai sebenarnya dari hasil pengukuran. Penting untuk mengestimasi ketidakpastian ini agar hasil pengukuran dapat dianggap valid. Estimasi ketidakpastian melibatkan analisis berbagai komponen yang mempengaruhi hasil pengukuran.
III. METODOLOGI
Bagian metodologi menjelaskan langkah-langkah yang diambil dalam penelitian, termasuk alat dan bahan yang digunakan, serta prosedur yang diikuti untuk menentukan kadar TSAI dalam tetes tebu. Metodologi yang jelas diperlukan untuk memastikan reproduksibilitas hasil.
3.1 Alat
Alat yang digunakan dalam penelitian ini termasuk gelas beaker, neraca analitik, pipet, buret, dan waterbath. Alat-alat ini dipilih untuk memastikan bahwa proses analisis dapat dilakukan dengan akurat dan efisien. Pemilihan alat yang tepat sangat penting untuk mendapatkan hasil yang valid.
3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi larutan Fehling A dan B, larutan EDTA, dan HCl. Bahan-bahan ini diperlukan untuk melakukan titrasi dan proses hidrolisis yang akan menghasilkan gula inversi dari tetes tebu. Kualitas bahan juga mempengaruhi hasil analisis.
3.3 Cara Kerja
Prosedur kerja dimulai dengan standarisasi larutan Fehling, diikuti dengan preparasi larutan contoh TSAI. Selanjutnya, dilakukan titrasi untuk menentukan kadar TSAI dalam tetes tebu. Setiap langkah dilakukan dengan hati-hati untuk memastikan hasil yang akurat dan dapat diandalkan.
3.3.1 Standarisasi Larutan Fehling
Standarisasi larutan Fehling dilakukan dengan melarutkan sukrosa dan menambahkan HCl. Setelah proses hidrolisis, larutan dinetralkan dengan NaOH dan dititrasi untuk menentukan faktor Fehling. Proses ini penting untuk memastikan bahwa larutan Fehling yang digunakan memiliki konsentrasi yang tepat.
3.3.2 Preparasi Larutan Contoh TSAI
Larutan contoh TSAI disiapkan dengan melarutkan sampel tetes tebu dalam air suling dan menambahkan HCl untuk menghidrolisis sukrosa. Larutan kemudian dipanaskan untuk mempercepat reaksi hidrolisis. Proses ini penting untuk memastikan semua gula dalam sampel dapat terukur.
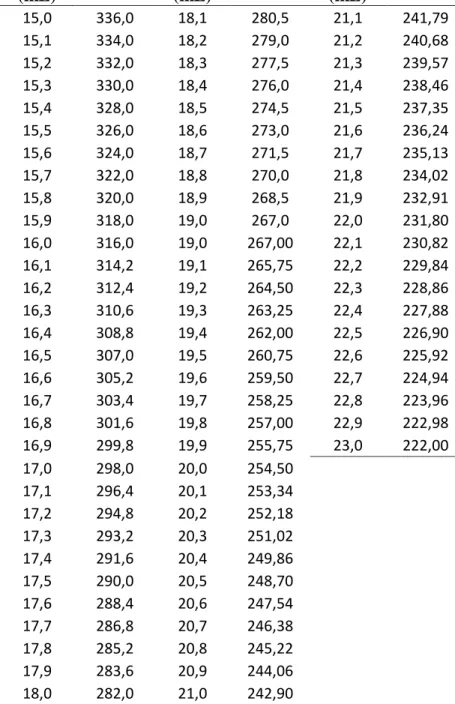
3.3.3 Penentuan TSAI Metode Lane Eynon
Penentuan TSAI dilakukan dengan menitrasi larutan contoh menggunakan larutan Fehling A dan B. Proses titrasi diakhiri saat terjadi perubahan warna, yang menunjukkan bahwa semua gula telah direduksi. Hasil titrasi digunakan untuk menghitung kadar TSAI dalam tetes tebu.
3.3.4 Penentuan Presisi
Uji presisi dilakukan dengan mengulangi titrasi menggunakan larutan contoh yang sama. Hasil dari setiap titrasi dicatat untuk menghitung nilai %RSD. Uji ini bertujuan untuk menilai konsistensi hasil analisis dan memastikan bahwa metode yang digunakan dapat diandalkan.
3.3.5 Penentuan Akurasi
Akurasi ditentukan dengan menambahkan standar glukosa ke dalam sampel dan melakukan titrasi. Hasil titrasi dibandingkan dengan nilai yang diharapkan untuk menghitung persentase recovery. Uji ini penting untuk memastikan bahwa metode yang digunakan dapat memberikan hasil yang akurat.
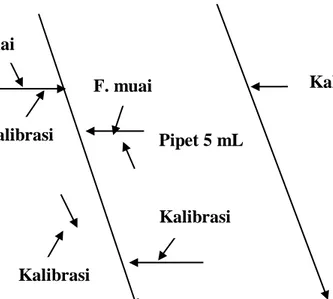
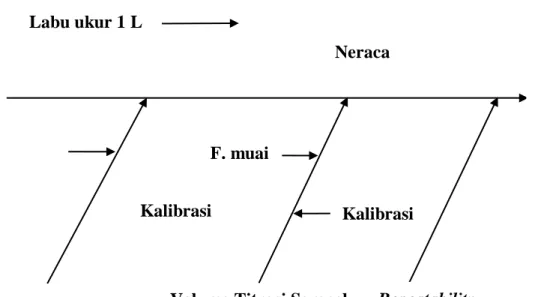
3.3.6 Penentuan Estimasi Ketidakpastian Pengukuran
Estimasi ketidakpastian dilakukan dengan menghitung nilai ketidakpastian baku, ketidakpastian gabungan, dan ketidakpastian diperluas. Proses ini penting untuk menilai seberapa valid hasil pengukuran dan untuk memahami faktor-faktor yang dapat mempengaruhi hasil tersebut.
IV. HASIL DAN PEMBAHASAN
Bagian ini menyajikan hasil dari analisis yang dilakukan serta membahas implikasi dari hasil tersebut. Hasil yang diperoleh dibandingkan dengan standar yang ditetapkan untuk menentukan apakah metode yang digunakan memenuhi kriteria yang diharapkan.
4.1 TSAI Metode Lane Eynon
Hasil penentuan TSAI menggunakan metode Lane Eynon menunjukkan bahwa kadar gula dalam tetes tebu dapat diukur secara akurat. Proses hidrolisis yang dilakukan berhasil mengubah sukrosa menjadi gula reduksi, yang kemudian dititrasi untuk menentukan kadar TSAI. Hasil ini menunjukkan bahwa metode Lane Eynon efektif untuk analisis rutin.
4.2 Standarisasi Larutan Fehling
Hasil standarisasi larutan Fehling menunjukkan bahwa faktor Fehling yang diperoleh konsisten dengan nilai yang diharapkan. Hal ini menunjukkan bahwa larutan Fehling yang digunakan dalam penelitian ini memiliki konsentrasi yang tepat, sehingga dapat digunakan untuk titrasi dengan akurat.
4.3 Penentuan Presisi
Hasil uji presisi menunjukkan nilai %RSD sebesar 0,87%, yang memenuhi kriteria akurasi yang ditetapkan. Ini menunjukkan bahwa metode yang digunakan memiliki konsistensi yang baik dan dapat diandalkan untuk analisis rutin di laboratorium.
4.4 Penentuan Akurasi
Hasil uji akurasi menunjukkan nilai recovery rata-rata sebesar 92,33%. Nilai ini menunjukkan bahwa metode yang digunakan memiliki akurasi yang baik, dengan hasil yang mendekati nilai yang diharapkan. Ini menunjukkan bahwa metode Lane Eynon dapat diandalkan untuk menentukan kadar TSAI.
4.5 Penentuan Estimasi Ketidakpastian
Estimasi ketidakpastian pengukuran menunjukkan bahwa kontribusi terbesar berasal dari pengulangan analisis. Hal ini menunjukkan pentingnya melakukan analisis secara berulang untuk mendapatkan hasil yang lebih akurat dan valid. Ketidakpastian yang diukur memberikan gambaran tentang keandalan hasil analisis.
V. KESIMPULAN DAN SARAN
Kesimpulan dari penelitian ini mencakup temuan utama mengenai keberhasilan metode Lane Eynon dalam menentukan kadar TSAI dalam tetes tebu. Saran diberikan untuk peningkatan metode dan penelitian lebih lanjut di bidang ini.
5.1 Kesimpulan
Dari hasil penelitian, dapat disimpulkan bahwa metode Lane Eynon dapat digunakan secara efektif untuk menentukan kadar Total Sugar As Invert dalam tetes tebu. Hasil analisis menunjukkan bahwa metode ini memiliki presisi dan akurasi yang baik, serta memenuhi standar yang ditetapkan.
5.2 Saran
Saran untuk penelitian selanjutnya adalah melakukan pengujian dengan variasi sampel yang lebih luas untuk memastikan konsistensi hasil. Selain itu, disarankan untuk mengeksplorasi metode lain yang mungkin lebih efisien dalam menentukan kadar gula dalam tetes tebu.