56
KARAKTERISASI SENYAWA TRITERPENOID DARI DAUN JABON (Anthocephalus cadamba (Roxb.) Miq)
Rugayah1*, Rudiyansyah1, Afghani Jayuska1
1Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi,
*email: [email protected]
ABSTRAK
Penelitian terhadap daun Jabon (Anthocephalus cadamba (Roxb.) Miq) bertujuan untuk menegtahui karate senyawa triterpenoid dari daun Jabon. Penelitian ini dilakukan dengan cara maserasi, uji fitokimia, dan kromatografi. Isolate yang diperoleh seberat 3 mg berbentuk padatan amorf putih. Isolate tersebut dianalisis dengan menggunakan spektrum 1H-NMR. Hasil dari spektrum 1H-NMR (CDCl3, 500 MHz) menunujukkan adanya 7 sinyal metil singlet
yang terletak pada pergeseran kimia (ppm) 0,75; 0,77; 0,90; 0,91; 0,98; dan 1,13. Pada pergeseran kimia menunjukkan adanya proton yang terikat pada gugus hidroksi serta pada pergeseran kimia menunjukkan adanya proton olefin. Berdasarkan analisis data 1H-NMR dan perbandingan dengan data 1H-NMR yang telah dilaporkan sesuai literature maka senyawa tersebut dapat diusulkan sebagai asam oleanolat (asam 3 -hidoksiolean-12-en-28-oat).
Kata kunci: Anthocephalus cadamba (Roxb.) Miq, asam oleanolat, triterpenoid, kromatografi
PENDAHULUAN
Tingginya keanekaragaman hayati di Indonesia dapat dijadikan sebagai bahan utam pengembangan dan penemuan berbagai senyawa kimia dari alam. Kandungan senyawa kimia dalam bahan alam tertentu dapat digunakan dalam bidang kesehatan. Berbagai tumbuhan dapat dijakan sebagai sumber obat seperti kelompok sayur-sayuran, buah-buahan, bumbu dapur dan bunga-bungaan, serta tumbuhan liar (Isa, 2008). Salah satu tanaman yang memiliki kandungan senyawa yang menarik adalah tanaman Jabon (Anthocephalus cadamba
(Roxb.) Miq).
Anthocephalus cadamba (Roxb.) Miq, yang juga dikenal dengan nama Jabon, merupakan jenis tanaman tropis yang berasal dari Asia Selatan dan Asia Tenggara termasuk Indonesia. Menurut Silk (2006), Jabon telah ditanam di Indonesia dalam skala besar sejak tahun 1930-an. Jenis ini juga telah dibididayakan di Jawa (trerutama Jawa Barat dan Jawa Timur), Kalimantan (terutama Kalimantan Selatan dan Kalimantan Timur), Sumatera
(hamper tersebar di seluruh provinsi) Sulawesi (hsmpir tersebar diseluruh provinsi), Sumbawa (Nusa Tenggara Barat dan Papua (Irian Jaya) (Martawijaya, dkk., 1989).
Di India, secara luas daun Jabon digunakan sebagai obat rakyat dalam pengobatan demam, anemia, keluhan rahim, penyakit darah, penyakit kulit, kusta, disentri, dan untuk peningkatan kualitas sperma. Daunnya direkomendasikan sebagai obat kumur dalam kasus stomatitis (sariawan) (Slkar
et al., 1992). Beberapa penelitian tentang tumbuhan Jabon menyatakan bahwa tanaman ini mengandung metabolit sekunder yang memiliki aktivitas antibakteri, antiinflamasi, antioksidan, antipiretik dan anifungal.
Penelitian kandungan kimia khususnya senyawa triterpenoid dari daun Jabon (A. cadamba (Rpxb.) Miq) belum pernah dilakukan. Oleh karena itu, dilakukan penelitian ini terhadap daun Jabon dari fraksi etil asetat guna mengetahui karakter dari senyawa
57 tritepnoid tersebut. Metode yang digunakan pada penelitian ini adalah pengolahan sampel, ekstraksi, uji fitokimia dan isolasi yang menggunakan metode kromatografi kolom. Isolate murni yang diperoleh dikarakterisasi dengan Spektrometer NMR (Nuclear Magnetic Resonance). Hasil penelitian ini diharapkan dapat mengungkapkan kandungan senyawa metabolit sekunder guna menambah referensi baru mengenai senyawa triterpenoid yang terdapat pada tanaman Jabon.
METODOLOGI PENELITIAN Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini yaitu chamber, corong pisah,
hot plate, kolom kromatografi, plat kromatografi lapis tipis, maserator, neraca analitik, 1H-NMR (500 MHz) agilent, pipet kapiler, dan seperangkat alat evaporatoe (Haidolph WB2000).
Bahan-bahan yang digunakan dalam penelitian ini yaitu asetat anhidrida, asam klorida, asam sulfat pekat, daun segar jabon, etanl, etil asetat, FeCl3 5%, kloroform, n-heksana, reagen serium sulfat 5%, serbuk Mg, silika gel 70 mesh, silica gel 200-400 mesh, silika gel G-60 dan plat KLT GF254.
Prosedur Kerja
Determinasi dan preparasi sampel Determinasi sampel yang digunakan dalam penelitian ini dilakukan di Laboratorium Biologi Fakultas MIPA Universitas Tanjungpura. Determinasi dilakukan berdasarkan pengamatan dari ciri taksonomi tumbuhan.
Daun segar A. cadamba (Roxb.) Miq yang diambil dari halaman FMIPA UNTAN dibersihkan dan digunting kecil-kecil, kemudian potongan daun ditimbang sehingga diketahui massa dari daun tersebut setelah itu dilakukan maserasi.
Ekstraksi dan partisi
Sebanyak 2 kg potongan daun segar Jabon (A. cadamba) dimaserasi dengan pelarut etanol selama 24 jam., kemudian dilakukan penyaringan. Ekstrak etanol yang diperoleh kemudian
dipekatkan menggunakan rotary evaporator.
Ekstrak etanol hasil evaporasi dilarutkan kembali dengan pelarut etanol kemudian ditambahkan air hangat setetes demi tetes sambil diaduk sampai terbentuk gumpalan. Gumpalan yang terbentuk didasar tabung dipisahkan, ekstrak kemudian disaring dan dilajutkan dengan proses partisimenggunakan n -heksana untuk memisahkan klorofil yang masih tersisa pada ekstrak etanol-air tersebut. Ekstrak etanol-air dipartisi dengan pelarut etil asetat sebanyak 3 kali dan fraksi etil asetat yang diperoleh dikeringkan sehingga diperoleh ekstrak etil asetat berwarna hijau pekat (Yulvianti, 2007).
Uji Fitokimia
Uji fitokimia dilakukan dngan pereaksi Liebermann-Burchard untuk mengidentifikasi golongan senyawa triterpenoid yang ada pada ekstrak etil asetat. Sampel diteteskan pada plat tetes kemudian ditambahkan 3 tetes asetat glasial dan 2 tetes H2SO4, sampel positif triterpenoid dengan terbentuknya warna merah (Harborne, 1987).
Kromatografi Vakum Cair
Pemisahan fraksi etil asetat yang positif senyawa triterpenoid dilakukan menggunakan kolom kaca berukuran diameter 6 cm. fasa diam yang digunakan yaitu silica gel 60 GF254. Silica gel tersebut dimasukkan ke dalam kolom dan dipadatkan menggunakan vakum. Setelah itu kolom dielusi dengan pelarut nonpolar (n-heksana).
Sebanyak 21 g sampel diimpregnasi dengan silika gel 70 mesh. Perbandingan sampel dengan silika adsorp yang digunakan dalam penelitian ini adalah 1:1. Proses fraksinasi dilakukan dengan menggunakan eluen n-heksana 100%, n -heksana : etil asetat (9:1, 9:2, 7:3, 6:4, 5:5, 4:6, 3:7, 2:8, 9:1), etil asetat 100%, dan etanol 100%. Jumlah eluen yang digunakan setiap satu kali elusi adalah 200 mL.
Fraksi-fraksi yang diperoleh dari hasil KVC diuapkan dengan cara diangin-anginkan dalam suhu ruang. Setelah kering, masing-masing fraksi ditimbang
58 untuk mengetahui beratnya. Fraksi-fraksi tersebut dianalisis dengan teknik KLT sehingga diperoleh fraksi gabungan KVC. Fraksi gabungan diperoleh selanjutnya dilakukan uji fitokimia dan ditentukan massanya.
Kromatografi kolom Flash
Kromatografi flash digunakan untuk pemisahan lanjut dari suatu fraksi sehingga diperoleh isolate murni. Kolom kromatografi flash yang digunakan berdiameter 2 cm. Fasa diam yang digunakan adalah silika gel 200-400 mesh dengan ketinggian silika kolom kira-kira 16cm. Silika gel dibuat dengan cara basah yaitu silika dibuat bubur dengan menggunakan pelarut n-heksana. Kolom yang telah diisi bubur silika tersebut dikondisikan selama 24 jam sebelum digunakan untuk elusi. Fasa gerak yang digunakan dalam penelitian ini adalah n -heksana : kloroform dengan perbandingan 6:4 secara isokratik.
Sebanyak 162,6 mg sampel diimpregnasi dengan silika adsorp. Perbandingan sampel dengan silika yang digunakan pada penelitian ini adalah 1:1. Selama proses elusi, kolom dialiri dengan udara bertekanan dan eluat ditampung dalam vial 10 mL. Masing-masing eluat diuanpkan pelarutnya denga cara diangin-anginkan. Masing-masing fraksi dilakukan uji KLT, untuk penggabungan fraksi yang memiliki spot noda yang sama. Uji fitokimia dilakukan untuk mengetahui fraksi mana yang positif triterpenoid. Fraksi yang mengandung triterpenoid dilanjutkan untuk pemishan selanjutnya.
Kromatografi Kolom Gravitasi
Kromatografi kolom gravitasi dilakukan berdasarkan dengan eluen yang memberikan profil KLT paling baik. Fase diamnya silica gel Merck 60 GF 254 yang diaktivasi 24 jam pada suhu 110 . Silica gel teraktivasi dibuat kolom dengan cara basah / dibuat bubur dengan pelarut n -heksana. Kolom tersebut dikondisikan selama 24 jam sebekum digunakan untuk elusi. Fasa gerak yang digunakan dalam penelitian ini adalah n-heksana : kloroform dengan perbandingan 4:6 secara isokratik.
Sebanyak 12,4 mg sampel diimpregnasi dengan silika adsorp. Perbandingan sampel dengan silika yang digunakan dalam penelitian ini adalah 2:1. Selama proses elusi, eluat ditampung dalam vial 10 mL. Semua fraksi dikeringkan dengan cara diangin-anginkan, kemudian ditimbang dan di analisis dengan KLT untuk mengetahui spot nodanya.
Uji Kemurnian dan Identifikasi Isolat Isolat yang diperoleh dari hasil KKG diuji kemurniannya menggunakan teknik KLT 2 dimensi dengan perbandingan pelarut n-heksana : kloroform (2:8). Jika hasil dari analisis menggunakan KLT 2D menunjukkan noda tunggal, maka isolate dapat dikatakan murni. Identifikasi isolate dilakukan dengan menggunakan reagen semprot berupa serium sulfat 5%.
Karakterisasi Struktur Senyawa
Isolat murni yang diperoleh dikarakterisasi dengan menggunakan spectrometer 1H-NMR yang dilakukan di Laboratorium Kimia Institut Teknologi Bandung.
PEMBAHASAN
Determinasi Sampel dan Pengumpulan Bahan Alam
Hasil determinasi sampel yang dilakukan di Laboratorium Biologi FMIPA UNTAN menunjukkan bahwa sampel yang digunakan dalam penelitian ini adalah
Anthocephalus cadamba (Roxb.) Miq atau tanaman Jabon (lampiran 1). Bahan tanaman yang digunakan berupa daun yang diperoleh dari halaman FMIPA UNTAN.
EkstraksiTanaman (A. cadamba (Roxb.) Miq
Potongan daun Jabon sebanyak 2 kg dimaserasi dengan etanol pada suhu kamar. Maserasi dilakukan selama 3x24 jam, hal ini dilakukan agar sebagian besar komponen terlarut ke dalam pelarut etanol. Maserat dikumpulkan kemudian diuapkan menggunakan rotary evaporator
pada suhu 40 . Ekstrak kental etanol yang didapatkan yaitu sebanyak 317,78 g dan berwarna hijau gelap.
59 Ekstrak pekat etanol dilarutkan kembali dengan pelarut etanol kemudian ditambahkan air panas dengan volume yang sama. Penambahan air dilakukan secara tetes demi tetes sambil diaduk hingga terbentuk gumpalan. Gumpalan yang terbentuk lalu disaring menggunakan kertas saring untuk memisahkan residu dan filtratnya. Hal ini dilakukan untuk memisahkan senyawa klorofil yang terdapat pada ekstrak daun. Selanjutnya maserat etanol dipartisi dengan menggunakan pelarut n-heksana dan etil asetat kemudian masing-masing fraksi diuapkan dengan menggunakan rotary evaporator. Berikut ini merupakan massa dari masing-masing fraksi.
Tabel 1. Berat masing-masing fraksi beserta rendemen terhadap ekstrak etanol
Fraksi Berat (g) Rendemen (%)
n-heksana 6,7497 2,1240 Etil asetat 21,0201 6,6147 Etanol 80,0037 25,1759
Penentuan Golongan Senyawa
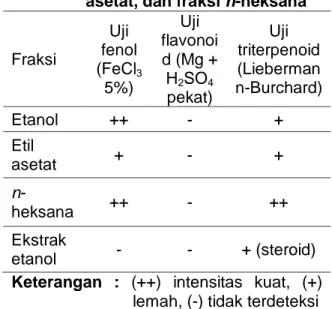
Uji fitokimia dilakukan terhadap masing-masing fraksi untuk mengidentifikasi golongan senyawa yang terkandung dalam masing-masing fraksi. Hasil dari uji fitokimia dapat dilihat pada Tabel 2.
Tabel 2. Hasil uji fitokimia pada ekstrak etanol, fraksi etanol, fraksi etil asetat, dan fraksi n-heksana
Fraksi Uji fenol (FeCl3 5%) Uji flavonoi d (Mg + H2SO4 pekat) Uji triterpenoid (Lieberman n-Burchard) Etanol ++ - + Etil asetat + - + n -heksana ++ - ++ Ekstrak etanol - - + (steroid) Keterangan : (++) intensitas kuat, (+)
lemah, (-) tidak terdeteksi
Uji golongan senyawa fenol dilakukan dengan menambahkan FeCl3 ke dalam masing-masing fraksi dan esktrak. Pada fraksi n-heksana tampak warna kuning, sedangkan padas ekstrak etanol, fraksi etanol, dan fraksi etil asetat ditandai dengan terbentuknya warna hijau tua yang menandakan bahwa pada ekstrak etanol, fraksi etanol, dan fraksi etil asetat daun segar Jabon terkandung senyawa-senyawa fenol.
Uji flavonoid menggunakan serbuk Mg kemudian ditambahkan dengan pelarut H2SO4 pekat. Pada uji flavoid ini, semua fraksi tidak ada menunjukkan perubahan warna yang signifikan yang menunjukkan adanya kandungan senyawa flavonoid.
Uji golongan triterpenoid menggunakan reagen Liebermann-Burchard. Pereaksi Liebermann-Burchard digunakan untuk identifikasi senyawa golongan triterpenoid dengan penampakkan warna merah jingga dan steroid berwarna hijau (Ahmad, 2006). Pewarnaan yang ditimbulkan dari hasil uji fitokimia ekstrak etanol, fraksi etanol, fraksi etil asetat menunjukkan reaksi positif adanya senyawa triterpenoid, sedangkan pada fraksi n-heksana positif adanya senyawa steroid.
Intensitas warna pada uji keberadaan senyawa triterpenoid kuat (++), hal ini menunjukkan bahwa senyawa terpenoid merupakan komponen utama dalam ekstrak etanol, fraksi etanol dan fraksi etil asetat. Semakin kuat intensitas warna yang terbentuk maka kuantitas senyawa yang ada pada fraksi tersebut makin banyak (Cannel, 1998).
Kromatografi Vakum Cair
Fraksi etil astat diteruskan pada kolom vakum cair. Massa fraksi tersebut adalah 20 g. Pada KVC ini digunakan eluen perbandingan n-heksana : etil asetat secara bergradien (n-heksana 100%, 1:9, 2:8, 3:7, 4:6, 5:5, 6:4, 7:3, 8:2, 9:1, etil asetat 100%). Dari hasil KVC di dapatkan 12 fraksi, kemudian semua fraksi tersebut dikering anginkan, sambil dilakukan KLT menggunakan eluen perbandingan n-heksana : etil asetat (7:3) untuk melihat kompleksitas noda pada tiap-tiap fraksi.
60
Gambar 1. Pola noda sampel hasil KVC (A. Saat dilampu UV; B. Setelah di semprot serium sulfat dan di oven)
Berdasarkan hasil KLT, kompleksitas dari fraksi 5 terlihat cukup baik dan hanya terdapat 2 noda utama. Pada saat disemprot dengan menggunakan pereaksi penampak noda serium sulfat, terjadi perubahan warna pada spot menjadi warna coklat dan merah, diduga terdapat senyawa fenolik dan triterpenoid. Fraksi 5 dengan massa 162,6 mg dilakukan pemisahan lanjutan yaitu menggunakan kromatografi kolom
flash.
Kromatografi Kolom Flash
Kromatografi flash dilakukan dengan menggunakan eluen yang sama secara isokratik dan didapatkan 15 fraksi. Fraksi-fraksi tersebut kemudian di KLT untuk melihat pola nodanya dengan eluen n -heksana : kloroform (6:4) dan di kering anginkan. Pada fraksi 9-15 memiliki pola noda yang sama sehingga ketujuh fraksi tersebut digabungkan.
Gambar 2. Pola noda sampel hasil kolom flash (A. Saat dilampu UV; B. Setelah dikering oven)
Hasil uji fitokimia yang dilakukan terhadap fraksi gabungan (9-15) ini menunjukkan bahwa positif mengandung triterpenoid dengan terjadinya perubahan warna merah pada sampel. Kemudian fraksi gabungan ini ditimbang dan di
dapatkan massa sampel 12,4 mg. Fraksi gabungan (9-15) ini dilanjutkan pemisahan dengan kromatografi kolom gravitasi, dengan tujuan untuk mendapatkan isolat murni.
Kromatografi Kolom Gravitasi
Pada tahap kolom gravitasi ini, eluen yang digunakan adalah n-heksana : kloroform (4:6) secara isokratik dan didapatkan 14 fraksi. Fraksi-fraksi tersebut kemudian di KLT menggunakan eluen n -heksana : kloroform (5:5) untuk melihat pola nodanya. Dari hasil KLT terlihat bahwa pada fraksi 4-9 dapat dilakukan penggabungan karena memiliki pola noda yang sama dan terlihat bahwa senyawanya sudah cukup murni.
Gambar 3. Pola noda hasil KKG (A. Saat dilampu UV; B. Setelah di semprot serium sulfat dan dikering oven) Gabungan fraksi ini dilanjutkan dengan KLT 2D untuk melihat tingkat kemurnian pada sampel. KLT 2D dilakukan menggunakan eluen n-heksana: kloroform (2:8). Dari hasil KLT tersebut dapat disimpulkan bahwa (senyawa 1) dengan massa 3,03 mg sudah cukup murni dan dapat dilanjutkan untuk keperluan karakterisasi isolat dengan menggunakan spektroskopi 1H-NMR.
Gambar 4. Pola noda hasil KLT 2 dimensi (A. Saat dilampu UV; B. Setelah di semprot serium sulfat dan dikering oven)
A B
A B
A B
61 Karakterisasi Struktur Senyawa
Analisis 1H-NMR senyawa 1 dilakukan untuk mengetahui gambaran berbagai jenis atom hidrogen dalam molekul. Spektrum 1H-NMR dapat menginformasikan mengenai lingkungan kimia dan jumlah atom hidrogen dalam setiap lingkungan, dan struktur gugus yang berdekatan dengan setiap atom hidrogen (Creswell, et al., 2005).
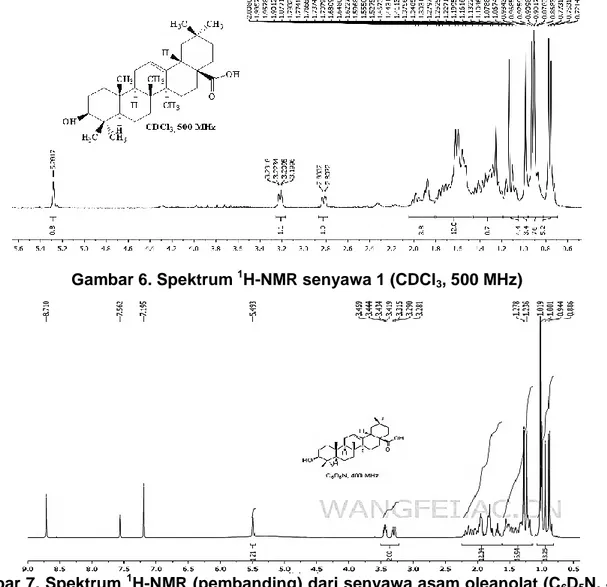
Analisis 1H-NMR senyawa 1 pada Gambar 6 memperlihatkan sinyal karakteristik untuk senyawa triterpenoid. Menurut Muharni dan Elfita (2011), karakteristik khas pola sinyal 1H-NMR untuk senyawa triterpenoid terlihat dari sinyal-sinyal yang berhimpit pada daerah geseran kimia (δH) di bawah 2 ppm untuk proton alifatik (CH3, CH2, dan CH) yang merupakan proton siklik dari kerangka dasar triterpenoid yang tidak terpisah dengan baik.
Informasi yang diperoleh dari data spektrum 1H-NMR senyawa 1 menunjukkan adanya 7 sinyal proton metil singlet masing-masing dengan integrasi 3H pada geseran kimia (δH) (0,75 ppm, 0,77 ppm, 0,90 ppm, 0,91 ppm, 0,92 ppm, 0,98 ppm, dan 1,13 ppm), menunjukkan keberadaan proton metil yang terikat pada atom karbon dalam lingkungan kepolaran yang berbeda. Menurut Elya dkk, (2009) munculnya 7 puncak metil tersebut pada spektrum 1H-NMR, merupakan ciri dari senyawa triterpenoid. Gambar 5 menunjukkan pola gugus metil pada kerangka triterpenoid.
Gambar 5. Gugus metil pada kerangka triterpenoid (Dewick, 2002)
Gambar 6. Spektrum 1H-NMR senyawa 1 (CDCl3, 500 MHz)
Gambar 7. Spektrum 1H-NMR (pembanding) dari senyawa asam oleanolat (C6D5N, 400
62
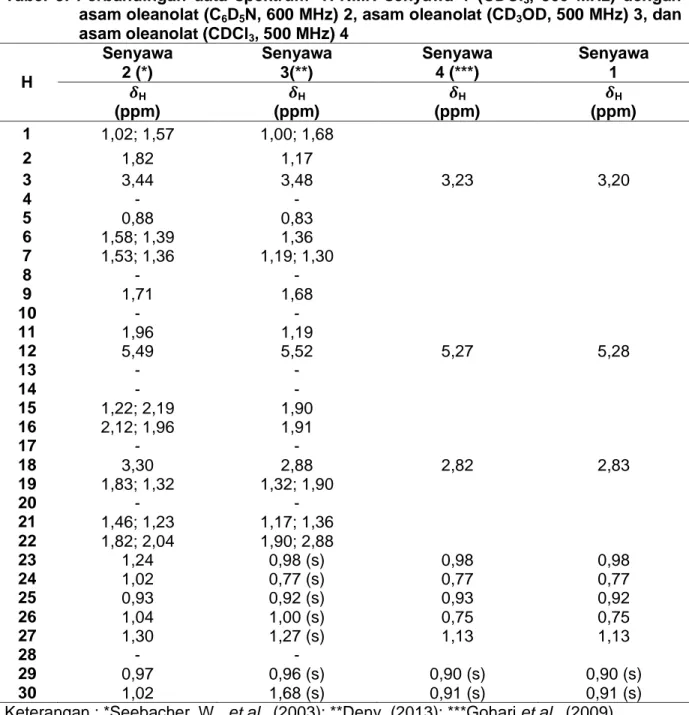
Tabel 3. Perbandingan data spektrum 1H-NMR senyawa 1 (CDCl3, 500 MHz) dengan
asam oleanolat (C6D5N, 600 MHz) 2, asam oleanolat (CD3OD, 500 MHz) 3, dan
asam oleanolat (CDCl3, 500 MHz) 4 H Senyawa 2 (*) Senyawa 3(**) Senyawa 4 (***) Senyawa 1 H (ppm) H (ppm) H (ppm) H (ppm) 1 1,02; 1,57 1,00; 1,68 2 1,82 1,17 3 3,44 3,48 3,23 3,20 4 - - 5 0,88 0,83 6 1,58; 1,39 1,36 7 1,53; 1,36 1,19; 1,30 8 - - 9 1,71 1,68 10 - - 11 1,96 1,19 12 5,49 5,52 5,27 5,28 13 - - 14 - - 15 1,22; 2,19 1,90 16 2,12; 1,96 1,91 17 - - 18 3,30 2,88 2,82 2,83 19 1,83; 1,32 1,32; 1,90 20 - - 21 1,46; 1,23 1,17; 1,36 22 1,82; 2,04 1,90; 2,88 23 1,24 0,98 (s) 0,98 0,98 24 1,02 0,77 (s) 0,77 0,77 25 0,93 0,92 (s) 0,93 0,92 26 1,04 1,00 (s) 0,75 0,75 27 1,30 1,27 (s) 1,13 1,13 28 - - 29 0,97 0,96 (s) 0,90 (s) 0,90 (s) 30 1,02 1,68 (s) 0,91 (s) 0,91 (s)
Keterangan : *Seebacher, W., et al., (2003); **Deny, (2013); ***Gohari et al., (2009)
Sinyal pada daerah ( H) 3,20 ppm merupakan sinyal khas proton metin pada kerangka triterpenoid yang terikat pada atom C yang mengikat gugus hidroksi (OH). Sinyal khas ini untuk triterpenoid pentasiklik yang mengikat OH pada posisi C-3 (Muharni, 2010). Data sinyal spectrum 1H-NMR senyawa 1 pada pergeseran kimia ( H) 5,28 ppm menunjukkan proton olefin yang tersubstitusi pada cincin siklik. Sinyal-sinyal proton dari spectrum 1 H-NMR tersebut mengidentifikasikan bahwa senyawa 1 diduga merupakan suatu kerangka triterpenoid turunan olean-12-en
yang tersubstitusi gugus hidroksi (OH) pada C-3.
Hasil perbandingan geseran kimia ( H) pada Tabel 3 dapat diketahui bahwa nilai geseran kimia ( H) senyawa 1 memiliki kesamaan dengan nilai eseran kimia dari senyawa triterpenoid pentasilklik asam oleanolat. Sehingga, struktur senyawa 1 disarankan sebagai asam oleanolat (asam-3 -hisroksiolean-12-en-28-oat).
63 SIMPULAN
Berdasarkan pembahasan dapat disimpulkan bahwa Senyawa asam oleanolat (asam 3β-hidroksiolean-12-en-28-oat) berbentuk padatan amorf putih (3,03 mg), telah diisolasi dari fraksi etil asetat dengan perbandingan pergeseran kimia (δH) spektrum NMR-1H dari senyawa 1 (CDCl3, 500 MHz) (ppm): 0,75; 0,77; 0,90; 0,91; 0,92; 0,98; 1,13; 2,83; 3,20; 5,28.
UCAPAN TERIMA KASIH
Terima kasih disampaikan kepada bapak Prof. Dr. Yana Maolana Syah yang telah membantu pengukuran spektrum 1H -NMR dan staf Laboratorium Biologi FMIPA UNTAN yang telah mengidentifikasi sampel tumbuhan yang digunakan dalam penelitian ini.
DAFTAR PUSTAKA
Deny, Rudiyansyah, dan Ardiningsih, P., 2003, Isolasi dan Karakterisasi Senyawa Triterpenoid dari Fraksi Kloroform Kulit Batang Durian Kura (D.
testudinarum Becc.), J.Kimia
Khatulistiwa, 2(1): 7-12.
Dewick, P. M., 2002, Medical Natural Products: A biosynthetic Approach, Second Edition, School of Pharmaceutical of Nottingham, UK. Elya, B., Koela, S., dan Hanafi, M., 2009,
Senyawa Triterpenoid dari Ekstrak n -heksan Kulit Batang Tanaman Garcinia benthami, J. Makara Sains, 13: 9-12. Gohari, AR., et al, 2009, Isolation and
Quantitative Analysis of Oleanolic Acid
from Satureja mutica Fisch. & C. A. Mey., Journal of Medicinal Plants, 8: 5. Harborne, J. B., 1987, Metode Fitokimia
Penuntun Cara Modern Menganalisis Tumbuhan, Bandung, ITB Press. Isa, Enda Pratiwi. 2008. Ekstraksi dan
identifikasi senyawa terpenoid pada tumbuhan meniran (Phyllanthus niruri Linnn) dengan metode kromatografi lapis tipis. Jurusan Pendidikan Kimia. Gorontalo, UNG (Skripsi).
Martawijaya, A., Kartasujana., K. Kadir., dan S. A. Prawira. 1989. Atlas Kayu Indonesia. Jilid II. Buku. Badan Litbang Kehutanan Departemen Kehutanan. Bogor. 167 p.
Muharni., 2010, Triterpenoid Lupeol dari Manggis Hutan (Garcinia bancana
Miq.), Penelitian Sains, 13: 41-45
.
Muharni dan Elfita., 2011, Triterpenoidβ-Amirin dari Kulit Batang Garcinia bancana Miq., Penelitian Sains, 14: 30-32.
Seebacher, W., et al, 2003, Complete assignments of 1H and 13C NMR resonances of oleanolic acid, 18 -oleanolic acid, ursolic acid and their 11-oxo derivatives, MRC, 41: 636-638. Slik, J.W.F. 2006 Trees of Sungai Wain.
National Herbarium Nederland, Leiden University Branch, Leiden, Belanda. http://www.nationaalherbarium.nl/sunga iwain/ [1 Desember 2015].
Slkar I V, Kakkar KK, Chakre O J. Glossary of Indian Medicinal Plants with Active Principles. New Delhi: CSIR; 1992. Part I, 75 p.
Yulvianti, M., 2007. Katecin dan Fzelecin dari Daun Artocarpus champeden Spreng. Institut teknologi Bandung. Bandung.