PERBANDINGAN METODE EKSTRAKSI CAIR-CAIR DAN ULTRASONIKASI UNTUK PEMISAHAN PIRANTEL PAMOAT DARI
SEDIAAN SUSPENSI MERK “X”®
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Victor Purnama Agung FanggidaE NIM: 098114129
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
i
PERBANDINGAN METODE EKSTRAKSI CAIR-CAIR DAN ULTRASONIKASI UNTUK PEMISAHAN PIRANTEL PAMOAT DARI
SEDIAAN SUSPENSI MERK “X”®
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Victor Purnama Agung FanggidaE NIM: 098114129
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
Persetujuan Pembimbing
PERBANDINGAN METODE EKSTRAKSI CAIR-CAIR DAN ULTRASONIKASI UNTUK PEMISAHAN PIRANTEL PAMOAT DARI
SEDIAAN SUSPENSI MERK “X”®
Skripsi yang diajukan oleh:
Victor Purnama Agung FanggidaE
NIM: 098114129
telah disetujui oleh:
iv
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaiman layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah
ini, maka saya bersedia menanggung segala sanksi sesuai peraturan
perundang-undangan yang berlaku.
Yogyakarta, 31 Mei 2013
Penulis
v
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Victor Purnama Agung FanggidaE Nomor Mahasiswa : 098114129
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PERBANDINGAN METODE EKSTRAKSI CAIR-CAIR DAN ULTRASONIKASI UNTUK PEMISAHAN PIRANTEL PAMOAT DARI
SEDIAAN SUSPENSI MERK “X”®
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 31 Mei 2013
Yang menyatakan
vi
HALAMAN PERSEMBAHAN
Kupersembahkan karyaku ini untuk:
T
T
u
u
h
h
a
a
n
n
k
k
u
u
,
,
J
J
u
u
r
r
u
u
s
s
e
e
l
l
a
a
m
m
a
a
t
t
k
k
u
u
,
,
P
P
e
e
n
n
o
o
l
l
o
o
n
n
g
g
k
k
u
u
,
,
Y
Y
e
e
s
s
u
u
s
s
K
K
r
r
i
i
s
s
t
t
u
u
s
s
P
P
a
a
p
p
a
a
t
t
e
e
r
r
s
s
a
a
y
y
a
a
n
n
g
g
,
,
i
i
b
b
u
u
n
n
d
d
a
a
t
t
e
e
r
r
c
c
i
i
n
n
t
t
a
a
,
,
d
d
a
a
n
n
k
k
a
a
k
k
a
a
k
k
-
-
k
k
a
a
k
k
a
a
k
k
k
k
u
u
t
t
e
e
r
r
k
k
a
a
s
s
i
i
h
h
T
T
e
e
m
m
a
a
n
n
-
-
t
t
e
e
m
m
a
a
n
n
k
k
u
u
,
,
s
s
a
a
h
h
a
a
b
b
a
a
t
t
-
-
s
s
a
a
h
h
a
a
b
b
a
a
t
t
k
k
u
u
A
vii PRAKATA
Puji dan Syukur kepada Tuhan Yang Maha Esa karena begitu besar kasih
setia, rahmat dan bimbingan tangan kasih-Nya sehingga penulis dapat
menyelesaikan skripsi yang berjudul “Perbandingan Metode Ekstraksi Cair-cair
dan Ultrasonikasi Untuk Pemisahan Pirantel Pamoat Dari Sediaan Suspensi Merk
“X"®” sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
(S.Farm.) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis menghaturkan ucapan terima kasih kepada semua pihak yang
selama ini telah membantu, mendorong, memotivasi dan memberikan saran
hingga selesainya skripsi ini, terutama kepada:
1. Bapak Prof. Dr. Sudibyo Martono, M.S., Apt. selaku dosen pembimbing yang
telah banyak meluangkan waktunya dalam membimbing, memberikan
masukan, kritik, solusi, dan dukungan kepada penulis selama penyusunan
skripsi ini.
2. Bapak Ipang Djunarko M.Sc, Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
3. Ibu Lucia Wiwid Wijayanti, M.Si. selaku dosen penguji yang memberikan
kritik dan saran untuk skripsi ini.
4. Bapak Jeffry Julianus, M.Si. selaku dosen penguji yang memberikan kritik
dan saran untuk skripsi ini.
5. PT KONIMEX, Indonesia atas pemberian bahan baku pirantel pamoat yang
viii
6. Ibu Rini Dwi Astuti, M.Sc, Apt. selaku Kepala Laboratorium Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta.
7. Segenap dosen dan karyawan atas ilmu dan pengalaman yang berharga
sehingga berguna dalam proses penyusunan skripsi.
8. Seluruh staff laboratorium, staff keamanan, dan kebersihan di Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta terutama Mas Bimo, Pak
Parlan, Mas Ottok, dan Mas Kunto, serta Mas Kethul.
9. Perpustakaan Universitas Sanata Dharma atas koleksi buku-buku serta akses
internetnya sehingga penulis memperoleh bahan-bahan yang cukup lengkap
dalam penulisan skripsi ini
10. Kedua orang tuaku, Bapak Christoffel Jusuf FanggidaE dan Ibu Marselina
Yohana Lay-FanggidaE atas doa, kasih sayang, dan dukungan semangat yang
diberikan kepada penulis.
11. Kakak-kakakku, Jeremi Herzon FanggidaE, Ronald Richard FanggidaE,
Justus Amardin FanggidaE, Robinson Gunawan FanggidaE dan Rianto Panca
Putra FanggidaE atas semangat dan inspirasi kesuksesan kalian sehingga
memacu penulis dalam menyelesaikan skripsi ini.
12. Agnes Mutiara Kurniawan dan Novia Sarwoning Tyas selaku teman
seperjuangan selama penelitian dan penyusunan skripsi.
13. Bernadetta Arum Wijayanti yang selalu mendukung penulis belajar menjadi
lebih baik, memberikan saran dan kritik, dan memberikan dorongan semangat
ix
14. Mas Dika, Ko Frank, Cik Lia, Mas Toni, Om Ridho yang telah meluangkan
waktu untuk memberikan diskusi terkait penelitian dan semangat yang
diberikan kepada penulis.
15. Teman-teman skripsi bimbingan Bapak Prof. Dr. Sudibyo Martono, M. S.,
Apt. : Shinta, Metri, Sasya atas kerjasama dan dukungannya selama proses
penelitian dan penyusunan skripsi.
16. Teman-teman sepenelitian di laboratorium: Jimmy, Rachel, Gunggek, Jo,
Nety, Saka, Felix, Jati, Leo, Ina, Topan, Agus, Febrin, Ozy, Wisnu atas
kebersamaan, tawa, keceriaan dan semangat yang diberikan.
17. Teman-teman kos “Khrisna House” yang menjadi teman seperjuangan di
Yogyakarta.
18. Liverpool FC, yang telah memberikan inspirasi dan motivasi lewat video
tentang arti perjuangan dan kerja keras kepada penulis sehingga tidak
menyerah untuk menyelesaikan rangkaian skripsi ini.
19. Teman-teman FST & FKK 2009 atas pengalaman, keceriaan, dan
kebersamaan yang tak akan terlupakan.
20. Semua teman-teman, baik di Fakultas Farmasi Universitas Sanata Dharma
maupun lainnya, terima kasih atas kebersamaannya.
x
Penulis menyadari bahwa skripsi ini masih terdapat banyak kekurangan.
Oleh karena itu penulis mengharapkan kritik dan saran untuk membantu penulis
dalam perkembangan selanjutnya. Akhir kata, semoga skripsi ini berguna bagi
pembaca.
xi DAFTAR ISI
Hal
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ...
HALAMAN PERSETUJUAN PUBLIKASI ...
HALAMAN PERSEMBAHAN ... iv
v
vi
PRAKATA ... vii
DAFTAR ISI ... xi
DAFTAR TABEL ... xv
DAFTAR GAMBAR ...
DAFTAR LAMPIRAN ...
xvi
xviii
INTISARI ... xx
ABSTRACT ... xxi
BAB I. PENGANTAR ...
A. Latar Belakang ...
1. Permasalahan ...
2. Keaslian penelitian ...
3. Manfaat penelitian ...
a. Manfaat metodologis ...
b. Manfaat praktis ... 1 1 3 3 4 4 4
xii
BAB II. PENELAAHAN PUSTAKA ... 5
A. Pirantel Pamoat ... 5
B. Suspensi ... 6
C. Ekstraksi ... 8
D. Ekstraksi Cair-cair ... 9
E. Spektrofotometri Ultraviolet ... 16
F. Landasan Teori ... 24
G. Hipotesis ... 26
BAB III. METODE PENELITIAN ...
A. Jenis dan Rancangan Penelitian ...
B. Variabel Penelitian ...
1. Variabel bebas ...
2. Variabel tergantung ...
3. Variabel pengacau terkendali ...
C. Definisi Operasional ...
D. Bahan Penelitian ...
E. Alat Penelitian ...
F. Tata Cara Penelitian ...
1. Pembuatan larutan stok baku pirantel pamoat (1 mg/mL) ...
2. Penentuan panjang gelombang maksimum pirantel pamoat ....
3. Pembuatan larutan seri baku dan kurva baku pirantel pamoat ..
4. Penetapan kadar pirantel pamoat dalam sampel sediaan
suspensi pirantel pamoat merk “X” ®...
xiii
a. Pembuatan larutan induk sampel pirantel pamoat xxx xx
(0,5 mg/mL) ...
b. Ekstraksi pirantel pamoat dengan metode ekstraksi
cair-cair menggunakan corong pisah ...
c. Ekstraksi pirantel pamoat dengan metode ekstraksi
Cair-cair menggunakan ultrasonikator ...
d. Penetapan kadar pirantel pamoat dalam sampel sediaan
suspensi pirantel pamoat merk “X”® ...
G. Analisis hasil ...
1. Panjang gelombang maksimum ...
2. Metode ekstraksi optimum ...
a. Presisi ...
b. Akurasi ...
BAB IV. HASIL DAN PEMBAHASAN ...
A. Pembuatan Larutan Baku Pirantel Pamoat ...
B. Optimasi Penentuan Panjang Gelombang Maksimum Pirantel
Pamoat ...
C. Pembuatan Kurva Baku Pirantel Pamoat ...
D. Preparasi Sampel ...
E. Ekstraksi Cair-cair Menggunakan Corong Pisah ...
F. Ekstraksi Cair-cair Menggunakan Ultrasonikator ...
G. Penetapan Kadar Pirantel Pamoat ...
H. Perbandingan Metode Ekstraksi ...
xiv
I. Perbandingan Hasil Penetapan Kadar Pirantel Pamoat dengan Proses
Ekstraksi pada Suspensi dan Tanpa Proses Ekstraksi pada Tablet ...
BAB V. KESIMPULAN DAN SARAN . ...
A.Kesimpulan ...
B.Saran ...
DAFTAR PUSTAKA ...
LAMPIRAN ...
BIOGRAFI PENULIS ... 48
52
52
52
53
57
xv
DAFTAR TABEL
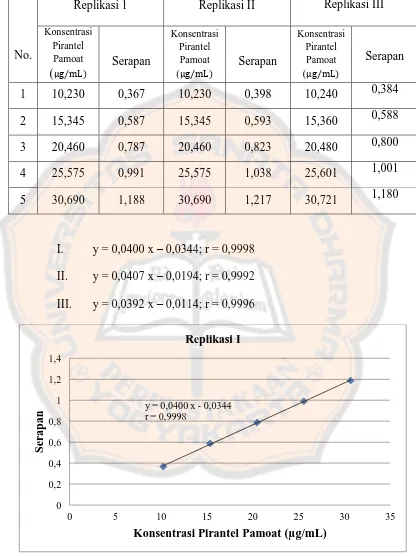
Tabel 1. Hasil Pengukuran Kurva Baku Pirantel Pamoat ...
Tabel 2. Data Indeks Polaritas Berbagai Macam Pelarut ...
Tabel.3. Hasil Pengukuran dan Penghitungan Recovery Metode
Ekstraksi Cair-cair Menggunakan Corong Pisah ...
Tabel.4. Hasil Pengukuran dan Penghitungan Recovery Metode
Ekstraksi Cair-cair Menggunakan Ultrasonikator ...
Tabel.5. Hasil Analisis Normalitas Data Metode Ekstraksi Cair-cair
Menggunakan Corong Pisah ...
Tabel.6. Hasil Analisis Normalitas Data Metode Ekstraksi Cair-cair
Menggunakan Ultrasonikator ...
Tabel.7. Hasil Analisis Varian Data Metode Ekstraksi Cair-cair
Menggunakan Corong Pisah dan Ultrasonikator ...
Tabel.8. .Hasil Analisis T Independent Metode Ekstraksi Cair-cair
MenggunakanCorong Pisah dan Ultrasonikator ...
Tabel.9. Data Penimbangan Baku Pirantel Pamoat ...
Tabel.10. Data Perhitungan Kadar Pirantel Pamoat ...
Tabel.11. Data Pengukuran Serapan Larutan Baku Pirantel Pamoat ...
Tabel.12. .Hasil Scanning Panjang Gelombang Maksimum Pirantel
Pamoat pada 3 Konsentrasi ...
Tabel.13. Hasil Pengukuran Recovery Pirantel Pamoat pada Sediaan
xvi
DAFTAR GAMBAR
Gambar 1. Struktur Pirantel Pamoat ...
Gambar 2. Proses Terjadinya Kavitasi ...
Gambar 3. Skema Cara Kerja Ekstraksi dengan Bantuan Ultrasonik ...
Gambar 4. Diagram Energi Tingkat Transisi Elektron ...
Gambar 5. Spektrofotometer Single Beam ...
Gambar 6. Spektrofotometer Double Beam ...
Gambar 7. Skema Penetapan Kadar Pirantel Pamoat ...
Gambar.8.. Spektra Serapan Maksimum yang Terbentuk Pada 3
...Konsentrasi ...
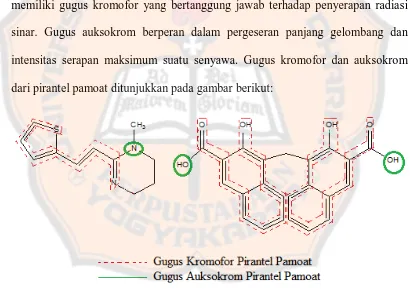
Gambar.9.. Gugus Kromofor dan Auksokrom Pada Struktur Pirantel
...Pamoat ...
Gambar.10.. Hubungan Antara Konsentrasi dengan Serapan Pirantel
....Pamoat Replikasi I ...
Gambar.11.. Pola Spektra Pirantel Pamoat Tanpa Ekstraksi Pada Sediaan
..Tablet ...
Gambar.12.. Pola Spektra Pirantel Pamoat Hasil Ekstraksi Menggunakan
..Ultrasonikator dalam Pelarut Metanol ...
Gambar.13.. Pola Spektra Pirantel Pamoat Hasil Ekstraksi Menggunakan
..Corong Pisah dalam Pelarut Metanol ...
Gambar.14. .Hubungan Antara Konsentrasi Pirantel Pamoat dengan
..Serapan Replikasi II ...
xvii
Gambar.15. .Hubungan Antara Konsentrasi Pirantel Pamoat dengan
..Serapan Replikasi III ...
Gambar 16. Hasil Scanning Blanko DMSO-Metanol ...
Gambar.17. Hasil Scanning Fase Polar Ekstraksi Menggunakan Corong
..Pisah dalam Pelarut Metanol ...
Gambar.18. Hasil Scanning Fase Non Polar Ekstraksi Menggunakan
..Corong Pisah dalam Pelarut Heksan ...
Gambar.19. Hasil Scanning Fase Polar Ekstraksi Menggunakan
..Ultrasonikator dalam Pelarut Metanol ...
Gambar.20. Hasil Scanning Fase Non Polar Ekstraksi Menggunakan
..Ultrasonikator dalam Pelarut Heksan ...
62
64
65
65
66
xviii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat Analisis Baku Pirantel Pamoat ...
Lampiran.2..Data Penimbangan Baku Serta Contoh Perhitungan Seri
Konsentrasi Baku ...
a. Skema Pembuatan ...
b. Penimbangan Baku Pirantel Pamoat ...
c. Perhitungan Seri Konsentrasi Pirantel Pamoat ...
d. Pengukuran Serapan Larutan Baku Pirantel Pamoat ...
e. Perhitungan Persamaan Kurva Baku Pirantel Pamoat
Menggunakan Regresi Linear ...
f. Kurva Baku Pirantel Pamoat ...
Lampiran.3..Hasil Scanning Panjang Gelombang Maksimum Pirantel
Pamoat ...
Lampiran.4..Data Perhitungan Pencuplikan Pirantel Pamoat yang Setara
50,0 mg ...
Lampiran.5. Hasil Scanning Blanko DMSO-Metanol ...
Lampiran.6..Hasil Scanning Fase Polar Ekstraksi Cair-cair Menggunakan
Corong Pisah ...
Lampiran.7..Hasil Scanning Fase Non Polar Ekstraksi Cair-cair
Menggunakan Corong Pisah ...
Lampiran.8. Hasil Scanning Fase Polar Ekstraksi Cair-cair Menggunakan
xix
Lampiran.9..Hasil Scanning Fase Non Polar Ekstraksi Cair-cair
Menggunakan Ultrasonikator ...
Lampiran.10. Hasil Penghitungan Recovery Pirantel Pamoat pada Sediaan
Tablet ... 66
xx INTISARI
Pirantel pamoat berkhasiat sebagai antelmintik dan paling sering digunakan sebagai pengobatan mandiri untuk mengatasi cacingan. Salah satu produk yang mengandung zat aktif pirantel pamoat yaitu suspensi pirantel pamoat merk “X”®
. Perlu dilakukan analisis untuk mengetahui kebenaran kandungan zat aktif pirantel pamoat dalam sediaannya. Tahapan penting dalam analisisnya yakni adanya ekstraksi zat aktif pirantel pamoat dari sediaannya. Dalam penelitian ini metode ekstraksi yang diperbandingkan adalah metode ekstraksi cair-cair menggunakan corong pisah dan ultrasonikator untuk kemudian ditetapkan kadarnya menggunakan spektrofotometer UV.
Ekstraksi cair-cair menggunakan corong pisah dilakukan ekstraksi sebanyak 3 kali (@ 10 mL) selama 1 menit, sedangkan pada ultrasonikator ekstraksi berlangsung selama 15 menit dengan perbandingan volume pelarut 1:3. Heksan berperan sebagai pelarut kedua pada kedua metode ekstraksi. Fungsinya untuk mengekstrak bahan tambahan sehingga diperoleh pirantel pamoat tetap berada pada pelarut pertama dan terbebas dari gangguan bahan tambahan lain.
Kedua metode tersebut memiliki recovery yang memenuhi syarat, dimana ekstraksi dengan corong pisah berada pada rentang 98,38-101,29% sedangkan dengan ultrasonikator berada pada rentang 99,29-100,96%. Ditemukan perbedaan yang tidak bermakna secara statistik diantara kedua metode tersebut pada uji T tak berpasangan dengan taraf kepercayaan 95% menggunakan softwa re R statistic version 2.14.1.
xxi ABSTRACT
Pyrantel pamoate have efficacy as anthelmintic and most often used as a self-treatment to overcome intestinal worms. One of the products that contain the pyrantel pamoate active substance which is brand “X”®
pyrantel pamoate suspension. Analysis is needed to determine the truth of the pyrantel pamoate active ingredients content in the preparations. . Important step in the analysis is the
extraction of active ingredient pyrantel pamoate from the preparations. The method of extraction were compared is a liquid-liquid extraction method using a separating funnel and ultrasonicator to subsequently established the content using UV spectrophotometer.
Liquid-liquid extraction using a separating funnel and the extraction of as much as 3 times (@ 10 mL) for 1 min, whereas the extraction ultrasonicator lasted for 15 minutes with the solvent volume ratio 1:3. Hexane acts as second solvent in both extraction methods. The function is to extract other ingredients so obtained pyrantel pamoate remain on the first solvent and free from the interferences.
Both of these methods have a qualified recovery, where the extraction of the separating funnel is at the range 98,38-101,29% whereas the ultrasonicator are on the range 99,29-100,96 %. Found that the difference was not statistically significant between the two methods is the unpaired t test with a 95% of confidence level using the R statistical software version 2.14.1.
1
BAB I PENGANTAR
A. Latar Belakang
Merupakan suatu pengetahuan umum bahwa masa anak-anak adalah
masa yang paling rentan mengalami berbagai macam penyakit. Salah satu
penyakit yang paling sering dialami adalah penyakit cacing atau biasa dikenal
dengan cacingan. Selain berefek pada gizi, kecerdasan, kesehatan dan konsentrasi
pun menjadi manifestasi lain yang harus dialami penderitanya. Kecenderungan
terjadinya penyakit ini tinggi, khususnya pada penduduk dengan tingkat ekonomi
yang rendah (Anonima, 2006).
Berbagai macam obat cacing yang beredar di pasaran, salah satu yang
paling sering digunakan adalah yang mengandung zat aktif pirantel pamoat.
Sediaan tersebut dapat berupa tablet ataupun suspensi dan sangat mudah
didapatkan di apotek-apotek sehingga sering dikonsumsi oleh penderita sebagai
suatu jalan untuk pengobatan mandiri mengatasi cacingan. Pirantel pamoat
berkhasiat sebagai antelmintik dan efektif untuk pengobatan infeksi yang
disebabkan oleh cacing di usus (Sukarban, 1995).
Kandungan zat aktif pirantel pamoat yang tertera di dalam label kemasan
sediaannya adalah 125 mg/5 mL. Penggunaan pirantel pamoat sebagai antelmintik
sesuai dosisnya akan memberikan efek farmakologis yang optimum. Dosis yang
tepat dapat dipastikan dengan melihat kesesuaian antara kadar senyawanya
sebagai pengobatan mandiri dalam masyarakat mendorong untuk dilakukannya
analisis sebagai suatu proses penjaminan mutu untuk memastikan kebenaran
kandungan zat aktif pirantel pamoat di dalamnya.
Pada penelitian-penelitian terdahulu telah dilakukan berbagai macam
analisis untuk menetapkan kadar pirantel pamoat. Dalam Farmakope Indonesia
edisi IV dan USP (United States Pharmacopoeia) XXX tahun 2007 dijabarkan
bahwa penetapan kadarnya dilakukan secara kromatografi cair kinerja tinggi
(KCKT) serta pada Farmakope Internasional (International Pharmacopoeia) edisi
IV tahun 2008 dijelaskan penetapan kadarnya secara kromatografi lapis tipis
(KLT). Metode KCKT dan KLT memiliki kekurangan, yakni alat dan biaya
operasional yang mahal, serta kedua metode ini juga membutuhkan waktu analisis
yang lama.
Oleh karena itu, diperlukan suatu metode analisis baru yang relatif
murah, waktu analisis yang cepat serta dapat memberikan hasil dan presisi yang
baik. Metode analisis yang dipilih adalah metode spektrofotometri UV, yang
memiliki kelebihan cepat dan mudah dalam penggunaannya, memiliki sensitivitas
dan selektivitas yang baik untuk penetapan kadar senyawa tunggal serta
merupakan metode dengan instrumen yang umum dimiliki laboratorium di
Indonesia.
Salah satu tahap dalam analisis penetapan kadar menggunakan
spektrofotometri UV adalah tahap optimasi metode ekstraksi zat aktif pirantel
pamoat dari bentuk sediaan suspensinya. Tahap penelitian ini merupakan salah
Berdasarkan studi pustaka yang dilakukan penulis, belum ditemukan adanya
penelitian khusus mengenai metode ekstraksi zat aktif pirantel pamoat dari bentuk
sediaannya.
Metode yang akan dioptimasi adalah metode ekstraksi cair-cair (
liquid-liquid extraction) menggunakan corong pisah dan metode ultrasonikasi. Sistem
metode ekstraksi yang digunakan dalam analisis ini belum pernah dilakukan
sebelumnya sehingga diperlukan suatu optimasi metode. Optimasi ini penting
dilakukan terlebih dahulu agar didapatkan metode ekstraksi yang memberikan
hasil paling optimum dalam memisahkan zat aktif pirantel pamoat dari bentuk
sediaannya karena sangat berpengaruh terhadap hasil penetapan kadarnya dengan
metode spektrofotometri UV.
1. Permasalahan
Berdasarkan latar belakang tersebut maka permasalahan yang muncul
adalah metode manakah diantara metode ekstraksi cair-cair (liquid-liquid
extraction) dan metode ultrasonikasi yang paling optimum digunakan untuk
mengekstraksi zat aktif pirantel pamoat dari sediaan suspensi merk “X”® ?
2. Keaslian penelitian
Penelitian mengenai pirantel pamoat yang pernah dilakukan sebelumnya
adalah tentang Penetapan Kadar Pirantel Pamoat dalam Sediaan Tablet Secara
Spektrofotometri Ultraviolet (Agustina, 2010) dan Spectrophotometric
Determination of Pyrantel Pamoate Bulk Samples and Pharmaceutical
Formulations (Forcier, Mushinsky and Wagner, 1971). Sejauh sepenelusuran
perbandingan metode ekstraksi zat aktif pirantel pamoat dari sediaan suspensi
merk “X”® dengan teknik ekstraksi cair-cair dan ultrasonikasi.
Penelitian lainnya menggunakan metode KCKT, yaitu Determination of
Fenbendazole, Praziquantel and Pyrantel Pamoate in Dog Plasma by
High-Performance Liquid Chromatography (Morovján, Csokán and Makranszki, 1998),
High-Performance Liquid Chromatographic Determination of Oxantel and
Pyrantel Pamoate (Allender, 1988), serta Simultaneous Determination of
Mebendazole and Pyrantel Pamoate from Tablets by High-Performance Liquid
Chromatography-Reverse Phase (RP-HPLC) (Argekar, Raj and Kapadia, 1997).
3. Manfaat penelitian
a. Manfaat metodologis. Hasil penelitian ini diharapkan akan menjadi
suatu metode yang baru dalam melakukan ekstraksi zat aktif pirantel pamoat
dalam sediaan suspensi merk “X”®
.
b. Manfaat praktis. Hasil penelitian ini diharapkan dapat menjadi
salah satu acuan metode bagi pihak industri untuk digunakan dalam analisis
penetapan kadar pirantel pamoat dalam sediaan tunggal menggunakan metode
spektrofotometri UV.
B. Tujuan Penelitian
Mendapatkan metode yang optimum dalam ekstraksi zat aktif pirantel
pamoat dari sediaan suspensi merk “X”® agar dapat ditetapkan kadarnya
5
BAB II
PENELAAHAN PUSTAKA
A.Pirantel Pamoat
Pirantel pamoat (gambar 1) merupakan turunan tetrahydropirimidine
dengan khasiat sebagai antelmintik pada saluran pencernaan dan mampu
mengobati infeksi yang disebabkan oleh beberapa jenis cacing di usus, seperti
cacing kremi (Enterobius vermicularis), cacing tambang (Necator americanus dan
Ancylostoma duodenale), cacing gelang (Ascaris lumbricoides), serta cacing
Trichostrongylus colubriformis dan Trichostrongylus orientalis (Sukarban, 1995).
Obat ini menjadi salah satu referensi obat yang sering digunakan dalam mengatasi
cacingan karena produknya yang mudah ditemukan di pasaran.
Gambar 1. Struktur Pirantel Pamoat (Anonimb, 2013)
Pirantel pamoat mengandung tidak kurang dari 97,0% dan tidak lebih
dari 103,0% C11H 14N2 S . C23H16 O6, dihitung terhadap zat anhidrat (Direktorat
Jenderal Pengawasan Obat dan Makanan RI, 1995). Pemeriannya berupa serbuk
kristal kuning sampai coklat. Zat ini praktis tidak larut dalam air, metanol, dan
etanol; larut dalam dimetil sulfoksida; serta sukar larut dalam dimetil formamida
Pirantel pamoat memberikan serapan maksimum pada dua panjang
gelombang, yakni pada panjang gelombang 300 nm dengan nilai sebesar
366 dan nilai Ɛ sebesar 21770 M-1
.cm-1, serta pada 288 nm dengan nilai
sebesar 370 dan nilai Ɛ sebesar 22000 M-1
.cm-1 (Moffat, Osselton and Widdop,
2005).
B. Suspensi
Suspensi merupakan suatu sediaan yang mengandung zat aktif ataupun
bahan obat dalam bentuk halus yang tidak larut tetapi tetap terdispersi dalam
pelarutnya. Selain zat aktif, bahan tambahan pada suspensi umumnya digunakan
untuk semakin meningkatkan kestabilannya, salah satu yang paling penting adalah
adanya suspending agent. Dibandingkan dengan bentuk sediaan kapsul atau
tablet, bahan aktif dalam sediaan suspensi memiliki keuntungan, yakni akan lebih
cepat penyerapannya oleh karena bentuk partikel yang lebih kecil dan
bioavailabilitasnya pun baik (Nanizar dan Joenoes, 1990).
Pirantel pamoat yang diformulasikan dalam bentuk sediaan suspensi oral
harus terdapat dalam cairan pembawa yang sesuai, dan terutama mengandung
basa pirantel (C11H14N2S) tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada label kemasan (Direktorat Jenderal Pengawasan
Obat dan Makanan POM RI, 1979). Beberapa komponen yang pada umumnya
terdapat dalam sediaan suspensi adalah sebagai berikut:
1. Suspending agent
Berfungsi untuk mendispersikan partikel zat aktif yang tidak larut
sedimentasi diperlambat. Bahan yang umum digunakan adalah bentonit,
CMC-Na, tragakan dan avisel.
2. Penyedap rasa dan aroma
Hal ini dimaksudkan untuk menutupi aroma yang tidak enak dari
zat aktif. Bahan yang umum digunakan adalah minyak aromatik (minyak
piperin dan minyak lemon), mentol dan peppermint.
3. Pemanis
Berfungsi untuk menutupi rasa yang tidak enak dalam suspensi
tersebut. Sukrosa adalah gula yang paling sering dipakai sebagai dalam
formulasi suatu suspensi, ataupun dapat diganti oleh gula yang lain seperti
dekstrosa, atau pengganti gula seperti sorbitol, gliserin dan propilen glikol.
4. Larutan penyangga (buffer)
Pemakaian buffer yang tepat tergantung pada pH dan kapasitas
larutan penyangga yang diperlukan. Sistem buffer yang paling dapat
diterima secara farmasi adalah sistem yang didasarkan pada karbonat,
sitrat, glukonat, laktat dan fosfat. Buffer dalam suspensi berguna untuk
menjaga pH larutan yang telah diformulasikan agar terjadi keseimbangan
antara pH yang secara fisiologis diterima dengan pH kelarutan dan
stabilitas maksimum.
5. Pewarna
Untuk menambah daya tarik suspensi digunakan bahan pewarna
digunakan umumnya larut dalam air dan kompatibel dengan bahan
tambahan lain, seperti eritrosin dan tartrazin.
6. Pengawet
Pengawet diperlukan untuk melindungi adanya pertumbuhan
mikroorganisme pada suspensi dengan air sebagai media pertumbuhannya.
Pengawet yang paling sering digunakan dalam suspensi dengan kadar
yang efektif adalah asam benzoat (batas maksimum 1 g/kg, natrium
benzoat (batas maksimum 1 g/kg) dan berbagai kombinasi metil-, propil-,
dan butil paraben (Ansel dan Howard, 1989).
C. Ekstraksi
Ekstraksi adalah metode pemisahan komponen dari suatu campuran
menggunakan pelarut yang sesuai. Ekstraksi digunakan untuk memisahkan
senyawa organik dari larutan yeng bersifat polar (pada umumnya air) dengan
larutan non polar (pada umumnya larutan organik) yang tidak saling campur dan
didiamkan hingga terbentuk dua lapisan yang kemudian dapat dipisahkan. Zat
terlarut akan terdistribusi dalam kedua lapisan tersebut berdasarkan kelarutan
relatifnya (Gandjar dan Rohman, 2007).
Faktor-faktor yang mempengaruhi laju ekstraksi adalah:
1. Tipe persiapan sampel
2. Waktu ekstraksi
3. Kuantitas pelarut
5. Tipe pelarut (Direktorat Jenderal Pengawasan Obat dan Makanan POM
RI, 1979).
D. Ekstraksi Cair-Cair
Ekstraksi cair-cair (liquid-liquid extraction) digunakan jika pemisahan
dengan teknik lainnya tidak dapat dicapai, antara lain seperti distilasi, evaporasi
dan kristalisasi. Ekstraksi cair-cair adalah proses pemisahan suatu komponen dari
fase cair ke fase cair lainnya berdasarkan kelarutan relatifnya. Teknik ekstraksi
cair-cair terdiri dari beberapa tahap, yaitu :
1. Kontak antara pelarut dengan fase cair yang mengandung komponen yang
akan diambil (solute), kemudian solute akan berpindah dari fase umpan
(diluen) ke fase pelarut.
2. Pemisahan dua fase yang tidak saling melarutkan, yaitu fase yang
banyak mengandung pelarut disebut fase ekstrak dan fase yang banyak
mengandung umpan disebut fase rafinat (Laddha and Degalesan, 1976).
Prinsip dasar ekstraksi cair-cair mengikuti Hukum Distribusi Nernst atau
disebut juga Hukum Partisi yang menyatakan bahwa “apabila suatu analit
dilarutkan ke dalam dua pelarut yang tidak saling campur, maka analit akan
terdistribusi dalam proporsi yang sama (merata) diantara dua pelarut yang tidak
saling campur”. Perbandingan konsentrasi pada kesetimbangan diantara dua
pelarut yang tidak saling campur disebut koefisien distribusi atau koefisien partisi
KD =
...(1)
Corg dan Caq masing-masing merupakan konsentrasi analit dalam fase pertama dan
dalam fase kedua. Semakin besar konsentrasi analit dalam fase pertama maka
akan semakin besar nilai koefisien distribusinya. Sebaliknya, semakin kecil
konsentrasi analit dalam fase pertama maka akan semakin kecil nilai koefisien
distribusinya.
Namun dalam kenyataannya, analit seringkali berada dalam bentuk kimia
yang berbeda karena adanya disosiasi (ionisasi), protonasi dan kompleksasi atau
polimerisasi sehingga definisinya dapat disebut rasio distribusi (D) atau rasio
partisi, yang ditulis dengan persamaan berikut:
D =
...(2)
(Cs)1 dan (Cs)2 masing-masing merupakan konsentrasi total analit (dalam segala
bentuk) dalam fase pertama dan fase kedua. Jika tidak ada interaksi antar analit
yang terjadi pada kedua fase tersebut maka nilai KD dan D adalah sama (Gandjar
dan Rohman, 2007).
Salah satu teknik ekstraksi cair-cair yang paling sering digunakan adalah
teknik ekstraksi berulang menggunakan corong pisah. Caranya paling sederhana,
yakni dengan hanya menambahkan pengekstrak yang tidak saling campur dengan
pelarut awal, kemudian dilakukan penggojogan hingga terjadi kesetimbangan
analit dalam kedua fase, didiamkan dan dipisahkan. Kelemahan ekstraksi ini yakni
kurang praktis, dan ada kemungkinan besar hilangnya analit selama proses
Dalam proses ekstraksi cair-cair, efisiensi ekstraksi (E) merupakan
parameter penting yang mendukung kesempurnaan ekstraksi tersebut. Efisiensi
ekstraksi tergantung pada nilai distribusi analit (D) dan volume relatif kedua fase.
Secara teoritis dapat dihitung jumlah analit yang terekstraksi dengan persamaan
sebagai berikut:
E =
...(3)
V1 dan V2 masing-masing merupakan volume fase pertama dan fase kedua yang
digunakan; dan D merupakan rasio distribusi. Secara teoritis, dilakukannya
ekstraksi berulang (bertingkat) dengan pelarut yang selalu baru akan
meningkatkan nilai efisiensi ekstraksi. Hal tersebut dapat dilihat berdasarkan
persamaan berikut
(Caq)n = Caq
]
n
...(4)
Keterangan : (Caq)n : banyaknya analit dalam fase air setelah n kali ekstraksi
(Caq) : banyaknya analit dalam fase air mula-mula
V1. : banyaknya volume fase organik
V2 . : banyaknya volume fase air
n : banyaknya ekstraksi (Gandjar dan Rohman, 2007).
Teknik ekstraksi cair-cair yang mulai dikembangkan akhir-akhir ini
adalah menggunakan ultrasonikator. Dalam penelitian-penelitian terdahulu,
metode ekstraksi dengan bantuan ultrasonikator digunakan untuk mengekstraksi
Hal ini tentu saja lebih efisien dibandingkan ekstraksi dengan metode
konvensional yang memerlukan waktu setidaknya 24 jam untuk mendapatkan
hasil yang sama. Dalam penelitian yang dilakukan Cameron and Wang (2006)
dibuktikan bahwa rendemen pati jagung yang diperoleh dari proses ultrasonik
selama 2 menit adalah sekitar 55,2-67,8%, hampir sama dengan rendemen yang
didapat dari pemanasan dengan air selama 1 jam, yaitu 53,4%.
Prinsip dasar penggunaan metode ultrasonikasi yaitu dengan mengamati
sifat akustik gelembung ultrasonik yang dirambatkan melalui medium yang
dilewati. Pada saat gelombang merambat, medium yang dilewatinya akan
mengalami getaran. Getaran akan memberikan pengadukan yang intensif terhadap
proses ekstraksi dan akan meningkatkan osmosis atau penetrasi dari senyawa
dengan pelarut sesuai dengan sifatnya sehingga akan meningkatkan proses
ekstraksi (Keil cit., Alupului, Calinescu andLavric 2009).
Cara kerja metode ultrasonik dalam mengekstraksi adalah sebagai beikut:
1. Gelombang ultrasonik terbentuk dari pembangkitan ultrason secara lokal
dari kavitasi mikro pada sekeliling bahan yang diekstraksi sehingga akan
terjadi pemanasan bahan tersebut dan membantu proses penetrasi senyawa
ekstrak sesuai dengan sifat pelarut pengekstrak.
2. Terdapat efek ganda yang dihasilkan yaitu pemecahan dinding sel sehingga
membebaskan kandungan senyawa yang ada di dalamnya dan pemanasan
3. Energi kinetik dilewatkan ke seluruh bagian cairan yang diikuti dengan
munculnya gelembung kavitasi pada dinding atau permukaan sehingga
meningkatkan transfer massa antara permukaan padat-cair.
4. Efek mekanik yang ditimbulkan adalah meningkatkan penetrasi dari cairan
menuju dinding membran sel, mendukung pelepasan komponen sel dan
meningkatkan transfer massa (Keil cit., Alupului, Calinescu and Lavric
2009).
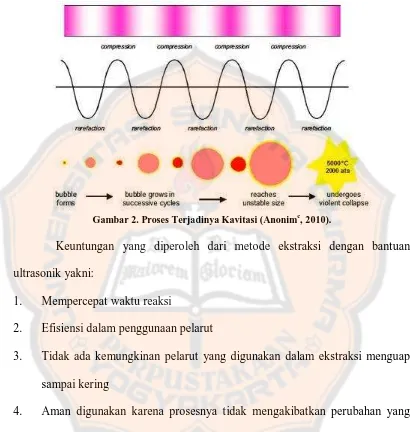
Kavitasi adalah gejala menguapnya zat cair yang sedang mengalir
sehingga membentuk gelembung-gelembung uap yang disebabkan karena
berkurangnya tekanan cairan tersebut sampai titik jenuh uapnya. Bila suatu cairan
diiradiasi dengan gelombang ultrasonik maka tekanan di dalam cairan akan
mengembang hingga tumbuh gelembung mikro (micro bubble). Jika amplitudo
yang dipacu gelombang akustik relatif besar, ketidakhomogenan lokal di dalam
cairan terjadi dan menimbulkan pertumbuhan gelombang secara serentak dalam
dimensi makroskopik. Gelembung tersebut tidak stabil pada kondisi konsentrasi
energi yang besar berakibat pertumbuhan yang tidak stabil sehingga menyebabkan
pecahnya gelembung. Faktor yang mempengaruhi kemampuan ekstraksi pada
penerapan gelombang ultrasonik dalam ekstraksi cair-cair adalah peningkatan
temperatur dalam skala molekuler, pencampuran akustik, timbulnya kavitasi dan
tegangan permukaan pada gelembung mikro, serta terbentuknya bintik panas
berupatekanan dan suhu tinggi sesaat pada dimensi molekuler (Susilo, Hawa dan
kavitasi ultrasonik menghasilkan daya yang akan memecah dinding sel secara
mekanis dan meningkatkan transfer material.
Gambar 2. Proses Terjadinya Kavitasi (Anonimc, 2010).
Keuntungan yang diperoleh dari metode ekstraksi dengan bantuan
ultrasonik yakni:
1. Mempercepat waktu reaksi
2. Efisiensi dalam penggunaan pelarut
3. Tidak ada kemungkinan pelarut yang digunakan dalam ekstraksi menguap
sampai kering
4. Aman digunakan karena prosesnya tidak mengakibatkan perubahan yang
signifikan pada struktur kimia, partikel dan senyawa bahan-bahan yang
digunakan.
5. Meningkatkan ekstraksi lipid dan protein dari biji tanaman, seperti kedelai
(misalnya, tepung kedelai atau yang dihilangkan lemak) atau bibit minyak
Kekurangan dari metode ekstraksi dengan bantuan ultrasonik yakni membutuhkan
biaya yang relatif mahal serta dapat menimbulkan bunyi yang bising (Santos,
Lodeiro, and Capelo-Martinez, 2009).
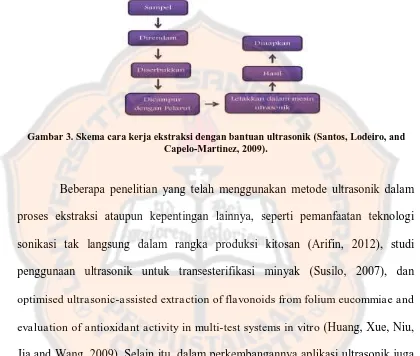
Gambar 3. Skema cara kerja ekstraksi dengan bantuan ultrasonik (Santos, Lodeiro, and
Capelo-Martinez, 2009).
Beberapa penelitian yang telah menggunakan metode ultrasonik dalam
proses ekstraksi ataupun kepentingan lainnya, seperti pemanfaatan teknologi
sonikasi tak langsung dalam rangka produksi kitosan (Arifin, 2012), studi
penggunaan ultrasonik untuk transesterifikasi minyak (Susilo, 2007), dan
optimised ultrasonic-a ssisted extra ction of flavonoids from folium eucommiae and
evaluation of antioxidant activity in multi-test systems in vitro (Huang, Xue, Niu,
Jia and Wang, 2009). Selain itu, dalam perkembangannya aplikasi ultrasonik juga
digunakan dalam pengolahan makanan, stabilisasi emulsi minyak, pengurangan
ukuran partikel, sistem penyaringan untuk partikel yang tersuspensikan,
homogenisasi, atomisasi, proteksi lingkungan, degassing suatu cairan dan transfer
E. Spektrofotometri Ultraviolet
Spektrofotometri UV-Vis adalah anggota teknik analisis spektroskopik
yang menggunakan sumber radiasi elektromegnetik ultraviolet dekat (190-380
nm) dan sinar tampak (380-780 nm) dengan menggunakan instrumen
spektrofotometer (Mulja dan Suharman, 1995). Spektrofotometri serapan
merupakan pengukuran suatu interaksi antara radiasi elektromagnetik dan molekul
atau atom dari suatu zat kimia.
Analisis secara spektrofotometri UV-Vis selalu melibatkan pembacaan
serapan radiasi elektromagnetik oleh molekul atau radiasi elektromagnetik yang
diteruskan. Keduanya dikenal sebagai serapan (A) dan transmitan dengan satuan
persen (%) T. Jika radiasi elektromagnetik dikenakan terhadap suatu zat yang
dengan intensitas radiasi datang (I0), maka hal yang terjadi radiasi tersebut dapat
diserap (Ia), diteruskan (It), dan dipantulkan (Ir) sehingga terdapat persamaan:
I0 = Ia + It + Ir ...(5)
Namun, nilai Ir (± 4%) dapat diabaikan karena digunakan larutan
pembanding dalam pengerjaannya sehingga persamaannya menjadi:
I0 = Ia + It ...(6)
Untuk mendapatkan suatu korelasi matematik antara transmitan atau
serapan terhadap intensitas radiasi atau konsentrasi zat yang dianalisis dan tebal
yang menyerap, maka didapatkan persamaan oleh Bouguer, Lambert dan Beer
T =
= 10
-Ɛbc
...(8)
A = log = Ɛbc ...(9)
Keterangan: T ..= persen transmitan
I0 = intensitas radiasi yang datang
It = intensitas radiasi yang diteruskan
A = serapan
Ɛ = daya serap molar (M-1cm-1)
Persamaan di atas dapat dijabarkan dengan asumsi sebagai berikut:
1. Jika suatu berkas radiasi monokromatik yang sejajar jatuh pada medium
penyerap pada sudut tegak lurus setiap lapisan yang sangat kecil akan
meneruskan intensitas berkas.
2. Jika suatu cahaya monokromatis mengenai pada medium yang transparan, laju
pengurangan intensitas dengan ketebalan medium sebanding dengan intensitas
cahaya.
3. Intensitas berkas sinar monokromatis berkurang secara eksponensial bila
konsentrasi zat penyerap bertambah (Khopkar, 1990).
Hubungan antara nilai dengan daya serap molar (Ɛ) adalah sebagai
berikut:
Ɛ = x M-1 cm-1 ...(10)
Nilai Ɛ merupakan daya serap molar atau koefisien ekstingsi molar. Nilai
Ɛ tiap molekul atau ion dalam pelarut tertentu memiliki karakter masing-masing,
pada panjang gelombang tertentu serta tidak dipengaruhi oleh konsentrasi dan
mempengaruhi puncak spektrum yang dihasilkan suatu zat. Beberapa karakteristik
nilai Ɛ yang berpengaruh terhadap puncak spektrum adalah sebagai berikut: 1-10
M-1.cm-1: sangat lemah; 10-102 M-1.cm-1: lemah; 102-103 M-1.cm-1: sedang; 103
-104 M-1.cm-1: kuat; 104-105 M-1.cm-1: sangat kuat (Mulja dan Suharman, 1995).
Daya serap oleh molekul dalam daerah spektrum ultraviolet dan visibel
tergantung dari struktur elektronik molekul itu sendiri. Keadaan dasar suatu
molekul organik mengandung elektron-elektron valensi dalam tiga jenis orbital
molekul utama, yaitu orbital sigma (σ), orbital pi () dan orbital elektron bebas
(n). Baik orbital σ maupun orbital dibentuk dari tumpang tindih dua orbital
atom atau hibrid. Oleh karena itu, masing-masing orbital molekul ini mempunyai
suatu orbital σ* atau * antiikatan yang berkaitan dengannya. Jika suatu molekul
dikenai oleh radiasi elektromagnetik maka akan mengakibatkan adanya eksitasi
atau transisi elektron ke tingkat energi yang lebih tinggi. Transisi-transisi elektron
mencakup promosi suatu elektron dari salah satu dari tiga keadaan dasar (σ; ;
atau n) ke salah satu dari dua keadaan eksitasi (σ* atau *). Terdapat empat
transisi yang mungkin, seperti diagram berikut :
Dalam proses penyerapan cahaya, kromofor memegang peranan penting
sebagai gugus yang berfungsi sebagai penjerap cahaya. Dalam transisi σ σ*
kromofor yang berperan adalah yang mempunyai elektron pada orbital molekul σ.
Molekul tersebut merupakan organik jenuh yang tidak mempunyai atom dengan
pasangan elektron bebas, seperti alkana (C-C dan C-H). Terjadi pada daerah
ultraviolet jauh (sekitar 150 nm) dan membutuhkan energi terbesar. Transisi n
σ* terjadi pada ultraviolet jauh, diperankan oleh kromofor dalam senyawa dengan
molekul organik jenuh yang mempunyai satu atau lebih atom dengan pasangan
elektron, seperti karbonil (C=O), C-S, C-N dan C-Cl. Transisi * terjadi pada
daerah ultraviolet jauh (sekitar 200 nm), diberikan oleh senyawa yang hanya
memiliki orbital molekul (alkena dan alkuna), seperti CC dan C=C (Anonimd,
2013).
Secara garis besar, terdapat tiga teknik untuk melakukan pengukuran
kuantitatif secara spektrofotometri, yakni sebagai berikut:
1. Analisis kuantitatif zat tunggal
Dilakukan pengukuran serapan menggunakan panjang gelombang
maksimum atau pada panjang gelombang minimum jika dilakukan pengukuran %
transmitan. Terdapat empat cara pelaksanaan analisis kuantitatif zat tunggal, yaitu:
a. Membandingkan serapan zat yang akan dianalisis dengan serapan
reference standa rd pada panjang gelombang maksimum. Persyaratannya,
pembacaan nilai serapan sampel dan reference standard tidak berbeda
b. Menggunakan kurva baku yang dipersiapkan dari larutan reference
standard dengan pelarut tertentu pada panjang gelombang maksimum.
Lalu dibuat sistem koordinat Cartesian dimana sebagai ordinat adalah
serapan dan sebagai absis adalah konsentrasi.
c. Menghitung nilai serapan jenis larutan sampel ( ) pada pelarut tertentu
dan dibandingkan dengan serapan jenis yang dianalisis, yang tertera pada
buku resmi.
d. Menggunakan perhitungan nilai ekstingsi molar (serapan molar Ɛ) sama
dengan cara (c) hanya saja perhitungan serapan molar lebih tepat karena
melibatkan massa molekul relatif.
2. Analisis kuantitatif campuran dua komponen zat
Merupakan pengembangan metode dari analisis kuantitatif zat tunggal. Pada
prinsipnya, dicari serapan atau beda serapan dari masing-masing komponen zat
yang memiliki korelasi linear dengan konsentrasi tertentu dan dihitung kadar
masing-masing komponen zat atau salah satu komponen zat yang terdapat dalam
campuran.
3. Analisis kuantitatif campuran tiga macam atau lebih zat
Prinsipnya dicari beda serapan antara masing-masing komponen
kemudian dikurangi dengan serapan yang dimiliki larutan standarnya
masing-masing (Mulja dan Suharman, 1995).
Dalam analisis kuantitatif zat tunggal pada spektrofotometri ditentukan
terlebih dahulu panjang gelombang maksimum yang didapatkan melalui
yang maksimum. Alasan digunakannya panjang gelombang maksimum adalah
sebagai berikut:
1. Memiliki kepekaan yang maksimal karena pada panjang gelombang
maksimum terjadi perubahan serapan untuk setiap satuan konsentrasi paling
besar.
2. Pada daerah sekitar panjang gelombang maksimum akan memiliki bentuk
kurva serapan yang linear (datar) sehingga hukum Lambert-Beer dapat
terpenuhi.
3. Akan memberikan kesalahan pengukuran yang kecil jika dilakukan pada
panjang gelombang maksimum (Gandjar dan Rohman, 2007).
Penggunaan pelarut yang tepat merupakan salah satu titik krusial dalam
analisis menggunakan metode spektrofotometri. Secara umum pelarut-pelarut
yang digunakan dalam spektrofotometri harus melarutkan analit, meneruskan
radiasi dalam daerah panjang gelombang yang dikehendaki, tidak memiliki sistem
ikatan rangkap terkonjugasi, tidak berwarna dan kemurniannya harus tinggi atau
derajat untuk analisis tinggi. Hal lain yang juga harus diperhatikan adalah
polaritas pelarut karena akan mempengaruhi pergeseran spektrum yang dianalisis.
Beberapa pelarut yang sering digunakan dalam daerah-daerah ultraviolet dan
visibel adalah aseton, benzen, karbon tetraklorida, kloroform, dioksan,
sikloheksan, isopropanol, diklorometan, etanol, etil, eter, metanol dan air
Secara umum rangkaian komponen penyusun spektrofotometer UV-Vis
dapat dilihat pada gambar berikut:
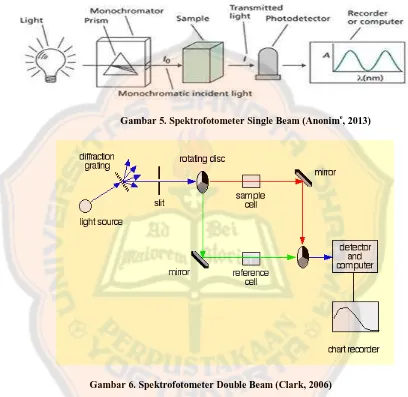
Gambar 5. Spektrofotometer Single Beam (Anonime, 2013)
Gambar 6. Spektrofotometer Double Beam (Clark, 2006)
Spektrofotometer dibagi menjadi dua jenis, yaitu spektrofotometer single
beam dan spektrofotometer double beam. Perbedaan kedua jenis spektrofotometer
tersebut terdapat pada pemberian cahaya, dimana pada single beam cahaya hanya
melewati satu arah dan yang diperoleh hanya nilai serapan dari larutan yang
dimasukkan. Berbeda dengan spektrofotometer double beam, nilai blanko dapat
satu kali proses yang sama. Prinsipnya adalah dengan adanya chopper yang akan
membagi sinar menjadi dua, dimana salah satunya melewati blanko (reference
beam) dan yang lainnya melewati larutan (sa mple beam). Spektrofotometer
double beam memiliki keunggulan yang lebih dibandingkan spektrofotometer
single beam karena nilai serapan larutannya yang telah mengalami pengurangan
nilai terhadap nilai serapan blanko. Selain itu, pada spektrofotometer double beam
juga dapat mengatasi kelemahan pada spektrofotometer single beam seperti
adanya perubahan intensitas cahaya akibat fluktuasi voltase sumber sinar.
Kelemahan spektrofotometer double beam yakni lebih rumit dan harganya lebih
mahal, dibandingkan dengan spektrofotometer single beam yang lebih sederhana
dan lebih murah (Sastrohamidjojo, 2001)
Fungsi beberapa bagian yang terdapat dalam rangkaian spektrofotometer adalah
sebagai berikut:
1. Sumber cahaya:
Sumber cahaya yang ideal untuk pengukuran serapan harus
menghasilkan spektrum yang terus-menerus dengan intensitas yang sama
pada kisaran panjang gelombang yang dijangkau. Sumber cahaya ultraviolet
yang biasa digunakan adalah lampu hidrogen dan lampu deuterium,
sedangkan untuk visibel digunakan lampu filamen tungsten atau wolfram.
2. Monokromator:
Berfungsi untuk mengubah cahaya polikromatis yang dipancarkan
sumber cahaya menjadi monokromatis (panjang gelombang tunggal) dan
yang mampu meneruskan radiasi pada daerah panjang gelombang tertentu
dan menyerap radiasi pada panjang gelombang yang lain.
3. Tempat cuplikan:
Cuplikan yang digunakan ditempatkan pada suatu sel atau yang
dikenal sebagai kuvet. Untuk daerah ultraviolet biasanya digunakan Quartz
atau sel dari silika yang dilebur, sedangkan untuk daerah visibel digunakan
gelas biasa atau Quartz.
4. Detektor:
Berfungsi untuk memberikan respon terhadap cahaya pada berbagai
panjang gelombang dan mengubah tenaga tersebut untuk dapat diukur
secara kuantitatif yang dicatat oleh meter pencatat (recorder)
(Sastrohamidjojo, 2001).
F. Landasan Teori
Berdasarkan karakteristik dan struktur pirantel pamoat, maka dapat
dilakukan analisis mengenai penetapan kadar pirantel pamoat, baik secara metode
spektrofometri maupun metode kromatografi. Hal ini telah dilaporkan dalam
jurnal-jurnal penelitian terdahulu tentang analisisnya. Metode penetapan kadar
pirantel pamoat dapat didahului dengan adanya ekstraksi zat aktif pirantel pamoat
dari bentuk sediaannya. Terdapat 2 metode ekstraksi yang bisa digunakan, yakni
ekstraksi cair-cair (liquid-liquid extraction) menggunakan corong pisah dan
ultrasonikator. Ekstraksi cair-cair menggunakan corong pisah memiliki kelebihan
yaitu teknik ekstraksinya yang sederhana, tetapi kurang praktis, kemungkinan
tergantung pada banyaknya ekstraksi yang dilakukan dan volume pelarut yang
digunakan. Dalam penelitian ini ekstraksi cair-cair menggunakan corong pisah
dilakukan selama 1 menit dengan pengulangan menggunakan pelarut yang baru
sebanyak 3 kali. Sedangkan pada ekstraksi menggunakan ultrasonikator,
berlangsung selama 15 menit, dimana pada prinsip kerjanya gelombang ultrasonik
yang dirambatkan melalui medium air akan menghasilkan getaran yang dapat
berperan sebagai pengadukan yang intensif sehingga kontak antara analit dan
pelarut lebih sering dan konstan. Efek lain yang dapat ditimbulkan karena adanya
getaran tersebut adalah peningkatan temperatur secara molekuler yang akan
mengakibatkan pecahnya gelembung-gelembung analit menjadi kecil (kavitasi)
sehingga memperbesar luas permukaan kontak analit dengan pelarut yang sesuai
dengan kelarutannya. Semakin besar luas permukaan kontak antara analit dan
pelarut, maka akan makin besar pula proses transfer material atau kelarutan analit
pada pelarut yang sesuai. Hal ini tentu saja akan dapat meningkatkan hasil
ekstraksi. Kelebihan lainnya, yakni lebih banyak dalam mengekstraksi pirantel
pamoat, lebih praktis dan tidak mengakibatkan perubahan struktur kimia dari
G. Hipotesis
Berdasarkan uraian di atas, dapat ditegakkan hipotesis bahwa cara
ekstraksi cair-cair menggunakan ultrasonikator akan lebih banyak mengekstraksi
bahan tambahan lain dalam sampel dibandingkan menggunakan corong pisah
sehingga dapat menghilangkan bahan-bahan tambahan yang bisa saja dapat
mengganggu dalam pengukuran zat aktif pirantel pamoat menggunakan
27
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian eksperimental dengan rancangan
penelitian eksperimental murni karena adanya perlakuan terhadap subyek uji serta
dilakukan randomisasi saat pengambilan sampel.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah metode ekstraksi cair-cair
menggunakan corong pisah dan ultrasonikator.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah kadar pirantel pamoat
yang terekstraksi.
3. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah bahan baku
pirantel pamoat yang digunakan memiliki kemurnian yang tinggi,
pengotor-pengotor yang berasal dari alat-alat gelas yang digunakan dikendalikan dengan
mencuci alat menggunakan asam pencuci, pengaruh paparan cahaya yang
mempengaruhi stabilitas pirantel pamoat sehingga dalam preparasinya ditutup
menggunakan alumunium foil, dan pelarut yang digunakan adalah pelarut dengan
C. Definisi Operasional
1. Baku pirantel pamoat yang dianalisis adalah baku pirantel pamoat yang
diperoleh dari P.T. Konimex, Indonesia (Certificate of Analysis pada
lampiran 1).
2. Optimasi dilakukan dengan membandingkan dua metode ekstraksi sehingga
diperoleh metode yang paling optimum untuk menetapkan kadar pirantel
pamoat.
3. Metode ekstraksi yang optimum dapat diketahui dari parameter presisi dan
akurasi.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah baku pirantel
pamoat (PT Konimex) dengan kemurnian 102,3 % secara HPLC, Metanol,
Heksan, Dimethyl sulfoxide dried (max 0,05 % H2O), (p.a., E.Merck), kertas
saring, kapas, akuades (Laboratorium Kimia Analisis Instrumental USD),
suspensi oral “X”®
yang mengandung pirantel pamoat.
E. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini meliputi spektrofotometer
UV-Vis merk Shimadzu UV-1800, kuvet UV merk Hellma, neraca analitik merk
Ohaus dengan kepekaan 0,1 mg (4 angka di belakang koma, satuan g), hot plate
merk LabTech, mikropipet skala 100-1000 µL merk Socorex, vortex merk Genie,
ultrasonikator merk Retsch UR-275, corong pisah merk Pyrex dan seperangkat
F. Tata Cara Penelitian
1. Pembuatan larutan stok baku pirantel pamoat (1 mg/mL)
Ditimbang saksama kurang lebih 100,0 mg baku pirantel pamoat,
dimasukkan ke dalam labu takar 100,0 mL, larutkan dengan DMSO sebanyak 8
mL dan encerkan dengan metanol hingga batas tanda.
2. Penentuan panjang gelombang maksimum pirantel pamoat
Dipipet 100; 200; dan 300 µL larutan stok baku pirantel pamoat 1 mg/mL,
dimasukkan ke dalam labu takar 10,0 mL dan encerkan dengan metanol hingga
batas tanda sehingga diperoleh kadar seri baku 10; 20; dan 30 µg/mL. Larutan
discan pada spektrofotometer UV-Vis antara panjang gelombang 200-400 nm
sehingga diperoleh spektrum serapan dan panjang gelombang maksimum.
3. Pembuatan larutan seri baku dan kurva baku pirantel pamoat
Dipipet 100; 150; 200; 250; dan 300 µL dari larutan stok baku pirantel
pamoat 1 mg/mL, kemudian dimasukkan ke dalam labu takar 10,0 mL. Encerkan
dengan metanol hingga batas tanda sehingga diperoleh kadar seri baku sebesar 10;
15; 20; 25; dan 30 µg/mL. Serapannya diukur pada panjang gelombang
maksimum yang diperoleh menggunakan spektrofotometer UV-Vis. Dibuat kurva
regresi linear antara kadar pirantel pamoat dan serapannya, kemudian tentukan
persamaan garis regresi linear dan nilai koefisien korelasinya. Suatu metode
dikatakan memiliki linearitas yang baik apabila memenuhi syarat, yakni memiliki
nilai koefisien korelasi (r)-nya ≥ 0,999, terutama untuk penetapan kadar senyawa
4. Penetapan kadar pirantel pamoat dalam sampel sediaan suspensi pirantel pamoat merk “X”®
a. Pembuatan larutan induk sampel pirantel pamoat (0,5 mg/mL). Dipipet
sampel sediaan suspensi pirantel pamoat merk “X”®
yang setara dengan
50,0 mg pirantel pamoat. Suspensi yang telah dipipet dilarutkan dengan
dimethyl sulfoxida (DMSO) sebanyak 6,0 mL, kemudian encerkan
dengan metanol dalam labu takar hingga volume tepat 100,0 mL. Larutan
kemudian disaring dengan melewatkan larutan sampel melalui corong
dengan kertas saring dan kapas sebagai penyaring.
b. Ekstraksi pirantel pamoat dengan metode ekstraksi cair-cair
menggunakan corong pisah. Dipipet 10,0 mL filtrat yang diperoleh
(larutan 4.a), kemudian dimasukkan ke dalam corong pisah. Tambahkan
10,0 mL heksan dan lakukan ekstraksi selama 1 menit. Fase heksan
dipisahkan dan ditampung dalam flakon. Lakukan ekstraksi berulang
sebanyak 3 kali dengan heksan sebanyak 10,0 mL. Fase metanol yang
telah diekstraksi ditampung dalam beaker glass, kemudian diuapkan
menggunakan hot plate sampai kering di lemari asam.
c. Ekstraksi pirantel pamoat dengan metode ekstraksi cair-cair
menggunakan ultrasonikator. Dipipet 10,0 mL filtrat yang diperoleh
(larutan 4.a), kemudian dimasukkan ke dalam beaker glass. Tambahkan
heksan sebanyak 30,0 mL. Lakukan ekstraksi menggunakan
ultrasonikator yang telah diisi air sebelumnya selama 15 menit. Fase
dalam beaker glass dan uapkan menggunakan hot plate sampai kering di
lemari asam.
d. Penetapan kadar pirantel pamoat dalam sampel sediaan suspensi pirantel
pamoat merk “X”®
. Hasil isolasi dengan cara ekstraksi menggunakan
corong pisah (4.b) dan dengan cara ekstraksi menggunakan ultrasonikator
(4.c) yang telah diuapkan kemudian masing-masing dilarutkan dengan
metanol dalam labu takar hingga volume tepat 25,0 mL. Larutan
kemudian dipipet masing-masing 1,5 mL dan encerkan dengan metanol
dalam labu takar sampai volume tepat 10,0 mL. Ukur serapannya
menggunakan spektrofotometer UV-Vis pada panjang gelombang
maksimum. Lakukan 6 kali replikasi untuk masing-masing metode
ekstraksi sehingga diperoleh 6 data. Hitung nilai coefficient of variation
(CV) dari serapan yang dihasilkan. Tentukan kadar yang diperoleh
menggunakan persamaan kurva baku, kemudian hitung persen perolehan
Gambar 7. Skema Penetapan Kadar Pirantel Pamoat
G. Analisis Hasil
Hasil optimasi perbandingan metode ekstraksi pirantel pamoat dalam
sediaan suspensi merk “X”®
dapat dilihat dari:
1. Panjang gelombang maksimum
Panjang gelombang maksimum yang dipilih adalah panjang gelombang
dimana pirantel pamoat memberikan serapan yang paling besar.
2. Metode ekstraksi optimum
a. Presisi. Metode ekstraksi optimum yang dipilih adalah metode ekstraksi
yang menghasilkan serapan yang reprodusibel dengan nilai coefficient of
variation (CV) berada dalam rentang kriteria yang berlaku.
CV =
x 100 % ...(12)
Kriteria presisi yang diterima untuk kadar zat analit 100 % adalah CV
b. Akurasi. Akurasi metode analisis dinyatakan dengan % perolehan
kembali (recovery) yang dihitung dengan cara sebagai berikut:
% recovery =
x 100 % ...(13)
Kriteria akurasi yang diterima untuk kadar zat analit 100 % adalah pada
34
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Larutan Baku Pirantel Pamoat
Larutan baku pirantel pamoat digunakan untuk optimasi metode ekstraksi
pirantel pamoat dalam sediaan suspensi merk “X®” sebagai pembanding untuk
memastikan analit yang terkandung dalam sampel adalah pirantel pamoat.
Kepastian mengenai analit yang terdapat di dalam sampel benar adalah analit yang
dimaksud dapat dilihat dari kesamaan spektra serapan yang diperoleh serta
mampu memberikan serapan paling besar pada panjang gelombang maksimum
yang telah ditentukan. Pelarut yang digunakan dalam penelitian adalah dimetil
sulfoksida (DMSO) karena analit dapat larut dengan baik dalam DMSO, serta
metanol p.a. dengan kemurnian tinggi (99,85%) karena panjang gelombang
maksimum yang dihasilkan analit pada literatur menggunakan pelarut metanol
(Moffat, Osselton and Widdop, 2005).
Konsentrasi larutan stok baku pirantel pamoat yang dibuat dalam
penelitian ini sebesar 100 µg/mL, yang kemudian digunakan untuk membuat 3
tingkat konsentrasi larutan seri baku pada penentuan panjang gelombang
maksimum, yaitu 10; 20; dan 30 µg/mL serta 5 tingkat konsentrasi untuk
B. Optimasi Penentuan Panjang Gelombang Maksimum Pirantel Pamoat
Penentuan panjang gelombang maksimum bertujuan untuk mengetahui
panjang gelombang dimana pirantel pamoat memberikan nilai serapan yang
paling besar untuk dibaca oleh detektor spetktrofotometri UV-Vis. Analisis
dilakukan pada panjang gelombang maksimum agar meningkatkan sensitivitas
alat dalam mendeteksi suatu analit, dimana pada daerah sekitar puncak kurva
panjang gelombang maksimum memiliki fluktuasi atau ketidakstabilan nilai
serapan yang minimal sehingga kesalahan pembacaan oleh detektor dapat
diminimalkan. Selanjutnya, panjang gelombang maksimum yang telah diperoleh
digunakan untuk mengukur serapan pirantel pamoat yang dianalisis.
Pengukuran panjang gelombang maksimum dilakukan menggunakan 3
seri kadar dengan tujuan untuk mengetahui keterulangan respon analit jika
konsentrasinya ditingkatkan serta meyakinkan hasil yang diperoleh benar-benar
panjang gelombang serapan maksimum pirantel pamoat. Seri kadar yang
digunakan adalah 10; 20; dan 30 µg/mL. Seri kadar tersebut mewakili seri kadar
rendah, sedang dan tinggi. Pembacaan serapan (scanning) dilakukan pada rentang
panjang gelombang 200-400 nm disebabkan karena panjang gelombang
maksimum pirantel pamoat berada pada rentang panjang gelombang tersebut.
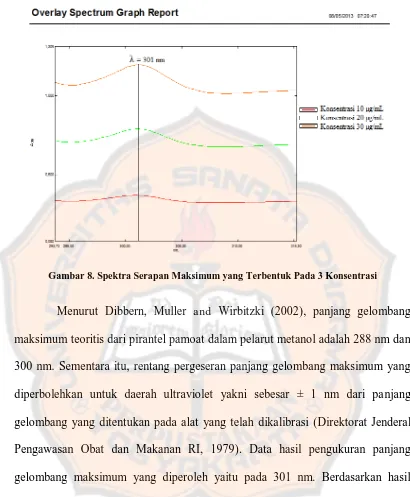
Gambar 8. Spektra Serapan Maksimum yang Terbentuk Pada 3 Konsentrasi
Menurut Dibbern, Muller and Wirbitzki (2002), panjang gelombang
maksimum teoritis dari pirantel pamoat dalam pelarut metanol adalah 288 nm dan
300 nm. Sementara itu, rentang pergeseran panjang gelombang maksimum yang
diperbolehkan untuk daerah ultraviolet yakni sebesar ± 1 nm dari panjang
gelombang yang ditentukan pada alat yang telah dikalibrasi (Direktorat Jenderal
Pengawasan Obat dan Makanan RI, 1979). Data hasil pengukuran panjang
gelombang maksimum yang diperoleh yaitu pada 301 nm. Berdasarkan hasil
tersebut diketahui bahwa panjang gelombang hasil pengukuran tidak menyimpang
lebih dari 1 nm dari panjang geombang teoritis (300 nm) sehingga dapat
dipastikan bahwa senyawa tersebut merupakan pirantel pamoat.
Digunakan panjang gelombang 300 nm sebagai acuan karena pada
panjang gelombang tersebut tidak mendapat gangguan yang disebabkan adanya
(DMSO) yang memiliki serapan (UV cut-off) pada 268 nm dan metanol dengan
nilai serapan (UV cut-off) 205 nm (Snyder, Kirkland and Glajch, 1997). Adanya
perbedaan panjang gelombang hasil pengukuran dengan panjang gelombang
teoritis dapat disebabkan karena kondisi penelitian yang berbeda, baik dari
spesifikasi alat yang digunakan serta bahan-bahan yang digunakan selama
penelitian.
Syarat suatu senyawa dapat ditetapkan kadarnya secara spektrofotometri
ultraviolet yakni memiliki gugus kromofor dan gugus auksokrom. Pirantel pamoat
memiliki gugus kromofor yang bertanggung jawab terhadap penyerapan radiasi
sinar. Gugus auksokrom berperan dalam pergeseran panjang gelombang dan
intensitas serapan maksimum suatu senyawa. Gugus kromofor dan auksokrom
dari pirantel pamoat ditunjukkan pada gambar berikut:
C. Pembuatan Kurva Baku Pirantel Pamoat
Pembuatan kurva baku pirantel pamoat bertujuan untuk mendapatkan
persamaan regresi linear sehingga dapat digunakan untuk analisis kuantitatif.
Kurva baku menyatakan hubungan antara konsentrasi dengan nilai serapan
dimana dengan meningkatnya konsentrasi yang digunakan maka akan
meningkatkan nilai serapan yang dihasilkan secara proporsional. Persamaan
regresi linear dapat diperoleh dengan melakukan pengukuran analit minimal lima
level (macam) konsentrasi analit (Anonimf, 2005).
Pada penelitian ini menggunakan 5 seri konsentrasi larutan baku pirantel
pamoat, yakni sebesar 10; 15; 20; 25 dan 30 yang masing-masing
dilakukan replikasi sebanyak 3 kali (Snyder, Kirkland, and Glajch, 1997).
Dilakukan replikasi sebanyak 3 kali bertujuan untuk mendapatkan kurva baku
dengan nilai koefisien korelasi (r) yang paling baik. Hal penting yang perlu
dipertimbangkan dalam penentuan kurva baku beberapa replikasi yaitu
berdasarkan pada nilai r terhitung, dimana suatu metode dikatakan memiliki
linearitas yang baik jika memiliki nilai r > 0,999 (Snyder, Kirkland,