PEMANFAATAN LIMBAH TULANG IKAN TUNA (Thunnus sp.) SEBAGAI SUMBER KALSIUM DENGAN METODE
HIDROLISIS PROTEIN
Oleh : Muhammad Nabil
C03400041
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR 2 0 0 5
RINGKASAN
MUHAMMAD NABIL. C03400041. Pemanfaatan Limbah Tulang Ikan Tuna (Thunnus sp.) sebagai Sumber Kalsium dengan Metode Hidrolisis Protein. Dibimbing oleh WINI TRILAKSANI dan ELLA SALAMAH
Tulang ikan tuna merupakan limbah hasil pengolahan ikan yang kaya akan kandungan kalsium, fosfor dan selenium. Pemanfaatan tulang tuna sebagai sumber kalsium pangan merupakan salah satu upaya dalam rangka memenuhi kebutuhan kalsium pangan sekaligus menambah nilai ekonomis limbah tulang ikan tuna. Tujuan dari penelitian ini adalah menghasilkan tepung tulang ikan tuna berkalsium tinggi serta mempelajari pengaruh waktu autoklafing dan frekuensi perebusan pada proses hidrolisis protein dalam pembuatan tepung tulang. Rancangan percobaan yang digunakan adalah rancangan acak lengkap (RAL) faktorial yang terdiri atas dua faktor, yaitu faktor waktu autoklafing (1, 2 dan 3 jam) dan frekuensi perebusan (1, 2 dan 3 kali). Periode waktu dan suhu perebusan yang digunakan adalah 30 menit pada suhu 100 oC.
Perlakuan waktu autoklafing dan frekuensi perebusan berpengaruh terhadap penurunan rendemen, kadar air, lemak, protein dan pH tepung tulang ikan, sedangkan kadar abu, derajat putih, kalsium dan fosfor tepung cenderung meningkat akibat adanya perlakuan. Hasil analisis ragam menunjukkan bahwa perlakuan waktu autoklafing berpengaruh nyata terhadap perubahan kadar air, abu, lemak, protein, derajat putih dan rendemen. Perlakuan perebusan hanya berpengaruh nyata pada rendemen, kadar abu dan derajat putih. Pengaruh interaksi kedua perlakuan hanya berbeda nyata pada rendemen, kadar abu dan derajat putih.
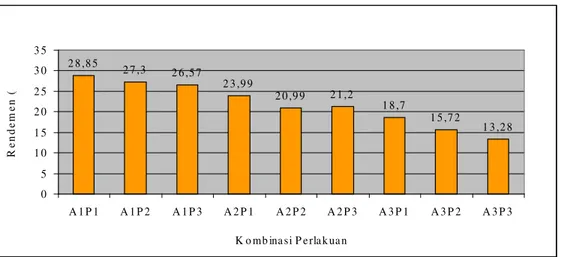
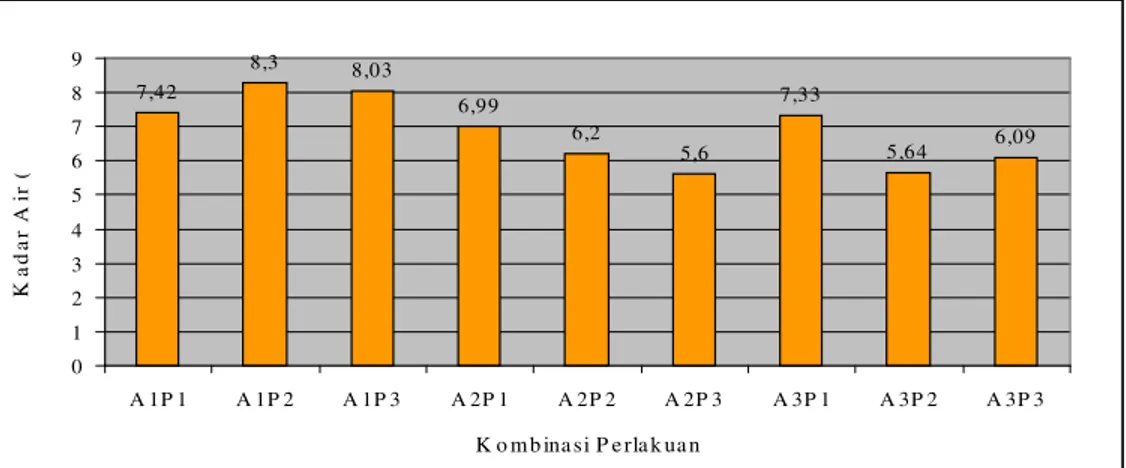
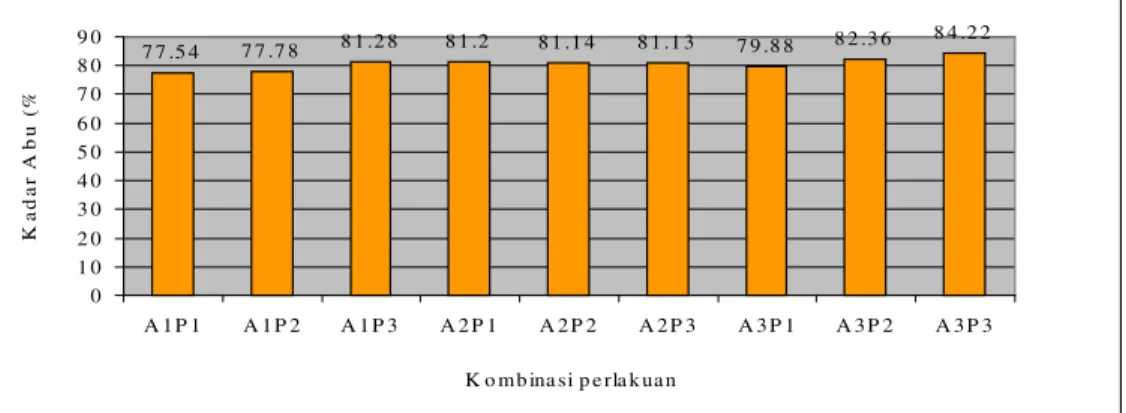
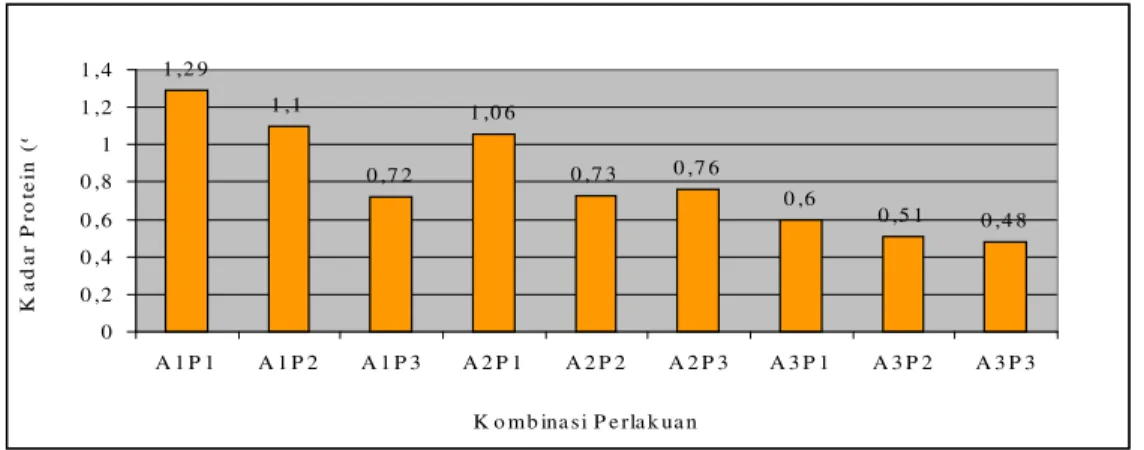
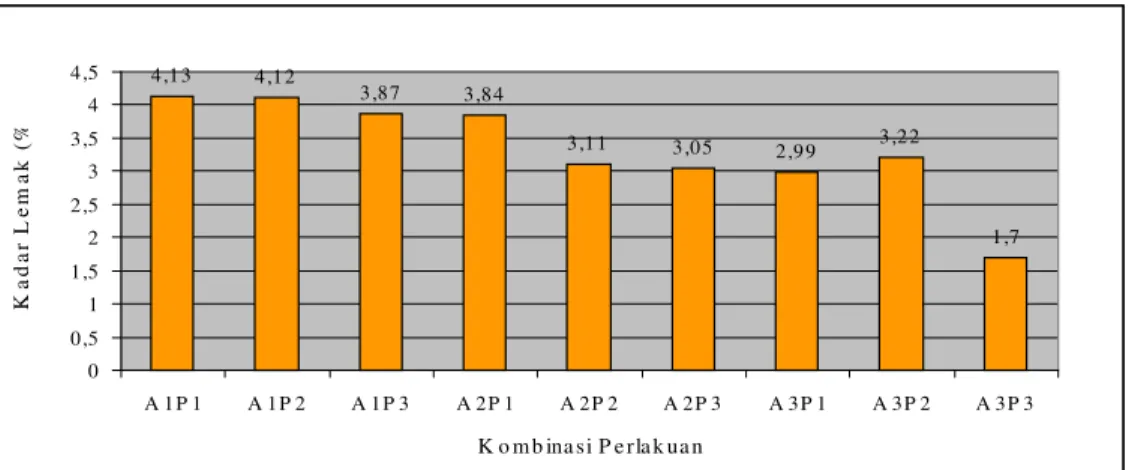
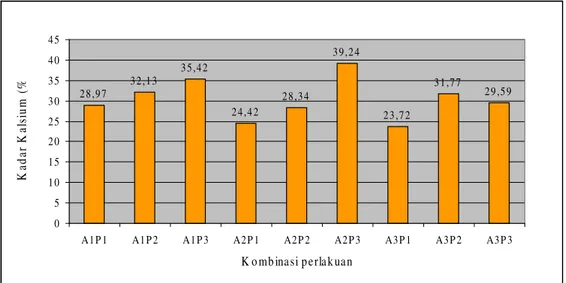
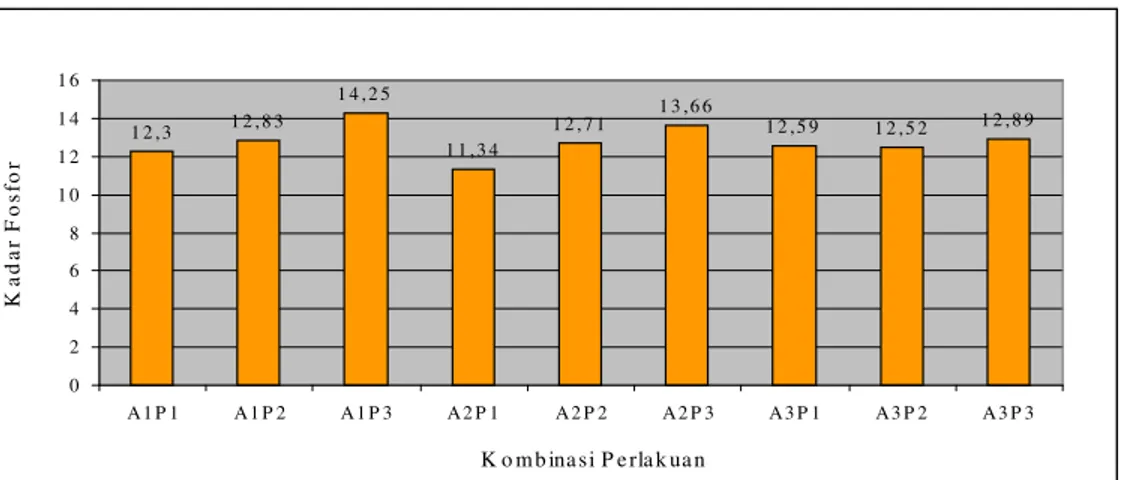
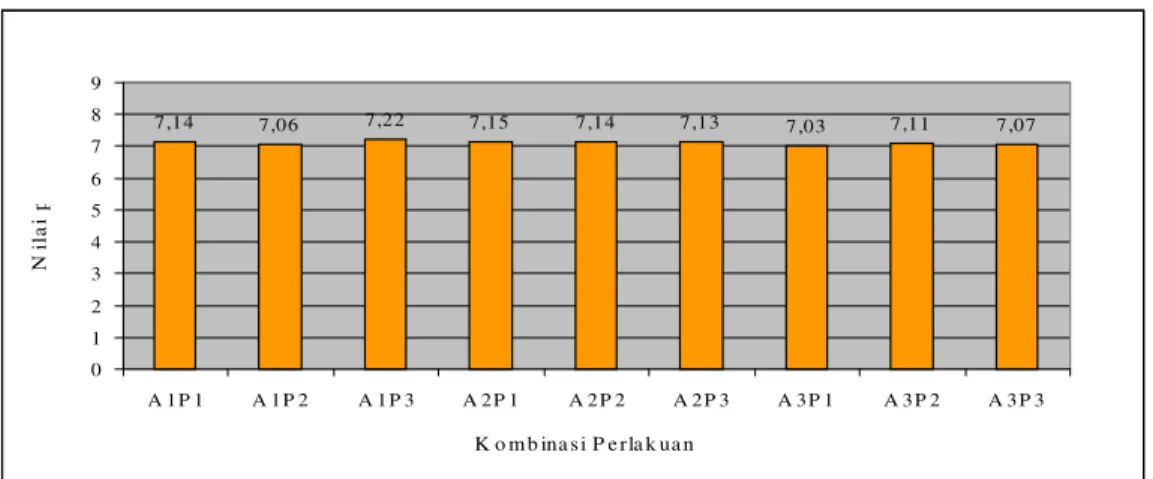
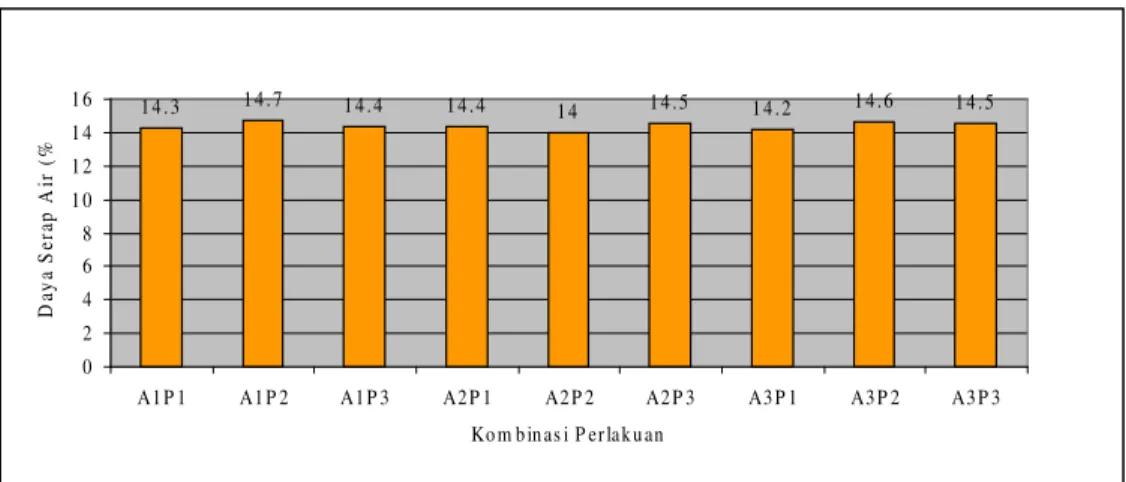
Tepung tulang ikan yang dihasilkan dalam penelitian ini mengandung kadar air sebesar 5,60 - 8,30 %, abu 77,54 – 84,22 % bb, protein 0,48 – 1,29 % bb dan lemak 1,7 - 4,13 % bb. Kadar kalsium dan fosfor yang dihasilkan berturut-turut sebesar 23,72 – 39,24 % dan 11,34 – 14,25 %. Rendemen yang dihasilkan sebesar 13,28 – 28,85 %. Nilai beberapa parameter fisik tepung tulang yang dihasilkan yaitu derajat putih 59,3 – 74,8 %, densitas kamba 7,42 – 9,42 g/ml, pH 7,03 – 7,22 dan daya serap air 14 – 14,7 %. Kemudahan melarut tepung sangat rendah, yaitu antara 0 – 4,45 % pada menit ke 15, sedangkan pada menit ke 180 nilai kelarutan yang diperoleh mencapai 8, 56 - 36,67 %.
Nilai bioavailabilitas kalsium secara in vitro yang dihasilkan tepung tulang ikan sebesar 0,86 %. Nilai penyerapan ini diperoleh dari hasil pengukuran pada tepung dengan kadar kalsium tertinggi (39,24 %) yaitu tepung A3P2 dengan perlakuan waktu autoklafing 3 jam dan perebusan 2 kali.
PEMANFAATAN LIMBAH TULANG IKAN TUNA (Thunnus sp.) SEBAGAI SUMBER KALSIUM DENGAN METODE
HIDROLISIS PROTEIN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh : Muhammad Nabil
C03400041
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR 2 0 0 5
Judul : PEMANFAATAN LIMBAH TULANG IKAN TUNA (Thunnus sp.) SEBAGAI SUMBER KALSIUM DENGAN METODE HIDROLISIS PROTEIN
Nama : Muhammad Nabil NRP : C03400041
Menyetujui,
Pembimbing I Pembimbing II
Ir. Wini Trilaksani, M.Sc. Dra. Ella Salamah, M.Si. NIP. 131 578 851 NIP. 131 788 597
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
RIWAYAT HIDUP
Penulis dilahirkan di Pekalongan pada tanggal 25 Mei 1982, sebagai anak ketiga dari sebelas orang bersaudara pasangan Muhammad Chuzaini dan Nur Chasanah. Riwayat pendidikan penulis dimulai dari SD Negeri Kedungwuni VI Pekalongan pada tahun 1988 - 1994. Penulis melanjutkan sekolah di SLTP Negeri 1 Wonopringgo Pekalongan dan lulus pada tahun 1997. Kemudian pada tahun yang sama penulis melanjutkan sekolah di SMU Negeri 1 Kedungwuni Pekalongan dan lulus pada tahun 2000. Penulis diterima sebagai mahasiswa IPB pada Program Studi Teknologi Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor pada tahun 2000 melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama menjadi mahasiswa IPB penulis pernah aktif di beberapa organisasi mahasiswa seperti DPM TPB, BEM FPIK, Himpunan Mahasiswa Teknologi Hasil Perikanan (HIMASILKAN) sebagai ketua umum periode 2003/2004, BEM KM IPB, serta Ikatan Mahasiswa Pekalongan Batang di Bogor (IMAPEKA) sebagai ketua umum. Penulis juga pernah menjadi asisten praktikum pada mata kuliah Avertebrata Air, Ikhtiologi dan Biokimia Hasil Perikanan. Penulis pernah magang di PT. Maya Food Industry dan pernah meraih medali perak untuk juara poster terbaik dalam Pekan Ilmiah Mahasiswa Nasional ke XVII di Bandung.
Penulis dinyatakan lulus dari Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor dengan hasil penelitian (skripsi) berjudul “Pemanfaatan Limbah Tulang Ikan Tuna (Thunnus sp.) sebagai Sumber Kalsium dengan Metode Hidrolisis Protein” pada tanggal 26 Oktober 2005.
KATA PENGANTAR
Segala puji syukur kehadirat Allah SWT atas anugerah, rahmat, dan hidayah yang telah diberikan-Nya kepada penulis dalam menyelesaikan penulisan skripsi dengan judul “Pemanfaatan Limbah Tulang Ikan Tuna (Thunnus sp.) sebagai Sumber Kalsium dengan Metode Hidrolisis Protein”.
Pada kesempatan ini penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Ir. Wini Trilaksani, M.Sc. sebagai ketua komisi pembimbing dan Ibu Dra. Ella Salamah, M.Si. selaku anggota komisi pembimbing yang telah bersedia membimbing penulis dalam penyelesaian skripsi ini.
2. Bapak Dr. Ir. Joko Santoso, M.Si. dan Ibu Tati Nurhayati, S.Pi, M.Si. sebagai dosen penguji atas masukan dan kritik yang membangun untuk perbaikan skripsi ini.
3. Bapak dan Ibu M.Chuzaini tercinta atas doa, kasih sayang, dorongan dan semangat yang diberikan.
4. Kakak dan adik-adik serta seluruh keluargaku, kalian adalah semangat yang mengobarkan perjuanganku.
5. Bapak Gandi dan Ibu Emma sebagai staf laboratorium Teknologi Hasil Perikanan yang telah banyak membantu penulis selama penelitian.
6. Sahabat-sahabatku Mahardiyan, Rhea, Henny, Yanne, Nano, Ismail, Hazil, Slamet, Dina, Leni, Citra, Nila, Sri Rahayu, Darma, Pai, Diki, Netto, Kacong, Venol dan Adit. Yakinlah kesuksesan pasti jadi milik kita.
7. Teman-teman AHP dan THP’37, 38, 39, 40 dan 41 tetap bersemangat dalam menuntut ilmu, jangan sia-siakan waktumu.
Akhir kata penulis berharap skripsi ini bermanfaat bagi semua pihak dan menjadi amal bagi penulis. Amin
Bogor, Oktober 2005
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
1. PENDAHULUAN... 1
1.1. Latar Belakang ... 1
1.2. Tujuan ... 3
2. TINJAUAN PUSTAKA... 4
2.1. Ikan Tuna (Thunnus sp.) ... 4
2.2. Limbah Perikanan... 5 2.3. Tulang Ikan ... 6 2.4. Kalsium... 7 2.4.1. Peranan kalsium ... 7 2.4.2. Kebutuhan kalsium... 8 2.4.3. Sumber kalsium... 9 2.4.4. Metabolisme kalsium... 10
2.4.5. Faktor yang mempengaruhi penyerapan kalsium ... 11
2.4.5.1. Fosfor... 11
2.4.5.2. Vitamin D ... 12
2.4.5.3. Protein... 12
2.4.5.4. Nilai pH dan kelarutan... 13
2.4.5.5. Zat organik... 13
2.4.5.6. Serat makanan ... 13
2.4.5.7. Faktor lain... 14
2.4.6. Proses pemisahan kalsium ... 14
2.4.6.1. Hidrolisis... 18 2.4.6.2. Pemasakan ... 19 2.4.6.3. Pengeringan... 20 2.5. Bioavailabilitas Kalsium... 21 2.6. Osteoporosis... 22 3. METODOLOGI ... 24
3.1. Waktu dan Tempat ... 24
3.2. Bahan dan Alat ... 24
3.3. Metode Penelitian... 25
3.3.1. Alur proses pemisahan kalsium ikan ... 25
3.2.2. Perlakuan... 27
3.4. Metode Analisis... 27
3.4.1. Rendemen (AOAC 1995) ... 27
3.4.2. Kadar air (AOAC 1995) ... 27
3.4.3. Kadar protein (AOAC 1995)... 28
3.4.4. Kadar lemak (AOAC 1995) ... 28
3.4.5. Kadar abu (AOAC 1995)... 29
3.4.6. Kadar kalsium (Apriyantono et al. 1989)... 29
3.4.7. Kadar fosfor (Apriyantono et al. 1989)... 30
3.4.8. Derajat keasaman (pH) (AOAC 1995) ... 31
3.4.9. Daya serap air (Fardiaz et al. 1992) ... 31
3.4.10. Densitas kamba (Wirakartakusumah et al. 1992)... 31
3.4.11. Derajat putih (Kett Whiteness Electric Laboratory 1981 diacu dalam Mulia 2004) ... 32
3.4.12. Kemudahan melarut (Pedroza-Isleas et al. 2000 diacu dalam Beatrice 2001)... 32
3.4.13. Bioavailabilitas kalsium (Roig et al. 1999)... 32
3.5 Rancangan Percobaan dan Analisis Data... 34
4. HASIL DAN PEMBAHASAN... 35
4.1. Rendemen ... 35 4.2. Analisis Proksimat... 36 4.2.1. Kadar air ... 37 4.2.2. Kadar abu... 39 4.2.3. Kadar protein ... 41 4.2.4. Kadar lemak ... 44 4.3. Kadar Kalsium ... 48 4.4. Kadar Fosfor ... 49 4.5. Derajat Keasaman (pH)... 50
4.6. Daya Serap Air... 51
4.7. Densitas Kamba ... 52
4.8. Derajat Putih ... 54
4.9. Kemudahan Melarut... 56
4.10. Bioavailabilitas Kalsium ... 58
5. KESIMPULAN DAN SARAN... 60
5.1. Kesimpulan ... 60
5.2. Saran... 60
DAFTAR PUSTAKA ... 61
DAFTAR TABEL
Halaman
1. Komposisi kimia tulang ikan tuna ...…… 6
2. Angka kecukupan rata-rata kalsium (mg/hari)…....……….. 8
3. Kandungan zat gizi tepung tulang ikan produksi ISA...…. 10
DAFTAR GAMBAR
Halaman
1. Ikan yellow fin tuna (Thunnus albacores)...…... 4
2. Alur proses pembuatan tepung tulang ikan metode Elfauziah (2003)... 16
3. Alur proses pembuatan tepung tulang ikan Metode Mulia (2004)... 17
4. Mekanisme reaksi hidrolisis... 18
5. Alur proses pembuatan tepung tulang ikan tuna... 26
6. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap rendemen ...… ... 35
7. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar air ... 37
8. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar abu ... 39
9. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar protein ... 42
10. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar lemak... 45
11. Reaksi antara trigliserida dengan NaOH... 47
12. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar kalsium... 48
13. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap kadar fosfor ... 49
14. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap nilai pH ... 51
15. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap nilai daya serap air... 52
16. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap densitas kamba... 53
17. Histogram hubungan lamanya waktu autoklafing dan frekuensi perebusan terhadap derajat putih... 55
DAFTAR LAMPIRAN
Halaman
1. Data rendemen tepung tulang ikan tuna (%) ...…… 68
2. Analisis ragam rendemen tepung tulang ikan tuna (%)...…… 68
3. Uji lanjut BNJ lama waktu autoklafing terhadap rendemen... 68
4. Data kadar air (% bb) tepung tulang ikan tuna...…… 69
5. Analisis ragam kadar air...…. 69
6. Uji lanjut BNJ lama waktu autoklafing terhadap kadar air... 69
7. Data kadar abu (% bb) tepung tulang ikan tuna...…… 70
8. Analisis ragam kadar abu...…. 70
9. Uji lanjut BNJ lama waktu autoklafing terhadap kadar abu ... 70
10. Uji lanjut BNJ frekuensi perebusan terhadap kadar abu... 71
11. Data kadar protein (% bb) tepung tulang ikan tuna...…… 73
12. Analisis ragam kadar protein...…. 73
13. Uji lanjut BNJ lama waktu autoklafing terhadap kadar protein... 73
14. Uji lanjut BNJ frekuensi perebusan terhadap kadar protein... 74
15. Data kadar lemak (% bb) tepung tulang ikan tuna...…… 74
16. Analisis ragam kadar lemak...…. 74
17. Uji lanjut BNJ lama waktu autoklafing terhadap kadar lemak... 75
18. Uji lanjut BNJ frekuensi perebusan terhadap kadar lemak... 75
19. Data kadar kalsium (%) tepung tulang ikan tuna...…… 75
20. Analisis ragam kadar kalsium...…. 76
21. Data kadar fosfor (%) tepung tulang ikan tuna...…… 76
22. Analisis ragam kadar fosfor...…. 76
23. Data nilai pH tepung tulang ikan tuna...…… 77
24. Analisis ragam nilai pH...…. 77
25. Data nilai daya serap air (%) tepung tulang ikan tuna...…… 77
26. Analisis ragam daya serap air...…. 77
27. Data densitas kamba (g/ml) tepung tulang ikan tuna...… 78
29. Data nilai derajat putih (%) tepung tulang ikan tuna...… 78
30. Analisis ragam derajat putih...…. 78
31. Uji lanjut BNJ lama waktu autoklafing terhadap derajat putih... 79
32. Uji lanjut BNJ frekuensi perebusan terhadap derajat putih... 79
33. Whitenesmeter (alat pengukur derajat putih pada tepung )...…. 81
34. Alat destilasi protein metode Kjeldahl...…. 81
35. Tulang ikan tuna setelah dibersihkan...…. 82
36. Proses hidrolisis dengan larutan NaOH...…. 82
37. Tepung tulang ikan tuna...…. 83
1. PENDAHULUAN
1.1. Latar Belakang
Mineral merupakan bagian dari unsur pembentuk tubuh yang memegang peranan penting dalam pemeliharaan fungsi tubuh baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan (Almatsier 2002). Unsur mineral esensial didefinisikan sebagai unsur penting yang dibutuhkan dalam kehidupan dan jika unsur tersebut dihilangkan dapat menyebabkan kerusakan fungsi fisiologis suatu organisme.
Beberapa mineral seperti kalsium dan fosfor terdapat dalam jumlah yang relatif besar dalam tubuh. Kalsium merupakan unsur terbanyak kelima dan kation terbanyak di dalam tubuh manusia, yaitu sekitar 1,5-2 % dari keseluruhan berat tubuh. Lebih dari 99 % kalsium terdapat pada tulang dalam bentuk hidroksiapatit. Kalsium dibutuhkan untuk proses pembentukan dan perawatan jaringan rangka tubuh serta beberapa kegiatan penting dalam tubuh seperti pembekuan darah, kontraksi otot, menjaga keseimbangan hormon dan katalisator pada reaksi biologis.
Salah satu dampak dari defisiensi kalsium yang sekarang ini banyak terjadi adalah osteoporosis. Osteoporosis atau yang dikenal dengan nama tulang keropos merupakan suatu penyakit rapuh tulang yang ditandai dengan hilangnya kepadatan tulang setelah mencapai usia tua. Pada anak-anak defisiensi kalsium dapat menyebabkan terhambatnya pertumbuhan tulang/rickets. Kekurangan kalsium dapat juga menyebabkan osteomalasia (Almatsier 2002). Orang Asia, khususnya Indonesia pada kenyataannya lebih mudah terserang osteoporosis karena tulang orang Asia umumnya lebih kecil dari tulang bangsa lain, terutama bangsa Eropa dan Amerika. Pada tahun 2050 diperkirakan sekitar 51 % penduduk dunia terserang osteoporosis, kemungkinan besar mereka yang tinggal di Asia (Anonymous 2002). Apalagi di Indonesia yang konsumsi kalsiumnya masih sangat rendah, diperburuk dengan pencegahan dan pengobatan osteoporosis yang belum intensif. Untuk mencegah kekurangan kalsium perlu konsumsi kalsium dalam jumlah yang cukup. Sumber kalsium yang populer saat ini adalah susu dan suplemen kalsium, akan tetapi sangat disayangkan keduanya cenderung masih
diluar jangkauan daya beli masyarakat Indonesia pada umumnya (Anonymous 2001). Oleh karena itu dibutuhkan alternatif sumber kalsium yang mampu memenuhi kebutuhan masyarakat dalam bentuk makanan atau minuman kaya kalsium yang murah dan melimpah.
Kalsium yang berasal dari hewan seperti limbah tulang ikan sampai saat ini belum banyak dimanfaatkan untuk kebutuhan manusia. Padahal tulang ikan menurut Basmal et al. (2000) mengandung trikalsium fosfat yang sangat ideal untuk tubuh manusia. Menurut laporan terakhir dari Departemen Kelautan dan Perikanan (2000), produksi perikanan Indonesia mencapai 5,3 juta ton dalam tahun 2000. Sekitar 20-30 % dari total jumlah ini adalah limbah. Ini berarti bahwa dalam tahun 2000, dihasilkan sebanyak 1,06-1,6 juta ton limbah ikan. Tulang merupakan salah satu bentuk limbah yang dihasilkan dari industri pengolahan ikan yang memiliki kandungan kalsium terbanyak dalam tubuh ikan. Dari sudut pandang pangan dan gizi, tulang ikan sangat kaya akan kalsium yang dibutuhkan manusia, karena unsur utama dari tulang ikan adalah kalsium, fosfor dan karbonat (Helve 1989 diacu dalam Lestari 2001). Dengan demikian limbah tulang ikan mempunyai potensi yang besar untuk dimanfaatkan sebagai bahan baku tepung tulang ikan yang kaya kalsium.
Ikan tuna merupakan salah satu komoditas perikanan Indonesia yang potensial, terbesar kedua setelah udang (Ilyas dan Suparno 1985). Peningkatan nilai produksi ikan tuna dari tahun ke tahun menunjukkan nilai yang cukup tajam. Tahun 1990 volume produksi masih 88.661 ton, tetapi tahun 1998 meningkat drastis mencapai 168.122 ton. Setahun berikutnya volume produksi menurun menjadi 151.231 ton. Setelah itu, tahun 2000 naik lagi menjadi 153.241 ton, dan pada tahun 2001 166.630 ton (Departemen Kelautan dan Perikanan 2001).
Peningkatan volume produksi ini akan meningkatkan volume limbah hasil industri pengolahan tuna tersebut. Pemanfaatan limbah tulang ikan tuna sebagai sumber kalsium merupakan alternatif pemanfaatan limbah yang tepat dalam rangka menyediakan sumber pangan kaya kalsium sekaligus mengurangi dampak buruk akibat pencemaran limbah pada industri pengolahan tuna.
1.2. Tujuan
Tujuan dari penelitian ini adalah :
1. Memanfaatkan limbah tulang ikan tuna dalam pembuatan tepung tulang berkalsium tinggi.
2. Mempelajari pengaruh lamanya proses autoklafing dan frekuensi perebusan terhadap karakteristik tepung tulang ikan tuna.
2. TINJAUAN PUSTAKA
2.1. Ikan Tuna
Menurut Saanin (1968), klasifikasi dan identifikasi ikan tuna adalah sebagai berikut : Filum : Chordata Subfilum : Vertebrata Kelas : Teleostei Subkelas : Actinopterygii Ordo : Perciformes Subordo : Scombroideae Famili : Scombroidae Genus : Thunnus
Spesies : Thunnus alalunga (albacores) Genus ini terdiri atas beberapa spesies antara lain Thunnus albacores yang paling banyak didapati di perairan Indonesia. Jenis ini dikenal dengan sebutan madidihang atau yellow fin tuna. Badan memanjang, bulat seperti cerutu dan termasuk jenis ikan buas dan bersifat predator. Panjang tubuh dapat mencapai 195 cm, namun umumnya 50-150 cm. Hidup bergerombol kecil (schooling) pada waktu mencari makan. Ikan yellow fin tuna (Thunnus albacores) yang terlihat pada Gambar 1, termasuk dalam famili Scombroidae yang tergolong ikan perenang cepat, memiliki dua sirip punggung. Sirip depan biasanya pendek dan terpisah dari sirip belakang, pada bagian punggung berwarna biru kehitaman dan berwarna keputih-putihan pada bagian perut (Ditjenkan 1983).
Ikan tuna memiliki kecepatan renang mencapai 50 km/jam. Kemampuan renang ikan ini merupakan salah satu faktor yang meyebabkan penyebarannya dapat meliputi skala ruang (wilayah geografis) yang cukup luas, termasuk diantaranya beberapa spesies yang dapat menyebar dan bermigrasi lintas samudera (Diniah et al. 2001).
2.2. Limbah Perikanan
Limbah merupakan suatu hasil samping yang kurang berharga bahkan merupakan suatu masalah di dalam suatu industri. Menurut Moeljanto (1979) limbah perikanan adalah ikan yang terbuang, tercecer dan sisa olahan yang pada suatu saat di tempat tertentu belum dapat dimanfaatkan secara ekonomis.
Jenis limbah dan hasil samping dapat dikelompokkan secara umum menjadi 4 kelompok (Moeljanto 1979) yaitu :
(1) hasil samping pada penangkapan suatu spesies atau sumber daya misalnya ikan rucah pada penangkapan udang dan ikan cucut pada penangkapan tuna;
(2) sisa pengolahan seperti bagian kepala, tulang, sisik, sirip, isi perut dan daging merah;
(3) surplus dari tangkapan (glut); (4) sisa distribusi.
Limbah pengolahan tuna dihasilkan pada pengolahan pengalengan, pembekuan atau pengolahan tradisional. Umumnya industri pengolahan tuna menghasilkan limbah industri yang cukup besar pada beberapa pusat pengolahan, karena tuna termasuk komoditas penting setelah udang (Ilyas dan Suparno 1985). Limbah tersebut berupa limbah padat, minyak, air sisa pemasakan dan lain-lain.
Tulang tuna dapat dijadikan sumber kalsium untuk keperluan pengayaan (enrichment) sebagai salah satu upaya fortifikasi zat gizi dalam makanan. Pemanfaatan limbah ini ditujukan untuk mendapatkan hasil guna dan daya guna sebesar mungkin tanpa mengganggu kelestarian lingkungan.
2.3. Tulang Ikan
Tulang ikan merupakan salah satu limbah hasil pengolahan perikanan yang dapat dimanfaatkan sebagai tepung untuk bahan pangan. Pemanfaatan tepung
tulang ikan dapat dilakukan dalam bentuk pengayaan (enrichment) sebagai salah satu upaya fortifikasi zat gizi dalam makanan. Di Jepang pemanfaatan tulang ikan dilakukan untuk memproduksi kalsium dalam bentuk tepung tulang yang dapat dikonsumsi manusia. Tulang ikan banyak mengandung kalsium dalam bentuk kalsium fosfat sebanyak 14 % dari total susunan tulang. Bentuk kompleks kalsium fosfat ini terdapat pada tulang dan dapat diserap oleh tubuh dengan baik sekitar 60-70 % (Subangsihe 1996).
Tulang dibentuk dalam dua proses yang terpisah, yaitu pembentukan matriks dan penempatan mineral ke dalam matriks tersebut. Tiga jenis komponen seluler terlibat didalamnya dengan fungsi yang berbeda-beda yaitu osteoblas dalam pembentukan tulang, osteosit dalam pemeliharaan tulang dan osteoklas dalam penyerapan kembali tulang. Osteoblas membentuk kolagen tempat mineral-mineral melekat. Mineral utama di dalam tulang adalah kalsium dan fosfor, sedangkan mineral lain dalam jumlah kecil adalah natrium, magnesium, dan fluor (Winarno 1997). Komposisi kimia tulang ikan tuna dapat dilihat pada Tabel 1. Tabel 1. Komposisi kimia tulang ikan tuna
No. Parameter Berat Kering Berat Basah
1 Air - 56,11 %
2 Abu 39,19 % 17,20 %
3 Protein 52,54 % 7,56 %
4 Lemak 23,06 % 3,32 %
Sumber : Lestari (2001)
Unsur utama yang menyusun tulang ikan adalah kalsium, fosfat dan karbonat, sedangkan yang terdapat dalam jumlah kecil yaitu magnesium, sodium, stronsium, sitrat, fluorida, hidroksida dan sulfat (Lovell 1989). Kandungan mineral pada ikan bergantung pada spesies, jenis kelamin, siklus biologis, dan bagian tubuh ikan yang dianalisis. Kandungan mineral juga tergantung pada faktor ekologis seperti musim, tempat pengembangan, jumlah nutrisi yang tersedia, suhu dan salinitas air (Navarro 1991 diacu dalam Martinez et al.1998). 2.4. Kalsium
Kira-kira 2 % dari seluruh bobot tubuh orang dewasa terdiri dari kalsium. Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh. Lebih
dari 99 % kalsium ada di dalam tulang dan gigi, yaitu bersama-sama dengan fosfat membentuk kristal tidak larut yang disebut kalsium hidroksiapatit (Ca3(PO4)2)3.Ca(OH)2 (Muchtadi et al. 1993). Jumlah kalsium dalam plasma darah kurang lebih 10 mg/100 ml dengan jumlah lebih kecil di dalam sel-sel, sedangkan jumlah fosfor kurang lebih 4 mg/100 ml, lebih banyak terdapat dalam sel (Sediaoetama 2000).
Hidroksiapatit merupakan suatu struktur kristal yang terdiri atas kalsium fosfat dan disusun di sekeliling matriks organik berupa protein kolagen untuk memberikan kekuatan dan kekakuan tulang. Di samping itu juga terdapat ion-ion lain, seperti fluor, magnesium, seng dan natrium. Melalui matriks dan diantara struktur kristal terdapat pembuluh darah dan limfe, syaraf dan sumsum tulang. Melalui pembuluh darah ini ion-ion mineral berdifusi ke dalam cairan ekstraseluler, mengelilingi kristal dan memungkinkan pengendapan mineral baru atau penyerapan kembali mineral dari tulang (Almatsier 2002).
Kalsium dan fosfat dibutuhkan dalam jumlah yang besar dalam tubuh, yaitu sekitar 99 % kalsium dan 80-90 % fosfat dalam tulang dan gigi, dan sekitar 1 % terdapat dalam jaringan lunak dan cairan tubuh ekstraselular (Martin 1965). Sisa kalsium tubuh yang ada dalam intra dan ekstraselular memegang peranan yang sangat vital dalam mengatur fungsi sel dan impuls syaraf (Linder 1992).
2.4.1. Peranan kalsium
Kalsium memegang peranan yang sangat penting di dalam tubuh (Muchtadi
et al. 1993) diantaranya, yaitu :
(1) sebagai komponen utama pembentuk tulang dan gigi serta memelihara ketegaran kerangka tubuh;
(2) mengatur proses pembekuan darah;
(3) sebagai intracelular regulator atau messenger, yaitu membantu regulasi aktivitas otot-otot kerangka, jantung dan jaringan lain;
(4) sebagai bagian dari enzim, yaitu lipase, suksinat dehidrogenase, adenosine trifosfatase dan beberapa enzim proteolitik tertentu;
(5) kontraksi dan relaksasi otot. Tanpa kalsium semua otot akan kehilangan kemampuannya untuk berkontraksi;
(7) mengirimkan isyarat saraf ke jaringan-jaringan tubuh; (8) penyimpanan dan pelepasan neurotransmiter;
(9) penyimpanan dan pelepasan hormon;
(10) pengaturan sekresi gastrin dan menjaga keseimbangan osmotik. 2.4.2. Kebutuhan kalsium
Kebutuhan mineral esensial untuk manusia bervariasi dari beberapa mikrogram perhari sampai sekitar 1 g/hari. Jika masukan mineral tersebut rendah untuk waktu-waktu tertentu, maka dapat menyebabkan defisiensi. Sebaliknya, jika masukan terlalu besar dapat menyebabkan terjadinya gangguan fungsi tubuh seperti konstipasi dan gangguan fungsi ginjal (Miller 1996). Tabel 2 menunjukkan kebutuhan kalsium tubuh rata-rata orang Indonesia per hari yang direkomendasikan dalam Widya Karya Pangan dan Gizi (1998). Diperkirakan kebutuhan kalsium untuk orang dewasa sekitar 800 mg/hari dan kebutuhan yang lebih tinggi yaitu sekitar 1200 mg/hari digunakan untuk wanita hamil dan menyusui (Miller 1996).
Tabel 2. Angka kecukupan rata-rata kalsium (mg/hari)
Golongan umur (tahun) Kebutuhan Ca (mg/hari) 1-9 10-15 16-19 500 700 600 Pria 20-45 45-59 >60 500 800 500 Wanita 20-45 46-59 >60 500 600 500 Hamil Menyusui +400 +400
Sumber : Widya Karya Pangan dan Gizi (1998)
Status kalsium ditentukan oleh kombinasi faktor usia, jenis kelamin dan faktor hormonal. Interaksi kompleks dari faktor tersebut menentukan jumlah kalsium tersedia yang dapat diserap, kapasitas intestin untuk menyerap, dan jumlah kalsium yang hilang dalam urin, kelenjar keringat maupun feses. Faktor
utama yang menentukan status kalsium adalah faktor nutrisi seperti laktosa dan oksalat. Faktor ini menentukan ketersediaan, fungsi tiroid dan paratiroid yang bekerja melalui vitamin D, hormon lain dan metabolisme fosfor (Miller 1996).
Kekurangan kalsium akan menyebabkan kadar kalsium darah menurun. Kondisi dimana kadar kalsium berada dibawah kisaran normal (9-10 mg/100 ml) disebut hipokalsemia. Hipokalsemia dapat menyebabkan tetani atau kejang. Kepekaan serabut saraf dan pusat saraf terhadap rangsangan meningkat, sehingga terjadi kejang otot misalnya pada kaki (Almatsier 2001).
Konsumsi kalsium sebaiknya tidak melebihi 2500 mg sehari. Kondisi kebalikan dari hipokalsemia adalah hiperkalsemia. Hiperkalsemia ini dapat menyebabkan hiperkalsiuria yaitu kondisi dimana kadar kalsium di dalam urin melebihi 300 mg/hari. Kelebihan kalsium dapat menimbulkan batu ginjal atau gangguan ginjal. Disamping itu dapat menyebabkan konstipasi (susah buang air besar). Kelebihan kalsium jarang terjadi akibat konsumsi makanan alami dan biasanya terjadi bila mengkonsumsi suplemen kalsium berupa tablet atau bentuk lain (Almatsier 2001).
2.4.3. Sumber kalsium
Sumber kalsium utama adalah susu dan hasil susu, seperti keju dan yogurt. Ikan yang dimakan dengan tulang, termasuk ikan kering merupakan sumber kalsium yang baik. Serealia seperti kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, dan sayuran hijau merupakan sumber kalsium yang baik juga, tetapi bahan makanan ini banyak mengandung serat, fitat dan oksalat yang dapat menghambat penyerapan kalsium (Almatsier 2002).
Sumber kalsium yang biasa digunakan dapat dikelompokkan menjadi tiga kelompok (Kaup et al.1991) yaitu :
(1) tepung tulang mono-kalsium dan di-kalsium fosfat yang ketersediaannya paling tinggi diantara sumber-sumber kalsium lainnya;
(2) ground limestone (batuan kapur yang biasanya mengandung magnesium dan bersifat agak asam), deflourined phosphate (garam kalium fosfat yang masih mengandung fluor yang bersifat racun bila kadarnya berlebihan) dan kalsium karbonat. Kelompok ini merupakan sumber kalsium yang ketersediaannya sedang;
(3) hay yaitu kalsium yang berikatan dengan mineral lain yang sukar larut. Sumber ini memiliki ketersediaan kalsium yang rendah.
Kebanyakan kalsium dari bahan nabati tidak dapat digunakan dengan baik karena berikatan dengan oksalat yang dapat membentuk garam yang tidak larut dalam air (Linder 1992). Kalsium yang dapat diserap oleh tubuh adalah kalsium dalam bentuk senyawa kalsium klorida, kalsium glukorat, kalsium karbonat dan kalsium fosfat. Kalsium fosfat merupakan sumber mineral yang memiliki nilai biologis yang sangat baik sebagai sumber kalsium dan fosfor (Kaup et al.1991). Suatu perusahaan di Amerika, International Seafood of Alaska (ISA) memproduksi tepung tulang ikan dengan harapan mengandung mineral seperti kalsium dan fosfor yang tinggi dan dapat digunakan sebagai bahan alam untuk mengatasi penyakit osteoporosis pada wanita. Kandungan gizi tepung tulang ikan produksi ISA tersebut disajikan pada Tabel 3.
Tabel 3. Kandungan zat gizi tepung tulang ikan produksi ISA
Zat Gizi Jumlah (%)
Air Lemak Karbohidrat Protein Abu Kalsium 3,6 5,6 23,5 34,2 33,1 11,9 Sumber: Rans (2002) 2.4.4. Metabolisme kalsium
Selama pencernaan, kalsium dan fosfor terpisah pada makanan yang dimakan dan terserap melalui dinding usus halus ke dalam aliran darah yang membawa mineral tersebut ke bagian-bagian tubuh yang memerlukan mineral. Kalsium diabsorbsi melalui duodenum dan jejunum proksimal oleh protein pengikat kalsium yang disintesis sebagai respon terhadap kerja 1,25-dihidroksikolekalsiferol (1,25-dihidroksivitamin D3). Mineral ini tidak seluruhnya terserap oleh tubuh, sisanya dikeluarkan melalui feses dan urin (Martin 1965). Menurut Heaney (2001), setiap hari sejumlah 100-200 mg kalsium diekskresikan melalui urin, 100-120 mg melalui feses dan 16-24 mg melalui keringat.
Dalam makanan yang mengandung sedikit kalsium, presentase penyerapan kalsium akan meningkat menjadi 60 % selama masa pertumbuhan, namun pada orang dewasa yang mengkonsumsi kalsium dalam jumlah yang cukup, penyerapannya akan menurun sebesar 10 %. Secara normal, penyerapan kalsium berkisar pada 30 %. Secara umum efisiensi penyerapan kalsium bervariasi secara berkebalikan dengan asupan kalsium. Semakin rendah kandungan kalsium produk, penyerapannya justru semakin tinggi (Allen dan Wood 1994).
Almatsier (2002) menyatakan bahwa kemampuan absorbsi lebih tinggi pada masa pertumbuhan, dan menurun pada proses menua. Kemampuan absorbsi pada laki-laki lebih tinggi dari pada perempuan pada semua golongan usia. Kemampuan ini akan menurun dengan semakin meningkatnya umur, tingginya pemasukan fosfat dan kalsium, atau rendahnya masukan vitamin D (McDowell 1992).
2.4.5. Faktor yang mempengaruhi penyerapan kalsium
Dalam keadaan normal sebanyak 30-35 % kalsium yang dikonsumsi akan diabsorbsi oleh tubuh. Beberapa faktor penting yang mempengaruhi tingkat penyerapan kalsium dalam tubuh adalah fosfor, vitamin D, protein, nilai pH dan kelarutan, zat organik, serat makanan dan faktor lain.
2.4.5.1. Fosfor
Kalsium dan fosfor saling berpengaruh erat dalam proses absorbsi kalsium. Menurut Sediaoetama (2000) untuk absorbsi Ca yang baik diperlukan perbandingan Ca:P dalam rongga usus 1:1 sampai 1:3. Guthrie (1975) menyebutkan batasan bagi rasio perbandingan Ca:P adalah dibawah 1:2. Perbandingan Ca:P yang lebih besar dari 1:3 akan menghambat penyerapan Ca, sehingga hidangan yang demikian akan menimbulkan penyakit defisiensi Ca, yaitu rakhitis (Sediaoetama 2000). Pada umumnya rasio Ca:P dalam makanan antara 1:1 dan 1:2. Hal tersebut didasarkan karena abu tulang mengandung sekitar 2 bagian kalsium dan 1 bagian fosfor (Anggorodi 1985).
2.4.5.2. Vitamin D
Proses penyerapan kalsium dipengaruhi oleh usia, masukan fosfat, kalsium, dan vitamin D (McDowell 1992). Kalsium diabsorbsi dari usus melalui
pengangkutan aktif, yaitu melalui suatu perbedaan konsentrasi dengan suatu proses yang membutuhkan energi. Vitamin D dalam bentuk 1,25-(OH)2D dibutuhkan untuk pengangkutan aktif kalsium tersebut. Protein pengikat kalsium diinduksi oleh vitamin D, demikian juga ATPase yang diaktifkan oleh kalsium, mungkin terlibat dalam modulasi vitamin D terhadap absorbsi kalsium.
Beberapa faktor dalam makanan dapat menurunkan atau meningkatkan absorbsi kalsium di dalam usus. Faktor dalam makanan yang meningkatkan absorbsi kalsium antara lain beberapa asam amino seperti lisin dan arginin, laktosa dan vitamin D. Bahan makanan yang mengandung banyak oksalat dan fitat, berbagai bentuk serat makanan dan lemak jenuh, dilaporkan dapat menurunkan absorbsi kalsium (Schuette dan Linkswiler 1988).
2.4.5.3. Protein
Protein berperan penting dalam penyerapan kalsium ke dalam mukosa usus karena transportasi kalsium melalui sel usus dapat terjadi melalui difusi yang menggunakan jasa protein pengikat kalsium yang mengantarkan kalsium sitoplasma eritrosit ke membran basal. Proses ini membutuhkan ATP (Groff dan Gropper 1990) dan kekurangan protein menyebabkan gangguan pada absorbsi dan transportasi zat-zat gizi (Almatsier 2002). Protein yang mendorong penyerapan kalsium berupa asam amino yaitu lisin dan arginin (Harland dan Oberleas 2001). Protein makanan dapat berpengaruh negatif terhadap ketersediaan biologis mineral jika mineral terperangkap dalam protein atau kompleks peptida yang resisten terhadap proteolisis. Situasinya serupa dengan kompleks mineral protein-fitat yang tidak tercerna dengan baik, sehingga penyerapan mineral menurun (Erdman et al. 1980 diacu dalam Greger 1988).
Protein pada tulang ikan sebagian besar terdiri atas kolagen yang sulit dicerna enzim pepsin dan pankreatin menjadi asam-asam amino. Menurut Winarno (1997) kolagen adalah protein dari golongan protein fibriler atau skleroprotein, yang struktur molekulnya berbentuk serabut. Jenis protein ini merupakan komponen utama dari tendon, ligamen, tulang dan tulang rawan (Soeparno 1992).
Secara nutrisi protein ini bukanlah protein yang baik. Selain komposisi asam aminonya tidak ideal (terlalu banyak Pro, Gly, Ala), kolagen pada kondisi alami juga sulit dicerna oleh tripsin dan kemotripsin (Alais dan Linden 1991).
2.4.5.4. Nilai pH dan kelarutan
Kalsium membutuhkan pH 6 agar dapat berada dalam keadaan terlarut. Kalsium hanya bisa diabsorbsi bila terdapat dalam bentuk larut air dan tidak mengendap karena unsur makanan lain seperti oksalat (Almatsier 2002). Kelarutan merupakan salah satu syarat dalam penyerapan kalsium. Menurut Allen dan Wood (1994) kelarutan kalsium meningkat dalam lingkungan asam pada perut, tetapi ion terlarut akan bergabung kembali kemudian berpresipitasi dalam jejunum dan ileum, dimana pH-nya mendekati netral. Menurut Anggorodi (1995) pH kandungan usus juga berpengaruh terhadap proses absorbsi kalsium dalam tubuh. Fosfor sulit diserap pada pH di atas 6,5 dan baik diserap pada pH di bawah 6,0 dimana nilai pH tersebut dapat dikontrol dengan cara tidak terlalu banyak memberikan kalsium.
2.4.5.5. Zat organik
Adanya zat organik seperti asam oksalat dan asam fitat dalam bahan dapat bergabung dengan kalsium membentuk garam yang tidak larut. Asam oksalat dan kalsium membentuk garam yang tidak larut, yaitu kalsium oksalat (Winarno 1997) sehingga mengendap di dalam rongga usus dan tidak dapat diserap ke dalam mukosa (Sediaoetama 2000).
2.4.5.6. Serat makanan
Serat makanan merupakan komponen tanaman yang tidak dapat dicerna oleh enzim pencernaan manusia, termasuk didalamnya komponen dinding sel tumbuhan (selulosa, hemiselulosa, pektin dan lignin) dan polisakarida intraseluler seperti gum dan mucilage (Trowell 1976 diacu dalam Spiller 2001). Pengaruh dari serat makanan terhadap ketersediaan biologis kalsium masih diperdebatkan karena hasil penelitian in vivo yang tidak konsisten (Kelsay et al. 1979 dan Wishker et al. 1991 diacu dalam Boccia et al. 1998). Harland dan Oberleas (2001) menyatakan bahwa serat bersama-sama dengan fitat dan oksalat mengurangi penyerapan kalsium.
Berdasarkan jenis kelarutannya, serat dibagi menjadi 2 yaitu serat larut air dan serat tidak larut air. Serat larut dapat mengikat air dan menciptakan larutan viskos dalam saluran pencernaan sehingga menyebabkan perlambatan pengosongan perut dari makanan, menghalangi percampuran makanan dengan enzim, mengurangi tingkat difusi nutrisi sehingga melalui mekanisme ini kalsium sulit terserap mukosa usus (Groff dan Gropper 1990).
Serat tidak larut, menurut Slavin (1985) diacu dalam Blaney et al. (1996) menghalangi lebih banyak kalsium daripada serat larut karena menurunkan waktu transit bahan pangan selama di usus halus sehingga mengurangi waktu penyerapan kalsium. Selanjutnya, serat tidak larut akan secara otomatis mengurangi kesempatan kerja enzim (Groff dan Gropper 1990).
2.4.5.7. Faktor lain
Beberapa faktor lain yang mempengaruhi penyerapan kalsium dalam tubuh adalah aktifitas fisik yang berpengaruh baik terhadap absorbsi kalsium. Laktosa meningkatkan absorbsi bila tersedia cukup enzim laktase. Sebaliknya, bila terdapat defisiensi laktase, laktosa mencegah absorbsi kalsium. Akan tetapi di luar kehamilan diragukan apakah laktosa masih dapat meningkatkan penyerapan kalsium (Allen dan Wood 1994). Lemak meningkatkan waktu transit makanan melalui saluran pencernaan, dengan demikian memberi waktu lebih banyak untuk absorbsi kalsium (Almatsier 2002). Tetapi Allen dan Wood (1994) pernah menuliskan bahwa lemak tidak mempengaruhi penyerapan kalsium.
2.4.6. Proses pemisahan kalsium
Ada beberapa metode yang digunakan untuk memperoleh tepung kalsium tulang (Anggorodi 1985), yaitu:
(1) pengukusan. Tulang dikukus kemudian dikeringkan dan digiling untuk menghasilkan tepung tulang;
(2) pemasakan dengan uap di bawah tekanan. Tulang dimasak dengan tekanan kemudian diarangkan dalam bejana tertutup sehingga didapat tulang dalam bentuk remah dan dapat digiling menjadi tepung;
(3) abu tulang yang diperoleh dari pembakaran tulang.
Proses pemisahan kalsium ikan juga dapat dilakukan dengan teknik deproteinasi melalui tahapan sebagai berikut : (1) pemotongan tulang menjadi
potongan-potongan kecil, (2) pencucian, (3) pengecilan ukuran (kira-kira 8-12 mm), (4) pencucian, (5) penghilangan protein tahap pertama, (6) pencucian, (7) penghilangan protein tahap kedua, (8) pencucian, (9) pemanasan, (10) pencucian, (11) pengeringan, (12) pemanasan dan pengeringan, (13) penghancuran 40 mesh, (14) penggilingan 300-3000 mesh, (15) penyortiran dan (16) penimbangan dan pengepakan (Sada 1984).
Prinsip penghilangan protein dari suatu bahan dapat dilakukan dengan cara hidrolisis menggunakan pelarut tertentu. Protein akan terhidrolisis apabila dicampurkan dengan asam atau alkali kuat atau enzim proteolitik melalui proses pemecahan protein secara bertahap menjadi molekul-molekul peptida yang sederhana dan asam-asam amino (Kirk dan Othmer 1964).
Penggunaan larutan yang bersifat basa lebih menguntungkan daripada larutan yang bersifat asam. Kelarutan dan hasil ekstraksi lebih tinggi pada daerah alkalin daripada daerah asam. Hal ini disebabkan karena jumlah gugus bermuatan negatif lebih banyak daripada jumlah gugus bermuatan positif, dengan demikian reaksi antara protein dan NaOH membentuk ester semakin sempurna sehingga protein yang dapat dihilangkan semakin besar Cheftel et al. (1985).
Efektifitas proses dengan larutan basa tergantung pada konsentrasi larutan basa dan suhu yang digunakan. Semakin kuat konsentrasi basa dan tingginya suhu yang digunakan, proses deproteinasi makin sempurna. Hidrolisis protein pada suasana basa biasanya dilakukan pada suhu antara 40-50 oC selama 12 sampai 24 jam (Karmas 1982).
Penghilangan protein pada kulit krustasea umumnya menggunakan larutan NaOH dengan konsentrasi 2-3 % dengan suhu 63-65 oC dalam waktu 1-2 jam. Teknik ini merupakan dasar untuk menghilangkan protein pada tulang ikan. Pada pH dan kekuatan ionik yang konstan, diketahui bahwa kelarutan protein meningkat pada kisaran suhu 40-50 oC. Pada kisaran tersebut, gerakan molekuler yang terjadi cukup untuk merusak ikatan-ikatan yang berperan untuk menstabilkan struktur sekunder dan tersier (Cheftel et al. 1985).
Pemisahan kalsium dapat dilakukan juga melalui proses pembakaran, tetapi dapat menimbulkan polusi terhadap lingkungan akibat gas pembakaran. Selain itu
bahan organik yang terkandung dalam bahan tidak dapat dimanfaatkan kembali, karena hilang akibat proses pembakaran (Mann 1967).
Beberapa penelitian tentang pemanfaatan tulang ikan tuna sebagai sumber kalsium sudah banyak dilakukan, diantaranya adalah penelitian Mulia (2004) dan Elfauziah (2003). Elfauziah (2003) menggunakan larutan alkali (NaOH) untuk menghidrolisis protein tulang ikan. Hasil penelitian Elfauziah menunjukkan bahwa penggunakan berbagai konsentrasi NaOH dan besarnya suhu ekstraksi tulang tuna, menghasilkan nilai kalsium tertinggi pada konsentrasi NaOH 1,5 N, suhu 60 oC selama 2 jam dengan perbandingan volume larutan NaOH dan berat tulang sebesar 5:2. Prosedur pembuatan tepung tulang ikan Elfauziah (2003) disajikan pada Gambar 2.
Gambar 2. Alur proses pembuatan tepung tulang ikan metode Elfauziah (2003). Mulia (2004) menggunakan metode hidrolisis murni untuk menghilangkan protein yang terdapat pada tulang ikan dengan proses perebusan dan autoklafing.
Tulang ikan
Perebusan 100 oC, 30 menit Pembersihan
Pengukusan 3 jam Pengecilan ukuran Ekstraksi NaOH 60 oC, 3 jam
Penetralan dengan pencucian Pengeringan 121 oC, 30 menit
Penepungan Tepung tulang ikan
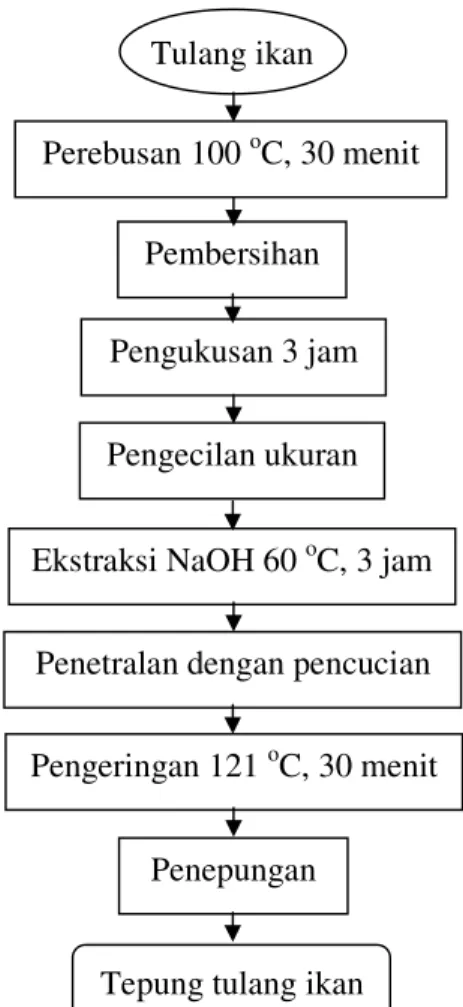
Proses pembuatan tepung tulang ikan menurut Mulia (2004) dapat dilihat pada Gambar 3.
Gambar 3. Alur proses pembuatan tepung tulang ikan metode Mulia (2004). Tulang ikan Pembersihan Perebusan 100 oC, 30 menit Pembersihan Perebusan 4 jam Autoklafing 121 oC, 1 jam Pengepresan manual
Pengeringan dengan Drum dryer 100 oC, tekanan 1 bar Pemblenderan
Pengayakan 100 mesh
Pengeringan dengan Oven 105 oC 90 menit Tepung tulang ikan
2.4.6.1. Hidrolisis
Menurut Kirk dan Othmer (1953) kata hidrolisis pada umumnya berhubungan dengan reaksi yang meliputi air dan dua atau lebih komponen produk. Pada hidrolisis, sebuah ikatan antara dua atom dipecah. Istilah hidrolisis kadang-kadang berkembang pada reaksi pemecahan banyak ikatan menjadi satu ikatan. Reaksi hidrolisis dapat dibagi dalam beberapa tipe, yaitu:
(1) hidrolisis murni, hanya dengan air yang digunakan untuk proses hidrolisis;
(2) hidrolisis dengan larutan asam; (3) hidrolisis dengan larutan alkali;
(4) hidrolisis dengan peleburan alkali yang menggunakan air atau tanpa air pada temperatur tinggi;
(5) hidrolisis dengan enzim sebagai katalisator.
Hidrolisis protein terjadi bila protein dipanaskan dengan asam, alkali kuat, atau dengan penggunaan enzim yang akan disertai dengan pembebasan asam amino penyusun model protein (Kirk dan Othmer 1953). Semua protein akan menghasilkan asam-asam amino bila dihidrolisis. Tetapi ada beberapa protein yang disamping menghasilkan asam amino juga menghasilkan molekul-molekul protein yang masih berikatan (West dan Todd 1964).
Turunan pertama dari protein adalah protean, meta protein dan protein terkoagulasi. Turunan keduanya adalah proteosa, pepton dan peptida (polipeptida) selanjutnya polipeptida ini dipecah lagi menjadi peptida-peptida sederhana dan akhirnya menjadi asam amino (Wertheim dan Jeskey 1956). Hidrolisis bisa terjadi dengan pemutusan gugus karboksil suatu asam amino dari asam amino yang lain (Gambar 4).
Gambar 4. Mekanisme reaksi hidrolisis (Hart dan Schuetz 1961).
H O H O H O H-N-C-C-OH H-N-C-C-OH H-N-C-C-OH H R1 H R2 H R3 H O H O H O H – N – C – C – N – C – C – N – C – C – OH H R1 H R2 H R3 Ikatan peptida H2O
Ikatan peptida pada protein dapat dihidrolisis dengan perebusan dalam asam atau basa kuat untuk menghasilkan komponen asam amino dalam bentuk bebas. Ikatan ini dapat juga dihidrolisis dengan enzim tertentu seperti tripsin dan kimotripsin (Lehninger 1993). Bahan kimia yang umum digunakan untuk menghidrolisis protein adalah HCl, NaOH, Ba(OH)2 (West dan Todd 1964). 2.4.6.2. Pemasakan
Perebusan adalah pemanasan di dalam air mendidih pada suhu 100 oC selama beberapa menit. Banyak spora bakteri yang tahan panas, masih hidup setelah perebusan beberapa jam (Fardiaz et al. 1992). Perebusan adalah cara termudah dan termurah untuk proses lanjutan, akan tetapi tidak menambah jumlah zat gizi produk pada suatu tingkat yang berarti (Zaitsev et al. 1969).
Pemasakan bertujuan untuk mengurangi air dan lemak yang berlebihan, menginaktifasi enzim-enzim yang dapat menyebabkan perubahan warna, menghilangkan udara dari jaringan dan mengurangi populasi bakteri (Winarno dan Fardiaz 1973). Selama proses pengolahan, bahan makanan terpengaruh dalam banyak hal termasuk perubahan protein, lemak dan karbohidrat yang dapat menyebabkan perubahan baik positif maupun negatif terhadap kualitas dan status gizinya (Dogerskog 1977 diacu dalam Nurhayati 1994).
Pada ikan yang mengalami perebusan akan terjadi hidrolisis kolagen dan koagulasi protein, albumin dan globulin akan mengalami denaturasi. Akibat dari koagulasi protein dan pembongkaran sel selama perebusan, daging akan melepaskan lemak dan air, substansi nitrogen, serta garam dan vitamin yang larut dalam air (Zaitzev et al. 1969).
Pemanasan akan menyebabkan kehilangan aktivitas enzim, terjadinya perubahan jumlah dan distribusi sulfhidril, formasi ikatan silang disulfida, interaksi dengan komponen lain, agregasi, hilang sebagian akibat dehidrasi, koagulasi, perubahan warna serta pemendekan sarkomer. Lemak juga akan mengalami hidrolisis atau autoksidasi sebagian serta ada yang berinteraksi dengan protein. Selain itu pemanasan juga akan menyebabkan kenaikan pH 0,3 – 0,5 satuan. Pada suhu 100 oC, protein akan terkoagulasi dan air dalam daging akan keluar (Zaitsev et al. 1969)
Suhu pemasakan tergantung pada jenis bahan mentah dan kesegarannya. Suhu pemasakan optimum antara 80-98 oC (Saleh et al. 1985). Menurut Lund (1988), pemasakan pendahuluan dengan menggunakan uap panas akan menyebabkan zat gizi yang hilang lebih sedikit jika dibandingkan dengan menggunakan air panas.
2.4.6.3. Pengeringan
Kualitas bahan makanan dalam keadaan biasa berhubungan dengan kadar air dari bahan makanan tersebut. Selain kadar air, kualitas bahan makanan juga dipengaruhi oleh temperatur, adanya oksigen, jamur, insekta dan lamanya penyimpanan. Pengeringan adalah proses pengeluaran atau pembuangan bahan cair dari suatu bahan yang mencakup pengeringan, pemanggangan, penguapan dan lain-lain. Hasil akhir pengeringan merupakan bahan yang bebas dari air (cairan) atau mengandung air dalam jumlah yang rendah (Hall 1979). Proses pengeringan didasarkan pada terjadinya penguapan air (pengisapan air oleh udara) sebagai akibat perbedaan kandungan uap air antara udara dan produk yang dikeringkan (Moeljanto 1992).
Prinsip pengeringan adalah mengurangi kandungan air atau menurunkan derajat kebasahan bahan makanan sehingga pada proses ini biasanya tidak hanya kadar air yang hilang. Melalui cara pengeringan ini biasanya kadar air dapat turun dan hilang sampai 60-70 %. Diusahakan untuk penyimpanan, kadar air bahan makanan adalah 10 % untuk menghindari kemungkinan tumbuhnya jamur yang akan mempengaruhi susunan atau nilai gizi bahan makanan (Winarno 1997).
Proses pengeringan ini dapat dilakukan secara alami (menggunakan sinar matahari) maupun dengan menggunakan alat pengering buatan. Pengeringan dengan sinar matahari merupakan metode pengeringan tradisional yang hingga saat ini masih banyak dilakukan di negara-negara berkembang. Pengeringan dengan sinar matahari sangat tergantung pada keadaan cuaca yang sering tidak menguntungkan, khususnya pada musin hujan (Suharto 1991).
Keuntungan pengeringan dengan sinar matahari adalah sebagai berikut (Buckle et al. 1987):
(1) menghasilkan bobot yang ringan karena hampir semua kadar air makanan dapat dikeluarkan dengan dehidrasi;
(2) kebanyakan produk yang dikeringkan membutuhkan tempat lebih sedikit daripada aslinya karena menghasilkan kemampatan yang baik;
(3) kestabilan dalam suhu penyimpanan pada suhu kamar.
Kerugian menggunakan sinar matahari adalah intensitas sinar yang tidak tetap sepanjang hari dengan disertai kenaikan suhu yang tidak dapat diatur menyebabkan waktu penjemuran sukar untuk ditentukan dengan tepat serta kebersihannya sukar dikontrol (Ilyas dan Suparno1985). Proses pengeringan dengan sinar matahari relatif berjalan lambat, sehingga memungkinkan ketengikan akan lebih cepat terjadi (Moeljanto 1992). Selain itu pengeringan dengan cara ini akan menyebabkan hilangnya flavor yang mudah menguap, perubahan struktur serta terjadinya kerusakan mikrobiologi bila kecepatan pengeringan awal berjalan lambat (Buckle et al. 1987).
Pengeringan dengan cara pemanasan disamping menurunkan kadar air, juga mengurangi bau ataupun enzim-enzim yang kadang-kadang mempengaruhi daya suka ataupun daya guna dari bahan makanan tersebut. Pengeringan yang kurang sempurna akan memungkinkan pertumbuhan jamur, kapang atau mikroorganisme lainnya (Winarno 1997).
Salah satu reaksi kimia yang terjadi selama proses pemanasan saat pengeringan tepung tulang ikan adalah oksidasi lemak yang menghasilkan senyawa-senyawa antara lain aldehida dan keton yang bisa bereaksi antara satu dengan yang lain membentuk polimer lipid. Proses oksidasi dapat berlangsung bila terjadi kontak antara sejumlah oksigen dengan lemak dan biasanya dimulai dengan pembentukan peroksida dan hidroperoksida. Tingkat selanjutnya adalah terurainya asam-asam lemak disertai dengan konversi hidroperoksida menjadi keton serta asam-asam lemak bebas (Ketaren 1986).
2.5. Bioavailabilitas (ketersediaan biologis) kalsium
Bioavailabilitas adalah proporsi zat gizi dari makanan yang tersedia untuk menjalankan fungsi metabolisme dalam tubuh pada kondisi normal (O’dell 1997). Lebih lanjut diuraikan bahwa bioavailabilitas mineral digunakan untuk menjelaskan proses fisikokimia dan fisiologis yang mempengaruhi penyerapan fraksional mineral dalam tubuh sehingga mineral tersebut dapat digunakan oleh tubuh untuk menjalankan fungsi metabolisme.
Pengukuran bioavailabilitas kalsium:
Pada prinsipnya, bioavailabilitas kalsium dapat diukur dengan menggunakan metode in vivo dan in vitro. Ada beberapa pendekatan yang dapat digunakan dalam mengukur bioavailabilitas atau penyerapan mineral. Menurut Heaney (2001), ada enam pendekatan yang umum digunakan untuk mengetahui bioavailabilitas kalsium, yaitu keseimbangan kalsium tubuh, konsentrasi kalsium dalam serum, konsentrasi kalsium dalam urin, konsentrasi kalsium dalam tubuh (menggunakan radioisotop), biomarker (konsentrasi hormon paratiroid/PTH) dan metode lain.
Metode in vitro, yaitu mengkondisikan proses seperti keadaan pencernaan sebenarnya yang terjadi di dalam tubuh. Prinsip pengukuran bioavailabilitas kalsium metode in vitro adalah dengan teknik dialisis yang menggunakan kantung dialisis. Dialisis digunakan untuk memisahkan molekul-molekul besar dari molekul-molekul kecil. Metode pemisahan ini didasarkan atas sifat membran semipermeabel yang meloloskan molekul-molekul kecil akan tetapi menahan yang besar. Kecepatan dialisis dipengaruhi oleh membran yang meliputi bahan, preparasi dan permeabilitas; kemudian pelarut meliputi pelarut cair dan larutan makromolekul serta faktor kondisi fisik yang meliputi suhu dan tekanan. Metode
in vitro dapat digunakan untuk mendeteksi faktor yang mempengaruhi penyerapan
kalsium dalam usus, namun tidak dapat mengukur bioavailabilitas secara tepat dibandingkan dengan metode in vivo. Gueguen dan Pointillart (2000) diacu dalam Heaney (2001)
2.6. Osteoporosis
Kadar mineral tulang mencapai puncaknya diawal masa dewasa, kemudian secara perlahan menurun bersama umur. Penurunan tersebut tidak dapat dihindarkan walaupun tingkat penurunan dapat diperlambat. Kegagalan pertumbuhan tulang yang berkaitan dengan usia adalah fenomena yang umum terjadi pada manusia dan berawal pada usia 40 tahunan pada wanita dan sekitar 60 tahunan pada pria (Schuete dan Linkswiller 1988). Tingkat penurunan terlalu cepat pada wanita setelah menopause dan dapat menyebabkan osteoporosis yang merupakan problema utama bagi wanita tua.
Osteomalasia dan osteoporosis keduanya menunjukkan kadar mineral dan kepadatan tulang menurun, tanpa atau dengan diikuti oleh penurunan bahan organik tulang. Bahan organik tulang adalah kolagen, osteoblas, osteoklas, dan tenunan pengikat. Osteomalasia biasanya terjadi pada umur muda, misalnya pada defisiensi kalsium pada saat kehamilan. Defisiensi kalsium ini disebabkan karena susunan zat pada tulang tidak memilki konsentrasi kalsium dan fosfat yang cukup untuk proses pengerasan tulang, sehingga tulang menjadi lebih lunak. Osteoporosis didefinisikan sebagai suatu kegagalan pertumbuhan tulang yang dapat mengakibatkan satu atau lebih patah tulang dengan gejala trauma minimal (Schuete dan Linkswiller 1988).
Beberapa hal umum yang merupakan ciri-ciri khas populasi yang dapat menderita osteoporosis (Schuete dan Linkswiller 1988), yaitu:
(1) kegagalan pertumbuhan tulang yang menyebabkan osteoporosis, sebagian dapat disebabkan oleh defisiensi relatif esterogen karena peningkatanresorbsi tulang selama pembentukannya;
(2) penderita osteoporosis pada umumnya menunjukkan tingkat pergantian tulang yang lebih tinggi, yang mempertajam perbedaan antara resorbsi dan pembentukan;
(3) penderita osteoporosis mungkin kurang mampu melakukan absorbsi kalsium yang disebabkan berkurangnya pengubahan 25-OH-D menjadi 1,35-(OH)2D; bila dibandingkan dengan orang-orang lanjut usia lainnya;
(4) penderita osteoporosis mungkin kurang mampu mempertahankan kalsium tubuh dengan cara mengurangi kehilangan kalsium dalam urin bila masukan kalsium berkurang;
(5) aktifitas fisik yang rendah dapat mempercepat proses kegagalan pertumbuhan tulang.
Secara umum, penelitian epidemiologis tidak menunjukkan suatu hubungan antara jumlah kalsium di dalam makanan dan kasus osteoporosis. Walaupun demikian, masukan kalsium yang tidak memadai tetap dipercaya sebagai salah satu faktor yang dapat menyebabkan osteoporosis (Schuete dan Linkswiller 1988).
3. METODOLOGI
3.1. Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan Januari sampai dengan Maret 2005 di Laboratorium Penanganan dan Pengolahan Hasil Perikanan, Laboratorium Biokimia Hasil Perikanan Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Laboratorium Ilmu dan Teknologi Pakan Departemen Ilmu dan Nutrisi Makanan Ternak, Pilot Plan Pusat Antar Universitas (PAU) Pangan dan Gizi IPB, Laboratorium Pengolahan GMSK serta Laboratorium Pengolahan Pangan, Departemen Teknologi Pangan dan Gizi, Institut Pertanian Bogor.
3.2. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah limbah tulang ikan tuna dari PT. Indomaguro Tunas Unggul Jakarta. Limbah tersebut berupa tulang belakang ikan tanpa kepala, sirip dan ekor. Panjang tulang ikan berkisar 75-85 cm dengan lebar 20-25 cm. Dalam penelitian ini, berat total tulang ikan yang digunakan sebanyak 15 kg.
Bahan-bahan lain yang digunakan adalah akuades, NaOH 1,5 N, H2SO4 pekat, asam borat 5 %, NaOH pekat, HCl 0,1 N, indikator tashiro, kertas saring Whatman 40, indikator fenolftalin, etil eter, asam nitrat pekat, lanthanum klorida 10 %, pereaksi vanadat-molibdat, larutan fosfat standar, HNO3 10 %, HCl 37 %, suspensi pepsin, pankreatin (Sigma p-1750), ekstrak bile (Sigma B-8631), NaHCO3 0,1 M, kantung dialisis Spectrapor I 6000-8000 MWCO (molecular weight cut off) dan bahan-bahan kimia yang digunakan untuk analisis proksimat. Alat yang digunakan adalah wadah untuk mencuci bahan, pisau, alat pemasak, neraca, penyaring, ayakan (100 mesh), pengaduk, tabung erlenmeyer 250 ml, penangas air bergoyang, botol gelas, AAS spektrofotometer, whitenessmeter, sentrifuse, autoklaf, alat soxhlet, alat destilasi uap, alat pengukur pH, labu Kjeldahl, hot plate, tungku pengabuan dan peralatan gelas untuk analisis.
3.3. Metode Penelitian
Penelitian ini dilakukan dalam dua tahap, yaitu pembuatan tepung tulang ikan tuna dan analisis kandungan zat gizi serta sifat fisik tepung tulang yang dihasilkan. Analisis yang dilakukan terhadap tepung tulang meliputi kadar air, abu, lemak, protein, kalsium, fosfor, pH, daya serap air, densitas kamba, kemudahan melarut, derajat putih, rendemen dan bioavailabilitas. Uji bioavailabilitas hanya dilakukan pada contoh dengan perlakuan yang menghasilkan kadar kalsium paling tinggi.
3.3.1. Alur proses pemisahan kalsium tulang ikan
Metode pemisahan kalsium dalam penelitian ini, merupakan modifikasi dari beberapa metode yang sebelumnya pernah dilakukan, yaitu kombinasi antara metode Elfauziah (2003) dan Mulia (2004). Pembuatan tepung tulang ikan tuna dimulai dengan membersihkan tulang ikan. Tulang ikan dicuci dan dibersihkan untuk menghilangkan kotoran. Bagian sirip ekor, sirip punggung, sirip anal dan
finlet yang masih melekat pada tulang dihilangkan. Tulang ikan tersebut kemudian
dipotong-potong untuk mendapatkan ukuran yang lebih kecil.
Tulang kemudian direbus dalam panci aluminium selama 30 menit pada suhu 80 oC. Pemasakan awal ini dilakukan untuk mempermudah pembersihan tulang dari daging, darah dan lemak yang menempel pada tulang. Proses selanjutnya tulang ikan dimasukkan ke dalam autoklaf selama 1-3 jam pada suhu 121 oC dengan tekanan uap absolut sebesar 1 atm. Fungsi dari proses ini adalah untuk mensterilkan tulang dari mikroba dan menghilangkan lemak yang terdapat pada tulang. Selain itu protein akan terdenaturasi dan menggumpal. Pemanasan ini juga bertujuan untuk mengempukkan tulang ikan sehingga mempermudah proses selanjutnya.
Tahap berikutnya dilakukan perebusan kembali tulang pada suhu 100 oC selama 30 menit. Tahap ini merupakan bagian dari perlakuan dimana tulang ikan direbus dengan frekuensi perebusan yang berbeda, yaitu 1, 2 dan 3 kali. Setiap ulangan perebusan dilakukan penggantian air dan penghitungan waktu dimulai pada saat air mendidih. Pemasakan ini secara efektif menghilangkan lemak yang terdapat dalam tulang.
Proses hidrolisis berlanjut dengan perendaman tulang ikan ke dalam larutan NaOH 1,5 N selama 2 jam pada suhu 60 oC. Setelah tulang dicuci dan dinetralkan dengan air, tahap terakhir pada proses pembuatan tepung kalsium tulang ikan ini adalah pengeringan dan penepungan. Proses pengeringan dilakukan selama tiga hari menggunakan sinar matahari. Tepung tulang yang telah kering dihaluskan menggunakan mortar dan disaring menggunakan penyaring tepung. Alur proses pembuatan tepung tulang ikan tuna yang digunakan dalam penelitian ini secara lengkap dapat dilihat pada Gambar 5.
Gambar 5. Alur proses pembuatan tepung tulang ikan tuna (modifikasi Elfauziah (2003) dan Mulia (2004))
Autoklafing (121 oC, 1 atm) Perebusan (100 o C, 30 menit) Pengecilan ukuran (5-10 cm)
Ekstraksi basa NaOH (1,5 N, 60 oC, 2 jam)
Pengeringan dan penepungan Tepung tulang ikan
Tulang Ikan Tuna Perebusan (80 oC, 30 menit)
Pencucian
Perlakuan frekuensi perebusan: 1, 2, 3 kali
Pencucian dengan air
Perlakuan lamanya autoklafing : 1, 2, 3 jam
3.3.2. Perlakuan
Perlakuan yang diberikan terdiri atas dua faktor, faktor pertama adalah lamanya proses autoklafing yang terdiri 3 taraf yaitu 1 (A1), 2 (A2) dan 3 (A3) jam. Faktor kedua adalah frekuensi perebusan yang terdiri atas 3 taraf yaitu 1 (P1), 2 (P2) dan 3 (P3) kali perebusan. Dalam penelitian ini data perlakuan masing-masing diambil tiga kali ulangan.
3.4. Metode Analisis
Beberapa parameter yang diamati pada tepung tulang ikan meliputi kadar air, abu, lemak, protein, kalsium, fosfor, pH, daya serap air, densitas kamba, kemudahan melarut, derajat putih, rendemen dan bioavailabilitas kalsium.
3.4.1. Pengukuran rendemen (AOAC 1995)
Rendemen adalah persentase bahan baku utama yang menjadi produk akhir, atau perbandingan produk akhir dengan bahan baku utama dapat dinyatakan dalam desimal atau persen.
Perhitungannya adalah sebagai berikut: % 100 x a b Rendemen = Keterangan:
Berat bahan baku awal = a gram Berat produk akhir = b gram
3.4.2. Kadar air (AOAC 1995)
Cawan kosong yang bersih dikeringkan dalam oven (105 oC) selama 1 jam dan didinginkan dalam desikator (cawan alumunium 10 menit dan cawan porselin 30 menit), kemudian ditimbang. Contoh sebanyak 5 g dimasukkan dalam cawan dan dipanaskan dalam oven pada suhu 105 oC selama 4–5 jam, kemudian ditimbang setelah didinginkan dalam desikator. Contoh dan cawan kemudian dimasukkan kembali dalam oven selama 1 jam pada suhu yang sama secara berulang-ulang sampai beratnya konstan, dan ditimbang setelah didinginkan dalam desikator. Presentase kadar air (berat basah) dapat dihitung dengan rumus:
Keterangan:
B = Berat sampel (gram)
B1 = Berat (sampel + cawan) sebelum dikeringkan B2 = Berat (sampel + cawan) setelah dikeringkan
% 100 x B B2 B1 air Kadar = −
3.4.3. Kadar protein metode mikro Kjeldahl (AOAC 1995)
Contoh (0,1 g) dimasukkan ke dalam tabung mikro Kjeldahl 30 ml, kemudian ditambahkan H2SO4 (2,5 ml) dan tablet Kjeldahl. Contoh dididihkan selama (1-1,5 jam) sampai cairan jernih kemudian didinginkan. Isi labu dituangkan ke dalam alat destilasi, labu dibilas 5-6 kali dengan akuades (20 ml). Air bilasan juga dimasukkan ke dalam alat destilasi dan ditambahkan larutan NaOH 40 % sebanyak 20 ml.
Cairan dalam ujung tabung kondensor ditampung dalam erlenmeyer 125 ml berisi larutan H3BO3 dan 3 tetes indikator (cairan metil merah dan metilen blue) yang ada di bawah kondensor. Destilasi dilakukan sampai diperoleh 200 ml destilat yang bercampur dengan H3BO3 dan indikator dalam erlenmeyer. Destilat dititrasi dengan HCl 0,1 N sampai terjadi perubahan warna menjadi merah. Hal yang sama juga dilakukan terhadap blanko. Perhitungan:
6,25 x N % Protein % % 100 x contoh mg 14,007 x HCl normalitas x blanko) ml HCl ml ( N % = − =
3.4.4. Kadar lemak metode soxhlet (AOAC 1995)
Metode yang digunakan dalam analisis lemak adalah metode ekstraksi soxhlet. Labu lemak yang akan digunakan dikeringkan dalam oven, kemudian didinginkan dalam desikator dan ditimbang beratnya. Contoh sebanyak 5 g dalam bentuk tepung dibungkus dalam kertas saring, kemudian kertas saring yang berisi contoh tersebut dimasukkan dalam labu lemak secukupnya. Selanjutnya dilakukan refluks selama 5 jam sampai pelarut yang turun kembali ke dalam labu lemak berwarna jernih.
Pelarut yang ada dalam labu lemak didestilasi, dan pelarut ditampung kembali. Kemudian labu lemak berisi lemak hasil ekstraksi dipanaskan dalam oven pada suhu 150 oC hingga mencapai berat yang tetap, kemudian didinginkan dalam desikator 20-30 menit. Selanjutnya labu beserta lemak didalamnya ditimbang dan berat lemak dapat diketahui.
% 100 x (g) Contoh Berat (g) Lemak Berat Lemak % =
3.4.5. Kadar abu (AOAC 1995)
Cawan kosong dipanaskan dalam oven kemudian didinginkan dalam desikator selama 30 menit. Contoh ditimbang kurang lebih 5 g dan diletakkan dalam cawan, kemudian dibakar dalam kompor listrik sampai tidak berasap. Cawan kemudian dimasukkan ke dalam tanur. Pengabuan dilakukan dalam dua tahap, tahap pertama pada suhu sekitar 450 oC dan tahap kedua dilakukan pada suhu 550 oC selama 5 jam. Cawan kemudian didinginkan dalam desikator, setelah dingin kemudian cawan ditimbang. Presentase dari kadar abu dapat dihitung menggunakan rumus sebagai berikut:
% 100 x (g) Sampel Bobot (g) Abu Bobot Abu % =
3.4.6. Kadar kalsium (Apriyantono et al. 1989)
Penetapan kadar kalsium dilakukan dengan mengukur contoh yang sudah di destruksi secara basah pada Atomic Absorbtion Spectrophotometer (AAS) dengan menggunakan panjang gelombang 420 nm. Contoh didestruksi dengan campuran asam kemudian dipisahkan dari residunya.
Analisis kadar kalsium contoh dilakukan dengan menimbang 0,1 gram contoh halus yang kemudian dimasukkan ke dalam labu Kjeldahl 100 ml dan ditambahkan 10-13 ml campuran asam yang terdiri dari HNO3, HClO4 dan HCl (perbandingan 6 : 6 : 1), larutan didestruksi sampai berwarna jernih kemudian didinginkan. Setelah dingin, campuran hasil destruksi disaring dengan kertas saring Whatman. Pada saat penyaringan, labu Kjeldahl dan corong dibilas dengan air bebas ion sebanyak 4 kali. Volume hasil penyaringan ditera hingga 100 ml dan siap diukur pada AAS dengan panjang gelombang 420 nm.
Larutan stok standar kalsium 1000 ppm dibuat dengan cara menimbang 2,497 g CaCO3 kemudian dilarutkan dengan asam nitrat 1:4 sampai 1 liter. Larutan standar dibuat dari larutan stok 1000 ppm. Seri larutan standar yang digunakan adalah 0, 2, 5, 10 dan 20 ppm dengan volume 100 ml. Larutan standar tersebut kemudian diukur absorbansinya dengan AAS. Berdasarkan nilai absorbansi yang dihasilkan AAS pada seri larutan standar, diperoleh hubungan antara konsentrasi dengan absorban melalui persamaan garis lurus y = a + bx (y sebagai absorban dan x sebagai konsentrasi).
Perhitungan kadar kalsium ditetapkan dengan rumus sebagai berikut:
3.4.7. Kadar fosfor (Apriyantono et al. 1989)
Pembuatan larutan fosfat standar dan kurva standar : sebanyak 3,834 g potasium dihidrogen fosfat (KH2PO3) dilarutkan dalam akuades dan diencerkan sampai volume 1 liter. Kemudian sebanyak 25 ml dari larutan tersebut dimasukkan dalam labu takar 250 ml dan diencerkan sampai tanda tera (1 ml = 0,2 mg P2O5).
Masing-masing sebanyak 0; 2,5; 5; 10; 20; 30; 40 dan 50 ml larutan fosfat standar dimasukkan ke dalam labu takar 100 ml. Kemudian larutan pada masing-masing labu takar diencerkan sampai volume 100 ml dengan akuades. Larutan didiamkan selama 10 menit dan diukur absorbansinya menggunakan spektrofotometer dengan panjang gelombang 400 nm. Masing-masing labu takar mengandung 0; 0,5; 1; 2; 4; 6; 8 dan 10 mg P2O5 / 100 ml. Kurva standar dibuat antara absorbansi dengan mg P2O5./100 ml.
Contoh ditimbang sebanyak 5 g dalam gelas piala 150 ml. Ke dalam gelas tersebut ditambahkan 20 ml asam nitrat pekat. Kemudian dididihkan selama 5 menit. Selanjutnya didinginkan dan ditambahkan 5 ml asam sulfat pekat.
Larutan dipanaskan dan disempurnakan (digestion) dengan penambahan HNO3 setetes demi setetes sampai larutan tidak berwarna, kemudian dilanjutkan dengan pemanasan hingga timbul asap putih dan didinginkan.
Ke dalam gelas piala ditambahkan 15 ml akuades dan dididihkan kembali selama 10 menit. Setelah dingin dipindahkan ke dalam labu takar 250 ml. Gelas piala dibilas sampai bersih dan air bilasan dimasukkan ke dalam labu takar. Selanjutnya larutan dalam labu takar diencerkan sampai tanda tera dengan akuades.
Sebanyak 10 ml larutan contoh dimasukkan ke dalam labu takar 100 ml. Kemudian di dalam labu takar ditambahkan 40 ml akuades dan 25 ml pereaksi vanadatmolibdat dan diencerkan sampai tanda tera. Larutan didiamkan 10 menit,
% 100 x 1000000 Ca ppm Ca % = (g) contoh bobot n pengencera faktor aliquot x ml x blanko) absorban contoh (absorban Ca ppm = −
kemudiaan diukur absorbansinya dengan spektrofotometer pada panjang gelombang 400 nm. Nilai absorbansi dibandingkan dengan standar fosfor yang telah diketahui konsentrasinya.
Keterangan:
C = Konsentrasi fosfor dalam contoh (mg/100 ml) yang terbaca dari kurva standar W = Berat contoh yang digunakan
3.4.8. Analisis derajat keasaman metode pH meter (AOAC 1995)
Contoh dihaluskan, ditimbang sebanyak 1 g dalam gelas piala. Kemudian ditambahkan 10 ml akuades pH 7 dan dilakukan pengadukan. Contoh dalam wadah diukur pH nya dengan menggunakan pH meter yang telah dikalibrasi dengan larutan buffer pH 4 dan larutan buffer pH 7. Nilai pH diperoleh berdasarkan hasil pembacaan pada pH meter sampai angka digital yang menunjukkan nilai konstan.
3.4.9. Analisis daya serap air metode gravimetri (Fardiaz et al. 1992)
Sebanyak 1 g contoh ditimbang kemudian dimasukkan kedalam tabung sentrifuse. Selanjutnya ditambahkan 10 ml air dan dikocok menggunakan forter mixer. Kemudian disentrifuse dengan kecepatan 3500 rpm selama 30 menit. Selanjutnya volume supernatant diukur dengan menggunakan gelas ukur 10 ml. Daya serap air ini dihitung sebagai berikut :
3.4.10. Analisis densitas kamba (Wirakartakusumah et al. 1992)
Pengukuran densitas kamba dilakukan dengan menggunakan gelas ukur. Bahan-bahan yang akan diukur ditimbang sebanyak 10 g, kemudian dimasukkan ke dalam gelas ukur 100 ml dan dibaca volumenya.
% 100 x W 2,5 x C bb) (% ) O (P contoh dalam Fosfor 2 5 = % 100 x air kadar -100 bb) (% ) O (P contoh dalam Fosfor bk) (% ) O (P contoh dalam Fosfor 2 5 5 2 = % 100 x contoh kering berat ) supernatan volume - awal air (volume air serap Daya % = (ml) bahan volume (g) bahan berat (g/ml) kamba Densitas =