SKRIPSI
KARAKTERISASI TAPIOKA
DAN PENENTUAN FORMULASI PREMIX
SEBAGAI BAHAN PENYALUT UNTUK PRODUK FRIED SNACK
Oleh :
JUANDA REPUTRA F24053088
2009
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
KARAKTERISASI TAPIOKA
DAN PENENTUAN FORMULASI PREMIX
SEBAGAI BAHAN PENYALUT UNTUK PRODUK FRIED SNACK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
Departemen Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
JUANDA REPUTRA F24053088
2009
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
KARAKTERISASI TAPIOKA
DAN PENENTUAN FORMULASI PREMIX
SEBAGAI BAHAN PENYALUT UNTUK PRODUK FRIED SNACK
SKRIPSI
Sebagai salah satu syarat untuk meraih gelar SARJANA TEKNOLOGI PERTANIAN
Departemen Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
JUANDA REPUTRA F24053088
Dilahirkan pada tanggal 07 November 1987 Di Bukittinggi
Tanggal Lulus : 28 Agustus 2009 Bogor,
Menyetujui,
Dr.Ir. Feri Kusnandar, M.Sc. Wati, S.TP
Pembimbing Akademik Pembimbing Lapang
Mengetahui,
Dr. Ir. Dahrul Syah
Juanda Reputra. F24053088. Karakterisasi Tapioka dan Penentuan Formulasi Premix sebagai Bahan Penyalut untuk Produk Fried Snack. Dibawah bimbingan Feri Kusnandar dan Wati
RINGKASAN
Produk fried snack merupakan jenis produk makanan ringan yang diolah melalui proses penggorengan. Salah satu jenis produk ini yang cukup digemari oleh masyarakat Indonesia yaitu kacang salut, yang dikenal juga dengan sebutan kacang atom. Produk-produk pangan yang digoreng memiliki karakteristik tekstur yang renyah, rasa matang yang gurih, warna yang lebih menarik, dan bau goreng yang khas. Hal ini dipengaruhi oleh beberapa faktor, diantaranya jenis tepung sebagai bahan penyalut dan minyak yang terserap oleh produk selama penggorengan. Jenis tepung yang digunakan sebagai bahan penyalut pada produk kacang salut adalah tepung tapioka. Tepung tapioka yang diperoleh produsen kacang salut adalah berupa tapioka alami (tapioka tanpa modifikasi). Tapioka alami yang diperoleh dari beberapa pemasok memiliki karakteristik yang berbeda sehingga dapat menghasilkan tekstur produk yang tidak seragam. Salah satu upaya yang dapat dilakukan yaitu melalui penggunaan premix tapioka sebagai bahan penyalut. Premix tapioka merupakan campuran beberapa jenis tapioka yang memiliki karakteristik berbeda.
Penelitian ini dilakukan dalam beberapa tahap. Pertama, karakterisasi sifat kimia dan fungsional beberapa jenis tepung tapioka. Tepung tapioka yang digunakan adalah tapioka alami, tapioka modifikasi dan premix kontrol. Karakteristik kimia dan fungsional yang dianalisis meliputi kadar air, kadar pati, nilai pH, kadar amilosa dan amilopektin, pola gelatinisasi pati, serta daya pengembangan dan kelarutan pati. Karateristik ini kemudian dikorelasikan dengan tingkat pengembangan papatan dan kerenyahan bagian penyalut pada kacang salut. Sifat kimia dan fungsional yang memiliki korelasi paling kuat terhadap pengembangan papatan dan kerenyahan penyalut akan digunakan sebagai dasar penentuan formulasi premix tapioka. Formulasi premix tersebut ditentukan melalui pendekatan karakteristik premix kontrol. Tahap selanjutnya yaitu melakukan pemilihan formulasi premix untuk memperoleh formulasi terbaik. Disamping itu, pada penelitian ini juga dilakukan variasi substitusi tapioka modifikasi terhadap formulasi premix terpilih dengan konsentrasi 2%, 4%, dan 6%.
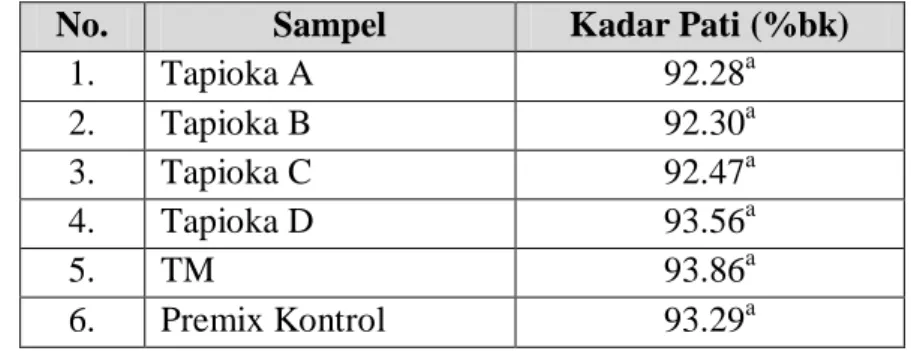
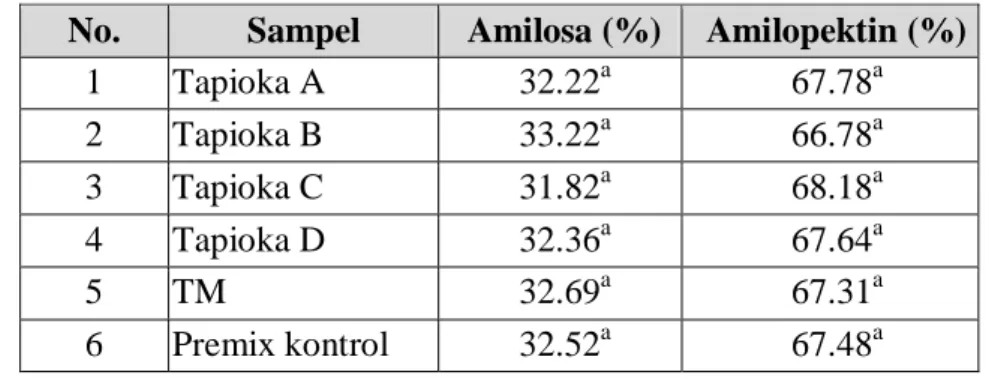
Tapioka alami yang dianalisis meliputi empat jenis tepung tapioka yang diperoleh dari pemasok yang berbeda. Tapioka modifikasi yang digunakan adalah tapioka yang dimodifikasi dengan teknik pregelatinisasi dan juga diperoleh dari pemasok. Sampel tapioka alami dan premix kontrol yang dianalisis memiliki kisaran kadar air antara 11.72-13.03%, kadar pati berkisar antara 92.28-93.56%bk, nilai pH antara 4.27-5.68, kadar amilosa berkisar antara 31.82-33.22%, dan amilopektin berkisar antara 66.78-68.18%. Sifat amilografi tapioka alami dan premix kontrol (suspensi 10%bb) yaitu suhu awal gelatinisasi berkisar antara 64.5-68.7oC, viskositas puncak berkisar antara 1100-1750 BU, suhu viskositas puncak berkisar antara 73.5-81˚C, viskositas breakdown berkisar antara 690-1232 BU, viskositas setback berkisar antara 695-1030 BU dan stabilitas fase pemanasan berkisar antara 140-290 BU. Nilai daya pengembangan tapioka alami dan premix
kontrol cenderung mengalami kenaikan dengan peningkatan suhu, akan tetapi mengalami penurunan setelah mencapai suhu 75-85°C, kecuali tapioka A. Sementara itu nilai kelarutan meningkat dengan peningkatan suhu pengukuran.
Sampel tapioka modifikasi memiliki nilai kadar air 4.95%, kadar pati 93.86%bk, kadar amilosa 32.69%, kadar amilopektin 67.31%, dan pH 4.51. Beberapa sifat amilografi tapioka modifikasi tidak dapat ditentukan karena sampel ini sudah tergelatinisasi pada awal proses pengukuran. Sifat amilografi yang dapat diketahui yaitu nilai stabilitas fase pemanasannya sebesar 65 BU. Nilai daya pengembangan dan kelarutan sampel tapioka modifikasi memiliki pola yang berbeda dan lebih besar daripada sampel tapioka alami.
Sifat kimia dan fungsional tapioka yang paling berkorelasi kuat terhadap pengembangan papatan dan kerenyahan penyalut adalah rasio amilosa dan amilopektin. Dengan demikian formulasi premix alternatif ditentukan berdasarkan pendekatan karakteristik rasio amilosa dan amilopektin. Disamping itu, penentuan formulasi juga dilakukan berdasarkan pendekatan tingkat pengembangan papatan. Setelah melalui tahap pemilihan formulasi dan variasi substitusi tapioka modifikasi , maka diperoleh dua formulasi alternatif utama yaitu, formulasi F3 yang terdiri dari 4%bk tapioka modifikasi, 10%bk tapioka A, 18.37%bk tapioka B, dan 67.63%bk tapioka D serta formulasi F11 yang terdiri dari 2%bb tapioka modifikasi,10%bb tapioka A, 6.23%bb tapioka C, dan 81.77%bb tapioka D.
Beberapa karakteristik kimia premix alternatif yang diperoleh tidak berbeda nyata dengan karakteristik premix kontrol pada taraf signifikansi 0.05. Karakteristik kimia premix alternatif F3 yaitu, kadar air 11.40%, pH 4.81, kadar pati 92.42%bk, kadar amilosa 32.87%, dan kadar amilopektin 67.13%. Sedangkan karakteristik kimia premix alternatif F11 yaitu, kadar air 11.44%, pH 4.83, kadar pati 91.12%bk, kadar amilosa 32.84%, dan kadar amilopektin 67.16%. Tingkat pengembangan papatan yang dibuat dengan menggunakan premix alternatif F3 adalah sebesar 311.6% dan F11 sebesar 310.23%.
Respon panelis terlatih terhadap kerenyahan penyalut yang dihasilkan oleh premix alternatif tidak berbeda nyata dengan produk kontrol pada taraf signifikansi 0.01. Sebagian besar panelis terlatih menilai formulasi F3 lebih renyah dibandingkan formulasi premix kontrol. Dengan demikian, Premix alternatif yang diperoleh pada penelititan ini (F3 dan F11) telah dapat digunakan sebagai pengganti premix kontrol.
RIWAYAT HIDUP PENULIS
Penulis dilahirkan di Bukittinggi, Sumatera Barat, pada tanggal 07 November 1987. Penulis merupakan anak ke-2 dari enam bersaudara pasangan Jafril dan Rasmita. Penulis mengawali jenjang pendidikannya di TK Masyitah Bukittinggi pada tahun 1992-1993, SD Negeri 37 PGRM Agam pada tahun 1993-1999, dilanjutkan ke SLTP Negeri 3 Tilatang Kamang Agam pada tahun 1999-2002, serta SMA Negeri 1 Bukittinggi pada tahun 2002-2005. Pada tahun 2005 penulis diterima di Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama menjalani studi di Institut Pertanian Bogor, penulis aktif di berbagai kegiatan dan organisasi kemahasiswaan, diantaranya menjadi pengurus Himpunan Mahasiswa Teknologi Pangan (Himitepa) divisi Information Technologi (IT) pada tahun 2008, dan pengurus Ikatan Pelajar Mahasiswa Minang (IPMM) Bogor divisi Pengembangan Sumberdaya Manusia (PSDM) pada tahun 2007. Kepanitiaan yang pernah diikuti penulis antara lain kepanitiaan Wisuda tahun 2007, Penyambutan Mahasiswa Baru tahun 2006 dan 2007, Seminar dan Pelatihan HACCP tahun 2007, Seminar dan Pelatihan ISO 9001 dan 22000 tahun 2008, Workshop mahasiswa teknologi pangan se-Indonesia tahun 2008 dan Seminar Prospek Pengembangan Kakao Indonesia pada tahun 2008.
Penulis pernah menjadi asisten praktikum pada mata kuliah Kimia Dasar I, Departemen Kimia, Fakultas MIPA, IPB (2006), dan asisten praktikum mata kuliah Evaluasi Sensori, Departemen ITP, FATETA, IPB (2008). Selama masa kuliah, penulis mendapatkan beasiswa PPA pada tahun 2006-2008 dan Tanoto Foundation pada tahun 2008-2009. Sebagai tugas akhir, penulis melakukan penelitian berupa magang di suatu perusahaan pangan di wilayah Jabotabek dengan judul „Karakterisasi Tapioka dan Penentuan Formulasi Premix sebagai Bahan Penyalut untuk Produk Fried Snack‟, di bawah bimbingan Dr. Ir. Feri Kusnandar, M.Sc. sebagai pembimbing akademik dan Wati, S.TP sebagai pembimbing lapang.
KATA PENGANTAR
Alhamdulillahirabbil‟alamin. Puji dan syukur kehadirat Allah SWT atas segala karunia, hidayah, dan rahmat-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul ‟Karakterisasi Tapioka dan Penentuan Formulasi Premix sebagai Bahan Penyalut untuk Produk Fried Snack’. Skripsi ini disusun oleh penulis dibawah bimbingan Dr.Ir. Feri Kusnandar, M.Sc dan Wati, STP.
Ucapan terima kasih dan penghargaan yang setinggi-tingginya penulis sampaikan kepada sejumlah pihak yang telah berkontribusi secara langsung maupun tidak langsung dalam penyelesaian skripsi ini. Semoga Allah SWT membalas budi baik semua pihak yang senantiasa membimbing, membantu, dan mendoakan penulis dalam menyelesaikan kegiatan magang dan penyusunan skripsi ini. Ucapan terima kasih ingin penulis sampaikan kepada:
1. Mama, Papa, Kakakku Erick, Adikku Egi, Zaki, Alvi, dan Intan yang telah memberikan begitu banyak dukungan baik secara moril maupun materil. Terima kasih atas semua kesabaran, doa, dan dorongannya sehingga penulis tetap bersemangat dan dapat menyelesaikan tugas akhir ini.
2. Dr.Ir. Feri Kusnandar, M.Sc. selaku dosen pembimbing akademik yang telah memberikan dukungan, motivasi, dan bimbingan sehingga tugas akhir ini dapat terselesaikan.
3. Iwan Surjawan, Ph.D selaku pembimbing lapang yang telah memberikan kesempatan kepada penulis untuk melakukan kegiatan magang.
4. Wati, S.TP selaku pembimbing lapang yang telah memberikan waktu, bimbingan, dan saran kepada penulis selama kegiatan magang.
5. Bpk Rahadi, mba Ocid, mba cimung, dan Bu Mike yang telah memberikan arahan dan bantuan selama kegiatan magang.
6. Teman-teman kosan Bogor: Nanda, Haris, Aji, dan Fuad. Hidup bersama kalian penuh suka dan duka.
7. Teman-teman satu tempat magang: Melisa, Wita, Resna, Reriel, Cani, dan Glenn, terima kasih atas semua bantuan dan dukungannya selama magang. 8. Teman-teman kosan Jakarta: Mas Nizar dan Kak Farid, terima kasih atas
9. Teman-teman satu divisi Snack: Mba Nita (Terima kasih banyak mba), Eni, Mba Herlina, Mba Lince, Mas Haris, dan Mas Novi. Teman-teman lab sentral : Bu Ratih, Mba Tri, Mas Wili, Mba Susan, Ahmad, dan Vio. Teman-teman SE : Mba Sesil, Mba Lia, Kristin, dan Ranto. Terima kasih atas semua bantuan dan ilmu yang telah diberikan selama magang.
10. Teman-teman kantor: Mas Nizar, Kak Farid, Kak Qia, Mas Trisno, Mba Ichi, Nanda DIB, Pak Molid, dll. Terima kasih atas semua dukungan dan kebersamaannya selama magang.
11. Teman-teman satu angkatan ITP 42 yang telah memberikan kebersamaan dan kehangatan selama menjalani kuliah.
12. Teman-teman organisasi HIMITEPA yang telah bekerjasama dalam beberapa kegiatan HIMITEPA.
13. Teman-teman organisasi daerah Sumatera Barat (IPMM) yang telah bekerjasama dalam beberapa kegiatan yang diadakan oleh organisasi daerah ini.
14. Terima kasih kepada Da Ji yang telah membimbing dan membantu penulis pada awal penulis diterima di IPB dan dukungannya sampai saat ini.
15. Terima kasih kepada Reni Setiawati atas semua hiburan dan dorongannya kepada penulis dalam menyelesaikan tugas akhir.
Penulis menyadari bahwa tugas akhir ini masih jauh dari sempurna. Oleh karena itu penulis memohon saran dan kritik demi perbaikan dan perkembangan selanjutnya. Semoga tugas akhir ini dapat bermanfaat bagi pengembangan ilmu dan teknologi, khususnya di bidang teknologi pangan.
Bogor, September 2009
DAFTAR ISI
Halaman
KATA PENGANTAR... i
DAFTAR ISI... iii
DAFTAR TABEL... vi
DAFTAR GAMBAR... vii
DAFTAR LAMPIRAN... viii
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. TUJUAN... 2
C. MANFAAT... 3
II. TINJAUAN PUSTAKA A. KACANG SALUT... 4
B. TEKSTUR PRODUK FRIED SNACK... 4
C. PATI... 6
i. Granula Pati... 6
ii. Amilosa dan Amilopektin... 7
iii. Daya Pengembangan (Swelling Power) dan Kelarutan Pati... 9
iv. Gelatinisasi Pati... 10
D. TAPIOKA...…... 12
i. Proses Pembuatan Tapioka... 12
ii. Karakteristik Tapioka... 14
E. PATI PREGELATINISASI... 16
III. KEGIATAN MAGANG A. DESKRIPSI KEGIATAN MAGANG... 19
B. RUMUSAN PERMASALAHAN... 19
C. METODOLOGI PEMECAHAN MASALAH... 20
i. Bahan dan Alat... 20
ii. Metode Penelitian... 21
1. Karakterisasi Tapioka... 22
b. Analisis Tingkat Pengembangan Papatan... 22
c. Analisis Kerenyahan Produk Kacang Salut... 23
2. Penentuan Formulasi Premix Alternatif... 24
a. Rancangan Formulasi Premix... 24
b. Pemilihan Formulasi Premix... 24
c. Variasi Substitusi Tapioka Modifikasi... 25
3. Uji Ranking Kerenyahan... 25
4. Karakterisasi Premix Alternatif... 25
iii. Metode Analisis... 25
a. Kadar Air (AOAC, 1995)... 25
b. Kadar Pati (SNI 01-2892-1992)... 26
c. Kadar Amilosa dan Amilopektin (Apriyantono et al., 1998).. 28
d. Nilai pH (AOAC 1995)... 29
e. Daya Pengembangan dan Kelarutan Pati (Li dan Yeh, 2001). 30 f. Pola Gelatinisasi... 32
g. Volume Papatan dan Kacang Salut... 32
h. Analisis Tekstur Secara Obyektif... 33
i. Analisis Tekstur Secara Subyektif... 33
j. Analisis Statistik... 33
IV. HASIL DAN PEMBAHASAN A. KARAKTERISASI TAPIOKA... 35
i. Sifat Kimia dan Fungsional Tepung Tapioka... 35
1. Kadar Air... 35
2. Nilai pH... 36
3. Kadar Pati... 37
4. Kadar Amilosa dan Amilopektin... 39
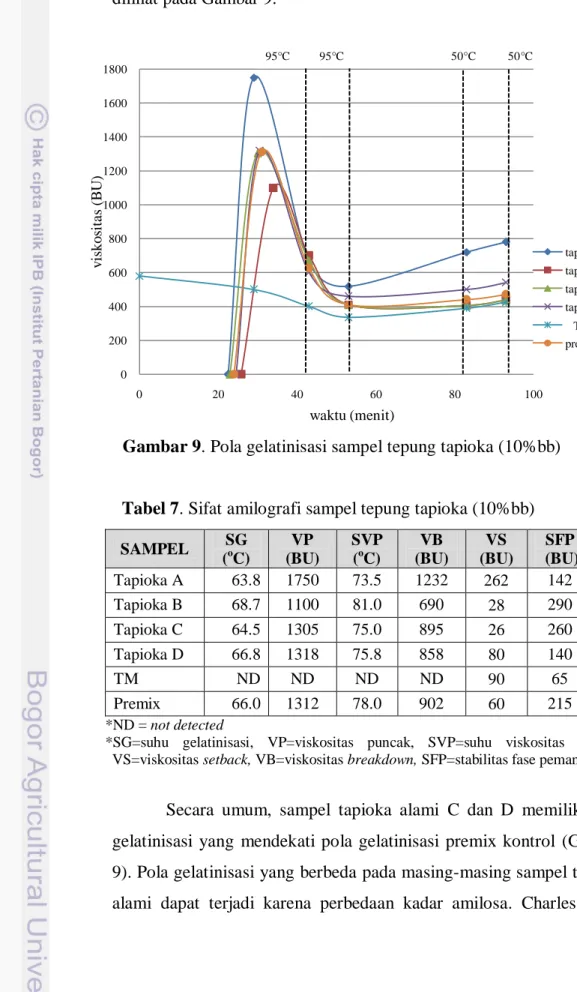
5. Pola Gelatinisasi... 39
6. Daya Pengembangan dan Kelarutan... 45
ii. Tingkat Pengembangan Papatan... 47
iii. Kerenyahan Produk Kacang Salut... 49
B. PENENTUAN FORMULASI PREMIX ALTERNATIF... 52
ii. Pemilihan Formulasi Premix... 54
1. Pemilihan Formulasi Tahap 1... 54
2. Pemilihan Formulasi Tahap 2... 55
iii. Variasi Substitusi Tapioka Modifikasi... 56
C. UJI RANKING KERENYAHAN... 58
D. KARAKTERISASI PREMIX ALTERNATIF... 59
V. KESIMPULAN DAN SARAN A. KESIMPULAN... 61
B. SARAN... 63
DAFTAR PUSTAKA... 64
DAFTAR TABEL
Halaman
Tabel 1. Komposisi kimia tepung tapioka... 14
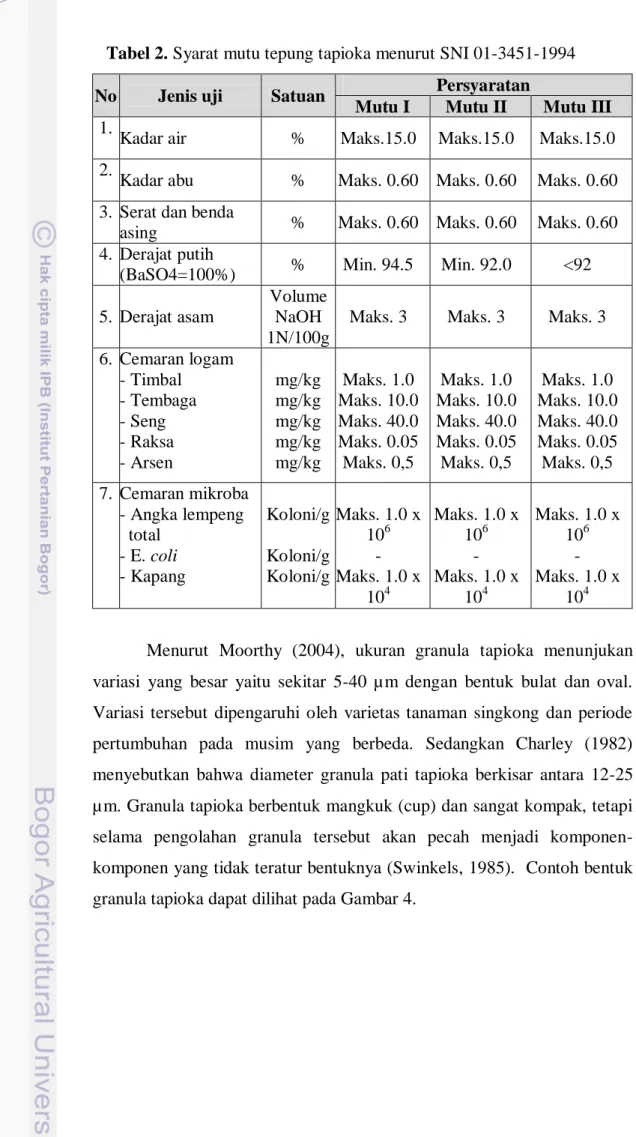
Tabel 2. Syarat mutu tepung tapioka menurut SNI 01-3451-1994... 15
Tabel 3. Kadar air sampel tapioka... 35
Tabel 4. Nilai pH sampel tapioka... 36
Tabel 5. Kadar pati sampel tapioka... 38
Tabel 6. Kadar amilosa dan amilopektin sampel tapioka... 39
Tabel 7. Sifat amilografi sampel tepung tapioka (10%bb)... 40
Tabel 8. Tingkat pengembangan papatan sampel tapioka... 48
Tabel 9. Hasil pengukuran gaya (gf) dan jarak (mm), serta skor kerenyahan penyalut pada produk kacang salut... 50
Tabel 10. Formulasi premix alternatif berdasarkan pendekatan rasio amilisa dan amilopektin (basis 100 gram bk)... 53
Tabel 11. Formulasi premix alternatif berdasarkan pendekatan pengembangan papatan (basis 100 gram bb)... 54
Tabel 12. Hasil pengukuran gaya (gf) dan jarak (mm) terhadap penyalut masing-masing formulasi... 55
Tabel 13. Hasil uji rating kerenyahan penyalut hasil pemilihan formulasi tahap 1... 56
Tabel 14. Formulasi premix dengan variasi konsentrasi TM... 57
Tabel 15. Hasil uji rating kerenyahan penyalut dengan variasi TM... 57
Tabel 16. Hasil uji preferensi dan komentar panelis terhadap penyalut dengan variasi TM... 58
Tabel 17. Hasil uji ranking kerenyahan dan penampakan pori-pori penyalut... 59
DAFTAR GAMBAR
Halaman
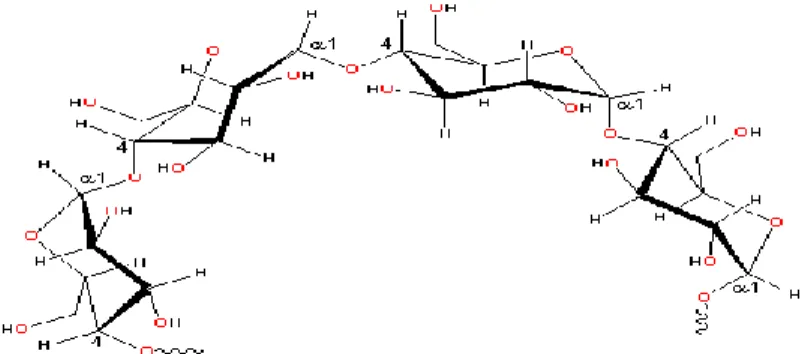
Gambar 1. Struktur amilosa (Chaplin, 2006)... 8
Gambar 2. Struktur amilopektin (Chaplin, 2006)... 8
Gambar 3. Diagram alir proses pembuatan tapioka pabrik modern... 13
Gambar 4. Granula tapioka (Anonim, 2008)... 16
Gambar 5. Granula pati pregelatinisasi (500x) metode spray cooked dan drum dried...…….... 18
Gambar 6. Diagram alir metode penelitian... 21
Gambar 7. Diagram alir pembuatan lem berbumbu... 22
Gambar 8. Diagram alir pembuatan kacang salut... 23
Gambar 9. Pola gelatinisasi sampel tepung tapioka (10%bb)... 40
Gambar 10. Pola daya pengembangan sampel tepung tapioka... 45
Gambar 11. Pola kelarutan sampel tepung tapioka... 47
Gambar 12. Proses pencampuran sampel tapioka... 52
DAFTAR LAMPIRAN
Halaman Lampiran 1. Rekapitulasi karakteristik kimia dan fungsional sampel
tapioka... 69
Lampiran 2. Pengukuran kadar air sampel tapioka... 70
Lampiran 3. Pengukuran kadar pati sampel tapioka... 71
Lampiran 4. Pengukuran kadar amilosa dan amilopektin sampel tapioka... 73
Lampiran 5. Pengukuran nilai pH sampel tapioka... 76
Lampiran 6. Pengukuran sifat amilografi sampel tapioka... 77
Lampiran 7. Pengembangan papatan penyalut dari sampel tapioka... 78
Lampiran 8. Kerenyahan penyalut dari sampel tapioka... 79
Lampiran 9. Uji korelasi sifat amilografi dengan kadar amilosa, rasio amilosa-amilopektin, pengembangan papatan, dan kerenyahan... 82
Lampiran 10a. Uji korelasi rasio amilosa-amilopektin, kadar pati, ph, daya pengembangan dan kelarutan dengan pengembangan papatan dan kerenyahan... 83
Lampiran 10b. Uji korelasi pengembangan papatan dan kerenyahan... 83
Lampiran 11 Penentuan formulasi berdasarkan pendekatan rasio amilosa-amilopektin... 84
Lampiran 12. Uji kerenyahan obyektif penyalut formulasi awal... 85
Lampiran 13. Uji kerenyahan subyektif (rating kerenyahan) penyalut hasil pemilihan formulasi tahap 1... 87
Lampiran 14. Kerenyahan subyektif (rating kerenyahan) penyalut hasil variasi substitusi tapioka modifikasi... 88
Lampiran 15. Uji subyektif (ranking kerenyahan dan penampakan pori-pori) penyalut hasil pemilihan formulasi tahap 2 dan premix kontrol... 90
Lampiran 16. Pengukuran karakteristik premix alternatif : kadar air dan nilai pH... 91
Lampiran 17. Pengukuran karakteristik premix alternatif : kadar pati, kadar amilosa-amilopektin, dan pengembangan papatan... 92 Lampiran 18. Analisis statistik karakteristik kimia premix alternatif dan
premix kontrol... 93 Lampiran 19. Analisis statistik pengembangan papatan premix alternatif
dan premix kontrol... 95 Lampiran 20. Quisioner uji organoleptik... 96 Lampiran 21. Setting alat texture analyser... 98
I. PENDAHULUAN
A. LATAR BELAKANG
Produk fried snack merupakan jenis produk snack yang diolah melalui proses penggorengan. Produk ini cukup digemari oleh masyarakat Indonesia sebagai salah satu pilihan makanan ringan. Menurut survey CIC (Corinthian
Infopharma Corpora) tahun 2005, market size snack modern mencapai 59,5
ribu ton pada tahun 2004 atau naik dari tahun 2003 sebesar 53,6 ribu ton. Sementara, nilai bisnisnya pun pada tahun 2004 sebesar Rp1,9 triliun, sedangkan tahun 2003 Rp 1,7 triliun (Hidayat, 2006).
Salah satu jenis produk fried snack yang telah dikenal oleh masyarakat secara luas adalah kacang salut. Produk ini dibuat dengan menyalut kacang tanah dengan lapisan batter, yang terbuat dari tepung dan lem berbumbu, kemudian digoreng dengan metode deep fat frying. Proses penyalutan kacang oleh batter dilakukan secara bertahap sehingga diperoleh lapisan penyalut yang kompak. Sedangkan proses penggorengan diikuti dengan pengadukan secara konsisten.
Produk-produk pangan yang digoreng, termasuk diantaranya kacang salut, umumnya memiliki karakteristik tekstur yang renyah, rasa matang yang gurih, warna yang lebih menarik, dan bau goreng yang khas (Fellow, 1992). Hal ini dipengaruhi oleh beberapa faktor, diantaranya jenis tepung sebagai bahan penyalut dan minyak yang terserap produk selama penggorengan. Menurut Balagopalan et al. (1988), tekstur pada produk berbahan dasar pati diperoleh dari hasil perubahan pati selama dan setelah pemasakan.
Jenis tepung yang digunakan sebagai lapisan bahan penyalut pada produk kacang salut adalah tepung tapioka. Karakteristik tepung tapioka yang digunakan diharapkan memiliki tingkat pengembangan dan kerenyahan yang baik pada produk kacang salut. Namun dalam aplikasinya, produsen kacang salut harus memasok tepung tapioka dari beberapa pemasok untuk menjamin ketersediaan bahan baku kacang salut. Penggunaan jenis tepung tapioka yang berbeda akan menghasilkan ketidakseragaman tekstur produk, sehingga dapat mempengaruhi preferensi konsumen. Bagi produsen, hal ini perlu diperhatikan
karena dapat memberikan dampak yang negatif. Salah satu upaya yang dapat dilakukan untuk memperoleh tekstur produk yang diinginkan adalah melalui penyeragaman bahan penyalut.
Proses penyeragaman bahan penyalut dapat dilakukan dengan proses pencampuran antar tapioka alami dan substitusi dengan tapioka modifikasi melalui formulasi yang tepat. Substitusi dengan tapioka modifikasi diharapkan dapat meningkatkan tingkat kerenyahan produk kacang salut. Dalam penentuan formulasi pencampuran, diperlukan karakteristik semua jenis tepung tapioka alami yang diterima oleh produsen kacang salut dan mengetahui karakteristik kimia atau fungsional yang memiliki hubungan paling kuat terhadap kerenyahan produk. Karakteristik ini dapat digunakan sebagai dasar penentuan formulasi pencampuran untuk memperoleh tekstur produk yang diinginkan.
Proses pencampuran tapioka akan menghasilkan suatu premix tapioka. Karakteristik premix tapioka yang diperoleh dapat digunakan oleh produsen sebagai standar mutu dalam menentukan jenis tapioka yang disuplai dari pemasok. Dengan demikian, melalui penelitian ini diharapkan dapat mengetahui karakteristik tapioka yang baik digunakan sebagai bahan penyalut pada produk kacang salut dan menghasilkan produk akhir yang lebih renyah.
B. TUJUAN
Secara umum tujuan dari kegiatan magang ini adalah untuk melatih mahasiswa terjun ke dalam dunia kerja dan diharapkan mampu menerapkan ilmu pengetahuan yang dipelajari dalam kuliah untuk memecahkan masalah yang mungkin timbul di lapangan.
Secara khusus magang ini dilakukan untuk mengetahui dan membandingkan karakteristik beberapa jenis tapioka, menentukan formulasi premix tapioka alternatif, serta mengetahui karakteristik premix tapioka yang dapat menghasilkan kerenyahan yang tepat dan penampakan pori-pori yang seragam pada penyalut produk kacang salut.
C. MANFAAT
Hasil yang diperoleh dari magang ini diharapkan dapat memberikan masukan bagi perusahaan dalam menentukan alternatif formulasi premix tapioka dan mengetahui karakteristik bahan penyalut yang dapat menghasilkan kerenyahan serta penampakan pori-pori yang optimal pada produk kacang salut.
II. TINJAUAN PUSTAKA
A. KACANG SALUT
Kacang salut merupakan makanan ringan berupa kacang tanah yang dibalut dengan adonan tepung kemudian digoreng dengan suhu tertentu sampai kacang tanahnya matang dan balutan tepungnya renyah (Wati, 2007). Kacang salut memiliki berbagai macam varian bentuk dan rasa. Di Indonesia, kacang salut sering dikenal dengan sebutan kacang atom. Kacang atom adalah kacang tanah yang dibalut dengan adonan tapioka kemudian digoreng sampai kering dan garing (Hasbullah, 2001). Citarasa kacang salut berasal dari penggunaan bumbu. Bumbu yang lazim digunakan antara lain garam, bawang putih, penyedap rasa dan gula. Bumbu-bumbu tersebut dimasukkan pada saat pembuatan adonan bumbu yang merupakan campuran bumbu, tepung, dan air. Proses pembuatan kacang salut cukup sederhana. Pertama, lem dibuat terlebih dahulu dengan mencampurkan tapioka dengan air, lalu dimasak sampai agak matang dan dicampurkan dengan bumbu-bumbu yang terdiri dari bawang, garam, dan bumbu lainnya. Kacang tanah dicampur dengan sedikit
lem berbumbu dan diaduk hingga semua kacang terbalut oleh lapisan tipis lem
berbumbu. Sedikit tapioka dan kacang tanah yang telah dilapisi lemberbumbu tersebut dimasukkan ke dalam mesin coating pan yang sedang berputar. Setelah semua tapioka melapisi kacang, kemudian dimasukkan sedikit lem. Setelah semua lem melapisi kacang, dimasukkan lagi tapioka. Demikian dilakukan seterusnya sampai lapisan dianggap sudah mencukupi tebal tertentu. Hasil yang diperoleh disebut dengan kacang atom mentah. Kacang atom mentah digoreng di dalam banyak minyak panas (suhu 170°C) sambil diaduk pelan-pelan sampai matang (Hasbullah, 2001).
B. TEKSTUR PRODUK FRIED SNACK
Penerimaan konsumen terhadap suatu produk dapat dipengaruhi oleh beberapa faktor organoleptik seperti tekstur, rasa, warna, dan aroma. Tekstur merupakan salah satu parameter yang sering digunakan dalam menganalisis produk pangan. Terdapat beberapa jenis parameter tekstur yang penting dan
sering digunakan yaitu kekerasan, kekenyalan, elastisitas, kelengketan, kerenyahan, kerapuhan dan sebagainya yang dapat diidentifikasi dengan indera manusia. Pada produk fried snack, seperti kacang salut, parameter tekstur yang penting yaitu kerenyahan.
Produk kacang salut termasuk ke dalam golongan produk berbasis pati. Pembentukan tekstur penyalut pada produk berbasis pati terjadi selama pengolahannya. Menurut Balagopalan et al. (1988), tekstur pada produk berbahan dasar pati diperoleh dari hasil perubahan pati selama dan setelah pemasakan. Pengolahan dari bahan berpati dapat dibagi menjadi beberapa tahapan yaitu bahan-bahan dicampur, diaduk, dan disiapkan. Variabel proses dari operasi pencampuran adalah kombinasi dari suhu, shear/stress, waktu, dan komposisi bahan. Bahan mentah dihidrasi dan komponen-komponen berinteraksi dalam pembentukan struktur. Struktur dapat dibentuk oleh beberapa pendekatan yang berbeda (Rosenthal, 1999).
Karakteristik tepung tapioka yang digunakan sebagai bahan penyalut pada kacang salut mempengaruhi kerenyahan pada produk akhirnya. Menurut Matz (1992), tingkat pengembangan dan tekstur dari makanan ringan (snack) dipengaruhi oleh rasio amilosa dan amilopektin. Pati yang memiliki kandungan amilopektin tinggi cenderung memberikan karakter produk yang
fragile (mudah pecah), sedangkan amilosa akan memberikan tekstur yang
lebih tahan terhadap kemudahan untuk pecah. Rasio amilosa dan amilopektin tertentu akan menghasilkan tingkat kerenyahan yang optimal pada tekstur produk. Kerenyahan produk kacang salut juga berkaitan dengan tingkat pengembangan produk tersebut. Rahman (2007) melaporkan bahwa adanya korelasi positif dan nyata antara tingkat pengembangan papatan dengan skor kerenyahan penyalut produk kacang salut, sehingga dapat disimpulkan bahwa semakin tinggi tingkat pengembangan papatan, maka kerenyahan penyalut pada produk kacang salut akan semakin tinggi.
Perubahan struktural pada tekstur produk snack timbul pada tingkat mikroskopik. Perubahan ini melibatkan peleburan biopolimer atau gelatinisasi pati secara spesifik, denaturasi protein, dan pembentukan kompleks dari komponen fungsional utama tersebut, serta dengan gula dan lemak. Perubahan
ini juga disertai dengan sifat reologi. Penguapan air dan pengembangan termal dari gas yang terperangkap juga terjadi selama proses. Interaksi matriks dan proses pelepasan gas adalah kompleks, tetapi penting untuk struktur produk (Rosenthal, 1999).
Kerenyahan kacang salut dapat dianalisis secara obyektif dengan menggunakan instrumen Texture Analyser dan secara subyektif menggunakan indera manusia (uji organoleptik). Indera manusia dapat merasakan kerenyahan produk snack yang sebenarnya berkaitan dengan sifat kerapuhan (fracturability) produk akibat gaya tekan. Analisis secara obyektif ditentukan dengan melihat gaya (force) pada puncak pertama di mana sampel mulai berubah bentuk (Faridah et al., 2009). Menurut Anonim (2005) diacu dalam Rahman (2007), untuk mengukur kerenyahan tidak hanya dilihat dari gaya (force) untuk mendeformasi sampel tetapi juga dilihat jarak saat gaya mulai menekan sampel (distance). Jika hasil pengukuran sampel memiliki gaya yang sama dengan jarak yang berbeda-beda, maka sampel yang paling renyah adalah sampel dengan jarak yang terdekat. Sebaliknya, jika hasil pengukuran sampel memiliki jarak yang sama, dengan gaya yang berbeda-beda, maka sampel yang paling renyah adalah sampel dengan gaya terendah. Untuk membandingkan kerenyahan antara dua sampel yang memiliki gaya dan jarak yang berbeda, uji organoleptik dapat digunakan untuk mengetahui sampel yang memiliki kerenyahan lebih tinggi.
C. PATI
1. Granula Pati
Pati merupakan polisakarida yang dibentuk dari sejumlah molekul glukosa dengan ikatan α-glikosidik. Oleh karena itu, pati dapat disebut sebagai karbohidrat kompleks (Brithis Nutrition Foundation, 2005). Pati terdiri dari butiran-butiran kecil yang disebut granula. Winarno (2002) menyatakan bahwa granula pati mempunyai sifat merefleksikan cahaya terpolarisasi, sehingga di bawah mikroskop terlihat kristal hitam putih. Sifat inilah yang disebut birefringent. Pada saat granula mulai pecah, sifat
tetapi akan mengembang dalam air panas atau hangat (Greenwood, 1979). Pengembangan granula pati tersebut bersifat bolak-balik jika tidak melewati suhu gelatinisasi dan menjadi tidak bolak-balik jika telah mencapai suhu gelatinisasi.
Secara alami granula pati bersifat semi kristal yang terdiri dari bagian kristal dan bagian amorpus. Level kristalisasi pada pati bervariasi tergantung dari sumbernya. Bagian kristal pada granula pati dipengaruhi oleh komponen amilopektin sedangkan bagian amorpus dipengaruhi oleh komponen amilosa (Zobel,1988). Bagian amorpus tidak tahan terhadap serangan enzim dan asam.
Granula pati dari tanaman yang berbeda memiliki karakteristik ukuran dan bentuk yang berbeda (Charley, 1982). Menurut Whister dan Bemiller (1997), struktur granula pati berbeda antara sereal, terigu, jagung dan umbi-umbian.
2. Amilosa dan Amilopektin
Granula pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi yang tidak terlarut disebut amilopektin (Winarno, 2002). Misela merupakan bagian molekul linier yang berikatan dengan rantai molekul terluar molekul cabang (Pomeranz, 1991). Ikatan ini terjadi apabila bagian-bagian linier molekul pati berada paralel satu sama lain, sehingga gaya ikatan hidrogen akan menarik rantai ini bersatu (Swinkels, 1985). Di antara misela terdapat daerah yang renggang atau amorf (Pomeranz, 1991). Daerah amorf ini kurang padat, sehingga mudah dimasuki air.
Amilosa tersusun dari molekul D-glukopiranosa yang berikatan α-(1,4) dalam struktur rantai lurus. Molekul amilosa lengkap dapat terdiri dari 3000 unit D-glukopiranosa.Panjang polimer dipengaruhi oleh sumber pati dan akan mempengaruhi berat molekul amilosa. Menurut Taggart (2004), amilosa memiliki kemampuan membentuk kristal karena struktur rantai polimernya yang sederhana. Strukturnya yang sederhana ini dapat membentuk interaksi molekular yang kuat. Interaksi ini terjadi pada gugus
hidroksil molekul amilosa. Pembentukan ikatan hidrogen ini lebih mudah terjadi pada amilosa daripada amilopektin. Struktur amilosa dapat dilihat pada Gambar 1.
Gambar 1. Struktur amilosa (Chaplin, 2006)
Amilopektin terdiri dari molekul D-glukosa yang berikatan α-(1,4) dan mengandung ikatan α-(1,6) pada percabangan rantainya. Ikatan ini menyebabkan penampilan molekul amilopektin bercabang-cabang, biasanya terdiri dari 24-30 unit D-glukosa berada di titik percabangan amilopektin (Wilbrahan dan Matta, 1992). Amilopektin juga dapat membentuk kristal, tetapi tidak sereaktif amilosa. Hal ini terjadi karena adanya rantai percabangan yang menghalangi terbentuknya kristal (Taggart, 2004). Struktur amilopektin dapat dilihat pada Gambar 2.
3. Daya Pengembangan (Swelling Power) dan Kelarutan Pati
Bila pati dimasukkan ke dalam air dingin, granula pati akan menyerap air dan membengkak. Namun demikian, jumlah air yang terserap dan pembengkakannya terbatas hanya mencapai 30% (Winarno, 2002). Ketika molekul pati dipanaskan dalam air, struktur kristalin rusak dan molekul air akan terikat oleh ikatan hidrogen pada gugus hidroksil amilosa dan amilopektin yang menyebabkan pengembangan dan kelarutan pada granula.
Perbedaan nilai daya pengembangan dan kelarutan pada beberapa macam pati dari sumber yang berbeda disebabkan oleh perbedaan struktur morfologi pada granula pati (Singh et al., 2002). Menurut Balagopalan et.
al. (1988), daya pengembangan merupakan pertambahan volume dan berat
maksimum yang dialami pati dalam air. Pengembangan terjadi pada daerah amorf granula pati. Ikatan hidrogen yang lemah antar molekul pati pada daerah amorf akan terputus saat pemanasan, sehingga terjadi hidrasi air oleh granula pati. Granula pati akan terus mengembang, sehingga viskositas meningkat hingga volume hidrasi maksimum yang dapat dicapai oleh granula pati (Swinkels, 1985).
Faktor-faktor seperti rasio amilosa-amilopektin, distribusi berat molekul dan panjang rantai, serta derajat percabangan dan konformasinya menentukan daya pengembangan dan kelarutan pati (Moorthy, 2004). Pengembangan granula pati merupakan sifat yang dipengaruhi oleh amilopektin (Li dan Yeh, 2001). Proporsi yang tinggi pada rantai cabang amilopektin memiliki kontribusi dalam peningkatan nilai pengembangan. Selain itu, terdapat korelasi yang negatif antara daya pengembangan pati dengan kadar amilosa (Sasaki dan Matsuki, 1998 diacu dalam Li dan Yeh, 2001). Amilosa dapat membentuk kompleks dengan lipida pada pati sehingga dapat menghambat pengembangan granula (Charles et al. 2005). Kandungan protein dan monogliserida menghambat tingkat pengembangan pada granula pati (Wang dan Seib, 1996; Roach dan Hoseney, 1995 diacu dalam Li dan Yeh, 2001).
Menurut Pomeranz (1991), daya pengembangan pati dapat diukur pada interval suhu 5°C pada kisaran suhu gelatinisasi sampai 100°C. Sementara itu, Li dan Yeh (2001) mengukur daya pengembangan dan kelarutan pati dengan interval 10°C yaitu pada suhu 55°C, 65°C, 75°C, 85°C, dan 95°C. Pengukuran daya pengembangan pati dapat dilakukan dengan membuat suspensi pati dalam botol sentrifusa lalu dipanaskan selama 30 menit pada suhu yang telah ditentukan. Kemudian bagian yang cair (supernatan) dipisahkan dari endapan. Daya pengembangan diukur sebagai berat pati yang mengembang (endapan) per berat pati kering.
Ketika pati dipanaskan dalam air, sebagian molekul amilosa akan keluar dari granula pati dan larut dalam air. Persentase pati yang larut dalam air ini dapat diukur dengan mengeringkan supernatan yang dihasilkan saat pengukuran daya pengembangan. Menurut Fleche (1985), ketika molekul pati sudah benar-benar terhidrasi, molekul-molekulnya mulai menyebar ke media yang ada di luarnya dan yang pertama keluar adalah molekul-molekul amilosa yang memiliki rantai pendek. Selama pemanasan akan terjadi pemecahan granula pati, sehingga pati dengan kadar amilosa lebih tinggi, granulanya akan lebih banyak mengeluarkan amilosa (Mulyandari, 1992). Semakin tinggi suhu maka semakin banyak molekul pati yang akan keluar dari granula pati. Menurut Pomeranz (1991), kelarutan pati semakin tinggi dengan meningkatnya suhu, serta kecepatan peningkatan kelarutan adalah khas untuk tiap pati.
4. Gelatinisasi Pati
Pomeranz (1991) menyatakan bahwa gelatinisasi merupakan proses pembengkakan granula pati ketika dipanaskan dalam media air.
Gelatinisasi diawali dengan pembengkakan granula, bersifat irreversible (tidak dapat kembali), dipengaruhi oleh suhu dan kadar air, menghasilkan peningkatan viskositas, serta dipengaruhi oleh kondisi pemanasan dan tipe granula pati (Huang dan Rooney, 2001).
Moorthy (2004) menyatakan bahwa gelatinisasi merupakan fenomena kompleks yang bergantung dari ukuran granula, persentase
amilosa, bobot molekul, dan derajat kristalisasi dari molekul pati di dalam granula. Pada umumnya granula yang kecil membentuk gel lebih lambat sehingga mempunyai suhu gelatinisasi yang lebih tinggi daripada granula yang besar. Makin besar bobot molekul dan derajat kristalisasi dari granula pati, pembentukkan gel semakin lambat. Proses gelatinisasi melibatkan peristiwa-peristiwa sebagai berikut: (1) hidrasi dan swelling (pengembangan) granula; (2) hilangnya sifat birefringent; (3) peningkatan kejernihan; (4) peningkatan konsistensi dan pencapaian viskositas puncak; (5) pemutusan molekul-molekul linier dan penyebarannya dari granula yang telah pecah.
Terdapat beberapa faktor yang mempengaruhi proses gelatinisasi pati diantaranya yaitu konsentrasi larutan pati, pH, dan karakteristik granula pati. Menurut Winarno (2002), Makin kental larutan, suhu gelatinisasi makin sulit tercapai dan bila pH terlalu tinggi, pembentukan gel semakin cepat tercapai tetapi cepat turun lagi. Pembentukan gel optimum pada pH 4-7. Selain itu, penambahan gula juga berpengaruh terhadap kekentalan gel yang terbentuk. Gula akan menurunkan kekentalan, hal ini disebabkan karena gula dapat mengikat air, sehingga pembengkakan butir-butir pati menjadi lebih lambat, akibatnya suhu gelatinisasi akan lebih tinggi. Adanya gula akan menyebabkan gel lebih tahan terhadap kerusakan mekanik. Sedangkan Charles et al. (2005) melaporkan bahwa suhu gelatinisasi dipengaruhi oleh kadar amilosa.
Salah satu metode yang dapat digunakan untuk melihat sifat gelatinisasi pati yaitu dengan melihat profil gelatinisasinya. Profil gelatinisasi dapat ditentukan dengan menggunakan alat Brabender Amilograph. Brabender Amilograph merupakan alat viscometer yang dirancang untuk dapat mengukur viskositas pasta pati secara kontinu selama pemanasan dan pendinginan (Wurzburg, 1989). Beberapa sifat anilografi yang dapat diperoleh yaitu diantaranya, waktu gelatinisasi, suhu gelatinisasi, waktu granula pecah, viskositas puncak, suhu granula pecah, viskositas pada suhu 95°C, viskositas pada suhu 95°C setelah holding, viskositas breakdown, kestabilan viskositas pasta selama pemanasan,
viskositas pada suhu 50°C, viskositas setback, dan kestabilan viskositas pasta terhadap proses pengadukan.
D. TAPIOKA
1. Proses Pembuatan Tapioka
Pabrik pembuatan tapioka digolongkan dalam tiga tipe, yaitu pabrik tradisional (kecil), semimodern (medium), dan modern (besar). Menurut Radley (1976), pada pabrik kecil pembuatan tapioka dilakukan oleh sebuah keluarga secara tradisional dan dapat memproduksi tapioka maksimal 200 kg per hari. Sedangkan pabrik medium menggunakan peralatan yang lebih efisien dan memproduksi 5000 kg per hari. Sementara itu, pabrik besar mampu memproduksi 40.000 kg tapioka kering per hari serta menggunakan singkong dengan varietas tertentu untuk mengontrol kualitas tapioka yang diproduksi. Jadi perbedaan diantara ketiga tipe pabrik tapioka tersebut diantaranya adalah peralatan yang digunakan, kapasitas produksi, dan kualitas tapioka yang dihasilkan.
Secara umum, proses pembuatan tapioka dibagi dalam empat tahap yaitu, pertama pembersihan, pengelupasan kulit, pemarutan dan penyaringan ampas dengan penambahan air. Kedua, pengendapan, pembersihan pati di dalam tangki, dan pemisahan endapan atau melalui sentrifugasi. Ketiga, proses pengeringan dan keempat, penggilingan (Radley, 1976).
Perbedaan peralatan yang digunakan untuk memproduksi tapioka oleh masing-masing jenis pabrik diantaranya adalah proses pemisahan pati pada industri modern menggunakan alat sentirfus sedangkan pada industri tradisional pemisahan pati dilakukan dengan proses pengendapan beberapa jam. Proses pengendapan ini akan mempengaruhi kualitas pati yang dihasilkan seperti nilai pH menjadi lebih rendah karena terbentuknya asam organik akibat fermentasi oleh bakteri (Radley, 1976). Proses pengeringan pada pabrik modern umumnya menggunakan alat pengering seperti oven dan flash drier, sedangkan pada pabrik tradisional menggunakan sinar matahari. Perbedaan proses pengeringan ini dapat mempengaruhi nilai
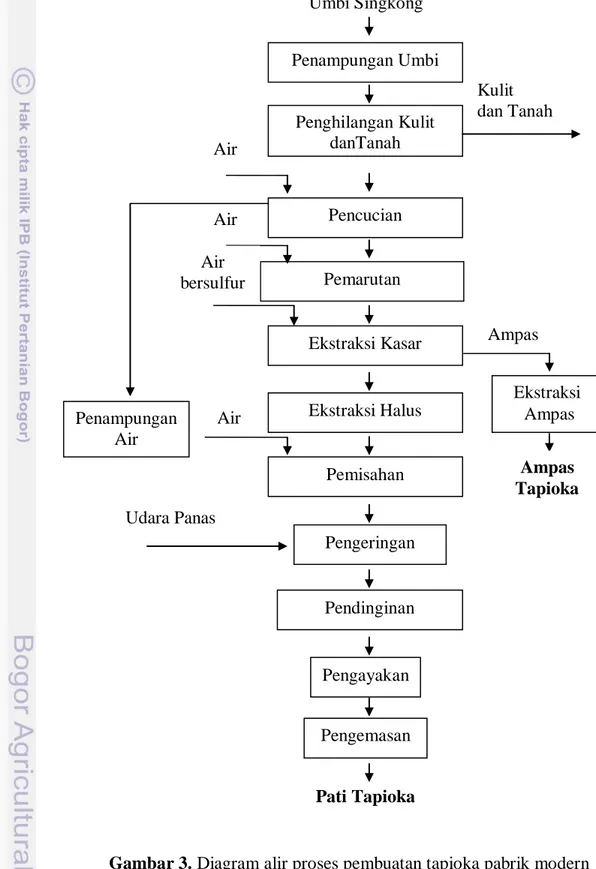
kadar air tapioka yang dihasilkan. Salah satu contoh alur proses pembuatan tapioka pada pabrik modern dapat dilihat pada Gambar 3.
Gambar 3. Diagram alir proses pembuatan tapioka pabrik modern Penampungan Umbi Penghilangan Kulit danTanah Pencucian Pemarutan Ekstraksi Kasar Ekstraksi Halus Pemisahan Pengeringan Pendinginan Pengayakan Pengemasan Pati Tapioka Umbi Singkong Air Air Ampas Ekstraksi Ampas Ampas Tapioka Penampungan Air Udara Panas Kulit dan Tanah Air Air bersulfur
2. Karakteristik Tapioka
Tapioka merupakan pati yang diekstrak dari umbi singkong. Juliana (2007) melaporkan rendemen pati singkong (tapioka) adalah 11.79% dengan kadar air 6.15% dari berat kering. Nilai pati pada singkong dipengaruhi oleh usia atau kematangan dari tanaman singkong. Komposisi kimia tepung tapioka dapat dilihat pada Tabel 1.
Tabel 1. Komposisi kimia tepung tapioka
Komposisi Jumlah Serat (%) 0.5 Air (%) 15 Karbohidrat (%) 85 Protein (%) 0.5-0.7 Lemak (%) 0.2
Energi (kalori/100 gram) 307
Sumber: Grace (1977)
Kadar pati tepung tapioka tidak dipersyaratkan dalam SNI. Rahman (2007) melaporkan kadar pati pada tepung tapioka berkisar antara 72-81%bb dan kadar abu pada tapioka berkisar antara 0.01-0.04%bb. Menurut Moorthy (2004), kadar amilosa tepung tapioka berada pada kisaran 20-27% dari kadar patinya dan kadar lipid pada tapioka sangat rendah (<0.1%).
The Tapioca Institute of America (TIA) menetapkan standar pH
tepung tapioka adalah 4.5-6.5 (Radley, 1976), sedangkan nilai keasaman tapioka berdasarkan SNI 01-3451-1994 ditetapkan dalam bentuk derajat asam, yaitu maksimal sebesar 3 NaOH 1N/100g. Syarat mutu tepung tapioka sesuai SNI dapat dilihat pada Tabel 2.
Tabel 2. Syarat mutu tepung tapioka menurut SNI 01-3451-1994
No Jenis uji Satuan Persyaratan
Mutu I Mutu II Mutu III 1.
Kadar air % Maks.15.0 Maks.15.0 Maks.15.0 2.
Kadar abu % Maks. 0.60 Maks. 0.60 Maks. 0.60 3. Serat dan benda
asing % Maks. 0.60 Maks. 0.60 Maks. 0.60 4. Derajat putih
(BaSO4=100%) % Min. 94.5 Min. 92.0 <92 5. Derajat asam
Volume NaOH 1N/100g
Maks. 3 Maks. 3 Maks. 3 6. Cemaran logam - Timbal - Tembaga - Seng - Raksa - Arsen mg/kg mg/kg mg/kg mg/kg mg/kg Maks. 1.0 Maks. 10.0 Maks. 40.0 Maks. 0.05 Maks. 0,5 Maks. 1.0 Maks. 10.0 Maks. 40.0 Maks. 0.05 Maks. 0,5 Maks. 1.0 Maks. 10.0 Maks. 40.0 Maks. 0.05 Maks. 0,5 7. Cemaran mikroba - Angka lempeng total - E. coli - Kapang Koloni/g Koloni/g Koloni/g Maks. 1.0 x 106 - Maks. 1.0 x 104 Maks. 1.0 x 106 - Maks. 1.0 x 104 Maks. 1.0 x 106 - Maks. 1.0 x 104 Menurut Moorthy (2004), ukuran granula tapioka menunjukan variasi yang besar yaitu sekitar 5-40 µm dengan bentuk bulat dan oval. Variasi tersebut dipengaruhi oleh varietas tanaman singkong dan periode pertumbuhan pada musim yang berbeda. Sedangkan Charley (1982) menyebutkan bahwa diameter granula pati tapioka berkisar antara 12-25 µm. Granula tapioka berbentuk mangkuk (cup) dan sangat kompak, tetapi selama pengolahan granula tersebut akan pecah menjadi komponen-komponen yang tidak teratur bentuknya (Swinkels, 1985). Contoh bentuk granula tapioka dapat dilihat pada Gambar 4.
Gambar 4. Granula tapioka (Anonim, 2008)
Pati singkong atau tapioka memiliki suhu gelatinisasi yang sangat rendah, lebih rendah dari pati umbi-umbian yang lain maupun pati sereal. Menurut Grosch dan Belitz (1987), pati dari akar dan umbi lebih mudah dan cepat mengembang dibandingkan dengan pati serealia karena pati serealia strukturnya lebih kompak. Suhu gelatinisasi tepung tapioka berada pada kisaran 52-64°C. Sedangkan Wurzburg (1989) melaporkan bahwa suhu gelatinisasi tepung tapioka berkisar antara 58.5-70°C. Tepung tapioka memiliki daya pengembangan yang besar (Balagopalan et al., 1988).
E. PATI PREGELATINISASI
Pati modifikasi merupakan pati yang diberi perlakuan tertentu agar dihasilkan sifat yang lebih baik dari sifat sebelumnya, terutama sifat fisiko-kimia dan fungsionalnya atau untuk mengubah beberapa sifat lainnya. Menurut Munarso (2004), pati modifikasi merupakan pati yang diberi perlakuan sedemikian rupa baik secara fisik maupun kimia sehingga mempunyai sifat reologi dan fungsional yang berbeda dari pati aslinya. Modifikasi pati dirancang untuk mengubah karakteristik gelatinisasi, hubungan padatan dan kekentalan, kecenderungan pembentukan gel pada dispersi pati, sifat hidrofilik, kekuatan menahan air pada dispersi pati saat suhu rendah, ketahanan dispersi terhadap penurunan kekentalan oleh asam, maupun perusakan secara fisik dan memasukkan sifat ionisasi pati asal (Erungan, 1991).
Beberapa metode modifikasi pati antara lain modifikasi dengan pemuliaan tanaman, konversi dengan hidrolisis (asam atau oksidator), cross
linking, derivatisasi secara kimia (esterifikasi dan eterifikasi), serta perlakuan
fisik yang akan menghasilkan perubahan bentuk, ukuran serta struktur molekul pati (Bao dan Bergman, 2004). Sedangkan menurut Tjokroadikoesoemo (1986), pati dapat dimodifikasi melalui cara hidrolisis, oksidasi, cross-linking atau cross bonding dan substitusi. Hasil modifikasi tersebut antara lain thin-boiling starch, pati teroksidasi, pati pregelatinisasi,
cross linked atau cross bonding starch, pati termodifikasi asam, dan pati
termodifikasi α-amilase. Modifikasi pati secara fisik melibatkan beberapa faktor yaitu suhu, tekanan, pemotongan, dan kadar air pati. Bila dibandingkan dengan modifikasi kimia, modifikasi fisik cenderung lebih aman karena tidak menggunakan berbagai pereaksi kimia. Perlakuan modifikasi secara fisik yaitu ekstrusi, praboiling (pregelatinisasi), steam-cooking, iradiasi microwave, pemanggangan, hydrotermal treatment, dan autoclaving (Bao dan Bergman 2004).
Pregelatinisasi merupakan teknik modifikasi pati secara fisik paling sederhana yang dilakukan dengan cara memasak pati di dalam air sehingga tergelatinisasi sempurna, kemudian mengeringkan pasta pati yang dihasilkan dengan menggunakan spray dryer atau drum dryer (Kusnandar, 2006). Menurut Light (1990), pregelatinisasi pati digunakan pada peningkatan viskositas dalam sistem instan, pengembangan pati pada air dingin untuk sistem instan yang membutuhkan ketahanan terhadap proses lain, dan penyesuaian ukuran partikel untuk mengontrol kemampuan dispersi dan hidrasi.
Pregelatinisasi menyebabkan kerusakan struktur granula dan ikatan hidrogen sehingga sifat alami pati tidak dapat dipertahankan. Modifikasi ini banyak digunakan untuk proses instan, agen penstabil koloid dan pengikat air pada makanan bayi, es krim, premix pada produk dry baking dan lainnya (Davidek et al.,1990). Menurut Grosch dan Belitz (1987), beberapa tepung pregelatinisasi dicampur dengan tepung guar atau dengan alginat. Contoh bentuk granula pati pregelatinisasi dapat dilihat pada Gambar 5.
(a)
(b)
Gambar 5. Granula pati pregelatinisasi (500x) metode spray cooked (a) dan drum dried (b) (Mitolo, 2006)
III. KEGIATAN MAGANG
A. DESKRIPSI KEGIATAN MAGANG
Kegiatan magang dilaksanakan di sebuah perusahaan snack di wilayah Jabotabek selama empat bulan. Kegiatan magang ini dimulai pada tanggal 10 Maret sampai dengan 10 Juli 2009 yang dilakukan setiap hari kerja dengan jam kerja 08.30 WIB sampai dengan 17.30 WIB. Kegiatan selama melakukan magang meliputi karakterisasi tapioka dan penentuan formulasi premix tapioka sebagai bahan penyalut untuk produk fried snack. Pada minggu pertama, kegiatan yang dilakukan adalah orientasi, penyediaan alat dan bahan penelitian yang akan digunakan. Kemudian pada minggu-minggu selanjutnya dilakukan penelitian terhadap topik magang. Hasil magang yang dilaporkan dalam skripsi ini adalah berupa data karakteritik tapioka, formulasi dan karakteristik premix tapioka alternatif terbaik.
B. RUMUSAN PERMASALAHAN
Tepung tapioka sebagai salah satu bahan baku utama dalam pembuatan kacang salut tentu mempengaruhi kualitas kacang salut yang dihasilkan. Tepung tapioka yang digunakan oleh perusahaan merupakan tepung tapioka yang dipasok dari beberapa produsen tapioka. Tepung tapioka yang diperoleh tersebut memiliki karakteristik yang tidak seragam. Pada produk kacang salut, tepung tapioka digunakan sebagai bahan penyalut. Penggunaan tepung tapioka yang tidak seragam akan menghasilkan kualitas tekstur produk kacang salut yang beragam pula. Salah satu upaya yang dapat dilakukan untuk memperoleh tekstur produk yang diinginkan adalah melalui penyeragaman bahan penyalut. Proses penyeragaman dapat dilakukan dengan cara pembuatan premix tapioka yang merupakan campuran beberapa jenis tapioka. Formulasi pencampuran diharapkan dapat menghasilkan tekstur produk kacang salut yang optimal.
Pada kegiatan magang ini dilakukan penelitian mengenai karakteristik beberapa jenis tapioka. Melalui karakteristik tersebut, dapat ditentukan formulasi premix yang cocok sebagai bahan penyalut pada produk kacang salut serta karakteristik bahan penyalut yang baik digunakan untuk produk
kacang salut. Karakteristik bahan penyalut yang baik digunakan pada produk kacang salut adalah bahan penyalut yang dapat menghasilkan tingkat kerenyahan yang optimal dan penampakan pori-pori yang seragam pada produk. Disamping itu, usaha peningkatan kerenyahan kacang salut dapat juga dilakukan dengan melakukan substitusi tapioka modifikasi pada bahan penyalut.
C. METODOLOGI PEMECAHAN MASALAH 1. Bahan dan Alat
Bahan utama yang digunakan untuk pembuatan kacang salut adalah kacang tanah, tepung tapioka, bumbu, air, minyak goreng. Sampel tapioka yang dianalisis ini terdiri dari tapioka alami, tapioka modifikasi dan premix kontrol. Sampel tapioka alami terdiri dari empat jenis tapioka yaitu Tapioka A, Tapioka B, Tapioka C, dan Tapioka D, yang diperoleh dari pemasok yang berbeda. Pati modifikasi yang digunakan adalah pati pregelatinisasi yang juga diperoleh dari pemasok. Premix kontrol merupakan premix tapioka yang biasa digunakan oleh perusahaan sebagai bahan penyalut pada produk kacang salut.
Bahan-bahan kimia yang digunakan untuk analisis adalah amilosa murni, etanol 95%, NaOH 1 N, asam asetat 1N, larutan Iod (0.2 gram iod dan 2 gram KI dalam 100 ml air), HCl 3% dan 25%, NaOH 3% dan 30%, buffer pH 4, buffer pH 7, Na2CO3 anhidarat, asam sitrat, CuSO4.5H2O,
indikator PP, H2SO4 25%, KI 20%, Na2S2O3 0.1N, K2Cr2O7, KI, indikator
kanji dan akuades.
Alat yang digunakan adalah mesin coating pan, mixer, kompor, neraca analitik, neraca teknis, penggorengan, kertas saring, corong, oven, cawan alumunium, gelas piala, labu takar, desikator, pipet, erlenmeyer asah, erlenmeyer biasa, hot plate magnetic stirrer, buret, Spektrofotometer, waterbath, vortex, pH-meter, Texture Analyser, Brabender Amylograph, sentrifus, dan alat-alat gelas lainnya.
2. Metode Penelitian
Tahapan penelitian yang dilakukan penulis selama kegiatan magang yaitu pertama, karakterisasi sampel tapioka (tapioka alami, tapioka modifikasi dan premix kontrol). Karakterisasi yang dilakukan meliputi sifat kimia dan fungsional, tingkat pengembangan papatan, serta analisis secara subyektif dan obyektif terhadap kerenyahan tekstur penyalut yang dihasilkan oleh masing-masing sampel tapioka. Selanjutnya dilakukan analisis korelasi untuk menentukan karakteristik yang paling berpengaruh terhadap pengembangan papatan dan kerenyahan penyalut.
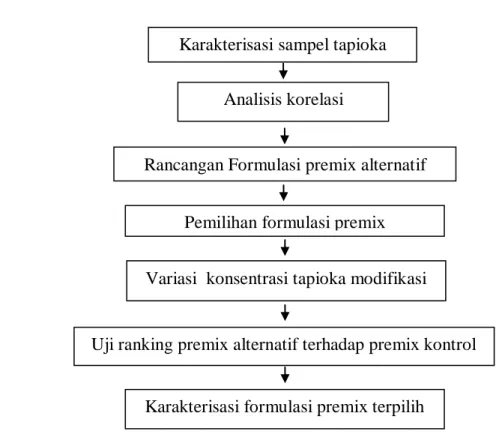
Tahap berikutnya adalah penentuan formulasi premix alternatif melalui rancangan formulasi, pemilihan formulasi terbaik dan variasi substitusi pati modifikasi. Formulasi terbaik yang diperoleh, kemudian dibandingkan dengan premix kontrol. Parameter yang dibandingkan berupa karakteristik, kerenyahan dan penampakan pori-pori penyalut yang dihasilkan oleh premix tersebut. Gambaran umum metode penelitian dapat dilihat pada Gambar 6.
Gambar 6. Diagram alir metode penelitian Karakterisasi sampel tapioka
Analisis korelasi
Rancangan Formulasi premix alternatif
Pemilihan formulasi premix Variasi konsentrasi tapioka modifikasi
Karakterisasi formulasi premix terpilih
a. Karakterisasi Tapioka
1) Analisis Sifat Kimia dan Fungsional Tepung Tapioka
Pada tahap ini dilakukan analisis beberapa sifat kimia dan fungsional sampel tapioka alami, tapioka modifikasi dan premix kontrol. Sifat kimia dan fungsional yang diuji meliputi kadar air, nilai pH, kadar pati, kadar amilosa dan amilopektin, daya pengembangan dan kelarutan, serta pola gelatinisasi.
2) Analisis Tingkat Pengembangan Papatan Kacang Salut
Papatan merupakan istilah yang digunakan untuk bagian
penyalut produk kacang salut sebelum dilakukan proses penggorengan. Papatan ini terdiri dari lapisan lem berbumbu dan tepung tapioka yang menyalut kacang tanah dengan menggunakan mesin coating pan. Analisis tingkat pengembangan papatan dilakukan pada sampel tapioka alami dan premix kontrol. Tingkat pengembangan papatan dipelajari dengan mengukur persentasi rasio volume spesifik kacang salut setelah digoreng terhadap volume spesifiknya sebelum digoreng. Diagram alir proses pembuatan lem berbumbu dapat dilihat pada Gambar 7 dan Diagram alir proses pembuatan kacang salut dapat dilihat pada Gambar 8.
Gambar 7. Diagram alir pembuatan lem berbumbu Bumbu
Lem berbumbu Air
Pencampuran
Gambar 8. Diagram alir pembuatan kacang salut
Tingkat pengembangan papatan = × 100% Keterangan :
V1 = volume kacang salut sebelum digoreng (cm3) V2 = volume kacang salut setelah digoreng (cm3)
3) Analisis Kerenyahan Produk Kacang Salut
Analisis kerenyahan tekstur produk dilakukan secara obyektif dan subyektif. Analisis ini dilakukan pada produk kacang salut yang menggunakan sampel tapioka alami dan premix kontrol sebagai bahan penyalutnya. Analisis obyektif kerenyahan kacang salut dilakukan dengan menggunakan instrumen Texture Analyser. Nilai kerenyahan obyektif ditentukan sebagai nilai kerapuhan (fracturability) yaitu berdasarkan besarnya gaya yang diperlukan untuk mendeformasi bagian salutan kacang salut. Semakin besar gaya yang diperlukan maka semakin rendah nilai kerenyahan
Lem berbumbu
Kacang Tanah
Kacang yang telah disalut papatan Kacang Salut Volume I (V1) Volume II (V2) Sampel tapioka Penyalutan di dalam coating pan Penirisan Penggorengan
sampel. Sedangkan analisis subyektif terhadap produk berupa analisis tekstur kerenyahan dengan pengujian organoleptik. Uji organoleptik yang digunakan pada tahap karakterisasi tapioka ini adalah uji rating intensitas kerenyahan produk dengan menggunakan 10 orang panelis terlatih.
b. Penentuan Formulasi Premix Alternatif 1) Rancangan Formulasi Premix
Premix merupakan campuran beberapa tapioka alami yang dilakukan melalui proses pencampuran kering dengan atau tanpa substitusi tapioka modifikasi. Rancangan formulasi pencampuran didasarkan pada pendekatan nilai parameter kimia atau fungsional premix kontrol melalui prinsip kesetimbangan massa. Parameter yang digunakan adalah sifat kimia atau fungsional yang paling berhubungan terhadap pengembangan papatan dan tekstur (kerenyahan) produk. Disamping itu, masing-masing formulasi premix disubstitusikan dengan tapioka modifikasi sebesar 4%.
2) Pemilihan Formulasi Premix
Pemilihan formulasi premix merupakan tahapan yang dilakukan untuk menyeleksi formulasi premix yang telah ditentukan. Proses penyeleksian dilakukan dengan mengaplikasikan formulasi premix sebagai bahan penyalut pada produk kacang salut. Karakteristik yang dinilai adalah kerenyahan bagian penyalut. Pemilihan formulasi ini dilakukan dalam dua tahap. Pemilihan formulasi tahap I dilakukan secara obyektif menggunakan instrumen Texture Analyser. Formulasi premix yang lolos tahap ini adalah formulasi yang menghasilkan nilai kerenyahan mendekati kerenyahan produk kontrol. Produk kontrol merupakan produk kacang salut yang menggunakan premix kontrol sebagai bahan penyalut.
Pemilihan formulasi tahap II dilakukan secara subyektif yaitu menggunakan uji rating terhadap atribut kerenyahan penyalut dengan menggunakan 10 orang panelis terlatih. Formulasi yang dipilih adalah formulasi yang menghasilkan penyalut dengan skor kerenyahan tertinggi.
3) Variasi Substitusi Tapioka Modifikasi
Variasi substitusi tapioka modifikasi dilakukan pada formulasi premix alternatif yang diperoleh melalui tahap pemilihan formulasi. Variasi konsentrasi yang dilakukan adalah 2, 4, dan 6%. Selanjutnya dilakukan uji rating kerenyahan penyalut yang dibuat dari beberapa konsentrasi tersebut dengan menggunakan 10 orang panelis terlatih.
c. Uji Ranking Kerenyahan
Uji ranking dilakukan untuk membandingkan kerenyahan produk yang menggunakan premix alternatif sebagai bahan penyalut dengan produk kontrol. Melalui uji ini, dapat diketahui apakah premix alternatif yang diperoleh pada penelitian ini telah dapat digunakan sebagai bahan penyalut pada produk kacang salut.
d. Karakterisasi Premix Alternatif
Karakterisasi premix alternatif dilakukan untuk mengetahui karakteristik bahan penyalut yang tepat digunakan sebagai bahan penyalut pada produk kacang salut. Parameter yang dianalisis adalah sifat kimia dan pengembangan papatan. Sifat kimia yang dianalisis adalah kadar air, pH, kadar pati, kadar amilosa dan kadar amilopektin.
3. Metode Analisis
a. Kadar Air (AOAC, 1995)
Cawan alumunium dikeringkan dalam oven pada suhu 105oC selama 15 menit, lalu didinginkan di dalam desikator selama 10 menit.
Cawan ditimbang menggunakan neraca analitik (A). Sampel sebanyak 5 gram (W) dimasukkan ke dalam cawan, kemudian cawan serta sampel ditimbang dengan neraca analitik. Cawan berisi sampel dikeringkan dalam oven pada suhu 105oC selama 6 jam. Selanjutnya cawan berisi sampel didinginkan dalam desikator, kemudian ditimbang (Y). Setelah itu, cawan berisi sampel dikeringkan kembali dalam oven selama 15-30 menit, lalu ditimbang kembali. Pengeringan diulangi hingga diperoleh bobot konstan. Kadar air diukur dengan cara sebagai berikut:
Keterangan :
W = bobot sampel awal (g)
Y = bobot sampel dan cawan setelah dikeringkan (g) A = bobot cawan kosong (g)
b. Kadar Pati (SNI 01-2892-1992) 1) Pembuatan Larutan Luff Schrool
Sebanyak 71.9 g Na2CO3 anhidrat dilarutkan dalam 300 mL
akuades yang dipanaskan. Setelah larut,kemudian ditambahkan 25 g asam sitrat yang telah dilarutkan dengan 25 mL akuades sedikit demi sedikit. Kemudian di tambahkan 8 g CuSO4.5H2O dalam 100
mL akuades sedikit demi sedikit. Setelah semua bercampur, kemudian penangas diturunkan suhunya dan dibiarkan selama 30 menit, setelah itu larutan ditera sampai 500 mL dan dibiarkan selama satu malam di tempat gelap.
2) Analisis sampel
Sebanyak 1 gram sampel tepung dilarutkan dalam 40 mL HCl 3%, dan di refluks selama 3 jam dengan suhu sekitar 200-250°C. Sampel didinginkan dan kemudian dinetralkan dengan menambahkan beberapa tetes NaOH 3% dengan bantuan indikator
PP sampai berwarna merah muda dan diasamkan sedikit dengan menggunakan HCl 3% sampai pH nya sedikit asam yaitu sekitar 6, kemudian ditera dalam labu takar 100 mL dengan menggunakan akuades lalu disaring menggunakan kertas saring. Sebanyak 5 mL filtrat dipipet ke dalam erlenmeyer asah dan ditambahkan 25 mL larutan Luff Schrool dan 20 mL akuades dan direfluks kembali selama 10 menit (dihitung pada saat mulai mendidih). Setelah mendidih, kemudian didinginkan dalam boks es selama beberapa menit. Kemudian sampel yang telah dingin ditambahkan 25 mL H2SO4 25% dan 15 mL larutan KI 20% lalu segera dititrasi dengan Na2S2O3 0.1 N yang telah distandarisasi. Penambahan
indikator kanji 0.5% dilakukan pada saat titrasi berlangsung yaitu pada saat larutan berubah warna menjadi kuning muda. Titrasi dihentikan pada saat larutan berubah warna dari ungu menjadi putih keruh.
Penentuan blanko dilakukan dengan mencampurkan 25 mL larutan Luff Schrool dan 25 mL akuades (tanpa sampel). Kemudian direfluks selama 10 menit (dihitung pada saat mulai mendidih ), lalu didinginkan dalam boks es selama beberapa menit. Kemudian ditambahkan 25 mL H2SO4 25% dan 10 mL larutan KI 20%, dan
segera dititrasi dengan larutan Na2S2O3 0.1N yang telah
distandarisasi. Penambahan indikator kanji 0.5% di lakukan pada saat titrasi berlangsung yaitu pada saat larutan berubah warna menjadi kuning muda. Titrasi dihentikann pada saat larutan berubah warna dari ungu menjadi putih keruh. Kadar pati basis kering pada sampel diukur dengan cara sebagai berikut:
Keterangan :
G = mg glukosa dari tabel glukosa “Luff-Schoorl” Fp = faktor pengenceran
W = bobot sampel (mg) Ka = kadar air sampel
c. Kadar Amilosa dan Amilopektin (Apriyantono et al., 1998) 1) Pembuatan kurva standar
Sebanyak 40 mg amilosa standar dilarutkan dalam 10 ml NaOH alkoholik (1 ml etanol 95% dan 9 ml NaOH 1 N). Campuran ini dipanaskan dalam air mendidih selama kurang lebih 10 menit sampai semua bahan terlarut, lalu didinginkan. Kemudian campuran tadi (larutan amilosa) dipindahkan ke dalam labu takar 100 ml dan ditambahkan air suling sampai tanda tera. Setelah itu, dipipet masing 1, 2, 3, 4, dan 5 ml larutan amilosa, masing-masing dimasukkan ke dalam labu ukur 100 ml. Larutan diasamkan dengan asam asetat 1 N masing-masing sebanyak 0.2, 0.4, 0.6, 0.8, dan 1.0 ml. Lalu ditambahkan 2.0 ml larutan iodine (0.2 gram iod dan 2 gram KI dalam 100 ml air) dan kemudian diencerkan dengan akuades sampai tanda tera, dikocok dan dibiarkan selama 20 menit. Larutan dianalisa dengan Spektrofotometer pada panjang gelombang 625 nm. Kurva amilosa standar dibuat dengan menghubungkan nilai kadar amilosa pada sumbu X dan absorbansi pada sumbu Y. Kemudian dihitung persamaan linear yang menggambarkan hubungan antar keduanya. 2) Analisis sampel
Sebanyak 100 mg sampel ditimbang dan dimasukkan dalam labu ukur 100 ml, kemudian 1 ml etanol 95% dan 9 ml NaOH 1 N ditambahkan ke dalam sampel. Larutan dipanaskan dalam water
bath (air mendidih) selama 10 menit (sampai pati tergelatinisasi).
Setelah itu, labu ukur yang berisi sampel didinginkan selama 1 jam dan ditambahkan akuades sampai tanda tera, kemudian dikocok.
Sebanyak 5 ml larutan sampel dipipet dan dimasukkan ke dalam labu ukur 100 ml yang telah diisi 40 ml akuades. Sebanyak 1 ml asam asetet 1 N dan 2 ml larutan, kemudian ditambahkan air sampai tanda tera. Larutan sampel dikocok dan dibiarkan selama 20 menit, kemudian warna biru yang terbentuk diukur intensitas dengan Spektrofotometer pada panjang gelombang 625 nm. Selain itu, dibuat juga larutan blanko dengan cara mencampurkan semua bahan kecuali sampel. Konsentrasi amilosa sampel (mg/ml) dihitung dengan menggunakan persamaan linear yang diperoleh dari kurva standar amilosa. Sedangkan persentase basis kering amilosa pada sampel dihitung dengan cara sebagai berikut :
Kadar amilosa bk (%) = x 100%
Keterangan :
A = konsentrasi amilosa dari kurva standar (mg/ml) Fp = faktor pengenceran
V = volume awal (ml) W = bobot awal (mg) Ka = kadar air sampel (%)
Kadar amilopektin ditentukan melalui selisih antara kadar pati dengan kadar amilosa sampel.
d. Nilai pH (AOAC 1995)
Nilai pH diukur dengan menggunakan pH-meter. Sebelum digunakan, pH meter dikalibrasi terlebih dahulu dengan menggunakan buffer pH 4 dan pH 7. Nilai pH sampel tapioka diukur dengan terlebih dahulu membuat suspensi tapioka 10%, yaitu 10 gram tepung tapioka dilarutkan dengan aquades bebas CO2 hingga mencapai volume 100
ml. Aquades bebas CO2 diperoleh dengan mendidihkan aquades
e. Daya Pengembangan dan Kelarutan Pati (Li dan Yeh, 2001)
Li dan Yeh (2001) mengukur daya pengembangan dan kelarutan pati dengan interval 10°C yaitu pada suhu 55, 65, 75, 85, dan 95°C. Pati dengan konsentrasi 1%bb dipanaskan pada waterbath dengan suhu 55, 65, 75, 85, dan 95 selama 30 menit, kemudian disentrifusi dengan kecepatan 3000 rpm selama 30 menit, lalu supernatan dipisahkan dari endapan. Nilai daya pengembangan diukur dengan membagi berat endapan dengan berat pati kering sebelum dipanaskan (g/g). Kelarutan diukur dengan mengeringkan supernatan hasil pemisahan sampai beratnya konstan. Kelarutan dinyatakan sebagai persen berat pati yang larut dalam air. daya pengembangan dan kelarutan diukur dengan cara sebagai berikut:
Keterangan :
W = berat sampel (g) x = berat cawan kosong (g) y = berat cawan dan endapan (g) ka = kadar air sampel (%)
Keterangan :
DP = daya pengembangan (g/g) W = berat sampel (g)
X = berat tabung kosong (g) Y = berat tabung dan endapan (g) ka = kadar air sampel (%)