83
Pengaruh Medium Tercemar Logam Pb dan Cu terhadap
Pertumbuhan Nannochloropsis Salina
Abd. Wahid Wahab, Yusafir Hala* dan Fibiyanthy
Jurusan Kimia Fakultas MIPA Universitas Hasanuddin, Makassar 90245
Effect of Medium Contaminated Pb and Cu toward
the Growth Ofnannochloropsis Salina
Abd. Wahid Wahab, Yusafir Hala* and Fibiyanthy
Chemistry DepartementFaculty of Mathematics and Natural Sciences Hasanuddin University Makassar 90245
ABSTRAK
ABSTRAK. Penelitian ini dilakukan dengan tujuan memanfaatkan fitoplankton Nannochloropsis salina sebagai
biosorben untuk polutan ion logam Pb dan Cu di perairan. Pada penelitian ini pemaparan ion logam Pb dan Cu dengan variasi konsentrasi masing-masing 10, 30, dan 50 ppm dilakukan di awal masa pertumbuhan N. salina dalam Medium Conwy pada salinitas 30‰, aerasi dan pencahayaan kontinyu, serta suhu ruangan 20 °C. Konsentrasi ion logam ditentukan dengan menggunakan spektrofotometer serapan atom (SSA). Pertumbuhan optimum N. salina sebagai kontrol diperoleh pada hari ke-8, sementara pertumbuhan N. salina setelah pemaparan ion logam menunjukkan populasi yang sangat rendah di awal kontak. Pola pertumbuhan meningkat seiring dengan bertambahnya waktu kontak N. salina dengan ion logam. Efisiensi penjerapan ion logam Pb dan Cu oleh N. salina berbanding terbalik dengan bertambahnya waktu kontak.
Kata kunci: ion Cu, ion Pb, bioremoval, Nannochloropsis salina, SSA.
ABSTRACT. This research was conducted with the aim of utilizing phytoplankton Nannochloropsis salina as
biosorbent for Pb and Cu metal ions pollutant in water. In this study, exposure to Pb and Cu metal ions with various concentrations of each of 10, 30, and 50 ppm conducted at the beginning of the growth of N. salina in Conwy Medium at 30‰ salinity, aeration and continuous illumination, as well as room temperature 20 °C. Metals ion concentration was determined by atomic absorption spectrophotometer (AAS). Optimum growth of
N. salina as a control obtained on day 8th, while the growth of N. salina after exposure the metal ions showed very low population in the initial contact. Trend of growth increases with contact time of N. salina with metal ions. The metals ion adsorption efficiency of Pb and Cu by N. salina inversely with increasing contact time.
Keywords: AAS,bioremoval,Cu ion, Nannochloropsis salina, Pb ion
PENDAHULUAN
Kegiatan industri, pertambangan,
pembakaran bahan bakar serta kegiatan domestik lainnya telah meningkatkan kandungan logam berat di perairan laut. Adanya logam berat yang terdistribusi di perairan laut akan meningkatkan
kandungan logam yang terakumulasi pada
organisme yang hidup di perairan. Logam berat umumnya bersifat racun, korosif, serta sulit
Penulis koresponden.
Alamat E-mail:yusafirhala@yahoo.co.in
terdegradasi di alam. Logam berat juga dapat terakumulasi pada organisme dan mengakibatkan timbulnya efek negatif [1]. Akan tetapi beberapa logam beratseperti V, Cr, Mn, Fe, Co, Ni, Cu, Zn dan Mo,termasuk esensial bagi tubuhpada kosentrasi yang sangat kecil [2].
Logam berat yang sering ditemukan di lingkungan perairan antara lain adalah Pb, Cr, Cd, Mn, Co, Fe, Zn, dan Ni. Bila konsentrasi logam-logam berat tersebut melebihi ambang batas yang diperbolehkan, maka dapat menimbulkan bahaya karena tingkat toksisitasnya akan mengganggu organisme yang ada diperairan maupun manusia
84
sebagai konsumen, baik langsung maupun tidak langsung [3].
Masalah pencemaran logam berat,
khususnya di perairan, dapat diatasi melalui beberapa teknik pengolahan limbah.Salah satu
diantaranya menggunakan teknik bioremoval
denganmemanfaatkan fitoplankton. Keberadaan
fitoplankton dapat dijadikan sebagai bioindikator terhadap perubahan lingkungan perairan yang disebabkan oleh ketidakseimbangan ekosistem akibat pencemaran [4].
Penelitian yang telah dilakukan oleh Astri [5] menunjukkan bahwaN. salinamampu menjerap ion Pb hingga konsentrasi 40 ppm, dan berdampak pada penurunan jumlah populasi fitoplankton bersangkutan. Hal ini mengindikasikan bahwa ion
Pbdapat menghambat pertumbuhan N.salina,
bahkan dapat menyebabkan kematian fitoplankton tersebut [6]. Hal ini terjadi karena pada umumnya fitoplankton mempunyai kemampuan menjerap dan mengakumulasi logam berat dari lingkungannya [7]. Dibandingkan dengan metode fisiko-kimia, pemanfaatan fitoplankton sebagai biosorben dalam penanganan kontaminasi logam berat di perairan merupakan alternatif dengan resiko yang relatif lebih kecil, lebih murah, dan biomassanya dapat dimanfaatkan untuk berbagai keperluan [8]. N.
salina, merupakan salah satu mikroalga yang
berfungsi sebagai produsen primer dalam rantai makanan di perairan laut dengan waktu regenerasi yang relatif cepat, sehingga interaksinya dengan bahan pencemar di laut dapat menyebabkan perubahan perilaku kehidupan seperti perubahan populasi, kecepatan pertumbuhan, aspek biokimia dan morfologinya [3].
Berkaitan dengan uraian di atas telah dilakukan penelitian tentang kajian dampak medium tercemar logam Pb dan Cu terhadap pertumbuhan N.
salina. Penelitian ini mengacu kepada penelitian
yang telah dilakukan oleh Tambung dkk [6] dimana pemaparan logam berat pada kultur N. salina dilakukan setelah pertumbuhan maksimum dicapai. Dengan mempertimbangkan aspek pemanfaatan N.
salina sebagai biosorben bagi logam berat Pb dan
Cu, maka dalam penelitian ini N.
salinaditumbuhkanlangsungpada medium yang
telah terkontaminasi logam beratPb dan Cu sejak awal. Penelitian ini diharapkan dapat menjadi salah satu alternatif solusi atas pencemaran logam berat di perairan laut, sehingga kelak dapat dijadikan dasar bagi pemanfaatan N. salina sebagai biosorben sekaligus sebagai alternatif solusi atas kasus pencemaran logam berat di perairan.
BAHAN DAN METODA
Penelitian ini dilaksanakan pada Bulan Agustus sampai November 2012 di Laboratorium Kimia Analitik dan Laboratorium Kimia Anorganik Fakultas MIPA Universitas Hasanuddin, serta Laboratarium Balai Penelitian dan Pengembangan Budidaya Air Payau (BPPBAP) Maros.
Bahan Penelitian
Bahan-bahan yang digunakan dalam
penelitian ini adalah larutan Medium Conwy [9], air laut steril, dan biakan murni N. Salina.Semua bahan
ini diperoleh dari BPPBAP Maros. Larutan HNO3
p.a., aquabides, alumunium foil, kertas saring
Whatman 42.Larutan induk Pb2+ 1000 ppm, yang
dibuat dengan cara menimbang1,5984 g kristal
Pb(NO3)2dan dilarutkan denganHNO3 p.a kemudian
diencerkan dengan aquabides dalam labu ukur 1000
mL.Larutan induk Cu2+ 1000 ppm, dibuat dengan
cara menimbang 3,8023 g kristal Cu(NO3)2.3H2O
dilarutkan dengan HNO3 p.a kemudian diencerkan
dengan aquabides dalam labu ukur 1000 mL.
Alat Penelitian
Peralatan yang digunakan dalam penelitian ini adalah alat gelas yang umum digunakan di laboratorium, aerator merk Amara, alat pencacah hemositometer merk Marienfeld LOT-No 4551,
hand counter, mikroskop Nikon SE dengan
perbesaran sampai dengan 125 kali, dan sentrifus. Peralatan ini milik Laboratorium Kimia Anorganik FMIPA Unhas.Sedangkan SSA Buck Scientific model 205 VGP, yang digunakan untuk penentuan
konsentrasi logam,milik Laboratorium Kimia
Analitik FMIPA Unhas.
Prosedur Kerja
Penelitian ini di lakukan 3 tahap yaitu: (1) Penentuan pertumbuhan optimum N.salinasebagai kontrol, (2) Pemaparan ion Pb dan Cu pada biakan
N. salina dan pengamatan pertumbuhan populasi N. salina, dan (3) Pengukuran konsentrasi logam yang
terjerap dengan menggunakan SSA.
Pertumbuhan optimum N.salina
N. salina ditumbuhkan dalamMedium
Conwy dan air laut steril, dengan kondisi: salinitas medium 30‰, pencahayaan yang kontinyu, aerasi dan suhu ruangan 20 °C.Pengamatan pertumbuhan
N. salina dilakukan menggunakan hemositometer
dan mikroskop,dengan cara menghitung jumlah sel
85
Pemaparan ion Pb dan ion Cu dan perhitungan populasi N. salina
Sebanyak 3 buah erlenmeyer 500 mL disiapkan. Air laut steril dimasukkan ke dalam masing-masing erlenmeyer tersebut, kemudian ditambahkan 1 mL larutan Medium Conwy, 1 tetes vitamin B1 dan B12, serta 2 mL biakan murni N.
salina.Selanjutnya dipaparkan ion Pb dengan
konsentrasi masing-masing Pb 10 ppm, 30 ppm, dan 50 ppm.Volume medium dicukupkan dengan air laut steril hingga 500 mL. Larutan diaduk perlahan
dan dihubungkan dengan aerator, kemudian
erlenmeyer ditutup dengan alumunium foil lalu didiamkan dalam ruangan bersuhu tetap dan cahaya cukup. Pengamatan pertumbuhan N. salinadimulai pada hari setelah ion logam Pb dipaparkan, dan
selanjutnya pengamatan dilakukan setiap
hari.Perlakuan yang sama juga dilakukan terhadap pemaparan ion logam Cu dankontrol, yakni biakan
N. salina tanpa penambahan ion logam. Selanjutnya
pada masing-masing erlenmeyer, filtrat dipipet dan konsentrasi ion Pb dan Cu dalam filtrat ditentukan dengan menggunakan SSA.
Pengukurankonsentrasi logam dengan SSA Pembuatan larutan standar
Untuk membuat larutan 100 ppm,sebanyak 1 mL larutan standar logam 1000 ppm dipipet kemudian dimasukkan ke dalam labu ukur 100 mL, selanjutnya ditambahkan aquabides sampai tanda batas. Dibuat seri larutan standar dengan konsentrasi ion Pb sebesar 1; 2,5; 5; 10; 20; 30 dan 50 ppm.Hal yang sama dilakukan untuk seri larutan standar Cu dengan konsentrasi 0,5; 1; 2; 3; 5; dan 10 ppm.
Efisiensi penjerapan ion Pb dan Cu
Efisiensi penjerapan ion Pbdan Cuoleh N.
salina dihitung berdasarkan perbandingan
konsentrasi ion Pb dan Cu yang terjerap dengan
konsentrasi logam mula-mula.Pengukuran
konsentrasi ion logam dilakukan dengan SSA pada filtrat medium setelah pemaparan. Konsentrasi ion logam yang terjerap oleh N. salina dihitung
menggunakan persamaan (1), di mana Cs adalah
konsentrasi ion logam yang terjerap oleh
fitoplankton, (Co) adalah konsentrasi awal, dan (Cf)
adalah konsentrasi ion logam dalam filtrat medium.
Untuk mendapatkan nilai efisiensi penjerapan (Ef)
digunakan persamaan (2).Dengan membandingkan
nilai Cs dan Co diperoleh nilai Ef.
Cs = C0 – Cf ... (1)
………(2)
HASIL DAN DISKUSI Profil pertumbuhan N. salina
Pertumbuhan fitoplanktonN. salina secara alami berlangsung dari populasi rendah, lalu mencapai pertumbuhan optimum, dan akhirnya mengalami penurunan jumlah populasi. Setelah pemaparan ion logam Pb dan Cu dengan variasi konsentrasi masing-masing 10, 30, dan 50 ppm, yang telah dilakukan pada awal pertumbuhan
dengan kepadatan awal 30x104sel/mL, pengamatan
terhadap laju pertumbuhan N. salina dilakukan setiap 24 jam pada kondisi salinitas 30 ‰, pencahayaan yang kontinyu, aerasi dan suhu ruangan 20 °C.
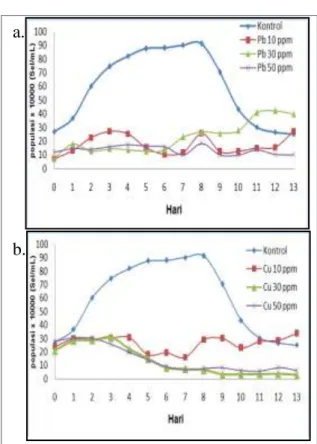
Gambar 1 menunjukkan laju pertumbuhan N.
salina setiap 24 jam. Pertumbuhan kontrol,
menunjukkan kenaikan populasi yang teratur hingga pada hari ke-8 diperoleh pertumbuhan sebesar
91,25x104 sel/mL,akan tetapi pada hari ke-9 mulai
terjadi penurunan populasi, yakni 70,25x104 sel/mL.
Karena itu hari ke-8 disebut pertumbuhan optimum.
Gambar 1. Pertumbuhan fitoplankton N. salina.a) setelah pemaparan ion Pb danb)setelah pemaparan ion Cu
Pertumbuhan N. salina berlangsung dengan pembelahan sel sehingga jumlah populasinya semakin bertambah dan setelah pertumbuhan
optimum dicapai jumlah populasinya pun
mengalami penurunan dalam medium. Hal ini terjadi karena ketersediaan nutrien dalam medium
a.
86
yang semakin berkurang seiring dengan
meningkatnya jumlah fitoplankton yang hidup dan mengkonsumsi nutrien tersebut. Jumlah populasi akan semakin menurun dengan adanya bahan organik dan fitoplankton yang mati,lalu mengendap ke dasar medium. Bahan-bahan tersebut berperan sebagai kompetitor baru bagi fitoplankton yang masih hidup dalam mengkonsumsi oksigen terlarut dalam lingkungan media pertumbuhan. Oleh karena
itu pertumbuhan fitoplankton akan semakin
terhambat [5].
Gambar 1 juga menunjukkan pertumbuhan
N. salinayang acak setelah pemaparan ion logam,
jika dibandingkan dengan kontrol. Hal ini terjadi karena ion-ion logam merupakan material toksik
yang sudah tentu menghambat pertumbuhanN.
salina[10].Pemaparan ion logam Pb dengan
konsentrasi 10, 30,dan50 ppm menyebabkan penurunan pertumbuhan N.salinadi awalproses yang signifikan dibanding kontrol. Medium kultivasi
mengalami kontaminasi logam Pb yang
toksiksehingga menghambat aktivitas pembelahan sel N. salina.Hal ini menunjukkan jumlah populasi yang jauh lebih kecil dibandingkan dengan kontrol. Akan tetapi pada pemaparan logam Pb dengan
konsentrasi 10 ppm, terjadikecenderungan
meningkatnya populasi sampai hari ke-5 dengan
jumlah populasi 15,25x104 sel/mL. Pemaparan ion
Pb dengan konsentrasi 30 dan 50 ppm, juga meningkatkan jumlah populasi sampai hari ke-3 dan hari ke-4 dengan jumlah populasi berturut-turut
14,25x104 sel/mL dan 17,0x104 sel/mL. Karena
pada akhir proses pertumbuhan,N. salinayang sudah mati (biomassa) juga mampu menjerap logam. Di samping itu pembelahan sel baru terjadi, sehingga populasiN. salina bertambah.
Setelah pemaparan ion Cu dengan konsentrasi berturut-turut 10, 30, dan 50 ppm, pertumbuhan awal dari N. salina hampir sama dengan pertumbuhan kontrol. Hal ini terjadi karena setelah pemaparan ion Cu jumlah populasi dapat bertahan karena Cu merupakan logam yang esensial dan
dibutuhkan dalam sel fitoplankton [11].
Pertumbuhan N. salina mengalami penurunan berturut-turut pada hari ke-5, hari ke-4 dan hari ke-3
dengan jumlah populasi 18,00x104 sel/mL; 22x104
sel/mL; dan 25,75x104 sel/mL.
Profil Penjerapan Ion Logam
Berdasarkan persamaan (2), hasil
perhitungan efisiensi penjerapan masing-masing ion logam dapat dilihat pada Gambar 2.Ion logam Pb mengalami penjerapan yang relatif tinggi oleh N.
salina diawal masa pertumbuhan, terutama ion Pb
dengan konsentrasi 10 ppm, yaitu sebesar
49,85%.Jika dibandingkan dengan pertumbuhan N.
salina setelah pemaparan logam Pb dengan
konsentrasi 30 dan 50 ppm,yang juga mengalami penurunan jumlah populasi yang signifikan, denganefisiensi penjerapan yang sedikit lebih rendah dibanding dengan konsentrasi Pb 10 ppm. Hal ini mengindikasikan bahwa kehadiran ion logam dapat menghambat pertumbuhan N.salina.Di samping itu biomassa N.salina masih dapat menjerap ion logam.
Gambar 2. a) Koefisien penjerapan ion Pb, b) Koefisien penjerapan ion Cu
Setelah pemaparan ion logam Cu dengan konsentrasi 10, 30, dan 50 ppm, efisiensi penjerapan ion logam oleh N. salina diawal pertumbuhan cukup tinggi yaitu berturut-turut 49,85%, 13,32%, dan 7,73%. Jika dibandingkan dengan ion Pb, jumlah populasi N. salina setelah pemaparan ion logam Cu relatif lebih tinggi. Hal ini disebabkan karena ion Cu termasuk dalam kelompok ion logam yang esensial, tetapi jika konsentrasinya tinggi tetap berpotensi menjadi toksik.Hal ini dapat dilihat pada efisiensi penjerapan ion logam Cu oleh N. salina pada konsentrasi 30 dan 50 ppm yang menunjukkan populasi yang relatif lebih rendah.
a.
87
Semakin tinggi konsentrasi ion logam dan semakin lama waktu kontak,efisiensi penjerapan ion logam Pb dan Cu oleh N. salina semakin rendah. Hal ini disebabkan oleh bertambahnya kandungan bahan organik mati dalam medium sebagai akibat semakin banyaknya N. salina yang
mati.Kondisi ini diperparah dengan
berkurangnyakandungan oksigen terlarut dalam
medium, yang berpotensi menyebabkan
pertumbuhan fitoplankton menjadi tidak terkontrol (blooming).
KESIMPULAN
Berdasarkan hasil penelitian yang telah dilakukan, dapat disimpulkan beberapa hal sebagai berikut:
1. Adanya ion logam Pb dan Cu di dalam medium kultivasi menghambat pertumbuhan N. salina. 2. Trend pertubuhanN. salina dalam medium yang
tercemar oleh ion logam Pb dan Cu meningkat seiring dengan bertambahnya waktu kontak, walau diawal proses mengalami penurunan pertimbuhan yang signifikan dibandingkan dengan kontrol.
3. Efisiensi penjerapan ion logam Pb dan Cu oleh
N. salinaberbanding terbalik dengan
bertambahnya waktu kontak.
UCAPAN TERIMA KASIH
Terima kasih disampaikan kepada
Direktorat Jendral Pendidikan Tinggi Kemdikbud Republik Indonesia, melalui Program Hibah Mandiri tahun 2012, yang telah membantu terlaksananya penelitian ini.
REFERENSI
1. Siregar, T. dan J.T. Murtni. 2005. Kandungan logam berat pada beberapa lokasi perairan
Indonesia pada tahun 2001 sampai dengan 2005,
Squalen 3 (1).
2. Housecroft, C.E., and A.G. Sharpe. 2005.
Inorganic Chemistry, 2nd.Ed., Pearson
Education, England, 830 pp.
3. Widowati, W., A. Sastiono., dan R.J.
Rumampuk. 2008. Efek Toksik Logam, ANDI Yogyakarta, Yogyakarta.
4. Asrib, F., 2010. Fitosorpsi bi-logam Pb(II) dan Zn(II) oleh Chaetoceros calcitrans dalam Medium Conwy, Skripsi tdak dipublikasikan,
Jurusan Kimia, FMIPA, Universitas
Hasanuddin, Makassar.
5. Astri, 2008. Pemanfaatan fitoplankton
Nannochloropsis salinasebagai penjerap logam
berat Pb, Skripsi tidak dipublikasikan, Jurusan
Kimia, FMIPA, Universitas Hasanuddin,
Makassar.
6. Tambung, A., A. Patabang, Astri, Y. Hala, dan P. Taba. 2007. Kajian interaksi ion logam Pb,
Cd, dan Zn dengan fitoplankton
Nannochloropsis salina, Marina Chimica Acta,
Edisi Khusus Seminar Nasional FK3TI, Oktober 2007: 42-46.
7. Hala, Y., P. Taba, dan M. Mariani. 2010. Fitosorpsi bi-logam Cd(II) dan Cu(II) oleh
Chaetoceros Calcitrans dalam Medium Conwy, Marina Chimica Acta 11(1): 30-35.
8. Arifin dan I. Raya. 1997. Studi interaksi antara
kadmium dan Tetracelmis di lingkungan perairan laut, Laporan Hasil penelitian FMIPA
Universitas Hasanuddin, Makassar.
9. Fogg, G. E., 1985. Algae culture and
phytoplankton ecology, 2nd Ed, The University of Wisconsin Press.
10. Gonzalez-Davila, M., 1995. The role of phytoplankton cells on the control of heavy metal concentration in seawater, Marine
Chemistry 48: 215-236.
11. Cobbet, C., S., 2000. Phytochelatin biosynthesis and function in heavy metal detoxification,
Current Opinions in Plant Biology 30(4):