ANALISIS AKUMULASI LOGAM BERAT TIMBAL (Pb) DAN KADMIUM (Cd)
PADA LAMUN Enhalus acoroides SEBAGAI AGEN FITOREMEDIASI DI
PANTAI PACIRAN, LAMONGAN
Riska Ayuk Novia Sugiyanto*, Defri Yona, Rarasrum Dyah Kasitowati
Fakultas Perikanan dan Ilmu Kelautan Universitas Brawijaya, Malang Jl. Veteran, 65145 Malang, Telp/Fax. 0341-557837
*Email : riskaayukns@gmail.com
Abstrak - Enhalus acoroides merupakan spesies lamun yang memiliki potensi sebagai agen fitoremediasi terhadap logam berat di perairan. Effisiensi Enhalus acoroides untuk fitoremediasi salah satunya dapat dilakukan dengan menentukan besarnya akumulasi logam berat Pb dan Cd dalam biomassa sampel lamun. Penelitian ini dilakukan pada bulan Februari 2016 untuk mengetahui konsentrasi logam berat Pb dan Cd pada akar dan daun lamun serta kemampuan dari Enhalus acoroides dalam mengakumulasi dan mentranslokasikan logam berat sehingga dapat digunakan sebagai agen fitoremediasi. Metode sampling logam berat dilakukan pada empat titik di area yang terdapat vegetasi Enhalus acoroides di Pantai Paciran, Lamongan. Hasil penelitian menunjukkan konsentrasi logam berat Pb dan Cd pada daun (0,2214-0,4201 ppm dan 0,0567-0,0794 ppm) lebih tinggi dari pada konsentrasinya di akar (0,067-0,4224 ppm dan 0,05-0,0684 ppm). Nilai BCF (bioakumulasi faktor) dan TF(translokasi faktor) lamun terhadap logam berat Pb dan Cd termasuk ke dalam kategori akumulator(>1) yang dapat mentranslokasikan logam berat secara optimal dari sedimen dan kolom air menuju akar ke daun lamun (mekanisme fitoekstraksi).Hasil perhitungan FTD (Fitoremediasi) pada akar dan daun lamun Enhalus acoroides terhadap logam berat Cd (3,00 dan 4,11) lebih tinggi dari pada FTD akar dan daun lamun terhadap logam berat Pb(0,08 dan 0,48). Sehingga, diperoleh kesimpulan bahwa lamun Enhalus acoroides dapat meremediasi lebih banyak logam berat Cd dari pada logam berat Pb di perairan melalui proses fitoekstraksi.
Kata Kunci: Enhalus acoroides,Logam berat, Bioakumulasi, Fitoremediasi, Paciran
Abstract - Enhalus acoroides is a seagrass species that has the potential as an agent phytoremediation of heavy metals in the water. The efficiency Enhalus acoroides for phytoremediation one of which can be done by determining the magnitude of the accumulation of heavy metals Pb and Cd in biomass of samplesseagrass. This study was conducted in February 2016 to determine the concentration of heavy metals Pb and Cd in the roots and leaves of seagrass as well as the ability of Enhalus acoroides toaccumulationand translocated of heavy metals that can be used as phytoremediation agents.The method of sampling heavy metal conducted at four points in the area that there are vegetation of Enhalus acoroides in the Paciran Beach, Lamongan. The results showed concentrations of heavy metals Pb and Cd in the leaves (0,2214 – 0,4201 ppm and 0,0567 – 0,0794 ppm) is higher than the concentration in the root (0,067 – 0,4224 ppm and 0,05 - 0,0684 ppm). BCF values (bioaccumulation factor) and TF (translocation factor) seagrass to heavy metals Pb and Cd included the category of accumulator (> 1) may be translocated heavy metals optimally from the sediment and the water column towards the roots to the leaves of seagrass (mechanism phytoextraction). The calculation result of FTD (Phytoremediation) on the roots and leaves of seagrass Enhalus acoroides to heavy metals Cd (3.00 and 4.11) higher than FTD in the roots and leaves of seagrass to heavy metals Pb (0.08 and 0.48). Thus, in conclusion that seagrass Enhalus acoroides more can remediate heavy metals Cd than the heavy metals Pb in waters through phytoextraction process.
I. PENDAHULUAN
Pantai Paciran merupakan salah satu wilayah pesisir yang memiliki potensi perikanan di Jawa Timur. Pantai Paciran terletak diantara 2 pelabuhan perikanan yaitu Pelabuhan Brondong dan Pelabuhan Pasar Kranji yang merupakan salah satu tempat pelelangan ikan (TPI) di Kabupaten Lamongan. Letak pantai yang strategis menyebabkan pengaruh tingginya aktivitas yang dapat mempengaruhi kondisi perairan seperti pengecatan kapal, pembuangan limbah kapal, bongkar muat kapal dan ditambah pemasukan limbah domestik serta limbah yang terbawa oleh aliran sungai. Aktivitas tersebut merupakan sumber pencemar salah satunya yaitu pencemaran logam berat di perairan. Jenis logam berat yang paling banyak berasal dari wilayah dekat pelabuhan adalah timbal (Pb) dan kadmium (Cd)[1]. Dampak pencemaran logam berat Pb dan Cd salah satu contohnya yaitu kematian massal ikan di Teluk Jakarta dengan konsentrasi logam berat Pb dan Cd masing-masing yaitu 0,55 dan 0,1 ppm [3]. Selain itu, pada
penelitiannya di Tanjung Emas, Semarang
menunjukkan hasil bahwa perairan perairan tersebut telah tercemar logam berat Pb dan Cd dengan nilai masing-masing 2,88-7,81 ppm dan 1,63-2,96 ppm yang
mengakibatkan penurunan hasil tangkapan dan
budidaya ikan [2].
Lamun merupakan tumbuhan berbunga yang mampu hidup di lingkungan laut. Habitat lamun di perairan dangkal menyebabkan ekosistem ini di pengaruhi oleh aktivitas yang ada di pesisir. Enhalus acoroides
merupakan jenis lamun yang memiliki kemampuan daya serap terhadap konsentrasi logam berat di perairan yang banyak ditemukan di Pantai Paciran.Pada
penelitiandi Waai dan Galala Pulau Ambon
menunjukkanadanya kemampuan akumulasi lamun
Enhalus acoroides terhadap logam berat Pb dan Cd pada bagian akar dan daun lamun[3].Berdasarkan hasil penelitian tersebut yang mendasari adanya penelitian
mengenai daya serap lamun Enhalus acoroides
terhadap logam berat khususnya Pb dan Cd yang berpotensi sebagai agen fitoremidiasi, dengan wilayah
yang berbeda untuk upaya pemantauan dan
pengendalian pencemaran laut di Pantai Paciran, Lamongan.
II.METODE PENELITIAN
2.1 Waktu dan Tempat Penelitian
Pengambilan sampel dilakukan pada tanggal 10 Februari 2016 di Pantai Paciran, Lamongan. Titik pengambilan sampel ditentukan dengan menggunakan
metode random sampling yaitu dengan cara
mengambil sampel logam berat secara acak pada area yang terdapat spesies lamunnya (Gambar 1).
Gambar 1. Peta Lokasi Pengambilan Sampel
Sampel yang diambil meliputi sampel air, sedimen, akar
dan daun lamun Enhalus acoroides, dan sampel
parameter dasar fisika dan kimia yang meliputi suhu, DO, salinitas dan pH. Titik koordinat pengambilan sampel dapat dilihat pada Tabel 1. Analisa sampel logam berat di laksanakan pada tanggal 11 Februari 2016 sampai dengan 22 Februari 2016 di laboratorium jurusan kimia, Fakultas Matematikan dan Ilmu Pengetahuan Alam, Universitas Negeri Malang.
Tabel 1. Koordinat pengambilan sampel tiap stasiun Titik Koordinat
1 S 06.87401O - E 112.37343O
2 S 6.872725O- E 112.373351O
3 S 06.87507O- E 112.38057O
4 S 06.87434O- E 112.38015O
2.2 Prosedur Pengambilan Data Lapang 2.2.1 Kualitas Air
Parameter kualitas air yang diukur konsentrasinya adalah suhu, pH, DO dan salinitas. Pengukuran suhu air laut dilakukan dengan menggunakan thermometer digital. Pengukuran pH air laut dilakukan dengan
menggunakan pH meter. Pengukuran salinitas
dilakukan dengan menggunakan salinometer.
Pengukuran DO dilakukan dengan menggunakan DO meter.
2.2.2 Sampel Air
Sampel air laut diambil dengan menggunakan botol polyethilen 500 ml secara langsung sesuai dengan jenis alat pengambilan sampel. Kemudian sampel air laut ditambahkan HNO3 pekat sebanyak 2 ml atau hingga pH sampel mencapai 2. Setelah itu, sampel air laut
dimasukkan ke dalam cool box untuk dianalisa di laboratorium.
2.2.3 Sampel Sedimen
Sampel sedimen diambil pada substrat padang lamun.
Sedimen diambil menggunakan PVC Core 30x5 cm
atau sebanyak ±750 mg, kemudian dimasukkan ke dalam plastik dan disimpan ke dalam cool box[4]. 2.2.4 Sampel Lamun
Sampel lamun dikumpulkan pada saat surut dimana sampel akar lamun diambil dari substrat dan sampel daun diambil yang berukuran besar dan tua dengan panjang ±20-25 cm atau ± 0,5 g[4]. Kemudian sampel lamun dicuci bersih dengan menggunakan air untuk menghilangkan sedimen dan fauna yang menempel dan dipisahkan antara bagian akar dan daun. Sampel akar dan daun lamun yang telah dibersihkan disimpan dalam plastik dan di masukkan ke dalam cool box untuk di analisa di laboratorium.
2.3 Analisa Kandungan Logam Berat 2.3.1 Analisa Logam Berat di Air
Prosedur analisa logam berat Pb dan Cd dilakukan dengan memasukkan sampel air laut ke dalam beaker glass 100 ml dan ditambahkan HNO3 pekat sebanyak 5 ml kemudian sampel diuji kadar logam beratnya
menggunakan Atomic Absorbtion Spectrophotometry
(AAS).
2.3.2 Analisa Logam Berat di Sedimen
Sampel sedimen dibersihkan dengan
menggunakanaquades dan kemudian dikeringkan pada suhu 105oC dengan menggunakan oven. Analisa sampel dilakukan setelah pengeringan, dimana sampel diambil sebanyak 0,5 -1 g dan dilarutkan dengan menggunakan
HNO3 2M hingga volumenya mencapai 50 ml.
Kemudian sampel diuji menggunakan AAS.
2.3.3 Analisa Logam Berat pada Akar dan Daun Lamun
Enhalus Acoroides
Lamun yang telah dicuci kemudian dikeringkan pada
suhu 105oC dengan menggunakan oven. Sampel lamun
sebanyak 1-0,5 g dilarutkan dengan menggunakan HNO32M dan di filter menggunakan kertas saring. Kemudian sampel lamun di campur dengan aquades hingga volumenya mencapai 50 ml. Konsentrasi logam berat pada lamun Enhalus acoroides baik akar maupun daun dianalisa menggunakan AAS.
2.4 Analisa Data
2.4.1 BCF (Bioaccumulation Concetration Factor)
Analisa BCF dilakukan untuk mengetahui tingkat akumulasi logam berat Pb dan Cd pada akar dan daun lamun Enhalus acoroides. Rumus perhitungan BCF yang digunakan oleh idalam rujukan [2]sebagai berikut :
BCF =
(1)
dengan kategori tanaman dibagi menjadi 3 yaitu : Akumulator : apabila nilai BCF >1
Excluder : apabila nilai BCF < 1
Indikator : apabila nilai BCF mendekati 1
2.4.2 TF ( Translocation Factor)
Analisa TF digunakan untuk menghitung proses translokasi logam berat Pb dan Cd dari akar ke daun. Perhitungan TF yang digunakan oleh Baker (1981)
dalamrujukan[2]yaitu : TF =
(2)
Nilai TF menurut Baker (1981) dalamrujukan [5]memiliki kategori yaitu:
TF >1 : Mekanisme fitoekstraksi
TF<1 : Mekanisme fitostabilisasi
2.4.3 FTD ( Fitoremediasi)
Fitoremediasi merupakan selisih antara BCF dengan TF. Nilai FTD diperoleh dengan mengurangi nilai BCF dengan nilai TF.
2.4.4 Analisa Statistik
Analisa statistik dilakukan dengan menggunakan metode uji Principal Component Analysis (PCA).
Analisis komponen utama atau PCA digunakan untuk mengetahui pengaruh kualitas air yang terdiri dari suhu, salinitas, pH dan DO terhadap logam berat Pb dan Cd pada air, sedimen, akar dan daun lamun. Analisa PCA dilakukan dengan menggunakan software XLStat
III. HASIL dan PEMBAHASAN
3.1 Kondisi Kualitas Air di Pantai Paciran Berdasarkan Parameter Fisika dan Kimia
Suhu di Pantai Paciran pada Tabel 2 memiliki kisiaran 28,6-27,6 dengan rata-rata 28,3±0,46oC. Suhu di Pantai Paciran pada umunya masih berada pada kategori suhu optimal untuk pertumbuhan lamun. Suhu optimal untuk pertumbuhan lamun berada pada kisaran 24-35 oC[6]. Pengaruh suhu terhadap ekosistem lamun yaitu
mempengaruhi proses-proses fisiologi seperti
fotosintesis, laju pertumbuhan dan reproduksi.
Pantai Paciran memiliki nilai salinitas yang homogen di tiap titik yaitu 31±0,0 ppt (Tabel 2). Lamun pada dasarnya mampu tumbuh dengan baik pada salinitas 35 ppt. Pada salinitas 40-45 ppt lamun akan mengalami gangguan fotosintesis dan pada salinitas <10 ppt (hiposalin) atau >45ppt (hipersalin) lamun akan mengalami stress dan menyebabkan kematian[7].
Kisaran nilai pH di Pantai Paciran pada yaitu 4,8-5,7 dengan rata-rata 5,3±0,45 (Tabel 2). pH air laut yang normal memiliki nilai 7 karena pada kisaran pH tersebut ion bikarbonat yang dibutuhkan oleh lamun untuk fotosintesis dalam keadaan yang berlimpah[6]. Rata-rata nilai pH yang cenderung asam di Pantai Paciran disebabkan karena pada waktu pengukuran diduga terjadi pemasukan senyawa organik maupun anorganik ke dalam Perairan[8].
Tabel 2. Data kualitas (suhu, salinitas, pH, dan DO) air di Pantai Paciran
Hasil pengukuran DO di Pantai Paciran pada Tabel 2 memiliki kisaran 5,8-7,76 dengan rata-rata DO
6,94±0,96 mg/l. Menurut penelitian pada rujukan [9]rata-rata DO pada ekosistem lamun di perairan Kabupaten Donggala adalah 7,31 mg/l. Tinggi rendahnya nilai DO kemungkinan disebabkan oleh penggunaan mikroorganisme dalam melakukan proses perombakan bahan-bahan organik.
3.2 Konsentrasi Logam Berat Pb dan Cd di Air danSedimen
Kisaran konsentrasi logam berat Pb di air 0,0352-0,2759 ppm dengan rata-rata 0,1490±0,099 ppm sedangkan kisaran di sedimen 0,1079-0,2611 ppm dengan rata-rata 0,1774±0,070 ppm(Gambar 2).
Gambar 2. Konsentrasi logam berat Pb di air dan sedimen
Kisaran konsentrasi logam berat Cd di air yaitu 0,0091-0,0504 ppm dengan rata-rata 0,0279±0,0170 ppm dan kisaran di sedimen 0,0089-0,0224 ppm dengan rata-rata 0,0155±0,0062 ppm (Gambar 3)
Gambar 3. Konsentrasi logam berat Cd di air dan sedimen Pantai Paciran
Konsentrasi logam berat Pb di air dan sedimen pada Gambar 2menunjukkan bahwa konsentrasi Pb lebih tinggi di sedimen dari pada di air. Pada dasarnya logam berat Pb memiliki karakteristik yang tidak mudah larut dan cenderung mengendap di sedimen sehingga konsentrasi Pb di sedimen lebih tinggi.Pada dasarnya tingkat kelarutan logam berat Pb di air cukup rendah sehingga konsentrasinya di air lebih rendah daripada di sedimen. Namun, hal ini bertentangan dengan konsentrasi logam berat Cd pada Gambar 3 dimana konsentrasinya lebih tinggi di air dari pada di sedimen. Faktor pH di Pantai Paciran yang cenderung asam yaitu 5,3 menyebabkan logam berat Cd lebih mudah larut dan terakumulasi ke dalam tubuh organisme. Pada pH 5 logam berat Cd mampu terakumulasi secara optimum ke dalam tubuh organisme hingga mencapai 10 mg/l sedangkan logam berat Pb cenderung mengendap dan berikatan dengan partikel tersuspensi ke dalam sedimen[10].
3.3 Konsentrasi Logam Berat Pb dan Cd pada Akar dan Daun Lamun
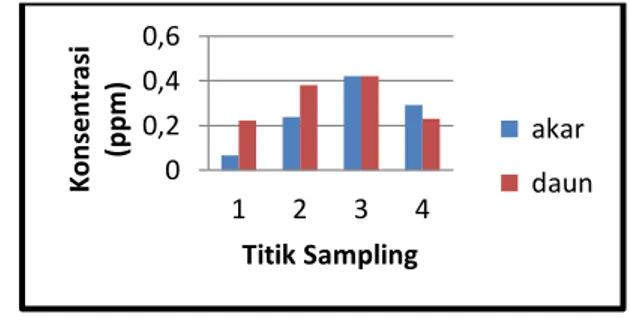
Hasil analisa logam berat Pb pada akar dan daun lamun di Pantai Paciran disajikan pada Gambar 4. Kisaran konsentrasi logam berat Pb pada akar 0,067-0,4224 ppm dengan rata-rata 0,2546 ±0,147 ppm dan pada
daun 0,2214-0,4201 ppm dengan rata-rata
0,3131±0,102 ppm..
Gambar 4. Konsentrasi logam berat Pb pada akar dan daun lamun Enhalus acoroides di Pantai
Paciran 0 0,1 0,2 0,3 1 2 3 4 K on sent ra si (p p m ) Titik Sampling air Sedimen 0 0,02 0,04 0,06 1 2 3 4 K on sent ra si ( p p m ) Titik Sampling air Sedimen 0 0,2 0,4 0,6 1 2 3 4 K on sent ra si (pp m ) Titik Sampling akar daun Parameter Max Min
Rata-rata Stdev Suhu 28,6 27,6 28,3 0,46 Salinitas 31 31 31 0,0 Ph 5,67 4,8 5,27 0,45 DO 7,76 5,8 6,94 0,96
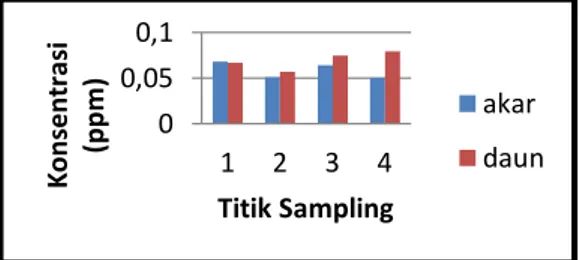
Konsentrasi logam berat Cd pada akar 0,05-0,0684 dengan rata-rata 0,0584±0,0092 ppm dan di daun ppm 0,0567-0,0794 ppm dengan rata-rata 0,0694±0,0099 ppm (Gambar 5).
Gambar 5. Konsentrasi logam berat Cd pada akar dan daun lamun Enhalus acorides di Pantai Paciran
Konsentrasi logam berat Pb dan Cd yang tinggi di daun (Gambar 4 dan 5) menunjukkan bahwa daun merupakan akumulator utama logam berat di perairan. Konsentrasi logam berat yang tinggi padalamun disebabkan karena proses penyerapan logam berat bersama dengan nutrien tidak hanya terjadi di akar namun juga terjadi di daun meskipun dalam jumlah yang lebih sedikit daripada di akar. Sehingga dapat diketahui bahwa konsentrasi Pb dan Cd di daun tidak hanya berasal dari mobilitas dari akar namun juga proses penyerapan oleh daun itu sendiri. Berdasarkanfaktor oseanografi, nilai pH di
Pantai Paciran yang cenderung asam akan
menyebabkan logam berat mudah terakumulasi pada jaringan lamun terutama daun dan sebagian akan mengendap ke sedimen bersama dengan padatan tersuspensi[10].
3.4 Faktor Biokonsentrasi Logam Berat Pb dan Cd pada Lamun Enhalus acoroides
Hasil perhitungan nilai BCF pada akar dan daun lamun terhadap logam berat Pb dan Cd disajikan pada Tabel 3. Rata-rata nilai BCF pada akar dan daun lamun Enhalus acoroides terhadap logam berat Pb adalah 1,44 dan 1,76 ; sedangkan rata-rata BCF Cd pada akar dan daun lamun adalah 3,77 dan 4,48. Apabila dikategorikan menurut rujukan[11]Enhalus acorides termasuk ke dalam tanaman akumulator terhadap logam berat Pb dan Cd dengan nilai BCF > 1. Tanaman akumulator adalah kemampuan tanaman dalam menyerap zat pencemar ke dalam jaringan tubuhnya.
Tabel 3. Nilai BCF akar dan daun lamun Enhalus acoroides terhadap logam berat Pb dan Cd di Pantai Paciran
BCF
Pb Cd Akar Daun Akar Daun
1,44 1,76 3,74 4,48
3.5 Faktor Translokasi Logam Berat Pb dan Cd pada Lamun Enhalus acoroides
Hasil perhitungan nilai TF Pb dan Cd pada lamun
Enhalus acoroides disajikan pada Tabel 4. Nilai TF logam berat Pb dari akar ke daun yaitu 1,23 dan nilai TF Cd dari akar ke daun yaitu 1,19. Apabila dikategorikan menurut rujukan [5]Enhalus acoroides
mempunyai kemampuan mekanisme fitoekstraksi (TF>1) logam berat Pb dan Cd. Fitoekstraksi adalah proses penyerapan logam berat oleh akar tanaman yang kemudian di translokasikan menuju batang dan daun.
Tabel 4. Nilai TF Lamun Enhalus acoroides
terhadap logam berat Pb dan Cd
TF Pb Cd
1,23 1,19
3.6 Analisa Logam Berat Pb dan Cd pada Lamun Enhalus acoroides sebagai Agen Fitoremidiasi (FTD)
Hasil perhitungan nilai FTD pada akar dan daun lamun
Enhalus acoroides terhadap logam berat Pb dan Cd disajikan pada Tabel 5. Rata-rata nilai FTD Pb akar dan
lamun Enhalus acoroides adalah 0,08 dan 0,48
sedangkan rata-rata nilai FTD Cd yaitu 3,00 dan 4,11.
Tabel 5. Nilai FTD logam berat Pb dan Cd pada akar dan daun lamun Enhalus acoroides
Nilai rata-rata FTD Enhalus acoroides terhadap logam berat Cd lebih tinggi daripada logam berat Pb. Sehingga diperoleh kesimpulan bahwa lamun Enhalus acoroides
mampu meremediasi lebih banyak logam berat Cd dari pada Pb dan dapat diketahui bahwa lamun Enhalus acoroides dapat digunakan untuk tujuan Fitoremidiasi logam berat Cd di perairan. Hal ini didukung dengan rata-rata nilai BCF atau tingkat akumulasinya pada akar dan daun logam berat Cd lebih tinggi dari pada Pb. Pada dasarnya nilai FTD akan maksimal apabila nilai BCF lebih besar dibandingkan nilai TF.Ion Cd memiliki karakteristik bioavaibilitas dan bioakumulasi yang tinggi ke dalam tubuh organisme dan tumbuhan[12]. Konsentrasi Cd pada tubuh organisme dan tumbuhan akan meningkat dan cenderung seragam dengan bertambahnya usia. Selain itu, konsentrasi logam berat Cd pada sedimen dan air yang lebih rendah dari pada konsentrasi Pb menandakan bahwa tumbuhan air ini mampu meremediasi logam berat Cd daripada Pb. Hal inilah yang menyebabkan lamun Enhalus acoroides
0 0,05 0,1 1 2 3 4 K on sent ra si (p p m ) Titik Sampling akar daun FTD Pb Cd Akar 0,21 2,54 Daun 0,54 3,29
mampu menjadi agen fitoremediasi logam berat Cd dari pada Pb.
3.7 Pengaruh kualitas Air Terhadap Konsentrasi logam berat Pb dan Cd di air, sedimen, akar dan daun lamun Enhalus acoroides
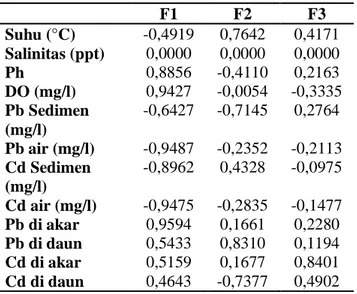
Berdasarkan hasil analisa faktor loading PCA pada Tabel 6 menunjukkan bahwa parameter DO memiliki pengaruh yang dominan dengan nilai 0,9427 tehadap konsentrasi logam berat Pb dan Cd di air, sedimen, akar dan daun lamun dibandingkan dengan parameter yang lainnya. Nilai DO yang tinggi akan mempermudah logam berat larut dalam air kemudian terakumulasi ke dalam jaringan lamun baik akar maupun daun.
Factor loading yang paling berpengaruh setelah DO adalah pH dengan nilai 0,8856. Pada dasarnya nilai pH
mempengaruhi tingkat kelarutan logam berat
diperairan. pH air laut yang asam akan mempengaruhi kelarutan logam berat dimana unsur logam berat akan mudah bereaksi dengan partikel badan air[12].
Tabel 6. Faktor loading kualitas air terhadap logam berat Pb pada air, sedimen, akar dan daun lamun
Enhalus acorides
Parameter suhu pada kolom F1 secara langsung tidak terlalu berpengaruh terhadap konsentrasi logam berat Pb dan Cd. Namun, pada kolom F2 nilai suhu secara tidak langsung memiliki pengaruh yang dominan terhadap logam berat Pb dan Cd pada air, sedimen, akar dan daun lamun dengan nilai 0,76. Salah satu contohnya yaitu ketika suhu naik akan menyebabkan penurunan DO dan pH yang berdampak pada meningkatnya toksisitas dan penurunan daya larut logam berat. Nilai salinitas bedasarkan factor loading
baik dari kolom F1 sampai dengan F3 tidak memiliki pengaruh yang dominan terhadap logam berat Pb dan Cd pada air dan sedimen. Hal ini disebabkan karena
nilai salinitas ditiap titik yang diambil memiliki nilai yang sama yaitu 31.
1V. Kesimpulan
Hasil pembahasan dari penelitian ini dapat diperoleh kesimpulan bahwa rata-rata konsentrasi logam berat Pb di air 0,1490 ppm dan rata-rata di sedimen 0,1774 ppm serta rata-rata konsentrasi logam berat Cd di air yaitu 0,0279 ppm dan di sedimen yaitu 0,0155 ppm. Rata-rata kandungan logam berat Pb di Pantai Paciran pada akar dan daun lamun masing-masing adalah 0,25463 ppm dan 0,31308 ppm sedangkan kandungan logam berat Cd pada akar dan daun lamun adalah 0,058375 ppm dan 0,0694 ppm. Rata-rata tingkat akumulasi (BCF) logam berat Pb pada akar dan daun lamun
Enhalus acoroides adalah 1,76 dan 2,16 sedangkan nilai rata-rata BCF logam berat Cd pada akar dan daun lamun adalah 4,21 dan 5,32. Hal ini menyatakan bahwa
lamun Enhalus acoroides merupakan tumbuhan dengan
kategori akumulator terhadap logam berat Pb dan Cd. Rata-rata nilai FTD Pb akar dan lamun Enhalus acoroides adalah 0,08 dan 0,48 sedangkan rata-rata nilai FTD Cd yaitu 3,00 dan 4,11. Nilai rata-rata FTD
Enhalus acoroides terhadap logam berat Cd lebih tinggi daripada logam berat Pb. Sehingga dapat diketahu bahwa lamun Enhalus acoroides dapat digunakan untuk tujuan Fitoremidiasi logam berat Cd.
DAFTAR PUSTAKA
[1] J. Triadi, “Konsentrasi Logam Timbal (Pb) dan Tembaga (Cu) pada Lamun Enhalus acoroides dan Sedimen di Pulau Bonetambung dan Gusung Tallang,” 2014.
[2] A. D. Puspita, A. Santoso, and B. Yulianto. Studi Akumulasi Logam Timbal (Pb) dan Efeknya Terhadap Kandungan Klorofil Daun Mangrove Rhizophora mucronata. J. Mar. Res., vol. 3, no. 1, pp. 44–53. 2014. [3] M. Rijal. Bioakumulation Heavy Metals Lead (Pb) and Cadmium (Cd) Seagrass (Enhalus acroides) in Waai and Galala Island Ambon. J. Mar. Resvol. 16, pp. 349– 356. 2014.
[4] C. Govindasamy, M. Arulpriya, P. Ruban, L. F. Jenifer, and A. Ilayaraja. Concentration of heavy metals in seagrasses tissue of the Palk Strait, Bay of Bengal.Int. J. Environ. Sci., vol. 2, no. 1, pp. 145–153. 2011.
[5] S. N. Majid, A. I. Khwakaram, G. A. M. Rasul, and Z. H. Ahmed. Bioaccumulation, Enrichment and Translocation Factors of some Heavy Metals in Typha Angustifolia and Phragmites Australis Species Growing along Qalyasan Stream in Sulaimani
F1 F2 F3 Suhu (°C) -0,4919 0,7642 0,4171 Salinitas (ppt) 0,0000 0,0000 0,0000 Ph 0,8856 -0,4110 0,2163 DO (mg/l) 0,9427 -0,0054 -0,3335 Pb Sedimen (mg/l) -0,6427 -0,7145 0,2764 Pb air (mg/l) -0,9487 -0,2352 -0,2113 Cd Sedimen (mg/l) -0,8962 0,4328 -0,0975 Cd air (mg/l) -0,9475 -0,2835 -0,1477 Pb di akar 0,9594 0,1661 0,2280 Pb di daun 0,5433 0,8310 0,1194 Cd di akar 0,5159 0,1677 0,8401 Cd di daun 0,4643 -0,7377 0,4902
City/IKR.. J. Zankoy Sulaimani-Part A, vol. 16, p. 4. 2014.
[6] F. Feryatun. Kerapatan dan Distribusi Lamun (Seagrass) Berdasarkan Zona Kegiatan yang Berbeda di Perairan Pulau Pramuka, Kepulauan Seribu.Manag. Aquat. Resour. J., vol. 1, no. 1, pp. 44–50, 2012. [7] K. Amri, D. Setiadi, I. Qayim, and D. Djokosetiyanto.
Dampak Aktivitas Antropogenik Terhadap Kualitas Perairan Habitat Padang Lamun di Kepulauan Spermonde Sulawesi Selatan. 2013.
[8] M. Simanjuntak. Kualitas Air Laut Ditinjau Dari Aspek Zat Hara, Oksigen Terlarut Dan Ph Di Perairan Banggai, Sulawesi Tengah Sea Water Quality Observed From Nutrient Aspect, Dissolved Oxygen And Ph In The Banggai Waters, Central Sulawesi,. J. Ilmu Dan Teknol. Kelaut. Trop., vol. 4, no. 2, p. 291, 2012.
[9] P. Taba, N. La Nafie, A. Noor, et. al. Analisis Besi dalam Ekosistem Lamun dan Hubungannya dengan Sifat Fisikokimia Perairan Pantai Kabupaten Donggala.
J. Nat. Indones., vol. 13, no. 2, 2012.
[10] N. Nurhasni. Penyerapan Ion Logam Kadmium Dan Tembaga Oleh Genjer (Limnocharis flava).VALENSI, vol. 1, no. 1. 2007.
[11] A. J. Baker. Accumulators and excluders-strategies in the response of plants to heavy metals.J. Plant Nutr., vol. 3, no. 1–4, pp. 643–654. 1981.
[12] H. Palar, Toksikologi dan Pencemaran Logam Berat, Jakarta: PT Rineka Cipta, 2004.
.