MAKALAH KONSEP KEREATIVITAS DAN SIFAT UNSUR GOLONGAN IA
Tugas Kimia Unsur 2016 Disusun oleh :
Nadhira Izzatur Silmi 145090200111026 Tomi Setiawan 145090200111020 Zulfatul Muzayyana 145090200111023
Golongan IA disebut juga golongan alkali monovalen. Golongan IA memiliki tujuh unsur, yaitu Hidrogen (H), Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Caesium (Cs) dan Fransium (Fr). Semua golongan alkali tampak mengkilat, berwarna keperakan, konduktor listrik dan panas yang baik, dan dapat dipotong dengan pisau. Logam alkali bersifat sangat lunak dan semakin lunak dengan naikknya nomor atom. Sebagian besar logam memiliki titik leleh yang sangat tinggi, tetapi logam alkali memiliki titik leleh yang rendah karena kerendahan titik leleh logam-logam alkali dapat dikaitkan dengan lemahnya ikatan metalik dalam unsur-unsur ini1. Logam Alkali menampakkan warna khas pada
nyala api bunsen, kejadian ini disebabkan karena adanya sejumlah kecil energi dari nyala api yang diserap oleh elektron pada kulit terluar, sehingga elektron tersebut mengalami eksitasi. Saat elektron kembali ke posisi semula, Elektron mengeluarkan energi yang telah diserap sebagai cahaya tampak. Logam alkali tanah memiliki tetapan-tetapan fisika yang berubah-ubah secara teratur dari satu logam ke logam lainnya2.
1 Sugiyarto, H, K, Retno, D, S, 2010, Kimia Anorganik Logam, Graha Ilmu, Jogjakarta
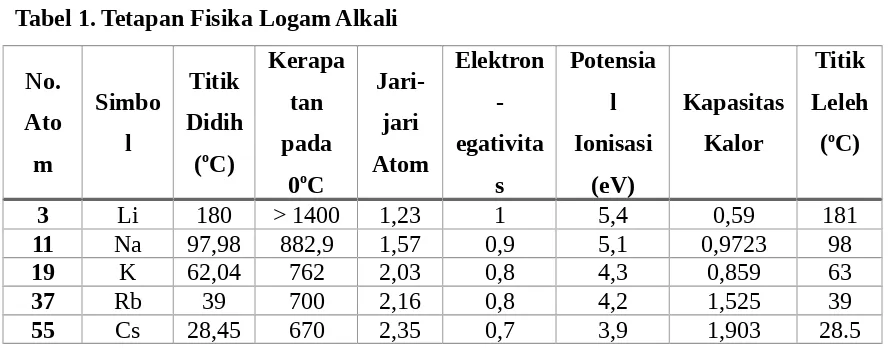
Tetapan fisika tersebut dapat dilihat di tabel berikut2 :
Tabel 1. Tetapan Fisika Logam Alkali No.
Senyawa logam alkali berkaitan dengan1 :
1. Karakter Ion.
Karakter ion logam alkali selalu memiliki tingkat oksidasi +1, sebagian senyawanya berupa padatan ionik, dan stabil. Senyawa-senyawanya tidak berwarna kecuali bila berikatan dengan ion yang berwarna seperti Kromat
dan Permanganat.
2. Hidrasi Ion
Semakin tinggi densitas muatan ion, maka kuat ion tesebut akan terhidrasi karena ogam-logam alkali memiliki densitas yang jauh lebih rendah (0,52-1,87 g cm-3) daripada densitas logam-logam pada umumnya (5-15 g cm-3),
maka energi hidrasi senyawa-senyawanya juga sangat rendah. Energi hidrasi semakain kecil dengan kenaikan jari-jari ion
3. Kelarutan
Setiap logam alkali menghasilkan warna nyala yang berbeda-beda, jika senyawa-senyawa alkali tersebut dibakar dalam nyala api. Warna yang terlihat dari masing-masing logam adalah merah tua (Lithium), Kuning (Natrium), Nila (Kalium), merah violet (Rubidium), Biru (Caesium)1.
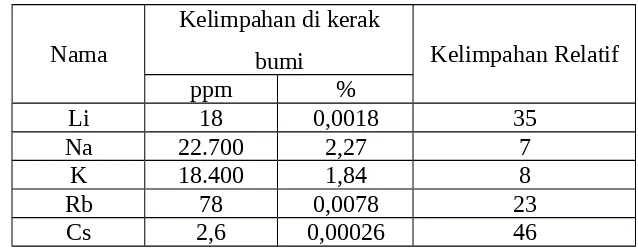
Kelimpahan unsur alkali pada kerak bumi dapat dilihat di tabel berikut3 :
Tabel 2. Kelimpahan Unsur Alkali pada Kerak Bumi
Nama
Kelimpahan di kerak
bumi Kelimpahan Relatif
ppm %
Li 18 0,0018 35
Na 22.700 2,27 7
K 18.400 1,84 8
Rb 78 0,0078 23
Cs 2,6 0,00026 46
Senyawa alkali merupakan senyawa yang sangat reaktif dan bereaksi secara cepat dengan udara kering. Natrium, Kalium, Rubidium, dan Caesium membentuk berbagai tipe oksida, tetapi Lithium membentuk campuran dari oksida dan nitrida.
Lithium merupakan satu-satunya unsur yang dapat beraksi dengan Nitrogen membentuk Nitrida. Lithium Nitrida (Li3N) merupakan ionik (3Li+ dan
N3-) dan berwarna merah rubi. Dua reaksi nitrida adalah yang paling penting.
Pertama, pemanasan pada temperatur tinggi akan menguraikan senyawa tersebut. Kedua, senyawa tersebut akan bereaksi dengan air dan akan menghasilkan amonia
2Li3N + O2 6Li + N2
Li3N + 3H2O 3LiOH + NH3