II. TINJAUAN PUSTAKA
2.1. Membran
2.1.1 Sejarah Membran
Sejarah membran diawali tahun 1748 saat Abbe Nolet, seorang fisikawan Perancis menemukan gejala osmosis pada membran kantung kemih babi. Dilanjutkan oleh Tzambe, kimiawan asal Jerman pada 1867 dengan serentetan percobaan membran sintesis. Sepanjang abad ke-19 hingga awal abad ke-20, membran tidak digunakan untuk industri ataupun tujuan komersil, tapi hanya sebagai peralatan laboratorium untuk mengembangkan teori fisika dan kimia.
Terobosan teknologi membran dimulai pada tahun 1960-an melalui pengembangan membran berpori asimetris oleh Loeb dan Sourirajan (UCLA). Membran pun mulai berkembang dengan sangat pesat sejak tahun 1970-an. Material membran jenis baru mulai digunakan, dimensi modul dan sistem membran semakin besar dengan kinerja yang makin piawai, tekanan operasi membran semakin kecil, dan peningkatan kontrol mutu telah dipadukan dengan sistem komputer (Hartomo dan Widiatmoko 1994; Nunes dan Peinemann 2001; Baker 2004).
Tabel 1 berikut menampilkan beberapa perkembangan proses membran dan aplikasinya. Dari tahun 1920 hingga 1950, proses membran masih digunakan dalam skala kecil, dan pada tahun 1950-an mulai diaplikasikan pada skala industri.
Tabel 1 Perkembangan teknik proses membran (Mulder 1996). Proses membran Negara Tahun Aplikasi
Mikrofiltrasi Jerman 1920 Laboratorium (filter bakteri)
Ultrafiltrasi Jerman 1930 Laboratorium
Hemodialisis Belanda 1950 Ginjal tiruan
Elektrodialisis USA 1955 Desalinasi
Hiperfiltrasi USA 1960 Desalinasi air laut
Ultrafiltrasi USA 1960 Pemisahan makromolekul Separasi gas USA 1979 Perolehan kembali hidrogen Membran distilasi Jerman 1981 Konsentrasi larutan encer Pervaporasi Jerman/Belanda 1982 Dehidrasi pelarut organik
2.1.2 Sifat dan Karakteristik Membran
Membran didefinisikan sebagai sebuah struktur yang memiliki dimensi lateral jauh lebih besar dari ketebalannya, dan sejumlah perpindahan massa dapat terjadi melalui membran di bawah berbagai variasi gaya penggerak (Pellegrino 2000). Membran dapat melewatkan molekul atau partikel dari fasa satu ke fasa lain karena beberapa faktor, seperti gradien temperatur, gradien konsentrasi, gradien tekanan, dan gradien energi (Baker 2004).
Membran dapat dianggap sebagai penghalang yang permeabel dan selektif antara dua fase. Fase pertama biasanya dianggap sebagai umpan (feed), sementara fase kedua adalah hasil pemisahan (permeate). Pemisahan tercapai karena membran memiliki kemampuan untuk mengangkut salah satu komponen campuran umpan lebih mudah daripada komponen lainnya. Membran dapat berukuran tebal ataupun tipis, strukturnya bisa homogen ataupun heterogen (komposit), dan proses perpindahan material melewati membran dapat terjadi melalui proses transpor aktif dan pasif. Transpor pasif dapat digerakkan oleh perbedaan tekanan, konsentrasi, atau perbedaan temperatur di antara kedua sisi membran (Mulder 1996). Proses pemisahan melalui membran dapat diilustrasikan seperti pada Gambar 1.
Gambar 1 Proses pemisahan oleh membran sintesis (Chelme-Ayala et al. 2009)
Secara umum, membran dibedakan atas membran alami dan sintesis. Membran alami adalah membran sel biologi pada makhluk hidup, sedangkan membran sintesis adalah membran buatan, yang terbagi atas membran organik (polimer atau cairan) dan anorganik (terbuat dari metal, gelas, keramik, dll.) (Mulder 1996). Berdasarkan strukturnya, membran dibedakan menjadi membran
simetrik dan asimetrik. Membran simetrik adalah membran dengan ukuran pori yang sama dari permukaan atas membran hingga permukaan bawahnya. Sedangkan membran asimetrik adalah membran yang memiliki ukuran pori berbeda antara permukaan atas dan bawahnya (Scott 1995).
Berdasarkan prinsip pemisahannya, membran dapat dibagi menjadi 3 jenis, sebagaimana diilustrasikan pada Gambar 2 (Mulder 1996).
Gambar 2 Jenis membran berdasarkan prinsip pemisahan
a. Membran berpori
Membran berpori melakukan pemisahan berdasarkan perbedaan ukuran partikel. Membran jenis ini digunakan dalam ultrafiltrasi dan mikrofiltrasi.. Selektivitas terutama ditentukan oleh ukuran pori terhadap ukuran partikel yang akan dipisahkan, di mana material membran tidak memberikan pengaruh yang begitu besar pada pemisahan tersebut. Selektivitas yang tinggi dapat diperoleh jika ukuran partikel terlarut relatif lebih besar dari pori membran. b. Membran non pori
Membran ini mampu memisahkan molekul yang berukuran hampir sama. Proses pemisahan terjadi melalui perbedaan daya larut dan/atau difusifitas. Ini berarti bahwa sifat intrinsik material menentukan tingkat selektifitas dan permeabilitas. Membran ini digunakan dalam pervaporasi dan pemisahan gas. c. Membran cair
Dengan membran jenis ini, proses transpor tidak dipengaruhi oleh membran atau material membran, tapi oleh molekul pembawa (carrier) yang sangat spesifik. Pembawa yang mengandung cairan berada di dalam pori membran. Permeselektivitas komponen terutama bergantung pada kekhususan molekul
pembawa. Komponen yang dipisahkan dapat berupa gas atau cairan, ionik atau non ionik. Pada beberapa tingkatan, fungsinya mendekati membran sel.
Berdasarkan gradien tekanan sebagai daya dorong dan permeabilitasnya, membran dibedakan menjadi (Nunes dan Painemann 2001; Baker 2004):
a. Mikrofiltrasi (MF). Membran jenis ini beroperasi pada tekanan berkisar 0,1-2 bar dan batasan permeabilitasnya lebih besar dari 50 L/m2.jam.bar.
b. Ultrafiltrasi (UF). Membran jenis ini beroperasi pada tekanan antara 1-5 bar dan batasan permeabilitasnya adalah 10-50 L/m2.jam.bar.
c. Nanofiltrasi. Membran jenis ini beroperasi pada tekanan antara 5-20 bar dan batasan permeabilitasnya mencapai 1,4-12 L//m2.jam.bar
d. Reverse osmosis (RO). Membran jenis ini beroperasi pada tekanan antara 10-100 bar dan batasan permeabilitasnya mencapai 0,005-1,4 L/m2.jam.bar
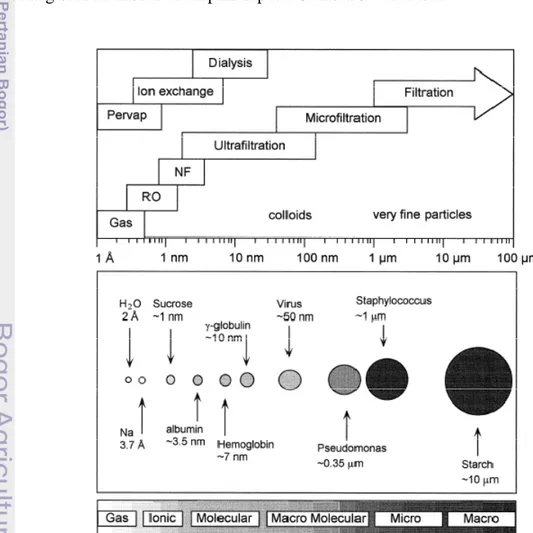
Jangkauan operasi membran, aplikasi, dan tujuan kontaminan yang disaring oleh membran ditampilkan pada Gambar 3 dan Tabel 2.
Tabel 2 Proses membran dan aplikasinya (Chelme-Ayala et al. 2009) Membran Target kontaminan utama Sumber air Aplikasi Mikrofiltrasi Kekeruhan, protozoa, dan
penghilangan bakteri
Air
permukaan
Sewer, aplikasi lahan (irigasi, perkolasi, kolam pengendapan) Ultrafiltrasi Kekeruhan, senyawa organik,
iron-manganese
Air tanah Aplikasi lahan, sewer Nanofiltrasi Kesadahan, padatan terlarut,
senyawa organik
Air tanah Sumur dalam, sewer Osmosis balik Padatan terlarut,
radionuklida, reklamasi air
Air tanah Surface discharge, sewer
2.1.3 Konduktansi Membran
Salah satu sifat listrik yang dimiliki oleh membran adalah konduktansi. Konduktansi merupakan ukuran yang menggambarkan kemampuan suatu bahan untuk membawa arus listrik. Sifat ini muncul karena adanya interaksi antara ion dengan membran. Konduktansi sangat penting dalam proses pemisahan pada membran karena dapat menentukan geometri dan dimensi pori. Besarnya konduktansi membran (G) dapat diperoleh dengan pendekatan persamaan:
G = n Gp (1)
dengan n adalah jumlah pori membran, dan Gp adalah konduktansi tiap pori
(asumsi pori-pori identik). Terdapat beberapa hal yang mempengaruhi nilai Gp, di
antaranya faktor geometri pori, konsentrasi pori, dan mobilitas ionnya. Dengan asumsi bahwa ion di dalam suatu medium dielektrik akan mengalami interaksi elektrostatik dengan membran.
Sebuah ion dengan radius d dan muatan zq (di mana z adalah bilangan valensi ion dan q adalah muatan ion), dalam suatu medium yang luasnya tak berhingga dengan konstanta dielektrik ε, akan memiliki energi diri U yang besarnya adalah:
U = z2 q2 / 8 π εo εm d (2)
Nilai energi diri ion akan berubah bagi ion yang mediumnya memiliki konstanta dielektrik tak seragam. Energi diri ion tersebut pun akan berubah tergantung kepada di mana ion tersebut berada. Oleha karena itu nilai ini sangat
bergantung pada konstanta dielektrik (ε). Nilai U akan naik secara teratur sesuai dengan banyaknya ion yang melewati suatu daerah dengan konstanta dielektrik ε lebih rendah. Konstanta dielektrik membran lebih kecil (biasanya εm = 3)
dibanding konstanta dielektrik pelarut (air, εs = 78.5).
Ion yang melewati membran dapat menyebabkan adanya perubahan energi diri sebesar ΔU, sebagai akibat interaksi medan listrik dengan konstanta dielektrik membran (εm), yang tergantung pada seberapa dekatnya ion pada membran.
Perubahan energi diri ΔU dapat ditentukan melalui : ΔU = z2
q2 α / 4 π εo εm b (3)
Dengan z adalah bilangan valensi ion, q adalah muatan ion, α merupakan nilai yang bergantung pada konstanta geometri dan dielektrik, εo adalah konstanta
resapan, dan b adalah jari-jari pori membran.
Peningkatan energi diri ΔU akan mempengaruhi konsentrasi ionik yang ada di dalam membran. Secara energetika, kenaikan energi diri kurang baik untuk ion yang berada dalam pori-pori membran yang rapat, dengan konstanta dielektrik rendah. Jika C adalah konsentrasi ion di pusat membran, Co adalah konsentrasi ion
pada jarak yang jauh dari membran, G adalah konduktansi di pusat membran, Go adalah konduktansi yang berjarak jauh dari membran, dengan konstanta
Boltzman k dan suhu T, maka koefisien partisi γ dapat dihitung dengan menggunakan statistik Boltzman:
γ = C/ Co = G/ Go = exp (-ΔU / k T) (4)
Pada elektrolit dengan konsentrasi kation P dan anion N, serta valensi zp dan zn,
dan dengan co adalah kekuatan ionik larutan, maka:
zp P = zn N = co (5)
Untuk membran dengan ukuran pori lebih besar dari panjang Debye dan dengan medan listrik konstan, maka besarnya nilai konduktansi untuk tiap pori Gp
terhadap ion yang mengalir adalah:
L T k b D z D z C q Gp p p p n n n 2 0 2 ) ( γ + γ π = (6) dengan :
(
zp q mbRT)
p α πε ε γ 0 2 2 4 exp − = (7)(
zn q mbRT)
n α πε ε γ 2 2 0 4 exp − = (8)Di mana b adalah jari-jari pori membran, L adalah ketebalan membran, K adalah konstanta Boltzman (1.38662 x 10-23 J/K), T merupakan suhu dalam Kelvin, dan R adalah konstanta molar gas (8.314 J/mol K).
Dari persamaan (6) dapat diamati bahwa ada kebergantungan dari Gp
terhadap temperatur, dan menunjukkan hubungan yang linear. Pada suhu yang tinggi, nilai G akan semakin besar, ini berarti pula bahwa pergerakan ion juga lebih besar. Di samping itu, koefisien partisi γ juga akan membesar, dengan demikian energi diri ΔU akibat interaksi medan magnet juga meningkat. Dengan menganggap konduktansi untuk tiap pori (Gp) adalah sama, maka jumlah pori n
dapat diketahui melalui persamaan (1), dan mekanisme transpor pun dapat diketahui (Smith et al. 1992).
2.1.4 Teknik Pembuatan Membran
Terdapat beberapa jenis pembuatan membran seperti sintering, stretching, track-etching, template leaching, coating, dan phase inversion (inverse fasa). Teknik inversi fasa adalah teknik yang umum digunakan untuk membran berbahan polimer. Inversi fasa adalah proses di mana polimer dibentuk dari keadaan cair menjadi padat dengan cara terkontrol (Mulder 1996).
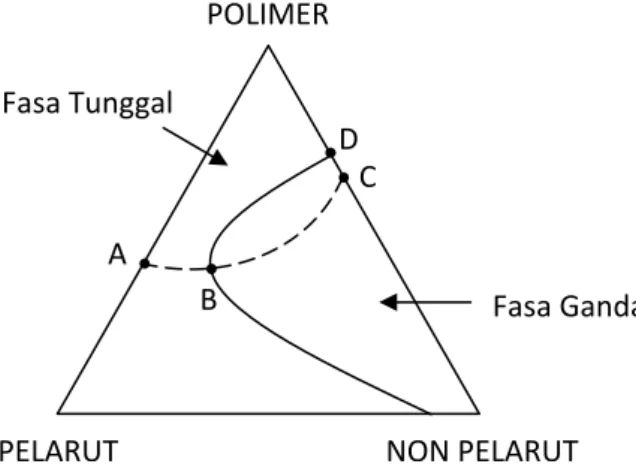
Mekanisme pembuatan membran dengan teknik inversi fasa dapat dijelaskan melalui diagram terner seperti terlihat pada Gambar 4. Seluruh sistem pada diagram dibagi menjadi dua daerah penting, yaitu daerah fasa tunggal dan fasa ganda. Sistem tersebut terdiri atas tiga komponen utama yang berperan dalam pembuatan membran yaitu polimer, pelarut, dan non pelarut. Pada daerah fasa tunggal, ketiga komponen larut membentuk larutan serba sama. Titik A menunjukkan larutan cetak membran yang mengandung polimer dan pelarut. Pada saat proses koagulasi di dalam non pelarut, pelarut akan berdifusi ke non pelarut. Dalam proses ini, fasa tunggal masih terbentuk hingga di titik B. Di saat yang bersamaan, di titik B juga mulai muncul daerah fasa ganda. Proses koagulasi yang lebih lama akan mengakibatkan semua pelarut berdifusi ke non pelarut dan berakhir pada titik C, di mana titik ini adalah komposisi membran keseluruhan.
Gambar 4 Diagram fasa pada pembentukan membran (Londsdale 1985)
Pada titik B, campuran 3-komponen melewati rongga pengendapan. Penukaran lebih lanjut pelarut oleh non pelarut mengakibatkan pergeseran ke arah fase di mana bagian polimer dominan. Pada titik C proses penguapan pelarut berakhir, dan semua pelarut telah digantikan oleh non pelarut; ada dua fase yang saling berdekatan, yaitu fase padat (polimer) yang membentuk struktur membran dan fase cair yang mengisi volume pori. Proses penguapan pelarut terjadi sesaat sebelum proses koagulasi. Penguapan menyebabkan lapisan atas membran kekurangan pelarut. Oleh karena itu, komposisi lapisan atas membran kaya akan polimer sebagaimana ditunjukkan pada titik D dalam diagram.
Proses pembuatan membran sesungguhnya tidak sederhana seperti yang tergambar pada diagram terner. Penjelasan tersebut adalah pendekatan proses kesetimbangan, sedangkan pembuatan membran sebenarnya bukan merupakan proses kesetimbangan. Namun demikian, pendekatan diagram fasa sangat berguna dalam pembuatan membran asimetrik (Londsdale 1985; Romli et al. 2006).
2.2 Arang Aktif
2.2.1 Sifat dan Struktur Arang Aktif
Arang adalah suatu bahan padat berpori, merupakan hasil pembakaran dari bahan yang mengandung unsur karbon. Sebagian besar dari pori-porinya masih tertutup dengan hidrokarbon, ter, dan senyawa organik lain. Komponen arang terdiri dari karbon terikat, abu, air, nitrogen, dan sulfur (Djatmiko et al. 1985). Arang aktif adalah arang yang konfigurasi atom karbonnya dibebaskan dari
A B D C POLIMER NON PELARUT PELARUT Fasa Ganda Fasa Tunggal
ikatan dengan unsur lain, serta porinya dibersihkan dari senyawa atau kotoran lain, sehingga permukaan dan pusat aktif menjadi luas, serta kemampuan adsorpsinya terhadap cairan dan gas meningkat (Sudradjat dan Soleh 1994).
Secara fisik arang aktif berbentuk padatan, berwarna hitam, tidak berbau, tidak berasa, bersifat higroskopis, tidak larut dalam air, basa, asam dan pelarut organik, serta tidak rusak karena perubahan pH maupun suhu. Susunan atom karbon dalam arang aktif mirip dengan susunan atom karbon dalam grafit, yang terdiri dari pelat-pelat datar di mana atom karbonnya tersusun dan terikat secara kovalen di dalam suatu kisi heksagonal secara paralel (Gambar 5). Struktur arang aktif berbeda dengan struktur grafit karena pelat-pelat karbon heksagonal dalam arang aktif tidak terorientasi sempurna tegak lurus terhadap sumbunya. Besar kecilnya ukuran pori dari kristalit arang aktif selain bergantung pada suhu karbonasi, juga bergantung pada bahan baku yang digunakan. Ukuran porinya dapat berkisar antara 10 – 250 Å (Pari 2004).
Gambar 5 Struktur heksagonal grafit (Marsh dan Rodriguez-Reinoso 2006)
Bonelli (2001) serta Daud dan Ali (2004) menyatakan bahwa struktur, penyebaran, dan ukuran pori arang aktif lebih dipengaruhi oleh sifat dasar bahan baku (lignin, selulosa dan holoselulosa). Arang aktif tempurung kelapa menun-jukkan distribusi pori halus (mikropori) lebih banyak dibanding arang aktif kayu.
Karbon aktif dengan struktur mesopori dapat digunakan untuk pemurnian air minum, perlakuan limbah cair, penghilangan warna pada makanan dan bahan kimia. Sedangkan pada struktur mikropori digunakan untuk mendaur ulang zat cair, pengendali emisi gas pada minyak gas, saringan pada rokok dan pengendali emisi gas pada industri. Penggunaan karbon sebagai penyerap juga dipengaruhi
oleh luas permukaan, penyebaran pori dan sifat kimia permukaan arang aktif (Benaddi et al. 2000).
2.2.2 Pembuatan Arang Aktif
Setiap material yang mengandung karbon (hewan, tumbuhan, atau bahan mineral) dengan konsentrasi karbon yang tinggi, dapat dibuat menjadi arang aktif. Bahan baku yang paling sering digunakan adalah kayu, arang kayu, kulit kacang-kacangan, batu bara, dan tulang. Polimer sintetik seperti PVC juga dapat digunakan untuk membuat arang aktif (Ansari dan Mohammad-Khah 2009). Di Indonesia sendiri, penelitian tentang arang aktif telah banyak dilakukan, dan umumnya menggunakan bahan baku dari biomassa, seperti tempurung kelapa dan kayu bakau (Hartoyo et al. 1990), tempurung biji-bijian (Hudaya dan Hartoyo 1990), berbagai jenis kayu (Pari 1996; Pari 2004), serta berbagai macam biomassa hutan, seperti kayu mani, bambu mayan, dan tempurung kemiri (Komarayati et al. 1998; Hendra dan Darmawan 2007).
Perubahan komponen kimia kayu dalam proses karbonisasi terjadi pada suhu 100 - 1000 oC, di mana perubahan terbesar terjadi pada suhu 200 - 500 oC. Reaksi pada proses karbonisasi adalah eksoterm, yaitu jumlah panas yang dikeluarkan lebih besar dari yang diperlukan. Reaksi eksoterm ini terlihat nyata pada suhu 300 - 400 oC, di mana suhu melonjak dengan cepat, meskipun jumlah panas yang diberikan tetap. Umumnya pembuatan arang dilakukan pada suhu di atas 500 oC. Garis besar proses karbonisasi kayu dibagi menjadi 4 tahap, yaitu: - Pada suhu 100 - 120 oC terjadi penguapan air, dan sampai suhu 270 oC mulai
terjadi penguraian selulosa. Destilat mengandung asam organik dan sedikit metanol. Asam cuka terbentuk pada suhu 200-270 oC.
- Pada suhu 270 - 310 oC reaksi eksotermik berlangsung, di mana terjadi peru-raian selulosa secara intensif menjadi larutan pirolignat, gas kayu, dan sedikit ter. Asam pirilignat merupakan asam organik dengan titik didih rendah seperti asam cuka dan metanol, sedangkan gas kayu terdiri dari CO dan CO2.
- Pada suhu 310 - 500 oC, terjadi peruraian lignin, dihasilkan lebih banyak ter, sedangkan larutan pirolignat menurun. Gas CO2 menurun sedang gas CO,
- Pada suhu 500 - 1000 oC, diperoleh gas kayu yang tidak dapat diembunkan, terutama terdiri dari gas hidrogen. Tahap ini merupakan proses pemurnian arang atau peningkatan kadar karbon
(Djatmiko et al. 1985; Sudradjat dan Soleh 1994).
Pada dasarnya ada dua cara membuat arang aktif, yaitu melalui aktivasi fisik dan kimia. Aktivasi fisik dilakukan dalam dua tahap, pertama karbonisasi dan kedua aktivasi pada suhu tinggi. Pada aktivasi kimia, bahan diimpregnasi terlebih dahulu dengan bahan pengaktif lalu dikarbonisasi. Tahap karbonisasi dan aktivasi dilakukan secara berlanjut (Hayashi et al. 2002). Aktivasi arang dilakukan dengan pemanasan pada temperatur tinggi (800-1000 oC), akibatnya produk pembakaran yang belum sempurna ini terbakar dan mengalami penguapan. Selanjutnya luas permukaan karbon akan semakin meningkat dengan pelepasan hidrokarbon atau ter, sebagaimana diilustrasikan pada Gambar 6 (Ansari dan Mohammad-Khah 2009).
Gambar 6 Tahapan proses aktivasi karbon selama perlakuan pemanasan
Saat proses aktivasi kimia, senyawa yang menutupi pori atau rongga arang dikeluarkan dengan cara dehidrasi menggunakan bahan pengaktif, dapat berupa garam jenuh seperti MgCl2, ZnCl2, CaCl2, juga asam atau basa seperti NaOH dan
H3PO4. Aktivasi fisika juga dapat dilakukan dengan memberikan aliran uap panas
(H2O) atau gas seperti N2 dan CO2 pada suhu tinggi (900 - 1000 oC). Agar unsur
karbon dapat dibebaskan dari ikatan dengan unsur lain terutama hidrogen dan oksigen, dilakukan oksidasi lemah pada suhu tinggi dengan uap air. Kualitas arang aktif dipengaruhi oleh berbagai faktor, antara lain sifat bahan baku, teknologi proses, ukuran partikel, dan cara penggunaan yang tepat (Hartoyo dan Pari 1993; Sudradjat dan Soleh 1994).
Pengaruh utama aktivasi arang dengan aliran uap (steam) adalah untuk menciptakan dan memperluas pori arang. Aktivasi dengan steam tidak hanya memindahkan material yang tidak diorganisir tetapi juga cukup efektif dalam membentuk dan melebarkan mikropori dengan naiknya suhu. Kenaikan suhu dari 750oC ke 800oC dapat meningkatkan terbentuknya pori dan pada akhirnya akan meningkatkan volume mikropori arang aktif. Pada batas tertentu peningkatan suhu justru akan menurunkan volume mikroporinya (Bansode et al. 2003; Ismadji et al. 2005; Pari 2006).
Marsh dan Rodriguez-Reinoso (2006) mengemukakan dua keuntungan dalam menggunakan metode aktivasi kimia dibanding aktivasi fisika. Pertama, rendemen yang dihasilkan lebih tinggi (27 - 47 wt% dibanding 6 wt% pada aktivasi fisika). Kedua, struktur permukaan dari karbon aktif serat dengan aktivasi kimia menunjukkan tingkat kerusakan yang lebih kecil.
2.2.3 Proses Adsorpsi Arang Aktif
Karbon aktif adalah salah satu jenis adsorben yang efektif digunakan untuk proses adsorpsi. Kemampuan adsorpsi ini didukung oleh beberapa faktor, di antaranya sifat kimia dan fisika karbon aktif, suhu air, waktu kontak, luas permukaan karbon aktif, konsentrasi serta ukuran partikel adsorbat, dan jenis adsorbat. Adsorbat yang mudah berikatan dengan gugus-gugus pengaktif adalah yang bersifat nonpolar, sehingga molekul organik akan berikatan kuat dengan gugus pengaktif (Atkins 1997; Sukarjo 1997).
Adsorpsi merupakan suatu reaksi reversibel, pada konsentrasi zat terlarut yang diberikan. Adsorbat dapat diadsorpsi melalui dua cara, yakni dengan adsorpsi fisika dan kimia. Pada adsorpsi fisika, ada gaya lemah Van der Waals
yang menarik adsorbat ke permukaan adsorben. Selama proses adsorpsi
fisika, sifat kimia adsorbat tidak berubah. Adsorpsi fisika adalah proses spontan (ΔG <0), karena ΔS negatif, maka ΔH menjadi eksoterm. Dalam adsorpsi kimia, adsorbat menempel dengan membentuk ikatan kimia dengan permukaan adsorben. Interaksi ini lebih kuat dari adsorpsi fisika, dan secara umum memiliki persyaratan yang lebih ketat untuk memperoleh kompatibilitas antara adsorbat dan permukaan adsorben (Ansari dan Mohammad-Khah 2009).
Adsorpsi dapat terjadi karena setiap molekul pada permukaan mempunyai energi yang besar sehingga membentuk tegangan permukaan, akibatnya molekul pada permukaan mempunyai energi bebas yang lebih besar dibanding molekul di bawah permukaan. Molekul pada permukaan selalu berusaha mendapatkan energi bebas serendah mungkin, maka permukaan akan menyerap fasa yang tegangan permukaannya lebih rendah untuk menurunkan energi bebasnya (Sukarjo 1997). Adsorpsi kontaminan terlarut merupakan fenomena kompleks, yang disebabkan oleh beberapa mekanisme, seperti Gaya London-Van der Waals, gaya Coulomb, ikatan hidrogen, pertukaran ligan, adsorpsi kimia, gaya dipol-dipol, dan gaya hidrofobik. Sebagai contoh, hidrokarbon paling sering menunjukkan adsorpsi melalui proses ikatan hidrofobik. Jadi sifat permukaan adsorben yang mempengaruhi proses adsorpsi adalah luas permukaan, ukuran pori, distribusi mikropori, dan polaritas (hidrofilik atau hidrofobik) (Ansari dan Mohammad-Khah 2009).
2.3 Aplikasi Terintegrasi Membran dan Arang Aktif
Penggunaan adsorpsi karbon aktif untuk pembersihan air telah banyak diaplikasikan dan diteliti untuk berbagai jenis kontaminan. Karbon aktif terbukti dapat digunkan untuk menghilangkan logam berat dari cairan, juga dari limbah industri elektroplating (Awwad et al. 2008; Husain et al. 2009), menghilangkan logam terlarut dalam air buangan perkotaan (Lienden et al. 2010), menurunkan kandungan COD dan BOD dari limbah cair hasil pemroresan kopi (Devi 2010), serta dapat mengadsorpsi bahan kimia berbahaya dari air baku untuk air minum (Ismaeel et al. 2010);
Karbon aktif juga dapat digunakan secara terintegrasi dengan reaktor membran untuk filtrasi air (Campos et al. 2000; Choon et al. 2006; Hu dan Stuckey 2007; Yang et al. 2010). Proses perlakuan awal pada air baku untuk air minum, dengan adsorpsi menggunakan karbon aktif bubuk sebelum masuk ke modul membran, terbukti mampu meningkatkan kemampuan sistem membran dalam menghilangkan material organik terlarut (Lebeau et al. 1998; Berube et al. 2002). Adsorpsi dengan karbon aktif sebelum penyaringan dengan membran, lebih efektif dalam menghilangkan substansi humat terlarut pada sumber air
minum dibanding filtrasi membran tunggal (Lin et al. 1999). Karbon aktif juga dapat digunakan setelah membran osmosis balik untuk menghilangkan mikropolutan organik yang masih lolos dari membran (Kegel et al. 2010).
Karbon aktif tidak hanya dapat diintegrasikan dengan membran filtrasi sebagai adsorban, namun dapat pula dibuat menjadi membran karbon (Drozdov et al. 2008). Lee et al. (2007) berhasil membuat membran karbon dari campuran beberapa polimer, yang dikarbonisasi dengan sistem pirolisis untuk aplikasi separasi gas. Sears et al. (2010) mengkaji proses pemurnian air dan pemisahan gas dengan membran karbon yang terbuat dari karbon nanotube. Sridhar et al. (2008) membuat membran dari poly(ether-block-amide) yang digunakan sebagai matriks polimer dan karbon aktif mikro-mesopori sebagai pengisi (filler). Membran polimer-karbon ini kemudian diaplikasikan dalam proses separasi gas, dan terbukti mampu meningkatkan permeabilitas dan sifat tahanan membran terhadap gas CO2 dan CH4. Brunet et al. (2008) membuat dan mengkarakterisasi membran
dari polisulfon sebagai matriks polimer, yang dicampur dengan karbon nanotube multiwall. Penambahan karbon nanotube ternyata tidak mengganggu struktur asimetrik serta sifat permeabilitas dan hidrofobik membran, tetapi meningkatkan kekasaran permukaan membran.
2.4 Polisulfon
Polisulfon adalah polimer yang banyak digunakan sebagai bahan dasar pembuatan membran. Polisulfon memiliki ketahanan yang baik terhadap temperatur tinggi, rentang pH yang lebar 1-13, memiliki resistansi yang baik terhadap klorin, serta mudah dipabrikasi (Wenten 1999).
Gambar 7 Struktur Polisulfon
Polisulfon sering digunakan sebagai bahan pembuatan membran karena memiliki sifat kestabilan kimia yang cukup tinggi, yaitu tahan terhadap perubahan pH, daya ulur rendah, dan kekuatan tarik tinggi. Polimer ini menunjukkan sifat
amorf pada keadaan seperti gelas, stabil terhadap panas dan oksida, dan derajat polimerisasi antara 50-80. Polisulfon bersifat hidrofob atau tidak suka air, juga tidak larut dalam larutan asam maupun alkali. Kelarutan polisulfon dalam larutan alifatik rendah tetapi masih dapat larut dalam beberapa pelarut polar seperti dimetil formamida (DMF), dimetil asetamida (DMAc), dan dimetil dulfide (DMSO) yang sering digunakan dalam pembuatan membran (Kesting 1993).
Menurut Romli et al. (2006), polisulfon sebagai material dasar memiliki gugus sulfon yang merupakan sink untuk elektron-elektron, sehingga menjadikannya tahan terhadap pengaruh termal maupun oksidasi. Gugus eter pada tulang belakangnya memberikan sifat fleksibel, serta adanya gugus alkil yang dapat menaikkan permeabilitas.