KARAKTERISASI FRAKSI EKSTRAK AGF MELALUI SKRINING FITOKIMIA DAN SPEKTROSKOPI FTIR
SKRIPSI
Diajukan untuk Memenuhhi Sebagian dari Syarat untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Novi Nurlaeli
1004563
PROGRAM STUDI KIMIA DEPARTEMEN PENDIDIKAN KIMIA
KARAKTERISASI FRAKSI EKSTRAK AGF MELALUI SKRINING FITOKIMIA DAN SPEKTROSKOPI FTIR
Oleh : Novi Nurlaeli
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
©Novi Nurlaeli
Universitas Pendidikan Indonesia Oktober 2015
Hak Cipta dilindungi undang-undang.
LEMBAR PENGESAHAN
KARAKTERISASI FRAKSI EKSTRAK AGF MELALUI SKRINING FITOKIMIA DAN SPEKTROSKOPI FTIR
Oleh : Novi Nurlaeli
1004563
Disetujui dan disahkan oleh : Pembimbing I
Dr. Hendrawan , M.Si. NIP. 196309111989011001
Pembimbing II
Dr. Iqbal Musthapa, S.Pd., M.Si. NIP. 1975122310011121001
Mengetahui
Ketuan Departemen Pendidikan Kimia FPMIPA UPI
BAB I PENDAHULUAN
A. Latar Belakang
Tanaman yang berpotensi sebagai bionutrien sebagian besar memiliki kemiripan ciri-ciri tanaman, seperti daun lebat dan berwarna hijau mengkilap, memiliki bau yang khas, memiliki daya tahan yang cukup tinggi dan memiliki kandungan N, P, dan K (Taufik, I., 2011:3). Sampai saat ini bionutrien yang telah ditemukan antara lain berasal dari tanaman AGF, CAF, KPD, MHR, RPS-GE, BCS, BGI, RSR, JPR, dan ARH (Nurmala, A.R., 2013:1).
Salah satu bionutrien yang baru-baru ini dikaji adalah bionutrien dengan kode AGF. Fadlie, M., (2011) mengekstrak tanaman AGF dengan pelarut etanol, etil asetat, diklorometana, dan n-heksana. Hasil menunjukkan bahwa ekstrak tanaman AGF berpotensi sebagai bionutrien karena mengandung kadar NPK yang tinggi. Hasil analisis terhadap kadar NPK untuk ekstrak AGF etil asetat yaitu kadar nitrogen sebesar 357 ppm, kadar fosfor sebesar 930 ppm, dan kadar kalium sebesar 10,255 ppm. Berdasarkan penelitian yang telah dikaji sebelumnya, bahwa pelarut etil asetat merupakan pelarut yang dapat mengekstrak senyawa metabolit sekunder yang terdapat pada tanaman AGF yang berpotensi sebagai bionutrien
dan biopestisida (Fadlie, M., 2011:100-101). Etil asetat ialah senyawa aromatik yang bersifat semipolar dengan rumus struktur CH3CH2OC(O)CH3 sehingga dapat menarik analit-analit yang bersifat polar dan nonpolar (Snyder, 1997). Hal ini berarti pelarut etil asetat mampu menarik komponen senyawa kimia yang terkandung didalam ekstrak (Artini, P. E. U. D., dkk. 2013 : 1). Ekstrak AGF etil asetat berpotensi sebagai biopestisida karena kelompok tanaman yang diberi ekstrak AGF etil asetat tidak terserang layu dan busuk, serta menunjukkan hasil panen yang baik (Fadlie, M., 2011).
Penelitian sebelumnya menunjukkan bahwa pemisahan terbaik metabolit sekunder hasil fraksinasi pada ekstrak AGF terjadi pada eluen etil asetat dan n-heksana dengan perbandingan 3:7, yaitu dapat meningkatkan daya tahan tanaman khususnya cabai merah keriting (Nurmala, A.R., 2013 :37). Karena keberhasilan ekstrak AGF sebagai pupuk organik dan biopestisida sehingga ekstrak AGF
tersebut dianggap memiliki potensi yang sangat baik untuk dikembangkan (Nur, A.A., 2013:2). Oleh karena itu perlu adanya penelitian lanjutan untuk mengkonfirmasi hasil fraksinasi pada ekstrak AGF etil asetat dengan perbandingan etil asetat dan n-heksna 3:7 serta mengetahui senyawa metabolit sekunder dan gugus fungsi yang terkandung di dalamnya.
Penelitian ini terdiri dari tahap preparasi sampel tanaman AGF, tahap ekstraksi dengan metode maserasi padat-cair, selanjutnya tahap analisis dan karakterisasi dengan kromatografi lapis tipis (KLT), skrining fitokimia, dan spektroskopi FTIR.
B. Rumusan Masalah
Berdasarkan latar belakang yang telah dikemukakan maka rumusan masalah penelitian ini adalah :
Golongan metabolit sekunder dan gugus fungsi apa sajakah yang terkandung dalam ekstrak AGF hasil fraksinasi pada komposisi etil asetat dan n-heksana dengan perbandingan 3:7 berdasarkan skrining fitokimia, dan spekroskopi FTIR?
C. Batasan Masalah
Penelitian ini dibatasi pada fraksinasi yang dilakukan menggunakan ekstrak
etil asetat dan n-heksana dengan perbandingan 3:7. Hal ini mengacu pada penelitian terdahulu (Nurmala, A.R., 2013) yang menunjukan bahwa hasil fraksinasi ini berpotensi sebagai biopestisida. Serta analisis dan karakterisasi hanya meliputi skrining fitokimia dan spektroskopi IR.
D. Tujuan Penelitian
E. Manfaat Penelitian
Hasil yang didapatkan dari penelitian ini diharapkan :
1. Memberikan informasi mengenai metabolit sekunder dan gugus fungsi yang terkandung pada ekstrak AGF.
2. Menjadi rujukan referensi mengenai golongan metabolit sekunder dan gugus fungsi yang terdapat dalam tanaman AGF untuk peningkatan kualitas dan keefektifitasan sebagai biopestisida.
F. Struktur Organisasi Skripsi
Skripsi ini terdiri dari lima bab yang meliputi bab I tentang pendahuluan, bab II tentang tinjauan pustaka, bab III tetntang metode penelitian, bab IV tentang hasil dan pembahasan, dan bab V tentang kesimpulan dan saran. Bab I yang merupakan pendahuluan berisi tentang latar belakang penelitian, rumusan masalah, batasan masalah, tujuan penelitian, manfaat penelitian, dan sistematika penulisan. Latar belakang penelitian membahas tentang kerangka pemikiran mengenai penelitian yang dilakukan. Rumusan masalah mencakup masalah-masalah yang dimunculkan pada penelitian. Manfaat penelitian berisi tentang manfaat penelitian secara keseluruhan. Sistematika penulisan berisi tentang sistematika penulisan skripsi secara keseluruhan.
13
BAB III
METODE PENELITIAN
A. Objek dan Lokasi Penelitian
Objek atau bahan yang digunakan untuk penelitian ini adalah tanaman dengan kode AGF yang diperoleh dari daerah Cihideng-Bandung. Penelitian berlangsung sekitar 9 bulan, terhitung dari bulan November 2014 sampai Juli 2015. Penelitian ini terdiri dari tiga tahap yaitu tahap preparasi sampel, tahap ekstaksi dan pemisahan, dan tahap analiasis dan karakterisasi.
Tempat penelitian pada masing-masing tahapan berbeda-beda, antara lain : Tahap preparasi sampel, ekstraksi dan pemisahan dilakukan di Laboratorium Riset Kimia Makanan FPMIPA UPI Bandung dan di Laboratorium Institut Teknologi Bandung. Sedangkan tahap analisis dan karakterisasi dilakukan di Laboratorium Kimia Instrumen Departemen Pendidikan Kimia FPMIPA UPI Bandung.
B. Alat dan Bahan
Alat-alat yang digunakan adalah gelas kimia (200 mL, 500 mL, 1L dan 3L), gelas ukur (10 mL, 100 mL dan 500 mL), kaca arloji, timbangan digital, botol semprot, kertas saring, kertas label, spatula, batang pengaduk, plastik wraps,
alumunium foil, pipet tetes, lumpang dan alu, labu erlenmeyer 1 L, labu erlenmeyer berpenghisap, corong buchner, mantel (pemanas listrik), magnetic stirrer, set alat destilasi, set alat evaporator, pompa vakum, botol kaca 1L, botol pial 20 ml, tabung reaksi, rak tabung, penjepit tabung reaksi, pinset, chamber, set alat freeze dryer Eyela FD-5N, spektroskopi FTIR (Shimadzu 8400).
14
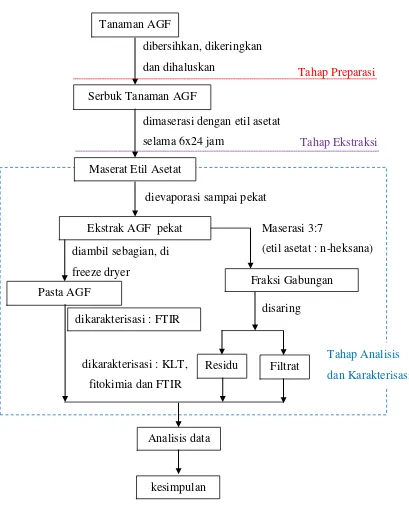
C. Prosedur Penelitian
15
Gambar 3.1. Bagan Alur Penelitian
Tahap Analisis
dan Karakterisasi dimaserasi dengan etil asetat
selama 6x24 jam
diambil sebagian, di freeze dryer
Tahap Ekstraksi
Tahap Preparasi
dibersihkan, dikeringkan dan dihaluskan
Tanaman AGF
Serbuk Tanaman AGF
Maserat Etil Asetat
dievaporasi sampai pekat
Ekstrak AGF pekat
Pasta AGF
Fraksi Gabungan
disaring
Filtrat Residu
Maserasi 3:7
(etil asetat : n-heksana)
Analisis data dikarakterisasi : KLT,
fitokimia dan FTIR
16
Uraian dari masing-masing langkah kerja adalah sebagai berikut : 1. Penyiapan Sampel Tanaman AGF
Sampel tanaman AGF yang akan digunakan dibersihkan terlebih dahulu dari kotoran seperti tanah dan tanaman parasit lain. Setelah itu dirajang kemudian dijemur sampai kering. Selanjutnya tanaman dihaluskan dengan cara ditumbuk dengan menggunakan lumpang dan alu hingga menjadi serbuk. Serbuk tanaman AGF kemudian diayak agar serbuk tersebut menjadi halus dan memiliki ukuran yang homogen sebelum dimaserasi.
2. Ekstraksi Tanaman AGF dengan Metode Maserasi
Metode yang digunakan untuk mengekstrak AGF adalah dengan metode maserasi. Metode maserasi merupakan metode ekstraksi padat-cair. Serbuk tanaman AGF ditimbang sebanyak 1,5 kg kemudian diekstraksi menggunakan pelarut etil asetat. Pelarut etil asetat yang di gunakan adalah sebanyak 9.250 mL pada hari pertama atau hingga seluruh serbuk terendam. Setelah satu hari proses perendaman, maserat kemudian disaring menggunakan corong buchner sehingga diperoleh ekstrak AGF etil asetat dan residunya. Residu yang dihasilkan di maserasi kembali dengan etil asetat sebanyak 6.035 mL. Kemudian disaring dan residu yang diperoleh di maserasi kembali dengan 5.405 mL etil asetat selama
6x24 jam. Filtrat hasil maserasi keseluruhan dipekatkan hingga menjadi 245 ml dengan menggunakan vacum rotary evaporator.
Kedalam maserat pekat yang diperoleh ditambahkan pelarut etil asetat dan n-heksana dengan perbandingan 3:7 sampai volume 500 mL, dikocok menggunakan
megnetic stirrer. Hal ini dilakukan untuk menghomogenkan ekstrak AGF tersebut. Kemudian dilakukan penyaringan dengan menggunakan corong buchner
dan hasilnya dikarakterisasi dengan metode kromatografi lapis tipis, skrining fitokimia, dan spektroskopi FTIR.
17
Kromatografi lapis tipis digunakan dalam penentuan eluen yang tepat untuk proses pemisahan (fraksinasi) dengan teknik KVC. Selain itu, KLT juga digunakan untuk menganalisis senyawa hasil pemisahan dengan KVC telah terpisah dengan baik atau telah murni.
Dalam pengerjaannya, lempeng tipis dengan silika gel 60 F245 disiapkan dengan ukuran panjang 5 cm sedangkan lebarnya 1 cm. Pada bagian atas dan bawah lempeng diberi garis atas dengan jarak 0,5 cm dari tepi lempeng. Sampel yang akan dianalisis ditotolkan pada bagian tengah garis batas bawah dengan menggunakan pipa kapiler. Lakukan penotolan berulang kali hingga cukup tebal dan dibiarkan beberapa saat agar kering. Chamber diisi dengan eluen yang akan digunakan untuk mengelusi lempeng tipis, dihomogenkan, dan didiamkan beberapa saat dengan kondisi tertutup agar chamber jenuh dengan uap eluen. Lempeng tipis yang telah disiapkan sebelumnya, kemudian dimasukan ke dalam
chamber dengan menggunakan pinset hingga bagian bawah lempeng tercelup sebagian. Lempeng tipis tersebut diletak tegak bersandar pada dinding chamber
kemudian ditutup.
4. Karakterisasi Fraksi AGF dengan skrining Fitokimia dan Spektroskopi FTIR
Karakterisasi yang di lakukan adalah dengan skrining fitokimia dan spektroskopi FTIR. Adapun langkah kerja yang di lakukan adalah sebagai berikut:
a. Karakterisasi Fraksi Ekstrak AGF dengan Skrining Fitokimia
Fraksi gabungan (FG) bionutrien AGF hasil dari tahap pemisahan, di identifikasi komponen fitokimianya dengan metode uji warna. Uji fitokimia ini bertujuan untuk mengetahui kelompok senyawa metabolit sekunder yang terkandung di dalam FG bionutrien AGF. Skrining fitokimia ini dilakukan terhadap metabolit sekunder golongan alkaloid, tanin, dan terpenoid.
Adapun prosedur kerja yang dilakukan adalah sebagai berikut : 1) Identifikasi Alkaloid
18
pereaksi mayer dan tabung reakai B ditambahkan pereaksi Wagner. Terbentuknya edapan putih mengindikasikan adanya alkaloid (Kavit Mehta, B.N. Patel, B.K. Jain,2013).
a) Pembuatan Pereaksi Mayer
Sebanyak 1 gram KI dialurkan dalam 20 mL aquades. Kemudian ditambahkan 0,2 gram HgCI2 dan diaduk hingga larut (Fadlie M., 2011). b) Pembuatan Pereaksi Wegner
Sebanyak 2,5 gram I2 dan 2 gram KI dimasukan ke dalam 10 mL aquades. Kemudian dilarutkan dan diencerkan dengan aquades hingga mencapai volume 200 mL (Diana K.M., Pringgenies D., Karna O.R., 2012)
2) Identifikasi Tanin
Sebanyak 2 mL konsentrat dicampurkan dengan 2 mL aquades. Campuran tersebut ditambahkan sedikit larutan FeCl3. Terbentuknya endapan berwarna hijau menunjukan adanya tanin (Kavit Mehta, et.al.,
2013).
3) Identifikasi Terpenoid
Sebanyak 2 mL konsentrat ditambahkan 2 mL Kloroform dan dievaporasi hingga kering. Setelah itu ditambahkan 2 mL H2SO4 dan
dipanaskan kembali selama 2 menit. Terbentuknya warna keabu-abuan menunjukan adanya terpenoid (Kavit Mehta, et.al., 2013).
b. Karakterisasi Fraksi AGF dengan Spektroskopi FTIR
28
BAB V
KESIMPULAN DAN SARAN A. Kesimpulan
Berdasarkan penelitian dan pembahasan yang dilakukan, didapatkan kesimpulan sebagai berikut :
Hasil analisis dengan skrining fitokimia menunjukan bahwa ekstrak AGF hasil fraksinasi etil asetat dan n-heksana 3:7 memiliki senyawa golongan alkaloid, terpenoid, dan tanin. Sedangkan hasil karakterisasi dengan spektroskopi IR memiliki gugus fungsi –OH, -C-H sp3, –C=O dan –C=C. Hasil pengujian spektroskopi IR mendukung hasil skrining fitokimia sehingga dapat disimpulkan bahwa senyawa alkaloid, terpenoid, dan tanin tersebut memiliki gugus fungsi –OH, -C-H sp3, –C=O dan –C=C
B. Saran
29
DAFTAR PUSTAKA
Akbar, Hendra Rizki. 2010. Isolasi dan Identifikasi Golongan Flavonoid Daun Dandang Gendis (Cinacanthus Nutans) Berpotensi Sebagai Antioksidan.
(Skripsi). Bogor : IPB.
Ballard, T. S. (2008). Optimizing the Extraction of Phenolic Antioxidant Compound from Peanut Skins. Dissertation, the Faculty of Virginia Polytechnic Institute and State University, Blacksbung, VA.
Bintang, M. (2010). Biokimia. : Teknik Penelitian. Jakarta : Penerbit Erlangga.
Clark, jim. (2007). Kromatografi Lapis Tipis. [online]. Tersedia: http://
www.chem.try.org.materi/instrumen analisis/kromatografi I/kromatografi
lapis tipis.htm. [13 Juli 2013].
Fadlie, M. (2011). Kajian Potensi Ekstrak Tumbuhan dengan Kode AGF sebagai
Bionutrien yang Diaplikasikan pada tanaman Cabai merah Keriting
(Capcisum Annum L). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia FPMIPA UPI Bandung : Tidak diterbitkan.
Guenther, E. 1987. Minyak Atsiri Jilid 1. UI Press. Jakarta.
Kastianti , N dan Amalia, Z.Q. 2008. Laporan Penelitian Pengambilan Minyak Atsiri Kulit Jeruk dengan Metode Ekstraksi Distilasi Vakum. Semarang : Jurusan Teknik Kimia Fakultas Teknik Undip.
30
Hayati, E.K, dkk. (2010). Fraksinasi dan Identifikasi Senyawa Tanin pada Daun Belimbing Wuluh (Averrhoa Bilimbi L). Jurnal Kimia Volume 4, Nomor 2, Juni 2010:193-200.
Hendayana, Sumar. (1994). Kimia Analitik Instrument. Semarang : Semarang Press.
Herbert, R.B., (1995). Biosynthesis of Secondary Metabolites, Eecond edition. New York: chapman and Hall.
Hostettmann, K., Hostettman M. Marston, A. (1995). Cara Kromatpgrafi Preparatif, Penggunaan Pada Isolasi Senyawa Alam. Bandung: ITB.
Khopar, S.M., (2003). Konsep Dasar Kimia Analitik. Jakarta: Universitas Indonsia.
Lenny, S. (2006). Senyawa Terpenoid dan Steroid. Karya Ilmiah pada De Partemen Kimia FMIPA Universitas Sumatra Utara.
Nur, Atthariq. A (2013). Isolasi dan Identifikasi Senyawa Metabolit Sekunder dalam Bionutrien AGF. Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia FPMIPA UPI Bandung : Tidak diterbitkan.
Nurmala, A. R., (2013). Fraksinasi dan Karakterisasi Ekstrak Etil Asetat AGF Serta Kajiannya sebagai Bionutrien pada Pertumbuhan Tanaman Cabai
Merah Keriting (Capcisum Annum L). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia FPMIPA UPI Bandung : Tidak diterbitkan.
31
Paniangan, Dingse., (2009). Produksi Metabolit Sekunder Alkanoid Secara In Vitro. Bandung. Unpad.pess.
Perwitasari B., tripatmasari M., Wasonowati C. (2012). Pengaruh Media Tanam dan Nutrisi Terhadap Pertumbuhan dan Hasil tanaman Pakchoi (Brassica
juncea l) dengan sistem Hidroponik. Jurnal Agrovigor Volume 5, nomor 1, Maret 2012.
Pratama, H.A (2011). Kajian Potensi Bionutrien hasil Ekstraksi Tanaman ARH dengan Variasi Tingkat Kepolaran Pelarut dan Aplikasinya pada Cabai
Merah Keriting (Capsicum annum L). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia FPMIPA UPI Bandung : Tidak diterbitkan.
Rowe, R. C., P. J. Shekey, and M. E. Quinn. 2009. Handbook of Pharmaceutical Excipients Sixth Edition. USA: Pharmaceutical Press and American Pharmacist Association.
Santosa, C. M. Dan Hertianti, T. (2005). Kandungan Senyawa Kimia dan Efek
Ekstrak Air Daun bangun-Bangun (Coleus amboinicus L) pada Aktivitas
Fagositosis Nertofil Tikus Putih. M a j Farm Indones, 16:141-148.
Stoenoiu, C.E., Bolbocoa, A. D., Jantshi, L (2006). Mobile phase Optimization for Steroid Separation. Medinformatics.
Sudarmadji S, B Haryono, dan Suhardi. 1989. Analisis untuk Bahan Makanan dan Pertanian. Yogyakarta : Liberty. 171 hal.
32
Supratman, U. (2010). Elusidasi Struktur Senyawa Organik : Metode spektroskopi untuk penentuan struktur senyawa organik. Bandung. Widya Padjadjaran.
Taufik, I. (2011). Kajian Potensi Tumbuhan BDI sebagai Bionutrien untuk Pertumbuhan dan Perkembangan Tanaman Cabai Merah Keriting
(Capcisum Annum L). Skripsi. Program Studi Kimia Jurusan Pendidikan Kimia FPMIPA UPI Bandung : Tidak diterbitkan.
USP Convention. 2007. United States of Pharmacopeia National Formulary, USP 30/ NF 25. Twinbrook Parkway: United States Pharmacopeial Convention.
Wardhani, L. K. Dan N. Sulistyani. 2012. Uji Aktivitas Antibakteri Ekstrak Etil Asetat Daun Binahong (Anredera Scandens (L.) Moq.) Terhadap Shigella
Flexneri Beserta Profil Kromatografi Lapis Tipis. Jurnal Ilmiah Kefarmasian, Vol. 2(1): 1-16.
Widiastuti, A. E. S., dkk. (2014). Skrining Fitokimia dan Identifikasi Komponen
Utama Ekstrak Metanol Kulit Durian (Durio zibethinus Murr.) Varietas
Petruk. Kimia Organik Bahan Alam. Program Studi Pendidikan Kimia Jurusan FMIPA FKIP UNS. Surakarta.
Widodo, N. (2007). Isolasi danKarakterisasi Senyawa alkalod yang Terkandung dalam Jamur Tiram Putih (pleurotus Ostreatus). Skripsi. FMIPA Universitas Negeri Semarang. Semarang.
Winarno, F. G. D. dkk. (1973). Ekstraksi Kromatografi dan Elektroforesis. Fakultas Teknologi Pertanian IPB. Bogor.