Prosiding PerteltUlan don Presentasi Ilmiah PPNY-BATAN Yogyakarta, 25-27 Apri/1995
96
Buku 11 351
PROSES KIMIA PENGOLAHAN LIMBAH KOROSIF
RADIOAKTIF DARI FABRIKASI BAHAN BAKAR NUKLIR
Zainus Salimin
PPTLR-BATAN, KawasanPuspitekSerpong, Tangerang 15310
ABSTRAK
PROSES KlM1A PENGOLAHAN LIMBAH KOROS1F RADIOAKTIF DARI FABRIKASI BAHAN BAKAR.NUKLIR. Telah dilakukan penelitian pengurangan kadarfluor dalam limbah korosif-radioaktif cair yang mengandung fluor 19430 ppm melalui metode kimia, kombinasi koagulasi-flokulasi-sedimentasi. Variasijenis koagulanyang digunakan adalah kalsium khlorida, tawas, resin WWS
116 don kombinasi resin tawas pada konsentrasiyang berbeda-beda.Percobaan pengendapan dengan
jenis don jumlah koagulan bervariasi diharapkan memberikan hasil penurunan kadar Fluor'dalam beningan sampai di bawah bolas maksimum yang diijinkall. Hasi/ percobaan menunjukkan bahwa koagulan kalsium khlorida dengan konsentrasi 1,3 mol/literpada pH 8 memberikan hasil yang terbaik, diperoleh penurunan kadar Fluor dalam limbah sebesar 99,97% sehingga kadar Fluor yang tertinggal dalam limbah menjadi 4,89 ppm yang telah memenuhipersyaratan baku mutu air buangan.
ABSTRACT
CHEMICAL PROCESS FOR TREATMENT OF CORROSIVE RADIOACTIVE WASTE FROM THE FABRICATION OF NUCLEAR FUEL. Experiments were carried out to decreasefluor concentration in corrosive radioactive liquid waste containing 19430ppm offluor by chemical methode Le. combination of coagulation, floculation and sedimentation. Calsium chloride, aluminium sulfate, resin WWS 116, and mix of aluminium sulfate and resin WWS 116 were used as chemical coagulant on variation of concentration. Theprecipitates offluor salt was separatedfrom the solution, and thanfluor concentration in solution is analyzed. The best result of optimum Fluor concentration in solution was achieved at 4.88 ppm by using of 1.3 mole/l calcium chloride coagulant at pH 8, the separationfactor is 99.97%.
PENDAHULUAN
L
imbah korosif-radioaktif daTiFabrikasi Bahan Bakar Nuklir-
Instalasi Produksi Elemen Bakar Reaktor Riset, PEBN berasal dari Unit Konversi. Limbah tersebut terbentuk ketika batao baku UF6 daD atau UOlNO3)2 dikonversikan menjadi Amonium Uranil Karbonat (AUK) yang mempunyai rumus (NH4f [UO2(CO3)r. Bila UF6 direaksikan seketika terbentuk pula garam NH4F, sementara hila UO2(CO3)2yang direaksikan akan dihasilkan pula NH4NO3.Setelah AUK dipisahkan melalui penyaringan, fiItratnya dididihkan untuk membebaskan amoniak daD karbon dioksida. Gugus uranil yang masih terkandung dalam filtrat diendapkan sebagai uranium peroksida dihidrat melalui penambahan hidrogen peroksida. Endapan dipisahkan dari larutannya melalui penyaringan, filtratnya yang mengandung komponen utama amonium fluorida kadar fluor 19.430 ppm daD kadar uranium kurang dari 50 fig/liter merupakan
limbah kimia korosif-radioaktif. Menurut perkiraan jumlah volume limbah tersebut adalah 900
liter/tatun.
Mengingat sifat korosif ion fluorida, maka perIn dilakukan pengolahan kimia terhadap limbah tersebut untuk mengendapkan fluorida. Pengolahan limbah cair yang mengandung fluorida dapat dilakukan melalui metode pengendapan kimia dengan kombinasi proses koagulasi, flokulasi daD sedimentasi, dimana zat kimia (sebagai koagulan daD flokulan) ditambahkan untuk mengikat ion Fluor sehingga terbentuk endapan. Berbagai macam batao koagulan daD flokulan ban yak digunakan, termasuk penggunaan bahan elektrolit. Keuntungan daTiproses koagulasi adalah mampu menangani berbagai kandungan bahan dalam umpan. Koagulasi kimia termasuk destabilisasi, pembentukan agregasi, daD ikatan bersama dari koloid. Koloid ini membentuk gumpalan kimia (flok) yang mengadsorpsi, menangkap atau membawa bersama suspensi padat yang actadalam limbah cair.(I,3)
352 Buku Il
Prosiding PertenUlan dun Presentasi Ilrmah PPNY-BATAN Yogyakarta, 25-27 April 1995
Ada 3 (tiga) langkah dalam proses koagulasi clanflokulasi:
1. Penambahan zat koagulasi ke alam limbah cair Agar zat kimia terbagi secara merata dalam waktu seketika perlu pengadukan yang cepat, hat ini guna menghindari reaksi kimia awal hanya terlokalisasi pacta titik pemberian zat koagulasi (koagulasi hanya tersebar secara perlahan).
2. Terjadinya proses koagulasi
Koagulasi terjadi karena reaksi kimia maupun kimia fisik yang kompleks clan perubahan terjadi mengarah ke pembentukan endapan padat yang halos.
3. Pembentukan flokulasi
Dengan cara pengadukan perlahan-Iahan, flokulasi terjadi karena partikelpartikel yang halos berhubungan clan kontak satu sarna lainnya membentuk gumpalan yang lebih besar, yang kemudian mengendap dengan membawa serta material koloidal yang terdapat dalam tarutao dengan cara pengikatan secara mekanis, adsorpsi dari koloid dengan gumpalan, clan netralisasi dari muatan listrik positif benda koloidal dengan muatan negatif dari gumpalan. Terjadinya flokulasi clan koagulasi dipengaruhi oleh kotoran kimia ("chemical impurities"), pH larutan, kekuatan ion, temperatur, tingkatan pencampuran clan flokulasi, clan adanya suspensi padat dalam cairan yang bertindak selaku inti untuk pengendapan.
TATAKERJA
Bahan yang dipakai
-
Limbah korosif~radioaktif cair kadar fluor19.430ppm - NaOHpadat - NatriumSitrat - HC125%
- CaCh
- Ah(SO4)3 18H2O - Aluminiumfoil -Kertas saring - Resin WWS 116Alat yang dipakai
-
Beaker glass-
Corong gelas-
pengaduk Magnit -Pipet ukur -Pro-pipet -pH meter - Batang pengaduk- Spatula
- Neraca analitik- Labuukur
- Cawan petri - Pipet tetes - Ion Analyzer merk Coming MetodeKe dalam limbah korosif-radioaktif cair yang mengandung Fluor ditambahkan bahan kimia sebagai koagulan clan flokulan untuk membentuk endapan. Dengan pengadukan cepat bahan kimia akan tercampur merata dengan cairan clan membentuk endapan. Melalui pengadukan lambat endapan akan bergabung membentuk gumpalan-gumpalan yang lebih besar yang akan mengendap dengan cepat. Melalui proses sedimentasi beningan dipisahkan dari endapannya, dianalisa kadar Fluor dalam beningan dengan menggunakan " Ion Analyzer ". Faktor perubah yang digunakan adalah jenis clankonsentrasi bahan koagulan. lenis bahan koagulan yang dipakai meliputi CaC b, Tawas clan Bahan Elektrolit Polirner Resin WWS 116.
Percobaan Pengendapan dengan Koagulan CaCh
1. Optimasi pH
Ke dalam beaker glass dimasukkan limbah korosif-radioaktif cair kadar Fluor 19.430 ppm sebanyak 50 ml
pH larutan diukur dengan menggunakan pHmeter (pH larutan awal 1,5)
Ditambahkan NaOH/HCI untuk mendapatkan pH limbah sebesar 6
Ke dalam limbah tersebut ditambahkan koagulan CaCh sebanyak 0,5 mole/I, kemudian diaduk. Pengadukan cepat (500 rpm) selama 5 menit, pengadukan lambat (250 rpm) selama 55 menit.
Limbah diendapkan, lain disaring dengan kertas saring
Beningan yang sudah disaring dari endapan diambil untuk dianalisa kadar Fluomya dengan menggunakan tarutao buffer Natrium Sitrat Pekerjaan tersebut di atas diulangi untuk pH 7, 8, 10 clan 12
Optirnasi pH diambil yang memberikan kadar Fluor dalam beningan paling rendah
2. Koagulasi clan tlokulasi
50 ml limbah mentah diatur pH-nya sesuai optirnasi pH yang telah diperoleh
Ke dalam lirnbah tersebut ditambahkan CaCh sebanyak 0,7 mole/l
Dilakukan pengadukan cepat (500 rpm) selama :!: 5 men it, dilanjutkan dengan pengadukan lambat (250 rpm) selama:!: 55 menit
Limbah kemudian didiamkan hingga terbentuk endapan
Prosiding Pertemuan dun Presentasi l/miah
PPNY-BATAN Yogyakarta, 25-27 April 1995 Buku II 353
2.
Endapan dipisahkan dari beningan melalui penyaringan, kemudian beningan dianalisa kadar fluomya
Prosedur di atas diulangi kembali untuk konsentrasi CaCh 0,1 moUI,0,3 moUI
Percobaan Pengendapan dengan Koagulan Tawas
Ke dalam 50 ml limbah mentah ditambahkan NaOH secukupnya hingga pH limbah mencapai
10,57
Kemudian ke dalamnya dimasukkan Tawas sebanyak 2,5 g
Limbah diaduk cepat (500 rpm) selama :!: 5 men it dan dilanjutkan dengan pengadukan lambat (250 rpm) selama:!:55 menit
Limbah kemudian didiamkan hingga terbentuk endapan
Beningan dipisahkan dari endapannya melalui penyaringan dan dianalisa kadar fluornya menggunakan larutan buffer Natrium Sitrat Prosedur di atas diulangi untuk konsentrasi
Tawas3 g/50ml, 3,5g/50ml,9g/50ml, 109/50
ml, 11g/50ml, 12g/50ml, 12,5g/50ml
Percobaan Pengendapan dengan Koagulan Resin WWS116
Ke dalam 50 ml limbah mentah ditambahkan NaOH secukupnya sehingga pH limbah mencapai 7 (netral) Kemudian ke dalamnya dimasukkan Resin WWS 116sebanyak 0, I ppm Limbah diaduk dengan kecepatan pengadukan
400 rpm selama 1 jam Limbah didiamkan
hingga mengendap, lalu disaring
Beningan dianalisa kadar fluornya dengan menggunakan larutan buffer Natrium Sitrat Prosedur di atas diulangi untuk konsentrasi Resin WWS 116I ppm, 2 ppm, 3 ppm, 3,5 ppm, 4ppm
4. Percobaan Pengendapan dengan Koagulasi Kombinasi Resin dan Tawas
3.
Ke dalam 50 ml limbah mentah ditambahkan NaOH secukupnya hingga pH limbah mencapai
10,57
Kemudian ke dalam limbah terse but ditambahkan Tawas 10 g, lalu diaduk dengan kecepatan 700 rpm selama :!:5 menit
Kemudian ditambahkan Resin 0,05 ppm, lalu diaduk dengan kecepatan 400 rpm selama :!:55 menit
Limbah didiamkan hingga mengendap, lalu disaring
Beningan dianalisa kadar fluornya dengan menggunakan larutan buffer Natrium Sitrat
Prosedur di atas diulangi untuk kombinasi Resin-Tawas 0,05 ppm: 12,g, 0,05 ppm: 12,5 g, 0,25 ppm: 10 g, 0,25 ppm: 12g, 0,25 ppm: 12,5 g, 0,5ppm: 10g,0,5ppm: 12g,0,5ppm: 12,5g
HASIL DAN PEMBAHASAN
1. HasH daD Pembahasan Percobaan Pengendapan dengan Koagulan CaCh Kadar Tetap 0,5 mol/llarutan limbah, Pada Variasi pH 6,7,8, 10 daD 12
Gambar1 menunjukkanhubungan kadar
fluor dalam beningan yang diperoleh dari proses pengendapan menggunakan 3,675 g CaCI2/50 ml larutan limbah dengan variasi pH.
Pacta Gambar1terlihat bahwa semakin
tinggi pH larutan semakin sedikit kadar fluor dalam beningan (semakin banyak fluor yang mengendap) sampai kadar minimum fluor dalam beningan 55,3 ppm pacta harga pH 8. Kadar fluor mula-mula 19.430 ppm, jadi pacta keadaan ini kadar fluor mengalami penurunan 99,72%. Hal tersebut disebabkansemakin pH naik (larutan semakin basa) maka semakin memberikan dorongan terjadinya ionisasi molekul NH4F dan CaCh sehingga terjadi reaksi pembentukan endapan CaF2 yang lebih banyak.
2NH4F + CaCh
-
CaF~+ 2NH4CI (1)(2)
2 J\'H4++ 2 F- + 2 Ca2+ + 2 cr
-
CaF;r 2 NH4CI400KadarFluDIIppml
0
5 9
pH
10 11 12 13
Gambar1. Hubungan antara kadar fluor do/am beningan yang dipero/eh daTi proses pengendapan menggunakan koagulan CaCh kadar tetap 0,5 mol/l larutan limbah pada variasi pH 6, 7, 8, 10 don 12
354 Bilk" II
Prosiding Pertemuan dan Presentasi llmiah PPNY-BATAN Yogyakarta, 25-27 April 1995
Dari Gambar } terlihat pactaharga pH lebih besar dari 8, kadar fluor dalam beningan naik kembali. Hal tersebut disebabkan karena pacta larutan yang semakin basa endapan CaF2 yang terbentuk menjadi larut kembali. Pacta pH larutan yang semakin basa terjadi persainganantar ion F daD ion OH- yang jumlahnya semakin banyak, sehingga Ca2+lebih eenderung berikatan dengan OH' untuk membentuk Ca(OH)2
2. HasH daD Pembahasan Percobaan Pengen-dapan dengan Koagulan CaCh Kadar Bervariasi Pacta pH Larutan 8
Gambar 2 menunjukkan hubungan kadar fluor dalam beningan yang diperoleh dari proses pengendapan menggunakan koagulan Kalsium Khlorida.
Pacta Gambar 2 tersebut terlihat bahwa semakin ban yak jumlah koagulan CaC h yang ditambahkan memberikan kadar fluor dalam beningan yang semakin keeil. Hal ini disebabkan karena dengan semakin besarnya konsentrasi CaCh maka semakin banyak CaCh yang terurai menjadi Ca2+daD 2 cr. Berdasar kan persamaan (2), Ca2+ yang terurai dari CaCf akan berikatan dengan ion Fyang actadalam limbah eair membentuk endapan CaF2. Jadi semakin banyak koagulan CaC}2yang ditambahkan maka endapan CaF2 yang terbentuk juga semakin banyak, sehingga kadar fluor dalam
beningan akan semakin keeil. 10Kaduflior !ppmlx 1000 8~--- 6~--~---
4~---4--
---0 0 0.5 1 1.5Kolmtrasi [alsi.1I Kilorida (mole/l!
Hubungan kadar fluor dalam beningan yang diperoleh daTi proses pengendapan dengan koagulan CaCh kadar bervariasi pada pH larutan 8
Dari pereobaan pengendapan dengan menggunakan koagulan CaCh, kadar fluor minimum yang terdapat dalam beningan dapat meneapai 0,65 ppm yang berarti mengalami penurunan sebesar 99,99 %
.
Berdasarkan Baku Mutu Air golongan D (yaitu penggunaan keperluan pertanian, usaha perkotaan, industri, listrik tenagaGambar2.
air, daD lain-lain) kadar fluor yang dii jinkan maksimal 5 ppm. Dari basil percobaan, dengan penambahan CaCh sebanyak },3 mol /1pactapH 8 kadar fluor dalam beningan dapat diturunkan sampai 4,89 ppm dengan pernellpenurunan sebesar 99,97%. Hasil ini telah memenuhi persyaratan Baku Mutu Air tersebut.
3. HasH daD Pembahasan Percobaan Pengen-dapan dengan Koagulan Tawas Kadar Bervariasi Pacta pH Larutan 10,57
Gambar 3 menunjukkan hubungan kadar fluor dalam beningan yang diperoleh dari proses pengendapan dengan koagulan Tawas kadar bervariasi. 4~ ~---3~ ~--- I~---0 0 4 6 8 10
Kouellrasi Tawas (g/50 mil
12 14
Gambar 3. Hubungan kadar fluor dalam
beningan yang diperoleh daTi proses pengendapan dengan
koagulan Tawaskadar bervariasi padapH larutan10,57
Pacta Gambar 3 tersebut terlihat bahwa semakin banyak jumlah koagulan Tawas yang ditambahkan memberikan kadar fluor dalam beningan yang semakin keeil (semakin banyak fluor yang mengendap). Hal ini dapat dijelaskan sebagai berikut:
Dengan menambahkan koagulan tawas ke dalam larutan, partikel-partikel di dalam larutan akan saling tarik-menarik sehingga partikel menjadi tidak stabil daD terjadi pengendapan. Endapan AI(OH)3 akan menarik ion F dalam larutan sehingga terperangkap dalam endapan tersebut. Penggunaan koagulan tawas yang semakin banyak akan memberikan endapan AI(OH)3yang semakin banyak, sehingga ion F dalam beningan juga akan semakin berkurang.
Dari basil pereobaan ini diperoleh penurunan kadar fluor yang acta dalam beningan hingga 92,2 ppm dengan penambahan tawas 12,5
g/50 ml limbah. Pacta keadaan ini kadar fluor
Prosiding Pertemuan dun Presentasi Ilmiah
PPNY-BATAN Yogyakarta, 25-27 April 1995 Buku Il 355
belum memenuhi persyaratan batas maksimum kadar fluor dalam beningan yang diijinkan. Jika dibandingkan dengan percobaan pengendapan menggunakan koagulan CaCh maka pemakaian koagulan tawas belum memberikan basil yang optimum.
4. HasH clan Pembahasan Percobaan Pengen-dapan dengan Koagulan Resin WWS 116 Kadar Bervariasi Pada pH larutan 7
Gambar 4 menunjukkan hubungan kadar fluor dalam beningan yang diperoleh dari proses pengendapan dengan koagulan resin WWS 116 kadar bervariasi pactapH larutan 7.
Pacta Gambar 4 tersebut terlihat bahwa penggunaan koagulan resin tidak menunjukkan grafik yang stabi!. Dengan dosis pemakaian resin
dari 0,1
-
3 ppm, Gambar 4 cenderung menunjukkanpenurunan, yang berarti bahwa semakin banyak jumlah koagulan resin WWS 116 yang
ditambahkan semakin kecil kadar fluor dalam beningan sampai kadar minimum 653,24ppm. Pacta keadaan ini kadar fluor mengalami penurunan sebesar 99,64%. Hal ini dapat dijelaskan bahwa resin WWS 116 sebagai polielektrolit kationik dapat merupakan penghubung diantara partikel membentuk flokulan yang besar sehingga terjadi pengendapan clan memberikan kadar fluor dalam beningan yang semakin keci!.
3500Kldl!Fllo!lppml 3000"" 2500I ', -2000""- - - -~ 1500r ; -1000""~ 500"" -0 0 I 2 3 4
Komllflsi ResilWWS 116Ippml Gambar4. Hubungan kadar fluor dalam
beningan yang diperoleh daTi proses pengendapan dengan koagulan Resin WWS 116 kadar bervariasi pada pH larutan 7
Pacta Gambar 4 juga terlihat bahwa penggunaan koagulan resin WWS 116di luar dosis pemakaian yang dianjurkan (koagulan yang berlebihan) sudah tidak efektif lagi untuk menurunkan kadar fluor dalam beningan. Hal ini disebabkan karena koagulan yang berlebihan akan mengurangi terjadinya agregasi clan suspensi
terdispersi membentuk gumpalan-gumpalan kecil clanpartikel-partikel individu yang stabi!.
5. HasH clan Pembahasan Percobaan Pengen-dapan dengan Koagulan Kombinasi Resin WWS 116
-
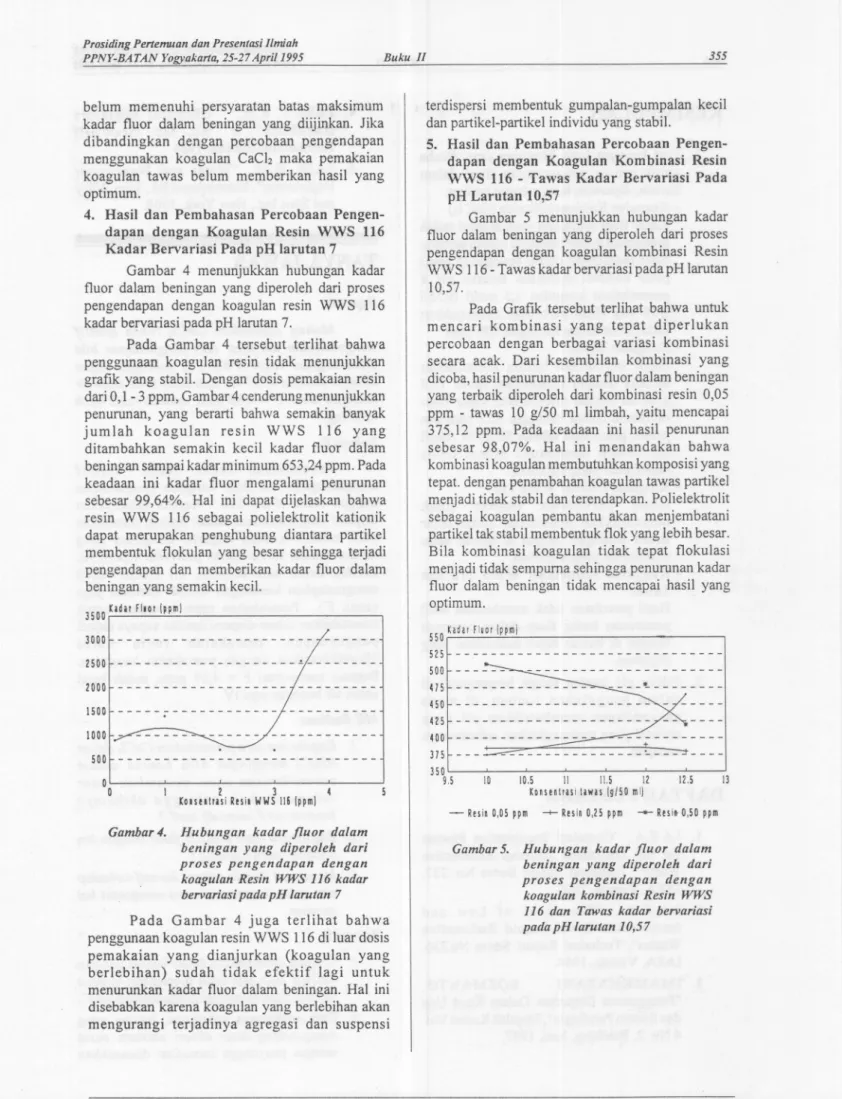
Tawas Kadar Bervariasi Pada pH Larutan 10,57Gambar 5 menunjukkan hubungan kadar fluor dalam beningan yang diperoleh dari proses pengendapan dengan koagulan kombinasi Resin WWS 116
-
Tawas kadar bervariasi pacta pH larutan10,57.
Pacta Grafik tersebut terlihat bahwa untuk mencari kombinasi yang tepat diperlukan percobaan dengan berbagai variasi kombinasi secara acak. Dari kesembilan kombinasi yang dicoba, hasilpenurunan kadar fluor dalam beningan yang terbaik diperoleh dari kombinasi resin 0,05 ppm
-
tawas 10 g/50 ml limbah, yaitu mencapai 375,12 ppm. Pacta keadaan ini basil penurunan sebesar 98,07%. Hal ini menandakan bahwa kombinasikoagulan membutuhkan komposisi yang tepat. denganpenambahan koagulan tawas partikel menjadi tidak stabil clanterendapkan. Polielektrolit sebagai koagulan pembantu akan menjembatani partikel tak stabilmembentuk flok yang lebih besar. Bila kombinasi koagulan tidak tepat flokulasi menjadi tidak sempuma sehingga penurunan kadar fluor dalam beningan tidak mencapai basil yang optimum. 550Kadarfluor Ippmi 515""- - - --500 475 450 415 400 375 350 9,5 ~ ~----10,5 II 11,5 12 KonsentrlsitlwlSjg/50mli-ResiI0,05ppm -+-ResinO,25ppm -+-ResiItO,50ppm
10 11,5 13
Gambar 5. Hubungan kadar fluor dalam beningan yang diperoleh daTi proses pengendapan dengan
koagulan kombinasi Resin WWS
116 dan Tawas kadar bervariasi
356
KESIMPULAN
1. Dari keempat jenis koagulan yang dicoba untuk proses pengendapan fluor dalam limbah, diperoleh hasil sebagai berikut:
-
Koagulan Kalsium Khlorida (CaCI2)Kadar fluor minimum yang dicapai sudah memenuhi syarat berada di bawah ambang batas maksimum dalam buangan (5 ppm) pacta kondisi optimum larutan pH 8 penambahan koagulan 1,3 molll (9,555
g/50 ml). Hasil percobaan menunjukkan
kadar fluor dalam beningan 4,89 ppm.
-Koagulan Tawas
Hasil percobaan belum memuaskan
dimana dengan konsentrasi tawas12,5
g/50ml limbah memberikankadar fluor
minimum dalam beningan 92,2 ppm clan persen penurunan sebesar 99,53 % . Hasil ini belum memenuhi syarat batas maksimum yang diijinkan.
- Koagulan Polimer WWS 116
Hasil percobaan limbah tidak menunjukkan penurunan kadar fluor dalam beningan sampai di bawah batas maksimum yang diijinkan.
- Koagulan Kombinasi WWS 116 clan Tawas
Hasi1 percobaan tidak memberikan hasil penurunan kadar fluor dalam beningan sampai di bawah batas maksimum yang diijinkan.
2. Faktor pH 1arutan sangat berpengaruh di dalam pengolahan limbah, di mana pengendapan membutuhkan pH yang optimal yang memungkinkan terbentuknya endapan.
DAFTAR PUSTAKA
1. LA.E.A., "Chemical Precipitation Process for the Treatment Aqueous Radioactive Waste", Technical Report Series No. 337, IAEA, Vienna, 1992.
2. I.A.E.A., "Treatment of Low and Intermediate-Level Liquid Radioactive Wastes", Technical Report Series No.236, IAEA, Vienna, 1984.
3. IMAMKHASANI SOEMANTO,
"Penggunaan Dispersan Dalam Ketel Uap clanSietem Pendingin", Majalah KorosiVol. 4 No.2, Bandung, Juni, 1992.
Buku /I
Prosiding Pertemuan dan Presentasi Ilmiah PPNY-BATAN Yogyakarta, 25-27 April 1995
4. PERRY, R.H., " Chemical Engineers Handbook", 6'" ed, Me. GrawHill International Edition, 1984
5. FAIR, G.M., "Water and Wastewater Engineering", International Ed., John Wiley and Sons Inc., New York, 1968.
TANYAJAWAB
Supardi
Mohon dijelaskan CaCl2 lebih efektif mengendapkan ion fluor dari pengendapan hila dibandingkan resin WWS 116 sehingga dapat dicapai efisiensi 99,97 %. Apa betul baku mutu air buangan untuk F = 4,89 ppm, apakah tidak lebih kecillagi ?
Zainus S
Penambahan CaCh lebih efektif mengendapkan ion fluor daripada pengendapan dengan resin WWS 116. Karena kebanyakan dispersi yang ditemukan dalam limbah distabilkan oleh muatan-muata~ negarif, koagulan yang dipakai adalah kation-kation polivalen seperti AI, Fe(III), Fe(II) atau kalsium, ini efektif seI(ali mengendapkan kandungan limbah (berlaku juga untuk F). Penambahan resin bertujuan untuk menstabilkan sistem dispersi larutan supaya teIjadi pengendapan, pemakaian rediD harus dikombinasikan dengan pemakaian koagulan. Batasan konsentrasi F = 4,89 ppm, sudah betul untuk air buangan rope IV.
ME Budiono
1. Bagaimana carapenambahan CaCl2dalam
NH4CI mengingat hila bentuk dalam cairan/larutan akan menambah besar volume limbah, sehingga akibatnya konsentrasi F. menjadi kedl ?
2. Bagaimana cara analisis fluor dengan ion
analyzer merk Corning?
3. Mengingatflorida sangat korosif terhadap
alar gelas, bagaimana cara mengatasi hal tersebut.
Zainus S
1. Ch yang ditambahkandalam bentuk padatan CaCh.2 H2O,jadi tidak menambah volume limbah, tidak mengurangi konsentrasi ion F'. 2. Cara analisisnya sederhana, larutan yang mengandung fluor diberi natrium sitrat sebagai penyangga kemudian dimasukkan
Prosiding Pertemuan don Presentasi 11miah PPNY-BATAN Yogyakarta, 15-17 April 1995
ke alat ion analyzer (yang telah dipasang elektroda). daTisistem alat tersebut, kita tinggal melakukan pembacaan.
3. Analisa tarutao/raw material dari PEBN perlu pengenceran terlebih dahulu mencegah korosifitasnya, untuk larutan yang encer dianalisa langsung dengan alat tersebut.
lndro Yuwono
1. Limbah radioaktif fluor adalah daTi campuran U, denganpengendapan apakah U nya juga ikut mengendap, hila tidak, harga 4,89ppmjluor masih mengandung U. Apakah bisa dibuang ke lingkungan ?
2. Berapa bolas maksimum kemampuan evaporator untuk kandunganfluor?
Zainus S
I. Dengan pengendapan, uranium juga akan ikut mengendap berdasar reaksi :
NH4 -IUO2(CO3)l + CaCh
-
CaIUO2(CO3)!2/ NH4CIJadi dalam pengendapan fluor sebagai CaF2 juga akan mengendap ion uranil karbonat,
tetapi ini tidak kami tinjau.
Buku JI 357
2. Evaporator PTPLR tidak dirancang untuk mengevaporasi limbah yang mengandung fluor.
St. Bambang G
I. Pada soot terjadinya kompetisi antara ion OH don cr terhadap ion Ca2+,ternyata justru terbentuk produk yang larut. lni berarti terjadi pembentukan CaCI2. Mengapa justru terbentuk CaCI2,padahal sifat kekomplekan ion antara OH don cr lebih besoT OH ?
2. Pada proses pengendapan florida daTi campuran (NHJ' + U) digunakan CaCI2. Apakah reaksi pertukaran antara ion CD terhadap ion F dapat terjadi dengan baik don sempurna. Mengingat sifat kimia florida lebih oksidator dibandingkan
klorida ?
Zainus S
1. Kompetisi ion F clan ion OH- (ion OB" jumlahnya lebih banyak) akan mendorong
Ca2+bereaksi dengan OB" membentuk Ca(OH)2
2. Sesuai dengan teori (literatur) clan sudah dipraktekkan CaCh akan bereaksi dengan NH4Fmembentuk CaF2,1'