PREFORMULASI DAN UJI TOKSISITAS AKUT Mg/Al
HIDROTALSIT HASIL SINTESIS DARI
BRINE WATER
SEBAGAI SEDIAAN ANTASIDA
Disusun oleh :
Muriah Dwi Budiarti
M0307057
SKRIPSI
Diajukan untuk memenuhi sebagian
persyaratan mendapatkan gelar Sarjana Sains
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SEBELAS MARET
SURAKARTA
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi saya yang berjudul
“PREFORMULASI DAN UJI TOKSISITAS AKUT Mg/Al HIDROTALSIT
HASIL SINTESIS DARI BRINE WATER SEBAGAI SEDIAAN ANTASIDA” ini
adalah benar-benar karya saya sendiri dan tidak terdapat karya yang pernah
diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan
sepanjang sepengetahuan saya juga tidak terdapat kerja atau pendapat yang ditulis
atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah
ini dan disebutkan dalam daftar pustaka.
Surakarta, Juli 2012
commit to user
PREFORMULASI DAN UJI TOKSISITAS AKUT Mg/Al
HIDROTALSIT HASIL SINTESIS DARI BRINE WATERSEBAGAI
SEDIAAN ANTASIDA
MURIAH DWI BUDIARTI
Jurusan Kimia. Fakultas MIPA. Universitas Sebelas Maret
ABSTRAK
Telah dilakukan penelitian tentang preformulasi dan uji toksisitas akut Mg/Al hidrotalsit dari brine water sebagai sediaan antasida. Penelitian ini bertujuan untuk mengetahui karakterisasi kimia fisika, kapasitas penetralan asam dan potensi toksisitas akut dari Mg/Al hidrotalsit. Mg/Al hidrotalsit dengan anion karbonat disintesis dengan perbandingan mol Mg/Al = 2꞉1 pada temperatur 70 ºC, pH 10 selama 1 jam.
Karakterisasi material hasil sintesis menggunakan XRD menunjukkan basal spacing d0037,78 Å yang merupakan Mg/Al hidrotalsit dengan anion antar
lapis karbonat. Hasil karakterisasi FTIR yang menunjukkan adanya gugus hidroksil pada bilangan gelombang sekitar 3471 cm-1 dan gugus karbonat pada 1369 cm-1. Puncak endotermis TG/DTA menunjukkan pelepasan gugus hidroksil pada suhu 235 ºC dan gugus karbonat pada suhu 420 ºC. Luas permukaan 43,104 m2/g dengan rata-rata jari pori 85,841 Å. Hasil penelitian menunjukkan berat jenis nyata 1,09 g/mL, berat jenis benar 1,82 g/mL, berat jenis mampat 1,49 g/mL, porositas 40%, kompresibilitas 27,15%, faktor hausner 1,37, kelarutan dari pH 1 sampai pH 3 yaitu 45,2%; 9,3%; 7,8%; dan kadar air 16,01%. Uji kapasitas penetralan asam pada tiga fraksi H1(100 mesh), H2(150 mesh), H3(180 mesh)
diperoleh 7,33; 8,20; 8,15 mEq. Uji toksisitas akut menunjukkan harga LC50 >
1000 µg/mL, menandakan Mg/Al hidrotalsit hasil sintesis tidak bersifat toksik.
PREFORMULATION AND DETERMINATION ACUTE
TOXICITY OF Mg/Al HYDROTALCITE FROM BRINE WATER AS
ANTACID DOSAGE
MURIAH DWI BUDIARTI
Department of Chemistry. Mathematic and Science Faculty
Sebelas Maret University
ABSTRACT
The research of preformulation and determination acute toxicity Mg/Al hydrotalcite from brine water and its potential as material antacid dosage has done. This research aims to synthesize Mg/Al hydrotalcite from brine water and do a characterization chemical physic to determine the characteristic of Mg/Al hydrotalcite as antacid dosage. Mg/Al hydrotalcite with carbonate anion synthesized with mole ratio of Mg/Al = 2/1 at a temperature of 70 ºC, pH 10 for 1 hour.
Characteristic of material synthesized with XRD showed basal spacing d0037,78 Å which indicate of Mg/Al hydrotalcite with interlayer carbonate anion.
While the presence of functional group is verified by FTIR indicated hydroxyl groups at wave number 3471 cm-1 and the carbonate group at 1369 cm-1. Endothermic of TG/DTA showed the release of the hydroxyl group at 235 ºC and carbonate at 420 ºC. surface area of Mg/Al hydrotalcite as 43.104 m2/g with pore radius 85.841 Å. Preformulation showed true density 1.82 g/mL, bulk density 1.09 g/mL, tapped density 1.49 g/mL, porosity 40%, hausner factor 1.37, compressibility 27.15%, moisture content 16.01% and solubility at pH 1= 45.2%, pH 2 = 9.3%, pH 3 = 7.8%. Acid Neutralizing Capacity (ANC) test on three fraction H1 (100 mesh), H2 (150 mesh), H3 (180 mesh) showed 7.33, 8.20, 8.15
mEq. Determination acute toxicity showed value LC50 > 1000 µg/mL indicating
that Mg/Al hydrotalcite has not toxic.
Key words꞉ Mg/Al hydrotalcite, brine water, preformulation, antacid, acid
commit to user
MOTTO“ Jadikanlah sabar dan sholat sebagai penolongmu, sesungguhnya Allah
bersama orang-orang yang sabar”
(Q.S. Al Baqoroh : 153)
“Kita dilahirkan dengan otak yang dilindungi oleh tulang tengkorak.
Meski tampak sangat miskin, tapi sesungguhnya kita kaya karena tidak ada
seorangpun yang dapat mencuri otak kita”
(Author Unknown)
“Tidak ada seorangpun dapat kembali ke masa lalu untuk membuat
suatu awal yang baru. Namun, setiap orang dapat memulai saat ini untuk
membuat suatu akhir yang baru”
(Author Unknown)
“Dan setangkai daun yang terjatuh pun sudah tertulis dalam takdir-Nya,
maka percayalah bahwa segala sesuatu yang terjadi adalah yang terbaik
meskipun bukan yang terindah”
(Author Unknown)
“Jarak paling dekat antara problem dengan solusi adalah sejauh jarak
antara lutut dengan lantai untuk bersujud”
PERSEMBAHAN
Alhamdulillahi Robbil ‘Alamiin, segala puji bagi Allah SWT untuk setiap
langkah yang telah terlampaui. Karya kecilku ini adalah sebuah
persembahan sederhana untuk :
Bapak & Ibu tercinta
Yang tak pernah lelah mencurahkan kasih sayang, do’a dan segala
perjuangan mulia yang tanpa pamrih. Semoga aku bisa seperti yang Bapak Ibu
harapkan. Amiin.
Keluarga kecilku
Suamiku yang selalu membuatku tersenyum bahagia dan memberiku
semangat saatku lelah, untuk Brilliandika Rafa Kharismaputra yang selalu aku
commit to user
KATA PENGANTARPuji syukur kehadirat Allah SWT atas segala rahmat dan anugrah yang tak
pernah berhenti. Segala pujian kepadaNya yang telah mengaruniakan keselamatan
kepada kita hingga akhir jaman.
Skripsi ini disusun dalam rangka memenuhi persyaratan untuk
memperoleh gelar sarjana di Jurusan Kimia Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sebelas Maret, Surakarta. Dalam penyusunan
skripsi ini banyak sekali bantuan, bimbingan, arahan dan petunjuk yang diberikan
kepada penulis sehingga dapat terselesaikan dengan baik. Oleh karena itu, penulis
ingin mengucapkan terima kasih kepada :
1. Bapak Drs. Ari Handoko, Ph.D., Dekan FMIPA UNS Surakarta.
2. Bapak Dr. Eddy Heraldy, Msi., Ketua Jurusan Kimia FMIPA serta
pembimbing I atas bantuan, arahan dan kesabarannya dalam membimbing
penyusunan skripsi ini.
3. Bapak Ahmad Ainurofiq, M.Si., Apt. selaku Ketua Program Studi Farmasi
FMIPA UNS dan sebagai pembimbing II.
4. Bapak I.F. Nurcahyo, MSi., Dosen Pembimbing Akademik dan Ketua
Laboratorium Kimia Dasar.
5. Seluruh Dosen di Jurusan Kimia, FMIPA UNS yang ikut membantu dalam
menyusun skripsi ini.
6. Semua teman-teman kimia, dan pihak-pihak yang tidak bisa penulis
sebutkan satu persatu.
Penulis menyadari bahwa laporan penelitian ini masih sangat jauh dari
sempurna. Oleh karena itu, penulis senantiasa mengharapkan saran dan kritik
yang membangun bagi kesempurnaan laporan penelitian ini. Penulis berharap
semoga laporan penelitian ini dapat memberikan manfaat bagi semua pihak.
Surakarta, Juli 2012
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN ABSTRAK ... iv ar Belakang Masalah ... 1
commit to user
akterisasi dan analisis hidrotalsit ... 11
4...Pre
formulasi Mg/Al hidrotalsit ... 15
5...Uji
toksisitas ... 17
6...Met
ode Brine Shrimp Lethality Test... 20
7...Ka
mpat dan Waktu Penelitian ... 23
C...Ala
t dan Bahan ... 23
D....Pro
sedur Penelitian ... 24
1...Pe
2....Uji
preformulasi ... 25
3...Uji
kapasitas penetralan asam ... 27
4...Uji
toksisitas akut ... 27
E...Tek
nik Pengumpulan Data ... 27
F...Tek
nik Analisa Data ... 28
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN
A....Sint
esis Mg/Al Hidrotalsit dari Brine Water ... 30
B...Kar
akterisasi Mg/Al Hidrotalsit ... 32
1...An
alisis struktur Mg/Al hidrotalsit dengan XRD ... 32
2....Anali
sis gugus fungsi Mg/Al hidrotalsit dengan FTIR ... 34
3...An
alisis luas permukaan Mg/Al hidrotalsit dengan SAA ... 36
4...An
alisis termal Mg/Al hidrotalsit dengan TG/DTA ... 38
C...Pre
formulasi Mg/Al Hidrotalsit ... 39
D...Uji
Toksisitas Mg/Al Hidrotalsit Terhadap Artemia Salina... 44
E....An
alisis Kapasitas Penetralan Asam ... 47
commit to user
A....Kes
impulan ... 49
B...Sar an ... 49
DAFTAR PUSTAKA ... 50
DAFTAR TABEL Tabel 1. Perbandingan komposisi kimia air laut dan brine water... 7
Tabel 2. Gugus fungsi Mg/Al hidrotalsit ... 13
Tabel 3. Nilai refleksi bidang Mg/Al hidrotalsit ... 33
Tabel 4. Tabulasi gugus fungsi Mg/Al hidrotalsit ... 34
Tabel 5. Data analisa luas permukaan Mg/Al hidrotalsit ... 36
Tabel 6. Preformulasi Mg/Al hidrotalsit sediaan farmasi ... 40
Tabel 7. Pengaruh variasi konsentrasi Mg/Al hidrotalsit terhadap larva Artemia SalinaLeach ... 45
DAFTAR GAMBAR
Gambar 1. Struktur skematis senyawa serupa hidrotalsit ... 8
Gambar 2. Struktur skematis senyawa hidrotalsit ... 8
Gambar 3. Difraktogram XRD Mg/Al hidrotalsit komersial
(Sharma et al., 2008) ... 12
Gambar 4. Termogram Mg/Al hidrotalsit (Yang et al.,2007)... 14
Gambar 5. Morfologi nauplius ... 19
Gambar 6. Difraktogam Mg/Al hidrotalsit (a) hasil sintesis
(b) bahan baku farmasi ... 32
Gambar 7. Spektra FTIR Mg/Al hidrotalsit (a) hasil sintesis
(b) farmasi bahan baku farmasi... 35
Gambar 8. Termogram TG/DTA Mg/Al hidrotalsit bahan baku farmasi ... 38
commit to user
DAFTAR LAMPIRANLampiran 1. Hasil AAS brine water... 57
Lampiran 2. Hasil AASstarting solution ... 58
Lampiran 3. Perhitungan sintesis Mg/Al hidrotalsit ... 59
Lampiran 4. Skema pengendapan ion kalsium dari brine water... 61
Lampiran 5. Skema sintesis hidrotalsit dari brine water... 62
Lampiran 6. Skema aplikasi Mg/Al hidrotalsit ... 63
Lampiran 7. Penentuan berat jenis nyata ... 65
Lampiran 8. Penentuan berat jenis benar ... 66
Lampiran 9. Penentuan berat jenis mampat ... 67
Lampiran 10. Penentuan porositas ... 68
Lampiran 11. Penentuan faktor hausner ... 68
Lampiran 12. Penentuan kompresibilitas ... 69
Lampiran 13. Penentuan kadar air ... 69
Lampiran 14. Kelarutan ... 70
Lampiran 15. Data JCPDS Mg/Al hidrotalsit ... 72
Lampiran 16. Perbandingan harga dsampel Mg/Al hidrotalsit bahan baku farmasi dengan data JCPDS Mg/Al hidrotalsit ... 73
Lampiran 17. Perbandingan harga dsampel Mg/Al hidrotalsit hasil sintesis dengan data JCPDS Mg/Al hidrotalsit ... 74
Lampiran 18. Spektra FTIR Mg/Al hidrotalsit bahan baku farmasi ... 76
Lampiran 20. Data luas area pemukaan Mg/Al hidrotalsit bahan
baku farmasi ... 78
Lampiran 21. Data luas area permukaan Mg/Al hidrotalsit
hasil sintesis ... 81
Lampiran 22. Termogram TG/DTA Mg/Al hidrotalsit bahan
baku farmasi... 84
Lampiran 23. Termogram TG/DTA Mg/Al hidrotalsit
hasil sintesis ... 85
Lampiran 24. Perhitungan kapasitas penetralan asam KPA ... 86
commit to user
BAB IA. Latar Belakang Masalah
Kegunaan air dalam proses industri sangat banyak selain sebagai bahan
baku pada industri air minum dan pemutar turbin pada pembangkit listrik, juga
sebagai alat bantu utama dalam kerja pada proses industri. PLTU dapat mengolah
air laut menjadi air baku produksi. Setiap PLTU dalam operasionalnya akan
banyak menggunakan air proses yang bersih (service water) dan air demin (demin
water). Dalam memenuhi kebutuhan air yang relatif besar ini, PLTU menyediakan
unit desalinasi. Dalam proses desalinasi, komposisi kimia air laut (sebelum
desalinasi) dan komposisi brine water adalah sama, perbedaanya hanya pada
konsentrasi dari komposisi kimia air laut dan brine water(Heraldy, 2012).
Usaha pemanfaatan kandungan logam alkali tanah berkonsentrasi tinggi
yang terdapat dalam brine waterbelum banyak dilakukan. Berdasarkan penelitian
(Kameda et al., 2000) brine water dapat disintesis menjadi hidrotalsit sehingga
diperoleh produk yang lebih bermanfaat. Kelompok penelitian (Kameda et al.,
2000) telah berhasil membuat hidrotalsit dari magnesium yang berasal dari laut.
Dalam pembuatan Mg/Al hidrotalsit tersebut, Kameda menggunakan air laut
buatan (artificial seawater) yang mengandung senyawa utama NaCl, Na2SO4,
MgCl2dan CaCl2.
Hidrotalsit terdiri dari tumpukan lapisan-lapisan hidroksida dari
magnesium dan aluminium yang bermuatan positif sehingga membutuhkan anion
(Orthman et al., 2000). Jumlah dan susunan anion penyeimbang muatan di dalam
hidrotalsit ditentukan oleh rasio mol Mg/Al (Newman and Jones, 1998). Menurut
penelitian (Jaubertie et al., 2006) material hidrotalsit yang dikenal luas adalah
Mg6All2(OH)16(CO3).4H2O yang merupakan turunan dari senyawa brucite
Mg(OH)2. Senyawa tersebut terdiri dari penata lapisan berbentuk heksagonal
dengan sisi oktahedral yang diisi oleh kation magnesium untuk setiap 2 lapis
hidroksida. Struktur oktahedral Mg2+ dan Al3+ yang sisinya saling berbagi akan
membentuk lembaran-lembaran (sheets) yang tak terbatas. Lembaran-lembaran ini
akan bertumpuk satu sama lain dan terikat dengan ikatan yang lemah melalui
ikatan hidrogen (Vaccari, 1998; Kovanda et al., 2005). Lapisan-lapisan ini
kemudian akan menjadi positif sehingga diperlukan anion-anion penyeimbang di
daerah antarlapis.
Mg/Al hidrotalsit telah dikenal sebagai salah satu mineral yang menarik,
prospektif dan menjanjikan karena dapat disintesis dengan mudah serta berguna
dalam berbagai aplikasi (Tong et al., 2003). Senyawa hidrotalsit sekarang ini telah
banyak dikembangkan karena potensi yang dimilikinya baik untuk adsorben
(Wright, 2002; Heraldy et al., 2011), penukar ion (Miyata, 1983), sebagai katalis
(Kishore and Kannan, 2002; 2004), bahan penstabil untuk formulasi obat-obatan
dan kosmetika (Xu et al., 2001) dan bahan pengontrol keluarnya bahan aktif
dalam obat (drug release control) (Ambrogi et al., 2001; Nakayama et al., 2003).
Sebagai bahan baku obat dalam industri farmasi (Hussein et al., 2009),
maka hidrotalsit hasil sintesis harus melewati berbagai macam pengujian antara
lain uji preformulasi meliputi pengujian berat jenis nyata, berat jenis mampat,
berat jenis benar, kelarutan, penentuan pH, kadar air (Anonim, 1995); Uji
toksisitas akut terhadap larva Artemia SalinaLeach dengan metode Brine Shrimp
Lethality Test (Meyer, 1982; Carballo et al., 2002); dan uji penentuan kapasitas
penetralan asam (Gunawan, 2008; Sari, 2012). Pengujian tersebut dibandingkan
dengan hidrotalsit bahan baku farmasi.
B. Perumusan Masalah
commit to user
Sintesis senyawa hidrotalsit dilakukan menggunakan magnesium dari
brine water. Dalam brine waterjuga kaya akan ion kalsium, apabila ion kalsium
dalam air laut tidak dihilangkan terlebih dahulu, ion kalsium akan mengendap
bersama-sama dengan Mg/Al hidrotalsit sebagai pengotor (Kameda et al., 2000)
Rasio mol Mg/Al secara khas berada pada kisaran antara 2,0 sampai 3,7
(Kameda et al., 2000). Menurut Heraldy (2010) kemurnian senyawa Mg/Al
hidrotalsit akan semakin tinggi dengan semakin berkurangnya nilai rasio mol
Mg/Al. Kemudian berdasarkan penelitian sebelumnya, kondisi optimum untuk
sintesis Mg/Al hidrotalsit dicapai dengan rasio Mg/Al = 2,0 (Prasasti, 2008).
Beberapa faktor dalam sintesis hidrotalsit dapat mempengaruhi hasil
sintesis seperti suhu, waktu maupun pH pada saat sintesis (Oh et al., 2002).
Menurut de Roy (2001), Mg/Al hidrotalsit terkristalisasi dengan baik pada pH
8-10,5 sementara Kameda (2000) yang telah membuat Mg/Al hidrotalsit dari
magnesium yang berasal dari air laut tiruan (artificial seawater) memperoleh
kondisi optimum pada pemanasan suhu 60 oC, pH 10 selama 1 jam. Kemudian
Savitri (2008) pada sintesis Mg/Al hidrotalsit memperoleh kondisi optimum pada
pH 10,5 dan temperatur sintesis 70 ºC.
Dalam membuat suatu bahan menjadi sediaan farmasi diperlukan
tahap-tahap proses yang meliputi preformulasi, formulasi dan proses pengontrolan.
Sebagai tahapan awal (preformulasi), dapat dilakukan karakterisasi kimia fisika
terhadap bahan sediaan farmasi untuk mengetahui karakteristik bahan tersebut
sebagai sediaan farmasi sehingga dapat digunakan pertimbangan formulator
dalam merancang formulasi obat untuk mencapai hasil yang diinginkan
(Ogungbenle, 2009).
Dalam menentukan efektivitas sediaan antasida dilakukan uji kapasitas
penetralan asam (KPA), dengan berbagai variasi distribusi ukuran partikel.
Toksisitas terdiri dari tiga macam yaitu toksisitas akut, toksisitas subakut atau
subkronis dan toksisitas kronis. Uji toksisitas akut menggunakan metode Brine
Shrimp Lethality Test(BST), dimana larva Artemia salinaLeach sebagai hewan
2. Batasan Masalah
Sintesis dan karakterisasi hidrotalsit dari brine waterdan kemampuannya
sebagai sediaan antasida masalah dibatasi untuk:
a. Brine waterdiperoleh dari PLTU Tanjung Jati B, Jepara, Jawa Tengah
yang merupakan limbah hasil dari proses desalinasi.
b. Melakukan sintesis senyawa Mg/Al hidrotalsit dari brine water, proses
sintesis dilakukan pada pH ± 10 dan temperatur ± 70˚C.
c. Melakukan pengendapan ion Ca2+ karena memiliki pengaruh besar
sebagai pengotor pada sintesis Mg/Al hidrotalsit.
d. Rasio mol yang digunakan dalam sintesis Mg/Al hidrotalsit dari brine
wateradalah 2:1
e. Preformulasi Mg/Al hidrotalsit sebagai bahan sediaan farmasi meliputi
beberapa pengujian yaitu pemerian, berat jenis nyata, berat jenis benar,
berat jenis mampat, pH, kadar air dan kelarutan.
f. Kriteria inklusi larva Artemia salina berumur 48 jam, dengan waktu
pengujian selama 24 jam dan kriteria eksklusi larva tidak
menunjukkan pergerakan selama beberapa detik saat pengamatan.
g. Rentang distribusi partikel yang digunakan adalah H1 (100 mesh), H2
(150 mesh), H3(180 mesh).
h. Uji preformulasi dan kapasitas penetralan asam Mg/Al hidrotalsit hasil
sintesis dibandingkan dengan Mg/Al hidrotalsit bahan baku farmasi.
3. Rumusan Masalah
Berdasarkan uraian yang dikemukakan pada pembatasan masalah di atas,
rumusan masalah dari penelitian yang akan dilakukan adalah sebagai berikut.
a. Bagaimana hasil karakterisasi dan preformulasi Mg/Al hidrotalsit hasil
sintesis dan Mg/Al hidrotalsit bahan baku farmasi?
b. Bagaimana perbandingan nilai Kapasitas Penetralan Asam Mg/Al
commit to user
c. Apakah kandungan senyawa Mg/Al hidrotalsit mempunyai potensi
toksisitas akut terhadap Artemia SalinaLeach?
C. Tujuan Penelitian
a. Mengetahui bagaimana hasil karakterisasi dan preformulasi Mg/Al
Hidrotalsit hasil sintesis dan Mg/Al hidrotalsit bahan baku farmasi.
b. Mengetahui perbandingan nilai Kapasitas Penetralan Asam Mg/Al
hidrotalsit hasil sintesis dengan Mg/Al hidrotalsit bahan baku farmasi.
c. Mengetahui apakah kandungan senyawa Mg/Al hidrotalsit hasil sintesis
mempunyai potensi toksisitas akut terhadap larva Artemia Salina Leach
D. Manfaat Penelitian
a. Segi teoritis, diharapkan dapat menambah khasanah ilmu pengetahuan
tentang hidrotalsit dalam bidang farmasi dan bidang lain, serta referensi
bagi penelitian selanjutnya.
b. Segi praktis, memberikan informasi mengenai potensi hidrotalsit sebagai
bahan sediaan farmasi dan sebagai alternatif pemanfaatan limbah hasil
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Brine water
Brine water merupakan air dengan larutan garam jenuh, air ini diperoleh
dari hasil samping desalinasi air laut. Desalinasi adalah proses yang
menghilangkan kadar garam berlebih dalam air (laut) untuk mendapatkan air yang
layak konsumsi. Dalam memenuhi kebutuhan air yang relatif besar ini, PLTU
menyediakan unit desalinasi. Dalam proses desalinasi, komposisi kimia air laut
(sebelum desalinasi) dan komposisi brine wateradalah sama, perbedaanya hanya
pada konsentrasi dari komposisi kimia air laut dan brine water(Heraldy, 2012).
Komposisi kimia brine water hasil desalinasi tergantung komposisi kimia
air lautnya. Dalam 1000 gram air laut, selain dengan jumlah sebanyak 965 gram
(96,5%), mengandung juga beberapa komponen garam-garam terlarut (salinitas)
sebanyak 35 gram (3,5%). Lebih dari 99% adanya salinitas ini karena keberadaan
enam ion utama dalam air laut, yaitu: ion klorida (Cl-), ion natrium (Na+), ion
sulfat (SO42-), ion magnesium (Mg2+), ion kalsium (Ca2+) dan ion kalium (K+).
(Anderson, 2003)
Komposisi kimia air laut tiruan (artificial seawater) hampir sama dengan
komposisi kimia air laut murni (natural seawater). Formula yang dikemukakan
oleh Lyman dan Fleming (1940) adalah salah satu formula yang paling sering
commit to user
analog dengan cara membuat air laut tiruan. Massa dari komponen air laut tiruan
per kilogram larutan dihitung dari komponen garam-garam terlarut (salinitas)
sebanyak 35% berdasarkan berat atom dan molekul.
Sintesis hidrotalsit dari brine water telah dilakukan Kameda dan kelompok
penelitiannya (2000) membuat Mg/Al HTLc yang berasal dari brine watertiruan
(artificial seawater). Sintesis ini diawali dengan membuat larutan awal (starting
solution) dengan cara menghilangkan ion kalsium terlebih dahulu. Menurut
Kameda apabila ion kalsium dalam air laut tidak dihilangkan terlebih dahulu, ion
kalsium akan mengendap bersama hidrotalsit sebagai pengotor. Berikut
perbandingan komposisi kimia antara air laut dengan brine wateryang tercantum
pada Tabel 1 di bawah ini :
Hidrotalsit merupakan salah satu jenis material anorganik yang telah
dipelajari secara luas karena memiliki potensi aplikasi dalam berbagai industri
dan proses kimia. Hidrotalsit termasuk dalam jenis lempung anionik yang
dikenal sebagai layer double hydroxides(LDH) yang memiliki rumus umum
[Mg2+1-x Al3+ x(OH)2]b+ [An-]b/n.mH2O dimana M2+ dan M3+ adalah kation
divalen dan trivalen yang menyusun sisi oktahedral pada lapisan
hidroksidanya. Nilai x pada umumnya berkisar antara 0,17 hingga 0,33.
Simbol An- merupakan anion yang mengisi interlayer yang disebabkan oleh adanya muatan positif pada permukaan hidrotalsit. Muatan positif pada
permukaan ini ditimbulkan oleh adanya substitusi anion divalen oleh anion
trivalen yang sering disebut sebagai substitusi isomorphous.
Muatan pada permukaan dinyatakan sebagai b dan m sebagai jumlah
molekul air pada interlayernya (Hickey et al., 2000). Struktur senyawa
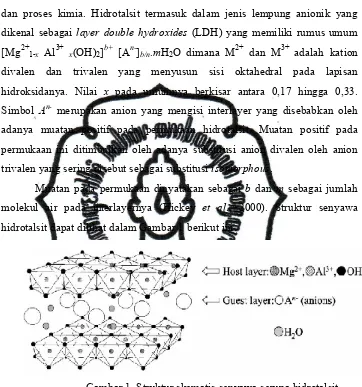
hidrotalsit dapat dilihat dalam Gambar 1 berikut ini.
Gambar 1. Struktur skematis senyawa serupa hidrotalsit (Palmer et al., 2009)
Menurut Jaubertie (2006) material hidrotalsit yang dikenal luas adalah
Mg6All2(OH)16(CO3).4H2O yang merupakan turunan dari senyawa brucite
Mg(OH)2. Senyawa tersebut terdiri dari penata lapisan berbentuk heksagonal
dengan sisi oktahedral yang diisi oleh kation magnesium untuk setiap 2 lapis
hidroksida. Struktur oktahedral Mg2+ dan Al3+ yang sisinya saling berbagi
akan membentuk lembaran-lembaran (sheets) yang tak terbatas.
Lembaran-lembaran ini akan bertumpuk satu sama lain dan terikat dengan ikatan yang
commit to user
Lapisan-lapisan ini kemudian akan menjadi positif sehingga diperlukan
anion-anion penyeimbang di daerah antarlapis untuk menghasilkan muatan listrik
yang netral. Gambar skematis struktur lapisan hidroksida dalam senyawa
hidrotalsit yang ditunjukkan pada Gambar 2.
Gambar 2. Struktur lapisan hidroksida senyawa hidrotalsit
(Palmer et al., 2009)
Kation divalen dan trivalen yang digunakan dalam pembuatan
hidrotalsit tidak terbatas pada satu macam kation saja. Kation divalen (M2+)
yang digunakan dapat berupa Mg2+, Mn2+, Fe2+, Co2+, Ni2+, Cu2+, Zn2+, dan
kation trivalen (M3+) dapat berupa Al3+, Cr3+, Mn3+, Fe3+, Co3+, La3+, dan
Ce3+. Oleh karena itu, sangat mungkin untuk mensintesis hidrotalsit yang
terdiri dari tiga atau lebih kation pada bidang lapisnya.
Pemasukan anion-anion lain (halida, anion kompleks, anion organik,
dan lain-lain) juga sangat mungkin terjadi. Di samping itu anion yang terdapat
pada bidang lapis hidrotalsit juga dapat tergantikan oleh anion-anion lain.
Kemudahan anion penyeimbang dalam interlayer hidrotalsit untuk
dipertukarkan dengan anion lain maka memungkinkan hidrotalsit sebagai
penukar ion.
Anion dan air terletak secara acak pada daerah interlayer dan bebas
bergerak dengan memutus ikatan hidrogen dan membentuk kembali ikatan
hidrogen yang lain seperti pada air sehingga mudah dipertukarkan tanpa
merusak struktur hidrotasit. Pada hidrotalsit dengan CO32- sebagai anion
penyeimbang, gugus hidroksi dapat berikatan dengan CO32- secara langsung
atau melalui perantara air dengan membentuk jembatan hidrogen (Cavani et
al., 1991)
Keistimewaan hidrotalsit tidak hanya pada kemampuannya sebagai
memory effect yang dimilikinya. Sifat memory effect ini memungkinkan
penataan ulang struktur lapisan hidrotalsit setelah kalsinasi apabila sudah
didispersikan dalam air (Orthman et al., 2004). Wright (2002) menyatakan hal
tersebut dapat terjadi asalkan temperatur kalsinasi tidak lebih dari 550–600oC.
Sifat ini dimanfaatkan untuk regenerasi hidrotalsit yang telah digunakan untuk
adsorpsi yaitu dengan memanaskannya pada suhu 450oC.
b) Metode Sintesis Hidrotalsit
Hidrotalsit secara alami dapat terbentuk di alam, akan tetapi jarang
ditemukan. Untungnya, hidrotalsit dapat disintesis dengan mudah di dalam
skala laboratorium (Wright, 2002). Ada beberapa metode dalam sintesis
hidrotalsit yang telah dikembangkan sesuai dengan tujuannya. Metode yang
paling umum digunakan adalah metode kopresipitasi. Pada metode ini,
campuran larutan yang mengandung kation divalen dan kation trivalen yang
ditambahkan anion ke dalamnya digunakan sebagai prekursor. Anion
antarlapisnya bisa ditambahkan secara langsung.
Metode kopresipitasi ini dilakukan dengan cara mengendapkan kedua
logam atau lebih dan memisahkan endapannya dibawah kondisi lewat jenuh
(Trifiro dan Vaccari, 1996). Kondisi lewat jenuh dapat dicapai dengan
mengontrol pH larutan. Pengaturan pH untuk menentukan kopresipitasi
kation-kation logam yang berbeda dapat dilakukan dengan cara titrasi.
Metode titrasi dapat dilakukan melalui peningkatan pH (penambahan
suatu larutan basa kedalam campuran larutan garam) atau melalui penurunan
pH (penambahan suatu campuran larutan garam kepada larutan basa).
Kelemahan metode ini adalah sering terbentuknya fasa padatan lain disamping
pembentukan fasa padatan hidrotalsit sendiri, terkait dengan adanya
pengendapan terlebih dahulu logam hidroksida yang kelarutannya lebih
rendah daripada pengendapan hidrotalsit.
c) Aplikasi Hidrotalsit
Hidrotalsit telah banyak dikembangkan dan diaplikasikan dalam
berbagai bidang diantaranya sebagai adsorben, penukar ion, stabilizer, katalis
commit to user
Beberapa studi juga menunjukkan bahwa hidrotalsit dapat juga
digunakan sebagai bahan penstabil (stabilizer) untuk formulasi obat-obatan
dan kosmetika (Xu et al., 2001; Ooishi et al., 1993; Ueno and Kubota, 1987)
serta sebagai bahan pengontrol keluarnya bahan aktif dalam obat (drug release
control) (Ambrogi et al., 2001, 2002, 2003 ; Nakayama et al., 2003).
Kemudian Roto (2007) telah mempelajari bahwa layered double hydroxides
(LDH) merupakan material host untuk bahan UV aktif p-aminobenzoic acid
(PABA). LDH yang terinterkalasi senyawa aktif p-aminobenzoic acid (PABA)
menghasilkan kombinasi senyawa LDH-PABA. Material tersebut memiliki
kemampuan yang tinggi sebagai sun protection factor (SPF) yang melindungi
kulit akibat pengaruh radiasi sinar UV dari sinar matahari. Menurut Carretero
and Pozo (2010), hidrotalsit adalah salah satu dari 30 mineral yang biasa
digunakan sebagai eksipien dan bahan aktif.
3. Karakterisasi dan Analisis Hidrotalsit
a) Analisis logam denganAtomic Absorption Spectrophotometer (AAS)
Spektrometri merupakan suatu metode analisis kuantitatif yang
pengukurannya berdasarkan banyaknya radiasi yang dihasilkan atau yang
diserap oleh spesi atom atau molekul analit. Salah satu bagian dari
spektrometri ialah Spektrometri Serapan Atom (SSA), merupakan metode
analisis unsur secara kuantitatif yang pengukurannya berdasarkan penyerapan
cahaya dengan panjang gelombang tertentu oleh atom logam dalam keadaan
bebas (Skoog et al., 2000).
Keuntungan metode AAS dibandingkan dengan spektrofotometer biasa
yaitu spesifik, batas deteksi yang rendah dari larutan yang sama bisa
mengukur unsur-unsur yang berlainan, pengukurannya langsung terhadap
contoh, output dapat langsung dibaca, cukup ekonomis, dapat diaplikasikan
pada banyak jenis unsur, batas kadar penentuan luas (dari ppm sampai %).
Sedangkan kelemahannya yaitu pengaruh kimia dimana AAS tidak mampu
menguraikan zat menjadi atom misalnya pengaruh fosfat terhadap Ca,
menimbulkan emisi pada panjang gelombang yang sama, serta pengaruh
matriks misalnya pelarut (Hendayana, 1994).
b) Analisis Struktur DenganX-Ray Difractometer (XRD)
Dalam mengetahui kritalinitas suatu zat padat, instrumen yang biasa
digunakan adalah X-Ray difraction (XRD). Setiap kristal mempunyai harga d
maka jenis kristalnya dapat diketahui. Referensi harga d dan intensitas suatu
senyawa dapat diperoleh dari data Joint Commite on Power Difraction
Standars (JCPDS) yang bersumber dari International Centre For Difraction
Data(West, 1992). Hidrotalsit dengan anion antar lapis berupa CO32-dicirikan
oleh harga d sekitar 7,80 Å. Perincian ini disebutkan pula dalam hasil
penelitian yang dilakukan oleh Kloprogge (2002).
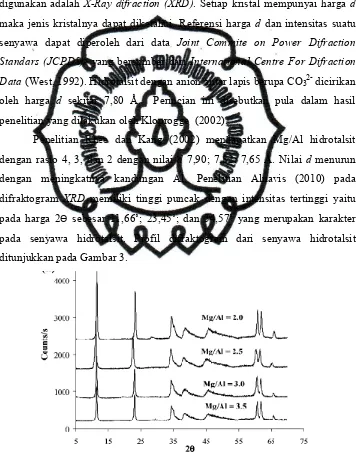
Penelitian Rhee dan Kang (2002) mendapatkan Mg/Al hidrotalsit
dengan rasio 4, 3, dan 2 dengan nilai d 7,90; 7,82; 7,65 Å. Nilai d menurun
dengan meningkatnya kandungan Al. Penelitian Alnavis (2010) pada
difraktogram XRD memiliki tinggi puncak dengan intensitas tertinggi yaitu
pada harga 2Ѳ sebesar 11,66˚; 23,45˚; dan 34,57˚ yang merupakan karakter
pada senyawa hidrotalsit. Profil difraktogram dari senyawa hidrotalsit
ditunjukkan pada Gambar 3.
commit to user
Menurut Sharma (2008) Kristalinitas menurun dengan meningkatnya
rasio mol Mg/Al. Presentase kandungan senyawa dalam sampel diketahui
dengan membandingkan intensitas puncak difraksi karena intensitas tersebut
sebanding dengan fraksi senyawa dalam sampel (Willard et al., 1988).
c) Analisis Gugus Fungsi Dengan Spektrofotometer Infra Merah (FT-IR)
Spektrofotometri Infra Merah merupakan suatu metode yang
mengamati interaksi molekul dengan radiasi elektromagnetik yang berada
pada daerah panjang gelombang 0,75–1.000 µm atau pada Bilangan
Gelombang 13.000–10 cm-1. Para ahli kimia telah memetakan ribuan spektrum
infra merah dan menentukan panjang gelombang absorbsi masing-masing
gugus fungsi.
Johnson dan Glasser (2003) telah melaporkan adanya puncak-puncak
yang khas dari vibrasi gugus-gugus fungsi pada senyawa hidrotalsit. Puncak
pada bilangan gelombang 3400 cm-1menunjukkan vibrasi ulur OH, 1400 cm-1
menunjukkan vibrasi ulur asimetris CO3, 800 cm-1 menunjukkan deformasi
luar bidang CO3, sementara pada bilangan gelombang 600-400 cm-1
menunjukkan vibrasi ulur M-Al-O dan vibrasi ulur serta tekuk dari M-O
dengan M adalah logam. Referensi gugus-gugus fungsi yang ada dalam
senyawa hidrotalsit dapat dilihat pada Tabel 2 :
Tabel 2. Gugus-gugus fungsi Mg/Al hidrotalsit
Gugus Fungsi Bilangan Gelombang (cm-1)
Uluran OH dan M-O 3400-3500a,b
Tekukan OH 1650d
Uluran simetris O=C-O 1385a,c
Uluran asimetris O=C-O 1500,5c
Tekukan O=C-O 650a
Uluran Mg-O dan Al-O 400-600a(2 puncak)
Sumber : aKannan (1995) dalam Johnson and Glasser (2003),
b
d) Analisis Termal Dengan TG/DTA
Analisis termal adalah pengukuran sifat fisika dan kimia sebagai
fungsi temperatur (Skoog et al., 1997). Ada dua teknik utama dalam analisis
yaitu Thermogravimetric Analyzer (TG) yang secara otomatis mencatat
perubahan sampel sebagai fungsi temperatur atau waktu dan Differential
Thermal Analyzer (DTA)yang mengukur perbedaan temperatur antara sampel
dan material pembanding inert sebagai fungsi temperatur. Oleh karena itu,
DTA mendeteksi perubahan pada kandungan panasnya. Dalam prakteknya
analisis termal ini meliputi entalpi, kapasitas panas, massa dan koefisisen
ekspansi termal.
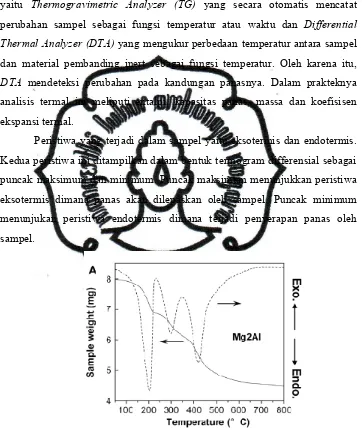
Peristiwa yang terjadi dalam sampel yaitu eksotermis dan endotermis.
Kedua peristiwa ini ditampilkan dalam bentuk termogram differensial sebagai
puncak maksimum dan minimum. Puncak maksimum menunjukkan peristiwa
eksotermis dimana panas akan dilepaskan oleh sampel. Puncak minimum
menunjukan peristiwa endotermis dimana terjadi penyerapan panas oleh
sampel.
Gambar 4. Termogram Hidrotalsit (Yang et al., 2007)
Dalam termogram pada Gambar 4 puncak endotermis pada suhu
sekitar 80 ºC sampai 250 ºC mengindikasikan tahap dehidrasi, kemudian pada
suhu 260 ºC sampai 600 ºC berhubungan dengan tahap dehidroksilasi dan
commit to user
puncak endotermis pada temperatur 116 ˚C yang menunjukkan pelepasan
molekul air pada antar lapisan dan temperatur 238 ˚C yang menunjukkan
pelepasan gugus OH (Xie et al., 2003). Pelepasan karbonat ditunjukkan oleh
puncak endotermis pada temperatur 414 ˚C sedangkan degradasi struktur
hidrotalsit terjadi pada 489˚C (Frost et al.,2005).
e) Analisis Luas Permukaan Dengan Surface Area Analyzer (SAA)
Surface Area Analyzer (SAA) merupakan salah satu alat utama dalam
karakterisasi material. Alat ini khususnya berfungsi untuk menentukan luas
permukaan material, distribusi pori dari material dan isotherm adsorpsi suatu
gas pada suatu bahan.
Alat ini prinsip kerjanya menggunakan mekanisme adsorpsi gas,
umumnya nitrogen, argon dan helium, pada permukaan suatu bahan padat
yang akan dikarakterisasi pada suhu konstan biasanya suhu didih dari gas
tersebut. Alat tersebut pada dasarnya hanya mengukur jumlah gas yang dapat
diserap oleh suatu permukaan padatan pada tekanan dan suhu tertentu. Secara
sederhana, jika kita mengetahui berapa volume gas spesifik yang dapat diserap
oleh suatu permukaan padatan pada suhu dan tekanan tertentu dan kita
mengetahui secara teoritis luas permukaan dari satu molekul gas yang diserap,
maka luas permukaan total padatan tersebut dapat dihitung.
4. Preformulasi Mg/Al Hidrotalsit
Preformulasi bahan sediaan farmasi bertujuan untuk mengetahui data-data
karakteristik bahan obat yang dapat dijadikan pertimbangan formulator dalam
merancang formulasi obat untuk mencapai hasil yang diinginkan (Ogungbenle,
2009). Preformulasi tersebut antara lain꞉
a. Berat Jenis
Berat jenis didefinisikan sebagai perbandingan antara massa bahan (g)
terhadap volumenya (mL), sehingga satuan berat jenis gram per milliliter
(g/mL). Menurut Wicaksono (2010) dengan mengetahui berat jenis maka
alir suatu material dapat mempengaruhi formulasi tabletisasi. Semakin baik
sifat alir suatu material maka semakin baik waktu hancurnya dalam bentuk
tablet. Zat padat tidak homogen dan serbuk yang memiliki pori dan ruang
rongga, berat jenis tidak lagi terdefinisi secara jelas sehingga harus dibedakan
antara berat jenis benar, berat jenis nyata, dan berat jenis mampat. Berat jenis
benar adalah perbandingan massa dengan volume dari zat padat tanpa pori dan
tanpa ruang rongga sedangkan berat jenis nyata adalah volumenya yang
membesar akibat adanya pori-pori yang ikut diperhitungkan. Berat jenis
mampat dinyatakan sebagai berat dimana satuan massa suatu produk
berbentuk serbuk berada pada kumpulannya yang terpadat tanpa perubahan
bentuk dari partikelnya (Voigt, 1994).
b. Sifat Alir
Secara umum, untuk partikel yang ekidimensional (teratur), semakin
besar diameter maka sifat alir semakin baik. Sifat alir terbaik terjadi pada
diameter optimum partikel. Pada umumnya semakin bulat maka sifat alir
semakin baik. Semakin tidak beraturan maka sifat alir semakin buruk. Tekstur
semakin halus maka semakin kecil gaya gesek antar partikel sehingga semakin
mudah mengalir, dan sebaliknya. Semakin besar porositas maka semakin kecil
kontak antar partikel maka kecepatan alir akan semakin baik. Pada kondisi
kandungan lembab yang tinggi ikatan antar partikel akan lebih kuat, karena
luas kontak antar permukaan serbuk naik. Apabila gaya tarik antar partikel
serbuk semakin kuat, maka serbuk akan semakin sukar mengalir (Martin et al.,
1993). Sifat alir dari suatu serbuk dan granulat dapat diperbaiki dengan
penambahan bahan pelincir yang dapat menurunkan gesekan partikel (Voigt,
1994).
c. pH
Reaksi penguraian dari larutan obat dapat dipercepat dengan
penambahan asam (H+) atau basa (OH-) dengan menggunakan katalisator yang
dapat mempercepat reaksi tanpa ikut bereaksi dan tidak mempengaruhi hasil
commit to user
(pH 8-10), karena antasida adalah senyawa basa yang mempunyai kemampuan
untuk menetralkan asam lambung.
d. Kadar Air
Pengukuran kadar air bertujuan untuk memberikan batasan minimal
atau rentang tentang besarnya kandungan air dalam bahan, dimana nilai
maksimal atau rentang yang diperbolehkan terkait dengan kemurniaan dan
kontaminasi. Salah satu cara untuk mengetahui kadar air suatu bahan padat
adalah dengan perhitungan menggunakan data berdasarkan bobot keringnya.
Angka hasil perhitungan ini dianggap sebagai kadar air atau kandungan
lembab.
e. Kelarutan
Dalam bidang farmasi, pengetahuan mengenai kecepatan disolusi atau
kelarutan sangat diperlukan untuk membantu dalam memilih medium pelarut
yang paling baik untuk obat atau kombinasi obat, membantu mengatasi
kesulitan-kesulitan tertentu yang timbul pada waktu pembuatan larutan
farmasetis dan dapat bertindak sebagai standar atau uji kemurnian (Ansel,
1989). Proses pelepasan zat aktif dari sediaannya dan proses pelarutannya
sangat dipengaruhi oleh sifat-sifat kimia dan fisika zat tersebut serta formulasi
sediaannya. Salah satu sifat zat aktif yang penting untuk diperhatikan adalah
kelarutan, karena pada umumnya zat baru diabsorpsi setelah terlarut dalam
cairan saluraan cerna (Martin et al., 1993).
5. Uji Toksisitas
Toksisitas didefinisikan sebagai kemampuan suatu zat untuk menimbulkan
kerusakan. Toksisitas merupakan suatu sifat relatif dari zat kimia dan sejauh
menyangkut diri manusia secara langsung atau tidak langsung. Toksisitas selalu
menunjukkan ke suatu efek berbahaya atas mekanisme biologi tertentu. Toksisitas
merupakan istilah relatif yang biasa dipergunakan dalam membandingkan suatu
zat kimia lebih toksik dari zat kimia lainnya. Perbandingan antara zat kimia
seperti itu sangat tidak informatif, kecuali jika pernyataan itu melibatkan
dalam kondisi bagaimana zat kimia tersebut berbahaya. Karena itu, pendekatan
toksikologi adalah dari segi tentang berbagai efek zat kimia atas berbagai sistem
biologi dengan penekanan pada sistem mekanisme efek berbahaya zat kimia itu
dan kondisi dimana efek berbahaya itu terjadi.
Dalam meneliti berbagai macam efek yang berhubungan dengan masa
inkubasi, uji toksikologi dibagi menjadi tiga kategori yaitu :
1. Uji Toksisitas Akut. Uji ini dirancang untuk menentukan efek toksik suatu
senyawa yang akan terjadi dalam masa inkubasi dengan waktu yang
singkat 24 jam, kecuali pada kasus tertentu selama 7-14 hari.
2. Uji Toksisitas Subkronis atau Subakut, dilakukan dengan memberikan zat
kimia yang sedang diuji tersebut secara berulang-ulang terhadap hewan uji
selama kurang dari 3 bulan.
3. Uji Toksisitas Kronis, dilakukan dengan memberikan zat kimia secara
berulang-ulang pada hewan uji selama lebih dari 3 bulan atau sebagian
besar dari hidupnya.
Kematian merupakan salah satu diantara beberapa kriteria toksisitas. Salah
satu caranya ialah menggunakan senyawa dengan dosis maksimal, kemudian
kematian hewan uji dicatat. Angka kematian hewan dihitung sebagai sebagai
harga median Lethal Dose (LD50) atau median Lethal Concentration (LC50).
Penggolongan toksisitas atas dasar jumlah besarnya zat kimia yang
diperlukan untuk menimbulkan bahaya. Suatu contoh penggolongan tersebut
yaitu:
1) Luar biasa toksik (1 mg/Kg atau kurang).
2) Sangat toksik (1-59 mg/Kg).
3) Cukup (50-500 mg/Kg).
4) Sedikit (0,5-5 g/Kg).
5) Praktis tidak toksik (5-15 g/Kg).
6) Relatif kurang berbahaya lebih dari 15 g/Kg
Penggolongan ini hanya berlaku untuk harga LD50pada hewan percobaan
untuk harga LC50hanya dibedakan menjadi:
commit to user
2) Tidak toksik (LC50> 1000 μg/mL) (Meyer et al., 1982; Carballo, 2002).
Artemia SalinaLeach
Artemia adalah sejenis udang primitif, hewan ini digunakan sebagai uji
dalam metode BST. Pada mulanya Artemia salina Leach ini mempunyai nama
spesies Cancer Salinus Linnaeus. Kemudian pada tahun 1819 diubah menjadi
Artemia salina oleh Leach. Artemia diperdagangkan dalam bentuk telur istirahat
yang disebut dengan kista, berbentuk bulat-bulatan kecil berdiameter antara
200-350 mikron dengan warna kelabu kecoklatan.
Artemia yang baru menetas disebut nauplius. Nauplius yang baru menetas
berwarna orange, berbentuk bulat lonjong dengan panjang sekitar 400 mikron,
lebar 170 mikron, dan berat 0.002 mg. Ukuran-ukuran tersebut sangat bervariasi
tergantung strainnya.
Artemia banyak ditemukan didanau-danau yang kadar garamnya sangat
tinggi sehingga disebut juga dengan brine shrimp. Pertumbuhan biomassa artemia
yang baik membutuhkan kadar garam antara 30-50 permil pada kisaran suhu
25-30 ºC. Akan tetapi kista yang kering sangat tahan terhadap suhu ekstrem dari -273
ºC hingga 100 ºC.
Gambar 5. Morfologi Nauplius (Isnansetyo, 1995 dalam Mutia, 2010 )
Artemia termasuk hewan euroksibion yaitu hewan yang mempunyai
kisaran toleransi yang lebar akan kandungan oksigen, pada kandungan oksigen 1
mg/L Artemia masih dapat bertahan. Artemia bersifat omnivora atau pemakan
dapat masuk mulut. Artemia dalam mengambil makanan bersifat penyaring tidak
selektif (non selective filter feeder), sehingga apa saja yang dapat masuk mulut
artemia seakan-akan menjadi makanannya. Akibatnya kandungan gizi Artemia
sangat dipengaruhi oleh kualitas pakan yang tersedia pada perairan tersebut.
Artemia mengambil pakan dari media hidupnya terus-menerus sambil berenang
(Isnansetyo, 1995 dalam Mutia 2010)
Artemia menjadi dewasa setelah umur 14 hari. Artemia dewasa ini biasa
menghasilkan telur sebanyak 50-300 butir setiap 4-5 hari sekali. Apalagi bila
kondisi lingkungan memungkinkan untuk melakukan perkawinan ovovivipar.
Perkembangbiakan secara ovovivipar ini biasa menghasilkan individu baru dalam
waktu yang relatif lebih cepat sehingga jumlah nauplius yang dihasilkan seoleh
setiap induk bisa lebih banyak. Umur maksimal Artemia sekitar 6 bulan, tetapi
karena Artemia dapat melakukan perkembangbiakan dengan dua cara, maka
memungkinkan organisme ini bertahan hidup sepanjang masa. Dalam keadaan
lingkungan yang tidak menguntungkan, induk Artemia mungkin mati, tetapi siste
atau telur yang dihasilkan dari perkawinan akan berkembang sebagai generasi
penerus (Mutia, 2010)
6. Metode Brine Shrimp Lethaly Test
Metode uji Brine Shrimp lethaly Test (BST) diperkenalkan oleh Meyer
pada tahun 1982 yang digunakan untuk memantau adanya aktifitas farmakologi
(terutama anti kanker). Metode ini menggunakan larva Artemia salina Leach
sebagai hewan coba. Uji toksisitas dengan metode BST ini merupakan uji
toksisitas akut dimana efek toksik dari suatu senyawa ditentukan dalam waktu
singkat setelah pemberian dosis uji. Prosedurnya dengan menentukan nilai LC50
dari aktivitas komponen aktif senyawa terhadap larva Artemia salina Leach.
Metode BST ini mempunyai keunggulan: waktu pelaksanaan cepat, biaya
relatif murah, praktis, tidak memerlukan teknik aseptis, tidak memerlukan
perawatan khusus, menggunakan sampel relatif sedikit, tidak memerlukan serum
commit to user
uji BST adalah menarik hubungan antara konsentrasi larutan senyawa terhadap
respon kematian Artemia salinaLeach (Carballo et al., 2002).
7. Kapasitas Penetralan Asam
Secara alami lambung memproduksi suatu asam yang disebut asam klorida
(HCl) yang berfungsi untuk membantu proses pencernaan protein. Asam ini
secara alami mengakibatkan kondisi isi perut menjadi asam, yakni antara kisaran
PH 2-3. Apabila kadar asam yang dihasilkan oleh lambung terlalu banyak maka
mekanisme perlindungan ini tidak terlalu kuat terhadap kerja asam lambung
sehingga mengakibatkan kerusakan pada organ-organ tersebut dan menghasilkan
gejala seperti rasa sakit pada perut dan ulu hati terasa terbakar.
Antasida adalah obat yang menetralkan asam lambung sehingga
efektifitasnya bergantung pada kapasitas penetralan dari antasida tersebut.
Kapasitas Penetralan Asam (dalam miliequivalen) adalah mEq HCl yang
dibutuhkan untuk mempertahankan suspensi antasida pada pH 3,5 selama 10
menit secara in vitro. Peningkatan pH cairan gastric dari 1,3 ke 2,3 terjadi
penetralan sebesar 90% dan peningkatan ke pH 3,3 terjadi penetralan sebesar 99%
asam lambung. Antasida dapat meningkatkan pH cairan lambung sampai pH 4,
dan menghambat aktifitas proteolitik dari pepsin. Antasida tidak melapisi dinding
mukosa namun memiliki efek adstringen. Secara kimia antasida merupakan basa
lemah yang bereaksi dengan asam lambung membentuk garam dan air.
Beberapa jenis antasida tersebut memiliki perbedaan terutama dalam efek
menetralkan asam lambung, istilah yang dipakai untuk menjelaskan hal ini adalah
ANC (antacid neutralizing capacity). ANC disajikan dalam bentuk perbandingan
mEq, dan FDA mengklasifikasikan per dosis antasida harus punya efek
menetralkan asam sebesar ≥5 mEq per dosisnya.
B. Kerangka Pemikiran
Hidrotalsit jarang ditemukan di alam akan tetapi mempunyai potensi untuk
diteliti dan dikembangkan lebih lanjut. Sintesis hidrotalsit sangat mungkin
hidroksida magnesium dengan aluminium yang formulanya secara umum dapat
dinyatakan dengan [Mg1-xAlx(OH)2]b +
. Sintesis hidrotalsit diawali dengan
mengendapkan ion Ca2+, karena ion Ca2+ berperan sebagai pengotor. Melakukan
perhitungan stoikiometri untuk menentukan rasio mol Mg/Al dengan
perbandingan 2:1. Kation divalen Mg2+ diperoleh dari brine water sedangkan
kation trivalen Al3+diperoleh dari bahan murni laboratorium AlCl3.6H2O.
Salah satu cara untuk mengetahui kualitas Mg/Al hidrotalsit yang
diperoleh dilakukan analisis karakterisasi menggunakan berbagai instrumen antara
lain꞉ Difraksi sinar X (XRD), Spektroskopi Infra Merah (FTIR), Analisis termal
(TG/DTA), dan Surface Area Analyzer (SAA). Data kualitatif yang diperoleh
dibandingkan dengan data Mg/Al hidrotalsit referensi.
Senyawa Mg/Al hidrotalsit mempunyai berbagai macam aplikasi antara
lain; adsorben (Wright, 2002; Heraldy, 2010), penukar ion (Miyata, 1983),
sebagai katalis (Kishore and Kannan, 2002; 2004), bahan penstabil untuk
formulasi obat-obatan dan kosmetika (Xu et al., 2001; Ooishi et al., 1993; Ueno
dan Kubota, 1987) dan bahan pengontrol keluarnya bahan aktif dalam obat (drug
release control) (Ambrogi et al., 2001; Nakayama et al., 2003). Dalam penelitian
ini Mg/Al hidrotalsit diaplikasikan dalam bidang farmasi sebagai sediaan antasida,
dengan demikian diperlukan preformulasi, uji kapasitas penetralan asam dan uji
toksisitas akut, yang berhubungan dengan sediaan antasida. Hasil uji karakterisasi
Mg/Al hidrotalsit hasil sintesis dibandingkan dengan referensi Mg/Al hidrotalsit
bahan baku farmasi.
C. Hipotesis
a. Hasil karakterisasi dan preformulasi antara Mg/Al hidrotalsit hasil sintesis
dengan Mg/Al hidrotalsit bahan baku farmasi tidak mempunyai kriteria yang
hampir sama.
b. Mg/Al hidrotalsit hasil sintesis dari brine water dan Mg/Al hidrotalsit bahan
baku farmasi mempunyai perbandingan nilai Kapasitas Penetralan Asam yang
commit to user
c. Mg/Al hidrotalsit terdiri dari unsur-unsur yang tidak berbahaya sehingga tidak
mempunyai potensi toksisitas akut terhadap larva Artemia SalinaLeach.
BAB III
METODOLOGI PENELITIAN
A. Metode Penelitian
Penelitian ini dilakukan dengan metode eksperimental laboratorium.
Dengan enam tahapan yaitu꞉ Pembuatan larutan awal (starting solution) dengan
mengendapkan ion kalsium dari brine water; Sintesis Mg/Al hidrotalsit dari
larutan awal (starting solution); Identifikasi Mg/Al hidrotalsit hasil sintesis
dengan XRD, FTIR, SAA, dan TG/DTA; Uji preformulasi untuk mengetahui sifat
kimia fisika; Uji kapasitas penetralan asam dan Uji toksisitas akut terhadap larva
Artemia SalinaLeach dengan Metode Brine Shrimp Lethality Test;.
B. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Dasar FMIPA UNS,
Laboratoratorium Kimia Terpadu FMIPA UNS, Laboratorium Kimia Analitik
FMIPA UGM dan Laboratorium Akademi Teknik Kulit (ATK). Waktu penelitian
dimulai pada bulan Desember 2011 sampai bulan Juni 2012.
C. Alat dan Bahan
1. Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah:
a. Seperangkat alat gelas (Pyrex)
b. Seperangkat alat refluks
c. Seperangkat alat titrasi
d. Hot Plate(Cole-Parmer model No. 4658)
f. pH meter digital (Lutron pH-207)
g. Magnetic Stirer
h. Termometer (Alkohol 100ºC)
i. Lumpang porselin
j. CentrifugeHermlez Z206A
k. Oven Fischer Scientific model 655F
l. Atomic Absorption Spectrophotometer (AAS) Shimadzu AA 630-12
m. X-Ray Diffractometer (XRD) D 8 Advance Bruker
n. Thermogravimetric/Differential Thermal Analysis (TG/DTA)PT-1600
o. Fourier Transform Infra Red (FTIR) SHIMADZU IRPrestige-21
p. Surface Area Analyzer (SAA) Quantachrome Nova Station A
2. Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah:
a. Brine waterdari PLTU Tanjung Jati B, Jepara, Jawa Tengah
b. Hidrotalsit bahan baku farmasi, Online Shop
c. Telur Artemia SalinaOsy Crystal, Online Shop
d. Air laut dari pantai selatan Pulau Jawa
e. Aquades (Laboratorium Kimia Dasar FMIPA UNS)
f. Kertas saring (Laboratorium Kimia Dasar FMIPA UNS)
g. Kertas pH (Laboratorium Kimia Dasar FMIPA UNS)
h. HCl 37% p.a (Laboratorium Kimia Dasar FMIPA UNS)
i. NaOH p.a. (E. Merck)
1. Pembuatan Hidrotalsit dari Brine water
commit to user
Sampel brine water sebanyak 1L ditambahkan larutan buffer yaitu
campuran larutan Na2CO3 0,04 M dan NaHCO3 0,08 M sebanyak 209,5 mL
dengan diaduk selama ± 1 jam dan dipanaskan pada ± 95 ˚C untuk
mengendapkan Ca2+. Kemudian dipisahkan antara padatan dan filtratnya,
padatan berwarna putih merupakan endapan Ca2+ dan filtrat merupakan
larutan awal (starting solution) untuk sintesis selanjutnya. Sebelum dan
sesudah pengendapan dilakukan analisis terhadap kandungan logam Ca dan
Mg menggunakan Atomic Absorption Spectrophotometer (AAS) (Kameda et
al., 2000; Heraldy, 2010).
b. Sintesis Mg/Al hidrotalsit
Sebanyak 7,199 g senyawa AlCl3.6H2O ditambahkan kedalam larutan
awal dengan rasio mol awal antara magnesium dengan aluminium adalah 2 : 1.
Sejumlah larutan Na2CO3 1 M ditambahkan kedalam 1000 mL larutan
perkusor hingga pH ± 10 dan kemudian larutan ini tetap diaduk selama 1 jam
pada suhu ± 70 ˚C. Hasil yang diperoleh berupa suspensi yang akan
mengendap setelah beberapa saat didiamkan. Endapan yang diperoleh dicuci
dengan akuades sampai bebas dari ion Cl-. Keberadaan ion Cl- diketahui
dengan menguji filtrat pencucian dengan AgNO3. Filtrat pencucian yang bebas
ion Cl- tidak menghasilkan endapan putih atau menjadi keruh apabila ditetesi
dengan AgNO3(Kameda et al., 2000).
Hidrotalsit berupa suspensi berwarna putih yang diperoleh disentrifus
dengan kecepatan 4000 rpm selama 15 menit, hasil berupa gel dikeringkan
dengan suhu 110 ˚C selama semalam. Setelah kering digerus sampai halus
sampai melewati 150 mesh. Kemudian dikarakterisasi dengan XRD, FTIR,
SAA, dan TG-DTA.
2. Uji Preformulasi Mg/Al Hidrotalsit
a. Penentuan berat jenis
1) Berat Jenis Mampat
Gelas ukur 10 mL kosong ditimbang, diperoleh berat gelas ukur
dan dimampatkan dengan diketukkan sebanyak 1250 kali sampai
volumenya tetap (V) lalu ditimbang, diperoleh berat gelas ukur yang berisi
Mg/Al hidrotalsit mampat pada volume tertentu (W2) (Wallis, 1995).
2) Berat Jenis Nyata
Gelas ukur 10 mL kosong ditimbang, diperoleh berat gelas ukur
kosong (W1). Dimasukkan sampel Mg/Al hidrotalsit ke dalam gelas ukur
sampai volume tertentu, diratakan lalu ditimbang, diperoleh berat gelas
ukur yang berisi Mg/Al hidrotalsit pada volume tertentu (W2) (Wallis,
1995).
3) Berat Jenis Benar
Penentuan berat jenis benar dilakukan menggunakaan piknometer
dan pelarut yang tidak melarutkan serbuk tersebut. Piknometer kosong
yang telah diketahui volumenya ditimbang beratnya, lalu diisi air dan
ditimbang lagi. Kemudian serbuk Mg/Al hidrotalsit sebanyak 1 g
dimasukkan dalam piknometer kosong dan ditimbang, lalu ditambahkan
air ke dalam piknometer sampai batas dan ditimbang lagi beratnya (Wallis,
1995)
b. Penentuan pH
Membuat larutan Mg/Al hidrotalsit dengan konsentrasi 2%. Kemudian
larutan tersebut diukur pH nya menggunakan pH meter yang telah dikalibrasi
sebelumnya, sehingga diperoleh harga pH Mg/Al hidrotalsit (Jati, 2011).
c. Penentuan kelarutan
Sebanyak 0,5 g sampel Mg/Al hidrotalsit dilarutkan ke dalam 100 mL
larutan dengan variasi pH 1 ; 2 ; 3. Kemudian larutan dihomogenkan dengan
distirrer selama 5 menit pada temperatur 37 oC. Larutan yang telah homogen
disaring, endapan yang ada di kertas saring dikeringkan dengan dioven pada
temperatur 100 oC selama 30 menit, lalu ditimbang berat endapan yang tidak
larut (Jati, 2011).
commit to user
Sampel Mg/Al hidrotalsit ditimbang sebanyak 0,5 g, kemudian
ditempatkan pada kurs porselen dan dipanaskan dalam ovenpada temperatur
105 oC selama 3 jam. Hasil pemanasan ditimbang dengan neraca analitik
(Halim, 1990; Anonim, 1995)
3. Uji Kapasitas Penetralan Asam
Dalam menentukan distribusi partikel dilakukan dengan metode
pengayakan. Ada tiga fraksi yang digunakan dalam penentuan kapasitas
penetralan asam yaitu H1(100 mesh); H2(150 mesh); H3(180 mesh). Dua gram
sampel Mg/Al hidrotalsit dilakukan pengayakan sesuai dengan fraksi
masing-masing sehingga diperoleh berat Mg/Al hidrotalsit yang lolos pengayakan.
Kapasitas Penetralan Asam dilakukan dengan melarutkan 0,2 g Mg/Al
hidrotalsit kedalam 100 mL akuades bersuhu 37 ºC kemudian ditambahkan 100
mL HCl 0,1 M diaduk selama 15 menit. Segera dititrasi setelah 15 menit dengan
NaOH 0,1 M dalam waktu kurang dari 5 menit hingga dicapai pH 3,5 yang stabil
(selama 10-15 detik). Dihitung jumlah NaOH 0,1 M yang dibutuhkan untuk
titrasi (Anonim, 1995; Sari, 2012)
4. Uji Toksisitas Akut
a. Penetasan telur Artemia SalinaLeach
Telur kista Artemia SalinaLeach sebanyak satu gram direndam dalam
1 L air laut (pH air laut ±7) dengan aerator dan lampu penerangan selama 48
jam. Telur akan menetas menjadi larva udang.
b. Pengujian toksisitas akut
Larva udang Artemia Salina Leach yang sudah berumur 48 jam
dimasukkan dalam larutan hidrotalsit dengan konsentrasi (µg/mL) yang
bervariasi. Sebagian besar hidrotalsit tidak larut namun tersuspensi. Setelah 24
jam dihitung jumlah larva yang mati, yaitu dengan kriteria tidak menunjukkan
pergerakan selama pengamatan. Jumlah larva yang mati dibagi jumlah total
larva tiap konsentrasi kemudian dikali 100% sehingga diperoleh presentase
E. Teknik Pengumpulan Data
Data kualitatif dan kuantitatif diperoleh dari hasil eksperimen. Data
kualitatif diperoleh dari hasil karakterisasi menggunakan Atomic Absorption
Spectrophotometer (AAS), X Ray Diffraction (XRD), Fourier Transform Infra
Red (FTIR), Thermogravimetric/Differential Thermal Analysis (TG/DTA), dan
Surface Area Analyser(SAA).
Analisis AAS diperoleh data konsentrasi Ca dan Mg dalam bentuk ppm
kemudian dikonversi ke mol logam. Dari analisis XRD diperoleh dengan
membaca difraktogram yang berupa suatu pola difraksi dengan puncak-puncak
pada 2Ѳ tertentu sehingga diperoleh jarak antara kisi kristal (d) yang sesuai
dengan hukum Bragg. Analisis termal menggunakan TG/DTA. Identifikasi gugus
fungsi menggunakan data FTIR. Dan untuk menganalisis luas area permukaan
menggunakan data SAA.
Data kuantitatif diperoleh dari uji sifat kimia fisika (preformulasi), uji
Kapasitas Penetralan Asam dan uji toksisitas akut terhadap Artemia Salina. Uji
sifat kimia fisika hidrotalsit sebagai sediaan farmasi dilakukan secara triplo dan
membandingkannya antara hidrotalsit hasil sintesis dari brine water dengan
hidrotalsit bahan baku farmasi. Uji toksisitas akut dilakukan terhadap larva udang
Artemia Salina dalam kurun waktu 24 jam, Sedangkan untuk uji kapasitas
penetralan asam dilakukan pada tiga fraksi (H1, H2, H3).
F. Teknik Analisa Data
Berdasarkan data yang diperoleh pada karakterisasi material hasil sintesis,
dapat dilakukan analisis sebagai berikut:
a. Jumlah Rasio mol Mg/Al dalam Mg/Al hidrotalsit diperoleh dari hasil analisis
menggunakan AAS, dengan data berupa konsentrasi ppm dalam sampel yang
dapat di konversi kedalam perbandingan mol.
b. Identifikasi material hasil sintesis dengan XRD dianalisis dengan
commit to user
hidrotalsit. Presentase kandungan Mg/Al hidrotalsit dalam sampel dapat
dihitung dengan membandingkan jumlah intensitas relatif total sampel.
c. Gugus fungsi yang ada di dalam Mg/Al hidrotalsit diketahui dengan
membandingkan dengan puncak-puncak spektra FTIR Mg/Al hidrotalsit
dengan referensi.
d. Analisis termal menggunakan TG/DTA. DTA akan mendeteksi setiap
perubahan termal yang terkait dengan peristiwa atau reaksi kimia, baik yang
berjalan secara eksotermik maupun endotermik. Sementara itu TGA
mendeteksi setiap perubahan massa yang terjadi pada cuplikan sebagai akibat
dari kenaikan suhu, baik yang diikuti oleh perubahan fasa kristal maupun
tidak.
e. Data permukaan meliputi surface area, average pore radius dan total pore
volumediperoleh dari analisa SAA dan dibandingkan dengan referensi.
f. Data kuantitatif uji sifat kimia fisik (preformulasi) dari hidrotalsit hasil sintesis
di bandingkan dengan hidrotalsit bahan baku farmasi. Meliputi penentuan
berat jenis, porositas, factor hausner, kompresibilitas, pH, kelarutan dan kadar
air.
g. Nilai toksisitas LC50ditentukan dari uji toksisitas akut terhadap larva Artemia
SalinaLeach dengan menghitung jumlah kematian.
h. Nilai kapasitas penetralan asam diperoleh dari jumlah miliekuivalen (mEq)
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Kesimpulan yang dapat diambil berdasarkan penelitian dan pembahasan
adalah sebagai berikut꞉
1. Hasil analisis Mg/Al hidrotalsit hasil sintesis dan Mg/Al hidrotalsit bahan
baku farmasi mempunyai karakterisasi yang hampir sama, sedangkan
untuk uji preformulasi ada perbedaan sifat kimia fisika antara Mg/Al
hidrotalsit hasil sintesis dan Mg/Al hidrotalsit bahan baku farmasi.
2. Nilai Kapasitas Penetralan Asam (KPA) Mg/Al hidrotalsit hasil sintesis
lebih tinggi daripada Mg/Al hidrotalsit farmasi, keduanya merupakan
antasida yang baik karena mempunyai nilai KPA > 5 mEq.
3. Kandungan senyawa Mg/Al hidrotalsit hasil sintesis tidak mempunyai
potensi toksisitas akut terhadap larva Artemia Salina Leach karena harga
LC50 > 1000 µg/mL sehingga aman jika digunakan sebagai bahan sediaan
antasida.
B. Saran
Saran yang dapat diberikan terkait penelitian ini adalah
1. Perlu dilakukan perhitungan lebih cermat, agar pada saat pengendapan Ca
dengan larutan bufferion Mg tidak ikut terendapkan.
2. Hasil Mg/Al hidrotalsit yang diperoleh seringkali mengandung senyawa
MgOH2 dan AlOH3, untuk itu perlu dilakukan analisis agar tidak terjadi
commit to user
3. Perlu dilakukan penelitian lebih lanjut agar dalam pencucian Mg/Al
hidrotalsit setelah sintesis tidak menghabiskan banyak akuades.
DAFTAR PUSTAKA
Alnavis, N. B., 2010. Mg/Al Hydrotalcite dari Brine Water : Sintesis dan
Aplikasinya sebagai Adsorben Eosin Yellow dan Methyl Violet. Yogyakarta꞉
Jurusan Kimia FMIPA Universitas Gadjah Mada.
Ambrogi, V., Fardella, G., Grandolini, G., and Perioli, L., 2001. Intercalation
Compounds of Hydrotalcite-like Anionic Clays with Anti-inflammatory
Agents, I: Intercalation and in vitro release of ibuprofen. International
Journal of Pharmaceutics, 220, 23-32.
Ambrogi, V., Fardella, G., Grandolini, G., Perioli, L., and Tiralti, C.M., 2002.
Intercalation Compounds of Hydrotalcite-like Anionic Clays with
Antiinflammatory Agents, II: Uptake of Diclofenac for a Controlled Release
Formulation. AAPS PharmSciTech, 3(3) article 26.
Ambrogi, V., Fardella, G., Grandolini, G., Nocchetti, M., and Perioli, L., 2003.
Effect of hydrotalcite-like compounds on the aqueous solubility of some
poorly water soluble drugs.Journal of Pharmaceutical Sciences, 92, 1407–
1418.
Anderson, G., 2003. Seawater Composition. Marine Science
Anonim, 1995. Farmakope Indonesia. Edisi ke-IV. Jakarta : Departemen Kesehatan Republik Indonesia.
Anonim, 2009. The British Pharmacopoeia. The Stationary Office under license