MIA KARFENY
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2011
ABSTRAK
MIA KARFENY. Degradasi in vitro Mikrosfer Polipaduan Poli(asam laktat) dengan
Poli(ε-kaprolakton). Dibimbing oleh TETTY KEMALA dan AHMAD SJAHRIZA.
Poli(asam laktat) (PLA) dan poli(ε-kaprolakton) (PCL) merupakan polimer yang
dapat digunakan sebagai matriks pengungkung obat karena sifatnya yang degradabel.
Sistem pengungkung obat tersebut dilakukan dengan cara pembuatan mikrosfer.
Mikrosfer dibuat dengan berbagai metode, salah satunya emulsifikasi. Penelitian ini
bertujuan mengamati degradasi secara in vitro mikrosfer polipaduan PLA-PCL pada pH
7.4. Tahapan penelitian ini adalah sintesis PLA, pembuatan polipaduan PLA-PCL,
pembuatan mikrosfer, pengamatan bentuk, dan uji degradasi secara in vitro. Sintesis PLA
menghasilkan bobot molekul 6064 g/mol. Mikrosfer dibuat dengan metode emulsifikasi
menggunakan polivinilalkohol (PVA) 1.5% (v/v) sebagai pengemulsi. Pengamatan
bentuk dilakukan dengan mikroskop stereo dan mikroskop elektron payaran (SEM). Uji
degradasi dilakukan selama 2 bulan pada pH 7.4, setiap minggu dianalisis bobot molekul
dan viskositasnya dengan viskometer sedangkan kehilangan bobot diukur dengan neraca
analitik. Hasil penelitian menunjukkan bahwa mikrosfer komposisi PLA:PCL 9:1
memiliki waktu degradasi lebih cepat daripada komposisi yang lain. Perbedaan komposisi
PLA dan PCL juga mempengaruhi struktur morfologi, viskositas, dan bobot mikrosfer
selama uji degradasi. Semakin besar komposisi PLA, semakin kecil nilai viskositas,
sehingga bobot molekul mikrosfer juga kecil. Selama masa degradasi nilai viskositas dan
%kehilangan bobot mikrosfer juga semakin menurun tiap minggunya. Kinetika
penurunan bobot mikrosfer mengikuti model kinetika antara orde nol dan orde kesatu.
ABSTRACT
MIA KARFENY. In Vitro Degradation of Polyblend of Poly(lactic acid) with
Poly(ε-caprolactone)
Microspheres.
Supervised
by
TETTY
KEMALA
and
AHMAD
SJAHRIZA.
Poly(lactic acid) (PLA) and poly(ε-caprolactone) (PCL) are examples of polymer
that can be used as a matrix in drug delivery system because of its degradability property.
Drug encapsulation system could be achieved by microspheres formation with emulsion
method. The aim of this research was to examine in vitro degradation of microspheres
obtained from PLA-PCL polyblend at pH 7.4. Several stages in the study consisted of
PLA synthesis, mixing of PLA-PCL in polyblend, microspheres formation, shape and
texture observation, and in vitro degradation test. Synthesis PLA produced a polymer
with molecular weight 6064 g/mol. Microspheres were formed by emulsification with
polyvinylalcohol (PVA) 1.5% (v/v) as an emulsifier. Physical texture of the microspheres
was observed with stereomicroscope and scanning electron microscope (SEM).
Degradation was analyzed weekly by measuring its molecular weight and viscosity using
a digital viscometer, while its weight loss was measured using an analytical balance. The
results showed that the composition of PLA microspheres: PCL (9:1) had degradation
time faster than the others and it also affected morphological structure, viscosity, and
weight of microsphere during degradation analysis. The higher the PLA composition the
lower the viscosity value, therefore, the lower the molecular weight of microspheres.
During degradation time, viscosity value and weight loss percentage decreased gradually.
Kinetics of microsphere weight loss followed between zero and first order kinetic model.
MIA KARFENY
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2011
Judul : Degradasi In Vitro Mikrosfer Polipaduan Poli(asam laktat) dengan
Poli(ε-kaprolakton)
Nama : Mia Karfeny
NIM
: G44062819
Menyetujui
Pembimbing I,
Pembimbing II,
Dr. Tetty Kemala, S.Si., M.Si.
Drs. Ahmad Sjahriza
NIP 19710407 199903 2 001
NIP 19620406 198903 1 002
Mengetahui:
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
Segala puji bagi Allah SWT berkat limpahan rahmat dan karunia-Nya
penulis dapat menyelesaikan karya ilmiah yang berjudul Degradasi In Vitro
Mikrosfer Polipaduan Poliasamlaktat dengan Polikaprolakton. Penelitian ini
dilaksanakan dari bulan Februari sampai September 2010 yang bertempat di
Laboratorium Kimia Anorganik, Departemen Kimia Fakultas Matematika dan
Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Terima kasih penulis ucapkan kepada Ibu Dr. Tetty Kemala, S.Si., M.Si. dan
Bapak Drs. Ahmad Sjahriza selaku pembimbing atas segala saran, kritik,
dorongan, dan bimbingannya selama penelitian. Selain itu, penulis sampaikan
terima kasih juga kepada Bapak Yani dari departemen Fisika dan seluruh pegawai
Laboratorium Kimia IPB yang membantu dan mempermudah saya dalam
menjalani penelitian ini.
Ungkapan terima kasih yang tak terhingga penulis sampaikan kepada Mama,
Papa, Kak Sumi, Mita dan seluruh keluarga atas nasihat, semangat, bantuan
materi, dan doa-doanya. Ucapan terima kasih kepada Rania, Evi, Peni, Siti, Nurul,
Nia, Wemby, Ningsih, teman-teman seperjuangan di Laboratorium Anorganik,
dan seluruh Kimia Angkatan 43 yang telah memberikan semangat, motivasi,
canda tawa dan dorongan; Kak Ikhsan, Kak Sulfi, dan Kak Nana yang banyak
membantu selama penelitian, memberi masukan, dan kritik dalam menyusun
karya ilmiah ini. Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Januari 2011
vi
RIWAYAT HIDUP
Penulis dilahirkan di Sumedang pada tanggal 5 Februari 1988 dari pasangan
Ano Sukarno dan Mimin Karmini. Penulis merupakan anak kedua dari tiga
bersaudara.
Tahun 2006 penulis lulus dari SMU Negeri 1 Sumedang dan pada tahun
yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis masuk Program Studi Kimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Penulis pernah menjadi asisten praktikum Kimia Dasar TPB pada tahun
ajaran 2009/2010, dan praktikum Kimia Polimer pada tahun 2009/2010. Pada
bulan Juli-Agustus 2009 penulis berkesempatan melaksanakan kegiatan Praktik
Lapangan di Laboratorium Quality Control PT Krakatau Tirta Industri di Cilegon.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ...
vi
DAFTAR TABEL ...
vi
DAFTAR LAMPIRAN ...
vii
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Biodegradasi polimer...
1
Poli(asam laktat) (PLA)...
2
Poli(ε-caprolakton) (PCL) ...
2
Poli(vinil alkohol)...
2
Mikrosfer ...
3
Mikroskop elektron payaran (SEM) ...
3
BAHAN DAN METODE
Alat dan bahan ...
3
Metode ...
3
HASIL DAN PEMBAHASAN
Sintesis poli(asam laktat)...
5
Mikrosfer ...
5
Perubahan morfologi mikrosfer...
7
Viskositas dan bobot mikrosfer ...
8
Kinetika penurunan bobot mikrosfer ...
9
SIMPULAN DAN SARAN
Simpulan ...
10
Saran ...
10
DAFTAR PUSTAKA ...
10
viii
DAFTAR TABEL
Halaman
1
Sifat fisik dan mekanis poli(asam laktat) ...
2
2
Sifat fisik poli(ε-kaprolakton) ...
2
3
Kinetika penurunan bobot mikrosfer ...
9
DAFTAR GAMBAR
Halaman
1
Struktur poli(asam laktat) ...
2
2
Struktur poli(ε-kaprolakton) ...
2
3
Struktur poli(vinil alkohol) ...
3
4
Skema SEM...
3
5
Hasil sintesis poli(asam laktat) ...
5
6
Persentase rendemen mikrosfer (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c)
PLA:PCL 7:3; (d) PLA:PCL 6:4...
5
7
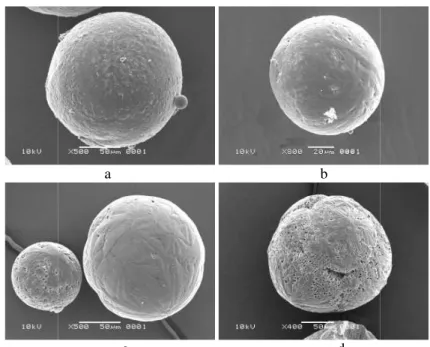
Foto SEM mikrosfer sebelum degradasi dengan perbesaran 800× (a)
PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d) PLA:PCL 6:4 ....
6
8
Foto SEM mikrosfer setelah degradasi 8 minggu dengan perbesaran
800× (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d)
PLA:PCL 6:4...
7
9
Foto Mikrosfer dengan mikroskop stereo pada minggu ke-8 dengan
perbesaran 40 X (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3;
(d) PLA:PCL 6:4 ...
8
10 Penurunan bobot mikrosfer selama 8 minggu...
8
DAFTAR LAMPIRAN
Halaman
1
Diagram alir kerja penelitian... 13
2
Penentuan bobot molekul poli(asam laktat)... 14
3
Persentase rendemen mikrosfer... 15
4
Gambar mikrosfer dengan mikroskop stereo ... 16
5
Penurunan bobot mikrosfer selama masa degradasi ... 20
6
Viskositas mikrosfer selama masa degradasi ... 24
PENDAHULUAN
Polimer adalah makromolekul yang
memiliki bobot molekul besar dan dibangun dari pengulangan unit monomer. Polimer dengan bobot molekul rendah yang hanya terdiri dari beberapa unit monomer disebut oligomer (Steven 2000). Polimer terdiri atas polimer biodegradabel dan polimer non-degradabel. Polimer biodegradabel merupakan polimer yang dapat terurai secara biologis. Poli(asam laktat) (PLA), poli(ε-kaprolakton) (PCL), dan poli(asam glikoat) (PGA) merupa-kan contoh polimer biodegradabel sintetik.
Poli(asam laktat) dapat disintesis melalui
polikondensasi langsung. Metoda ini
merupakan metoda paling murah untuk
menghasilkan PLA, namun sangat sulit untuk mendapatkan PLA dengan bobot molekul yang tinggi (Averous 2008). Sintesis PLA
umumnya menggunakan katalis Sn(Oct)5
(Steven 2001). Logam dari katalis ini bersifat
toksik dan sulit dipisahkan bila sudah
berikatan dengan polimer, sehingga akan berbahaya untuk PLA yang diaplikasikan sebagai kebutuhan medis (Badami 2004).
Hasil penelitian Rusmana (2009)
menunjukkan PLA disintesis dengan
polikondensasi langsung tanpa menggunakan katalis menghasilkan berat molekul yang tidak
jauh berbeda dengan sintesis PLA
menggunakan katalis. Pencampuran PLA
dengan polimer lain seperti PCL atau PLGA memiliki fungsi yang lain seperti pembuatan plastik dan sebagai pengukung obat.
PCL digunakan sebagai pengukung obat karena mempunyai permeabilitas obat yang baik, memiliki kekuatan mekanik yang cukup baik, tapi memiliki waktu degradasi dalam tubuh lebih dari 24 bulan. Menurut Gunatilake dan Adhikari (2003) sistem pengukung obat merupakan salah satu aplikasi modifikasi pencampuran PCL dengan polimer lain yang memiliki berat molekul yang lebih rendah.
Penggabungan PCL dan PLA dapat
menurunkan sifat degradibilitas dan memiliki banyak keuntungan karena dapat didegradasi oleh proses hidrolisis dalam tubuh sehingga dapat digunakan sebagai sistem transplantasi atau pengukung obat (Lu & Chen 2004).
Sistem pengukung obat dilakukan dengan cara pembuatan mikrosfer yang berbahan
dasar polimer biodegradabel. Pembuatan
mikrosfer dilakukan dengan berbagai metode seperti emulsifikasi, pemisahan fase, dan pengeringan semprot. Pembuatan mikrosfer
dengan metode emulsifikasi mempunyai
keuntungan lebih, yakni akan mendapatkan
mikrosfer dengan diameter sesuai dengan yang diinginkan sehingga dapat digunakan sebagai pengungkung obat (Jain 2000). PLA dan PCL dalam diklorometana tidak dapat bercampur dengan air karena perbedaan bobot
jenis dan kepolaran. Kecepatan putar
pengadukan yang tinggi akan membentuk suatu emulsi antara air dan diklorometana sehingga keduanya terlihat satu fase pada awalnya tetapi semakin lama akan terlihat
perbedaan fase. Penambahan poli(vinil
alkohol) (PVA) ke dalam air berfungsi
sebagai pengemulsi. Gugus hidroksi dari PVA yang bersifat polar akan berinteraksi dengan molekul air, sedangkan rantai vinilnya akan berinteraksi dengan molekul diklorometana
sehingga emulsi menjadi lebih stabil.
Penggabungan PLA dan PCL dapat
menurunkan sifat degradibilitas. Perbedaan
komposisi penggabungan PLA dan PCL
mempengaruhi perbedaan dalam aplikasinya. PLA dan PCL memiliki sifat mekanik
berbeda yang apabila dicampurkan akan
menghasilkan polipaduan. Nurhayani (2008) telah melakukan penelitian tentang degradasi polipaduan PLA dan PCL yang diaplikasikan dalam pembuatan plastik. Pada penelitian ini polipaduan PLA dan PCL dibuat untuk
pembuatan mikrosfer yang diaplikasikan
sebagai pengukung obat. Penelitian bertujuan mengamati degradasi secara in vitro mikrosfer polipaduan PCL dan PLA pada pH 7.4 menggunakan pengemulsi PVA 1.5 %.
TINJAUAN PUSTAKA
Polimer Biodegradabel
Averous (2008) mengelompokkan polimer biodegradabel ke dalam dua kelompok, yaitu yang pertama agropolimer yang terdiri dari
polisakarida, protein, dan yang kedua
biopoliester seperti PLA, polihidroksi
alkanoat (PHA) dan poliester alifatik. Polimer biodegradabel adalah polimer yang dapat terdegradasi karena mikroorganisme.
Degradasi adalah proses terurainya suatu senyawa menjadi lebih sederhana. Proses degradasi melibatkan fotodegradasi (degradasi yang melibatkan cahaya), degradasi kimiawi
(hidrolisis), degradasi enzimatik, dan
degradasi mekanik (angin, abrasi) (Latief 2001). Degradasi dapat terjadi melalui empat tahap, yaitu penyerapan air, pengurangan
kekuatan mekaniknya (modulus dan
kekuatan), pengurangan masa molar, dan kehilangan bobot.
Poli(asam laktat)
Poli(asam laktat) (Gambar 1) merupakan polimer sintetik yang bersifat biodegradabel dan biokompatibel. PLA dapat terdegradasi secara alami oleh panas, cahaya, bakteri, maupun oleh proses hidrolisis. PLA dapat terdegradasi dalam tubuh tanpa menimbulkan efek yang berbahaya, bersifat termoplastik,
dan termasuk dalam kelompok poliester
alifatik. Polimer ini tidak larut dalam air tetapi larut dalam pelarut organik seperti kloroform dan diklorometana (Algaer 1989). PLA dapat
disintesis dari pembukaan cincin laktida
dengan penambahan katalis seperti PbO, SbF5,
Sn (Oct)5atau pemanasan pada suhu 140 °C
(Ajioka 1995 dan Baimarck 2004).
n
CH3 O HC C
O
Gambar 1 Struktur poli(asam laktat). PLA mempunyai titik leleh yang tinggi dan dapat dibuat menjadi lembaran film yang transparan. Sifat fisik PLA disajikan dalam Tabel 1. Sifat fisik dan mekanis PLA dapat berubah apabila dicampur dengan polimer lain (Lu&Chen 2004).
Tabel 1 Sifat fisik poli(asam laktat)
Sifat Fisik Poli(asam laktat)
Suhu Transisi Kaca (°C) 55-75
Titik leleh (°C) 130-215
Kuat tarik (Mpa) 49
Elongasi (%) 2.5
Densitas (g/cm3) 1.25
Sumber : Lu&Chen 2004
PLA dapat berada dalam bentuk optis aktif (L-PLA) dan (D,L-PLA) atau dalam bentuk campuran rasemiknya yang tidak bersifat optis
aktif. L-PLA yang terdapat di alam
mempunyai struktur kristalin dengan derajat kristalinitas sekitar 37%. Bentuk D,L-PLA mempunyai struktur amorf karena rantai polimernya tidak teratur. Umumnya polimer ini tersusun dari campuran struktur kristalin dan amorf, dengan struktur yang dominan akan mempengaruhi sifat mekanik polimer
tersebut. Bentuk D,L-PLA lebih disukai
daripada L-PLA karena lebih mampu
didispersikan obat secara homogen dalam matriks polimer (Gonzales 1999).
Poli(ε-kaprolakton)
Poli(ε-kaprolakton) (Gambar 2) merupa-kan polimer semikristalin bersifat termo-plastik. Plastik biodegradabel ini disintesis dari turunan minyak mentah melalui proses polimerisasi pembukaan cincin kaprolakton.
PCL memiliki sifat tahan terhadap air,
minyak, dan klorin, mempunyai titik leleh, dan kekentalan yang rendah (Flieger et al. 2003).
n O (CH2)5 C
O
Gambar 2 Struktut poli(ε-kaprolakton).
Pencampuran PCL dengan polimer
berbentuk serat (seperti selulosa) dapat
menghasilkan polimer yang biodegradabel. Laju rata-rata hidolisis dan biodegradasi PCL bergantung pada bobot molekul dan derajat kristalinitas. Namun, banyak jenis mikrob di alam yang mampu mendegradasi PCL. Sifat
fisik poli(ε-kaprolakton) disajikan dalam
Tabel 2.
Tabel 2 Sifat fisik poli(ε-kaprolakton)
Sifat fisik Poli(ε-kaprolaktan)
Suhu transisi kaca (°C) -60
Titik leleh (°C) 60
Kuat tarik (MPa) 4
Elongasi (%) 800-1000
Densitas (g/cm3) 1,145
Sumber : Lu&Chen 2004
Poli(vinil alkohol)
Poli(vinil alkohol) (Gambar 3) adalah polimer yang terbentuk dari vinil alkohol. PVA terbentuk ketika banyak molekul vinil alkohol terhubung secara bersama membentuk polimer yang panjang (Flieger et al. 2003). PVA dibuat dari monomernya vinil asetat, PVA dijual dalam bentuk emulsi dalam air sebagai bahan perekat seperti kayu. PVA juga dapat digunakan untuk melindungi keju dari
jamur dan kelembaban. PVA bereaksi
perlahan dengan basa dan membentuk asam asetat sebagai hasil hidrolisis.
PVA berfungsi sebagai pengemulsi dalam pembuatan mikrosfer. Gugus hidroksi dari PVA yang bersifat polar akan berikatan dengan molekul air sedangkan rantai vinilnya akan berikatan dengan molekul diklorometana sehingga emulsi menjadi lebih stabil (Robani 2007).
CH OH
Gambar 3 Struktur poli
Mikrosfer
Mikrosfer adalah partikel berbentuk bola berskala mikron, yang terbuat dari bahan keramik, kaca, atau polimer yang digunakan
sebagai pengungkung gas, larutan atau
padatan dalam bentuk senyawa organik
maupun anorganik (Sudaryanto 2003).
Mikrosfer dapat dibuat dengan banyak cara, salah satunya dengan cara melarutkan bahan dasar mikrosfer meggunakan pelarut atsiri kemudian mendispersikan dalam pelarut lain
yang tak campur. Setelah itu, dengan
menguapkan pelarut awaln mikrosfer berupa serbuk halus yang tak larut dalam air.
Ukuran mikrosfer beragam sesuai dengan
fungsinya berkisar antara 1
Menurut Jain (2000), u
sebagai pembawa obat tidak boleh lebih besa dari 250 μm, idealnya <125 μm. M mikrosfer dan pelepasan obat harus didapat secara berulang dalam batas yang ditetapkan, dan mikrosfer yang didapat harus berupa
serbuk murni tanpa pengotor dan tidak
berbentuk agregat atau
Keunggulan lain dari mi
pelepasan obatnya dalam tubuh terjadi secara bertahap sehingga cocok untuk membawa obat-obat yang dibutuhkan oleh tubuh dalam jumlah yang tetap dan terus menerus seperti hormon (Xing et al. 1999).
Mikroskop Elektron Payaran
Mikroskop elektron payaran (SEM) adalah mikroskop yang menggunakan pancaran sinar yang timbul akibat eksitasi elektro
melihat partikel berukuran mikro. Sejak tahun
1950, SEM dikembangkan dan banyak
digunakan dalam bidang medis maupun dalam pengembangan ilmu pengetahuan. SEM telah banyak digunakan oleh para peneliti untuk menguji dan menemukan berbagai spesimen. Dibandingkan dengan mikros
sional, SEM dapat menunjukkan gambar spesimen dengan jelas dan memiliki tingkat resolusi lebih tinggi.
SEM mampu memfoto suatu permukaan
dengan perbesaan dari 20
Prinsip kerja SEM adalah permuka
dibombardir oleh elektron berenergi tinggi
CH2
n
Struktur poli(vinil alkohol).
Mikrosfer
Mikrosfer adalah partikel berbentuk bola berskala mikron, yang terbuat dari bahan keramik, kaca, atau polimer yang digunakan
sebagai pengungkung gas, larutan atau
padatan dalam bentuk senyawa organik
anik (Sudaryanto 2003).
Mikrosfer dapat dibuat dengan banyak cara, salah satunya dengan cara melarutkan bahan dasar mikrosfer meggunakan pelarut atsiri kemudian mendispersikan dalam pelarut lain
yang tak campur. Setelah itu, dengan
menguapkan pelarut awalnya, dapat diperoleh mikrosfer berupa serbuk halus berukuran kecil eragam sesuai dengan
berkisar antara 1-1000 µm.
Menurut Jain (2000), ukuran mikrosfer
tidak boleh lebih besar 250 μm, idealnya <125 μm. Mutu mikrosfer dan pelepasan obat harus didapat secara berulang dalam batas yang ditetapkan, dan mikrosfer yang didapat harus berupa
serbuk murni tanpa pengotor dan tidak
berbentuk agregat atau menggumpal.
Keunggulan lain dari mikrosfer adalah sifat pelepasan obatnya dalam tubuh terjadi secara bertahap sehingga cocok untuk membawa obat yang dibutuhkan oleh tubuh dalam jumlah yang tetap dan terus menerus seperti
1999).
Mikroskop Elektron Payaran (SEM)
roskop elektron payaran (SEM) adalah mikroskop yang menggunakan pancaran sinar timbul akibat eksitasi elektron untuk melihat partikel berukuran mikro. Sejak tahun
1950, SEM dikembangkan dan banyak
digunakan dalam bidang medis maupun dalam ilmu pengetahuan. SEM telah banyak digunakan oleh para peneliti untuk menguji dan menemukan berbagai spesimen. Dibandingkan dengan mikroskop konven-sional, SEM dapat menunjukkan gambar spesimen dengan jelas dan memiliki tingkat mampu memfoto suatu permukaan
dengan perbesaan dari 20–100.000 kali.
Prinsip kerja SEM adalah permukaan contoh tron berenergi tinggi
dengan energi kinetik antara 1
Elektron yang langsung menumbuk contoh ini
dinamakan elektron primer sedangkan
elektron yang terpantul dari contoh dinamakan elektron sekunder. Elektron sekunder yang berenergi rendah dilepaskan dari atom
yang ada pada permukaan contoh dan
menentukan bentuk rupa contoh. Skema SEM tersaji di Gambar 3.
Sampel dalam pengukuran menggunakan
SEM harus merupakan zat yang dapat
menghantarkan arus listrik atau dilapisi
dengan logam yang dapat menghantarkan arus listrik. Dua alasan utama untuk melapisi sampel yang tidak dapat menghantarkan arus listrik adalah untuk mengurangi artifak yang disebabkan oleh beban elektrik dan muatan termal (Mulder 1996). Logam emas lebih disukai sebagai lapisan penghantar listrik
karena emas merupakan
sehingga tidak turut bereaksi dengan PLA maupun PLC.
Gambar 4 Skema SEM.
BAHAN DAN METODE Alat dan Bahan
Alat-alat yang digunakan adalah peralatan gelas, alat pengaduk, viskometer
TV-10, SEM merk Jeol seri JSM
dan mikroskop stereo merk Kruss Optronic Germany.
Bahan-bahan yang digunakan adalah
asam laktat p.a, PCL (BM 42.000 g/mol) berasal dari Sigma-Aldrich
g/mol) berasal dari Merck, diklorometana berasal dari Bratachem, buffer fosfat
dan akuades.
Metode
Metode penelitian yang telah dilakukan mengikuti diagram alir pada Lampiran 1 Metode penelitian meliputi sintesis PLA,
3
energi kinetik antara 1-25 kV.
Elektron yang langsung menumbuk contoh ini
dinamakan elektron primer sedangkan
elektron yang terpantul dari contoh dinamakan elektron sekunder. Elektron sekunder yang berenergi rendah dilepaskan dari atom-atom
permukaan contoh dan
menentukan bentuk rupa contoh. Skema SEM Sampel dalam pengukuran menggunakan
SEM harus merupakan zat yang dapat
menghantarkan arus listrik atau dilapisi
dengan logam yang dapat menghantarkan arus n utama untuk melapisi sampel yang tidak dapat menghantarkan arus listrik adalah untuk mengurangi artifak yang disebabkan oleh beban elektrik dan muatan termal (Mulder 1996). Logam emas lebih disukai sebagai lapisan penghantar listrik
karena emas merupakan logam lembam
sehingga tidak turut bereaksi dengan PLA
Skema SEM.
BAHAN DAN METODE Alat dan Bahan
gunakan adalah peralatan viskometer Ostwald dan , SEM merk Jeol seri JSM-6360LA, merk Kruss Optronic
bahan yang digunakan adalah
, PCL (BM 42.000 g/mol) Aldrich, PVA (BM 72.000 g/mol) berasal dari Merck, diklorometana buffer fosfat pH 7.4,
Metode
Metode penelitian yang telah dilakukan mengikuti diagram alir pada Lampiran 1. meliputi sintesis PLA,
pembuatan polipaduan PLA-PCL, pembuatan mikrosfer, uji degradasi selama 8 minggu,
karakterisasi dengan mengukur nilai
viskositas dan bobot mikrosfer tiap minggu, dan pengamatan bentuk mikrosfer dengan fotomikroskop dan SEM.
Pembuatan PLA (Rusmana 2009 &
Gonzales, Ruseckaite, Cuadrado 1999)
Pembuatan PLA tanpa katalis dapat dibuat
optimal pada suhu 150 °C selama 24 jam.
Gelas piala 100 mL dibersihkan, dikeringkan, dan ditimbang bobotnya. Lalu asam laktat sebanyak 25 mL dimasukkan ke dalam gelas piala dan ditimbang. Selanjutnya, asam laktat tersebut dipanaskan secara perlahan-lahan sampai suhu 120 ºC selama 1 jam. Pemanasan
dilanjutkan sampai suhu 150 °C selama 24
jam. Kemudian PLA yang dihasilkan
didinginkan pada suhu ruang dan ditimbang.
Pembuatan Campuran PLA-PCL
(Nurhayani 2007)
Campuran PLA dengan PCL disiapkan
dengan komposisi total 1 gram dan
perbandingan komposisi PLA terhadap PCL 9:1, 8:2, 7:3, dan 6:4. Pembuatan dilakukan
dengan mencampurkan masing-masing
polimer, kemudian dilarutkan menggunakan 10 ml diklorometana, sehingga didapatkan larutan campuran. Larutan kemudian diaduk dengan pengaduk magnet sampai homogen.
Pembuatan Mikrosfer Polipaduan dan
PVA (Hasanah 2009 & Dinarvand R et al. 2003)
Masing-masing komposisi polipaduan
diemulsikan dalam 10 ml PVA 1.5%
menggunakan motor pengaduk dengan
kecepatan putar 600 rpm selama 30 menit. Emulsi tersebut didispersikan ke dalam gelas piala berisi 300 ml akuades sambil diaduk
menggunakan motor pengaduk dengan
kecepatan 900 rpm selama 90 menit. Setelah itu, campuran didekantasi hingga mikrosfer
yang terbentuk mengendap. Endapan
kemudian dicuci dengan akuades.
Selanjutnya, endapan mikrosfer disaring untuk memisahkan endapan tersebut dengan air lalu dibilas sebanyak tiga kali dengan akuades. Mikrosfer yang diperoleh dikeringudarakan selama 1 hari, lalu dikeringkan di dalam oven pada suhu 40 ºC selama 1 jam. Mikrosfer yang didapatkan diamati bentuknya dengan menggunakan SEM.
Pengamatan Bentuk Menggunakan
Mikroskop dan SEM
Permukaan sampel diamati menggunakan mikroskop stereo. Setiap 2 minggu, sampel diambil beberapa milligram lalu diletakkan di atas kaca preparat dan diamati permukaannya dengan mengatur perbesaran pada mikroskop sehingga bentuk permukaan sampel dapat teramati dengan baik. Pada minggu ke-nol dan
minggu ke-8, bentuk permukaan sampel
diamati pula menggunakan SEM. Beberapa miligram mikrosfer dikeringkan hingga bebas air yang dapat menguap ketika ditambahkan elektron. Sampel selanjutnya diletakkan pada pelat alumunium yang memiliki dua sisi kemudian dilapisi dengan lapisan emas setebal 48 nm. Sampel yang telah dilapisi diamati menggunakan SEM dengan tegangan 15 kV dan perbesaran 800x.
Degradasi Polipaduan secara In Vitro
(Kaitian et al. 1996)
Semua mikrosfer PLA-PCL setiap minggu diamati degradasinya dan dihitung perubahan massa sampel (kehilangan bobot), viskositas,
dan bobot molekulnya. Sampel direndam
dalam buffer pH 7.4 lalu diinkubasi pada suhu
37 °C di analisis tiap minggu selama 8
minggu.
Setiap mikrosfer dari masing-masing
komposisi diambil dan dikeringkan pada suhu ruang lalu ditimbang perubahan massanya dengan neraca analitik setiap minggunya. Setelah itu, sampel dilarutkan menggunakan pelarut diklorometana sampai homogen lalu
ditera menggunakan labu takar 25 mL.
Larutan dipipet sebanyak 20 mL ke dalam viskometer Ostwald pada suhu 25 °C (suhu
konstan) untuk menentukan waktu alir
sampel. Setelah itu, viskositas relatif (ηr)
ditentukan dengan cara membandingkan
waktu alir pelarut dengan waktu alir larutan
polimer (t0/t). Viskositas intrinsik [η] dicari
dengan cara memplotkan ηspesifik/[PLA]
sebagai sumbu y dan konsentrasi sebagai sumbu x.
Bobot molekul (Mv) dan bobot molekul
rata-rata ditentukan berdasarkan persamaan Mark-Houwink:
[η] = k(Mv)a
k dan a merupakan tetapan yang bergantung
pada pelarut, polimer, dan suhu. Nilai k dan a secara berturut-turut dengan menggunakan
pelarut etil asetat pada suhu 25 °C adalah
5
HASIL DAN PEMBAHASAN
Sintesis Poli(asam laktat)
Sintesis poli(asam laktat) dalam penelitian ini menggunakan metode polikondensasi asam laktat secara langsung dengan suhu tinggi tanpa menggunakan katalis. Tahap awal pada
pembuatan PLA, monomer asam laktat
dipanaskan terlebih dahulu selama 1 jam pada
suhu 120 °C. Hal ini bertujuan melepaskan
molekul air dan pembentukan dimer asam laktat. Setelah itu, suhu dinaikkan menjadi
150 °C selama 24 jam, pada tahap ini terjadi
pembukaan cincin laktida (Ajioka 1995).
Semakin tinggi suhu pemanasan akan
menghasilkan residu karbon yang banyak dan
terjadi oksidasi yang berlebih sehingga
menghasilkan warna PLA yang lebih pekat atau gelap (Rusmana 2009), sehingga lamanya pemanasan mempengaruhi warna hasil PLA.
Hasil PLA yang diperoleh berwarna
kuning muda (Gambar 5), akan tetapi
memiliki bobot molekul lebih rendah yaitu 6064.18 g/mol. Hal ini disebabkan oleh kondisi penghilangan uap air oleh pompa
vakum yang kurang optimum. Menurut
Kaitian et al. (1995) PLA yang memiliki bobot molekul lebih rendah disebabkan oleh
keberadaan molekul air yang masih
terkandung pada asam laktat sehingga
mengganggu proses polimerisasi dan
mempengaruhi rendemen PLA.
Gambar 5 Hasil sintesis poli(asam laktat). Rendemen PLA yang diperoleh dari hasil sintesis ini sebanyak 15.2021 gram dari bobot awal monomer asam laktat 29.4931 gram (25 mL). Rendemen diukur menggunakan neraca analitik sedangkan pengukuran bobot molekul PLA menggunakan viskometer ostwald yang dihitung berdasarkan laju alirnya.
Pengukuran bobot molekul dari PLA hasil
sintesis menggunakan metode viskometri
dapat dilihat pada Lampiran 2. Pelarut yang
digunakan adalah etil asetat
.
Pelarut etil asetatdigunakan pada pengukuran bobot molekul PLA karena sifatnya yang nonpolar, tidak
beracun, dan tidak higroskopis. Fungsi
penangas air pada pengukuran bobot molekul ialah untuk menjaga suhu agar tetap konstan pada suhu 25 °C. PLA yang dihasilkan dari sintesis ini kemungkinan berupa campuran
rasemiknya (D,L-PLA) karena menurut
Dutkiewicz et al. (2003) PLA yang disintesis
pada suhu lebih dari 140 оC akan dihasilkan
bentuk rasemiknya. PLA dalam bentuk D,L-PLA memiliki waktu degradasi yang lebih cepat dibandingkan L-PLA (Lu & Chen 2004).
Mikrosfer
Mikrosfer dibuat dari polipaduan PLA
dengan PCL menggunakan metode
emulsifikasi. Pengemulsi yang digunakan
adalah PVA 1.5 % karena memiliki efisiensi
enkapsulasi yang optimum. Efisiensi
mikroenkapsulasi memperlihatkan seberapa besar suatu senyawa atau obat dapat tersalut baik oleh polimer (Kemala 2010). Setelah emulsifikasi, polipaduan didispersi dengan akuades dengan sitem penguapan pelarut minyak dalam air (o/w).
Saat emulsi didispersikan dengan akuades,
volume akuades berpengaruh dalam
menghasilkan endapan mikrosfer karena
volume akuades yang sedikit atau terlalu berlebih akan menghasilkan mikrosfer yang pecah ditandai adanya gelembung saat proses
pendispersian. Hal ini disebabkan oleh
kestabilan mikrosfer yang terbentuk antara air
dan polipaduan yang telah mengalami
emulsifikasi dengan PVA pecah. Mikrosfer dikering-udarakan selama 1 hari kemudian dikeringkan lagi dengan menggunakan oven pada suhu di bawah 40°C agar mikrosfer tidak
rusak dan tidak menggumpal sehingga
diperoleh mikrosfer berupa serbuk halus. Menurut Jain (2000) mikrosfer yang diperoleh berupa serbuk murni tanpa pengotor dan tidak
berbentuk agregat atau menggumpal.
Mikrosfer yang menggumpal akan
mempengaruhi rendemen mikrosfer.
Rendemen mikrosfer yang diperoleh
dalam penelitian berkisar antara 61-71%. Ulangan ke-1, ke-3, dan ke-4 menunjukkan
mikrosfer nisbah PLA:PCL 6:4 bobot
rendemennya paling besar. Pada ulangan ke-2, bobot rendemen paling besar terdapat pada mikrosfer nisbah PLA:PCL 7:3 (Lampiran 3). Berdasarkan hasil penelitian, rendemen rata-rata mikrosfer dengan nisbah PLA:PCL 6:4
menghasilkan rendemen paling banyak
Gambar 6 Persentase Rendemen Mikrosfer
( ) PLA:PCL 9:,1( ) PLA : PCL
8:2, ( ) PLA:PCL 7:3, ( )
PLA:PCL 6:4.
Mikrosfer yang dihasilkan dengan nisbah PLA:PCL 9:1 memiliki struktur mikrosfer
yang lebih padat apabila dilihat dari
permukaannya (Gambar 7
nisbah PLA:PCL 6:4 sedikit rusak terlihat dari permukaannya yang berlubang mempunyai pori-pori cukup banyak di minggu ke PCL memiliki titik leleh 60
Gambar 7 Foto SEM mikrosfer dengan perbesaran PLA:PCL 7:3; (d) 60.00 62.00 64.00 66.00 68.00 70.00 72.00 % re nd em en nisbah PLA:PCL
Gambar 6 Persentase Rendemen Mikrosfer
( ) PLA:PCL 9:,1( ) PLA : PCL
8:2, ( ) PLA:PCL 7:3, ( )
PLA:PCL 6:4.
Mikrosfer yang dihasilkan dengan nisbah PLA:PCL 9:1 memiliki struktur mikrosfer
yang lebih padat apabila dilihat dari
7). Mikrosfer dengan nisbah PLA:PCL 6:4 sedikit rusak terlihat dari permukaannya yang berlubang mempunyai ukup banyak di minggu ke-nol.
leleh 60 °C sehingga
memungkinkan mikrosfer
kondisi suhu yang panas saat penyimpanan atau saat proses preparasi pengeringan sampel sebelum dilakukan SEM
minggu ke-nol.
Mikrosfer yang dihasilkan berbentuk bulat padat, berwarna putih, dan berukuran mikron. Foto SEM digunakan untuk melihat struktur mikrosfer dengan lebih jelas. Penglihatan
mikrosfer melalui mikroskop dengan
perbesaran 40x hanya menggambarkan
mikrosfer secara keseluruhan. Mikrosfer yang di dapat di penelitian ini rata
ukuran yang seragam. Menurut (2005) keseragaman dan ukuran bergantung pada kecepatan putar
tinggi kecepatan putar maka mikrosfer yang dihasilkan akan lebih seragam dan ukurannya lebih kecil. Kecepatan dan waktu dispersi yang dilakukan di penelitian ini merujuk pada Hasanah (2009) tentang optimasi pembuatan mikrosfer polipaduan PLA dan PCL, yaitu menggunakan kecepatan putar 900
lama dispersi 90 menit.
a b
c d
mikrosfer dengan perbesaran 800× (a) PLA:PCL 9:1; (b) ; (d) PLA:PCL 6:4.
1
nisbah PLA:PCL
memungkinkan mikrosfer sudah rapuh pada kondisi suhu yang panas saat penyimpanan atau saat proses preparasi pengeringan sampel sebelum dilakukan SEM walaupun masih di ikrosfer yang dihasilkan berbentuk bulat padat, berwarna putih, dan berukuran mikron. Foto SEM digunakan untuk melihat struktur mikrosfer dengan lebih jelas. Penglihatan
mikrosfer melalui mikroskop dengan
perbesaran 40x hanya menggambarkan
keseluruhan. Mikrosfer yang di dapat di penelitian ini rata-rata memilki Menurut Zang et al. (2005) keseragaman dan ukuran mikrosfer kecepatan putar. Semakin tinggi kecepatan putar maka mikrosfer yang ebih seragam dan ukurannya . Kecepatan dan waktu dispersi yang dilakukan di penelitian ini merujuk pada Hasanah (2009) tentang optimasi pembuatan mikrosfer polipaduan PLA dan PCL, yaitu menggunakan kecepatan putar 900 rpm dan
Perubahan Morfologi
Mikrosfer yang awalnya memiliki
permukaan halus dan pejal menjadi tida halus lagi dan berubah bentuk
kualitatif ini bertujuan melihat perubahan
morfologi mikrosfer sebelum, saat, dan
setelah degradasi dengan komposisi penyusun polipaduan mikrosfer yang berbeda.
morfologi mikrosfer dilakukan dengan waktu degradasi pada minggu ke 0, 2, 4, 6, dan 8 dengan mikroskop stereo perbesaran 40 X dan dengan SEM pada minggu ke
Pengamatan menggunak lihatkan permukaan mikrosfer
sehingga terlihat mikrosfer dalam penelitian ini yang awalnya permukaan halus dan berpori sedikit sudah rusak pada minggu ke (Gambar 8). Bentuk mikrosfer sebagian ada
yang pecah menjadi molekul
mikrosfer dan sebagian lagi ada yang terkikis dan lepas dari permukaan mikrosfer awalnya.
Pengamatan hasil degradasi morfologi
mikrosfer menunjukkan bahwa adanya
perbedaan morfologi dari tiap mikrosfer. Perubahan morfologi mikrosfer terjadi secara bertahap pada tiap minggun
dengan nisbah PLA:PCL pada minggu ke
sudah banyak yang rusak atau pecah
(Lampiran 4.a), begitupun dengan mikrosfer
yang memiliki nisbah PLA:PCL 8:2
(Lampiran 4.b). Mikrosfer yang memilik nisbah PLA:PCL 7:3 (Lampiran
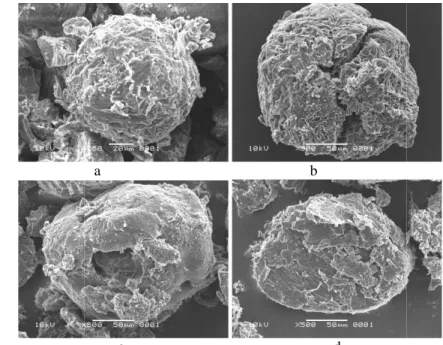
Gambar 8 Foto SEM mikrosfer setelah degradasi 8 minggu dengan perbesaran 800× (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d) PLA:PCL 6:4.
Perubahan Morfologi Mikrosfer
Mikrosfer yang awalnya memiliki
permukaan halus dan pejal menjadi tidak halus lagi dan berubah bentuk. Analisis kualitatif ini bertujuan melihat perubahan
morfologi mikrosfer sebelum, saat, dan
setelah degradasi dengan komposisi penyusun uan mikrosfer yang berbeda. Pencirian morfologi mikrosfer dilakukan dengan waktu degradasi pada minggu ke 0, 2, 4, 6, dan 8 dengan mikroskop stereo perbesaran 40 X dan dengan SEM pada minggu ke-nol dan ke-8. Pengamatan menggunakan SEM memper-permukaan mikrosfer dengan jelas mikrosfer dalam penelitian ini yang awalnya permukaan halus dan berpori sedikit sudah rusak pada minggu ke-8 ). Bentuk mikrosfer sebagian ada
yang pecah menjadi molekul-molekul
gian lagi ada yang terkikis dan lepas dari permukaan mikrosfer awalnya.
Pengamatan hasil degradasi morfologi
mikrosfer menunjukkan bahwa adanya
perbedaan morfologi dari tiap mikrosfer. Perubahan morfologi mikrosfer terjadi secara bertahap pada tiap minggunya. Mikrosfer dengan nisbah PLA:PCL pada minggu ke-2
sudah banyak yang rusak atau pecah
), begitupun dengan mikrosfer
i nisbah PLA:PCL 8:2
). Mikrosfer yang memiliki nisbah PLA:PCL 7:3 (Lampiran 4.c) dan 6:4
(Lampiran 4.d) hanya sedikit pecah. Degradasi pada minggu ke
memperlihatkan kerusakan sampel di setiap nisbah PLA:PCL. Mikrosfer pada minggu ke 8 hampir semua sudah rusak.
nisbah mikrosfer PLA:PCL 6:4 masih ada sebagian mikrosfer yang berbentuk utuh bulat, tidak semuanya rusak seperti mikrosfer lain (Gambar 9). Hal ini dapat dikatakan bahwa
semakin banyak kandungan PLA yang
menyusun polipaduan mikrosfer maka
degradasi mikrosfer semakin cepat. Polimer penyusun mikrosfer mempernga
degradasi.
Secara umum, proses degradasi pada perusakan mikrosfer diawali dengan proses
perusakan langsung pada permukaan
mikrosfer. Mikrosfer yang telah terdegradasi umumnya masih memiliki bentuk bulat hanya permukaannya sudah rusak
beberapa mirosfer yang sudah pecah.
Permukaan mikrosfer yang awalnya rusak
menyebabkan air buffer mudah meresap
sehingga ikatan antar molekul polipaduan
menjadi melemah dan molekul
mikrosfer pecah menjadi molekul
baru dan ada pula sebagian mikrosfer terkikis dari mikrosfer awalnya (Kemala
Pori-pori mikrosfer juga menjadi lebih besar seperti lubang-lubang besar pada permukaan mikrosfer sehingga bentuk mikrosfer tidak beraturan.
a b
c d
Foto SEM mikrosfer setelah degradasi 8 minggu dengan perbesaran 800× (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d) PLA:PCL 6:4.
7
) hanya sedikit yang rusak atau pecah. Degradasi pada minggu ke-4 dan ke-6 memperlihatkan kerusakan sampel di setiap nisbah PLA:PCL. Mikrosfer pada minggu ke-8 hampir semua sudah rusak. Namun, pada nisbah mikrosfer PLA:PCL 6:4 masih ada er yang berbentuk utuh bulat, seperti mikrosfer lain Hal ini dapat dikatakan bahwa
semakin banyak kandungan PLA yang
menyusun polipaduan mikrosfer maka
degradasi mikrosfer semakin cepat. Polimer penyusun mikrosfer memperngaruhi proses proses degradasi pada awali dengan proses
perusakan langsung pada permukaan
mikrosfer. Mikrosfer yang telah terdegradasi umumnya masih memiliki bentuk bulat hanya udah rusak walaupun ada pula
beberapa mirosfer yang sudah pecah.
Permukaan mikrosfer yang awalnya rusak
menyebabkan air buffer mudah meresap
sehingga ikatan antar molekul polipaduan
menjadi melemah dan molekul-molekul
mikrosfer pecah menjadi molekul-molekul sebagian mikrosfer terkikis (Kemala et al 2010). pori mikrosfer juga menjadi lebih besar lubang besar pada permukaan mikrosfer sehingga bentuk mikrosfer tidak
a
c
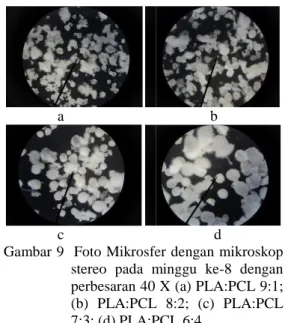
Gambar 9 Foto Mikrosfer dengan mikroskop stereo pada minggu ke
perbesaran 40 X (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d) PLA:PCL 6:4.
Viskositas dan Penurunan Bobot
Degradasi mikrosfer dilakukan selama 8 minggu direndam dengan buffer fosfat pH 7.4
pada suhu 37 °C yang disesuaikan dengan
kondisi pH dalam darah dan suhu tubuh manusia yang sehat. Perubahan morfologi mikrosfer telah menjelaskan bahwa mikrosfer dengan nisbah PLA:PCL 9:1 lebih mudah terdegradasi. Hal ini di
yang mempunyai sifat mudah rapuh dan memiliki waktu degradasi yang lebih pendek
Gambar 10 Penurunan bobot mikrosfer s ( ) PLA:PCL 7:3, ( 0.00 5.00 10.00 15.00 20.00 25.00 30.00 35.00 40.00 pe nu ru na n bo bo t( b/ b% ) b d
Foto Mikrosfer dengan mikroskop stereo pada minggu ke-8 dengan perbesaran 40 X (a) PLA:PCL 9:1; (b) PLA:PCL 8:2; (c) PLA:PCL 7:3; (d) PLA:PCL 6:4.
Penurunan Bobot
Degradasi mikrosfer dilakukan selama 8 minggu direndam dengan buffer fosfat pH 7.4 C yang disesuaikan dengan kondisi pH dalam darah dan suhu tubuh manusia yang sehat. Perubahan morfologi mikrosfer telah menjelaskan bahwa mikrosfer ah PLA:PCL 9:1 lebih mudah sebabkan oleh PLA mempunyai sifat mudah rapuh dan memiliki waktu degradasi yang lebih pendek
daripada PCL, sehingga pada minggu ke mikrosfer dengan nisbah PLA:PCL 6:4 masih ada sebagian yang utuh. W
PLA yang pendek ini terbukti dengan
persentase penurunan bobot mikrosfer nisbah PLA:PCL 9:1 berkurang paling besar sebanyak 37.98% (Lampiran
8:2 31.06% (Lampiran 5.b 23.55% (Lampiran 5.c), dan
22.68% (Lampiran 5.d). Hal ini menjelaskan bahwa ada pengaruh komposisi PLA: dengan penurunan bobot mikrosfer selama proses degradasi. Semakin besar komposisi PLA maka penurunan bobot molekul semakin besar tiap minggunya. (Gambar
lama juga waktu perendaman maka jumlah
bobot mikrosfer yang berkurang semakin
banyak selama proses degradasi.
Proses degradasi PLA dan PCL terjadi secara hidrolisis. PLA dan PCL merupakan
polimer jenis poliester. Degradasi
dalam lingkungan berair t
pemutusan ikatan pada sambungan ester dari tulang punggung polimer. Serangan air pada
rantai poliester menyebabkan terputusnya
ikatan ester menghasilkan oligomer
poliester dengan bobot molekul lebih rendah daripada molekul poliester
dan Steven 2000). Selain adanya penurunan bobot, degradasi mikrosfer ditandai pula dengan adanya penurunan viskositas.
Penurunan bobot mikrosfer selama 8 minggu ( ) PLA:PCL 9:,1( ) PLA : PCL 8:2, ( ) PLA:PCL 7:3, ( ) PLA:PCL 6:4
1 2 3 4 5 6 7 8
minggu
daripada PCL, sehingga pada minggu ke-8 mikrosfer dengan nisbah PLA:PCL 6:4 masih ada sebagian yang utuh. Waktu degradasi
PLA yang pendek ini terbukti dengan
persentase penurunan bobot mikrosfer dengan nisbah PLA:PCL 9:1 berkurang paling besar sebanyak 37.98% (Lampiran 5.a), PLA:PCL 31.06% (Lampiran 5.b), PLA:PCL 7:3 ), dan PLA:PCL 6:4 ). Hal ini menjelaskan ahwa ada pengaruh komposisi PLA:PCL dengan penurunan bobot mikrosfer selama proses degradasi. Semakin besar komposisi PLA maka penurunan bobot molekul semakin besar tiap minggunya. (Gambar 10). Semakin juga waktu perendaman maka jumlah
bobot mikrosfer yang berkurang semakin
banyak selama proses degradasi.
PLA dan PCL terjadi . PLA dan PCL merupakan
polimer jenis poliester. Degradasi poliester
dalam lingkungan berair terjadi melalui
pemutusan ikatan pada sambungan ester dari tulang punggung polimer. Serangan air pada
rantai poliester menyebabkan terputusnya
ikatan ester menghasilkan oligomer-oligomer poliester dengan bobot molekul lebih rendah daripada molekul poliester awal. (Hanifa 2008 Selain adanya penurunan bobot, degradasi mikrosfer ditandai pula dengan adanya penurunan viskositas.
Nilai viskositas yang semakin menurun menunjukan bahwa bobot molekul mikrosfer menurun pula tiap minggunya
Menurut persamaan Mark
Sakurada, nilai viskositas berbanding lurus dengan besarnya bobot molekul sehingga
dapat dikatakan bahwa bobot molekul
mikrosfer tiap minggunya menurun. Gambar
10 menunjukkan bahwa nilai viskositas
mikrosfer nisbah PLA:PCL
tiap minggunya daripada mikrosfer nisbah PLA:PCL 9:1. Hal ini menunjukkan bahwa bobot molekul mikrosfer PLA:PCL 6:4 lebih besar pula daripada bobot molekul mikrosfer PLA:PCL 9:1. Bobot molekul PLA hasil
sintesis yang kecil mempengaruhi bo
molekul mikrosfer.
Kinetika Penurunan
Model kinetika yang digunakan untuk analisis mikrosfer secara
et al. (2006) adalah orde nol, orde satu, orde
dua, Higuchi, Crossmayer
Hixson-Crowel. Orde nol, orde
Higuchi lebih digunakan dalam penelitian ini karena PLA dan PCL
yang bersifat erosi sedangkan
crossmayer-peppas dan Hixon
cenderung untuk polimer yang bersifat
hidrogel (Muthu MS dan
Metode yang dapat digunakan untuk
menghitung model kinetika kimi
metode substitusi, metode grafis, dan metode waktu fraksional. Penelitian ini menggunakan perhitungan metode grafis sehingga diperoleh persamaan garis dan koefisien korelasi.
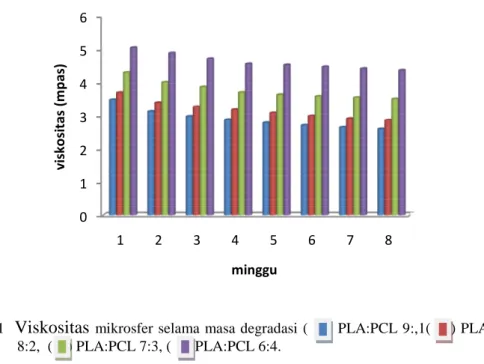
Gambar 11
Viskositas
8:2, ( ) PLA:PCL 7:3, ( ) PLA:PCL 6:4. 0 1 2 3 4 5 6 vi sk os ita s (m pa s)Nilai viskositas yang semakin menurun menunjukan bahwa bobot molekul mikrosfer menurun pula tiap minggunya (Lampiran 6 ).
Menurut persamaan
Mark-Houwink-Sakurada, nilai viskositas berbanding lurus dengan besarnya bobot molekul sehingga
dapat dikatakan bahwa bobot molekul
mikrosfer tiap minggunya menurun. Gambar
10 menunjukkan bahwa nilai viskositas
mikrosfer nisbah PLA:PCL 6:4 paling besar tiap minggunya daripada mikrosfer nisbah PLA:PCL 9:1. Hal ini menunjukkan bahwa bobot molekul mikrosfer PLA:PCL 6:4 lebih besar pula daripada bobot molekul mikrosfer PLA:PCL 9:1. Bobot molekul PLA hasil
sintesis yang kecil mempengaruhi bobot
Kinetika Penurunan Bobot Mikrosfer
Model kinetika yang digunakan untuk secara in vitro oleh Shoaib adalah orde nol, orde satu, orde
dua, Higuchi, Crossmayer-Peppas, dan
rde nol, orde satu, dan lebih digunakan dalam penelitian ini dan PCL merupakan polimer
yang bersifat erosi sedangkan model
peppas dan Hixon-Crowel
cenderung untuk polimer yang bersifat
dan S Singh 2009).
Metode yang dapat digunakan untuk
menghitung model kinetika kimia, yaitu
metode substitusi, metode grafis, dan metode waktu fraksional. Penelitian ini menggunakan perhitungan metode grafis sehingga diperoleh persamaan garis dan koefisien korelasi.
Berdasarkan hasil yang diperoleh (Tabel 3) terlihat bahwa koefisien korelasi penurunan bobot molekul yang paling tinggi untuk mikrosfer PLA: PCL yaitu pada orde antara nol dan satu. Model orde nol menjelaskan bahwa penurunan bobot mikrosfer bergantung
pada bobot molekul polimer
penyusunnya. Koefisien korelasi yang paling baik adalah koefisien korelasi yang nilainya paling mendekati angka satu. Perhitungan kinetika penurunan bobot mikrosfer tercantum di lampiran 7.
Tabel 3 Kinetika penurunan
PLA:PCL Koefisien korelasi (r
Orde nol Orde satu
9:1 0.9870 0.9955
8:2 0.9899 0.9792
7:3 0.9929 0.9948
6:4 0.9878 0.9817
Kinetika pelepasan obat pada penelitian Shoaib et al. (2006) dan Bolourtchian (2005)
menghasilkan kinetika yang koefisien
korelasinya paling tinggi adalah model
Higuchi, sedangkan Muthu MS dan S Singh (2009) mendapatkan hasil kinetika dengan koefisien korelasi yang tinggi pada model orde satu. Perbedaan model kinetika yang memiliki koefisien korelasi paling tinggi
berhubungan dengan faktor
mempengaruhi kinetika laju reaksi yaitu
macam zat yang bereaksi, konsentrasi
pereaksi, suhu, katalis, tekanan, luas
permukaan, dan cahaya.
Viskositas
mikrosfer selama masa degradasi ( ) PLA:PCL 9:,1( ) PLA : PCL8:2, ( ) PLA:PCL 7:3, ( ) PLA:PCL 6:4.
1 2 3 4 5 6 7 8
minggu
9
rkan hasil yang diperoleh (Tabel 3) terlihat bahwa koefisien korelasi penurunan bobot molekul yang paling tinggi untuk mikrosfer PLA: PCL yaitu pada orde antara nol dan satu. Model orde nol menjelaskan bahwa penurunan bobot mikrosfer bergantung
molekul polimer-polimer
penyusunnya. Koefisien korelasi yang paling baik adalah koefisien korelasi yang nilainya paling mendekati angka satu. Perhitungan kinetika penurunan bobot mikrosfer tercantum
Tabel 3 Kinetika penurunan bobot mikrosfer
Koefisien korelasi (r2)
Orde satu Higuchi
0.9955 0.9966
0.9792 0.9495
0.9948 0.9895
0.9817 0.9539
Kinetika pelepasan obat pada penelitian (2006) dan Bolourtchian (2005)
menghasilkan kinetika yang koefisien
korelasinya paling tinggi adalah model
Higuchi, sedangkan Muthu MS dan S Singh (2009) mendapatkan hasil kinetika dengan koefisien korelasi yang tinggi pada model orde satu. Perbedaan model kinetika yang ien korelasi paling tinggi
berhubungan dengan faktor-faktor yang
mempengaruhi kinetika laju reaksi yaitu
macam zat yang bereaksi, konsentrasi
pereaksi, suhu, katalis, tekanan, luas
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian, mikrosfer
nisbah PLA:PCL 9:1 memiliki waktu
degradasi paling cepat dibandingkan
mikrosfer nisbah PLA:PCL yang lain. Hasil SEM mikroskop foto stereo membuktikan bahwa telah terjadi perubahan morfologi mikrosfer sebelum, saat, dan setelah proses
degradasi. Komposisi polimer dalam
mikrosfer mempengaruhi nilai viskositas dan bobot mikrosfer selama proses degradasi. Bobot molekul hasil sintesis PLA akan mempengaruhi bobot molekul dan viskositas mikrosfer polipaduan PLA:PCL. Semakin
besar komposisi PLA dalam mikrosfer
polipaduan maka waktu degradasi semakin
cepat dan persentase penurunan bobot
molekul semakin besar. Kinetika penurunan bobot mikrosfer mengikuti model kinetika antara orde nol dan orde satu.
Saran
Mikrosfer yang tersalut obat
(mikro-kapsul) perlu diteliti untuk mengetahui
perbedaan degradasi antara mikrosfer dengan mikrokapsul.
DAFTAR PUSTAKA
Algaer MSM. 1989. Polymer Science
Dictionary. London: Elsevier Applied
Sciene.
Ajioka et al. 1995. The basic properties of poly(lactic acid) produced by the direct Condensation Polymerization of Lactic Acid. J Environ Polymer Degradation 4 : 225.
Averous L, Belgacem MN, Gandini A, editor.
2008. Polylactic Acid: Synthesis,
Properties and Applications, in
Monomers, Polymers and Composites
from Renewable Resources. Ed ke-1.
Amsterdam: Elsevier Ltd.
Badami AS. 2004. Bioresorbable electrospun tissue scaffolds of poly(ethylene glycol
-lactide) copolymers for bone tissue
engineering. [thesis]. Virginia: Virginia Polytechnic Institute and State University.
Bolourtchian N, K Karimi, R Aboofazeli. 2005. Preparation and characterization of ibuprofen. Journal of Microencapsulation
microspheres 55 : 529-538.
Dinarvard R, Moghadam SH, Mohammadfard
L, Atyabi F. 2003. Preparation of
biodegradable microspheres and matrikx
devices containing naltrexone. AAPS
Pharm Sci Tech 7:E1-E8.
Dutkiewicz S, Daniela GL, Tomaszewski W. 2003. Synthesis of poly (L(+)) lacticacid by polycondensation method in solution.
Fibres & Textiles in Eastern Europe
11:66-70.
Flieger M et al. 2003. Biodegradable plastics from renewable sources. Folia Microbiol 48 (1):27-44.
Gonzalez MF, Ruseckaite RA, Cuadrado TR. 1999. Structural changes of poly(lactic
acid) (PLA) microspheres under
hydrolytic degradation. J Appl Polym Sci 71:1221-1230.
Gunatillake PA, Raju A. 2003. Biodegradable synthetic polymers for tissue engineering.
Eur Cells and Materials 5:1-16.
Hanifa IK. 2008. Optimasi Poli(vinil alkohol) pada pembuatan mikrosfer polipaduan
poli(asam laktat) dengan
poli(ε-kaprolakton) [skripsi]. Bogor: Fakultas Matemetika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hasanah SM. 2009. Optimasi pembuatan mikrosfer polipaduan poli(asam laktat)
dengan poli(ε-kaprolakton) [Skripsi].
Bogor: Fakultas Matemetika dan Ilmu
Pengetahuan Alam, Institut Pertanian
Bogor.
Jain RA. 2000. The manufacturing techniques of various drug loaded biodegradable
poly(lactide-co-glycolide) (PLGA)
devices. Biomaterial 21:2475-2490. Kaitian X et al. 1996. Poly(D,L-lacticacid)
homopolimers: Synthesis and
characterisation. Turkey Journal of
Chemistry 20:43-53.
Kemala T. 2010. Mikrosfer polipaduan
poli(asam laktat) dengan
11
ibuprofen secara in vitro [disertasi].
Jakarta : Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Indonesia. Kemala T, Emil B, Bambang S. 2010.
Preparation and charachterization of
microspheres based on blend poly(lactid
acid) and poly(ε-caprolactone) with
poly(vinyl alcohol) as emulsifier. Arabian
Journal of Chemistry 1-6.
Latief R. 2007. Pembuatan pencirian
poli(asam laktat) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lu Y, Chen SC. 2004. Micro and
nanofabrication of biodegradable polymers for drug delivery. Advanced drug Delivery
Reviews 56:1621-1633.
Muthu MS dan S Singh. 2009. Poly (D, L-Lactide) nanosuspensions of risperidone for parenteral delivery: formulation and
In-Vitro evaluation. Current drugs delivery 6:
62-68.
Mulder M. 1996. Basic Principle of
Membrane Technology. Ed ke-2.
Dordrecht: Kluwer.
Nurhayani. 2008. Degradasi poliblend
poli(asam laktat) dengan
poli(ε-kaprolakron) secara in vitro [skripsi]. Bogor: Fakultas Matemetika dan Ilmu
Pengetahuan Alam, Institut Pertanian
Bogor.
Robani MN. 2004. Biodegradasi struktur dan
morfologi mikrosfer poli(asam laktat)
[skripsi]. Bogor: Fakultas Matemetika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Rusmana N. 2009. Optimasi pembuatan
poliasamlaktat tanpa katalis [skripsi].
Bogor: Fakultas Matemetika dan Ilmu
Pengetahuan Alam, Institut Pertanian
Bogor.
Shoaib et al. 2006. Evaluation of drug release kinetics from ibuprofen matrix tablets using HPMC. Pak. J. Pharm. Sci 19: 119-124.
Steven MP. 2000. Kimia Polimer. Sopyan I, penerjemah. Jakarta : Pradnya Paramitha. Terjemahan dari Polymer Chemistry : An
Introduction.
Sudaryanto, Sudirman, Alona K. 2003.
Pembuatan Mikrosfer Berbasis Polimer
Biodegradabel Polilaktat, Prosiding
Simposium Nasional Polimer IV. 8 Juli 2003. 181-188
Xing DKL et al . 1999. Physicochemical and immunological studies on the stability of free and microsphere-encapsulated tetanus toxoid in vitro. Vaccine 14: 1205-1213. Zang et al. 2005. Preparation of bovine serum
albumin loaded poly (D,
L-lactic-co-glycolic acid) microspheres by a modified phase separation technique. Journal of
13
Lampiran 1 Diagram alir kerja penelitian
Sintesis PLA
PLA
PCL
POLIPADUAN
PLA:PCL
(9:1; 8:2; 7:3; 6:4)
PVA 1.5 %
MIKROSFER
Degradasi
(8 Minggu)
Viskositas
Mikroskop
stereo
SEM
Lampiran 2 Penentuan bobot molekul PLA
[PLA] (g/dL) t (detik) η relatif η spesifik η reduktif (dL/g)
0.0000 40.428 − − − 0.1018 41.061 1.0157 0.0157 0.1539 0.2026 41.788 1.0336 0.0336 0.1660 0.3000 42.578 1.0532 0.0532 0.1773 0.4106 43.681 1.0805 0.0805 0.1960 0.5080 44.593 1.1030 0.1030 0.2028 Contoh perhitungan: [PLA] = 0.1018 g/dL η relatif
=
୲ୱୟ୫ ୮ୣ୪ ୲୮ୣ୪ୟ୰୳୲ ik ik det 428 . 40 det 061 . 41
= 1.0157 η spesifik = η relatif – 1 = 1.0157 –1 = 0.0157 η reduktif=
ηୱ୮ୣୱ୧ϐ୧୩ [] = dL g / 1005 . 0 0271 . 0 = 0.1539 dL/gPenentuan bobot molekul
Persamaan garis: y = 0.1410 + 0.1255x Viskositas intrinsik ([η]) = 01410 [η] = 1.58 x 10-4(Mv)0.78 0.1410 = 1.58 x 10-4(Mv)0.78 (Mv)0.78= 892.405 Mv = 6064.18 g/mol y = 0.125x + 0.141 R² = 0.989 0 0.05 0.1 0.15 0.2 0.25 0 0.1 0.2 0.3 0.4 0.5 0.6 η re du kt if [PLA] g/dL
15
Lampiran 3 Persentase rendemen mikrosfer
PLA:PCL Ulangan Bobot
PLA (g) Bobot PCL (g) Bobot kertas saring kosonng (g) Bobot kertas saring + mikrosfer (g) Bobot mikrosfer (g) Rendemen (%)
9:1
1
0.4535
0.0524
1.2641
1.5774
0.3133
61.92
2
0.4506
0.0524
1.2571
1.5838
0.3267
64.95
3
0.4577
0.0546
1.2502
1.5724
0.3222
62.89
4
0.4514
0.0515
1.2524
1.5812
0.3288
65.38
8:2
1
0.4015
0.1024
1.2759
1.5990
0.3231
64.12
2
0.4055
0.1019
1.2445
1.5838
0.3393
66.87
3
0.4003
0.1084
1.2469
1.5656
0.3187
62.65
4
0.4048
0.1019
1.2506
1.5704
0.3198
63.11
7:4
1
0.3519
0.1503
1.2696
1.6015
0.3319
66.09
2
0.3532
0.1568
1.2803
1.6491
0.3688
72.31
3
0.3515
0.1534
1.2852
1.6202
0.3350
66.35
4
0.3515
0.1523
1.2996
1.6458
0.3462
68.72
6:4
1
0.3031
0.2034
1.3006
1.6736
0.3730
73.64
2
0.3026
0.2034
1.3373
1.6699
0.3326
65.73
3
0.3037
0.2048
1.3666
1.7265
0.3599
70.78
4
0.3008
0.2000
1.3042
1.6578
0.3536
70.61
Contoh perhitungan :Perlakuan PLA:PCL 9:1 ulangan pertama
Bobot mikrosfer = (bobot kertas saring+mikrosfer) – bobot kertas saring kosong = 1.5774 gram – 1.2641 gram
= 0.3133 gram
Rendemen = bobot mikrosfer * 100 %
Bobot PLA + bobot PCL
= 0.3133 * 100 %
0.4535 + 0.0524 = 61.92 % (b/b)
Lampiran 4 Gambar mikrosfer dengan mikroskop stereo perbesaran 40x
a) PLA:PCL 9:1
Minggu
ke-Ulangan 1 Ulangan 2 Ulangan 3
0
2
4
6
17
b) PLA:PCL 8:2
Minggu
ke-Ulangan 1 Ulangan 2 Ulangan 3
0
2
4
6
c)
PLA:PCL 7:3
Minggu
ke-Ulangan 1 Ulangan 2 Ulangan 3
0
2
4
6
19
d)
PLA:PCL 6:4
Minggu
ke-Ulangan 1 Ulangan 2 Ulangan 3
0
2
4
6
Lampiran 5 Penurunan bobot mikrosfer selama masa degradasi
a)
PLA : PCL 9:1
Minggu Ulangan Bobot Bobot mikrosfer (g) Penurunan Rata-rata
ke- botol kosong (g) Sebelum degradasi Setelah degradasi + botol Setelah degradasi bobot (%) penurunan bobot (%)
0
1
11.6530
0.0200
11.6730
0.0200
0.00
2
11.6304
0.0202
11.6506
0.0202
0.00
3
11.9192
0.0201
11.9393
0.0201
0.00
0.00
1
1
11.6530
0.0200
11.6720
0.0200
5.00
2
11.6304
0.0202
11.6497
0.0193
4.46
3
11.9192
0.0201
11.9380
0.0188
6.47
5.31
2
1
11.6034
0.0201
11.6208
0.0174
13.43
2
11.6428
0.0202
11.6608
0.0180
10.89
3
11.6437
0.0201
11.6613
0.0176
12.44
12.25
3
1
11.5338
0.0200
11.5505
0.0167
16.50
2
11.6650
0.0200
11.6814
0.0164
18.00
3
11.3852
0.0203
11.4017
0.0165
18.72
17.74
4
1
11.8760
0.0200
11.8914
0.0154
23.00
2
12.5223
0.0200
12.5380
0.0157
21.50
3
11.8311
0.0200
11.8466
0.0155
22.50
22.33
5
1
11.6259
0.0200
11.6409
0.0150
25.00
2
11.6102
0.0201
11.6253
0.0151
24.88
3
11.7527
0.0201
11.7676
0.0149
25.87
25.25
6
1
11.5658
0.0201
11.5800
0.0142
29.35
2
11.6833
0.0200
11.6971
0.0138
31.00
3
11.5608
0.0201
11.5748
0.0140
30.35
30.23
7
1
11.6083
0.0201
11.6214
0.0131
34.83
2
11.4644
0.0200
11.4775
0.0131
34.50
3
13.0278
0.0202
13.0413
0.0135
33.17
34.16
8
1
11.5969
0.0202
11.6097
0.0128
36.63
2
11.5070
0.0201
11.5194
0.0124
38.31
3
11.6345
0.0200
11.6467
0.0122
39.00
37.98
21
b) PLA : PCL 8:2
Minggu Ulangan Bobot Bobot mikrosfer (g) Penurunan Rata-rata
ke- botol kosong (g) Sebelum degradasi Setelah degradasi + botol Setelah degradasi bobot (%) penurunan bobot (%)
0
1
12.8189
0.0201
12.8390
0.0201
0.00
2
11.5770
0.0200
11.5970
0.0200
0.00
3
11.7282
0.0201
11.7483
0.0201
0.00
0.00
1
1
12.8189
0.0201
12.8381
0.0192
4.48
2
11.5770
0.0200
11.5962
0.0192
4.00
3
11.7282
0.0201
11.7472
0.0190
5.47
4.65
2
1
11.5954
0.0200
11.6137
0.0183
8.50
2
10.3989
0.0202
10.4175
0.0186
7.92
3
11.7604
0.0201
11.7788
0.0184
8.46
8.29
3
1
11.7555
0.0201
11.7732
0.0177
11.94
2
11.6540
0.0200
11.6719
0.0179
10.50
3
11.9067
0.0201
11.9246
0.0179
10.95
11.13
4
1
11.5309
0.0200
11.5481
0.0172
14.00
2
11.8362
0.0201
11.8535
0.0173
13.93
3
11.8253
0.0200
11.8423
0.0170
15.00
14.31
5
1
11.5020
0.0200
11.5185
0.0165
17.50
2
11.7058
0.0201
11.7226
0.0168
16.42
3
11.5450
0.0201
11.5615
0.0165
17.91
17.28
6
1
11.9124
0.0200
11.9279
0.0155
22.50
2
11.8593
0.0202
11.8751
0.0158
21.78
3
11.7138
0.0200
11.7292
0.0154
22.90
22.39
7
1
10.3712
0.0200
10.3858
0.0146
27.00
2
11.4046
0.0201
11.4195
0.0149
25.87
3
11.6261
0.0202
11.6409
0.0148
26.73
26.53
8
1
11.4962
0.0201
11.5099
0.0137
31.84
2
11.5590
0.0200
11.5728
0.0138
31.00
3
11.6146
0.0201
11.6286
0.0140
30.35
31.06
c) PLA : PCL 7:3
Minggu ulangan Bobot Bobot mikrosfer (g) Penurunan Rata-rata
ke- botol kosong (g) Sebelum degradasi Setelah degradasi + botol Setelah degradasi bobot (%) penurunan bobot (%)