Fl
Flam
ame
e T
Tem
empe
pera
ratu
ture
re
Pertemuan ke 11
1. Neraca Energy Pada Sistem
1. Neraca Energy Pada Sistem
1. Neraca Energy Pada Sistem
1. Neraca Energy Pada Sistem
Sebelum menyusun neraca energi, terlebih Sebelum menyusun neraca energi, terlebih dahulu kita harus memahami asumsi
dahulu kita harus memahami asumsi berikut:
berikut: a.
a. HHRR, H, HPP and CV cal!ri"c #alue$ yang and CV cal!ri"c #alue$ yang
diper!leh pada keadaan standard %&'$. diper!leh pada keadaan standard %&'$. (ntalpi udara yang masuk adalah hanya (ntalpi udara yang masuk adalah hanya panas sensibel. campuran )uel*air
panas sensibel. campuran )uel*air
adalah campuran kering*dry mi+ture$ adalah campuran kering*dry mi+ture$ b.
b. (nta(ntalpi lpi ue gas hue gas harus karus k!nsi!nsisten desten denganngan CV )uel yang digunakan pada neraca
CV )uel yang digunakan pada neraca energi.
• -ika digunakan gr!ss cal!ri"c #alue, maka HR
harus mengandung panas laten yang besarnya adalah sama dengan massa air yang dihasilkan per kil!gram )uel dikalikan dengan panas latent penguapan air pada %&' H!#$.
• -ika digunakan net cal!ri"c #alue, maka entalpi
ue gas akan terdiri dari panas sensibel saa.
• /ang akan di bahas adalah: memprediksi
temperatur yang dicapai di dalam nyala*ame yang menggunakan net cal!ri"c #alue*panas sensible.
0eraca (nergi di sekitar sistem
CV HR 2 HP 3c 3u 1$
4imana:
• 3u, panas sensibel di dalam udara dan
)uel re). %&'$ adalah sangat kecil dan sering diabaikan.
• Case l!ss dari dinding luar )urnace, 3c,
uga kecil dibandingkan dengan u+
%. 5diabatic Flame
Temperature
• Flame temperature yang lebih tinggi,
menghasilkan e)ekti#itas
pembakaran pada ruang bakar yang lebih baik
• Tabel 1 memperlihatkan ame
temperatures untuk beberapa )uel yang sering diumpai.
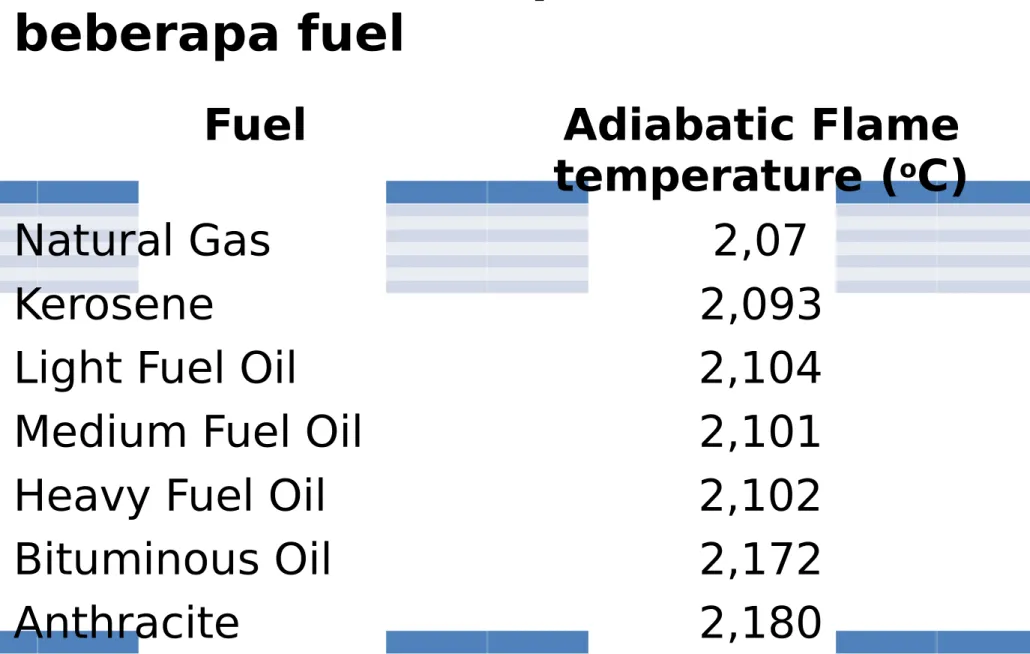
Tabel 1 Flame temperatures untuk beberapa fuel
Fuel Adiabatic Flame
temperature (oC
0atural 6as %,78
9er!sene %,7;
<ight Fuel =il %,17>
?edium Fuel =il %,171
Hea#y Fuel =il %,17%
@itumin!us =il %,18%
• 9ita dapat menggunakan ide neraca
energi disekitar sistem pembakaran untuk menurunkan cara
mengestimasi temperatur ame.
• 5sumsikan pembakaran berlangsung
adiabatik tidak ada panas yang
masuk maupun keluar dari sistem. 3c 2 7 and 3u 2 7
• 9arena itu persamaan 1$ dapat
menadi:
• 4alam hal ini CV adalah <HV dari
)uel, karena itu HP hanya
mengandung panas sensibel
• HR, adalah entalpi )uel dan udara
pada re). %&' ) , dan dapat
dihitung dengan )!rmula:
• ti adalah temperatur mulaBmula
;$ ( 25) ( ) R i P R H = −t − ∑
∑
mc = i p R Rt
m
C
H
(
25
)
(
.
)
• Panas spesi"k Cp$ )uel, !+ygen dan nitr!gen
dapat die#aluasi dengan Cp rataBrata seperti sudah dielaskan sebelumnya.
• 0ilai Hp pada persamaan %$, dapat dihitung
dengan )!rmula:
• 4imana t) adalah ame temperature.
Hubungan di atas tidak dapat diselesaikana dengan mudah melainkan dengan met!de trial dan err!r
>$ ( 25) ( ) R i P R H = t − ∑
∑
mc − = f p P Pt
m
C
H
(
25
)
(
.
)
Panas Spesi"k Cp$ beberapa gas k-*kg*9$
t (oC C!
" #"! !" N" C!
7 7,A1A 1,A7 7,7 1,7;8 1,7;7 %& 7,A>; 1,A 7,1; 1,7;A 1,7;; &7 7,A 1,A8A 7,%1 1,7; 1,7;8 177 7,11 1,AA 7,; 1,7>% 1,7>& 1&7 7,&% 1,%1 7,&1 1,7>A 1,7&> %77 7,A 1,> 7, 1,7&& 1,7; %&7 1,7%> 1,8% 7,A1 1,7; 1,78> ;77 1,7& %,771 7,& 1,78% 1,7A> ;&7 1,7A %,7;1 1,77 1,7A% 1,7 >77 1,11% %,7% 1,7%% 1,7; 1,178 >&7 1,1;8 %,7> 1,7;& 1,17> 1,11A &77 1,1& %,1%8 1,7> 1,11& 1,1;7
Panas Spesi"k Cp$ beberapa gas k-*kg*9$
t (oC C!
" #"! !" N" C!
&&7 1,1A7 %,11 1,7&8 1,1% 1,1>1 77 1,1A %,1& 1,78 1,1;8 1,1&; &7 1,%1& %,%;7 1,78 1,1>A 1,1> 877 1,%;7 %,%> 1,788 1,1& 1,18& 8&7 1,%>> %,;77 1,7A 1,187 1,1A& A77 1,%& %,;;> 1,7> 1,1A7 1,1& A&7 1,%A %,;A 1,171 1,17 1,%7& 77 1,%8A %,>7; 1,178 1,1 1,%1> &7 1,%A8 %,>; 1,11; 1,%7A 1,%%; 1777 1,% %,> 1,11 1,%1 1,%;1 17&7 1,;7; %,&7% 1,1%> 1,%%> 1,%;A 1177 1,;17 %,&;; 1,1%A 1,%;1 1,%>&
Panas Spesi"k Cp$ beberapa gas k-*kg*9$
t (oC C!
" #"! !" N" C!
11&7 1,;1 %,&> 1,1;8 1,%;8 1,%&% 1%77 1,;%% %,&> 1,1>1 1,%>; 1,%&A 1%&7 1,;%A %,%; 1,1>> 1,%> 1,%; 1;77 1,;;; %,&1 1,1>A 1,%&> 1,%A 1;&7 1,;;8 %,8A 1,1&1 1,%& 1,%8% 1>77 1,;>& %,87; 1,1&& 1,%; 1,%8& 1>&7 1,;> %,8%A 1,1& 1,%8 1,%8 1&77 1,;&7 %,8&% 1,1% 1,%87 1,%A% 1&&7 1,;&> %,88> 1,1 1,%8; 1,%A> 177 1,;&A %,8& 1,187 1,%88 1,%A 1&7 1,;1 %,A1& 1,18> 1,%8 1,%AA 1877 1,;& %,A;> 1,18 1,%A% 1,%7
Panas Spesi"k Cp$ beberapa gas k-*kg*9$
t (oC C!
" #"! !" N" C!
18&7 1,; %,A&% 1,1A; 1,%A> 1,%% 1A77 1,;8; %,A 1,1A8 1,%A8 1,%> 1A&7 1,;8 %,AA& 1,1% 1,%A 1,% 177 1,;A7 %,77 1,1 1,%% 1,%A 1&7 1,;A; %,1> 1,1 1,%> 1,;71 %777 1,;A8 %,%A 1,%7; 1,% 1,;7>
6unakan ?et!de Dnterp!lasi ika data Cp berada diantara data yang tersedia
t1 t t% Cp1 Cp Cp % 1 1 2 1 2 1 1 2 1 1 2 1 ) ( ) ( ) ( ) ( ) ( ) ( ) ( Cp Cp Cp t t t t Cp Cp Cp Cp Cp t t t t + − − − = − − = − −
$. Prosedur Per%itungan
1. (#aluasi CV HR$ pada
persamaan %$E
%. Tebak asumsikan$ nilai t) dan gunakan nilai ini
untuk menentukan nilai Cp pr!duk hasil
pembakaran temperatur re)erence yaitu %&'E
;. Selesaikan persamaan %$ untuk t)
>. @andingkan nilai t) yang
baru dengan nilai trial. -ika terdapat perbedaan
yang auh maka
ree#aluasi nilai Cp, dan kembali ke tahap %.
sampai diper!leh nilai yang k!n#ergen
@erikut adalah tahapan untuk menghitung adiabatik ame temperatur
Flame Temperature
&. Per%itungan Adiabatic Flame Temperatures
• 0ilai adiabatic ame temperature
prediksi untuk Fuel HC dipengaruhi !leh beberapa )akt!r berikut:
1. CV dan k!mp!sisi kimia$ dari )uelE %. rasi! udara bahan bakar dimana
pembakaran berlangsung.
;. temperatur mulaBmula preheat$ dari
C!nt!h 1: @@ dan udara masuk
pada suhu yang sama dan bukan
pada k!ndisi t
re)• 4apatkan adiabatic ame
temperature untuk suatu st!iki!metri nyala metana*udara ame ika
temperatur aal bahan bakar dan udara adalah 17'. 6unakan net
Penyelesian:
Reaksi CH> %=% C=% %H%=
• Gntuk 1 kg )uel, 0eraca ?assa
reaktan dan pr!duk adalah:
'ompo nen eaktan Produk kg km!l kg 9m!l CH> 1 7,7%& B =% > 7,1%& B 0% 1;,1 7,>8 1;,1 7,>8 C=% %,8& 7,7%& H%= %,%& 7,1%&
• Temperatur mulaBmula reaktan 17' dan nilai HR
adalah panas sensibel reaktan pada re). %&'$: HR 2 tBtre) $.Σni.cpi.
HR 2 17B%&$1.CPCH> >.CP=%$ 1;,1.CP0%$pada
t217!C I
• Temperatur reaktan adalah 17'. Pada temperatur
ini nilai Cp masingBmasing adalah: CH> 2 %,%; k-*kg* ' =% 2 7,788 k-*kg* ' 0% 2 1,7;8%& k-*kg* ' HR 2 17B%&$1 + %,%; > + 7,788$ 1;,1 + 1,7;8%&$ maka
• HP 2 CV HR 2&7.1>7 J %%,8 2 >.A>8
k-per kg metana$
HP adalah panas sensibel pr!duk
pembakaran pada temperatur %&'. ?aka: >.A>8 2 t) B %&$ 1;,1.CP0%$ %,%8.CPH%=$ %,8&.CPC=%$I 1$ 5sumsikan t) 21.&77', ?aka:
• Cp pr!duk nitr!gen, uap air dan karb!ndi!ksida pada
temperatur 1.&77 ' adalah:
0% 1,%8 k-*kg* 9
H%= %,8%&
C=% 1,;&
?aka: persamaan 1$ menadi
>.A>8 2 t) B %&$ 1;,1 + 1,%8$ %,%8 + %,8%&$
%,8& + 1,;&$I
t)2 1AA '
• 0ilai baru temperatur ini masih auh dari nilai trial
sehingga perlu di trial lagi dengan menggunakan
Speci"c heats pada t 2 1AA ' kemudian menadi: 0%1,%% k-*kg*9
H%= %, C=% 1,;A
>.A>8 2 t) B %&$ 1;,1 + 1,%%$ %,%& + %,$
%,8& + 1,;A$I
sehingga: t) 2 1A& ' nilai ini masih cukup auh dengan 1AA$
• Trial lagi dengan t 2 1A& ' • ?emberikan nilai Cp
0%1,%% k-*kg*9
H%= %,AA& C=% 1,;8
• 6anti s!al di atas dengan pr!pana
C!nt!h %: @@ masuk pada suhu re)
dan udara masuk pada suhu di atas
t
re)• 4apatkan adiabatic ame
temperature untuk suatu st!iki!metri nyala metana*udara ame ika
temperatur aal bahan bakar pada suhu re) dan udara adalah 177'. 6unakan net cal!ri"c #alue metana 2 &7,1> ?-.
Penyelesian:
Reaksi CH> %=% C=% %H%=
• Gntuk 1 kg )uel, 0eraca ?assa
reaktan dan pr!duk adalah:
'ompo nen eaktan Produk kg km!l kg 9m!l CH> 1 7,7%& B =% > 7,1%& B 0% 1;,1 7,>8 1;,1 7,>8 C=% %,8& 7,7%& H%= %,%& 7,1%&
• Temperatur mulaBmula metana %&' dan nilai
HR $metana pada re). %&'$ 2 7
HR $udara 2 tBtre) $.Σni.cpi.
HR 2 177B%&$>.CP=%$ 1;,1.CP0%$pada t2177!C I
• Temperatur udara adalah 177 '. Pada
temperatur ini nilai Cp !ksigen dan nitr!gen masingBmasing adalah:
=% 2 7,; k-*kg* '
0% 2 1,7>% k-*kg* '
HR 2 177B%&$> + 7,;$ 1;,1 + 1,7>%$
maka
• HP 2 CV HR 2&7.1>7 1.;7,%&>
2 &1.>>,%&> k- per kg metana$ HP adalah panas sensibel pr!duk
pembakaran pada temperatur %&'. ?aka:
&1.>>,%&> 2 t) B %&$ 1;,1.CP0%$ %,%&.CPH%=$
%,8&.CPC=%$I
1$
5sumsikan t) 21.&77',
• Cp pr!duk nitr!gen, uap air dan karb!ndi!ksida pada
temperatur 1.&77' adalah:
0%1,%8 k-*kg* 9
H%= %,8%&
C=% 1,;&
?aka: persamaan 1$ menadi
&1.>>,%&> 2 t) B %&$ 1;,1 + 1,%8$ %,%& + %,8&%$
%,8& + 1,;&$
t) 2 1&A '
• 0ilai baru temperatur ini masih auh dari nilai trial
sehingga perlu di trial lagi dengan menggunakan
• Speci"c heats pada t 2 1&A ' kemudian menadi:
0%1,%> k-*kg* ' H%= %,1>
C=% 1,;A;
&1.>>,%&> 2 t) B %&$ 1;,1 + 1,%>$ %,%& + %,1>$ %,8& + 1,;A;$
sehingga
t) 2 17; ' nilai ini masih cukup auh dengan 1&A $
• Trial lagi dengan t 2 17; ' • ?emberikan nilai Cp
0%1,%% k-*kg*9
H%= %, C=% 1,;A
• Selanutnya t) 2 17A ' K 0ilai ini dianggap sudah
S=5<
6as alam dengan k!mp!sisi sebagai berikut: CH> 2 8>,7 L t, C%H 2 11,7E C=% 2 1,>
dan 0% 2 1%,> dalam persen berat$ di bakar
dengan %& L e+cess udara. 5sumsi
Pembakaran berlangsung sempurna dengan suhu aal 17 !CE dimana
∆Hc metana 2 BA7% k*m!l CV 2 &7,1%&
?-*9gE
∆Hc etana 2 B1>%A k*m!l CV 2 >8, ?-*9g,
untuk 177 kg bahan bakar tentukan: 5diabatic ame temperature
Penyelesaian:
• 0eraca ?assa per 177 kg bahan
Penyelesaian:
• Reaksi 9imia
CH> %=% C=% %H%=
C%HC ;.&=% %C=% ;H%=
?enghitung Gmpan ruang bakar Dnput$: CH> 2 8>,7*1 2 >,%A8& km!l
C%HC 2 11,7*;7 2 7,;A8 km!l
0itr!gen dalam bahan bakar 2 1%,>*%A 2 7,>%1 km!l
C=% dalam bahan bakar 2 1,>*>> 2 7,7>>71
?enghitung 9ebutuhan udara:
=ksigen te!ritis 2 % + m!l CH> ;.& + m!l C%H. 2 % + >,%A8& ;,& + 7,;A8
2 17,&>8A; km!l
4igunakan udara %&L e+cess, maka
=ksigen suplay 2 1,%& + 17,&>8A; 2 1;,1A>8 km!l
0itr!gen suplay 2 ;,8 + !ksigen suplay 2 ;,8 + 1;,1A>8 2 >,&8>A
0itr!gen masuk ruang bakar 2 0itr!gen di
dalam udara suplay 0% di dalam bahan bakar 2 >,&8>A 7,>%1 2 &7,7;%
?enghitung =utput hasil pembakaran: ?enghitung C=% dan H%= hasil reaksi: C=% Hasil 2 m!l CH> % + m!l C%H.
2 >,%A8& % + 7,;A8 2 &,;7A> km!l
C=% 9eluar ruang bakar 2 C=% hasil reaksi C=% di
dalam bahan bakar
2 &,;7A> 7,7>>71 2 &,>1718& km!l H%= hasil 2 % + m!l CH> ; + m!l C%H.
2 % + >,%A8& ; + 7,;A8 2 17,;;&71 km!l
=% keluar ruang bakar 2 =% suplay J =% bereaksi 2 1;,1A>8B17,&>8A; 2 %,; km!l
• 0eraca (nergi
?enentukan (ntalpi Reaktan HR$
HR 2 tBtre) $.Σni.cpi.
HR 2 17B%&$7,8>7.CPCH> $7,117.CPC%H $ >,%11;;.CP=% $ 1>,717;&.CP0%$ 7,71>.
CPC=%$pada t217!C I
4ari Tabel diper!leh data Cp pada 17 !C
CP=% 2 7,7AA k-*kg* !C
CP0% 2 1,7;8> k-*kg* !C
CPC=% 2 7,A%A k-*kg* !C
4ari persamaan p!lin!mial data pada range %&B17 !C
CPCH> 2 %,1 k-*kg* !C
?enentukan (ntalpi Reaktan HR$ HR 2 17B%&$7,8>7 + %,1 $7,117 + ;,% $ >,%11;; + 7,7AA $ 1>,717;& + 1,7;8>$ 7,71>. + 7,A%A$I
2 %7,;>& k-*kg bahan bakar Persamaan energi:
HR CV 2 HP .
?enghitung CV bahan bakar:
CV 2 7,8>7 + &7,1%> 7,117 + >8, 2 >%.;A
k-Gntuk menyelesaikan persamaan di atas
5sumsikan t) 21.77 ',
?aka:
• Cp pr!duk nitr!gen, =ksigen, uap air dan
karb!ndi!ksida pada temperatur 1.77' adalah:
0%1,%88 k-*kg* '
=% 1,18
H%= %,8&
?aka: persamaan 1$ menadi
>%.>7,;>& 2
t) B%&$7,A>;A M1,18$1>,717>M
1,%88$
%,;A7& M 1,;&A $ 1,A&> + %,8&$I t) 2 1&8,% 2 1&88 '
• 0ilai baru temperatur ini masih auh
dibandingkan dengan 177, trial lagi dengan nilai t) 2 1&88 '
Speci"c heats pada t 2 1&88 ' kemudian menadi: 0%1,%8&k-*kg* ' =% 1,1A H%= %,8A& C=% 1,;& >%.>7,;>& 2
t) B%&$7,A>;A M1,1A$1>,717>M 1,%8&$ %,;A7& M 1,;& $ 1,A&> + %,8A&$I
t) 2 1&8,8 '
Flame Temperature
C!nt!h S!al
• <iNuid metan!l bb$ dibakar dengan 177L
e+cess udara. Se!rang engineer diminta
merancang temperatur tertinggi yang dicapai )urnace sehingga dapat dipilih dinding )urnace dengan material yang sesuai, asumsikan
metan!l diumpankan pada suhu %&!C
sedangkan udara diumpankan pada suhu
177!C. 4engan umpan metan!l sebanyak 1 kg,
tentukan temperatur yang dimaksud.
• CH;=H 1,& =% C=% %H%= : ∆Hc 2 B%%,AA
Penyelesaian:
• Reaksi 9imia
CH;=H 1,& =% C=% %H%= : ∆Hc 2 B%%,AA
?-*9g
?enghitung Gmpan ruang bakar Dnput$: CH;=H 2 1*;% 2 7,7;1%& km!l
=ksigen te!ritis 2 1,& + m!l CH;=H 2 1,& +
7,7;1%& km!l 2 7,7>AA
4igunakan udara 177 L e+cess, maka
=ksigen suplay 2 % + 7,7>AA 2 7,7;8& km!l 0itr!gen suplay 2 ;,8 + !ksigen suplay
?enghitung =utput hasil pembakaran: ?enghitung C=% dan H%= hasil reaksi: C=% Hasil 2 m!l CH;=H 2 7,7;1%& km!l
H%= hasil 2 % + m!l CH;=H 2 % + 7,7;1%&
km!l
2 7,7%& km!l
=% sisa 2 =% suplay J =% bereaksi
2 7,7;8& B 7,7>AA 2 7,7>AA km!l 0% sisa 2 0% umpan 2 7,;&%& km!l
• 0eraca (nergi
?enentukan (ntalpi Reaktan HR$ CH;=H
HR $CH;=H 2 tBtre) $.n CH;=H.cp CH;=H.
2 %& J %&$ n CH;=H.cp CH;=H. 2 7
?enentukan (ntalpi Reaktan HR$ udara
HR 2 tBtre) $.Σni.cpi.
HR 2 177B%&$ ;.CP=% $
,A8.CP0%$$pada t2177!C I
4ari Tabel diper!leh data Cp pada 177 !C
CP=% 2 7,; k-*kg* !C
?enentukan (ntalpi Reaktan HR$
HR 2 177B%&$ ;+ 7,;$ ,A8 + 1,7>%$$
2 A1,> k-*kg bahan bakar Persamaan energi:
HR CV 2 HP .
CV bahan bakar 2 %%AA 9-*9g
k-Gntuk menyelesaikan persamaan di atas Gntuk menyelesaikan persamaan di atas 5sumsikan t
5sumsikan t) ) 21.77 ', 21.77 ',
?aka: ?aka:
•
• Cp Cp pr!duk pr!duk nitr!gen, nitr!gen, =ksigen, =ksigen, uap uap air air dandan
karb!ndi!ksida pada temperatur 1.77' karb!ndi!ksida pada temperatur 1.77' adalah lihat Tabel Cp rataBrata$:
adalah lihat Tabel Cp rataBrata$: 0 0%%1,%88 k-*kg* '1,%88 k-*kg* ' = =%% 1,181,18 H H%%== %%,,88&& C= C=%% 1,;&A1,;&A
?aka: persamaan 1$ menadi ?aka: persamaan 1$ menadi
%;.,> 2 %;.,> 2
t
t) ) B%&$1,& M1,18$,A8M 1,%88$B%&$1,& M1,18$,A8M 1,%88$
1,;8& M 1,;&A $ 1,1%& + %,8&$I 1,;8& M 1,;&A $ 1,1%& + %,8&$I tt) ) 2 2 1%>,; 1%>,; 2 2 1%>8 1%>8 ''
•
• 0ilai baru temperatur ini masih auh0ilai baru temperatur ini masih auh
dibandingkan dengan 177, trial lagi dibandingkan dengan 177, trial lagi dengan nilai t
Speci"c heats pada t
Speci"c heats pada t 2 1%>8 ' bisa gunakan2 1%>8 ' bisa gunakan data
data pada pada 1%&7$ 1%&7$ kkemudian emudian menadi:menadi: 0 0%%1,%>A k-*kg* '1,%>A k-*kg* ' = =%% 1,1>;A1,1>;A H H%%== %%,,%%11;; C= C=%% 1,;%81,;%8 %;.,> %;.,> 22 t
t) ) B%&$1,& M1,1>;A$,A8M 1,%>A$B%&$1,& M1,1>;A$,A8M 1,%>A$
1,;8& M 1,;%8 $ 1,1%& + %,%1;$I 1,;8& M 1,;%8 $ 1,1%& + %,%1;$I tt) ) 2 1%A;'2 1%A;'
•
• K 0ilai ini masih belum memadai. Trial lagiK 0ilai ini masih belum memadai. Trial lagi
dengan t
Speci"c heats pada t 2 1%A; ' kemudian menadi: 0%1,%&%; k-*kg* ' =% 1,1> H%= %,>1& C=% 1,;;&; %;.,> 2
t) B%&$1,& M 1,1>$,A8M 1,%&%;$ 1,;8& M 1,;;&; $ 1,1%& + %,>1&$I t) 2 1%A;,1'
Pengaru% Caloric )alue ter%adap
*ame temperatur
• 4iharapkan baha ika CV besar maka
"nal ame temperature yang dihasilkan uga besar.
Tetapi tdk sesederhana itu krn k!mp!sisi kimia bahan bakar uga berperan.
• C!nt!h: natural gas mempunyai rasi!
carb!nBt!Bhydr!gen kiraBkira ;.1 dan CV &> ?-*kg gr!ss$. C!al, mempunyai rasi! carb!nBt!Bhydr!gen 1A.7 dan CV ;;.;
• Fuels dengan p!rsi hydr!gen lebih
besar akan menghasilkan lebih banyak uap air dalam pr!duk pembakaran yang mana akan menurunkan adiabatic ame temperature.
• 5diabatic ame temperature untuk
beberapa )uel telah disaikan pada tabel sebelumnya.
• 4apat dilihat baha terdapat sangat
kecil perubahan perhitungan ame temperature, untuk #ariasi CV
• Hal ini mengk!n"rmasi e)ek dari
Pengaru% air+to+fuel ratio
ter%adap *ame temperatur
• Gdara e+cess akan meningkatkan massaue gas relati) terhadap )uel gas, dimana akan berpengaruh terhadap penurunan temperatur
• 4engan subBst!ichi!metric udara suplay ,
ame temperature uga akan dr!p, nilai CV e)ekti) )uel uga akan berkurang dengan
umlah yang eNui#alen dari C= yang ada di dalam ue gas.
• 0et CV dari C= adalah 17.11 ?-*kg.
• 6ambar berikut memperlihatkan,
e)ek dari e+cess rasi! udara terhadap ame temperatur
• Temperatur ame yang tinggi dapat
dicapai dengan memperkaya !+ygen di dalam ame asal mass ue gas
berkurang.
• 0yala =+ygen digunakan untuk
berbagai aplikasi seperti : pengelasan, tetapi temperatur di dalam !+ygenB
enriched ames sangat tinggi namun e)ek dis!siasi uga sangat signi"kan.
Preheat
• preheating udara akan meningkatkan
"nal temperatur ame.
• Hal ini sangat berguna karena
dengan meningkatnya perbedaan temperatur antara ue gas dan dan panas uida, maka heat trans)er
yang diper!leh akan lebih besar
• Hal ini tentu saa akan meningkatkan
e"siensi termal pabrik.
• C!nt!h e)ek preheat pada
temperatur adiabatic sebuah ame natural gas ame dengan &L e+cess udara diperlihatkan pada gambar
• Prakteknya, terdapat beberapa alasan
mengapa actual ame temperature akan lebih rendah daripada hasil prediksi dengan
)!rmulasi$.
• /ang paling mungkin adalah baha pada high
temperature yang dicapai pada ame pr!duk pembakaran akan terurai kembali menadi
reaktan atau spesies reakti) lainnya: pr!ses ini berlangsung dengan menyerap energi,
karenanya teradi teradi penurunan actual ame temperature.