BAB II
TINJAUAN PUSTAKA
2.1 Sosis
Sosis berasal dari bahasa latin yaitu salsus yang berarti digarami atau daging yang disiapkan melalui penggaraman. Sosis adalah produk daging giling yang dimasukkan ke dalam selongsong/casing sehingga mempunyai bentuk bulat panjang dengan berbagai ukuran (Nursiam, 2010). Sosis merupakan suatu makanan yang terbuat dari daging cincang, lemak hewan, dan rempah, serta bahan-bahan lain. Sosis umumnya dibungkus dalam suatu pembungkus yang secara tradisional menggunakan usus hewan, tapi sekarang sering kali menggunakan bahan sintetis seperti plastik, serta diawetkan dengan cara, pengasapan. Pembuatan sosis merupakan suatu teknik produksi dan pengawetan makanan yang telah dilakukan sejak sangat lama. Sosis terdiri dari dua tipe, yaitu ada sosis mentah dan sosis matang (Anonima, 2010).
Daging olahan seperti sosis dan burger biasanya menggunakan bahan pengawet. Pengawet yang biasa digunakan adalah natrium/kalium nitrit dan natrium/kalium nitrat. Penggunaan pengawet tersebut bertujuan untuk mencegah kerusakan pada daging yang terjadi akibat proses pembusukan oleh bakteri. Selain sebagai pengawet, nitrit dan nitrat juga dapat memberikan warna merah pada produk daging, sehingga memberikan tampilan segar dan menarik. Nitrit dapat mencegah pertumbuhan bakteri Clostridium botulinum yang dapat menghasilkan racun botulinum (Anonimb, 2010).
Toksin botulinum adalah toksin yang dihasilkan oleh bakteri Clostridium
botulinum. Toksin ini merupakan tipe neurotoksin yang memiliki aksi pada
transmisi impuls dari sel saraf ke sel otot. Toksin botulinum terikat pada sel saraf dan menghambat pelepasan neurotransmiter yang disebut asetilkolin. Asetilkolin berperan dalam menginduksi kontraksi otot. Akibatnya, toksin ini menghambat kontraksi otot (Pratiwi, 2008).
2.2 Nitrit dan Nitrat
Nitrit dan nitrat adalah senyawa nitrogen alami yang terdapat dalam air, tanah, dan air permukaan. Kalium/natrium nitrit dan kalium/natrium nitrat telah digunakan dalam daging olahan (kuring) selama berabad-abad diberbagai negara, termasuk Indonesia. Nitrit merupakan senyawa nitrogen yang reaktif. Sumber utama nitrit secara umum adalah makanan, terutama sayuran, dan air minum. Hal yang perlu diperhatikan adalah pemakaian pupuk pada sayuran. Jika pupuk urea banyak digunakan, akan menyebabkan paparan pada manusia melalui sayuran, terutama sayuran yang berwarna hijau serta sayuran dari umbi dan air minum (Silalahi, 2005).
Kuring adalah suatu proses pengolahan yang dapat menghambat pertumbuhan organisme melalui penggunaan garam nitrit dan nitrat dan juga berfungsi untuk mempertahankan warna daging. Manfaat melakukan kuring adalah untuk mempertahankan warna yang stabil, aroma, tekstur dan kelezatan yang baik, dan untuk mengurangi pengerutan daging selama proses pengolahan, serta memperlama masa simpan produk daging (Soeparno, 1994).
Nitrit dan nitrat terjadi secara alamiah dalam lingkungan dan juga sengaja ditambahkan pada beberapa makanan olahan seperti daging olahan dan awetan dimana nitrit berfungsi sebagai pengawet dan pewarna. Nitrat dan nitrit sebagai pengawet makanan yang diizinkan, tetapi perlu diperhatikan penggunaannya
dalam makanan agar tidak melampaui batas, sehingga tidak berdampak negatif bagi kesehatan manusia (Cory, 2009).
Penggunaan nitrit sebagai pengawet memiliki tujuan yaitu pertama untuk menghambat pertumbuhan mikoba patogen, mikroba patogen paling berbahaya yang tedapat di dalam daging adalah Clostridium botulinum. Nitrit dapat menghambat poduksi toksin Clostridium botulinum dengan menghambat pertumbuhan dan perkembangan spora atau dengan cara membentuk senyawa penghambat yang akan terbentuk bila nitrit dalam daging dipanaskan. Kedua membentuk cita rasa, peranan nitrit yang berhubungan dengan cita rasa adalah sifat nitrit sebagai antioksidan yaitu nitrit akan menghambat oksidasi lemak yang akan membentuk senyawa-senyawa karbonil seperti aldehid, asam-asam dan keton yang menyebabkan bau dan rasa tengik. Ketiga memberikan warna yang menarik, penambahan nitrit pada daging olahan terutama bertujuan untuk memberi warna merah yang menarik. Pigmen dalam otot daging terdiri dari protein yang disebut mioglobin. Mioglobin dengan oksigen akan membentuk oksimioglobin yang berwarna merah terang. Warna merah dari oksimioglobin tidak stabil, dan dengan oksidasi berlebih akan membentuk methemoglobin yang berwarna coklat (Soeparno, 1994).
2.3 Efek Toksik Nitrit dan Nitrat
Nitrit dapat bereaksi dengan zat-zat yang ada dalam saluran pencernaan. Nitrit juga dapat terbentuk melalui reduksi nitrat oleh bakteri pada infeksi kelenjar kemih. Sintesa nitrit dan nitrat juga terjadi di dalam jaringan tubuh mamalia oleh bakteri heterotrop. Jika pH lambung meningkat, bakteri akan berkembang yang kemudian dapat mereduksi nitrat menjadi nitrit. Nitrat diabsorbsi dengan cepat pada saluran pencernaan bagian atas, dan sebagian besar dikeluarkan melalui urin.
Pengeluaran melalui urin mempunyai waktu paruh sekitar 5 jam. Sebagian nitrat yang diangkut dalam darah dikeluarkan melalui kelenjar ludah. Nitrat yang berada dalam rongga mulut dapat direduksi menjadi nitrit oleh mikroba rongga mulut dan kemudian tertelan. Sebanyak 25% dari asupan nitrat dikeluarkan melalui kelenjar ludah. Sekitar 20% dari nitrat dalam kelenjar ludah direduksi menjadi nitrit, dengan demikian sekitar 5% dari seluruh asupan nitrat akan direduksi menjadi nitrit dalam ludah dan tertelan kembali. (Silalahi, 2005).
Dalam hemoglobin terdapat besi dalam bentuk ferro (Fe2+) yang dapat teroksidasi menjadi ion ferri (Fe3+). Hemoglobin yang mengikat ion ferri disebut methemoglobin yang menghasilkan warna hijau kecoklatan hingga hitam dan tidak mampu lagi untuk mengikat oksigen dan karbon monoksida. Zat kimia yang dapat menyebabkan kondisi methemoglobin adalah nitrit. Methemoglobinemia adalah suatu keadaan darah yang mengandung methemoglobin, yang menimbulkan efek yang merugikan bagi kesehatan akibat paparan nitrat atau nitrit terhadap manusia. Kadar methemogobin 1% terdapat secara klinis dalam darah dan bisa mencapai 10% tanpa menyebabkan keadaan patologis. Tetapi pada level di atas 10%, methemoglobin menyebabkan sianosis dan konsentrasi yang lebih tinggi menyebabkan asfiksia (Dewi, 2005).
Normalnya jumlah methemogobin dalam darah sekitar 2%, dan tanda-tanda klinis dari methemoglobin seperti sianosis menjadi nampak jelas ketika jumlah methemoglobin mencapai 15% atau lebih. Methemogobin dalam eritrosit dalam jumlah yang sedikit akan direduksi menjadi hemoglobin oleh enzim methemoglobin reduktase, tetapi jika jumlah methemogobin telah melampaui, maka enzim methemoglobin reduktase tidak mampu lagi untuk mereduksi methemoglobin. Enzim methemoglobin reduktase membutuhkan glutation sebagai
kofaktor pereduksi. Pembentukan glutation tergantung pada perubahan glukosa-6-fosfat dengan bantuan glukosa-6-glukosa-6-fosfat dehidrogenase. Karena itu kekurangan enzim ini yang terjadi secara genetik akan sangat mempengaruhi pembentukan methemoglobin (Dewi, 2005).
Penggunaan nitrit dan nitrat sebagai pengawet untuk mempertahankan warna daging atau ikan ternyata menimbulkan efek yang membahayakan. Nitrit dapat berikatan dengan amino atau amida dan membentuk turunan nitrosamin yang bersifat toksik. Nitrosamin merupakan senyawa yang bersifat karsinogenik, nitrosamin dapat menimbulkan tumor pada bermacam-macam organ, termasuk hati, ginjal, kandung kemih, paru-paru, lambung, saluran pernafasan, pangkreas dan lain-lain (Muchtadi, 2008).
Senyawa nitrosamin yang dihasilkan dari reaksi nitrit dengan amin sekunder merupakan senyawa yang bersifat karsinogenik. Amin-amin sekunder yang paling banyak ditemukan dalam daging adalah piperidin, dietil amin, pirolidin, dan dimetil amin (Lawrie, 2003). Untuk mencegah terbentuknya nitrosamin maka dianjurkan untuk menambahkan zat yang dapat menghambat proses tersebut misalnya penambahan asam askorbat dan vitamin E (Silalahi, 2005).
Penelitian tentang penetapan kadar nitrit dalam makanan telah dilakukan sebelumnya terhadap sampel korned sapi kalengan, daging burger sapi dan sop daging sapi dengan metode spektrofotometri sinar tampak dimana digunakan pereaksi asam sulfanilat dan N-(1-naftil) etilen diamin dihidroksida (NED). Kadar nitrit pada berbagai sampel dapat dilihat pada Tabel 2.1 di bawah ini.
Tabel 2.1 Kadar nitrit pada berbagai sampel
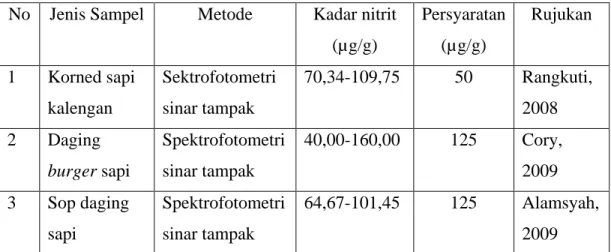
No Jenis Sampel Metode Kadar nitrit (µg/g) Persyaratan (µg/g) Rujukan 1 Korned sapi kalengan Sektrofotometri sinar tampak 70,34-109,75 50 Rangkuti, 2008 2 Daging burger sapi Spektrofotometri sinar tampak 40,00-160,00 125 Cory, 2009 3 Sop daging sapi Spektrofotometri sinar tampak 64,67-101,45 125 Alamsyah, 2009
Dari Table 2.1 dapat dilihat bahwa pada sampel sop daging sapi dan daging burger mengandung nitrit tetapi masih memenuhi persyaratan untuk dikonsumsi karena kadarnya berada di bawah batas maksimum yang diizinkan yaitu 125 µg/g, Sedangkan pada sampel korned sapi kalengan, diperoleh hasil bahwa sampel korned sapi kalengan mengandung nitrit yang melebihi batas maksimum yang diizinkan yaitu 50 µg/g .
2.4 Pemeriksaan Kualitatif Nitrit
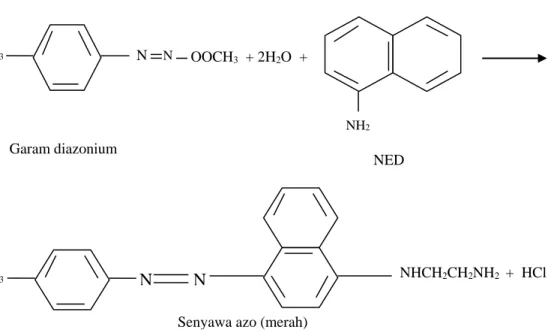
Pemeriksaan kualitatif dapat dilakukan dengan menggunakan pereaksi asam sulfanilat dan N-(1-naftil) etilen diamin dihidroksida (NED), larutan KI dalam asam asetat dan kloroform. Larutan yang mengandung nitrit dimasukkan ke dalam tabung reaksi, kemudian ditambahkan beberapa tetes asam sulfanilat dan NED lalu dikocok, dibiarkan beberapa menit, terbentuk warna ungu merah (Vogel, 1990). Reaksi antara nitrit dengan asam sulfanilat dan NED dilihat pada Gambar 1.1. Garam diazonium Asam sulfanilat NH2 CH3COOH + HNO2 HSO3 N OOCH3 + 2H2O = N _--_ _ _ = HSO3
Gambar 1.1 Reaksi antara nitrit dengan asam sulfanilat dan NED (Vogel, 1985).
Dimasukkan larutan ke dalam larutan kalium iodida, kemudian diasamkan dengan asam asetat encer, maka akan terbentuk larutan berwarna kuning karena adanya iod yang dibebaskan, yang dapat diidentifikasi dengan penambahan kloroform maka lapisan kloroform akan berwarna ungu (Vogel, 1985). Persamaan reaksinya adalah:
2NO2- + 2I- + 2CH3COOH I2 + 2NO2 + 2CH3COO- + 2H2O
2.5 Pemeriksaan Kualitatif Nitrat
Pemeriksaan kualitatif dapat dilakukan dengan mereduksi nitrat menjadi nitrit menggunakan logam Zn, pereaksi asam sulfanilat dan NED, perekasi ferro sulfat dalam asam sulfat pekat. Larutan yang mengandung nitrat direduksi menjadi nitrit dengan cara ke dalam filtrat dimasukkan sedikit logam Zn dalam larutan asam asetat. Kemudian nitrat dapat dideteksi memakai pereaksi asam
Senyawa azo (merah) N = N N _--_ __ = OOCH3 + 2H2O + HSO3 Garam diazonium NED NH2 HSO3 N N NHCH2CH2NH2 + HCl
sulfanilat dan NED, warna ungu merah menunjukkan adanya nitrat. Larutan yang mengandung nitrat dimasukkan ke dalam larutan ferro sulfat yang diasamkan dengan asam sulfat pekat, maka akan terbentuk cincin coklat pada perbatasan antara kedua cincin itu (Vogel, 1985). Persamaan reaksi cincin coklat adalah: 2NO3- + 4H2SO4 + 6Fe2+ 6Fe3+ + 2NO + 4SO42- + 4H2O Fe2+ + NO {Fe(NO)}2+
2.6 Penentuan Kadar Nitrit dan Nitrat 2.6.1 Penentuan Kadar Nitrit
2.6.1.1 Penentuan Kadar Nitrit dengan Metode Spektrofotometri Sinar Tampak
Metode spektrofotometri sinar tampak digunakan untuk pemeriksaan kuantitatif nitrit dengan pereaksi asam sulfanilat dan NED yang membentuk warna ungu merah dan dapat diukur dengan panjang gelombang maksimum 540 nm (Herlich, 2000). Metode ini berdasarkan atas reaksi diazotasi dimana senyawa amin primer aromatik dikopling dengan NED. Dengan adanya nitrit maka akan menghasilkan senyawa yang berwarna ungu kemerahan yang dapat diukur secara spektrofotometri sinar tampak. Pada analisis menggunakan alat spektrofotometer sinar tampak dapat dilakukan pemilihan panjang gelombang dan pembuatan kurva kalibrasi. Panjang gelombang yang digunakan adalah panjang gelombang yang memiliki absorbansi maksimum dari suatu larutan baku pada konsentrasi tertentu. Kurva kalibrasi menunjukkan hubungan antara absorbansi dan konsentrasi baku sehingga diperoleh persamaan regresi linier. Persamaan regresi ini dipakai untuk menghitung kadar analit dalam sampel (Rohman, 2007). Persamaan reaksinya dapat dilihat pada Gambar 1.1 halaman 11.
2.6.1.2 Penentuan Kadar Nitrit dengan Metode Volumetri
Metode volumetri dilakukan secara permanganometri dan serimetri (Vogel, 1994). Permanganometri adalah suatu cara titrasi memakai kalium permanganat sebagai pentiter. Kalium permanganat merupakan oksidator paling kuat, dan asam sulfat merupakan asam yang paling cocok digunakan sebagai pelarut dalam proses ini karena jika digunakan asam klorida maka sebagian permanganatnya akan membentuk klorin (Rohman, 2007). Metode serimetri menggunakan serium (IV) sulfat dimana kelebihan serium (IV) sulfat dititrasi dalam ammonium besi (II) sulfat dan asam N-fenilantranilat sebagai indikator. Tetapan volume larutan serium (IV) sulfat standar yang telah bereaksi dengan larutan nitrit, dan dihitung kadar nitrit (Vogel, 1994).
2.6.2 Penentuan Kadar Nitrat
2.6.2.1 Penentuan Kadar Nitrat dengan Metode Diazotasi
Logam Zn dapat dipakai untuk mereduksi nitrat menjadi nitrit. Prosedur yang umum dilakukan untuk mereduksi nitrat menjadi nitrit menggunakan reduktor logam Zn dan penentuan hasil nitrit berdasarkan atas reaksi diazotasi dimana senyawa amin primer aromatik dikopling dengan NED. Dengan adanya nitrit akan menghasilkan senyawa berwarna ungu kemerahan yang dapat diukur secara spektrofotometri sinar tampak. Maka kadar nitrat adalah selisih total nitrit sebelum reduksi dengan nitrit sesudah reduksi (Vogel, 1985). Persamaan reaksinya dapat dilihat pada Gambar 1.1 halaman 11.
2.6.2.2 Penetapan Kadar Nitrat dengan Metode Asam Phenoldisulfat
Menurut Boltz dalam Dewi (2005), asam phenoldisulfat mempunyai kelemahan pada keadaan tertentu seperti adanya bahan-bahan biologis, walaupun begitu pereaksi ini dapat digunakan untuk menganalisa beberapa sampel dengan
hasil yang akurat. Metode ini mempunyai kepekaan yang tinggi karena dapat mengukur kadar nitrat dengan jumlah yang sedikit yaitu 1 µg. Pembentukan warna dari asam phenoldisulfat dengan nitrat memenuhi hukum Beer dengan jarak panjang gelombang yang luas. Sensitivitas dan kekuatan terbesar diperoleh ketika pengukuran dilakukan pada panjang gelombang 410 nm.
2.6.2.3 Penentuan Kadar Nitrat dengan Metode Asam Kromatropat
Menurut Boltz dalam Dewi (2005), asam kromatropat (asam 1,8-dihidroksi-3, 6-naphthalenisulonat) adalah pereaksi yang sangat peka dan selektif dalam media asam sulfat pekat untuk penentuan nitrat. Dua mol nitrat bereaksi dengan 1 mol asam kromatropat. Pengukuran dilakukan pada panjang gelombang 410 nm. Ion iodida, iodat, selenite, selenate, lead, barium dan strontium tidak boleh ada dalam sampel. Chromium (III) merupakan gangguan jika jumlahnya di atas 20 µg/g. Gangguan-gangguan oleh nitrit dan bahan pengoksidasi lainnya dapat dihilangkan dengan penambahan larutan sulfit urea. Gangguan yang disebabkan oleh klorida dihindari dengan penambahan larutan antimony (III) sulfat agar membentuk kompleks dengan klorida.
2.6.2.4 Penetapan Kadar Nitrat dengan Metode Brucin
Reaksi nitrat dengan brucin dalam media asam sulfat, membentuk warna merah yang berubah dengan cepat menjadi kuning. Warna kuning merupakan hasil oksidasi yang menyerap dengan kuat pada panjang gelombang 400-410 nm. Pembentukan warna yang baik dapat terjadi bila perbandingan asam sulfat pekat dan larutan nitrat sebanyak 2:1. Ada dua kelemahan dari sistim pewarnaan brucin. Pertama, tidak memenuhi hukum Beer pada daerah panjang gelombang yang memberikan serapan maksimum. Kedua, warna yang terbentuk tidak stabil, oleh karena itu seluruh perlakuan harus dilakukan secara tepat (Herlich, 1990).
2.7 Validasi
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapa parameter validasi adalah kecermatan (accuracy), keseksamaan (precision), Selektivitas (spesifikasi), linearitas dan rentang, batas deteksi dan batas kuantitasi, ketangguhan metode (rugged-ness), dan kekuatan (robustness) (Harmita, 2004). Validasi dilakukan untuk menjamin bahwa metode analisis yang dilakukan akurat, spesifik, reprodusibel dan tahan pada kisaran analit yang dianalisis (Rohman, 2007).
2.7.1 Perolehan Kembali
Metode adisi dapat dilakukan dengan dua cara yaitu metode simulasi (spiked-placebo recovery) dan metode penambahan baku (standard addition
method). Dalam metode simulasi sejumlah analit bahan murni (senyawa
pembanding kimia) ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar sebenarnya). Dalam metode penambahan baku, sampel dianalisis lalu sejumlah analit yang diperiksa dengan konsentrasi tertentu ditambahkan ke dalam sampel dicampur dan kemudian dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar sebenarnya (Harmita, 2004).
Rumus perhitungan persen perolehan kembali: % perolehan kembali = CF - CA
C*A
x 100%
Keterangan:CF = Konsentrasi analit dalam sampel yang diperoleh setelah penambahan bahan baku
CA = Konsentrasi analit dalam sampel sebelum penambahan bahan baku C*A = Konsentrasi bahan baku yang ditambahkan di dalam sampel
2.7.2 Penentuan Batas Deteksi dan Batas Kuantitas
Batas deteksi atau Limit Of Detection (LOD) adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon siknifikan dibandingkan dengan blanko (Harmita, 2004).
Rumus perhitungan batas deteksi:
Batas deteksi = 3× sy/x Slope
Batas kuantitas atau limit of quantitation (LOQ) adalah kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004). Batas kuantitasi dapat dihitung dengan rumus sebagai berikut: Rumus perhitungan batas kuantitas:
Batas kuantitasi = 10× Sy/x Slope
2.7.3 Analisis Data Secara Statistik
Kadar dapat dihitung dengan persamaan garis regresi dan untuk menentukan data diterima atau ditolak digunakan rumus:
thitung = | Xi – X n - 1 |
Dengan dasar penolakan apabila t hitung ≥ t tabel. Untuk mencari kadar sebenarnya dengan α 1/2 = 0,025, dk = n - 1, digunakan rumus:
μ = X ± t x SD √n Keterangan:
μ = Kadar sebenarnya
X = Kadar analit dalam sampel n = Jumlah pengulangan
t = Harga ttabel sesuai dk
dk = derajat kebebasan (dk = n - 1) α = Tingkat kepercayaan