x INTISARI
Alga coklat adalah alga laut yang terbesar ukurannya dan bentuknya sangat beragam. Salah satunya adalah Sargassum cymosum C. Agardh yang banyak tumbuh di perairan Indonesia. Tumbuhan alga, khususnya alga coklat mengandung phlorotannin yang memiliki beberapa aktivitas biologik. Namun pemanfaatan sumber bahan bioaktif dari alga di bidang industri farmasi, kosmetik, dan makanan belum banyak dilakukan.
Tujuan dari penelitian ini adalah untuk mendapatkan phlorotannin dan menetapkan kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh menggunakan metode kolorimetri Folin Ciocalteau. Metode penelitiannya adalah non eksperimental. Ektraksi menggunakan metode soxhletasi dengan cairan penyari metanol. Ekstrak kental kemudian difraksinasi dengan kloroform, akuades, dan etil asetat untuk mendapatkan phlorotannin.
Kadar phlorotannin dalam fraksi etil asetat ditetapkan dengan metode kolorimetri Folin Ciocalteau. Menggunakan larutan standar phloroglucinol yang dibuat seri konsentrasi baku 1,0; 2,0; 3,0; 4,0; 5,0; dan 6,0 ppm dengan pelarut aseton 75%. Konsentrasi phlorotannin dihitung equivalen dengan phloroglucinol (mg PGE/g fraksi). Kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh yang didapat adalah 6,36 ± 0,04 mg PGE/ g fraksi yang diukur menggunakan spektrofotometri, dibaca pada panjang gelombang 750,1 nm.
Kata kunci : phlorotannin, alga coklat Sargassum cymosum C. Agardh, Folin Ciocalteau.
xi
ABSTRACT
Brown alga is kind of seaweeds whose the biggest size and vary in its kind. One of them is Sargassum cymosum C. Agardh which grows in Indonesian sea. Algae, particularly brown algae contains of phlorotannin which has some biologic activity whereas, rarely pharmacy industries, cosmetics, and food used the algae’s bioactive source.
The goals of this study is for getting phlorotannin and determining phlorotannin concentration in ethyl acetate fractional of brown alga Sargassum cymosum C. Agardh by colorimetric Folin Ciocalteau method. The method of this study is non experimental. Extraction have been done by soxhletation method with methanol solvent. The viscous extract than was fractionated with methanol, chloroform, aquadest and ethyl acetate to gain phlorotannin.
Concentration of phlorotannin in ethyl acetate fractional was determined by colorimetric Folin Ciocalteau method. Using phloroglucinol standard that was made in calibration series 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; 6,0 ppm with acetone 75 % solvent. Phlorotannin concentration was equivalently calculated with phloroglucinol (mg PGE/g fractional). Concentration of phlorotannin in ethyl acetate fractional of brown alga Sargassum cymosum C. Agardh has been investigated was 6,36 ± 0,04 mg PGE /g fractional was scanned using spectrophotometric at 750,1 nm the maxima wavelength.
Keyword : phlorotannin, polifenol, brown alga Sargassum cymosum C. Agardh, Folin Ciocalteau.
PENETAPAN KADAR
PHLOROTANNIN
DALAM FRAKSI ETIL
ASETAT ALGA COKLAT
Sargassum cymosum
C. Agardh
DENGAN METODE KOLORIMETRI FOLIN CIOCALTEAU
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Diajukan oleh : Andriani Noerlita Ningrum
NIM :048114063
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
2008
ii
PENETAPAN KADAR
PHLOROTANNIN
DALAM FRAKSI ETIL
ASETAT ALGA COKLAT
Sargassum cymosum
C. Agardh
DENGAN METODE KOLORIMETRI FOLIN CIOCALTEAU
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Diajukan oleh : Andriani Noerlita Ningrum
NIM :048114063
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
2008
iii
iv
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma : Nama : Andriani Noerlita Ningrum
Nomor Mahasiswa : 048114063
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
“Penetapan Kadar Phlorotannin dalam Fraksi Etil Asetat Alga Coklat Sargas-sum cymoSargas-sum C. Agardh dengan Metode Kolorimetri Folin Ciocalteau”
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 27 Juni 2008
Yang menyatakan
Andriani Noerlita Ningrum
v
HALAMAN PERSEMBAHAN
Siapapun yang bermaksud menjadi seorang guru bagi manusia, biarlah dia mengawali dengan mengajari dirinya sendiri sebelum mengajari orang lain, dan
mengajar dengan teladan sebelum mengajar dengan kata-kata. Selama dia mengajar dirinya sendiri dan memperbaiki perilakunya sendiri, ia lebih patut
dihargai dan dihormati, daripada dia yang mengajari dan mencoba memperbaiki perilaku orang lain (Kahlil Gibran).
Skripsi ini kupersembahkan untuk: Keluarga, ayah, ibu, adik-adikku tercinta, Teman-teman dan penyemangat hidupku, Almamaterku.
vi P R A K A T A
Puji syukur kami panjatkan kehadirat Tuhan Yang Maha Esa atas terselesaikannya penelitian untuk skripsi yang berjudul ”Penetapan Kadar
Phlorotannin dalam Fraksi Etil Asetat Alga Coklat Sargassum cymosum C. Agardh dengan Metode Kolorimetri Folin Ciocalteau”. Penelitian ini merupakan bagian dari program hibah penelitian, dan menjadi tahap awal penelitian selanjutnya yaitu aplikasi phlorotannin yang terkandung dalam alga di bidang kosmetik khususnya sebagai sunscreen yang memiliki efek fotoprotektif.
Selama pelaksanaan penelitian hingga selesainya penyusunan skripsi, penulis menerima banyak bantuan, dukungan dan kerjasama dari berbagai pihak. Oleh karena itu, penulis mengucapkan terimakasih yang sebesar-besarnya kepada:
1. Allah SWT yang telah memberikan rahmat dan karunia-Nya, yang selalu memberi petunjuk dalam setiap langkah.
2. Ibu Rita Suhadi, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
3. Ibu Dra. A. Nora Iska Harnita, M.Si., Apt., selaku Ketua peneliti dalam salah satu penelitian program hibah. Terima kasih telah menjadikan penulis sebagai bagian dari proyek ini, memberikan semangat dan kritik yang membangun.
vii
4. Bapak Ign. Kristio Budiasmoro, M.Si., selaku dosen pembimbing dan penguji yang telah banyak meluangkan waktu, memberi saran, kritik, serta dorongan sehingga proses penyusunan skripsi ini dapat berjalan lancar.
5. Ibu Christine Patramurti, M.Si., Apt., selaku dosen penguji yang telah banyak memberi masukan dan arahan untuk perbaikan skripsi ini.
6. Ibu Erna Tri Wulandari, M.Si., Apt., selaku dosen penguji yang telah banyak memberi masukan yang bermanfaat bagi skripsi ini.
7. Semua dosen yang telah menjadikan penulis ada dan berguna. Terima kasih atas bimbingannya.
8. Semua laboran khususnya laboran lantai 4 (Mas Kunto, Mas Parlan, Mas Wagiran, Pak Prapto) untuk kerja sama dan bantuannya selama penelitian. 9. Keluarga tercinta, Bapak, Ibu, Dek Ari, Dek Rio yang tak bosan-bosannya
memberikan kasih sayang dan semangat untuk terus melangkah.
10. Wisnu, yang mengajariku untuk terus berusaha dan bertahan sampai akhir. Terima kasih untuk perhatian, support, dan harapan yang membuatku terus terjaga. Terima kasih untuk tiap detik yang terasa semakin singkat.
11. Teman-teman satu proyek, Hendry, Angel, Dewi, Fani, Elsa, Dipta, teman-teman proyek ”teh” (esp. Dona), terima kasih atas support dan bantuannya selama penelitian sampai penyusunan skripsi.
12. The big family of ”kontrakan kartun”, felic, ndk, pakdhe, gogon, bela, tedy, tembi, edo, anna, cicil, tery, ina, chacha, ririn. Thanks for the amazing life.
viii
13. Teman-teman Fakultas Farmasi Universitas Sanata Dharma dan semua yang berperan dalam penelitian sampai penyusunan skripsi, yang tidak dapat penulis sebutkan satu persatu.
Penulis menyadari bahwa masih banyak kekurangan dalam penyelesaian skripsi ini, sehingga penulis mengharapkan kritik dan saran yang dapat membantu menyempurnakan skripsi ini. Semoga skripsi ini dapat berguna bagi banyak orang. Terima kasih.
Yogyakarta, 19 April 2008 Penulis
Andriani Noerlita Ningrum
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 19 April 2008 Penulis
Andriani Noerlita Ningrum
x INTISARI
Alga coklat adalah alga laut yang terbesar ukurannya dan bentuknya sangat beragam. Salah satunya adalah Sargassum cymosum C. Agardh yang banyak tumbuh di perairan Indonesia. Tumbuhan alga, khususnya alga coklat mengandung phlorotannin yang memiliki beberapa aktivitas biologik. Namun pemanfaatan sumber bahan bioaktif dari alga di bidang industri farmasi, kosmetik, dan makanan belum banyak dilakukan.
Tujuan dari penelitian ini adalah untuk mendapatkan phlorotannin dan menetapkan kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh menggunakan metode kolorimetri Folin Ciocalteau. Metode penelitiannya adalah non eksperimental. Ektraksi menggunakan metode soxhletasi dengan cairan penyari metanol. Ekstrak kental kemudian difraksinasi dengan kloroform, akuades, dan etil asetat untuk mendapatkan phlorotannin.
Kadar phlorotannin dalam fraksi etil asetat ditetapkan dengan metode kolorimetri Folin Ciocalteau. Menggunakan larutan standar phloroglucinol yang dibuat seri konsentrasi baku 1,0; 2,0; 3,0; 4,0; 5,0; dan 6,0 ppm dengan pelarut aseton 75%. Konsentrasi phlorotannin dihitung equivalen dengan phloroglucinol (mg PGE/g fraksi). Kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh yang didapat adalah 6,36 ± 0,04 mg PGE/ g fraksi yang diukur menggunakan spektrofotometri, dibaca pada panjang gelombang 750,1 nm.
Kata kunci : phlorotannin, alga coklat Sargassum cymosum C. Agardh, Folin Ciocalteau.
xi
ABSTRACT
Brown alga is kind of seaweeds whose the biggest size and vary in its kind. One of them is Sargassum cymosum C. Agardh which grows in Indonesian sea. Algae, particularly brown algae contains of phlorotannin which has some biologic activity whereas, rarely pharmacy industries, cosmetics, and food used the algae’s bioactive source.
The goals of this study is for getting phlorotannin and determining phlorotannin concentration in ethyl acetate fractional of brown alga Sargassum cymosum C. Agardh by colorimetric Folin Ciocalteau method. The method of this study is non experimental. Extraction have been done by soxhletation method with methanol solvent. The viscous extract than was fractionated with methanol, chloroform, aquadest and ethyl acetate to gain phlorotannin.
Concentration of phlorotannin in ethyl acetate fractional was determined by colorimetric Folin Ciocalteau method. Using phloroglucinol standard that was made in calibration series 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; 6,0 ppm with acetone 75 % solvent. Phlorotannin concentration was equivalently calculated with phloroglucinol (mg PGE/g fractional). Concentration of phlorotannin in ethyl acetate fractional of brown alga Sargassum cymosum C. Agardh has been investigated was 6,36 ± 0,04 mg PGE /g fractional was scanned using spectrophotometric at 750,1 nm the maxima wavelength.
Keyword : phlorotannin, polifenol, brown alga Sargassum cymosum C. Agardh, Folin Ciocalteau.
xii DAFTAR ISI
Halaman
HALAMAN JUDUL... ii
HALAMAN PERSETUJUAN PEMBIMBING... iii
HALAMAN PENGESAHAN... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI... x
ABSTRACT... xi
DAFTAR ISI.. ... xii
DAFTAR GAMBAR... xvi
DAFTAR TABEL... xvii
DAFTAR LAMPIRAN... xviii
BAB I. PENGANTAR... 1
A. Latar Belakang ... 1
B. Perumusan Masalah ... 3
C. Keaslian Penelitian... 3
D. Manfaat ... 3
1. Manfaat teoritis ... 3
2. Manfaat metodologis ... 4
xiii
3. Manfaat praktis... 4
E. Tujuan ... 4
1. Tujuan umum... 4
2. Tujuan khusus ... 4
BAB II. TINJAUAN PUSTAKA... 5
A. Alga Coklat Sargassum C. Agardh... 5
B. Polifenol Alga (Phlorotannin)... 6
C. Soxhletasi ... 7
D. Spektrofotometri... 9
E. Kolorimetri... 11
F. Metode Folin Ciocalteau... 12
G. Keterangan Empiris... 14
BAB III. METODOLOGI PENELITIAN ... 16
A. Jenis Rancangan Penelitian ... 16
B. Variabel Penelitian dan Definisi Operasional ... 16
1. Variabel Penelitian ... 16
2. Definisi Operasional ... 16
C. Bahan dan Alat... 17
1. Bahan ... 17
2. Alat... 18
D. Tata Cara Penelitian ... 18
1. Preparasi sampel alga coklat Sargassum cymosum C. Agardh... 18
xiv
2. Uji kualitatif senyawa fenolik... 19
a. Preparasi ekstrak ... 19
b. Uji tannin dan polifenol ... 19
3. Isolasi crude phlorotannin... 20
4. Optimasi metode kolorimetri dengan Folin Ciocalteau ... 21
a. Pembuatan larutan standar ... 21
b. Penentuan operating time (OT)... 21
c. Penentuan panjang gelombang maksimum (? maks)... 21
5. Penetapan kurva baku phloroglucinol ... 22
6. Estimasi kadar polifenol total pada fraksi etil asetat alga coklat Sargassum cymosum C. Agardh... 22
BAB IV. HASIL DAN PEMBAHASAN ... 24
A. Preparasi sampel alga coklat Sargassum cymosum C. Agardh... 24
B. Uji kualitatif senyawa fenolik... 28
C. Isolasi crude phlorotannin... 29
D. Optimasi metode kolorimetri dengan reagen Folin Ciocalteau... 31
1. Pembuatan larutan standar phloroglucinol... 31
2. Penentuan operating time (OT)... 32
3. Penentuan panjang gelombang maksimum (? maks)... 33
E. Penetapan kurva baku phloroglucinol ... 35
F. Penetapan kadar phlorotannin fraksi etil asetat alga coklat Sargassum cymosum C. Agardh... 37
xv
BAB V. KESIMPULAN DAN SARAN... 43
A. Kesimpulan ... 43
B. Saran... 43
DAFTAR PUSTAKA ... 44
LAMPIRAN... 48
BIOGRAFI PENULIS ... 61
xvi
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur phloroglucinol... 7
Gambar 2. Struktur fucofuroeckol ... 8
Gambar 3. Diagram sederhana spektrofotometer... 9
Gambar 4. Proses oksidasi fenol oleh enzim PPO... 26
Gambar 5. Reaksi penetapan kadar air dengan Karl Fischer... 27
Gambar 6. Reaksi pembentukan kompleks gugus fenolik dan FeCl3... .... 29
Gambar 7. Kurva baku vs serapan hasil penetapan operating time... 33
Gambar 8. Hasil pembacaan ? maks phloroglucinol (0,1; 0,3; dan 0,6 ppm) setelah direaksikan dengan Folin Ciocalteau... 34
Gambar 9. Kurva baku hubungan kadar dan absorbansi phloroglucinol... 37
Gambar 10. Kesetimbangan reaksi phloroglucinol dalam suasana basa... 38
Gambar 11. Reaksi phloroglucinol dengan reagen Folin Ciocalteau... 39
xvii
DAFTAR TABEL
Halaman Tabel I. Hasil uji kandungan senyawa polifenol serbuk alga... 28 Tabel II. Data untuk persamaan kurva baku... 36 Tabel III. Hasil pembacaan absorbansi fraksi etil asetat alga coklat Sargassum
cymosum C. Agardh... 40 Tabel IV.Hasil penetapan kadar phlorotannin dalam fraksi etil asetat alga coklat
Sargassum cymosum C. Agardh... 41
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat keterangan hasil identifikasi spesies alga coklat... ... 48
Lampiran 2. Data perhitungan kadar air dengan Karl Fischer... 50
Lampiran 3. Data penimbangan replikasi seri baku phloroglucinol... 51
Lampiran 4. Contoh perhitungan seri kadar baku phloroglucinol... 52
Lampiran 5. Hasil scanning operating time (OT)... 52
Lampiran 6. Hasil scanning ? maks kadar phloroglucinol 1,0 ppm setelah direaksikan dengan Folin Ciocalteau... 53
Lampiran 7. Hasil scanning ? maks kadar phloroglucinol 3,0 ppm setelah direaksikan dengan Folin Ciocalteau... 54
Lampiran 8. Hasil scanning ? maks kadar phloroglucinol 6,0 ppm setelah direaksikan dengan Folin Ciocalteau... 55
Lampiran 9. Hasil pembacaan absorbansi seri baku phloroglucinol pada ketiga ? maks... 55
Lampiran 10. Kurva baku phloroglucinol... 56
Lampiran 11. Data penimbangan sampel... 56
Lampiran 12. Data absorbansi sampel fraksi etil asetat Sargassum cymosum C. Agardh... 57
Lampiran 13. Contoh perhitungan kadar sampel ... 57
Lampiran 14. Foto hasil uji kualitatif alga coklat Sargassum cymosum C. Agardh... 58
xix
Lampiran 15. Foto instrumen spektrofotometer UV-VIS Perkin Elmer
Lambda-20... 59 Lampiran 16. Foto autoklaf... 59 Lampiran 17. Foto vacuum rotary evaporator... 60
1 BAB I PENGANTAR
A. Latar Belakang
Alga coklat adalah alga laut yang terbesar ukurannya, bentuknya sangat beragam dan tersebar hampir di seluruh perairan pantai. Salah satu genus alga coklat adalah Sargassum yang merupakan spesies yang kompleks baik morfologi maupun susunan anatominya. Sargassum merupakan salah satu genus yang paling menonjol dari kelas Phaeophyceae yang diperkirakan ada 400 spesies yang tersebar di daerah tropis dan subtropis.
Salah satu kandungan dari tumbuhan alga adalah polifenol yang dikenal sebagai phlorotannin dan merupakan senyawa polifenol yang hanya ditemukan pada tumbuhan alga khususnya jenis-jenis alga coklat (Burtin, 2003). Beberapa aktivitas biologik phlorotannin yang telah diteliti adalah antiproliferasi dan antioksidan (Athukorala et al., 2006; Yuan dan Walsh, 2006; Kang et al., 2005a), antiinflamasi (Shin et al., 2006), efek protektif terhadap ionizing radiation (Kang et al., 2006), inhibitor matriks metalloroteinase (Kim et al., 2006), kemampuan untuk mengabsorbsi sinar UV (Roleda et al., 2006; Swanson dan Druchl, 2002), sitoprotektif terhadap stres oksidatif (Kang et al., 2005b), dan inhibitor HIV-1 reverse transcriptase dan protease (Ahn et al., 2004).
Eksplorasi senyawa polifenol terus dilakukan, akan tetapi eksplorasi tersebut masih mengandalkan tumbuhan-tumbuhan terestrial. Tumbuhan alga merupakan salah satu kekayaan laut Indonesia yang sangat potensial, namun
2
pemanfaatannya sebagai agen biomedis belum cukup maksimal. Fokus pengembangan produk alam dari terestrial menjadi pengembangan berbasis kelautan sangat diperlukan, mengingat wilayah laut Indonesia sebagai ”the largest marine-mega biodiversity” (Dahuri, 2003).
Penelitian yang dilakukan terbatas pada phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh. Phlorotannin dalam fraksi etil asetat merupakan phlorotannin dengan polimer intermediet yang memiliki aktifitas mengabsorbsi radiasi sinar ultraviolet secara maksimum sehingga dapat dikembangkan menjadi produk sediaan sunscreen. Phlorotannin dengan polimer intermediet akan memberikan serapan pada panjang gelombang UV A (400-320 nm) dan UV B (320 – 280 nm), sedangkan pada polimer panjang phlorotannin akan memberikan serapan pada daerah visibel (400 – 800 nm) sehingga tidak dapat dikembangkan menjadi sediaan sunscreen.
Zhang et al. (2006) telah melakukan penelitian tentang metode sederhana untuk estimasi kandungan polifenol total pada rumput laut dan ekstraknya berdasarkan reaksi kolorimetri Folin Ciocalteau. Metode Folin Ciocalteau merupakan metode pilihan untuk mengestimasi kadar fenol total dalam tanaman tanpa interferensi dari senyawa lain. Kelebihan metode Folin Ciocalteau diantaranya adalah memiliki prosedur yang sederhana dan hanya membutuhkan satu jenis reagen.
Penetapan kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh dihitung ekivalen dengan phloroglucinol. Digunakan standar phloroglucinol karena merupakan salah satu monomer dari
3
phlorotannin, memiliki gugus pereduksi yang dapat dikembangkan sebagai produk sediaan sunscreen, strukturnya mirip dengan polifenol alga, dan mudah diperoleh dalam bentuk murni.
B. Perumusan Masalah
Permasalahan dalam penelitian ini difokuskan pada phlorotannin dalam fraksi etil asetat yang diisolasi dari alga coklat Sargassum cymosum C. Agardh yang hidup tersebar di pantai selatan Yogyakarta. Rumusan masalah sebagai berikut:
a. Apakah phlorotannin dapat diisolasi dari alga coklat Sargassum cymosum C. Agardh?
b. Berapakah kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh yang diukur dengan metode Folin Ciocalteau?
C. Keaslian Penelitian
Sepengetahuan peneliti belum pernah dilakukan penelitian tentang penetapan kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh dengan metode Folin Ciocalteau.
D. Manfaat 1. Manfaat teoritis
Penelitian ini diharapkan dapat memberi informasi kandungan phlorotannin hasil isolasi dari alga coklat Sargassum cymosum C. Agardh.
4
2. Manfaat metodologis
Penelitian ini dapat menjadi acuan tentang penggunaan metode Folin Ciocalteau dalam penetapan kadar phlorotannin.
3. Manfaat praktis
Memberi informasi kepada masyarakat kandungan polifenol alga coklat Sargassum cymosum C. Agardh yang bermanfaat di bidang industri farmasi,kosmetik, dan makanan.
E. Tujua n Penelitian 1. Tujuan umum :
Tujuan umum penelitian ini adalah menetapkan kadar phlorotannin alga coklat Sargassum cymosum C. Agardh.
2. Tujuan khusus :
a. Melakukan isolasi phlorotannin berupa phlorotannin kasar pada fraksi etil asetat alga coklat Sargassum cymosum C. Agardh.
b. Mengetahui kadar phlorotannin dalam alga coklat Sargassum cymosum C. Agardh yang diukur dengan metode Folin Ciocalteau.
5
BAB II
PENELAAHAN PUSTAKA
A. Alga coklat Sargassum C. Agardh
Alga coklat marga Sargassum termasuk dalam kelas Phaeophyceae tumbuh subur di daerah tropis, pada kedalaman laut 0,5 – 10 m, suhu perairan 27,25 – 29,30ºC, salinitas 32 – 33,5%, dan intensitas cahaya matahari berkisar 6500-7500 lux (Kadi, 2007). Alga Sargassum tumbuh berumpun dengan untaian bercabang-cabang dengan panjang thalli utama mencapai 1-3 m dan tiap percabangan terdapat gelembung udara berbentuk bulat (Boney, 1965).
Tempat tumbuh alga Sargassum paling banyak di daerah perairan jernih yang mempunyai substrat dasar batu karang, karang mati, batuan vulkanik dan benda-benda yang bersifat massive yang berada di dasar perairan. Jenis alga Sargassum yang banyak tersebar di pantai selatan Pulau Jawa di antaranya adalah Sargassum binderi, Sargassum crassifolium, Sargassum duplicatum, Sargassum hystrix, dan Sargassum sp. (Kadi, 2007)
Reproduksi marga Sargassum yang termasuk bangsa Fucales, marga Sargassaceae dikenal dua cara yaitu; reproduksi asexual (vegetatif) dan sexual (generatif). Reproduksi vegetatif dilakukan melalui fragmentasi yaitu potongan thallus berkembang melakukan pertumbuhannya. Reproduksi generatif yaitu perkembangan individu melalui organ jantan (antheridia) dan organ betina (oogenia). Organ-organ tersebut terjadi dan berada dalam satu lubang yang disebut koseptakel (Kadi, 2007).
6
Kandungan bahan kimia utama Sargassum sebagai sumber alginat yaitu senyawa makronutrien heteropolisakarida. Kandungan makronutrien yang lain berupa mineral yang tinggi (yodium dan kalsium), protein dan asam amino, lipid dan asam lemak (asam linolenat, asam eikosapentoat dan asam arakidonat). Selain itu juga terdapat kandungan mikronutrien antara lain vitamin C, vitamin E, polifenol, dan karotenoid (Kadi, 2007).
B. Polifenol Alga (Phlorotannin)
Polifenol merupakan suatu senyawa aromatik yang mengandung substituen gugus –OH. Diantara banyak polifenol tumbuhan, flavonoid seperti kuersetin adalah bentuk yang paling banyak ditemukan. Akan tetapi, senyawa fenolik seperti kuinon, lignan, xantin, kumarin, dan lain- lain masih ditemukan dalam jumlah tertentu. Dengan penambaha n struktur monomer dan dimer, terdapat tiga bentuk penting polimer fenolik yaitu, lignin yang merupakan dinding sel, melanin sebagai pigmen warna tanaman, dan tannin yang terdapat pada kulit tanaman (Harborne, 1989).
Polifenol alga atau dikenal sebagai phlorotannin berasal dari unit phloroglucinol (1,3,5-trihydroxybenzine)(Burtin, 2003). Phlorotannin terdiri dari molekul dengan struktur dan tingkat polimerisasi yang heterogen yaitu phloroglucinol (2%) dan oligomernya seperti eckol (trimer, 3%), phlorofucofuroeckol A (pentamer, 28%), dieckol (hexamer, 7%), 8,8’-bieckol (hexamer, 7%) dan lainnya (30%). Struktur dan tingkat polimerisasi yang heterogen memungkinkan phlorotannin memiliki aktivitas biologik yang luas.
7
Kandungan phlorotannin yang paling tinggi ditemukan pada alga coklat, yaitu antara 5-15% berat kering (Nagayama et al., 2002).
Menurut Glombitza dan Gerstberger (1985), Phlorotannin telah diisolasi dari spesies pada beberapa genus alga coklat (Eisenia, Fucus, Cystophora, Chorda, Cystoseria, Laminaria, Bifurcaria) dimana phlorotannin terdiri dari unit phloroglucinol dengan berpasangan secara oksidatif C – C atau C – O (cit., Harborne, 1989). Grosse-Dambues et al. (1983) melaporkan adanya cincin aromatik yang terhalogenasi dan molekul yang mengandung phloroglucinol sampai 8 unit. Salah satu bentuk strukturnya adalah fucofuroeckol dari Eisenia arborea (cit., Harborne, 1989). Dari alga coklat yang lain yaitu Bifurcaria bifurcata, diisolasi sebuah difenil eter dan dikarakterisasikan sebagai paracetate. Senyawa ini dinamakan bifuhalol yang diduga sebagai prekursor tannin Phaeophyta.
O H
O H HO
Gambar 1. Struktur Phloroglucinol
8
Gambar 2. Struktur Fucofuroeckol
C. Soxhletasi
Soxhletasi merupakan salah satu metode ekstraksi kontinyu yang sering digunakan jika perbandingan distribusi relatif kecil sehingga untuk pemisahan yang kuantitatif diperlukan beberapa tahap ekstraksi. Efisiensi pada ekstraksi jenis ini tergantung pada viskositas fase organik (Khopkar, 1990).
Penyarian berkesinambungan menggunakan alat soxhlet merupakan penyarian yang menghasilkan ekstrak cair dan dilanjutkan dengan proses penguapan. Cairan penyari dipanaskan hingga mendidih, kemudian uap penyari akan naik ke atas kemudia n akan mengembun karena didinginkan oleh pendingin balik. Embun akan turun melalui serbuk simplisia sambil melarutkan kandungan serbuk simplisia (Anonim, 1986). Pada soxhletasi larutan berkumpul di dalam wadah gelas dan setelah mencapai tinggi maksimal secara otomatis ditarik ke dalam labu, dengan demikian zat yang terekstraksi tertimbun melalui penguapan kontinyu dari bahan pelarut murni (Voigt, 1994).
Metode soxhletasi lebih menguntungkan karena uap panas tidak melalui serbuk simplisia tetapi melalui pipa samping, cairan penyari yang dibutuhkan
9
lebih sedikit, dan penyarian dapat langsung diteruskan tanpa menambah volume cairan penyari (Anomim, 1986).
D. Spektrofotometri
Spektrofotometri adalah metode analisis yang mengamati interaksi radiasi elektromagnetik dengan materi. Spektrofotometri memiliki ciri-ciri, yaitu dapat digunakan pada sistem organik dan anorganik, memiliki selektivitas sedang sampai tinggi, akurasinya baik, dan mudah dilakukan (Skoog et al., 1998).
Spektrofotometer adalah suatu instrumen yang digunakan untuk mengukur transmitan atau serapan suatu sampel sebagai fungsi panjang gelombang, pengukuran terhadap sederetan sampel pada suatu panjang gelombang tunggal dapat pula dilakukan (Day dan Underwood, 2002). Sastrohamidjojo (1991) menyatakan komponen-komponen pokok dari spektrofotometer meliputi: (1) sumber tenaga radiasi yang stabil, (2) sistem yang terdiri atas lensa- lensa, cermin, celah-celah, dan lain- lain, (3) monokromator untuk mengubah radiasi menjadi komponen-komponen panjang gelombang tunggal, (4) tempat cuplikan yang transparan, dan (5) detektor radiasi yang dihubungkan dengan sistem meter atau pencatat.
Gambar 3. Diagram sederhana spektrofotometer (Sastrohamidjojo, 1991)
sumber
10
Spektrofotometri visibel adalah bagian dari analisis spektroskopik yang menggunakan sumber radiasi elektromagnetik sinar tampak (380-780 nm) dengan instrumen spektrofotometer (Mulja dan Suharman, 1995).
Spektrofotometri dapat digunakan untuk analisis kuantitatif, oleh karena banyaknya cahaya yang diserap di frekuensi atau panjang gelombang tertentu sesuai transisi elektron yang terjadi, sehingga akan menentukan intensitas serapan (Willard et al., 1988).
Absorbsi radiasi visibel oleh kompleks logam disebabkan satu atau lebih transisi berikut, yaitu eksitasi ion logam, eksitasi ligan, atau transisi charge transfer. Eksitasi ion logam dalam kompleks biasanya memiliki daya serap molar yang kecil (e), 1-100 dan ini tidak berguna dalam analisis kuantitatif (Christian, 2004), akan tetapi transisi kompleks logam menunjukkan serapan yang sangat intens (e = 103-105) dalam visibel (Ohannesian dan Streeter, 2002).
Kompleks charge transfer terdiri dari gugus elektron donor yang berikatan dengan elektron aseptor. Ketika mengabsorpsi radiasi, elektron dari donor berpindah ke orbital aseptor (Skoog et.al., 1993).
Pada absorbsi senyawa anorganik, terjadi transisi antara orbital d yang terisi dengan tak terisi dengan energi yang bergantung dari ikatan ligan ke ion pusat (Skoog et.al., 1993). Pada kompleks ion logam dan ligan terjadi transisi orbital elektron d dari ion logam ke orbital p* dari ligan atau dari orbital elektron p ligan ke orbital d dari ion logam (Ohannesian dan Streeter, 2002).
11
Intensitas suatu serapan dapat dinyatakan sebagai transmitans (T) yang didefinisikan sebagai berikut :
....1
Rumusan yang lebih tepat untuk intensitas serapan diturunkan dari hukum Lambert-Beer. Hukum ini menyatakan hubungan antara serapan dengan tebalnya cuplikan dan konsentrasi bahan penyerap.
Hubungan tersebut dinyatakan sebagai berikut :
....2 Keterangan :
T = persen transmitan
Io = intensitas radiasi yang datang I = intensitas radiasi yang diteruskan e = daya serap molar (L.mol-1.cm-1) c = konsentrasi larutan (mol.L-1) b = panjang sel (cm)
A = serapan (Silverstein et al., 1991)
E. Kolorimetri
Kolorimetri adalah suatu teknik pengukuran cahaya yang diabsorbsi oleh zat berwarna, baik yang terbent uk dari asalnya maupun yang bereaksi dengan zat lain (Khopkar, 1990). Metode kolorimetri didasarkan pada gugus amin aromatik, amin alifatik, atau gugus yang bereaksi membentuk kompleks serta memiliki rantai panjang. Metode ini lebih banyak digunakan karena lebih sederhana dan lebih sensitif. Yang ditentukan pada kolorimetri adalah serapan cahaya oleh
A =
12
larutan yang berwarna. Kadar larutan dibuat dengan konsentrasi menaik dan membandingkan dengan senyawa yang dianalisis. Kolorimetri juga mencakup pengubahan senyawa tidak berwarna menjadi berwarna dan penentuan fotometrinya dilakukan dalam daerah sinar tampak (Roth dan Blaschke, 1994). Kriteria analisis kolorimetri yang baik adalah :
a. menghasilkan reaksi warna yang khusus dan intensif
Untuk mendapatkan hasil yang akurat maka warna yang dihasilkan harus sama dan waktu untuk mencapai warna yang maksimal harus cukup lama.
b. keterulangan
Kolorimetri harus memberikan hasil reprodusibel pada kondisi spesifik. c. kejernihan larutan
larutan harus bebas dari pengo tor jika pembanding yang dibuat dengan standar. Kekeruhan akan menyerap cahaya.
d. kepekaan yang tinggi
hal ini baik bila waktunya sudah ditentukan, maka reaksi warnanya memiliki kepekaan yang tinggi. Hal ini juga akan menarik bila hasil reaksi menyerap secara kuat dalam visibel daripada dalam UV (Vogel,1978)
F. Metode Folin Ciocalteau
Menurut Van Alstyne (1995), total senyawa fenolik dapat ditentukan dengan metode Folin Ciocalteau yang dimodifikasi (cit., Hammerstrom, Dethier, dan Duggins, 1998) dan diband ingkan dengan standar phloroglucinol. Metode Folin Ciocalteau direkomendasikan karena lebih memberikan warna pada sampel
13
dan sedikit kecenderungan untuk berinterferensi dengan komponen non-fenolik daripada metode yang lain (Waterman dan Mole, 1994).
Reagen Folin Ciocalteau merupakan larutan kompleks ion polimerik dari asam fosfomolibdat dan asam heteropolifosfotungstat (Jansoon, 2005). Reagen ini dibuat dengan mencampur sodium tungstat dan asam fosfomolibdat dalam asam fosfat, dididihkan selama 2 jam, kemudian didinginkan, dipekatkan, dan disaring. Modifikasi dari metode ini terdiri dari penambahan lithium sulfat dan bromin ke dalam reagen fosfotungstat–fosfomolibdat pada akhir fase pendidihan, dilanjutkan dengan pendinginan dan pemekatan. Penambahan lithium mencegah pembentukan endapan yang dapat berinterferensi dengan pembentukan intensitas warna (Folin dan Ciocalteau, 1944).
Reaksi ini berdasar pada reduksi campuran dari reagen fosfotungstat (WO4-) – fosfomolibdat (MoO42-) oleh gugus hidroksil fenolik (Box, 1983). Reagen Folin Ciocalteau merupakan rangkaian polimerik yang memiliki bentukan umum dengan pusat unit tetrahedral fosfat (PO43-) yang dikelilingi beberapa unit oktahedral asam-oksi molibdenum. Sehingga kompleks oktahedral yang terbentuk merupakan kompleks MoO3-fosfat dengan fosfor (P) sebagai pusatnya. Molibdat pada kompleks tersebut dapat disubstitusi oleh tungsten (W). Reaksi tersebut menghasilkan warna biru ungu yang dapat diukur absorbansinya dengan spektrofotometer (Jansoon, 2005).
14
G. Keterangan empiris
Tumbuhan alga mengandung phlorotannin yang merupakan senyawa polifenol yang hanya ditemukan pada tumbuhan alga khususnya spesies alga coklat.
Phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh merupakan phlorotannin dengan polimer intermediet yang memiliki aktifitas mengabsorbsi radiasi sinar ultraviolet secara maksimum sehingga dapat dikembangkan menjadi produk sediaan sunscreen.
Crude phlorotannin dapat diperoleh dengan mengekstraksi tanaman menggunakan metode soxhletasi dengan penyari metanol. Dipilih metode soxhletasi untuk efisiensi penyari dan phlorotannin masih dapat dipertahankan hingga suhu 170°C dilihat dari sifat fisika-kimia monomernya yaitu phloroglucinol. Ekstrak kental kemudian difraksinasi dengan kloroform, akuades, dan etil asetat sehingga didapatkan fraksi etil asetat alga coklat. Digunakan penyari metanol, dimana dari hasil orientasi diperoleh rendemen lebih banyak dibandingkan dengan penyari etanol.
Dalam pengukuran kadar digunakan me tode kolorimetri dengan pereaksi Folin Ciocalteau sebagai senyawa pengkompleks membentuk senyawa berwarna biru yang dapat diukur absorbansinya menggunakan spektrofotometer visibel. Metode ini digunakan karena merupakan metode pilihan untuk mengestimasi kandungan fenol total dalam tanaman. Metode Folin Ciocalteau berdasar atas kemampuan mereduksi gugus hidroksil pada fenol sehingga tidak spesifik namun
15
sangat sensitif untuk mendeteksi semua kandungan senyawa polifenol dalam fraksi etil asetat alga coklat. Keuntungan metode Folin Ciocalteau adalah prosedurnya sederhana dan praktis karena hanya menggunakan satu jenis pereaksi.
Kadar phlorotannin yang terukur adalah kadar phlorotannin ekivalen dengan phloroglucinol (mg PGE/ g fraksi). Digunakan standar phloroglucinol karena merupakan monomer dari phlorotannin. Phloroglucinol memiliki gugus pereduksi yang dapat dikembangkan sebagai produk sediaan sunscreen, strukturnya sederhana, mirip dengan struktur polifenol alga dan mudah diperoleh dalam bentuk murni.
16 BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini termasuk dalam penelitian non-eksperimental karena tidak ada intervensi atau perlakuan terhadap fenomena yang diamati.
B. Variabel dan Definisi Operasional 1. Variabel Penelitian
a. Variabel penelitian ini adalah kadar phlorotannin dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh.
b. Variabel pengacau terkendali dalam penelitian ini adalah volume cairan penyari untuk mengisolasi phlorotannin alga coklat Sargassum cymosum C. Agardh, tempat panen alga coklat di pantai Drini, waktu panen pada bulan Maret, komposisi reagen saat analisis.
c. Variabel pengacau tak terkendali dalam penelitian ini adalah umur alga coklat yang dipanen, suhu dan kelembaban ruangan saat percobaan.
2. Definisi Operasional
a. Simplisia alga coklat merupakan alga coklat Sargassum cymosum C. Agardh yang diambil dari Pantai Drini, Gunung Kidul, Yogyakarta dengan ciri thallus alga pendek berwarna coklat, daun panjang, dan bentuk kantung udara bergerigi .
17
b. Ekstrak metanol alga coklat Sargassum cymosum C. Agardh adalah hasil ekstraksi serbuk simplisia alga coklat Sargassum cymosum C. Agardh dengan metode soxhletasi menggunakan pelarut metanol sampai jernih selama 56 jam.
c. Fraksi etil asetat alga coklat Sargassum cymosum C. Agardh adalah fraksi yang diperoleh dengan cara fraksinasi dengan pelarut etil asetat dari ekstrak metanol simplisia alga coklat Sargassum cymosum C. Agardh. d. Kadar phlorotannin adalah jumlah polifenol total yang terhitung ekivalen
dengan phloroglucinol dalam fraksi etil asetat alga coklat Sargassum cymosum C. Agardh (mg PGE/g fraksi) yang ditetapkan secara spektrofotometri dengan metode kolorimetri Folin Ciocalteau.
C. Bahan atau Materi Penelitian
Bahan yang digunakan dalam penelitian adalah sebagai berikut:
1. simplisia alga coklat (Sargassum cymosum C. Agardh) dari pantai Drini, Gunung Kidul, Yogyakarta
2. metanol p.a (pro analisis) (Merck, Germany) 3. kloroform p.a. (Merck, Germany)
4. etil asetat p.a. (Merck, Germany) 5. aseton (Merck, Germany)
6. phloroglucinol (Merck, Germany) 7. Na-Karbonat (Merck, Germany)
8. reagen Folin Ciocalteau ( Sigma Chem, Co., USA.)
18
9. akuades (Fakultas Farmasi Universitas Sanata Dharma)
D. Alat Penelitian
Alat-alat yang digunakan dalam penelitian adalah sebagai berikut: 1. seperangkat spektrofotometer UV-VIS Perkin Elmer Lambda 20 2. timbangan elektrik BP 160 dan scaltec SBC 22 readability 0,01 mg 3. seperangkat alat titrasi Karl Fischer Mettler DL-18
3. vaccum rotary evaporator (Buchi) 4. waterbath (Abo-tech)
5. mikropipet 0,5-10 _l, 100-1000 _l. (Acura 825, Socorex) 6. tabung reaksi bertutup (Scott-Germany)
7. alat-alat untuk soxhletasi, yaitu soxhlet, kertas filter Schleicher & Schuell, labu alas bulat (Schott Duran,
Germany), heating mantle
8. alat sentrifus, homogenizer (Vortex Genie) 9. corong pisah 500 mL
10. alat-alat gelas yang lazim digunakan untuk penelitian di laboratorium analisis (PYREX-GERMANY)
E. Tata Cara Penelitian
1. Preparasi sampel alga coklat Sargassum cymosum C. Agardh.
Simplisia alga coklat Sargassum cymosum C. Agardh yang diperoleh dari petani dikumpulkan dan dicuci dengan air mengalir, kemudian diuapi dengan air
19
mendidih. Selanjutnya dikeringkan dengan oven pada suhu 90º C dan diserbuk. Penetapan kadar air serbuk alga dilakukan dengan menggunakan metode Karl Fischer. Serbuk alga ditimbang 0,2 gram, kemudian tambahkan 10 mL metanol, didiamkan selama 1 hari pada suhu kamar. Dilakukan pre-titrasi pada alat, lalu dilakukan uji kebocoran alat, hingga didapat angka drift 10-50 pada alat. Dilakukan standardisasi dengan cara menimbang spuit berisi air dan dimasukkan 1 tetes air ke dalam alat. Kemudian ditimbang kembali untuk menentukan berat air yang dimasukkan. Dihitung kesetaraan air. Dimasukkan 1 mL metano l dan dititrasi dengan alat (blanko). Kemudian 1 mL sampel dimasukkan, dititrasi dengan alat, dihitung kadar air dalam sampel dengan menggunakan rumus :
Kadar Air =
x = angka yang muncul pada alat(%) x 10.000 mg atau berat konversi.
2. Uji kualitatif senyawa fenolik a. Preparasi eksktrak
Tiga puluh mL metanol 80 % ditambahkan pada 10 g serbuk alga. Lalu diletakkan ke dalam wadah dan dipanaskan pada waterbath selama ± 1 jam. Dinginkan pada suhu ruang. Kemudian disaring menggunakan corong Buchner yang sesuai. Ditambahkan 5 mL metanol 80 % lagi dan disaring.
b. Uji polifenol dan tannin
Sejumlah volume yang setara dengan 10 g ekstrak metanol 80 % yang telah disiapkan sebelumnya pada langkah preparasi ekstrak, diuapkan
20
menggunakan waterbath. Ditambahkan 25 mL akuades panas, dicampur secara merata. Dibiarkan hingga dingin pada suhu kamar. Ditambahkan 3-4 tetes larutan NaCl 10 %. Kemudian ekstrak disaring dengan menggunakan vacuum. Filtrat dibagi ke dalam 4 tabung masing- masing 3 mL. Pada tabung I ditambahkan 4-5 tetes larutan gelatin 1 %. Pada tabung II ditambahkan 4-5 tetes pereaksi garam gelatin (gelatin 1% ditambahkan NaCl 10 %). Pada tabung III ditambahkan 3-4 tetes ferri klorida. Tabung IV dijadikan kontrol dan tidak ditambahkan pereaksi apapun. Diamati warna yang terbentuk pada setiap tabung.
3. Isolasi crude phlorotannin
Serbuk alga ditimbang sebanyak 80 g. Kemudian serbuk dimasukkan ke dalam kertas filter Schleicher & Schuell dan dimasukkan dalam labu soxhlet. Setelah itu diberi pelarut metanol sebanyak 2 kali sirkulasi. Proses soxhletasi dilakukan sampai tetesan pelarut jernih dengan suhu ± 120º C. Hasil soxhletasi diuapkan pelarutnya dengan menggunakan vacuum rotary evaporator sampai volume yang kecil (1/10 dari volume mula-mula). Selanjutnya ditambahkan 60 mL metanol, 120 mL kloroform, dan 45 mL air kemudian digojog dan didiamkan hingga membentuk dua lapisan. Dipisahkan antara lapisan atas dan lapisan bawah, selanjutnya lapisan atas diekstraksi dengan etil asetat dua kali masing-masing 75 mL. Fraksi etil asetat dikumpulkan, selanjutnya diuapkan, dan diperoleh ekstrak yang merupakan crude phlorotannin.
21
4. Optimasi metode kolorimetri dengan Folin Ciocalteau a. Pembuatan larutan standar
Standar (phloroglucinol) ditimbang seksama lebih kurang 0,05 g, kemudian dilarutkan dalam aseton 75% sampai volume 50,0 mL. Seri konsentrasi larutan intermediet dipipet dari larutan induk sebanyak 0,5; 1,0; 2,0; 3,0; 4;0; 5,0; dan 6,0 mL dan dimasukkan ke dalam labu ukur 10,0 mL dilarutkan dengan aseton 75%, sehingga konsentrasinya menjadi 0,5; 1,0; 2,0; 3,0; 4;0; 5,0; dan 6,0 ppm.
b. Penentuan operating time (OT)
Larutan intermediet 4,0 ppm dipipet sebanyak 0,5 mL dan dimasukkan ke dalam labu ukur 50,0 mL yang mengandung 2,5 mL pereaksi fenol Folin Ciocalteau yang telah diencerkan dengan akuades (1:1). Campuran didiamkan selama 2 menit lalu ditambahkan 7,5 mL Na2CO3 1,9 M, dan ditambah akuades sampai volume 50,0 mL. Absorbansi diukur setiap 2 menit pada panjang gelombang teoritis phloroglucinol (750 nm) selama 90 menit.
c. Penentuan panjang gelombang maksimum (? maks)
Larutan intermediet phloroglucinol dengan konsentrasi 1,0; 3,0; dan 6,0 ppm dipipet sebanyak 0,5 mL dan dimasukkan ke dalam labu takar 50,0 mL yang mengand ung 2,5 mL pereaksi fenol Folin Ciocalteau yang telah diencerkan dengan akuades (1:1). Campuran didiamkan selama 2 menit, lalu ditambah 7,5 mL Na2CO3 1,9 M, dan akuades sampai volume 50,0 mL. Campuran diinkubasi pada suhu ruang selama OT. Pada 15 menit pertama dan 15 menit kedua,
22
campuran divortex selama 30 detik, kemudian campuran hasil reaksi disentrifus dengan kecepatan 4000 rpm selama 5 menit. Supernatan diukur serapannya pada operating time pada rentang panjang gelombang 400 – 900 nm. Panjang gelombang maksimum ditentukan dari spektrogram yang didapatkan.
5. Penetapan kurva baku phloroglucinol
Larutan intermediet dipipet masing-masing sebanyak 0,5 mL dan dimasukkan
ke dalam labu ukur 50,0 mL yang mengandung 2,5 mL pereaksi fenol
Folin-Ciocalteau yang diencerkan (1:1), biarkan selama 2 menit. Selanjutnya ditambahkan
7,5 mL Na2CO3 1,9 M dan dicampur dengan akuades sampai 50,0 mL. Campuran
divortex setiap 15 menit, selama 30 detik, sebanyak 2 kali vortex. Kemudian
disentrifus selama 5 menit dengan kecepatan 4000 rpm dan diambil supernatannya.
Absorbansi diukur pada panjang gelombang maksimum hasil scanning (750,1 nm). Replikasi dilakukan sebanyak tiga kali. Dihitung data yang didapat dengan program regresi linier sehingga didapatkan persamaan kurva baku.
6. Estimasi kadar polifenol total pada sampel fraksi etil asetat alga coklat
Sargassum cymosum C. Agardh
Lebih kurang 0,05 g fraksi etil asetat alga coklat Sargassum cymosum C. Agardh ditimbang dengan seksama, kemudian dilarutkan dalam aseton 75% hingga volumenya 50,0 mL. Diambil 10,0 mL larutan sampel alga coklat dan dimasukkan ke dalam labu takar 50,0 mL yang mengandung 2,5 mL pereaksi fenol Folin Ciocalteau yang telah diencerkan dengan akuades 1:1. Campuran didiamkan selama 2 menit kemudian ditambahkan 7,5 mL Na2CO3 1,9 M dan
23
akuades sampai volume 50,0 mL. Campuran tersebut diinkubasi pada temperatur ruang selama OT untuk menyempurnakan reaksi sampai terbentuk warna biru (pada 15 menit pertama dan 15 menit kedua, campuran tersebut divortex selama 30 detik). Kemudian, campuran reaksi disentrifus dengan kecepatan 4000 rpm selama 5 menit dan diukur absorbansinya pada panjang gelombang maksimum menggunakan spektrofotometer visibel. Absorbansi dimasukkan ke persamaan kurva baku. Konsentrasi polifenol total dihitung ekivalen dengan phloroglucinol (mg PGE / g fraksi).
24 BAB IV
HASIL DAN PEMBAHASAN
A. Preparasi Sampel Alga Coklat Sargassum cymosum C. Agardh Pengambilan simplisia dilakukan di Pantai Drini, Gunung Kidul, Yogyakarta. Simplisia alga coklat Sargassum cymosum C. Agardh diperoleh dari petani alga pada tanggal 23 Maret 2007 pada pukul 16.00 – 17.00 WIB. Menurut petani, saat pengambilan simplisia temperatur air sekitar 27º-30º C, cuaca mendung dan gerimis. Hal tersebut perlu diketahui sebab menurut Yates dan Peckol (1993) parameter lingkungan seperti salinitas, ketersediaan nutrisi dan cahaya, irradiasi UV, dan intensitas herbivora dapat mempengaruhi kadar phlorotannin (cit., Koivikko, 2005).
Selanjutnya simplisia alga coklat yang didapat diidentifikasi dengan bantuan dari Laboratorium Sistematika Tumbuhan (Fakultas Biologi UGM, Yogyakarta). Dengan kesimpulan bahwa simplisia alga coklat termasuk dalam ordo Fucales, familia Sargassaceae, genus Sargassum, spesies Sargassum cymosum C. Agardh. (lihat lampiran 1).
Simplisia Alga coklat Sargassum cymosum C. Agardh dicuci dengan air mengalir untuk menghilangkan pengotor-pengotor yang berupa epifit, pasir (silikat), dan benda-benda asing yang ikut terbawa saat proses pengambilan simplisia. Pengotor-pengotor harus dihilangkan sebab dapat mengganggu hasil analisis. Senyawa silikat dapat membentuk kompleks molibdat yang berupa H6[SiMo12O40].n H2O dari reagen Folin Ciocalteau dalam suasana asam sehingga
25
bila tidak dihilangkan akan mengganggu dalam analisis sampel (Auterhoff dan Knabe, 1978).
Alga coklat Sargassum tumbuh dalam habitat laut yang terdiri dari bermacam- macam species alga. Maka perlu dilakukan sortasi untuk memisahkan spesies alga coklat Sargassum cymosum C. Agardh dari species alga coklat Sargassum yang lain. Pemisahan dilakukan dengan melihat ciri-ciri fisik dari alga coklat Sargassum cymocum C. Agardh yaitu thallus pendek berwarna coklat, daun panjang dan bentuk kantung udara yang bergerigi. Sortasi dilanjutkan dengan membuang bagian akar dengan bantuan pisau atau gunting. Hal ini untuk menghilangkan materi asing berupa karang yang masih melekat pada akar tumbuhan alga. Saat sortasi juga ditemukan senyawa kalsium berupa butiran kapur berwarna putih yang merupakan hasil kalsifikasi tumbuhan alga. Akan tetapi Ca bukanlah reduktor sehingga tidak dapat mereduksi reagen Folin Ciocalteau, dan kalsium disini tidak akan mengganggu proses analisis.
Setelah simplisia yang dikumpulkan benar-benar merupakan alga coklat Sargassum cymosum C. Agardh, maka selanjutnya simplisia diproses dalam autoklaf pada suhu 100º C selama 30 menit untuk menginaktivasi enzim polimerase yaitu Polyphenol Oxydase (PPO). Menurut Mustapha dan Ghalem (2007), enzim PPO dapat menjadi inaktif dengan direbus dalam air panas pada 100º C selama 1,5 menit.
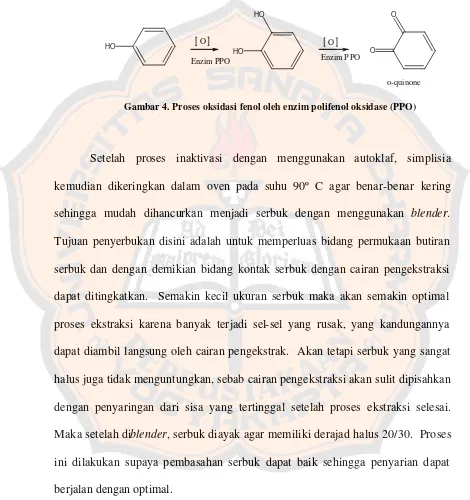
Enzim PPO mengkatalisis hidroksilasi monofenol menjadi o-difenol, yang selanjutnya dapat mengkatalisis oksidasi o-difenol menjadi o-kuinon. Polimerasi o-kuinon menghasilkan pigmen berupa senyawa polifenol. Jika enzim PPO
26
inaktif maka proses polimerasi fenol akan terhenti dan tidak akan terbentuk polimer polifenol yang lebih panjang. Proses oksidasi fenol oleh enzim PPO dapat digambarkan sebagai berikut:
HO
Gambar 4. Proses oksidasi fenol oleh enzim polifenol oksidase (PPO)
Setelah proses inaktivasi dengan menggunakan autoklaf, simplisia kemudian dikeringkan dalam oven pada suhu 90º C agar benar-benar kering sehingga mudah dihancurkan menjadi serbuk dengan menggunakan blender. Tujuan penyerbukan disini adalah untuk memperluas bidang permukaan butiran serbuk dan denga n demikian bidang kontak serbuk dengan cairan pengekstraksi dapat ditingkatkan. Semakin kecil ukuran serbuk maka akan semakin optimal proses ekstraksi karena banyak terjadi sel-sel yang rusak, yang kandungannya dapat diambil langsung oleh cairan pengekstrak. Akan tetapi serbuk yang sangat halus juga tidak menguntungkan, sebab cairan pengekstraksi akan sulit dipisahkan dengan penyaringan dari sisa yang tertinggal setelah proses ekstraksi selesai. Maka setelah diblender, serbuk diayak agar memiliki derajad halus 20/30. Proses ini dilakukan supaya pembasahan serbuk dapat baik sehingga penyarian dapat berjalan dengan optimal.
Selanjutnya serbuk di tetapkan kadar airnya dengan metode Karl Fischer. Kadar air harus di kontrol di bawah 10% sebagaimana disebutkan dalam Materia
27
Medika Indonesia (MMI) untuk simplisia tanaman pada umumnya. Hal ini karena kandungan air memungkinkan terjadinya kontaminasi mikrobial. Selain itu reaksi hidrolitik oleh air dapat pula mengakibatkan cepatnya perusakan bahan aktif. Prinsip penetapan kadar air dengan metode Karl Fischer adalah reaksi kuantitatif antara larutan anhidrat belerang dioksida dengan iodium dengan adanya dapar yang bereaksi dengan ion hidrogen. Reaksi ini merupakan reaksi redoks dimana iod akan mereduksi garam dioksida dan iod sendiri mengalami oksidasi. Kelebihan metode Karl Fischer adalah spesifik mengukur kadar air dalam sampel, jumlah sampel yang digunakan untuk analisis relatif sedikit, dan hasilnya akurat.
H2O + I2 + SO2 2HI + SO3 (3)
Gambar 5. Reaksi penetapan kadar air dengan Karl Fischer (Evans, 2002)
Kadar air yang terukur dari serbuk alga dengan 3 kali replikasi sebesar 3,7%; 3,5%; dan 2,7%. Sehingga hasil penetapan kadar airnya adalah 3,3 ± 0,5 % dan memenuhi syarat untuk simplisia kering menurut MMI.
28
B. Uji Kualitatif Senyawa Fenolik
Salah satu kandungan mikronutrien dari tumbuhan alga coklat adalah polifenol yang dikenal sebagai phlorotannin yang berbeda dari polifenol pada tumbuhan terestrial (Burtin, 2003)
Tujuan dilakukannya uji polifenol adalah untuk memperkuat bukti adanya kandungan polifenol dalam alga coklat Sargassum cymosum C. Agardh. Adanya polifenol ditunjukkan dengan warna hijau-biru yang terjadi pada filtrat alga setelah ditetesi pereaksi FeCl3.
Hasil pengamatan sampel serbuk alga coklat Sargassum cymosum C. Agardh menunjukkan hasil positif mengandung senyawa polifenol. Sebelum penambahan FeCl3 filtrat ekstrak alga coklat berwarna kuning pucat. Warna biru yang terjadi setelah penambahan FeCl3 dikarenakan terbentuknya kompleks ion Fe3+ dengan gugus- gugus fenol. Hasil uji polifenol ditunjukkan pada tabel I berikut:
Tabel I. Hasil uji kandungan senyawa polifenol serbuk alga Sargassum cymosum C.
Agardh
Warna sebelum reaksi Warna sesudah reaksi
Kuning pucat biru gelap di bagian tengah (+)
29
Gambar 6. Reaksi pembentukan kompleks gugus fenolik dan FeCl3
Adanya senyawa fenol berupa tannin juga ditunjukkan dengan terbentuknya endapan setelah penambahan gelatin maupun setelah penambahan gelatin dan NaCl. Penambahan NaCl dapat meningkatkan kepekaan reaksi sehingga akan dihasilkan endapan dalam jumlah lebih banyak dibandingkan dengan penambahan gelatin saja. Endapan terjadi karena kemampuan tannin menyamak kulit. Selain itu tanin memiliki afinitas yang kuat terhadap gelatin sehingga gelatin mengalami presipitasi. Ikatan yang terjadi antara tannin dan gelatin merupakan ikatan hidrogen dan terdapat interaksi hidrofobik sehingga endapan yang terbentuk bersifat reversible.
C. Isolasi CrudePhlorotannin
Serbuk alga ditimbang lebih kurang 80 g kemudian diekstraksi dengan metode soxhletasi dengan cairan penyari metanol. Dipilih metode soxhletasi untuk efisiensi penyari dan phlorotannin masih dapat dipertahankan hingga suhu 170°C dilihat dari sifat fisika-kimia monomernya yaitu phloroglucinol. Metanol
30
digunakan untuk menarik senyawa-senyawa yang bersifat polar. Metanol memiliki gugus hidroksil sehingga mampu membentuk ikatan hidrogen intramolekular dengan gugus hidroksil pada senyawa fenolik sehingga polifenol cenderung larut dalam metanol. Ekstraksi dihentikan sampai cairan penyari benar-benar jernih untuk memastikan semua senyawa polar telah larut dalam metanol. Akan tetapi hal tersebut tidak menjamin bahwa seluruh kandungan phlorotannin telah larut dalam metanol dengan sempurna. Untuk itu sebenarnya perlu dilakukan optimasi terhadap lama waktu soxhletasi. Namun dalam penelitian ini hal tersebut tidak dilakukan dan soxhletasi berlangsung selama 56 jam. Kemudian hasil soxhletasi diuapkan pelarutnya menggunakan vacuum rotary evaporator agar diperoleh ekstrak kental.
Selanjutnya dilakukan fraksinasi terhadap ekstrak metanol kental dengan menggunakan pelarut kloroform dan air sehingga terjadi pemisahan menjadi 2 lapisan. Hal ini dikarenakan adanya perbedaan berat molekul (BM) dimana fraksi metanol-air lebih ringan daripada fraksi kloroform. Kloroform merupakan pelarut yang cenderung non polar dibanding dengan metanol-air, sehingga memiliki kecenderungan menarik kandungan non polar seperti lipid (Padda, 2006). Sedangkan metanol-air cenderung menarik kandungan polar karena sifatnya yang lebih polar dibandingkan kloroform.
Lapisan bawah (fraksi kloroform) dibuang dan lapisan atas (fraksi metanol-air) difraksinasi kembali dengan etil asetat sebanyak 2 kali. Fraksinasi dilakukan secara berulang dengan jumlah pelarut sedikit dimaksudkan untuk mengefektifkan permurnian artinya senyawa yang diinginkan akan didapatkan
31
dalam jumlah yang lebih banyak. Fraksi etil asetat dikumpulkan dan diuapkan pelarutnya untuk selanjutnya ditetapkan kadarnya secara kolorimetri dengan reagen Folin Ciocalteau.
D. Optimasi Metode Kolorimetri dengan Reagen Folin Ciocalteau 1. Pembuatan larutan standar phloroglucinol
Standar yang digunakan adalah phloroglucinol yang merupakan monomer dari phlorotannin. Standar phloroglucinol dilarutkan dalam aseton 75 %. Tidak digunakan pelarut metanol karena masih memiliki gugus hidroksil yang dapat mereduksi kompleks asam dalam reagen Folin Ciocalteau sehingga meningkatkan resiko kesalahan saat pembacaan absorbansi. Untuk itu diganti menggunakan pelarut aseton 75% untuk menghilangkan intervensi absorbansi warna dari pelarut metanol. Selanjutnya larutan direaksikan dengan reagen Folin Ciocalteau, dibiarkan selama 2 menit, lalu ditambahkan Na2CO3 1,9 M untuk memberikan suasana basa. Setelah penambahan basa larutan menjadi berwarna biru. Kemudian campuran divortex agar homogen dan disentrifus dengan kecepatan 4000 rpm selama 5 menit untuk mengendapkan senyawa-senyawa yang tidak larut dalam aseton maupun air. Supernatan yang berupa larutan jernih hasil sentrifugasi berwarna biru sedangkan endapan berwarna putih. Supernatan tersebut yang kemudian dibaca absorbansinya menggunakan spektrofotometer visibel.
32
2. Penentuan operating time (OT)
Operating time merupakan tahap pertama yang harus dilakukan dalam optimasi metode kolorimetri. Penentuan OT bertujuan untuk mengetahui waktu pengukuran dimana pada rentang waktu tersebut senyawa memberikan serapan yang stabil. Hal itu berarti semua senyawa fenolat telah mereduksi reagen Folin Ciocalteau dengan sempurna.
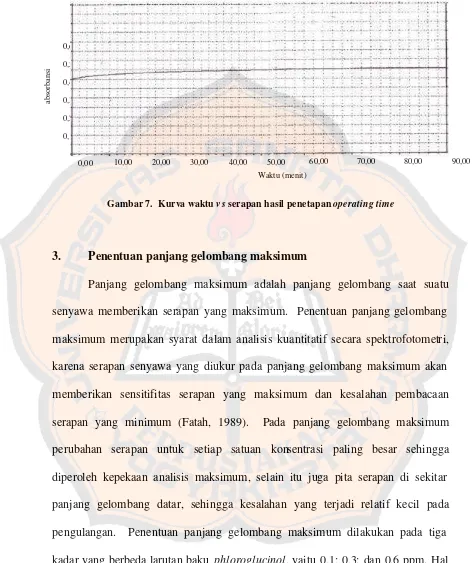
Pada penelitian ini pengukuran OT dilakukan setelah penambahan Na2CO3 atau sejak terbentuknya warna. Pengukuran operating time kompleks molybdenum blue dihasilkan dari larutan baku phloroglucinol dengan konsentrasi 4,0 ppm dilakukan pada panjang gelombang teoritis yaitu 750 nm. Hasil penetapan operating time berupa kurva hubungan serapan vs waktu menunjukkan serapan stabil pada menit ke 50 hingga menit ke 90 dengan absorbansi 0,454. Pengukuran serapan untuk kurva baku dan sampel dilakukan menit ke-60 agar semua pengukuran dilakukan pada rentang waktu operasi yang sama sehingga semua mendapat perlakuan yang sama. Berikut ini adalah hasil pengukuran operating time yang disajikan dalam bentuk kurva waktu vs serapan :
33
Gambar 7. Kurva waktu vs serapan hasil penetapan operating time
3. Penentuan panjang gelombang maksimum
Panjang gelombang maksimum adalah panjang gelombang saat suatu senyawa memberikan serapan yang maksimum. Penentuan panjang gelombang maksimum merupakan syarat dalam analisis kuantitatif secara spektrofotometri, karena serapan senyawa yang diukur pada panjang gelombang maksimum akan memberikan sensitifitas serapan yang maksimum dan kesalahan pembacaan serapan yang minimum (Fatah, 1989). Pada panjang gelombang maksimum perubahan serapan untuk setiap satuan konsentrasi paling besar sehingga diperoleh kepekaan analisis maksimum, selain itu juga pita serapan di sekitar panjang gelombang datar, sehingga kesalahan yang terjadi relatif kecil pada pengulangan. Penentuan panjang gelombang maksimum dilakukan pada tiga kadar yang berbeda larutan baku phloroglucinol, yaitu 0,1; 0,3; dan 0,6 ppm. Hal ini dilakukan agar didapat hasil yang meyakinkan bahwa pada panjang gelombang tersebut memang terjadi serapan yang maksimum. Warna kompleks molybdenum
34
blue berada di daerah panjang gelombang cahaya tampak, sehingga pengukuran panjang gelombang maksimum dilakukan dalam rentang 400 nm sampai 900 nm karena daerah cahaya tampak terletak antara 380 nm sampai 780 nm. Berikut hasil pengukuran panjang gelombang serapan maksimum:
λ (wavelength)
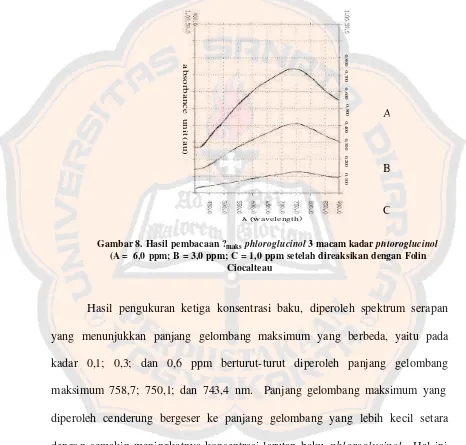
Gambar 8. Hasil pembacaan ?maksphloroglucinol 3 macam kadar phloroglucinol
(A = 6,0 ppm; B = 3,0 ppm; C = 1,0 ppm setelah direaksikan dengan Folin Ciocalteau
Hasil pengukuran ketiga konsentrasi baku, diperoleh spektrum serapan yang menunjukkan panjang gelombang maksimum yang berbeda, yaitu pada kadar 0,1; 0,3; dan 0,6 ppm berturut-turut diperoleh panjang gelombang maksimum 758,7; 750,1; dan 743,4 nm. Panjang gelombang maksimum yang diperoleh cenderung bergeser ke panjang gelombang yang lebih kecil setara denga n semakin meningkatnya konsentrasi larutan baku phloroglucinol. Hal ini mungkin dikarenakan adanya ionisasi fenolik menjadi ion fenolat yang dapat mengabsorbsi cahaya pada tingkat energi lebih kecil sehingga panjang gelombang menjadi lebih besar. Akan tetapi pada pembacaan absorbansi standar
A
B
C
35
phloroglucinol pada ketiga panjang gelombang tersebut diperoleh hasil pembacaan absorbansi yang tidak berbeda jauh. Perbedaan panjang gelombang maksimum ini dapat juga dikarenakan tidak terkontrolnya pH larutan sehingga terjadi dua bentuk reduksi dari reagen Folin Ciocalteau. Senyawa kompleks molybdenum blue yang terukur bukan merupakan satu bentuk senyawa namun berupa campuran dari dua bentuk senyawa molydenum blue dengan rumus struktur yang berbeda.
Menurut penelitian Zhang et al. (2006) tentang estimasi kandungan polifenol total berdasarkan reaksi Folin Ciocalteau, panjang gelombang maksimum untuk sampel A. nodosum dan standar phloroglucinol adalah 750 nm. Sehingga dipilih panjang gelombang 750,1 nm untuk pengukuran sampel dan baku karena mendekati panjang gelombang teoritis.
E. Penetapan Kurva Baku Phloroglucinol
Pembuatan kurva baku bertujuan mendapatkan persamaan garis regresi linier yang digunakan menghitung kadar phlorotannin dalam sampel. Pembuatan kurva baku digunakan 6 seri larutan phloroglucinol dengan konsentrasi yang berbeda yakni 0,1024; 0,2048; 0,3071; 0,4095; 0,5119; dan 0,6143 mg/100mL. Kemudian, seri kadar larutan baku phloroglucinol diukur serapannya pada panjang gelombang maksimum 750,1 nm dan selanjutnya dibuat kurva hubungan antara kadar dengan serapan. Replikasi kurva baku dilakukan tiga kali. Hasil pengukuran serapan larutan phloroglucinol untuk pembuatan kurva baku disajikan pada tabel di bawah ini.
36
Tabel II. Data untuk persamaan kurva baku
Replikasi I Replikasi II Replikasi III
Seri
Koefisien korelasi menunjukkan hubungan antara konsentrasi dengan serapan. Nilai koefisien korelasi mendekati satu artinya hubungan antara kadar dan serapan mendekati linier dan sesuai hukum Lambert-Beer. Berdasarkan nilai r hitung yang diperoleh, ketiga kurva baku tersebut kemudian dibandingkan nilai r tabel (pada taraf kepercayaan 95%, df 4) diperoleh nilai r hitung ketiga kurva baku lebih besar dari r tabel yakni 0,811. Intersep dari persamaan garis regresi linier hasil replikasi I kecil yakni 0,0082. Hal ini berarti ada korelasi yang baik antara konsentrasi dengan serapan, dan korelasi terbaik dihasilkan oleh kurva baku replikasi I yang dibuktikan dengan nilai r hitung kurva baku replikasi I > r hitung kurva baku replikasi III > r hitung kurva baku replikasi II. Maka dari ketiga persamaan kurva baku tersebut dipilih kurva baku I untuk menetapkan kadar sampel. Persamaan kurva baku yang digunakan adalah Y = 1,2665 X + 0,0082.
37
Hubungan antara kadar phloroglucinol dan nilai absorbansi dari persamaan baku yang dipilih (replikasi I) disajikan pada gambar 9 di bawah ini:
Gambar 9. Kurva baku hubungan kadar dan absorbansi phloroglucinol
F. Penetapan Kadar Phlorotannin Fraksi Etil Asetat Alga Coklat
Sargassum cymosum C. Agardh
Prosedur dimulai dengan melarutkan crude phlorotannin dari fraksi etil asetat dengan aseton 75%. Phlorotannin merupakan suatu polifenol dan komponen fenolik biasanya lebih larut dalam pelarut yang kurang polar dibanding air. Biasanya digunakan campuran air dengan metanol, etanol, atau aseton (Waterman dan Mole, 1994). Tidak digunakan pelarut metanol karena masih memiliki gugus hidroksil yang dapat mereduksi kompleks asam dalam reagen Folin Ciocalteau sehingga meningkatkan resiko kesalahan saat pembacaan absorbansi. Untuk itu diganti menggunakan pelarut aseton 75% untuk
Kurva Baku
0.0000 0.1000 0.2000 0.3000 0.4000 0.5000 0.6000 0.7000
Konsentrasi (ppm)
Absorbansi
y = 1,2665 x + 0,0082
38
menghilangkan intervensi absorbansi warna dari pelarut metanol dan perlu dibuat blanko sebagai faktor koreksi. Tujuan dari pembuatan blanko agar serapan yang diinginkan saja yang terukur. Serapan yang ingin diukur yakni serapan komp leks molybdenum blue. Fraksi etil asetat yang telah larut dalam aseton 75% kemudian direaksikan seperti pada standar phloroglucinol dan diukur absorbansinya pada panjang gelombang 750,1 nm.
Senyawa fenolik merupakan asam lemah yang dalam keadaan netral mudah melepaskan ion H+ dan akan berada dalam kesetimbangan dengan ion fenolat. Penambahan Na2CO3 akan memberikan suasana basa sehingga kesetimbangan akan lebih bergeser ke arah terbentuknya ion fenolat. Kemudian ion fenolat inilah yang akan mereduksi kompleks asam heteropoli dari fosfotungstat dan fosfomolibdat membentuk senyawa molybdenum blue. Ketika ion fenolat bereaksi dengan reagen Folin Ciocalteau, maka jumlah ion fenolat akan berkurang dan kesetimbangan akan bergeser ke arah terbentuknya ion fenolat sehingga akan lebih banyak lagi ion fenolat yang dihasilkan. Reaksi ini akan berlangsung hingga semua fenol habis. Selama reaksi terjadi, reagen Folin Ciocalteau harus tetap bertahan dalam kondisi basa. Digunakan Na2CO3 untuk mempertahankan supaya kebasaan berada pada pH sedang (pH 9 – 10).
OH
Gambar 10. Kesetimbangan reaksi phloroglucinol dalam suasana basa
39
Prinsip reaksi kolorimetri dengan reagen Folin Ciocalteau adalah reduksi reagen Folin Ciocalteau oleh ion fenolat membentuk kompleks molybdenum blue dan oksidasi ion fenolat menjadi senyawa kuinon oleh reagen Folin Ciocalteau. Reaksi oksidasi senyawa fenol:
phloroglucinol
Reaksi reduksi reagen Folin Ciocalteau:
H3PO4(MoO3)12 + 2e- + 2H+ H5(PMo12O40)
Gambar 11. Reaksi phloroglucinol dengan reagen Folin Ciocalteau
40
Pada saat reaksi terjadi, reagen Folin Ciocalteau mengalami reduksi karena mendapatkan proton (H+) dari gugus fenol sampel membentuk kompleks oktahedral molybdenum blue. Sementara itu gugus fenol akan mendapatkan tambahan oksigen dari air dan reagen (teroksidasi) sehingga membentuk senyawa kuinon. Semakin banyak senyawa fenolik maka akan semakin banyak ion fenolat yang terbentuk dan komp leks ion polimerik dari reagen Folin Ciocalteau akan semakin tereduksi menghasilkan senyawa molybdenum blue yang semakin pekat. Sehingga warna yang dihasilkan setara dengan konsentrasi ion fenolat dan kandungan senyawa fenolik dalam sampel yang dapat diuk ur serapannya menggunakan spektrofotometer.
Tabel III. Hasil pembacaan absorbansi fraksi etil asetat alga coklat Sargassum cymosum C.
Agardh
Panjang Gelombang 750,1 nm Absorbansi
Replikasi I 1 0,172
Data serapan yang diperoleh kemudian diolah dengan menggunakan persamaan kurva baku I, yaitu Y = 1,2665 X + 0,0082 sehingga diperoleh kadar terukur phlorotannin. Pengukuran serapan dilakukan dengan 3 replikasi dan masing- masing replikasi dianalisis dengan duplo seperti yang disajikan pada tabel IV.