PENGARUH KONSENTRASI TWEEN 80 SEBAGAI PENETRATION ENHANCER PADA FORMULASI MIKROEMULSI EKSTRAK TEMPE
DENGAN METODE FRANZ DIFFUSION CELL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Chrisilia Cahyani
NIM : 108114136
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH KONSENTRASI TWEEN 80 SEBAGAI PENETRATION ENHANCER PADA FORMULASI MIKROEMULSI EKSTRAK TEMPE
DENGAN METODE FRANZ DIFFUSION CELL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Chrisilia Cahyani
NIM : 108114136
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Aku bersyukur kepada-Mu, sebab Engkau telah menjawab aku dan telah menjadi
keselamatanku (Mazmur 118:21)
Serahkanlah segala kekuatiranmu kepada-Nya, sebab Ia yang memelihara kamu
( 1 Petrus 5 :7)
Sebab segala sesuatu adalah dari Dia, dan oleh Dia, dan kepada Dia : Bagi Dialah
kemuliaan sampai selama-lamanya! ( Roma 11:36)
Kupersembahkan untuk :
Tuhan Yesus, Papa, Mama , Mbak Tika, Dek Putri,
Sahabat-sahabatku,
v
PRAKATA
Puji syukur kepada Tuhan Yesus atas berkat dan kasih karunia-Nya yang
melimpah sehingga penulis dapat menyelesaikan penelitan serta penyusunan skripsi
yang berjudul “Pengaruh Konsentrasi Tween 80 Sebagai Penetration Enhancer
Pada Formulasi Mikroemulsi Ekstrak Tempe Dengan Metode Franz Diffusion Cell
“ yang disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
(S.Farm.) Progam Studi Farmasi, Universitas Sanata Dharma , Yogyakarta.Dalam
pelaksanan penelitian, penyusunan skripsi hingga penyelesaian skripsi ini, penulis
mendapatkan bantuan dan dukungan dari banyak pihak, skripsi ini dapat
diseleseikan dengan baik, untuk itu penuli ingin mengucapkan terima kasih kepada
1. Fx. Sutopo Broto dan Juli Indrajani, Attrika Windaresti Cahyani dan Maria
Florence Cahya Putri atas dukungan dan semangat kepada penulis selama
proses penelitian hingga penyusunan naskah skripsi.
2. Aris Widayati,M.Si.,Ph.D, Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta
3. Dr. Sri Hartati Yuliani, M.Sc., Apt., selaku dosen pembimbing dan Kepala
laboratorium, atas masukan, bimbingan, kritik, saran, dan bahan penelitian
yang diberikan kepada penulis.
4. C. M. Ratna Rini Nastiti, M. Pharm., Apt. selaku dosen penguji dan juga
atas saran serta dukungan yang membangun.
5. Yohanes Dwiatmaka, M.Si. selaku dosen penguji dan juga atas saran serta
vi
6. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma
yang telah membagikan ilmu serta pengalaman selama perkuliahan.
7. Djanuar Davidzon Pah yang selalu setia memberi perhatian, kritik maupun
saran serta dukungan dan semangat kepada penulis selama proses
penelitian hingga penyusunan naskah skripsi.
8. Pak Wagiran, Pak Musrifin, Pak Heru, Pak Parlan, Mas Bimo, Mas Kunto,
Mas Agung, serta laboran lain atas segala bantuan yang telah diberikan
kepada penulis.
9. Kelvin, Bakti, Eliza, Nessya, Sefi, Cindy, Tere, Jessi, Mega, teman-teman
satu kelompok praktikum dan kelompok presentasi, teman-teman FSM C
2010, FST B 2010 dan seluruh angkatan 2010 atas kebersamaan yang indah
dan keceriaannya selama ini.
10.Serta semua pihak yang telah membantu penulis dan tidak dapat disebutkan
satu per satu.
Tidak ada hal yang sempurna di dalam hidup ini maka dari itu penulis
menyadari masih terdapat kekurangan dalam penulisan skripsi ini. Penulis
mengharapkan kritik dan saran dari pembaca yang membangun dan menjadi
pembelajaran bagi penulis untuk menjadi lebih baik. Penulis berharap skripsi ini
dapat bermanfaat dan menjadi sumbangan bagi ilmu pengetahuan.
Yogyakarta, 3 Juni 2014
x
B. Aging ...
C. Isoflavon dan Tempe ...
D. Enhancer ...
E. Mikroemulsi...
F. Absorpsi Perkutan...
G. Kromatografi Cair Kinerja Tinggi...
H. Virgin Coconut Oil...
BAB III METODOLOGI PENELITIAN...
A. Jenis dan Rancangan Penelitian...
B. Variabel Penelitian...
2. Standarisasi Ekstrak Tempe ...
xi
a. Pembuatan fase gerak...
b. Pembuatan larutan baku genistein...
c. Penetapan panjang gelombang maksimum...
d. Penetapan kurva ekstrak tempe ...
3. Orientasi dan Formulasi Mikroemulsi ...
a. Formula...
b. Pembuatan Mikroemulsi Ekstrak Tempe ...
4. Uji Stabilitas Fisik...
a. Uji Organoleptis dan pH...
b. Uji Viskositas...
c. Uji Pengukuran Droplet Size...
d. Cycling test...
5. Uji Permeasi Franz Diffusion Cell...
a. Pembuatan PBS pH 7,4 konsentrasi 0,15 M ( sebagai
medium kompartemen aseptor)...
b. Pembuatan NaCl 9 % Fisiologis...
c. Preparasi sel difusi dengan membran kulit mencit...
d. Uji in-vitro dengan menggunakan Franz-cell
modifikasi...
6. Analisis statistik nilai fluks genistein yang
terpenetrasi...
BAB IV HASIL DAN PEMBAHASAN...
xii
B. Standarisasi Ekstrak Tempe...
1. Pembuatan Fase Gerak...
2. Pembuatan Kurva Baku...
3. Penetapan Panjang Gelombang Maksimum Genistein...
4. Penetapan Kadar dengan High Perfomance Liquid
Chromatograpy (HPLC)...
a. Analisis Kualitatif...
b. Analisis Kuantitatif...
C. Orientasi dan Formulasi Komposisi Mikroemulsi Ekstrak
Tempe...
D. Uji Sifat Fisik dan Stabilitas Fisik Mikroemulsi...
1. Uji Organoleptis dan pH...
2. Uji Viskositas...
3. Uji Pengukuran Droplet Mikroemulsi......
4. Cycling Test...
E. Uji Penetrasi Genistein dengan Franz Diffusion Cell Modifikasi..
BAB V KESIMPULAN DAN SARAN...
xiii
Fase Diam pada Sistem Kromatografi...
Fase Gerak pada Sistem Kromatografi...
Komponen VCO...
Formula Mikroemulsi Ekstrak Tempe...
Data Kurva Baku Genistein...
Kadar Genistein Dalam Ekstrak Etanolik Tempe Yang
Sudah Mengalami Fraksinasi Bertingkat...
Data Uji Sifat Fisik dan Stabilitas Mikroemulsi Ekstrak
Tempe Formula I hingga Formula III...
Nilai Fluks, Koefisien Difusifitas Dan Jumlah Kumulatif
Genistein Dari Sediaan Mikroemulsi Yang Mengandung
xiv
Jalur Umum Senyawa Dalam Menembus Kulit ...
Struktur Isoflavon Aglikon...
Grafik Hubungan antara Profil Jumlah Kumulatif Genistein
yang terpenetrasi dari Formula I – III... Grafik hubungan Fluks rata-rata Genistein yang
xv
Skema Pembuatan Seri Larutan Baku...
Perhitungan Seri Baku Kadar Genistein...
Fraksinasi Genistein Dari Tempe...
Data Kromatogram Standarisasi Genistein Dari
Tempe...
Contoh Perhitungan Jumlah Genistein yang Terpenetrasi
Dari Sediaan Mikroemulsi Pada Menit ke-60...
Contoh Perhitungan Jumlah Genistein yang Terpenetrasi
Dari Sediaan Mikroemulsi Pada Menit ke-120...
Contoh Perhitungan Fluks Tiap Waktu Genistein dari
xvi
INTISARI
Fenomena aging atau penuaan dini tidak dapat terhindarkan. Salah satu penyebab aging adalah terpaparnya kulit oleh sinar ultraviolet (UV). Genistein merupakan senyawa yang dapat mencegah penuaan dini dengan mekanisme antioksidan. Genistein adalah isoflavon dalam bentuk aglikon dimana bentuk aglikon ini dapat dijumpai di produk fermentasi kedelai yakni tempe. Genistein memiliki kelarutan yang rendah dalam minyak. Sediaan mikroemulsi untuk penggunaan topikal dapat meningkatkan kelarutan genistein sehingga dapat terabsorpsi ke dalam kulit dengan baik. Penelitian ini bertujuan untuk formulasi mikroemulsi dari ekstrak tempe dan melihat pengaruh konsentrasi tween 80 sebagai
penetration enhancer dengan metode Franz Diffusion Cell.
Uji difusi dilakukan dengan membandingkan 3 formula dimana Formula I memiliki konsentrasi tween 80 : PEG 400 (1:1), Formula II memiliki konsentrasi tween 80 : PEG 400 (2:1), Formula III memiliki konsentrasi tween 80 : PEG 400 (3:1). Uji difusi menggunakan Franz Diffusion Cell, kadar kemudian diukur menggunakan HPLC. Kadar genistein yang terpenetrasi tiap jam dinyatakan sebagai nilai fluks. Nilai-nilai fluks tiap formula diuji statistik menggunakan
ANOVA. Hasil dari uji absorpsi perkutan menunjukkan tidak ada perbedaan antar formula.
xvii
ABSTRACT
The aging phenomenon can not be avoided. Skin aging is caused by exposured to ultraviolet light (UV). Genistein is a compound that can prevent aging by antioxidant mechanisms. Genistein which is in the aglycone form can be found in fermented soy product like tempeh. Genistein has a low solubility in oil. Microemulsion for topical use can increase the solubility of genistein that can be well absorbed into the stratum corneum. This study aimed to formulate microemulsion of tempeh extract and analyze the effect of tween 80 concentration as penetration enhancers by Franz Diffusion Cell.
There were three formulas which were used in diffusion test ; 1st Formula was consist of tween 80 : PEG 400 (1:1), 2nd Formula was consist of tween 80 : PEG 400 tween 80 : PEG 400 (2:1), 3rd Formula was consist of tween 80 : PEG 400 (3:1). The percutaneuous absorption test using Franz Diffusion Cell , the genistein level that permeate into the stratum corneum was measured using HPLC. The penetrated-genistein solute level was considered as flux time. Flux time values were statistically tested using ANOVA. The percutaneuos absorption test results showed there are no differences in each formula.
1
BAB I PENGANTAR
A. Latar Belakang
Aging didefinisikan sebagai suatu penurunan fungsi biologik pada
organisme. Aging tidak terhindarkan dan berjalan dengan kecepatan yang berbeda,
tergantung dari susunan genetik, lingkungan dan gaya hidup, sehingga aging dapat
terjadi lebih dini atau lambat tergantung kesehatan masing-masing individu
(Salavkar, Tamanekar,and Athawale, 2011). Penuaan dini dapat dilihat dari kulit
kering dan kasar, kulit berkerut, muncul noda-noda hitam pada kulit, kulit kusam,
dan tidak bercahaya.
Proses penuaan kulit dapat disebabkan oleh dua faktor yakni penuaan
intrinsik dan penuaan ekstrinsik. Proses penuaan intrinsik dapat disebabkan secara
fisiologis seperti faktor ras, hormonal, dan genetik. Proses penuaan pada kulit yang
disebabkan oleh faktor ekstrinsik dapat disebabkan oleh sinar ultraviolet (UVR),
merokok, infeksi, polusi udara, kelembaban udara dan faktor ekstrinsik lainnya
(Chuarienthong, Lourith, and Leelapornpisid, 2010). UVR dapat menyebabkan
perubahan pada kulit yakni sunburn, kanker kulit, dan photoaging (Jing-Yi,
Tournas, Burch, Monteire, and Zielinsk, 2007). Pemaparan UVR dapat
menghasilkan ROS (Reactive Oxygen Spesies) atau radikal bebas sehingga sel akan
diserang. Sel yang diserang ROS kemudian akan merusak membran lipid, protein
dan DNA selular dalam tubuh sehingga akan berakibat penuaan pada kulit yang jika
diamati secara visual akan terlihat kerutan pada epidermis dan mengalami
memproteksi kulit dari kerusakan oksidatif yang disebabkan pemaparan UVR
dalam jangka waktu yang panjang (Chuarienthong, Lourith, and Leelapornpisid,
2010). Kerusakan yang disebabkan oleh pemaparan UVR dapat diproteksi oleh
senyawa antioksidan. Menurut Cornwell et al.(cit., Chaiyavat, Kumar, Tipduangta,
and Rungseevijitprapa, 2010) Isoflavon adalah senyawa alami yang mempunyai
aktivitas antioksidan. Menurut Murphy et al. (cit., Lee, Renita, Fioritto, Martin,
Schwartz, and Vodovotz, 2004), Isoflavon yang ditemukan pada kedelai memiliki
beberapa bentuk yakni aglikon, β-glukosida, 6-O”-malonil-β-glukosida , 6-O” -asetil- β-glukosida. Bentuk glikosida terdapat pada kedelai yang tidak difermentasi
sedangkan bentuk aglikon terdapat pada kedelai yang sudah difermentasi, misalnya
tempe (Astuti, 2012). Dalam perkembangan sediaan kosmetik, isoflavon digunakan
dalam bentuk aglikon karena dalam kulit tidak terdapat enzim penghidrolisis
sehingga tidak dapat terpenetrasi hingga lapisan kulit yang lebih dalam misalnya
lapisan epidermis (Schmid and Zulli, 2002).
Menurut Berghofer et al. (cit., Chaiyavat, Kumar, Tipduangta, and
Rungseevijitprapa, 2010) Studi menunjukkan bahwa produk kedelai hasil
fermentasi tidak kehilangan aktivitas antioksidannya. Daya antioksidan meningkat
dibandingkan pada produk kedelai yang tidak difermentasi. Genistein memiliki
kelarutan yang rendah dalam minyak (Daniel and Zulli, 2002). Sediaan
mikroemulsi untuk penggunaan topikal dapat meningkatkan kelarutan genistein
yang rendah dalam minyak sehingga dapat terabsorpsi ke dalam kulit dengan baik.
Kelebihan mikroemulsi adalah mempunyai kestabilan dalam jangka waktu yang
pembuatan murah, daya kelarutan tinggi, serta mempunyai kemampuan
berpenetrasi yang baik (Agoes, 2009). Karakteristik tersebut membuat mikroemulsi
mempunyai peranan penting dalam formula untuk zat aktif yang tidak larut.
Salah satu komponen penyusun mikroemulsi adalah surfaktan, surfaktan
biasanya digunakan sebagai suspending agent, wetting agent,dan emulsifier.
Surfaktan juga memiliki efek terhadap permeabilitas membran biologis seperti kulit
sehingga dapat juga berfungsi sebagai penetration enhancer. Penggunaan
penetration enhancer dapat meningkatkan kelarutan suatu senyawa, surfaktan dapat
berfungsi juga sebagai penetration enhancer dengan mekanisme menembus ke
daerah diantara stratum korneum kemudian meningkatkan fluiditas dan melarutkan
komponen lipid atau masuk melalui jalur interseluler dan berikatan dengan filamen
keratin. Tween 80 merupakan surfaktan non-ionik polysorbate yang umumnya
digunakan sebagai penetration enhancer (Som, Bhatia, and Yasir, 2012). Pengaruh
penetration enhancer terhadap permeasi kulit dapat dievalusi secara in-vitro yakni
dengan uji difusi franz-cell.
1. Permasalahan
Apakah peningkatan konsentrasi tween 80 sebagai penetration enhancer
dapat berpengaruh pada proses absorpsi perkutan mikroemulsi ekstrak tempe
dengan metode Franz Diffusion Cell ?
2. Keaslian penelitian
Penelitian yang telah dilaksanakan dan terkait dengan penelitian ini sejauh
a. Akhtar (2011) meneliti efek dari penetration enhancer dari polysorbate 20
dan polysorbate 80 terhadap pengaruh absorpsi perkutan pada asam askorbat. Dari
penelitian tersebut didapat hasil semakin tinggi konsentrasi penetration enhancer
maka semakin tinggi pula permeabilitas dari asam askorbat.
b. Chadha (2009) meneliti genistein yang diformulasikan dalam bentuk gel
dengan berbagai penetration enhancer golongan terpene seperti menthol, limonene,
cineole, carvone, Lauroglycol® 90, Labrasol® ,dan Transcutol®P . Hasil penelitian
menunjukkan bahwa penetration enhancer seperti menthol, Lauroglycol® 90,
Labrasol® , Transcutol®P merupakan enhancer yang paling efisien dalam
meningkatkan permeasi kulit.
c. Georgetti, Casagrande, Verri, Lopez, and Fonseca (2008) melakukan
penelitian dengan menggunakan soybean extract sebagai senyawa aktif dalam
pembuatan emulsi yang digunakan secara topikal untuk mengurangi efek oksidatif
pada kulit. Formulasi kemudian ditindaklanjuti dengan studi absorpsi perkutan
dengan menggunakan KCKT. Hasil penelitian menunjukkan bahwa genistein tidak
terdeteksi dalam kompartemen reseptor sehingga aktivitas antiosidannya juga tidak
dapat diketahui, hal ini dikarenakan jumlah yang menembus kulit dibawah LOD
yakni (0,1 µg/mL).
Perbedaan penelitian ini dengan penelitian yang pernah dilakukan tersebut
terletak pada sumber senyawa aktif yang digunakan, membran kulit yang
digunakan, dan penetration enhancer yang digunakan. Sejauh penelusuran pustaka
penetration enhancer pada formulasi mikroemulsi ekstrak tempe dengan metode
Franz Diffusion Cell.
3. Manfaat Penelitian a. Manfaat Teoretis
Menambah pengetahuan tentang pengaruh penetration enhancer pada absorpsi
perkutan mikroemulsi ekstrak tempe.
b. Manfaat Praktis
Menghasilkan formulasi mikroemulsi ekstrak tempe yang memiliki sifat fisik
dan stabilitas fisik yang baik.
B. Tujuan Penelitian
Mengetahui apakah peningkatan konsentrasi tween 80 sebagai penetration
enhancer berpengaruh pada absorpsi perkutan mikroemulsi ekstrak tempe dengan
6
BAB II
PENELAAHAN PUSTAKA
A. Kulit
Kulit adalah organ terbesar pada tubuh yang menutupi sekitar 1,7 m2 tubuh
dan berisi kira-kira 10 % dari total berat badan orang berukuran sedang. Fungsi
utama dari kulit adalah untuk menyediakan barrier perlindungan antara tubuh
dengan lingkungan luar (Benson, 2012). Struktur serta fungsi dari kulit manusia
yang terdiri dari empat bagian utama yakni : stratum korneum, viable epidermis,
dermis, dan jaringan subkutan . (Gambar 1)
Struktur kulit meliputi bagian-bagian di bawah ini :
a) Stratum korneum yang disebut juga non-viabel epidermis merupakan
lapisan kulit paling luar yang merupakan penghalang utama masuknya
senyawa asing. Rata-rata ketebalan stratum korneum adalah 10-20 µm
dengan struktur terdiri dari brick dan mortar yang merupakan barrier
pengontrol kecepatan dalam absorbsi transdermal. Stratum korneum
sebagian besar terdiri dari protein dan keratin sehingga punya daya
absorbsi yang besar terhadap air dan bahan-bahan yang bersifat polar
lainnya (Walter, 2008).
b) Epidermis merupakan bagian dari kulit yang berlapis-lapis dengan
ketebalan 0,06 mm pada kelopak mata dan sekitar 0,08 mm pada telapak
tangan dan telapak kaki. Pembuluh darah tidak terdapat dalam epidermis.
(Benson, 2012).
c) Dermis mempunyai ketebalan sekitar 2-5 mm dan terdiri atas fibril
kolagen sebagai penyangga, dan elastic connective tissue yang
menyediakan elastisitas dan fleksibilitas yang melekat dalam matriks
mucopolysaccharide. Dermis menyediakan perlindungan saat terjadi
permeasi oleh obat tetapi dapat mengurangi permeasi ke dalam jaringan
yang lebih dalam saat obat yang sangat lipofilik masuk (Benson, 2012).
d) Jaringan Subkutan terdiri dari lapisan sel lemak yang tersusun sebagai
lobula dengan adanya kolagen yang saling berhubungan dan elastin fibers.
Fungsi utama di jaringan subkutan yakni menyekat panas dan melindungi
Gambar 2. Jalur Umum Senyawa Aktif Dalam Menembus Kulit (Lane, 2013)
Jalur umum yang dilewati senyawa aktif untuk menembus kulit yakni
melalui lapisan stratum korneum, jalur interseluler, dan jaringan tambahan.
(Gambar 2)
a) Melalui lapisan stratum korneum
Jalur transeluler, jalur dimana obat menyeberangi kulit secara langsung
dengan melewati kedua fosfolipid membran dan sitoplasma keratinosit mati
yang merupakan stratum korneum (Benson, 2012).
b) Jalur interseluler, jalur dimana obat melintasi kulit dengan melewati
ruang-ruang kecil di antara sel-sel kulit (Benson, 2012).
c) Jaringan tambahan pada kulit yakni folikel dan kelenjar (Benson, 2012).
B. Aging
Kulit manusia akan berubah seiring dengan bertambahnya usia. Proses skin
aging tidak dapat dihindari, maka pemahaman tentang proses yang terjadi di kulit
sangatlah penting. Adanya paparan sinar matahari dipercaya akan mempercepat
berada di sekitar kita (Yaar and Gilchrest, 2007).
Skin aging dapat disebabkan oleh berbagai macam faktor internal
maupun eksternal, salah satu faktor eksternal tersebut adalah paparan sinar
matahari yang sering disebut photo aging. Mekanisme penuaan yang dipicu oleh
faktor eksternal paparan sinar matahari adalah adanya penurunan jumlah ceramide
akibat reaksi dengan Reactive Oxygen Species yang dapat dihambat dengan adanya
antioksidan sebagai salah satu mekanisme anti aging (Schimd and Zulli, 2002).
C. Isoflavon dan Tempe
Isoflavon merupakan salah satu anggota utama dalam phytoestrogens,
sebuah senyawa polifenol non-steroid yang berasal dari tanaman (Jing-Yi, Tournas,
Burch, Monteire, and Zielinsk, 2007). Menurut Cornwell et al.(cit., Chaiyavat,
Kumar, Tipduangta, and Rungseevijitprapa, 2010) Isoflavon adalah senyawa alami
yang mempunyai aktivitas antioksidan. Isoflavon banyak terdapat pada
buah-buahan, sayuran dan biji-bijian seperti kacang kedelai yang digunakan sebagai
pangan fungsional dengan berbagai kegunaan untuk pengatasan masalah
osteoporosis dan masalah kesehatan jantung. Menurut Murphy et al. (cit., Lee,
Renita, Fioritto, Martin, Schwartz, and Vodovotz, 2004), Isoflavon yang ditemukan
pada kedelai memiliki beberapa bentuk yakni aglikon, β-glukosida, 6-O”
-malonil-β-glukosida , 6-O”-asetil-β-glukosida.
Kedelai yang tidak mengalami proses fermentasi banyak mengandung
isoflavon dalam bentuk glukosida dan bentuk aglikonnya hanya dalam persentase
sedangkan bentuk aglikon terdapat pada kedelai yang sudah difermentasi, misalnya
tempe (Astuti, 2012). Bentuk glikosida yang terdegradasi menjadi bentuk aglikon
akan lebih mudah diserap oleh tubuh (Astuti, 2012). Isoflavon dalam bentuk
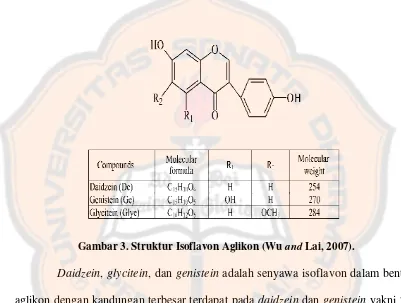
aglikon mempunyai struktur molekul sebagai berikut :
Gambar 3. Struktur Isoflavon Aglikon (Wu and Lai, 2007).
Daidzein, glycitein, dan genistein adalah senyawa isoflavon dalam bentuk
aglikon dengan kandungan terbesar terdapat pada daidzein dan genistein yakni
26-32 mg dan 28-39 mg dalam 100 g tempe (Haron, Ismail, Azlan, Shahar, and Peng,
2010). Selama proses fermentasi kedelai enzim β-glukosidase akan aktif dan
mengubah glisitin, genistin,dan daidzin yang ada menjadi glisitein, genistein, dan
daidzein dimana ikatan –O glikosida pada isoflavon akan terhidrolisis sehingga terbentuk senyawa gula dan aglikon bebas dari isoflavon (Pawiroharsono, 2009).
Senyawa aglikon ini dapat mengalami transformasi membentuk senyawa baru
yakni Faktor-II (6,7,4'trihidroksi isoflavon) dimana senyawa ini merupakan
lebih besar dari senyawa antioksidan biasa dan hanya terdapat pada tempe karena
terbentuk selama proses fermentasi (Pawiroharsono, 2009).
Dalam perkembangan sediaan kosmetik isoflavon digunakan dalam
bentuk aglikon karena dalam kulit tidak terdapat enzim penghidrolisis sehingga
dapat terpenetrasi hingga lapisan kulit yang lebih dalam misalnya lapisan
epidermis karena lapisan lemak yang dibentuk oleh epidermis akan membiarkan
senyawa yang dapat lewat adalah aglikon yang dapat larut dalam air (Schimd and
Zulli, 2002).
Mekanisme isoflavon dalam mencegah penuaan dini yakni dengan efek
phytoestrogen, isoflavon akan berpasangan dengan reseptor estrogen dalam inti sel
sehingga memiliki potensi yang sama untuk menghambat penipisan kulit, dan
mekanisme antioksidan, atom hidrogen pada isoflavon akan bertindak sebagai agen
antioksidan yang akan mengikat elektron dari ROS sehingga tidak terjadi aktivasi
MMPs dan tidak terjadi reaksi photoaging (Chiang, Wu, Fang, Chen, Kao, Chen, et
al., 2007).
D. Enhancer
Enhancer kimia adalah senyawa yang dapat meningkatkan penetrasi
perkutan obat dengan berpartisi pada stratum korneum dan mengubah susunan
lipid-protein di kulit. Perubahan ini menyebabkan perubahan sifat stratum korneum
dan terjadi penurunan pertahanan pada stratum korneum. Enhancer kimia dapat
meningkatkan permeabilitas stratum korneum melalui beberapa mekanisme yaitu
1) meningkatkan fluiditas lipid di kulit;
3) melalui aksi keratolitik;
4) meningkatkan kelarutan obat;
5) meningkatkan partisi stratum korneum (Kumar and Philip, 2007).
Penambahan surfaktan ke dalam suatu formula berfungsi untuk melarutkan
senyawa aktif yang bersifat lipofilik. Surfaktan juga mempunyai potensi untuk
melarutkan lipid pada lapisan stratum korneum. Surfaktan biasanya terdiri dari alkil
lipofilik atau aril rantai lemak dengan gugus hidrofilik pada bagian kepala.
Surfaktan anionik seperti sodium lauryl sulphate (SLS) dan surfaktan kationik
seperti cetyltrimethyl ammonium bromide berbahaya bagi kulit manusia (Williams
and Barry, 2004). Menurut Tupker, Pinnagoda, and Nater (cit., Williams and Barry,
2004) SLS merupakan iritan kuat dan dapat meningkatkan trans epidermal water
loss saat dilakukan pengujian secara in-vivo pada manusia. Surfaktan anionik
maupun kationik dapat mengembangkan lapisan stratum korneum dan berinteraksi
dengan lapisan interselular pada keratin sehingga dalam jumlah besar dapat
menyebabkan iritasi.
Surfaktan non-ionik merupakan surfaktan yang aman digunakan, memiliki
toksisitas kronis rendah dan banyak studi menunjukkan bahwa surfaktan non-ionik
dapat menaikkan nilai fluks dari materi untuk berpermeasi melalui membran
biologis. Banyak studi mengevaluasi aktivitas peningkatan permeabilitas pada
penggunaan surfaktan anionik dan non-ionik. Surfaktan anionik cenderung
memiliki permeasi yang rendah melalui lapisan stratum korneum manusia dalam
permeabilitas surfaktan non-ionik pada kulit manusia lebih kecil dibandingkan
surfaktan anionik.
Surfaktan non-ionik yang biasanya digunakan adalah polyoxyethylene alkyl
ether (Brij) dan polyoxythylene sorbitan fatty acid ester (Tween). Studi DSC pada
surfaktan non-ionik mengindikasikan bahwa surfaktan akan berinteraksi dengan
kulit dan mengubah struktur lipid dan meningkatkan permeabilitas dimana
kemampuan surfaktan mempengaruhi permeasi kulit tergantung dari sifat fisika
kimianya (Lane, 2013).
E. Mikroemulsi
Mikroemulsi adalah suatu sistem yang terdiri dari minyak, air dan
surfaktan, dan dikombinasikan dengan penambahan ko-surfaktan yang bersifat
isotropik, stabil secara termodinamika, transparan (Talegaonkar, Azeem, Ahmad,
Khar, Pathan, and Khan, 2008). Mikroemulsi mempunyai ukuran droplet dengan
rentang 10-100 nm. Sistem homogen mikroemulsi dipersiapkan dengan adanya
konsentrasi surfaktan, minyak dan air yang sesuai (Singh, Bushetti, Raju, Ahmad,
Singh, and Bisht, 2011).
Mikroemulsi terbentuk spontan tanpa pengadukan dengan kecepatan
tinggi karena tegangan antar muka yang sangat rendah yakni mendekati nol antara
fase air dan fase minyak sehingga energi bebas menjadi negatif. Pembentukan
mikroemulsi membutuhkan konsentrasi surfaktan yang lebih tinggi daripada emulsi
biasa. Pembentukan mikroemulsi tergantung dari struktur dan tipe surfaktan. Pada
1) sifat dasar dan konsentrasi minyak, surfaktan, kosurfaktan dan fase air;
2) perbandingan minyak/surfaktan dan surfaktan/kosurfaktan;
3) temperatur dan pH lingkungan;
4) sifat fisikokimia dari obat seperti hidrofilisitas/lipofilisitas, pKa dan
polaritas (Date, Abjhijit, and Nagarsengker, 2008).
Tipe mikroemulsi dibagi menjadi empat tipe yaitu tipe I, tipe II, tipe III,
dan tipe IV. Mikroemulsi tipe I dengan tipe m/a yakni surfaktan yang digunakan
lebih larut dalam air dan jumlah fase air lebih banyak dibandingkan fase minyak.
Mikroemulsi tipe II terbentuk mikroemulsi dengan tipe a/m karena surfaktan yang
digunakan akan lebih larut dalam fase minyak dan jumlah fase minyak lebih banyak
daripada fase air. Mikroemulsi tipe III terbentuk sistem tiga fase karena surfaktan
akan larut dalam fase minyak dan fase air. Mikroemulsi tipe IV terbentuk
mikroemulsi satu fase (isotropik) karena surfaktan dan alkohol dalam formula
(Singh, Bushetti, Raju, Ahmad, Singh, and Bisht, 2011).
F. Absorpsi Perkutan
Absorpsi perkutan melibatkan bagian dari molekul obat berdifusi dari
permukaan kulit ke dalam stratum korneum dibawah pengaruh gradien konsentrasi
dan juga berdifusi melalui stratum korneum, epidermis, melalui dermis, dan ke
dalam sirkulasi darah. Kulit merupakan bagian yang sangat efektif sebagai tempat
suatu zat untuk berpenetrasi dan berperan sebagai penghalang yang bersifat pasif
pada senyawa penetration enhancer. Kulit terdiri atas beberapa bagian salah
penetrasi (Sinha and Kaur, 2000). Absorpsi perkutan suatu senyawa diketahui
dengan melakukan uji difusi in-vitro dengan melibatkan sel difusi yang terdiri dari
dua kompartemen yaitu kompartemen donor dan kompartemen akseptor yang
dipisahkan oleh membran. Membran yang dapat digunakan untuk uji transpor yaitu
kulit tikus, babi, marmut, kelinci, ular, manusia atau membran kulit sintetik. Kulit
manusia adalah pilihan utama untuk uji absorpsi perkutan tetapi sulit untuk
didapatkan, sehingga banyak digunakan kulit tikus sebagai penggantinya (Nair and
Panchagula, 2004). Studi permeasi in-vitro menggunakan kulit tikus dapat
memberikan informasi yang berguna untuk memanipulasi desain pemberian obat
secara transdermal, sehingga dapat dicapai permeasi obat yang menembus kulit
(Al-Saidan, Krishnaiah, Chandrasekhar, Lalla, Rama, Jayaram, et al., 2004).
Studi permeasi in-vitro menggunakan sel difusi karena dapat menguji obat
dalam bentuk larutan, sediaan semi padat ataupun patch transdermal (Roberts and
Walters, 1998). Senyawa uji diletakkan pada kompartemen donor dalam bentuk
larutan, formula tertentu, atau patch transdermal. Evaluasi yang dilakukan berupa
transfer massa menembus kulit dengan mengukur kadar obat dalam aseptor
(Roberts and Walters, 1998). Uji permeasi in-vitro yang menggunakan sel difusi
franz-cell harus memperhatikan kondisi penghantaran obat yang dikontrol karena
permeasi obat dapat tergantung pada kulit atau membran yang digunakan.
Faktor-faktor yang perlu diperhatikan dalam uji permeasi in-vitro yaitu
1) Pemilihan membran
Penggunaan kulit manusia sebagai membran uji mempunyai beberapa
mengontrol jenis kelamin, ras, umur, dan kondisi kulit, sehingga untuk uji in-vitro
ini biasa digunakan kulit binatang seperti kulit tikus, babi, marmut, kelinci,dan ular.
2) Larutan donor
Senyawa yang dilarutkan atau didispersikan dalam pembawa (enhancer)
akan berdifusi melalui pembawa menuju ke permukaan kulit sebelum obat
diabsorpsi. Pembawa dapat mempengaruhi pelepasan senyawa dari pembawa dan
dapat berinteraksi dengan stratum korneum. Faktor yang mempengaruhi pelepasan
obat meliputi sifat fisikokimia zat aktif dan pembawa yakni kelarutan, ukuran
molekul, viskositas dan polaritas (Wiechers, 1989).
3) Larutan akseptor
Larutan akseptor yang digunakan dalam sel difusi sebaiknya tidak hanya
berperan sebagai penerima obat yang mengalami permeasi di dalamnya tetapi
sebaiknya menyediakan air, bahan-bahan biokimia, dan ion-ion yang diperlukan
untuk membran kulit dalam mempertahankan fungsinya dalam permeasi pada pH
dan kekuatan osmotik yang diinginkan (Skelly, 1987).
Larutan yang digunakan sebagi kompartemen akseptor yaitu dapat berupa
larutan fisiologis salin, larutan ringer, atau larutan fisiologis lainnya yang relevan.
Faktor penting lain dari larutan akseptor yang perlu diperhatikan yaitu suhu,
kelarutan senyawa dalam medium, dan pengadukan (Friend, 1992). Pengaturan
temperatur larutan akseptor penting untuk meminimalkan adanya variasi dalam
kondisi percobaan. Suhu sebaiknya dijaga pada kondisi fisiologi normal dengan
kenaikan temperatur dapat meningkatkan hidrasi dari kulit. Kenaikan suhu 10ºC
Pengadukan pada larutan aseptor akan membuat larutan lebih homogen (Friend,
K = Koefisien Partisi Obat
h = Tebal membran Difusi
Cd = Konsentrasi obat dalam kompartemen donor
Cr = Konsentrasi obat dalam kompartemen reseptor
Nilai fluks (J) atau laju penetrasi obat dari kompartemen donor ke
kompartemen reseptor dapat dihitung dengan menggunakan persamaan:
Dimana :
Q = Jumlah obat yang terpenetrasi
kp = Koefisien permeabilitas stratum korneum
A = Luas area pemberian obat
Cv = Konsentrasi obat dalam sediaan
{ ∑ }
Keterangan :
Q = Jumlah kumulatif genistein yang terpenetrasi per luas area difusi (µg
cm2)
Cn = Konsentrasi genistein (µg/mL) pada sampling menit ke-n
V = Volume sel difusi Franz ( mL)
∑
= Jumlah konsentrais genistein (µg/mL) pada sampling pertama (menit ke
– n) hingga sebelum menit ke – n
S = Volume sampling ( mL)
A = Luas area membran (cm2)
Dimana :
J = Fluks (µg cm-2 jam-1)
Q = Jumlah kumulatif genistein yang melalui membran (µg)
T = Waktu (jam)
G. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi adalah metode pemisahan dimana komponen yang
dipisahkan terdistribusi dalam dua fase, yakni fase diam (stationary phase) dan fase
gerak (mobile phase) yang bergerak ke satu arah (Rohman, 2007). Kromatografi
Cair Kinerja Tinggi (KCKT) biasa digunakan untuk menghitung kuantitas dalam
tekanan kolom yang mengandung partikel-partikel fase diam dengan diameter 3-10
µm dimana partikel sampel dimasukkan melalui bagian atas kolom melalui katup
lengkung dan pemisahan akan dilakukan berdasarkan lamanya waktu relatif yang
diperlukan oleh komponen di dalam fase diam. Penentuan elemen yang keluar
dapat ditentukan dengan berbagai detektor (Watson, 2005).
Pemurnian senyawa alam biasanya digunakan teknik kromatografi untuk
memisahkan komponen senyawa alam yang kompleks. Ada beberapa metode
pemisahan dari kromatografi dalam pemurnian senyawa alami, metode pemisahan
tersebut yaitu kromatografi fase terbalik (reverse phase chromatography),
kromatografi fase normal (normal phase chromatography), dan gel permeation
chromatography (Sarker, Latif, and Gray, 2006). Kromatografi fase terbalik
(Reverse phase chromatography) adalah metode kebalikan dari kromatografi fase
normal dimana fase diam lebih bersifat non-polar daripada fase gerak ( Sarker,
Latif, and Gray, 2006). Kromatografi fase terbalik (Reverse phase
chromatography) merupakan pilihan pertama ketika akan dilakukan suatu
pemisahan senyawa yang mempunyai bentuk ionik atau bersifat netral.
Fase diam dalam sistem kromatografi sangat menentukan waktu retensi
dan selektivitas dalam pembacaan data, dalam kromatografi fase terbalik kolom
yang digunakan terdiri dari fase yang lebih kurang polar seperti C8 atau C18,
organosilan yang diikat kovalen dengan gugus silanol pada permukaan silika untuk
membentuk fase gerak atau ligan R, biasanya- Cl,-Oet, atau –CH3 (Snyder,
Kirkland, and Dolan, 2010). Macam fase diam yang biasa digunakan dalam sistem
pada kromatografi fase normal yakni silika. Struktur fase diam masing-masing
sistem kromatografi dapat dilihat pada tabel I (Sarker, Latif, and Gray, 2006).
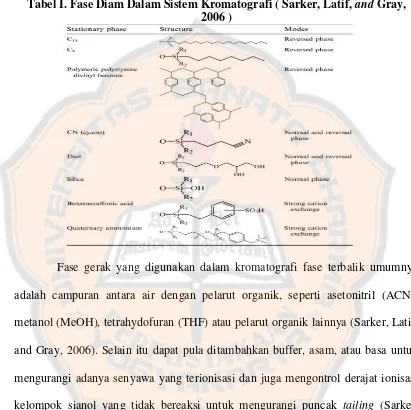
Tabel I. Fase Diam Dalam Sistem Kromatografi ( Sarker, Latif, and Gray, 2006 )
Fase gerak yang digunakan dalam kromatografi fase terbalik umumnya
adalah campuran antara air dengan pelarut organik, seperti asetonitril (ACN),
metanol (MeOH), tetrahydofuran (THF) atau pelarut organik lainnya (Sarker, Latif,
and Gray, 2006). Selain itu dapat pula ditambahkan buffer, asam, atau basa untuk
mengurangi adanya senyawa yang terionisasi dan juga mengontrol derajat ionisasi
kelompok sianol yang tidak bereaksi untuk mengurangi puncak tailing (Sarker,
Latif, and Gray, 2006). Fase gerak yang digunakan dalam sistem kromatografi
memiliki kriteria yakni
1) memiliki kemurnian yang tinggi untuk mempertahankan integritas
sistem kromatografi dan sampel;
2) memiliki kompaktibilas dengan detektor dan tidak menganggu saat
3) memiliki kompatibilitas yang baik dengan sampel baik dalam hal
solubilitas dan ketidakreaktifan;
4) memiliki viskositas yang rendah untuk menjaga tekanan pada sistem
tetap stabil; dan
5) harganya terjangkau (Sarker, Latif, and Gray, 2006).
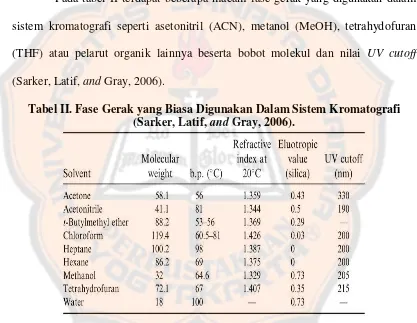
Pada tabel II terdapat beberapa macam fase gerak yang digunakan dalam
sistem kromatografi seperti asetonitril (ACN), metanol (MeOH), tetrahydofuran
(THF) atau pelarut organik lainnya beserta bobot molekul dan nilai UV cutoff
(Sarker, Latif, and Gray, 2006).
Tabel II. Fase Gerak yang Biasa Digunakan Dalam Sistem Kromatografi (Sarker, Latif, and Gray, 2006).
Fase gerak juga harus bebas dari gas yang keluar dari solvent dengan cara
degassing, solvent yang tidak di degassing akan membentuk gelembung
mikroskopis dimana akan menganggu analisis. Selain degassing ada langkah lain
untuk menghilangkan gas yakni teknik vakum atau menempatkan wadah fase gerak
yang akan digunakan juga harus disaring terlebih dahulu untuk menghindari adanya
partikel-partikel kecil yang akan menyumbat kolom (Rohman, 2009).
H. Virgin Coconut Oil
Virgin Coconut Oil (VCO) merupakan minyak yang diproses dari buah
kelapa tanpa mengalami pemanasan, berwarna bening dan mengandung banyak
asam laurat serta asam lemak rantai menengah (Medium Chain Fatty Acid)
sebanyak 60 % (Yulian, 2007). VCO dapat ditemukan dalam sediaan kosmetik
maupun sediaan topikal sebagai komponen salep, krim, dan emulsi. Manfaat pada
VCOdalam sediaan topikal yakni
1) mempunyai sifat daya sebar pada kulit yang baik;
2) tidak menghambat respirasi kulit;
3) mempunyai sifat penetrasi yang baik;
4) mempunyai sifat emolien yang baik;
5) lapisan yang terbentuk pada saat diaplikasikan ke kulit tidak terlihat;
6) kompaktibilitas yang baik; dan
7) mempunyai stabilitas yang baik terhadap terjadinya oksidasi (Rowe et
al., 2009).
VCO dapat digunakan sebagai moisturizer untuk penggunaan kulit kering
tanpa adanya efek samping (Gediya, 2011). VCO mengandung trigliserida,
komponen asam lemak terutama asam laurat dan asam misristat dan sebagian asam
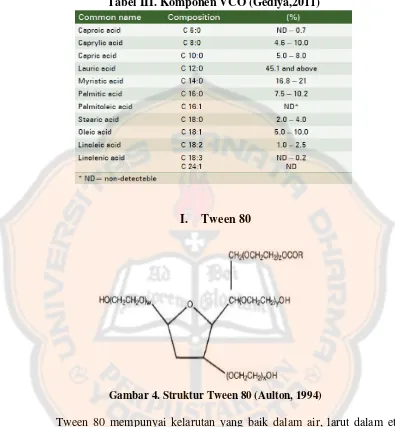
kaprat, kaproat, kaprilat, oleat, palmitat dan stearat. Tabel dibawah menunjukkan
Tabel III. Komponen VCO (Gediya,2011)
I. Tween 80
Gambar 4. Struktur Tween 80 (Aulton, 1994)
Tween 80 mempunyai kelarutan yang baik dalam air, larut dalam etanol
95% dan etilasetat, dan tidak larut dalam parafin cair (Depkes RI, 1993). Tween 80
memiliki nilai HLB sebesar 15 (Zhong, Xu, Fu, and Li, 2012). Penggunaan tween
80 dalam farmasi yakni sebagai emulsifying agent, wetting agent, penetrating agent,
dan diffusan (Som, Bhatia, and Yasir, 2012). Tween 80 dapat menurunkan tegangan
antarmuka antara obat dan medium sekaligus membentuk misel sehingga molekul
J. Nipagin
Gambar 5. Struktur Nipagin (Rowe, et.all, 2009)
Nipagin merupakan kristal tidak berwarna serta memberikan rasa panas
dan bau tidak spesifik. Nipagin mempunyai kelarutan yang baik dalam aseton,
etanol, eter, gliserin, dan praktis tidak larut dalam air. Nipagin berfungsi sebagai
pengawet aktif pada pH 4-8 dan dikombinasikan dengan paraben lain. Nipagin
digunakan sebagai antimikroba pada penggunaan topikal dengan konsentrasi 0,01
%-0,6%. Aktivitas antimikrobia dari nipagin akan berkurang dengan kehadiran
surfaktan nonionik sebagai akibat dari adanya proses miselisasi (Rowe, et.all,
2009). Nipagin biasa digunakan sebagai pengawet di sediaan kosmetik (Rowe,
et.all, 2009).
K. Nipasol
Gambar 6. Struktur Nipasol (Rowe, et.all, 2009)
Nipasol digunakan sebagai antimikroba pada kosmetik, makanan, dan
rantai gugus alkil dan kelarutannya dalam air akan menurun. Nipasol dapat
digunakan dengan campuran paraben lain untuk menghasilkan efek antimikroba
ayng lebih efektif. Konsentrasi penggunaan nipasol sebagai antimikroba pada
sediaan topikal adalah 0,02 %-0,3% (Rowe et al., 2009).
L. Landasan Teori
Kulit merupakan barrier perlindungan antara tubuh dengan lingkungan
luar dimana terdiri dari empat bagian utama yakni stratum korneum, viable
epidermis, dermis, dan jaringan subkutan. Seiring bertambahnya usia kulit dapat
mengalami skin aging yang dapat disebabkan oleh faktor internal maupun
eksternal yakni paparan sinar matahari yang sering disebut photoageing. Isoflavon
dalam tempe mempunyai bentuk aglikon dan dalam perkembangan sediaan
kosmetik isoflavon digunakan dalam bentuk aglikon yakni genistein. Mekanisme
isoflavon dalam mencegah penuaan dini yakni dengan mekanisme antioksidan.
Mekanisme antioksidan terjadi di sirkulasi sistemik maka genistein harus
terabsorpsi secara perkutan dengan berdifusi dari permukaan kulit ke dalam stratum
korneum dibawah pengaruh gradien konsentrasi dan juga berdifusi melalui stratum
korneum, epidermis, melalui dermis, dan ke dalam sirkulasi darah.
Mikroemulsi adalah salah satu sistem penghantaran obat yang terdiri dari
minyak, air dan surfaktan. Surfaktan juga memiliki efek terhadap permeabilitas
membran biologis seperti kulit sehingga dapat juga berfungsi sebagai penetration
enhancer. Penggunaan penetration enhancer dapat meningkatkan kelarutan suatu
senyawa, surfaktan dapat berfungsi juga sebagai penetration enhancer. Surfaktan
meningkatkan permeasi. Keberadaan enhancer akan meningkatkan penetrasi
perkutan genistein dengan berpartisi pada stratum korneum dan mengubah susunan
lipid-protein di kulit maka genistein dapat berpenetrasi dengan baik. Uji absorpsi
perkutan menggunakan Franz Diffusion Cell modifikasi untuk mengukur jumlah
zat aktif yang terpenetrasi dari membran dan kadar genistein yang terpenetrasi ke
dalam kompartemen reseptor diukur dengan HPLC.
M. Hipotesis
Berdasarkan landasan teori, dapat disusun hipotesis bahwa kenaikan
konsentrasi tween 80 sebagai penetration enhancer memiliki pengaruh pada
absorpsi perkutan formulasi mikroemulsi ekstrak tempe dengan metode Franz
27
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian tentang pengaruh konsentrasi surfaktan terhadap penetrasi
genistein termasuk jenis penelitian eksperimental murni dengan rancangan
penelitian acak lengkap pola searah.
B. Variabel Penelitian 1. Variabel Utama
a. Variabel bebas pada penelitian ini adalah konsentrasi surfaktan yakni
tween 80.
b. Variabel tergantung pada penelitian ini adalah nilai fluks genistein yang
terabsorpsi ke dalam stratum korneum.
2. Variabel Pengacau
a. Variabel pengacau terkendali pada penelitian ini adalah suhu dan
kecepatan pengadukan pada saat uji Franz Diffusion cell modifikasi.
b. Variabel pengacau tak terkendali pada penelitian ini adalah kelembaban
ruangan.
C. Definisi Operasional
1. Mikroemulsi adalah suatu sistem yang terdiri dari minyak, air dan surfaktan
dan ekstrak tempe serta memiliki ukuran partikel dari dibawah 100 nm dengan
2. Tween 80 adalah surfaktan non-ionik yang bertindak sebagai penetration
enhancer pada mikroemulsi ekstrak tempe.
3. Absorpsi perkutan genistein adalah genistein yang terabsorpsi secara perkutan
dengan berdifusi dari permukaan kulit ke dalam stratum korneum dibawah
pengaruh gradien konsentrasi.
4. Franz Diffusion Cell Modifikasi adalah alat untuk studi difusi secara in-vitro
menggunakan sel difusi franz-cell modifikasi untuk menguji genistein yang
terpenetrasi dari mikroemulsi ekstrak tempe.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah tween 80, Virgin
Coconut Oil (VCO), PEG 400, ekstrak tempe, aquadest, minyak mawar, etanol
teknis, etanol p.a, etil asetat teknis, metanol p.a, aquabidest, petroleum eter, NaCl,
KCl, Na2HPO4, KH2PO4, mencit galur Swiss.
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah alat-alat gelas
(PYREX-GERMANY), corong pisah, cawan porselen, neraca digital, waterbath, magnetic
stirer, tabung effendorf, pipet volume, HPLC (High Perfomance Liquid
Chromatography), sendok, alat cukur, alat bedah, Franz-cell (modifikasi
Laboratorium Formulasi Teknologi Sediaan Farmasi, USD,Yogyakarta), pH meter
(pH meter 744 Methrom), mikropipet Socorex, DeltaTM Nano C Particle Size
aquadest, spuit, Viskometer seri VT 04 (RION-JAPAN), scalpel, pH stick, kolom
C18, syringe filter 0,22 μm, syringe filter 0,45 μm, degassing, botol fase gerak, Spektrofotometer, Franz-Diffusion Cell Modifikasi.
F. Tata Cara Penelitian
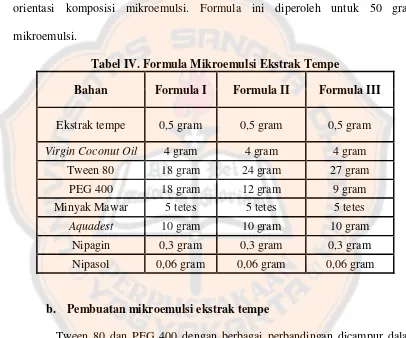
Tata cara penelitian secara umum digambarkan dalam bagan berikut :
Gambar 7 . Bagan Rancangan Penelitian
1. Ekstraksi Tempe
Tempe ditimbang sebanyak 1 kg kemudian diblender selanjutnya
ditambah petroleum eter dengan perbandingan 1:1 hingga tempe terendam dengan
petroleum eter selama ± 40 menit. Petroleum eter dibuang dengan cara menyaring
Ekstraksi Tempe
Pembuatan Kurva Baku
Penetapan KadarGenisteinPada tempe
Orientasi dan Formulasi Komposisi Mikroemulsi
Uji Permeasi dengan Franz Diffusion Cell Modifikasi Uji Stabilitas Fisik – Uji Organoleptis dan pH; Uji Viskositas; Uji Pengukuran Particle Size Analyzer; Cycling
tempe dengan corong Buncher. Tempe yang sudah disaring kemudian dimaserasi
dengan etanol teknis 96% selama 12 jam dengan kecepatan 150 rpm. Hasil
maserasi disaring dengan corong Buncher sehingga didapatkan residu padat dan
larutan kuning kecoklatan. Hasil maserasi berupa ekstrak cair dipekatkan
menggunakan rotary evaporator selama 45-60 menit hingga didapatkan volume
sebanyak 10% volume awal. Ekstrak tempe kemudian dikeringkan dalam oven
dengan suhu 50 ºC hingga bobot tetap.
2. Standarisasi Ekstrak Tempe a. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian ini adalah metanol:air pada
perbandingan (70:30). Fase gerak yakni 500 ml metanol p.a dan aquabidest difilter
terlebih dahulu dengan menggunakan syringe filter 0,22 μm. Metanol p.a dan
aquabidest dilakukan sonifikasi terlebih dahulu sebelum dipompakan pada system
HPLC, untuk mengusir gelembung dan gas yang terlarut dalam solvent. Metode
HPLC yang digunakan adalah isokratik dengan kolom C18, flow rate 1 ml / menit
dan volume injeksi sebanyak 10 µl untuk sampel dan pembuatan kurva baku.
b. Pembuatan larutan baku genistein
Kurva baku dibuat dengan menginjeksikan standar genistein dengan kadar
5 seri konsentrasi baku genistein, yaitu 0,1 µg/ml, 0,5 µg/ml, 1 µg/ml, 5 µg/ml dan
10 µg/ml. Setelah didapatkan persamaan dari kurva baku data respon yang didapat
pada analisis sampel ekstrak dimasukkan ke dalam persamaan kurva baku untuk
c. Penetapan panjang gelombang maksimum
Seri larutan baku konsentrais rendah, sedang dan tinggi yakni 0,1 µg/ml, 1
µg/ml, dan 10 µg/ml masing-masing dilakukan scanning dengan spektofotometer
UV pada panjang gelombang 200-300 nm kemudian ditentukan λ maksimumnya.
d. Penetapan kadar ekstrak tempe
Ekstrak tempe yang mencapai bobot tetap ditimbang 0,5 gram kemudian
dilakukan fraksinasi dengan menambahkan air dan etil asetat ke dalam cawan
porselen sambil dipanaskan di atas waterbath. Larutan dipindahkan ke dalam
corong pisah untuk dilakukan liquid-liquid extraction sebanyak 1 hingga 3 kali,
kemudian dikeringkan hingga bobot tetap. Hasil setiap sampel hasil liquid-liquid
extraction kemudian dilarutkan dalam etanol p.a. sebanyak 25 ml. Masing-masing
sampel hasil liquid-liquid extraction kemudian diambil 50 µl kemudian ditambah
950 µl etanol p.a dan di-milipore dan degassing selama 2 menit sebelum
dimasukkan dalam vial HPLC. Setelah itu, kadar genistein dalam sampel hasil
liquid-liquid extraction diukur dengan menginjeksikannya ke dalam kolom HPLC.
3. Orientasi dan Formulasi Komposisi Mikroemulsi
Orientasi komposisi mikroemulsi dilakukan dengan mencampurkan PEG
400 terlebih dahulu dan Tween 80 dengan perbandingan 1:1, 1:2 , 1:2, 1:3, 1:4, 1:5,
1:6, 1:7, 1:8, 1:9, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1. Larutan kemudian divortex
dan disentrifuge 3000 rpm selama 15 menit. Larutan yang tidak memisah (jernih)
dicampur dengan fase minyak yakni Virgin Coconut Oil sebanyak 1 mL, 2 mL, dan
tidak memisah saat ditambah Virgin Coconut Oil kemudian dilakukan penambahan
aquadest mL sebanyak untuk terbentuknya mikroemulsi.
a. Formula
Formula yang digunakan untuk pembuatan mikroemulsi didapat dari hasil
orientasi komposisi mikroemulsi. Formula ini diperoleh untuk 50 gram
mikroemulsi.
Tabel IV. Formula Mikroemulsi Ekstrak Tempe
Bahan Formula I Formula II Formula III
Ekstraktempe 0,5 gram 0,5 gram 0,5 gram
Virgin Coconut Oil 4 gram 4 gram 4 gram
Tween 80 18 gram 24 gram 27 gram
PEG 400 18 gram 12 gram 9 gram
Minyak Mawar 5 tetes 5 tetes 5 tetes
Aquadest 10 gram 10 gram 10 gram
Nipagin 0,3 gram 0,3 gram 0,3 gram
Nipasol 0,06 gram 0,06 gram 0,06 gram
b. Pembuatan mikroemulsi ekstrak tempe
Tween 80 dan PEG 400 dengan berbagai perbandingan dicampur dalam
beaker glass terlebih dahulu. Ekstak tempe dan Virgin Coconut Oil ditambahkan
kemudian larutan diaduk menggunakan magnetic stirer dengan kecepatan 1000 rpm
selama 3 menit. Nipagin dan nipasol ditambahkan ke dalam formula kemudian
dilanjutkan dengan penambahan aquadest yang dicampur dengan fase minyak dan
diaduk menggunakan magnetic stirer dengan kecepatan 1000 rpm selama 3 menit.
4. Uji Stabilitas Fisik
a. Uji Organoleptis dan pH
Uji organoleptis dilakukan dengan mengamati kejernihan,sedimentasi, bau
dan perubahan warna mikroemulsi pada 24 jam hingga sebulan penyimpanan.
Pengukuran pH dilakukan dengan menggunakan bantuan kertas indikator pH (pH
stick) dengan cara memasukkannya ke dalam sediaan dan membandingkan warna
dengan standar.
b. Uji Viskositas
Uji viskositas dilakukan satu kali setelah 24 jam pembuatan mikroemulsi
dengan menggunakan alat Viscotester Rion seri VT 04 . Ukuran rotor yang
digunakan adalah 3. Data yang didapat kemudian dikonversi ke dalam cP
(centipoise).
c. Uji Pengukuran droplet size
Ukuran droplet size dilakukan dengan menggunakan alat DeltaTM Nano
Beckman Coulter pada suhu 25ºC.
d. Cycling Test
Sediaan disimpan pada suhu 4ºC ± 2ºC selama 24 jam kemudian
dikeluarkan dan ditempatkan di suhu 40ºC ± 2ºC selama 24 jam. Perlakuan ini
merupakan perlakuan satu siklus. Percobaan diulang hingga enam siklus. Stabilitas
mikroemulsi dievaluasi selama percobaan dengan melihat ada tidaknya endapan
5. Uji Permeasi menggunakan Franz Diffusion Cell Modifikasi
a. Pembuatan PBS pH 7,4 konsentrasi 0,15 M (sebagai medium kompartemen aseptor)
Aquabidest 200 mL dimasukkan dalam gelas beker 500 mL, kemudian
ditambahkan 2,0454 g NaCl, 8,6596 g Na2HPO4, dan 5,3075 g KH2PO4 diaduk
dengan pengaduk magnetik hingga larut sempurna. Derajat keasaman larutan
diukur dengan pH meter, dan pH larutan dibuat 7,4 dengan penambahan Na2HPO4
0,1 M tetes demi tetes. Larutan dipindahkan dalam labu takar 250 mL, kemudian
ditambahkan aquabidest sampai tanda.
b. Pembuatan NaCl 0,9 % Fisiologis
Sebanyak 9 gram NaCl ditimbang dan dilarutkan dalam 1 L aquadest steril
. larutan kemudian dihomogenkan dan disterilisasikan pada metode sterilisasi panas
basah menggunakan autoklaf dengan suhu sterilisasi 121 ºC selama 15 menit.
c. Preparasi sel difusi dengan membran kulit mencit
Mencit betina galur Swiss usia 1,5-2,5 bulan dimasukkan dalam chamber
jenuh kloroform hingga mati dan dikerjakan dalam lemari asam. Mencit yang sudah
mati dibedah untuk diambil kulit bagian punggungnya. Lemak yang menempel
dibersihkan dengan scalpel, rambut dibersihkan dengan silet. Kulit yang sudah
bersih dipotong berbentuk lingkaran dengan diameter 1,33 cm, sesuai dengan sel
difusinya. Membran kulit ini dicuci dengan aquadest lalu disimpan dalam NaCl
fisiologis 0,9%. Kulit segar langsung dipasang dalam sel difusi yang sudah berisi
larutan kompartemen aseptor yaitu dapar posfat pH 7,4 sebanyak 26,0 ml . Bagian
d. Uji in-vitro dengan menggunakan Franz-cell Modifikasi
Ambil 1 gram mikroemulsi anti-aging lalu diletakkan di bagian stratum
korneum menghadap bagian atas (kompartemen donor). Kompartemen reseptor
mempunyai kapasitas total sebanyak 26 ml dan mempunyai dua lengan.
Kompartemen reseptor mengandung PBS dengan suhu dijaga 37ºC± 1 ºC. Sampel
kemudian diambil dari kompartemen reseptor pada menit ke 0, 60, 120, 180, 300,
hingga 420 menit lalu ganti dengan volume larutan PBS yang sama. Sampel
cuplikan dari kompartemen reseptor kemudian ditambahkan HCl hingga pH ± 5.
Etil asetat sebanyak 1,5 mL kemudian ditambahkan dan dilakukan pemisahan
antara dua fase. Fase atas diambil dan diuapkan hingga mencapai bobot tetap. Fase
atas yang sudah mencapai bobot tetap kemudian ditambahkan etanol p.a sebanyak 1
mL , dimilipore dan dimasukkan ke dalam vial HPLC lalu di-degassing kemudian
diukur dengan menggunakan instrument HPLC pada 261 nm.
6. Analisis Statistik Nilai Fluks Genistein
Data uji permeasi genistein dibuat dalam bentuk kurva hubungan antara
jumlah fluks yang terpenetrasi terhadap waktu. Perhitungan statistik dilakukan
dengan menganalisis data nilai fluks rata-rata hingga menit ke-420 yang
36
BAB IV
HASIL DAN PEMBAHASAN
A. Ekstraksi Tempe
Proses ekstraksi tempe dalam penelitian ini menggunakan tempe yang
didapatkan dari Pasar Demangan Baru untuk menyamakan perlakuan sehingga
tidak didapati hasil ekstrak yang berbeda. Tempe ditimbang sebanyak 1 kg untuk
proses ekstraksi. Penulis melakukan pengecilan ukuran partikel tempe sehingga
proses maserasi berjalan maksimal. Tempe direndam petroleum eter selama 1 jam
dengan perbandingan 1:1 untuk efisiensi proses maserasi. Perendaman dilakukan
untuk menghilangkan komponen non-polar yaitu lemak. Tempe yang sudah
direndam selama 1 jam kemudian disaring dengan corong Buncher dengan bantuan
pompa vakum untuk memastikan tidak ada petroleum eter yang tertinggal pada
tempe dan dilakukan maserasi dengan etanol 96%.
Metode ekstraksi tempe menggunakan metode maserasi dengan pelarut
etanol 96%. Isoflavon dalam tempe sebagian besar terikat dalam bentuk glukosida
sehingga bersifat polar, etanol 96% yang bersifat polar sangat efektif dalam
melarutkan isoflavon tersebut. Etanol 96% sebagai pilihan sangat efektif karena
memiliki toksisitas rendah, murah, dan kompaktibilitas yang baik dengan
Komponen dari tempe yang hendak diekstraksi yakni genistein,
kandungan genisteinpada tempe mempunyai konsentrasi sebesar 7,2 mg dalam 100
gram tempe (Nakajima, Nozaki, Ishihara, Ishikawa, and Tsuji, 2005). Kandungan
genistein pada produk kedelai yang sudah mengalami fermentasi lebih besar
daripada produk kedelai yang tidak mengalami fermentasi karena genistein sudah
dalam bentuk aglikon pada tempe sedangkan pada produk kedelai yang tidak
mengalami fermentasi perlu dilakukan hidrolisis dahulu menggunakan asam kuat
(Rostagno, Villares, Guillamon, Garcia-Lafuente, and Martinez, 2009). Tempe
memiliki kadar aglikon yang lebih besar dibandingkan produk kedelai lainnya
karena adanya enzim penghidrolisis selama proses fermentasi dimana produk
kedelai yang tidak difermentasi mengandung kadar glikosida yang lebih besar.
Ekstrak tempe selanjutnya dipekatkan dengan vacuum rotary evaporator
dengan tekanan rendah selama 60 menit pada suhu 60ºC untuk menguapkan etanol
96% sehingga didapatkan 300 ml ekstrak cair dari 1000 mL larutan yang
dimaserasi. Ekstrak cair yang didapat berwarna kuning kecoklatan. (Lampiran I).
Ekstrak yang sudah dipekatkan kemudian dikeringkan hingga bobot tetap di oven
pada suhu 50-55 ºC, suhu dibawah 50-55 ºC akan menyebabkan adanya jamur atau
kapang pada ekstrak. Tujuan dari pengeringan hingga bobot tetap yaitu untuk
memastikan tidak ada pelarut yang tertinggal dalam ekstrak kental yang dapat
B. Standarisasi Ekstrak Tempe 1. Pembuatan fase gerak
Sistem HPLC yang dilakukan dalam penelitian ini merupakan sistem
HPLC fase terbalik dimana fase gerak bersifat lebih polar dibandingkan dengan
fase diam. Fase diam yang digunakan yakni C18 bersifat kurang polar dan fase
gerak merupakan metanol:air (70:30). Pemilihan fase gerak harus menggunakan
fase gerak yang optimal terkait dengan polaritas fase gerak dengan sampel yang
dapat mempengaruhi pemisahan genistein. Selain itu fase gerak yang dipilih harus
memiliki nilai UV cut off yang cukup jauh dari deteksi sampel. Metanol
mempunyai nilai UV cut off sebesar 205 nm dan aquadest mempunyai nilai UV cut
off sebesar 170 nm (Rohman, 2009), kedua pelarut ini mempunyai nilai UV cut off
yang cukup jauh dari λmaks genistein yakni 261 nm sehingga tidak akan
mengganggu serapan. Genistein memiliki log Kow 2,94 yang merupakan senyawa
hidrofobik, maka digunakan sistem KCKT fase terbalik dimana fase gerak bersifat
lebih polar dibandingkan dengan fase diam sehingga genistein dapat berinteraksi
dengan fase diam. Fase diam C18 sesuai digunakan untuk senyawa genistein yang
memiliki log Kow 2,94 karena adanya ikatan hidrofobik atau van der waals dari
Gambar 8. Struktur Genistein
Bagian cincin benzen (warna hijau) dari genistein merupakan bagian
hidrofobik yang akan berinteraksi dengan fase diam, dan bagian polar (warna
merah) genistein akan berinteraksi dengan fase gerak yang bersifat lebih polar
dibandingkan dengan fase diam sehingga genistein dapat terelusi keluar dari kolom
kemudian dideteksi oleh UV. (Gambar 8)
Waktu retensi pemisahan senyawa tergantung dari kelarutannya dalam
aquadest atau sifat hidrofobisitas isoflavon. Waktu retensi akan semakin meningkat
seiring meningkatnya sifat hidrofobisitas senyawa pada kolom. Senyawa aglikon
mmepunyai nilai retensi yang paling tinggi dibanding β-glukosida,
malonil-glukosida dan asetil-β-glukosida. Waktu retensi dari pemisahan isoflavon dapat
dipengaruhi oleh beberapa faktor seperti afinitas terhadap fase diam, komposisi fase
gerak dan profil gradien elusi (Klejdus, Vacek, Benesova, Kopecky,Lapcik, and
Kuban, 2007).
2. Pembuatan kurva baku
Penelitian ini menggunakan 5 seri konsentrasi baku genistein yaitu 0,1
µg/ml, 0,5 µg/ml, 1 µg/ml, 5 µg/ml dan 10 µg/ml. Larutan baku genistein dibuat
mempunyai kelarutan tinggi dalam pelarut organik dengan sifat polar. Pemilihan
seri konsentrasi ini disesuaikan dengan melihat respon detektor terhadap peak yang
dihasilkan dan juga respon genisteindalam ekstrak tempe dapat masuk dalam range
respon seri larutan baku. Hasil pengukuran respon dari tiap kadar baku genistein
dapat dilihat pada tabel V :
Tabel V. Data Kurva Baku Genistein
Seri Baku (µg/ml) AUC
Kurva baku atau kurva kalibrasi adalah kurva yang menunjukkan hubungan
antara respon instrumen dengan konsentrasi analit pada beberapa seri baku.
Analisis respon instrumen dalam menggunakan HPLC merupakan area under curve
(AUC) dimana y merupakan respon instrumen, x adalah konsentrasi, a adalah
intersep, dan b adalah slope. Kurva baku yang digunakan adalah kurva baku yang
memiliki linearitas yang baik yaitu r mendekati 0,999. Linearitas menyatakan
adanya hubungan respon pengukuran yang secara langsung proporsional terhadap
konsentrasi jumlah analit. Hasil kurva baku menunjukkan nilai r sebesar 0,9989 ,
persamaan kurva baku kemudian digunakan dalam analisis kuantitatif untuk
menentukan konsentrasi suatu analit dalam sampel dengan memasukkan nilai y,
3. Penetapan panjang gelombang maksimum genistein
Penetapan panjang gelombang maksimum genistein bertujuan untuk
mengetahui panjang gelombang dimana genistein memberikan serapan yang
maksimum sehingga hasil yang diperoleh reprodusibel pada pengulangan
pengukuran, memiliki sensitivitas pengukuran yang tinggi, dan meminimalkan
kesalahan dalam pengukuran. Penetapan panjang geombang maksimum ini
dilakukan dengan menggunakan spektrofotometer UV. Genistein memiliki gugus
kromofor yaitu rangkap terkonjungasi pada cincin benzennya dimana ia dapat
memberikan serapan pada daerah sinar ultraviolet sehingga dapat menyerap sinar
pada daerah ultraviolet. Menurut Wu, Wang, and Simon (cit.,Luthria and
Natarajan, 2009) Isoflavon mengabsorpsi spektrum UV pada dua macam range
yakni 245 hingga 275 nm dan 300 dan 330 nm. Pengukuran panjang gelombang
maksimum dilakukan pada rentang panjang gelombang 200-300 nm karena λmaks genisteinberada pada rentang tersebut yakni 261 nm.
Pada penetapan panjang gelombang maksimum dilakukan pada 3 seri
konsentrasi dengan tujuan untuk melihat apakah ketiga konsentrasi yang mewakili
ini dapat menghasilkan spektrum serapan maksimum yang sama. Gambar 10
menunjukkan λmaks genistein berada pada rentang 261 nm pada 3 seri konsentrasi
Gambar 9. Spektra Panjang Gelombang Maksimum Genistein Di 261 nm Menggunakan Spektrofotometer
4. Penetapan Kadar dengan High Perfomance Liquid Chromatography
(HPLC)
a. Analisis Kualitatif
Tujuan analisis kualitatif untuk mengetahui secara pasti puncak (peak)
yang merupakan puncak genistein yang terukur oleh sistem HPLC pada
kromatogram. Analisis ini merupakan langkah awal untuk mengetahui puncak yang
akan digunakan untuk perhitungan AUC. Puncak (peak) dicari yang mempunyai
waktu retensi dan bentuk puncak yang sama dengan puncak pada kromatogram
baku standar genistein dimana bentuk puncak yang serupa menggambarkan profil
kromatografis yang mirip. Waktu retensi antara sampel dan baku menunjukkan
hasil yang hampir serupa dan berkisar antara 5,029-5,270 menit, sedangkan untuk
waktu retensi pada baku didapat 5,237 menit. Faktor yang mempengaruhi
perbedaan waktu retensi antara sampel dengan baku adalah pengaruh dari matriks
sampel yang berbeda sehingga mampu menggeser waktu retensi (Snynder,