PENGARUH VARIASI METODE EKSTRAKSI SECARA
MASERASI DAN DENGAN ALAT SOXHLET TERHADAP
KANDUNGAN KURKUMINOID DAN MINYAK ATSIRI
DALAM EKSTRAK ETANOLIK KUNYIT
(Curcuma domestica Val.)
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh :
Joice Sola Gratia Sitepu NIM : 068114103
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
PENGARUH VARIASI METODE EKSTRAKSI SECARA
MASERASI DAN DENGAN ALAT SOXHLET TERHADAP
KANDUNGAN KURKUMINOID DAN MINYAK ATSIRI
DALAM EKSTRAK ETANOLIK KUNYIT
(Curcuma domestica Val.)
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh :
Joice Sola Gratia Sitepu NIM : 068114103
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi
HALAMAN PERSEMBAHAN
Karya ini hanya kupersembahkan untuk: Yesus Kristus, Tuhan, dan Juruselamatku. Papa dan Mama Bang Icho dan kak Ikka Daveed Teman – temanku Dan teristimewa Almamaterku, Sanata Dharma
Yogyakarta
“Tuhan, ajari aku untuk selalu berserah
kepada-MU untuk langkah apapun yang kuambil demi
masa depanku, aku percaya ada rencana Tuhan
yang indah bagiku, aku percaya janji-Mu
Tuhan.”
Tetapi buah Roh ialah….
vii PRAKATA
Terpujilah nama Tuhan kita Yesus Kristus, karena begitu besar Kasih-Nya kepada penulis sehingga penulis dapat menyelesaikan skripsi yang berjudul ”Pengaruh Variasi Metode Ekstraksi Secara Maserasi dan Dengan Alat Soxhlet Terhadap Kandungan Kurkuminoid dan Minyak Atsiri Dalam Ekstrak Etanolik Kunyit”.
Pada kesempatan kali ini, penulis mengucapkan terimakasih yang amat sangat dalam atas bantuan yang diberikan kepada penulis baik bantuan secara moril maupun materiil kepada :
1. Erna Tri Wulandari M.Si., Apt. selaku Dosen Pembimbing yang dengan sabar membimbing, memberikan waktu luangnya untuk memberi saran dan kritik sejak awal penelitian, penyusunan proposal hingga selesainya skripsi ini. 2. Dr. C. J. Soegihardjo, Apt. selaku Dosen Penguji yang telah meluangkan waktu
untuk menguji serta memberi kritik dan saran yang membangun.
3. Lucia Wiwid Wijayanti, M. Si., selaku Dosen Penguji yang telah meluangkan waktu untuk menguji serta memberi kritik dan saran yang membangun.
x INTISARI
Rimpang tanaman kunyit (Curcuma domestica Val.) telah digunakan secara turun temurun oleh masyarakat Indonesia sebagai obat tradisional. Senyawa aktif dalam rimpang kunyit yang sering digunakan sebagai obat tradisional adalah kurkuminoid sebagai antiinflamasi dan minyak atsiri berkhasiat mencegah keluarnya asam lambung yang berlebihan.
Penelitian ini merupakan penelitian quasi eksperimental yaitu untuk membandingkan kadar kurkuminoid dan minyak atsiri dalam kunyit yang diperoleh secara maserasi dan dengan alat Soxhlet sehingga penelitian ini dapat membantu produsen obat tradisional yang menggunakan kunyit sebagai bahannya untuk memperoleh senyawa kurkuminoid dan minyak atsiri secara maksimal.
Ekstrak rimpang kunyit diekstraksi dengan dua jenis metode yaitu maserasi dan dengan alat Soxhlet menggunakan penyari etanol, kemudian dikentalkan dengan rotary vacuum evaporator. Kadar kurkuminoid kemudian ditetapkan dengan spektrofotometer visible sedangkan kadar minyak atsiri ditetapkan dengan destilasi Stahl dalam % v/b.
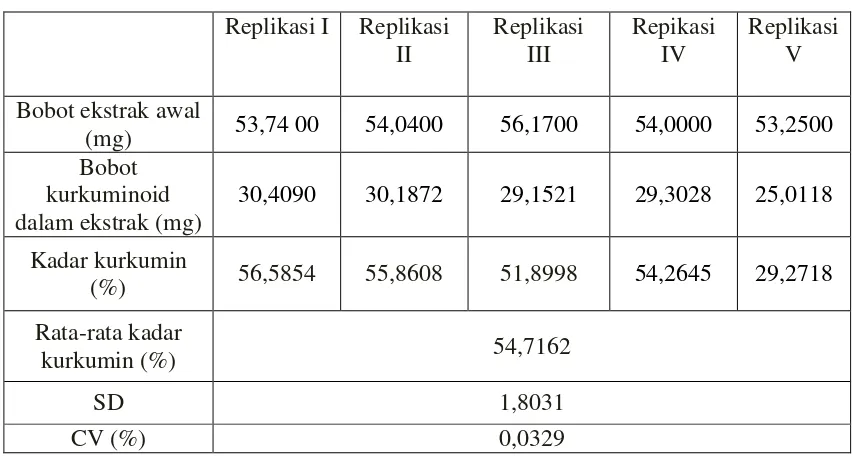
Hasil dari penelitian ini diperoleh kadar kurkuminoid 46,2636% dari metode maserasi, dan 54,7162% dari metode dengan alat Soxhlet, kemudian diperoleh juga kadar minyak atsiri 17,2210% dari metode maserasi, dan 19,3105% dari metode dengan alat Soxhlet. Sehingga diperoleh kesimpulan dari uji T bahwa metode ekstraksi dengan alat Soxhlet adalah metode yang terbaik untuk memperoleh kadar kurkuminoid karena berbeda signifikan dengan metode maserasi, dan untuk minyak atsiri dapat digunakan kedua metode ekstraksi karena tidak berbeda signifikan.
xi ABSTRACT
Rhizome turmeric plant (Curcuma domestica Val.) have been used from generation to generation by Indonesian society as a traditional medicine. Active compounds in the rhizome of turmeric, which is often used as traditional medicine is curcuminoid as anti-inflammatory and essential oils efficacious to prevent the release of excessive stomach acid.
This is a quasi-experimental research to compare the content of curcuminoid in turmeric and essential oils obtained by maceration and with tool of Soxhlet. The aim is to help the producers of traditional medicines to obtain the maximum curcuminoid and essential oils.
The rhizome of turmeric was extracted with two kinds of methods such as maceration and with tool of Soxhlet using ethanol then thickened with a rotary vacuum evaporator. Curcuminoid then determined by visible spectrophotometer and essential oils levels set by distillation Stahl in % v/b.
The results are curcuminoid obtained from the maceration method 46.2636%, and with Soxhlet tool method 54.7162%. The essential oils content obtained from the maceration method is 17.2210% and with Soxhlet tool method is 19.3105%. The t-test result shows that the with Soxhlet tool extraction method is the best method to obtained curcuminoid from turmeric. The essential oils can use both extraction methods.
xii DAFTAR ISI
HALAMAN SAMPUL .…...………... i
HALAMAN JUDUL ………... ii
HALAMAN PERSETUJUAN PEMBIMBING ……… iii
HALAMAN PENGESAHAN………... iv
HALAMAN PERSETUJUAN PUBLIKASI... v
HALAMAN PERSEMBAHAN……… vi
PRAKATA ………. vii
PERNYATAAN KEASLIAN KARYA....………... ix
INTISARI………... x
ABSTRACT………... xi
DAFTAR ISI ………... xii
DAFTAR TABEL ………... xvii
DAFTAR GAMBAR ………. xx
DAFTAR LAMPIRAN……….. xxii
DAFTAR SINGKATAN……… xxiv
BAB I. PENDAHULUAN ………. 1
A. Latar Belakang ………... 1
1. Rumusan masalah ………... 6
2. Keaslian penelitian..………. 6
3. Manfaat penelitian ….………... 7
B. Tujuan Penelitian .………... 7
BAB II. TINJAUAN PUSTAKA ……….. 8
A. Uraian Kunyit ………... 8
1. Keterangan botani... 8
2. Uraian rimpang kunyit... 9
3. Kandungan kimia... 10
4. Khasiat dan kegunaan... 10
B. Uraian Kurkuminoid ……….. 11
xiii
D. Penyulingan Minyak Atsiri ………. 15
1. Penyulingan dengan air……… 15
2. Penyulingan dengan air dan uap……….. 16
3. Penyulingan dengan uap……….. 16
E. Uraian Metode Ekstraksi ……… 17
1. Tujuan ekstraksi ………. 17
2. Jenis – jenis ekstraksi ………. 17
a. Cara dingin……….. 17
b. Cara panas………... 18
3. Uraian maserasi………... 19
4. Uraian dengan alat Soxhlet……….. 20
5. Cairan penyari………. 22
a. Kriteria cairan penyari……… 22
b. Etanol……….. 22
F. Uraian Ekstrak ………... 23
1. Definisi ekstrak ………... 23
2. Pengelompokan ekstrak ……….. 23
3. Ekstrak kunyit……….. 24
G. Penguapan Ekstrak Cair……….. 24
H. Uraian Spektrofotometri …..……….. 25
I. Validasi Metode .……… 26
1. Akurasi……… 26
2. Presisi……….. 26
3. Linieritas dan rentang………. 27
4. Spesifisitas………... 27
5. Limit of Detection dan Limit of Quantitation..……….…… 28
J. Keterangan Empiris……….... 28
BAB III. METODOLOGI PENELITIAN ………..………... 30
A. Jenis dan Rancangan Penelitian ...………... 30
1. Jenis penelitian.. ………...…….. 30
xiv
B. Variabel dan Definisi Operasional ………. 31
1. Klasifikasi variabel………..………. 31
a. Variabel bebas………. 31
b. Variabel tergantung………. 31
c. Variabel pengacau tidak terkendali... 31
d. Variabel pengacau terkendali... 31
2. Definisi operasional………. 31
a. Maserasi………..………. 31
b. Dengan alat Soxhlet………... 32
c. Ekstrak kunyit maserasi………... 32
d. Ekstrak kunyit dengan alat Soxhlet..………..………. 32
e. Penetapan minyak atsiri……….. 32
f. Penetapan kadar kurkuminoid dalam ekstrak rimpang kunyit… 32 g. Pengaruh variasi metode ekstraksi………..……… 33
C. Bahan atau Materi Penelitian .………... 33
D. Alat atau Materi Penelitian……… 33
E. Jalannya Penelitian ……….…..……….. 33
1. Identifikasi rimpang kunyit...…………..……… 34
2. Pembuatan simplisia ...……….. 34
a. Pengumpulan bahan……… 34
1) Sortasi basah………. 34
2) Pencucian………. 34
3) Perajangan……… 35
4) Pengeringan………. 35
5) Sortasi kering……… 35
6) Pembuatan serbuk simplisia……….. 35
b. Pembuatan ekstrak rimpang kunyit...……….. 36
1) Metode maserasi……….... 36
2) Metode dengan alat Soxhlet……….. 36
c. Pengentalan ekstrak rimpang kunyit... 37
xv
e. Penetapan kadar kurkuminoid yang dihitung dalam persen
kurkumin……….. 37
1) Pembuatan larutan stok……….. 37
2) Pembuatan larutan intermediet……….. 37
3) Penetapan panjang gelombang maksimum (λ maks)……… 37
4) Validasi metode……… 38
a) Akurasi……… 38
b) Presisi……….. 39
c) Linieritas dan rentang……….. 39
d) Spesifisitas………..………. 39
e) Limit of Detection dan Limit of Quantitation..………… 40
5) Pembuatan kurva baku……….. 40
6) Penetapan kadar kurkuminoid dalam sampel……… 41
f. Analisa data………..………... 41
BAB IV. HASIL DAN PEMBAHASAN ……….…..……… 42
A. Identifikasi Rimpang Kunyit………...……….…..………….... 42
1. Organoleptik………. 42
2. Makroskopis………. 43
3. Mikroskopis……….. 44
B. Pembuatan Simplisia ……….…..………... 45
1. Pengumpulan rimpang kunyit……….. 45
2. Sortasi basah ……….…..……… 45
3. Pencucian rimpang kunyit.………... 46
4. Perajangan rimpang kunyit ………. 46
5. Pengeringan rimpang kunyit .………... 47
6. Sortasi kering ……….…..………... 48
7. Pembuatan serbuk ……….…..……… 48
C. Cara Maserasi ……...…..………... 49
D. Cara Dengan Alat Soxhlet…..………. 51
E. Pengentalan Ekstrak Rimpang Kunyit.………... 52
xvi
G. Penetapan Kadar Kurkuminoid dengan Spektrofotometri Visible…….. 55
1. Penetapan panjang gelombang maksimum (λ maks)……… 56
2. Validasi metode……… 56
a. Akurasi………...………. 57
b. Presisi……….………. 57
c. Linearitas………. 58
d. Spesifisitas……….……….. 59
e. Limit of Detection dan Limit of Quantitation..……… 59
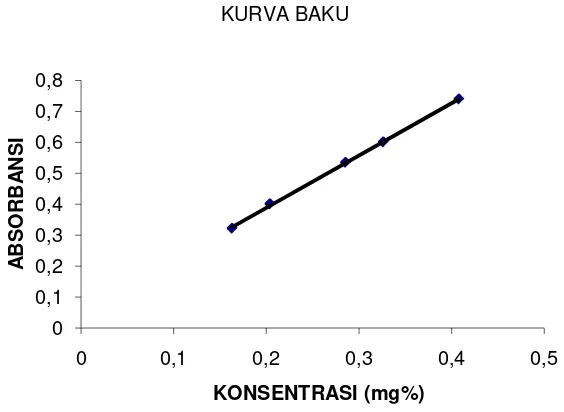
3. Pembuatan kurva baku………. 60
4. Penetapan kadar kurkuminoid dalam sampel……….. 61
BAB V. KESIMPULAN DAN SARAN…..………. 68
A. Kesimpulan .…..………. 68
B. Saran .…..………... 68
DAFTAR PUSTAKA .…..………. 69
LAMPIRAN .…..……… 75
xvii
DAFTAR TABEL
Tabel I. Data perbandingan organoleptik rimpang kunyit dan Materia Medika Indonesia………... 42 Tabel II. Data perbandingan makroskopik rimpang kunyit dan
Materia Medika Indonesia... 43 Tabel III. Data hasil penetapan kadar minyak atsiri metode ekstraksi
maserasi... 55 Tabel IV. Data hasil penetapan kadar minyak atsiri metode ekstraksi
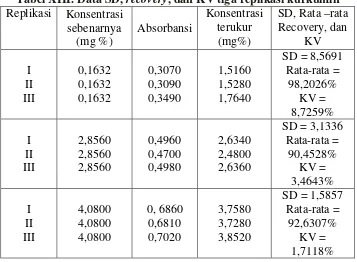
dengan alat Soxhlet... 55 Tabel V. Hasil rata–rata recovery tiga konsentrasi kurkumin
penentuan akurasi………... 57 Tabel VI. Hasil rata – rata tiga konsentrasi kurkumin penentuan
koefisien variasi... 58 Tabel VII. Data penentuan persamaan kurva baku………... 60 Tabel VIII. Data penetapan kadar kurkuminoid ekstrak hasil maserasi. 65 Tabel IX. Data penetapan kadar kurkuminoid ekstrak hasil dengan
alat Soxhlet... 66 Tabel X. Data penimbangan ekstrak rimpang kunyit metode
ekstraksi maserasi... 76 Tabel XI. Data penimbangan ekstrak rimpang kunyit metode
xviii
tiga replikasi kurkumin...
Tabel XIV.
Data Limit of Detection dan Limit Of Quantification
kurkumin………... 81 Tabel XV. Data bobot ekstrak orientasi metode ekstraksi maserasi... 81
Tabel XVI. Data bobot ekstrak orientasi metode ekstraksi dengan alat Soxhlet... 82 Tabel XVII. Data bobot ekstrak replikasi I metode ekstraksi maserasi... 83
Tabel XVIII. Data bobot ekstrak replikasi II metode ekstraksi maserasi.. 83
Tabel XIX. Data bobot ekstrak replikasi III metode ekstraksi maserasi.. 84
Tabel XX. Data bobot ekstrak replikasi IV metode ekstraksi maserasi.. 84
Tabel XXI. Data bobot ekstrak replikasi V metode ekstraksi maserasi... 85
Tabel XXII. Data bobot ekstrak replikasi I metode ekstraksi dengan lat Soxhlet... 86 Tabel XXIII. Data bobot ekstrak replikasi II metode ekstraksi dengan
alat Soxhlet... 86 Tabel XXIV. Data bobot ekstrak replikasi III metode ekstraksi dengan
alat Soxhlet... 87 Tabel XXV. Data bobot ekstrak replikasi IV metode ekstraksi dengan
Alat Soxhlet... 87 Tabel XXVI. Data bobot ekstrak replikasi V metode ekstraksi dengan
xix
xx
DAFTAR GAMBAR
Gambar 1. Struktur molekul kurkuminoid……….. 12 Gambar 2. Penampang rimpang kunyit dan irisannya……… 43 Gambar 3. Penampang melintang sampel rimpang kunyit... 44 Gambar 4. Penampang melintang rimpang kunyit Materia Medika 44 Gambar 5. Grafik kurva baku kurkumin…...…………... 61 Gambar 6. Gugus kromofor dan auksokrom senyawa kurkumin…... 62 Gambar 7. Surat jaminan keaslian kurkumin………... 91 Gambar 8. Alat maserasi………... 92
Gambar 9. Alat Soxhlet……… 92
Gambar 10. Ekstrak hasil maserasi (kanan) dan ekstraksi hasil
sokletasi (kiri)………... 92 Gambar 11. Destilasi Stahl………... 92 Gambar 12. Larutan standar kurkumin... 93 Gambar 13. Panjang gelombang maksimum kurkumin (λmax) 93
replikasi 1 kadar 0,1632 mg%... Gambar 14. Panjang gelombang maksimum kurkumin (λmax
94 )
replikasi 1 kadar 0,2856 mg%... Gambar 15. Panjang gelombang maksimum kurkumin (λ max.)
replikasi 1 kadar 0,4080 mg%... 94 Gambar 16. Panjang gelombang maksimum kurkumin (λmax)
xxi
replikasi 2 kadar 0,2856 mg%... 95 Gambar 18. Panjang gelombang maksimum (λ max.) replikasi 2
kadar 0,4080 mg%... 96 Gambar 19. Panjang gelombang maksimum (λmax
96 ) replikasi 3 kadar 0,1632 mg%... Gambar 20. Panjang gelombang maksimum kurkumin (λmax
97 ) replikasi 3 kadar 0,2856 mg%... Gambar 21. Panjang gelombang maksimum kurkumin (λ max.)
replikasi 3 kadar 0,4080 mg%... 97 Gambar 22. Absorbansi kurva baku larutan standar kurkumin
replikasi I..…... 98 Gambar 23. Kurva baku kurkumin replikasi I……….. 98 Gambar 24. Absorbansi kurva baku larutan standar kurkumin
replikasi II………. 99 Gambar 25. Kurva baku kurkumin replikasi II………. 99 Gambar 26. Absorbansi kurva baku larutan standar kurkumin
xxii
DAFTAR LAMPIRAN Lampiran 1.
Lampiran 2.
Data pengentalan ekstrak rimpang kunyit... 76 Data bobot ekstrak hasil maserasi dan ekstrak hasil
dengan alat Soxhlet... 76 Lampiran 3 Penetapan kadar minyak atsiri... 77 Lampiran 4.
Lampiran 5.
Perhitungan konsentrasi larutan stok, intermediet, dan
kurva baku kurkumin... 78 Validasi metode dengan menggunakan kurkumin
standar………. 79
Lampiran 6. Lampiran 7.
Orientasi sampel ... 81 Penetapan kadar kurkuminoid dihitung sebagai
persen kurkumin dalam sampel ekstrak rimpang
kunyit... 83 Lampiran 8.
Lampiran 9.
Analisis hasil kadar minyak atsiri dan kurkuminoid
pada sampel ………. 89
Surat pernyataan jaminan keaslian bahan kurkumin
standar hasil sintesis………... 91 Lampiran 10.
Lampiran 11
Alat maserasi dan ekstrak hasil maserasi... 92 Alat dengan alat Soxhlet dan ekstrak hasil dengan
Alat Soxhlet... 92 Lampiran 12.
Lampiran 13.
Alat pengental ekstrak hasil maserasi dan ekstrak
xxiii
Stahl……….. Lampiran 14. Penetapan panjang gelombang maksimum (λmax)
pada larutan kurva baku
………...………… 93
Lampiran 15. Penetapan absorbansi larutan kurva baku dan grafik
xxiv
DAFTAR SINGKATAN
EHM = Ekstrak Hasil Maserasi
EHS = Ekstrak Hasil dengan alat Soxhlet EK = Ekstrak Kental
EKM = Ekstrak Kental Maserasi EKS = Ekstrak Kental Sokletasi KV = Koefisien Variansi LOD = Limit of Detection LOQ = Limit of Quantitation
MA = Minyak Atsiri
MEM = Metode Ekstraksi Maserasi MES = Metode Ekstaksi Sokletasi MMI = Materia MEdika Indonesia RK = Rimpang Kunyit
SD = Simpangan Deviasi
1 BAB I PENDAHULUAN
A. Latar Belakang
Indonesia merupakan Negara yang kaya akan sumber daya alam, terutama tanaman obat. Tanaman obat penggunaannya dapat dalam bentuk segar, tunggal maupun campuran, serta dapat berupa ramuan yang lebih dikenal sebagai obat tradisional. Berdasarkan pengalaman nenek moyang obat tradisional relatif aman dikonsumsi manusia. Meskipun demikian pembuktian ilmiah tetap diperlukan (Suharmiati dan Handayani, 2006).
Undang-undang nomor 23 tahun 1992 menyebutkan bahwa obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral atau campuran dari bahan tersebut yang secara turun-temurun telah digunakan untuk pengobatan berdasarkan pengalaman (Anonim, 1992).
Berdasarkan hasil survei tahun 2003, kebutuhan RK berdasarkan jumlahnya yang diserap oleh industri obat tradisional di Jawa Timur menduduki peringkat pertama dan di Jawa Tengah termasuk lima besar bersama-sama dengan bahan baku obat lainnya (Kemala et al, 2000).
Kunyit (Curcuma domestica Val.) termasuk salah satu tanaman rempah dan obat yang sering dimanfaatkan untuk menyembuhkan berbagai penyakit. Sebagian besar jamu yang beredar di Indonesia, Malaysia, dan beberapa Negara lain selalu menggunakan kunyit sebagai salah satu bahan baku (Nugroho, 1998).
Kunyit sudah digunakan dalam pengobatan tradisional bagi beberapa penyakit misalnya antiinflamasi, alergi dan antibakteri. Bagian tanaman kunyit yang paling banyak digunakan adalah rimpang (Nurfina, 1998). RK juga berkhasiat untuk mengobati sakit perut, diare, asma, sakit kepala, keputihan, haid tidak lancar, dan sebagai ekspektoran (Duke, 2008).
50-60% dari total kurkuminoid. Kadar total kurkuminoid sering dihitung sebagai presentase kurkumin (Sumiati et al, 2004).
Kurkuminoid tergolong senyawa fenol yang memiliki dua cincin fenol simetris dan dihubungkan dengan satu rantai heptadiena (Suwanto, 1983 yang diacu dalam Sihombing, 2007) sehingga sering dikatakan juga bahwa kurkuminoid termasuk golongan polifenol (Oomah, 2000).
Kunyit mengandung senyawa minyak atsiri (MA) (6%) yang terdiri dari sejumlah monoterpen dan keton seskuiterpen, termasuk zingiberen, kurkumen, α- dan β-turmeron, tumeon, zingiberen, felandren, sabinen, borneol, sineol (Wikipedia, 2007; Anonim, 1999). MA dari RK berkhasiat untuk mencegah keluarnya asam lambung yang berlebihan dan mengurangi peristaltik usus yang terlalu kuat (Tampubolon, 1981). Selain mengandung kurkuminoid seperti yang telah disebutkan (Sumiati et al, 2004), kunyit juga mengandung protein, fosfor, kalium, besi dan vitamin C (Soedibjo, 1998).
Sesuai dengan perkembangan zaman, industri obat –obatan dan obat tradisional maju pesat, sehingga obat tradisional pun telah berhasil membuat sediaan galenik atau pembuatan ekstrak. Pembuatan sediaan ekstrak dimaksudkan agar zat berkhasiat yang terdapat di simplisia terdapat dalam bentuk yang mempunyai kadar yang tinggi dan hal ini memudahkan zat berkhasiat dapat diatur dosisnya. (Anief, 1997).
yang digunakan untuk dapat menghasilkan ekstrak dengan kandungan senyawa aktif yang maksimal.
Ekstraksi merupakan kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair (Anonim, 1986). Metode ekstraksi dibagi menjadi dua jenis, antara lain cara dingin dan cara panas. Metode ekstraksi yang tergolong cara dingin adalah maserasi dan perkolasi sedangkan metode ekstraksi yang tergolong cara panas adalah refluks, dengan alat Soxhlet, digesti, dan infus (Anonim, 2000).
Untuk menunjang peningkatan kualitas ekstrak yang menghasilkan ekstrak dengan kandungan senyawa aktif secara maksimal, maka pada penelitian ini dilakukan ekstraksi RK dengan menggunakan metode pembuatan ekstrak RK secara maserasi dan sokletasi yang akan memberikan hasil yang berbeda, sehingga dari perbedaan tersebut dapat diketahui metode pembuatan ekstrak yang paling baik. Senyawa aktif yang diekstraksi dengan kedua metode ekstraksi tersebut adalah kurkuminoid dan MA sebagai kandungan utama kunyit (Rukmana, 1994).
Maserasi merupakan cara penyarian yang sederhana (Anonim, 1986) bila dibandingkan dengan metode ekstraksi lainnya. Hal ini dikarenakan cara pengerjaannya sederhana dan peralatannya mudah diusahakan, sederhana, dan tidak memerlukan alat khusus (Indraswari, 2008; Runadi, 2007).
mengandung zat aktif yang mudah larut dalam cairan penyari (Anonim, 1986). Remaserasi merupakan bagian dari maserasi. Remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Anonim, 2000).
Pembuatan ekstrak dengan alat Soxhlet digunakan untuk simplisia yang bertekstur lunak dan tidak tahan pemanasan secara langsung karena suhu pemanasan dapat diatur (Utami, 2009).
RK termasuk simplisia yang lunak, mudah diserbuk sehingga halus dan memungkinkan perendaman sehingga metode maserasi cocok untuk mengekstraksi RK. Kandungan kurkuminoid yang terkandung di dalam RK tidak tahan pemanasan secara langsung karena akan terurai sehingga metode dengan alat soxhlet cocok digunakan untuk mengekstraksi RK.
Digunakan metode ekstraksi RK secara maserasi (cara dingin) dan dengan alat Soxhlet (cara panas) untuk mengetahui metode ektraksi terbaik di antara kedua metode ekstraksi tersebut dalam mengekstraksi kurkuminoid dan MA yang terkandung dalam RK setelah kurkuminoid dan MA dari masing- masing metode ekstraksi ditetapkan kadarnya secara spektrofotometri visible pada panjang gelombang yang sesuai (Anonim, 1993). Kadar MA dapat ditentukan dengan membaca jumlah volume MA yang tertampung dalam buret berskala pada rangkaian alat destilasi air dengan metode destilasi Stahl. Kemudian banyaknya MA yang telah dibaca dibuat kadarnya dalam % v/b (Anonim, 2004).
yang dapat menarik hampir sebagian besar senyawa kimia yang terkandung di dalam herba (Runadi, 2007). Pertimbangan lainnya adalah etanol sebagai penyari karena lebih selektif, kapang dan kuman sulit tumbuh, tidak beracun, netral, dan panas yang diperlukan untuk pemekatan relatif lebih sedikit (Anonim, 1986), juga etanol tidak menyebabkan pembengkakan membran sel dan mampu mengendapkan albumin dan menghambat kerja enzim (Voigt, 1994).
Parameter kadar kurkuminoid yang baik dalam RK adalah 33,9% dan MA kunyit 3,2% (Anonim, 2004). Berdasarkan hal tersebut diharapkan RK penelitian ini baik dengan menggunakan metode ekstraksi maserasi (MEM) maupun metode ekstraksi dengan alat Soxhlet (MES) mengandung kurkuminoid dan MA sesuai dengan parameter yang baik pada Anonim, 2004.
1. Rumusan masalah
a. Adakah pengaruh metode yaitu maserasi dan dengan alat Soxhlet terhadap kadar kurkuminoid dalam ekstrak etanolik RK?
b. Adakah pengaruh variasi metode yaitu maserasi dan dengan alat Soxhlet terhadap kadar MA dalam ekstrak etanolik RK?
2. Keaslian penelitian
Sepanjang kepustakaan yang ditelusuri belum banyak diperoleh keterangan penelitian tentang pengaruh cara ekstraksi maserasi dan dengan alat Soxhlet terhadap kandungan kurkuminoid dan MA dalam ekstrak RK.
Dibuat Secara Maserasi Dan Perkolasi (Kartika Noor Endah, 1998), dan Ekstraksi Kurkumin Dari Kunyit (Wahyuni, A. Hardjono, dan Paskalina Hariyantiwasi Yamrewav, 2004).
3. Manfaat penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan sumbangan ilmiah bagi perkembangan ilmu pengetahuan yang menunjang obat tradisional khususnya dalam bidang pembuatan sediaan galenika untuk produsen obat tradisional dalam memperoleh kandungan kurkuminoid dan MA yang tinggi.
b. Manfaat praktis
Dari penelitian ini akan diketahui metode ekstraksi RK yang paling baik dalam memperoleh kandungan kurkuminoid dan MA secara maksimal.
B. Tujuan Penelitian
1. Tujuan umum
Dapat dipilih metode ekstraksi untuk mendapatkan ekstrak RK yang paling baik di antara kedua metode ekstraksi, yaitu maserasi dan dengan alat soxhlet.
2. Tujuan khusus
BAB II
TINJAUAN PUSTAKA
A. Uraian Kunyit 1. Keterangan botani
Kunyit merupakan tanaman obat berupa semak dan bersifat tahunan (perenial) yang tersebar di seluruh daerah tropis. Tanaman kunyit tumbuh subur dan liar di sekitar hutan/bekas kebun. Tanaman ini banyak dibudidayakan di Asia Selatan khususnya di India, Cina Selatan, Taiwan, Indonesia (Jawa), dan Filipina (Anonim, 2006).
Kunyit merupakan herba yang memiliki terklasifikasi sebagai berikut : Divisio : Spermatophyta
Subdivisio : Angiospermae Classis : Monocotyledonae Ordo : Zingiberales Familia : Zingiberaceae
Spesies : Curcuma domestica Valleton
Sinonim : Curcuma longa Linn; Amomum curcuma Jacq; Stissera curcuma Raevsch; Curcuma domestica Rumph; Curcuma longa Auct; Amomum Curcuma Murs (Anonim, 2006). Kunyit memiliki sebutan berbeda dimasing-masing daerah. Beberapa nama yang digunakan untuk menyebut Kunyit adalah sebagai berikut.
c. Nama daerah : Kakunye (Sumatera), Kunir (Jawa Tengah), Jange henda (Kalimantan), Kunyit (Nusa Tenggara), Uinida (Sulawesi), Kurlai (Maluku), Rame (Irian), Koneng (Sunda) (Anonim, 1985).
2. Uraian rimpang kunyit
RK adalah rimpang Curcuma domestica Valleton (Anonim, 1977). Pemerian. Bau khas aromatik; rasa agak pahit, agak pedas, lama kelamaan menimbulkan rasa tebal (Anonim, 1977).
Makroskopik. Kepingan : Ringan, rapuh, warna kuning jingga, kuning jingga kemerahan sampai kuning jingga kecoklatan; bentuk hampir bundar sampai bulat panjang, kadang–kadang bercabang; lebar 0,5 cm sampai 3 cm, panjang 2 cm sampai 6 cm, tebal 1 mm sampai 5 mm (Anonim, 1977).
3. Kandungan kimia
Zat warna curcuminoid suatu senyawa diarylheptanoide 3 – 4% terdiri dari curcumin, desmetoxycurcumin dan bidesmethoxy-curcumin. MA 2-5% terdiri dari seskuiterpen dan turunan phenylpropane yang meliputi turmeron, ar-turmeron, alfa dan beta ar-turmeron, curlon, curcumol, atlanton, turmerol (minyak turmerin yang menyebabkan aroma dan wangi kunyit), beta-bisabolen, beta – sesquiterphenalendren, zingiberen, ar-curcumen, humulen, arabinosa, fruktosa, glukosa, pati, tanin dan damar serta mineral, yaitu Mg, Mn, Fe, Cu, Ca, Na, K, Pb, Zn, Co, Al, dan Bi (Sudarsono, 1996).
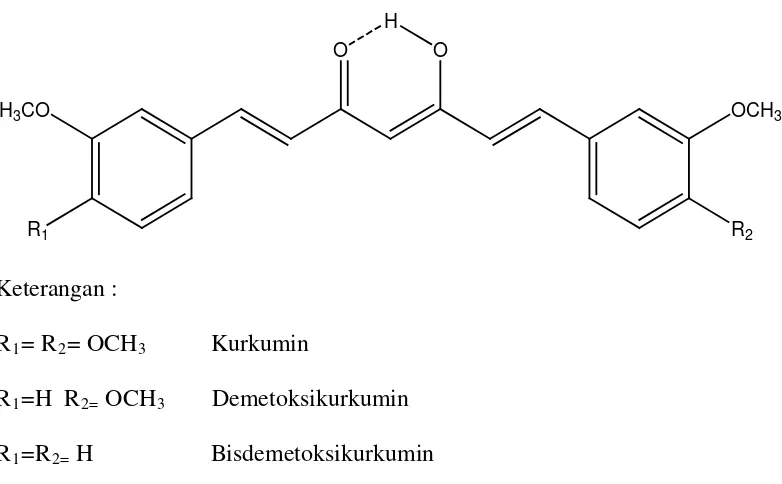
Ada pula literatur yang mengatakan bahwa kunyit mengandung senyawa MA (6%) yang terdiri dari sejumlah monoterpen dan keton seskuiterpen, termasuk zingiberen, kurkumen, tumeon, felandren, sabinen, borneol, sineol, selain yang telah dijelaskan oleh Sudarsono, 1996 (Wikipedia, 2007). Basis warna kunyit (5%) disebabkan adanya kurkuminoid, 50 – 60% merupakan campuran dari kurkumin, monodesmetoksikurkumin, dan bisdemetoksikurkumin (Anonim, 1999), kunyit juga mengandung protein, fosfor, kalium, besi, dan vitamin C (Soedibjo, 1998).
4. Khasiat dan kegunaan
meningkatkan aktivitas seksual (Winarto, 2003). Khasiat kunyit lainnya, yaitu sebagai penawar racun (antidota), penguat lambung dan penambah nafsu makan (Rukmana, 2004).
B. Uraian Kurkuminoid
Kunyit memiliki senyawa yang berkhasiat obat yang disebut dengan kurkuminoid. Kurkuminoid adalah senyawa yang memberikan warna kuning pada kunyit (Chattopadhyay et al, 2004 ; Sumiati et al, 2004; Dandekar dan Kaikar, 2002) oleh sebab itu kurkuminoid (kebanyakan berupa kurkumin) banyak menjadi pusat peneliti (Dandekar et al, 2002). Kurkuminoid terdiri atas kurkumin sebanyak 50 – 60%, desmetoksikurkumin, dan bidesmetoksikurkumin (Anonim, 1999). Kurkumin merupakan komponen terbesar dari kurkuminoid sehingga sering kadar total kurkuminoid dihitung sebagai % kurkumin (Sumiati et al, 2004). Kurkumin murni sangat sulit diperoleh langsung dari RK karena seringkali tercampur dengan dua turunannya, yaitu demetoksikurkumin dan bisdemetoksikurkumin (Donatus, 1994).
Kurkumin merupakan senyawa kandungan utama tanaman kunyit (Curcuma longa L.) terdapat juga dalam tanaman temulawak (Curcuma xanthorrhiza, Roxb.) dan pada tanaman temugiring (Curcuma heyneana, Val. & Ziep.) (familia Zingiberaceae) (Tonnesen, 1989; Masuda, Isobe, Jitoe, dan Nakatani, 1992; Masuda et al, 1993; van der Goot, 1997).
Karlsen, 1983; Wikipedia, 2007). Kurkumin tergolong senyawa diarilheptanoid dengan rumus molekul C21O6H2
Pertama kali kurkumin ditemukan pada tahun 1815 oleh Vogel dan Pelletier (van der Goot, 1997). Kristalisasi kurkumin pertama kali dilakukan oleh Daube pada tahun 1870 dan elusidasi struktur kimia dilakukan pada tahun 1910 oleh Lampe. Sintesis kurkumin pertama kali dilakukan oleh Lampe dan Milobedzka pada tahun 1913 (Roughly and Whiting, 1973). Struktur kimia terlihat pada gambar sebagai berikut.
O (Tonnesen et al, 1985).
Gambar. I Struktur molekul kurkuminoid (Roughly et al, 1973) H Bisdemetoksikurkumin
yang menyebabkan terjadinya degradasi fotokimia senyawa tersebut (van der Goot, 1997; Supardjan, dan Meiyanto, 2002) dan oleh sinar ultraviolet (Bermawie, et al., 2005).
Kurkumin larut dalam asam asetat glasial, alkohol, (Windholz, 1981; Tarujaya, 1992) dan aseton (Joe, Vijaykumar, Lokesh, 2004; Chattopadhyay et al, 2004; Araujo dan Leon, 2001) tetapi tidak dapat larut dalam air, eter (Windholz, 1981; Tarujaya, 1992).
Kurkuminoid mempunyai aktivitas antiinflamasi (Timmerman, 1995; Kohli, 2005). Kurkuminoid menghambat senyawa eicosanoid seperti prostaglandin, tromboksan dan prostasiklin dengan cara menghambat aktivitas enzim cyclooxygenase (COX). Kurkuminoid juga menghambat pembentukan senyawa leukotrien dengan menghambat aktivitas enzim lipoxygenase (LOX) (Kohli, 2005). Dari tiga senyawa kurkuminoid, kurkumin mempunyai aktivitas antiinflamasi yang paling kuat dibandingkan senyawa turunannya (Agnam, Samhoedi, Timmerman, Venie, Sugiyanto, Goot, 1995; Bermawie, 2006; Hadi, 1985; Majeed, Badmaev, Shivakumar, Rajendran, 1995; Punithavathi, Venkatesan, Babu, 2000; Siddiqui, Cui, Wu, Dong, Zhou, Hu, Simms, Wang, 2006; Goot, 1997).
sering disebut sebagai senyawa polifenol (Madigan, 2005; Oomah, 2000; Wikipedia, 2007).
Kurkumin yang bercampur dengan kedua turunannya yang juga berwarna kuning yaitu bisdemetoksikurkumin dan desmetoksikurkumin ditetapkan sebagai kadar kurkuminoid dengan menggunakan spektrofotometri visible (Anonim, 1977; Anonim, 1993).
C. Uraian Minyak Atsiri
MA merupakan salah satu hasil proses metabolisme dalam tanaman (Anonim, 1985). MA adalah zat berbau yang terdapat dalam berbagai bagian tanaman, karena menguap bila dibiarkan di udara pada suhu kamar, maka disebut minyak menguap, minyak eteris, atau minyak esensial (Claus, 1959).
MA terdapat pada bagian khusus tanaman, tergantung pada tanaman tersebut. Pada tumbuhan Zingiberaceae MA terdapat dalam sel –sel rimpang. Kunyit merupakan salah satu tumbuhan Zingiberaceae sehingga bagian rimpangnya yang digunakan untuk mengambil MA (Tyler, Brady, Robbers, 1988).
Kunyit mengandung MA 2-5% terdiri dari seskuiterpen dan turunan phenylpropane yang meliputi turmeron, ar-turmeron, alfa dan beta turmeron, curlon, curcumol, atlanton, turmerol (minyak turmerin yang menyebabkan aroma dan wangi kunyit), beta-bisabolen, beta – sesquiterphenalendren, zingiberen, ar-curcumen, humulen, Arabinosa, fruktosa, glukosa, pati, tanin dan damar serta mineral, yaitu Mg, Mn, Fe, Cu, Ca, Na, K, Pb, Zn, Co, Al, dan Bi (Sudarsono, 1996).
MA kunyit memiliki berat jenis 0,941, rotasi optik pada suhu 20°C adalah -190.18, indeks bias pada suhu 20°C adalah 1.5025. Warna MA kuning dan mempunyai bau yang khas dan rasa pedas (Guenther, 1952).
MA dari RK berkhasiat untuk mencegah keluarnya asam lambung yang berlebihan dan mengurangi peristaltik usus yang terlalu kuat (Tampubolon, 1981).
D. Penyulingan Minyak Atsiri
Sebagian besar MA umumnya diperoleh dengan cara penyulingan. Penyulingan didefinisikan sebagai pemisahan komponen–komponen suatu campuran dari dua jenis cairan atau lebih berdasarkan perbedaan tekanan uap dari masing –masing zat (Guenther, 1948).
Pada industri MA dikenal tiga macam metode penyulingan, yaitu : 1. Penyulingan dengan air
dengan metode pemanasan yang biasa dilakukan, yaitu dengan panas langsung, mantel uap, pipa uap melingkar terbuka atau berlubang. Ciri khas dari metode ini ialah kontak langsung antara bahan dengan air mendidih (Guenther, 1948).
2. Penyulingan dengan air dan uap
Penyulingan ini dilakukan pada material basah ataupun kering yang bisa rusak karena perebusan. Pada metode penyulingan ini, bahan olah diletakkan di atas rak –rak atau saringan berlubang. Ketel suling diisi dengan air sampai permukaan air berada tidak jauh di bawah saringan. Air dapat dipanaskan dengan berbagai cara yaitu dengan uap jenuh yang basah dan bertekanan rendah. Ciri khas dari metode ini adalah: 1) uap selalu dalam keadaan basah, jenuh dan tidak terlalu panas; 2) bahan yang disuling hanya berhubungan dengan uap dan tidak dengan air panas (Tyler et al, 1988; Guenther, 1948).
3. Penyulingan dengan uap
E. Uraian Metode Ekstraksi
1. Tujuan ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair (Anonim, 1986).
Ekstraksi dilakukan untuk menyari zat –zat berkhasiat atau zat –zat aktif dari bagian tanaman obat, hewan dan beberapa jenis ikan termasuk biota laut. Zat–zat aktif terdapat di dalam sel, namun sel tanaman dan hewan berbeda demikian pula ketebalannya, sehingga diperlukan metode ekstraksi dengan pelarut tertentu dalam mengekstraksinya (Harbone, 1987).
Tujuan ekstraksi bahan alam adalah untuk menarik komponen kimia yang terdapat pada bahan alam. Ekstraksi ini didasarkan pada prinsip perpindahan massa komponen zat ke dalam pelarut, dimana perpindahan mulai terjadi pada lapisan antar muka kemudian berdifusi masuk ke dalam pelarut (Anonim, 1986). 2. Jenis – jenis ekstraksi
Metode ekstraksi dengan menggunakan pelarut, terdiri dari : a.
1) Maserasi Cara dingin.
2) Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru, yang umumnya dilakukan pada temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahapan maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali jumlah bahan.
b.
1) Refluks Cara panas
Refluks adalah ekstraksi dengan pelarut pada temperatur pada titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga proses ekstraksi sempurna.
2) Dengan alat Soxhlet
Dengan alat Soxhlet adalah ekstraksi yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinyu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3) Digesti
4) Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur 96-98 C selama waktu 15-20 menit di penangas air, berupa bejana infus tercelup dalam penangas air mendidih (Anonim, 2000).
3. Uraian maserasi
Istilah maceration berasal dari bahasa latin macerare, yang artinya “merendam”. Merupakan proses paling tepat dimana obat yang sudah halus memungkinkan untuk direndam dalam pelarut sampai meresap dan melunakkan susunan sel, sehingga zat –zat yang mudah larut akan melarut (Ansel, 1985).
Maserasi merupakan cara penyarian yang sederhana dan digunakan untuk simplisia yang mengandung zat aktif yang mudah larut dalam cairan penyari. Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari.
Cairan penyari akan menembus dinding sel dan masuk kedalam rongga sel yang mengandung zat aktif. Zat aktif akan larut dan karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dan di luar sel, maka larutan yang pekat didesak keluar. Peristiwa tersebut berlanjut sehingga terjadi keseimbangan konsentrasi antara larutan di luar dan di dalam sel. Cairan penyari yang digunakan dapat berupa air, etanol, air-etanol, atau pelarut lain.
Bila cairan penyari yang digunakan adalah air maka untuk mencegah timbulnya kapang dapat ditambahkan bahan pengawet, yang diberikan pada awal penyarian (Anonim, 1986). Semakin besar perbandingan cairan pengekstraksi terhadap simplisia, akan semakin banyak hasil yang diperoleh (Voigt, 1994).
pengerjaannya lama dan penyariannya kurang sempurna, juga adanya kejenuhan konsentrasi di dalam larutan penyari, di mana konsentrasi di dalam simplisia dengan
di dalam penyari sama (Dinda, 2008).
Pada penyarian dengan cara maserasi perlu dilakukan pengadukan. Pengadukan diperlukan untuk meratakan konsentrasi larutan di luar butir serbuk simplisia, sehingga dengan pengadukan tersebut tetap terjaga adanya derajat perbedaan konsentrasi yang sekecil-kecilnya antara larutan di dalam dengan di luar sel. Hasil penyarian dengan cara maserasi perlu dibiarkan selama waktu tertentu. Waktu tersebut diperlukan untuk mengendapkan zat-zat yang tidak diperlukan tetapi ikut terlarut dalam cairan penyari seperti penyari malam dan lain-lain (Anonim, 1986). Cara ekstraksi maserasi ini dilakukan 3 x 24 jam, hal ini dilakukan supaya senyawa yang terkandung dalam herba tertarik (Runadi, 2007). 4. Uraian dengan alat Soxhlet
Alat Soxhlet adalah suatu suatu alat terbuat dari gelas yang bekerja secara kontinyu dalam menyari. Pada proses ini sampel yang akan disari dimasukkan pada alat Soxhlet, lalu setelah dielusi dengan pelarut yang cocok sedemikian rupa sehingga akan terjadi dua kali sirkulasi dalam waktu 30 menit (Harborne, 1987).
Bahan yang akan diekstraksi diletakkan dalam sebuah kantong ekstrak (kertas, karton, dan sebagainya) di dalam sebuah alat ekstraksi dari gelas yang bekerja kontinyu. Wadah gelas yang berisi sampel diletakkan di antara labu suling dan suatu pendingin aliran balik. Labu tersebut berisi bahan pelarut yang menguap dan mencapai ke dalam pendingin aliran balik melalui pipa pipet, berkondensasi di dalamnya, menetes ke atas bahan yang akan diekstraksi dan membawa keluar bahan yang diekstraksi. Larutan yang terkumpul dalam wadah gelas dan setelah mencapai tinggi maksimal secara otomatis dipindahkan ke dalam labu dengan demikian zat yang akan terekstraksi terakumulasi melalui penguapan bahan pelarut murni berikutnya. Pada cara ini bahan terus diperbaharui artinya dimasukkan bahan pelarut bebas bahan aktif (Voigt, 1971).
Keuntungan dengan alat Soxhlet adalah membutuhkan pelarut yang sedikit dan untuk penguapan pelarut biasanya digunakan pemanasan. Kelemahannya adalah waktu yang dibutuhkan untuk ekstraksi cukup lama sampai beberapa jam, sehingga kebutuhan energinya tinggi dan dapat berpengaruh negatif terhadap bahan tumbuhan yang peka suhu (Voigt, 1971).
5. Cairan penyari a.
Pemilihan cairan penyari harus mempertimbangkan banyak faktor. Cairan penyari yang baik harus memenuhi kriteria berikut ini: murah dan mudah diperoleh, stabil secara fisika dan kimia, bereaksi netral, tidak mudah menguap dan tidak mudah terbakar, selektif yaitu hanya menarik zat yang berkhasiat yang dikehendaki, tidak mempengaruhi zat yang berkhasiat, dan diperbolehkan oleh peraturan (Anonim, 1986).
Kriteria cairan penyari
Pelarut yang digunakan dalam ekstraksi harus dipilih berdasarkan kemampuannya dalam melarutkan kandungan zat aktif yang maksimal dan seminimal mungkin bagi unsur yang tidak diinginkan (Ansel, 1985).
Cairan penyari yang biasa digunakan adalah air, eter atau campuran etanol dan air (Anonim, 1979). Air atau etanol menjadi acuan cairan pengekstraksi, karena banyak bahan tumbuhan larut dengan air atau etanol (Voigt, 1971).
b.
Etanol digunakan sebagai pelarut karena etanol merupakan pelarut yang universal yang dapat menarik hampir sebagian besar senyawa kimia yang terkandung di dalam herba (Runadi, 2007). Etanol tidak menyebabkan pembengkakan membran sel dan memperbaiki stabilitas bahan obat terlarut.
Etanol
Etanol 95% sangat efektif dalam menghasilkan jumlah bahan aktif yang optimal, di mana bahan pengganggu hanya skala kecil yang turut ke dalam cairan pengekstraksi, selain itu ekstrak etanol sulit ditumbuhi kapang dan kuman, dan tidak beracun (Voigt, 1971).
F. Uraian Ekstrak 1. Definisi ekstrak
Ekstrak adalah sediaan yang dapat berupa kering, kental, dan cair (Anonim, 1979) yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian sehingga memenuhi standar baku yang telah ditetapkan (Anonim, 2000). Tujuan pembuatan sediaan ekstrak dimaksudkan agar zat berkhasiat yang terdapat di simplisia terdapat dalam bentuk yang mempunyai kadar yang tinggi (Anief, 1997).
2. Pengelompokan ekstrak
(c) ekstrak kering (extractum siccum) memiliki konsistensi kering dan mudah hancur. Melalui penguapan cairan pengekstraksi dan pengeringan sisanya terbentuk suatu produk, yang mengandung air tidak lebih dari 5%, (d) Ekstrak cair (extractum fluidum), memiliki konsistensi cair dan mudah dituang (Voigt, 1994). 3. Ekstrak kunyit
EK RK adalah ekstrak yang dibuat dari rimpang tumbuhan Curcuma domestica Valetton suku Zingiberaceae, mengandung MA tidak kurang dari 3,2% dan kurkuminoid tidak kurang dari 33,9% (Anonim, 2004).
a. Pemerian :Bentuk: kental; warna: kuning; bau: khas; rasa: agak pahit. b. Identitas :RK memiliki kandungan kimia berupa: kurkumin,
desmetoksikurkumin, bidesmetoksikurkumin, MA, dan oleoresin. Senyawa identitas dari RK adalah kurkumin, desmetoksikurkumin, dan bidesmetoksikurkumin (Anonim, 2004).
G. Penguapan Ekstrak Cair
Penguapan adalah proses terbentuknya uap dari permukaan cairan. Faktor-faktor yang mempengaruhi penguapan adalah suhu, waktu, cara penguapan, dan konsentrasi (Anonim, 1986).
Pengentalan ekstrak cair menggunakan VRE memungkinkan penguapan larutan pengekstraksi yang lebih cepat karena adanya tekanan dan suhu yang diatur tidak terlalu tinggi untuk menjaga stabilitas senyawa (Voigt, 1994). Tujuan ekstrak dikentalkan adalah mempermudah dalam pengukuran dan penimbangan (Anonim, 2000).
H. Uraian Spektrofotometri
Prinsip kerja spektrofotometri adalah berdasarkan atas interaksi antara radiasi elektromagnetik dengan materi. Materi dapat berupa atom, ion, atau molekul, sedang variasi elektromagnetik merupakan salah satu jenis energi yang ditransmisikan dalam ruang dengan kecepatan tinggi. Interaksi antara molekul yang mempunyai gugus kromofor dan radiasi elektromagnetik pada daerah ultraviolet (200 nm-400 nm) dan sinar tampak (400 nm-800 nm) akan menghasilkan spektra serapan elektronik, spektra serapan ini dapat digunakan untuk menganalisis kuantitatif karena jumlah radiasi elektromagnetik yang diserap ada hubungannya dengan jumlah molekul penyerap (Skoog, 1985).
Pada pengukuran serapan suatu larutan selalu diperlukan suatu larutan blanko. Maksud dari larutan blanko adalah untuk mengatur spektrofotometer hingga pada panjang gelombang yang digunakan mempunyai serapan nol (Anonim, 1974).
I. Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Untuk itu diperlukan suatu pedoman mengenai kesahihan metode analisis yang didukung oleh parameter – parameter di bawah ini :
1. Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
2. Presisi
memiliki presisi yang baik apabila memiliki KV < 2% tetapi kriteria ini fleksibel tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi laboratorium (Harmita, 2004).
3. Linieritas dan rentang
Linieritas merupakan kemampuan suatu metode (pada rentang tertentu) untuk mendapatkan hasil uji yang secara langsung proporsional dengan konsentrasi (jumlah) analit dalam sampel. Rentang adalah jarak antara level terbawah dan teratas dari metode analisis yang telah dipakai untuk mendapatkan presisi, linieritas, dan akurasi yang bisa diterima (Harmita, 2004). Persyaratan data linearitas yang bisa diterima jika memenuhi nilai koefisien korelasi (r) > 0,99 atau r2
4. Spesifisitas
≥ 0,997 (Pelczar, Roger, and Chan, 1977).
Spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel. Selektivitas metode ditentukan dengan membandingkan hasil analisis sampel yang mengandung cemaran, hasil urai, senyawa sejenis, senyawa asing lainnya atau membawa placebo dengan hasil analisis sampel tanpa penambahan bahan –bahan tadi. Penyimpangan hasil merupakan selisih dari hasil uji keduanya (Harmita, 2004).
5. Limit Of Detection (LOD) dan Limit Of Quantitation (LOQ)
criteria akurasi dan presisi. LOD dan LOQ dapat dihitung secara statistik melalui garis regresi linier dari kurva kalibrasi. Nilai pengukuran akan sama dengan nilai b pada persamaan garis linier Y = A + BX, sedangkan simpangan baku blangko sama dengan simpangan baku residual (Sy/x), sehingga LOD dan LOQ dapat
dihitung menggunakan rumus : LOD = dan LOQ =
(Harmita, 2004).
J. Keterangan Empiris
RK mempunyai kandungan kimia utama yaitu kurkuminoid dan MA (Rukmana, 2004). Kurkuminoid larut dalam alkohol dan asam asetat glasial, tetapi tidak dapat larut dalam air dan eter (Windholz, 1981; Tarujaya, 1992).
Maserasi merupakan metode penyarian dengan cara menggojog simplisia dan pelarutnya lalu merendamnya selama beberapa waktu (Voigt, 1971), sedangkan dengan alat Soxhlet dilakukan dengan cara mengalirkan cairan penyari secara kontinyu sehingga pelarut menjadi selalu baru ketika melalui kantong ekstrak serbuk simplisia (Voigt, 1971).
dibandingkan MEM hal ini dikarenakan proses ekstraksi dengan dengan alat Soxhlet menggunakan pemanasan dan menggunakan pelarut etanol sehingga kurkuminoid terlarut sempurna (Jacobs, 1944; Lenny, 2006).
Kurkumin murni sulit diperoleh karena sering tercampur dengan turunannya yaitu bisdemetoksikurkumin dan demetoksikurkumin (Donatus, 1994) sehingga untuk analisa kuantitatif ditetapkan kadar kurkuminoid dengan menggunakan spektrofotometri visible (Anonim, 1977; Anonim, 1993). Kurkumin merupakan komponen terbesar dari kurkuminoid sehingga sering kadar total kurkuminoid dihitung sebagai % kurkumin (Sumiati et al., 2004).
MA kunyit memiliki berat jenis 0,941, rotasi optik pada suhu 20°C adalah -190.18, indeks bias pada suhu 20°C adalah 1.5025. Warna MA kuning dan mempunyai bau yang khas dan rasa pedas (Guenther, 1952). MA ditetapkan kadarnya dalam % v/b menggunakan destilasi Stahl (Anonim, 2004).
30 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian 1. Jenis penelitian
Penelitian ini merupakan model rancangan quasi eksperimental yaitu membandingkan kadar kurkuminoid dan MA dalam ekstrak RK dengan variasi metode secara maserasi dan dengan alat Soxhlet sebagai perlakuan. Penelitian ini dilakukan di laboratorium Farmakognosi Fitokimia dan Analisis Instrumental Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Tahapan penelitian
a. Identifikasi RK secara organoleptik, makroskopik, dan mikroskopik b. Pembuatan Simplisia
c. Pembuatan ekstrak RK 1) Ekstraksi dengan metode maserasi
2) Ekstraksi dengan metode dengan alat Soxhlet d. Pengentalan ekstrak RK
e. Penetapan kadar MA dalam ekstrak RK
B. Variabel dan Definisi Operasional 1. Klasifikasi variabel
a.
Metode ekstraksi RK, yaitu maserasi dan dengan alat Soxhlet. Variabel bebas
b.
Kadar kurkuminoid dan MA yang diperoleh dari pengekstrakkan kunyit secara maserasi dan dengan alat Soxhlet.
Variabel tergantung
c.
Umur RK.
Variabel pengacau tidak terkendali
d.
Sumber pembelian RK. Dalam hal ini sumber pembelian RK merupakan variabel pengacau namun dapat dikendalikan karena pembelian RK dilakukan hanya pada satu pedagang di pasar Bringhardjo, sehingga diharapkan bila tanaman kunyit berasal dari satu daerah memiliki kandungan kurkuminoid dan MA yang sama. Bila berbeda daerah asal, maka dapat mempengaruhi kadar kurkuminoid dan MA hal ini dikarenakan adanya perbedaan iklim, suhu tanah, kandungan tanah, keasaman tanah, jenis tanah, umur tanaman, dan faktor lainnya yang dapat mempengaruhi kadar zat aktif tanaman kunyit (Mariastuty, 2002).
Variabel pengacau terkendali
2. Definisi operasional a.
Merupakan metode ekstraksi penggojogan sekaligus perendaman serbuk RK dengan pelarut etanol 95% sebanyak 1000 ml selama 3 x 24 jam dan
setiap 24 jam sekali diganti dengan pelarut etanol 95% sebanyak 1000 ml yang masih baru.
b.
Merupakan metode ekstraksi berkesinambungan karena pelarut selalu baru membasahi sampel. Ekstraksi dihentikan apabila warna pelarut dalam tabung sifon telah bening secara visual.
Dengan alat Soxhlet
c.
Merupakan hasil penyarian serbuk simplisia RK secara maserasi yang telah dikentalkan dengan alat VRE sampai volum ekstrak cairnya seperlima dari volum ekstrak cair semula yang dimasukkan.
Ekstrak kunyit maserasi
d.
Merupakan hasil penyarian serbuk simplisia RK dengan alat Soxhlet yang telah dikentalkan dengan alat VRE sampai volum ekstrak cairnya setengah dari volum ekstrak cair semula yang dimasukkan.
Ekstrak kunyit dengan alat Soxhlet
e.
Merupakan volume MA yang diperoleh dari masing–masing metode ekstraksi yakni maserasi dan dengan alat Soxhlet yang dihasilkan dari setiap bobot penimbangan ekstrak dengan menggunakan destilasi Stahl dan dihitung kadarnya sebagai % v/b.
Penetapan minyak atsiri
f.
Merupakan jumlah total kurkuminoid yang terukur oleh spektrofotometer visible yang telah tervalidasi dengan menggunakan kurkumin baku pada panjang gelombang maksimum 420 nm.
g.
Merupakan perbedaan secara signifikan kadar kurkuminoid dan MA antara hasil MEM dan hasil MES setelah dilakukan uji T.
Pengaruh variasi metode ekstraksi
C. Bahan atau Materi Penelitian
1. Bahan utama yang digunakan adalah ekstrak kental RK yang diperoleh dari hasil ekstraksi RK dengan larutan penyari etanol.
2. Bahan lain yang digunakan antara lain yaitu Aquadest, aseton p.a. (Merck), asam borat p.a.(Merck), asam oksalat p.a., etanol teknis 95% (Merck), dan baku kurkumin yang diperoleh dari PPOT, UGM Yogyakarta.
D. Alat atau Materi Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah blender, ayakan, timbangan analitik, oven, labu berskala, VRE, spektrofotometer UV – Vis SP 3000, pompa vacuum, timbangan, alat-alat gelas, labu alas bulat 1 L, alat Soxhlet, seperangkat maserator, Corong Buchner, dan kertas saring Whatman No. 4.
E. Jalannya Penelitian
1. Identifikasi rimpang kunyit (Anonim, 1977)
Identifikasi dilakukan secara organoleptik, makroskopik, mikroskopik
dengan cara sebagai berikut :
a. Organoleptik : pengawatan warna, bau, dan rasa RK.
b. Makroskopik : pengamatan morfologi RK.
c. Mikroskopik : RK kering direndam dalam air panas sekitar 30 menit, lalu dibuat irisan melintang dan diamati.
2. Pembuatan simplisia (Anonim, 1985):
a.
RK yang digunakan sebagai bahan utama dibeli dari Pasar Bringharjo, Yogyakarta sebanyak 10 kg dari satu orang pedagang. RK yang digunakan sebagai bahan utama karena merupakan bagian tanaman yang paling banyak
digunakan dan di dalamnya banyak mengandung MA dan kurkumin (Nurfina, 1998; Oomah, 2000; Rukmana, 1994).
Pengumpulan bahan
1) Sortasi basah
RK yang telah dibeli sebanyak 10 kg kemudian dipisahkan dari tanah atau pengotor lainnya yang ikut terbawa.
2) Pencucian
Setelah sortasi basah, dilakukan pencucian dengan menggunakan air
3) Perajangan
RK yang telah kering, dirajang dengan pisau stainless steel sehingga diperoleh
irisan tipis dengan ukuran kira-kira 0,5 cm agar rimpang cepat mengering bila djemur.
4) Pengeringan
Irisan tipis RK tersebut lalu dijemur di bawah sinar matahari dengan ditutupi kain hitam agar tidak merusak kandungan dalam RK yang bersifat
fotodegradasi, misalnya kurkuminoid. Irisan tipis dijemur dan tidak lupa untuk dibolak-balik agar pengeringan merata. Pengeringan dihentikan bila irisan RK
kering, yaitu dengan ditandainya irisan RK tersebut mudah dipatahkan. Biasanya lama pengeringan ini berlangsung 1 hari.
5) Sortasi kering
Irisan RK yang telah kering tersebut dipisahkan dari benda-benda asing seperti bagian-bagian tanaman asing lainnya yang tidak diinginkan yang masih
tertinggal.
6) Pembuatan serbuk simplisia
Simplisia kunyit yang telah kering diserbuk dengan mesin penyerbuk dan
diayak dengan ayakan 8/14 sehingga didapatkan serbuk yang homogen. Serbuk kemudian dimasukkan ke dalam wadah yang kedap udara (Anonim, 1985;
b.
1) Metode maserasi
Pembuatan ekstrak rimpang kunyit
Ditimbang 100 g serbuk kering kunyit dan dimasukkan ke dalam maserator ditambah 1,0 L etanol 95 %. Ekstraksi dilakukan selama tiga hari,
setiap 24 jam sekali pelarut diganti dengan pelarut yang baru, prosedur per harinya adalah bahan dalam alat gelas (Erlenmeyer) digojog dengan alat maserasi yang telah diatur untuk menggojog selama 6 jam, kemudian alat dengan otomatis
berhenti, kemudian bahan didiamkan sampai mencapai waktu 24 jam. Setelah itu hasil ekstraksi dimasukkan ke dalam wadah dengan cara disaring dengan kain
katun agar serbuk tidak ikut masuk ke dalam wadah tertentu. Setelah tiga kali penggantian pelarut, hasil ekstraksi yang telah ditampung dalam wadah tertentu yang berwujud ekstrak cair kemudian dikentalkan dengan VRE untuk
mendapatkan ekstrak kental (EK) kunyit. Replikasi dilakukan sebanyak 5 kali. 2) Metode dengan alat Soxhlet
Ditimbang 100 g serbuk kering kunyit dan dimasukkan ke dalam sifon kemudian ditambahkan dengan 2 kali sirkulasi etanol 95 % (total pelarut ±544,6 ml per replikasi). Ekstraksi dilakukan sampai semua kandungan kimia simplisia terekstraksi ditandai dengan jernihnya larutan penyari di dalam tabung sifon, biasanya larutan penyari dalam tabung sifon menjadi jernih bila telah mengalami
c.
Ekstrak cair yang diperoleh dari proses ekstraksi dengan metode maserasi dan dengan alat Soxhlet dikentalkan dengan menggunakan VRE pada suhu 50
Pengentalan ekstrak rimpang kunyit
0 C dan tekanan 72 mbar, kemudian hasil berupa ekstrak cair, dikentalkan menggunakan oven pada suhu 400
d.
C.
Ditimbang 2,0 g ekstrak kental rimpang kunyit dan dimasukkan ke dalam
labu alas bulat, kemudian ditambahkan aquadest 200 ml. Labu dipanaskan dengan penangas, sehingga penyulingan pun berlangsung selama 6 jam. Setelah selesai,
dibiarkan selama tidak kurang dari 15 menit, volume MA pada labu berskala dicatat. Kadar MA dihitung dalam % v/b.
Penetapan kadar minyak atsiri
e.
1) Pembuatan larutan stok
Penetapan kadar kurkuminoid yang dihitung dalam persen kurkumin
Kurang lebih 20,0 mg kurkumin baku yang ditimbang seksama
dilarutkan dalam aseton dengan menggunakan labu ukur 100,0 ml. 2) Pembuatan larutan intermediet
Larutan stok dengan kadar 20 mg % diambil sebanyak 25 ml dan dimasukkan ke dalam labu ukur 100,0 ml, kemudian diencerkan dengan aseton hingga tanda sehingga diperoleh larutan intermediet kurkumin dengan kadar 5 mg %.
3) Penetapan panjang gelombang maksimum (λ maks)
sampai tanda. Larutan kurkumin dengan konsentrasi 0,1632 mg%, 0,2856 mg %, dan 0,4080 mg % ini kemudian dibaca serapannya pada panjang gelombang 400 nm sampai 700 nm.
4) Validasi metode
Larutan intermediet dengan kadar 5 mg % diambil 0,8 ml; 1,4 ml; 2,0ml dengan pipet ukur dan dimasukkan ke dalam labu 25 ml, kemudian diencerkan dengan aseton sampai tanda. Larutan kurkumin dengan konsentrasi 0,1632 mg%, 0,2856 mg %, dan 0,4080 mg % ini kemudian dibaca serapannya pada panjang gelombang maksimum, kemudian dihitung kadarnya menggunakan persamaan kurva baku.
(a) Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat
kedekatan hasil analisis dengan kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Larutan
masuk rentang persen recovery yang dipersyaratkan atau tidak. Bila masuk persyaratan, maka akurasi metode ini baik.
(b) Presisi
Presisi biasanya dinyatakan dalam Koefisien Variasi (KV) atau
coefficient variation (CV). Presisi menunjukkan keterulangan dan ketertiruan hasil
yang diperoleh. Prosedurnya hampir sama dengan akurasi, yaitu tiga konsentrasi dengan tiga replikasi, namun dalam presisi yang dihitung adalah Simpangan
Deviasi (SD) masing–masing replikasi dan konsentrasi dibagi dengan harga rata – rata replikasi per konsentrasi dikalikan dengan 100%. Setelah didapatkan CV
masing –masing konsentrasi, dihitung CV rata-rata untuk seluruh konsentrasi. CV rata –rata seluruh konsentrasi kemudian dibandingkan dengan persyaratan presisi yang baik untuk suatu metode. Bila angka presisi masuk dalam persyaratan maka
presisi metode tersebut baik.
(c) Linieritas dan rentang
Linieritas dan rentang didapatkan dari hasil perhitungan regresi linier antara absorbansi dengan konsentrasi. Dalam hal ini, dihitung 5 konsentrasi yang telah diukur absorbansinya untuk 1 kali replikasi. Dibuat 5 konsentrasi dengan 3
replikasi. Kemudian masing –masing replikasi dihitung secara regresi linier dan didapatkan r. Bila nilai suatu r semakin mendekati 1, maka linieritas dan rentang
metode semakin tinggi. (d) Spesifisitas
menggunakan spektrofotometri visible karena panjang gelombangnya berada pada sinar tampak yaitu antara 400 – 700 nm (Skoog, 1985).
(e) LOD dan LOQ
LOD dan LOQ dihitung secara statistik melalui garis regresi linier, dari kurva kalibrasi.menggunakan rumus: LOD = 3 Syb/x dan LOQ = 10 Syb/x. Dihitung menggunakan 5 konsentrasi dan masing –masing absorbansinya dengan perhitungan regresi linier. Kemudian didapatkan persamaan Y = BX + A, dari absorbansi larutan baku didapatkan absorbansi (Y’), maka Y yang merupakan absorbansi seharusnya pada konsentrasi baku yang tepat 0,1632 mg% dikurangi dengan Y’. Hasil pengurangan Y-Y’ kemudian dipangkatkan. Dilakukan untuk 4 konsentrasi lainnya. Kemudian (Y-Y’)2
Sb ( y/x) =
dari berbagai konsentrasi ditotal dan dilakukan perhitungan Sb (y/x) yang memiliki rumus :
dihitung LOD dengan rumus 3Sb(y/x) dan LOQ dengan rumus 10 Sb(y/x). 5) Pembuatan kurva baku
Larutan intermediet dengan kadar 5 mg % diambil 0,8 ml; 1,0 ml; 1,4 ml; 1,6 ml; 2,0 ml dan dimasukkan ke dalam labu 25,0 ml, kemudian diencerkan
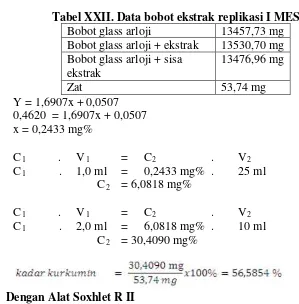
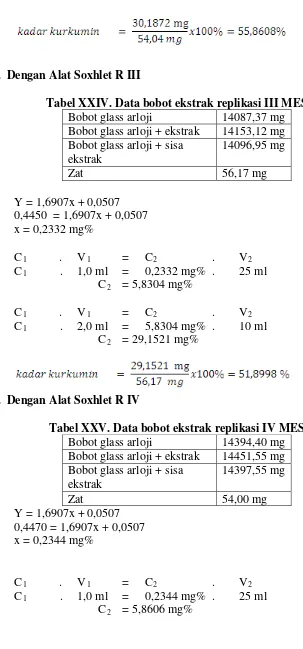
6) Penetapan kadar kurkuminoid dalam sampel
Kadar kurkuminoid ditetapkan dengan spektrofotometri sinar tampak
pada panjang gelombang maksimum. Ekstrak yang mengandung 50,0 mg kurkuminoid dimasukkan ke dalam beaker glass, kemudian dilarutkan dengan
aseton. Ekstrak yang telah larut aseton dituang ke dalam labu ukur 50,0 ml melalui kertas saring, diteruskan dengan penambahan aseton hingga tanda batas. Diambil 2,0 ml dimasukkan ke dalam labu ukur 10 ml ditambah aseton hingga
tanda. Diambil 1,0 ml dimasukkan dalam labu ukur 25,0 ml dan ditambahkan aseton hingga tanda. Kemudian dibaca serapannya. Hitung kadar dalam % b/b
dengan perbandingan kurva baku. Dilakukan replikasi sebanyak lima kali.
f.
Statistik yang digunakan untuk membandingkan kurkuminoid dengan metode maserasi dan metode dengan alat Soxhlet adalah metode analisis two
sample t-test dengan taraf kepercayaan 95%. Analisis two sample T-test merupakan suatu analisis untuk menguji perbedaan dari data dependent (sampel tergantung). Rumus dasar two sample T-test adalah sebagai berikut :
Analisa data
Dimana : t = t-test x1
x
= rata-rata kadar kurkuminoid dengan metode ektraksi maserasi
1
42 BAB IV
HASIL DAN PEMBAHASAN A. Identifikasi Rimpang Kunyit
Identifikasi dilakukan untuk mengidentifikasi suatu bagian tanaman, dalam hal ini RK. Apakah RK tersebut setelah diidentifikasi benar- benar merupakan bagian dari tanaman kunyit. Untuk mengidentifikasinya dilakukan perbandingan dengan literatur. Literatur yang dipakai adalah Materia Medika Indonesia (MMI), 1977. Identifikasi dapat dilakukan dengan uji organoleptik, makroskopis, dan mikroskopis.
1. Organoleptik
Tabel I. Data perbandingan organoleptik RK dan MMI Pengamatan
Organoleptik Kunyit Sampel MMI
Bau Khas aromatis Khas aromatik
Rasa Agak pahit, pedas, lidah terasa tebal
Agak pahit, agak pedas, lama kelamaan menimbulkan rasa tebal Warna Kuning jingga- coklat
kemerahan
Kuning jingga – coklat kemerahan Bentuk Bulat pipih, bulat panjang Hampir bulat, bulat
panjang
bentuk rimpang tersebut sudah sesuai dengan karakteristik standar RK secara organoleptis pada MMI.
2. Makroskopis
Tabel II. Data perbandingan makroskopik RK dan MMI
Jenis Bentuk Warna
Kunyit Sampel
Kepingan bulat, ringan, keras tapi rapuh,
Diameter= 1,5-3 cm, tebal= 1-3 mm
Jingga kecokelatan
MMI
Kepingan hampir bundar sampai bulat panjang, ringan,
rapuh,
Diameter= 0,5 - 3 cm, tebal= 1- 5 mm
Kuning jingga, kuning jingga kemerahan sampai kuning jingga
kecoklatan
Dari tabel II tersebut dapat dipastikan bahwa rimpang yang diidentifikasi secara makroskopik merupakan RK karena ciri- ciri makroskopisnya, ditinjau dari bentuk rimpang sampel telah memenuhi kriteria pada RK pada MMI, yaitu bentuk kepingan bulat, pada MMI disebutkan kepingan hampir bundar sampai bulat panjang, dan diameter rimpang sampel 1, 5 – 3 cm dengan tebal 1 -3 mm, telah memenuhi syarat diameter RK pada MMI, yaitu diameter 0,5 – 3 cm, dan tebal 1-5 mm. Warna rimpang sampel telah sama dengan kriteria warna RK pada MMI. Gambar II berikut merupakan gambar RK sampel yang dibandingkan dengan MMI.
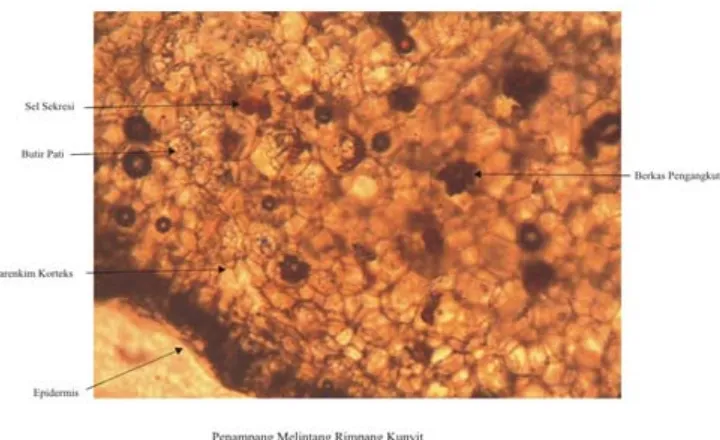
3. Mikroskopis
Gambar 3. Penampang melintang sampel rimpang kunyit
Gambar 4. Penampang melintang rimpang kunyit MMI
pembuluh atau berkas pengangkut sama – sama tersebar tidak beraturan pada parenkim korteks. Hal ini menunjukkan bahwa rimpang yang diidentifikasi secara mikroskopis dalam penelitian ini adalah benar- benar rimpang kunyit.
B. Pembuatan Simplisia 1. Pengumpulan rimpang kunyit
RK (10 kg) yang digunakan dalam penelitian ini adalah rimpang utuh dan masih segar yang dibeli dari Pasar Bringhardjo karena Pasar Bringhardjo termasuk pasar besar yang banyak dikunjungi oleh konsumen. Pembelian dilakukan hanya kepada satu pedagang saja untuk menyamakan perlakuan. Pembelian rimpang dilakukan pada musim kemarau (18 Mei 2009) karena pada musim kemarau kandungan kunyitnya maksimum (Anonim, 2006), diharapkan kunyit yang telah dibeli pemanenannya dilakukan pada musim kemarau.
Musim kemarau Indonesia terjadi pada bulan April sampai Oktober (Anonim, 2008) sehingga dapat dipastikan kandungan kunyit yang dipakai pada penelitian ini memiliki kandungan yang maksimum. Rimpang yang diperoleh masih banyak terdapat bahan pengotor seperti tanah yang menempel pada rimpang, kerikil, dan pasir yang menempel pada tanah yang menempel pada rimpang, oleh karena itu dilakukan sortasi basah terlebih dahulu agar kotoran yang menempel pada RK dapat dikurangi.
2. Sortasi basah
kerikil, pasir, dan sebagainya sebagai langkah awal pengurangan jumlah mikroba. Mikroba dapat mempercepat pembusukan RK apabila tidak segera dibersihkan. 3. Pencucian rimpang kunyit
Pencucian RK dilakukan setelah sortasi basah dengan air bersih agar dapat membersihkan RK hasil sortasi basah dengan baik. Air bersih kemudian ditampung dalam ember, RK hasil sortasi basah dimasukkan ke dalamnya. Sikat digunakan untuk mempercepat proses pembersihan kunyit.
Setelah semua RK dibersihkan, air yang telah keruh diganti dengan air bersih, hal ini dilakukan agar didapatkan RK yang bersih. Penggantian air bisa dilakukan beberapa kali sampai akhirnya air pencucian RK tidak keruh setelah membilas RK.
RK yang telah bersih kemudian dikeringkan dari air pencucinya dengan cara diangin–anginkan. Hal ini bertujuan agar rimpang mengering karena dengan diangin -anginkan dapat mempercepat penguapan air. RK yang kering lebih sulit ditempeli oleh partikel –partikel asing bila dibandingkan dengan RK yang masih basah sehingga RK yang kering lebih awet atau lebih sulit membusuk karena bukan media yang baik untuk pertumbuhan mikroba.
4. Perajangan rimpang kunyit
5. Pengeringan rimpang kunyit
RK yang telah dirajang kemudian dikeringkan. Pengeringan bertujuan mendapatkan simplisia agar tidak mudah rusak, sehingga dapat disimpan dalam wadah yang lebih lama. Penurunan mutu atau perusakan simplisia dapat dihambat dengan pengurangan kadar air dan penghentian reaksi enzimatik. Kandungan air dalam simplisia pada kadar tertentu dapat merupakan media pertumbuhan kapang dan jasad renik lainnya.
6. Sortasi kering
Setelah proses pengeringan selesai, maka akan dilanjutkan dengan sortasi kering. Tujuan sortasi kering untuk memisahkan benda – benda asing seperti kerikil atau batu –batu kecil atau juga bagian dari simplisia selain rimpangnya yang mungkin terikut ke dalam simplisia RK ketika proses pengeringan.
Sortasi kering penting dilakukan agar nantinya yang terekstrak benar-benar hanya RK sehingga didapatkan kadar kurkuminoid dan MA yang berasal dari RK, bukan dari bagian lain tanaman kunyit (Nurfina, 1998; Oomah, 2000; Rukmana, 1994).
7. Pembuatan serbuk
RK yang telah kering kemudian diserbuk dengan grinder. Tujuan penyerbukan adalah untuk memperkecil ukuran simplisia, sehingga semakin luas permukaan akan berkontak dengan larutan penyari, sehingga penyarian dapat dilakukan dengan optimal.