APLIKASI TANAMAN PINGGIR DAN EKSTRAK DAUN
PAGODA UNTUK PENGENDALIAN Bean common mosaic virus
PADA KACANG PANJANG DI LAPANGAN
LESTARI PEBRIYENI
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRAK
LESTARI PEBRIYENI. Aplikasi Tanaman Pinggir dan Ekstrak Daun Pagoda untuk Pengendalian Bean common mosaic virus pada Kacang Panjang di Lapangan. Dibimbing oleh TRI ASMIRA DAMAYANTI.
Bean common mosaic virus adalah salah satu virus penting dan merupakan
salah satu penyebab penyakit mosaik kuning pada kacang panjang. Penelitian ini dilakukan untuk menguji efektivitas tanaman pinggir dan ekstrak daun pagoda yang diterapkan secara terpisah atau bersama-sama terhadap penekanan infeksi BCMV di lapangan. Jagung sebagai tanaman penghalang ditanam 4 minggu sebelum kacang panjang. Penyemprotan ekstrak daun pagoda pada daun dilakukan satu hari sebelum penularan BCMV. Penularan BCMV oleh Aphis
craccivora mengandung virus dan dilepaskan pada empat titik di lapangan.
Peubah yang diamati adalah periode inkubasi, kejadian dan keparahan penyakit, dan akumulasi BCMV. Gejala yang teramati bervariasi dari mosaik ringan sampai sampai mosaik berat, mosaik kuning, kuning, tulang daun menjaring, dan malformasi daun dan buah. Masa inkubasi dari tanaman perlakuan relatif 1-2 hari lebih lama dibanding kontrol tanpa perlakuan. Kejadian, keparahan penyakit dan akumulasi BCMV dari tanaman perlakuan lebih rendah, terutama perlakuan tanaman pinggir dan ekstrak daun pagoda secara kombinasi nyata lebih rendah dibandingkan kontrol tanpa perlakuan. Diantara semua perlakuan, aplikasi tanaman pinggir dikombinasikan dengan ekstrak daun pagoda merupakan perlakuan yang paling baik dalam menekan BCMV di lapangan.
ABSTRACT
LESTARI PEBRIYENI. Application of Barrier crop and pagoda leaf extract to control Bean common mosaic virus on yard long bean in the field. Supervised by TRI ASMIRA DAMAYANTI.
Bean common mosaic virus is the one of an important virus and is one of
causal of yellow mosaic diseases on yard long bean. The research was done to test the effectiveness of barrier crop and pagoda leaf extract which applied either separately or together to suppressed BCMV infection in the field. Maize as
barrier crop was grown at 4 weeks prior yard long bean. Pagoda leaf extract was
applied as leaf spraying at one day prior BCMV transmission. BCMV was transmitted by releasing viruliferous Aphis craccivora at four site points in the field. The incubation period, disease incidence, severity and BCMV accumulation were observed. The symptom were vary from mild up to severe mosaic, yellow mosaic, yellowing, leaf vein netting, leaf and fruit malformation. The incubation period of treatment plants were relatively 1-2 days longer than untreated control. The disease incidence, severity and BCMV accumulation of the treatment plants were lower, especially on combination treatment was significantly lower than control plants. Among tested treatments, the application of barrier crop in combine with pagoda leaf extract was the best treatment in suppressing BCMV in the field.
18
© Hak Cipta milik IPB, tahun 2013 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya tulis dalam bentuk apa pun tanpa izin IPB.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Pertanian
pada
Departemen Proteksi Tanaman
APLIKASI TANAMAN PINGGIR DAN EKSTRAK DAUN
PAGODA UNTUK PENGENDALIAN Bean common mosaic virus
PADA KACANG PANJANG DI LAPANGAN
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul Skripsi : Aplikasi Tanaman Pinggir dan Ekstrak Daun Pagoda untuk Pengendalian Bean common mosaic virus pada Kacang Panjang di Lapangan
Nama : Lestari Pebriyeni NIM : A34080017
Disetujui oleh
Dr. Ir. Tri Asmira Damayanti, M.Agr. Dosen Pembimbing
Diketahui oleh
Dr. Ir. Abdjad Asih Nawangsih, M.Si. Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga penulis dapat menyelesaikan tugas akhir ini dengan judul “ Aplikasi Tanaman Pinggir dan Ekstrak Daun Pagoda untuk Pengendalian
Bean common mosaic virus pada Kacang Panjang di Lapangan”.
Terima kasih penulis ucapkan kepada kedua orang tua Radilis (ibu), Taslim (ayah) dan Damra (adik) yang selalu mendoakan dan memberikan semangat hingga terselesaikannya skripsi ini. Terimakasih kepada Dr. Ir. Tri Asmira Damayanti, M.Agr. selaku dosen pembimbing yang selalu memberikan saran dan dorongan selama penelitian sampai penulisan ini serta memotivasi dalam proses kehidupan. Terimakasih kepada bapak Dr. Ir. Hermanu Triwidodo, MSc. selaku pembimbing akademik yang selalu memberikan dukungan dalam proses pembelajaran. Terimakasih kepada teman-teman Proteksi Tanaman khususnya angkatan 45, anggota laboratorium virologi tumbuhan khususnya Edi Supardi, Melinda, Sari Nurulita, Hamdayanti, Yudia, Nisa, Titin, Dita dan Saudari Tuti Legiastuti yang telah membantu selama pengumpulan data. Ungkapan terima kasih juga disampaikan kepada Reza Febrian yang selalu mendampingi dalam proses penulisan skripsi ini.
Semoga hasil penelitian ini dapat bermanfaat sebagai informasi dalam bidang pertanian dan dapat digunakan sebagai acuan untuk penelitian selanjutnya. Penulis menyadari masih terdapat banyak kekurangan, kritik dan saran sangat diharapkan oleh penulis untuk perbaikan kegiatan selanjutnya.
Bogor, Mei 2013
DAFTAR ISI
DAFTAR TABEL ix DAFTAR GAMBAR ix DAFTAR LAMPIRAN iix PENDAHULUAN 1 Latar Belakang 1 Tujuan Penelitian 2 Manfaat Penelitian 2BAHAN DAN METODE 3
Tempat dan Waktu Penelitian 3
Metode Penelitian 3
Perbanyakan Inokulum 3
Penyiapan Kutudaun Bersayap dan Mengandung Virus 3
Persiapan Lahan dan Tanaman Uji 3
Pembuatan Ekstrak Tanaman 4
Perlakuan 4
Peubah Pengamatan 4
Deteksi BCMV Secara Serologi 5
Rancangan Percobaan dan Analisis Data 6
HASIL DAN PEMBAHASAN 7
Pengaruh Perlakuan Terhadap Periode Inkubasi dan Tipe Gejala 7
Pengaruh Perlakuan Terhadap Kejadian Penyakit 8
Pengaruh Perlakuan Terhadap Keparahan Penyakit 9
Pengaruh Perlakuan Terhadap Akumulasi BCMV 10
Pengaruh Perlakuan Terhadap Nilai AUDPC dan Penghambatan Penyakit 11
KESIMPULAN DAN SARAN 13
Kesimpulan 13
Saran 13
DAFTAR PUSTAKA 14
LAMPIRAN 16
DAFTAR TABEL
1. Pengaruh perlakuan terhadap waktu inkubasi dan tipe gejala BCMV pada
tanaman 7
2. Pengaruh perlakuan terhadap nilai AUDPC, penghambatan penyakit, dan
virus pada 4 MSP 11
DAFTAR GAMBAR
1. Denah petak percobaan di lapangan 3
2. Skor keparahan penyakit berdasarkan gejala visual 4
3. Variasi gejala infeksi BCMV di lapangan 8
4. Perkembangan kejadian penyakit tanaman dari minggu ke 1-8 8 5. Perkembangan keparahan penyakit tanaman dari minggu 1-8 9
5. Rata-rata NAE BCMV dari tanaman uji 11
DAFTAR LAMPIRAN
1. Kejadian penyakit pada minggu ke 1-8 17
2. Keparahan penyakit pada minggu 1-8 17
3. Rata-rata nilai absorban ELISA 18
4. NAE sampel komposit pada 4 MSP 18
5. Hasil analisis ragam kejadian penyakit minggu ke-2 pada taraf α = 5% 19 6. Hasil analisis ragam kejadian penyakit minggu ke-3 pada taraf α = 5% 19 7. Hasil analisis ragam kejadian penyakit minggu ke-4 pada taraf α = 5% 19 8. Hasil analisis ragam kejadian penyakit minggu ke-5 pada taraf α = 5% 19 9. Hasil analisis ragam kejadian penyakit minggu ke-6 pada taraf α = 5% 19 10. Hasil analisis ragam kejadian penyakit minggu ke-7 pada taraf α = 5% 19 11. Hasil analisis ragam kejadian penyakit minggu ke-8 pada taraf α = 5% 20 12. Hasil analisis ragam keparahan penyakit minggu ke-2 pada taraf α = 5% 20 13. Hasil analisis ragam keparahan penyakit minggu ke-3 pada taraf α = 5% 20 14. Hasil analisis ragam keparahan penyakit minggu ke-4 pada taraf α = 5% 20 15. Hasil analisis ragam keparahan penyakit minggu ke-5 pada taraf α = 5% 20 16. Hasil analisis ragam keparahan penyakit minggu ke-6 pada taraf α = 5% 21 17. Hasil analisis ragam keparahan penyakit minggu ke-7 pada taraf α = 5% 21 18. Hasil analisis ragam keparahan penyakit minggu ke-8 pada taraf α = 5% 21
Latar Belakang
Kacang panjang merupakan sayuran penting dan sudah lama dikenal dan ditanam oleh petani di Indonesia. Sayuran ini memiliki banyak manfaat di antaranya sebagai sumber protein, vitamin dan mineral, terutama pada polong muda. Selain bergizi, tanaman ini juga dapat meningkatkan kesuburan tanah, karena akar-akar bersimbiosis dengan bakteri rhizobium yang mampu mengikat nitrogen (N2) dari udara. Limbah dari tanaman kacang panjang juga dapat
dimanfaatkan sebagai pupuk organik. Oleh karena itu potensi pengembangan kacang panjang sangat besar karena mempunyai banyak kegunaan sebagai produk pertanian. Sehingga dalam pengembangan usaha pertanian tanaman kacang panjang sangat potensial untuk dikembangkan, selain mudah dibudidayakan, nilai jual di pasar juga cukup tinggi (Haryanto et al. 2007).
Di Indonesia produksi kacang panjang mengalami penurunan setiap tahun. Badan Pusat Statistik (BPS) (2012) melaporkan produksi kacang panjang pada tahun 2008 mencapai 455.524 ton, pada tahun 2009 dan 2010 produksi mengalami peningkatan 483.793 sampai 489.449 ton. Sedangkan pada tahun 2011 terjadi penurunan produksi kacang panjang menjadi 458.307 ton. Hal ini dapat disebabkan oleh adanya gangguan dari beberapa penyakit tanaman, seperti antraknosa (Colletotrichum sp.), nematoda puru akar (Meloidogyne sp.) dan penyakit virus mosaik. Menurut Udayashankar et al. (2010) penyakit virus menyebabkan penurunan produksi terbesar pada kacang panjang. Salah satu virus penyebab mosaik pada kacang panjang yaitu Bean Common Mosaic Virus (BCMV).
BCMV merupakan salah satu virus penting pada kacang-kacangan dan dapat ditularkan melalui vektor kutudaun Aphis craccivora Koch. Vektor ini banyak ditemukan pada tangkai bunga tanaman kacang panjang. A. craccivora dapat menularkan lebih dari 30 virus tanaman secara nonpersisten (Hooks dan Fereres, 2006).
Pada tahun 2008-2009 dilaporkan terjadi ledakan penyakit mosaik kuning akibat serangan BCMV strain Black eye cowpea (BCMV-BlC) pada tanaman kacang panjang yang meluas di beberapa daerah di Jawa Barat dan Jawa Tengah. Kejadian penyakit BCMV di lapangan dapat mencapai 80-100% (Damayanti et al. 2009).
Pengendalian virus secara umum dilakukan dengan beberapa cara seperti usaha mengendalikan serangga-serangga yang dapat menularkan penyakit virus dengan pestisida, karantina, dan menggunakan benih yang sehat dan bebas virus. Cara pengendalian yang dilakukan petani adalah dengan penggunaan pestisida untuk mengendalikan serangga. Penggunaan pestisida yang tidak tepat dapat menimbulkan berbagai dampak negatif seperti munculnya populasi hama yang resisten, terjadi resurgensi hama, munculnya hama sekunder dan pencemaran terhadap lingkungan. Oleh karena itu penggunaan pestisida harusnya seminimal mungkin.
Pengendalian virus yang efektif dilakukan dengan menggunakan varietas tahan, namun tidak banyak tersedia kultivar komersial dan tahan virus di pasaran. Menurut Setyastuti (2008), dari 9 kultivar kacang panjang yang diuji respon
2
ketahanannya terhadap BCMV menjelaskan semua rentan terhadap infeksi BCMV secara mekanis, maupun melalui vektor kutudaun (Susetio, 2011). Oleh karena itu diperlukan alternatif pengendalian BCMV, seperti metode yang dapat meningkatkan ketahanan sistemik tanaman dan melindungi tanaman dari infeksi BCMV.
Menurut Verma et al (1996) ekstrak Clerodendrum aculeatum (sejenis daun pagoda) mengandung protein berukuran 34 kDa yang menyebabkan tembakau imun terhadap virus. Selain itu ekstrak daun pagoda mampu meningkatkan ketahanan tanaman terhadap infeksi virus dengan meningkatkan kandungan asam salisilat dalam daun cabai (Hersanti 2007). Kurnianingsih (2010) melaporkan bahwa ekstrak daun bunga pagoda mampu menekan infeksi BCMV sampai 100% pada kacang panjang di rumah kaca.
Tanaman pinggir merupakan tanaman penghalang yang dapat melindungi tanaman utama dari infeksi virus yang ditularkan oleh vektor kutudaun secara non-persisten. Fungsi dari tanaman penghalang berupa manipulasi habitat, sehingga menarik kutudaun untuk makan pada tanaman tersebut, sehingga kutudaun yang masuk ke tanaman kacang panjang telah bebas dari virus (Hooks dan Fereres, 2006). Suryadi et al. (2008) juga melaporkan penggunaan jagung sebagai tanaman pinggir (barrier crop) efektif menekan kejadian penyakit oleh infeksi BCMV pada kacang panjang sampai 93.33% di rumah kaca.
Sampai saat ini kejadian penyakit mosaik kuning kacang panjang masih tinggi di lapangan. Sehingga perlu diupayakan cara pengendalian untuk mengatasinya. Keefektifan penggunaan tanaman pinggir dan ekstrak daun pagoda dalam menekan BCMV masih sebatas percobaan rumah kaca. Oleh karena itu kedua cara pengendalian tersebut perlu diuji di lapangan untuk mengetahui konsistensi keefektifannya dalam menekan BCMV.
Tujuan Penelitian
Penelitian ini bertujuan menguji keefektifan tanaman pinggir dan ekstrak daun pagoda baik digunakan secara tunggal ataupun kombinasi untuk menekan infeksi BCMV yang ditularkan kutudaun di lapangan.
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat menjadi upaya pengendalian yang cukup efektif dalam menekan infeksi BCMV di lapangan yang dapat dimanfaatkan dan diaplikasikan secara luas.
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Lahan Kebun Percobaan Cikabayan dan Laboratorium Virologi Tumbuhan Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor. Penelitian dilaksanakan dari bulan Agustus sampai Desember 2012.
Metode Penelitian Perbanyakan Inokulum
Isolat BCMV strain Black eye cowpea (BCMV-BlC) asal Cangkurawok, Dramaga, Bogor yang digunakan adalah koleksi Laboratorium Virologi Tumbuhan, Departemen Proteksi Tanaman. Inokulum diperbanyak pada tanaman kacang panjang kultivar Parade. Kacang panjang berumur 7 hari setelah tanam (HST) diinokulasi dengan BCMV secara mekanis dan dipelihara sebagai sumber inokulum.
Penyiapan Kutudaun Bersayap dan Mengandung Virus
Aphis craccivora Koch. diperoleh dari lapangan dibebasviruskan pada daun
talas selama semalam. Kutudaun yang lahir dipelihara pada tanaman kacang panjang sehat. Identifikasi dilakukan berdasarkan kunci identifikasi Blackman dan Eastop (2000). Kemudian kutudaun dipindahkan pada tanaman sakit untuk makan akuisisi dan dibiarkan berkembang hingga muncul populasi bersayap.
Persiapan Lahan dan Tanaman Uji
Persiapan lahan. Total petak terdiri dari 24 yang diatur secara acak, masing-masing berukuran 2 x 5 m, dengan jarak antar petak 60 cm (Gambar 1).
Gambar 1 Denah petak percobaan di lapangan. Kotak tebal: petak dengan tanaman pinggir, kotak bergaris putus-putus: petak tanpa tanaman pinggir. TP, tanaman pinggir; EDP, ekstrak daun pagoda; K, kontrol. Penanaman tanaman pinggir. Jagung varietas Pertiwi ditanam 4 minggu sebelum penanaman kacang panjang, dan ditanam di pinggir petak perlakuan.
Penanaman tanaman kacang panjang. Kacang panjang kultivar Parade ditanam dan dipupuk sesuai petunjuk Adijaya et al. (2005). Sebelum ditanam, benih kacang panjang direndam dalam ekstrak daun pagoda selama 24 jam. Benih ditanam dengan jarak tanam 20 x 60 cm, setiap lubang diisi 3 benih kacang panjang. Tanaman yang paling baik tumbuhnya yang digunakan dalam pengujian.
TP+ EDP EDP EDP K TP K TP TP+ EDP E D P EDP EDP TP TP TP+ EDP E D P TP+ EDP EDP TP+ EDP E D P K K EDP K EDP EDP TP+ EDP E D P TP TP K
4
Pembuatan Ekstrak Tanaman
Daun bunga pagoda (Clerodendrum japonicum) digerus dengan mortar dalam air steril 1 : 10 (b/v), dan disaring untuk mendapatkan ekstrak daun kasar. Ekstrak kasar diaplikasikan pada tanaman dengan disemprot sehari sebelum pelepasan kutudaun.
Perlakuan
Perlakuan yang diuji ada 4 yaitu :
TP+EDP = Tanaman pinggir + Ekstrak daun pagoda TP = Tanaman pinggir
EDP = Ekstrak daun pagoda
K = Kontrol
Setelah daun kacang panjang membuka penuh, kutudaun bersayap yang telah makan akuisisi pada tanaman sakit dilepas ke pertanaman kacang panjang. Setiap perlakuan terdiri dari 6 petak ulangan.
Peubah Pengamatan
Peubah pengamatan yang diamati sebagai berikut : 1. Periode inkubasi virus dan tipe gejala
2. Persentase kejadian penyakit (KP) dihitung dari minggu ke 1-8 setelah infeksi BCMV dengan rumus :
∑ tanaman terinfeksi
Kejadian Penyakit = x 100% ∑ tanaman yang diuji
3. Persentase keparahan penyakit dihitung dari minggu ke 1-8 setelah infeksi BCMV dengan menggunakan skala kategori serangan sebagai berikut :
0 : tidak bergejala 1 : gejala mosaik ringan 2 : gejala mosaik sedang 3 : gejala mosaik berat
4 : gejala mosaik berat dengan malformasi daun yang parah, kerdil, atau mati
Gambar 2 Skor keparahan penyakit berdasarkan gejala visual (a) skor 0, (b) skor 1, (c) skor 2, (d) skor 3, dan (e) skor 4.
Nilai skor yang diukur dikonversi dalam nilai keparahan penyakit (disease
severity) berdasarkan rumus Townsend dan Heuberger (1974 dalam Agrios 2005):
I = x 100%
N x V I = keparahan penyakit
ni = jumlah tanaman dengan skor ke-i
vi = nilai skor penyakit
N = jumlah tanaman yang diamati V = skor tertinggi
Seluruh data intensitas serangan penyakit digunakan untuk membuat grafik perkembangan penyakit. Menurut Shaner dan Finney (1977) dalam Strange (2003), total luas area dibawah kurva perkembangan penyakit (Area Under
Disease Progress Curve / AUDPC) dihitung dengan menggunakan rumus : n Yi + Yi+1
AUDPC = ∑ [ ] (ti+1 – ti) i=1
2 Yi = data pengamatan ke-i
Yi+1 = data pengamatan ke-i+1
ti = waktu pengamatan ke-i
ti+1 = waktu pengamatan ke-i+1
Persentase penghambatan penyakit karena perlakuan dihitung berdasarkan rumus :
AUDPC kontrol positif – AUDPC perlakuan
Penghambatan penyakit = x 100% AUDPC kontrol positif
4. Akumulasi BCMV dideteksi secara serologi pada sampel yang berumur 4 minggu setelah penularan. Sampel uji diambil dari 10 tanaman uji tiap perlakuan yang diambil dengan pola zig zag.
5. Persentase penghambatan virus dihitung berdasarkan rumus : NAE kontrol – NAE perlakuan
Penghambatan virus = x 100% NAE kontrol
Deteksi BCMV Secara Serologi
BCMV dideteksi dengan metode Indirect ELISA (I-ELISA) menggunakan antiserum spesifik BCMV dengan prosedur sesuai panduan produsen antiserum (Agdia Inc.). Untuk tiap petak diambil sampel secara sistematis sebanyak 10 tanaman yang mewakili perlakuan dalam petak. Sampel dari tiap petak perlakuan dibuat menjadi 1 sampel komposit. Sehingga tiap perlakuan terdiri dari 6 sampel komposit yang mewakili ulangan tiap perlakuan.
Sampel daun digerus dengan bufer ekstraksi (Na2C03 0.159 g, NaHCo3
0.293 g, NaN3 0.02 g, Polyvinylpyrrolidone (PVP) 2 g dilarutkan dalam 100 ml
air destilata pH 9.6) dengan perbandingan 1:100 (b/v). Sebanyak 100 µl ekstrak daun (sap) diisikan ke dalam sumuran plat mikrotiter. Sebagai pembanding sumuran plat mikrotiter diisi dengan 100 µl bufer ekstraksi, ekstrak tanaman sehat (kontrol negatif), ekstrak tanaman terinfeksi BCMV (kontrol positif). Plat mikrotiter kemudian diinkubasi pada suhu ruang dalam kotak plastik tertutup yang dilapisi dengan tisu basah selama satu jam. Selanjutnya plat mikrotiter dicuci
6
dengan menggunakan PBST (NaCl 0.2 g, Na2HPO4 0.115 g, KH2PO4 0.02 g, KCl
0.02 g, NaN3 0.2 g, tween-20 0.005 g) sebanyak 8 kali.
Antiserum spesifik BCMV kemudian dimasukkan sebanyak 100 µl ke dalam sumuran plat mikrotiter sesuai peta yang telah dibuat. Antiserum sebelumnya diencerkan dengan bufer ECI [bovine serum albumin (BSA) 0.1 g, PVP 1 g, PBST 50 ml] dengan perbandingan 1:300. Kemudian plat mikrotiter diinkubasi selama 2 jam pada suhu ruang dalam kotak plastik tertutup yang dilapisi dengan tisu basah. Selanjutnya plat dicuci dengan menggunakan PBST seperti tahapan pencucian sebelumnya. Antiserum kedua (RAM-AP) dimasukkan pada plat mikrotiter sebanyak 100 µl setelah dilakukan pengenceran dengan bufer ECI (1:300). Plat mikrotiter kemudian diinkubasi pada suhu ruang selama 1 jam kemudian dicuci menggunakan PBST sebanyak 8 kali.
Tahapan terakhir adalah memasukkan 100 µl substrat pewarna PNP
[p-Nitrophenyl Phosphate 5 mg dalam bufer substrat 5 ml (MgCl2 0.006 g, NaN3
0.0125 g, diethanolamine 97 ml, air destilata 50 ml)] ke dalam sumuran plat mikrotiter. Plat mikrotiter tersebut kemudian diinkubasi dalam ruang gelap pada suhu ruang selama 1 jam. Nilai absorbansi ELISA (NAE) dibaca menggunakan ELISA reader model 550 (Bio-Rad, USA) pada panjang gelombang 405 nm. NAE diukur setiap 15 menit sampai 60 menit. Sampel dinyatakan positif jika nilai absorbansi sampel 2 kali lebih besar dari nilai absorbansi kontrol negatif.
Percobaan dan Analisis Data
Percobaan dirancang menggunakan rancangan acak lengkap (RAL). Data yang diperoleh dianalisis menggunakan analisis ragam (ANOVA) menggunakan program MINITAB Release 14.12.0. Perlakuan yang memberikan pengaruh nyata diuji dengan uji lanjut Duncan Multiple Range Test (DMRT) pada taraf α = 5 %.
Pengaruh Perlakuan Terhadap Periode Inkubasi dan Tipe Gejala
Periode inkubasi adalah waktu yang dibutuhkan virus sejak masuk ke tanaman hingga gejala pertama pada tanaman teramati. Rata-rata periode inkubasi tanaman perlakuan relatif lebih lama 1-2 hari dibandingkan dengan rata-rata periode inkubasi pada kontrol. Periode inkubasi terpanjang ditunjukkan oleh perlakuan TP+EDP dan tersingkat pada perlakuan kontrol, walaupun secara statistik tidak berbeda nyata (Tabel 1).
Gejala infeksi tunggal BCMV umumnya berupa mosaik, malformasi daun, penebalan tulang daun dan klorosis ringan sampai sedang, namun tidak seterang dan sekuning yang teramati di lapangan. Gejala tanaman uji yang teramati menunjukkan gejala yang bervariasi seperti mosaik ringan sampai berat, daun agak menggulung dan mengkerut sepanjang tulang daun (malformasi daun), tulang daun menjaring dan malformasi pada daun-daun muda dan buah (Gambar 3). Gejala yang teramati di lapangan ini lebih parah dibandingkan gejala infeksi BCMV-BlC, menunjukkan dugaan adanya infeksi campuran virus lain yang terjadi secara alami bersama BCMV, terutama pada tanaman kontrol.
Tabel 1 Pengaruh perlakuan terhadap periode inkubasi dan tipe gejala BCMV pada tanaman
Perlakuana Periode inkubasib (HSPc) Tipe Gejalad
TP+EDP 13.50 ± 2.43 a Mr,Ms
TP 12.17 ± 2.32 a Mr,Ms
EDP 12.33 ± 2.94 a Mr,Ms
K 11.17 ± 3.13 a Mr,Ms,Mb,Vn,Mk,Kng
a TP+EDP= Tanaman pinggir + ekstrak daun pagoda, TP= Tanaman pinggir, EDP= Ekstrak daun pagoda, K=kontrol
b Angka yang diikuti huruf yang sama menunjukkan hasil tidak berbeda nyata (uji selang berganda Duncan α = 5%)
c Hari setelah penularan.
d Mr = Mosaik ringan, Ms = Mosaik sedang, Mb = Mosaik berat, Vn= vein netting, Mk=mosaik kuning, Kng=kuning.
8
Gambar 3 Variasi gejala infeksi BCMV di lapangan. (a) Daun sehat, (b) Mosaik ringan, (c) Mosaik sedang, (d) Mosaik berat diikuti malformasi daun, (e) Tulang daun menjala (vein netting) (f) Mosaik dan malformasi pada buah.
Pengaruh Perlakuan Terhadap Kejadian dan Keparahan Penyakit
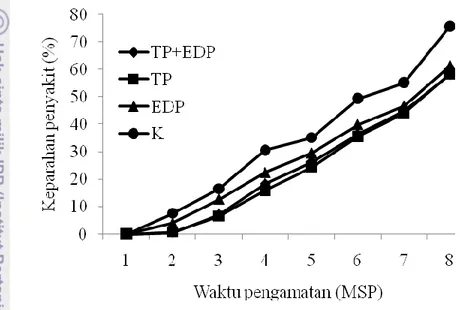
Kejadian penyakit adalah menggambarkan banyaknya tanaman yang terinfeksi dalam suatu populasi/area/lahan (Agrios 2005). Perkembangan kejadian penyakit teramati mulai 2 minggu setelah penularan (MSP), dan semakin meningkat hingga minggu ke-8 (Gambar 4). Tanaman perlakuan menunjukkan kejadian penyakit yang nyata lebih rendah dibandingkan dengan tanaman kontrol tanpa perlakuan pada 2-7 MSP, dan tidak berbeda nyata pada 8 MSP (Lampiran 1). Kejadian penyakit dari minggu ke 1-8 sebesar 0-72.59% pada perlakuan TP+EDP, 71.11% pada perlakuan TP, 74.07% pada perlakuan EDP dan 0-77.78% pada kontrol tanpa perlakuan(Gambar 4, Lampiran 1).
Gambar 4 Perkembangan kejadian penyakit tanaman dari minggu ke 1- 8.
f d
a b c
penyakit yang bergejala dalam suatu tanaman. Hasil yang hampir sama ditunjukkan oleh keparahan penyakit. Secara umum keparahan penyakit semua tanaman perlakuan menunjukkan nyata lebih rendah dibandingkan dengan tanaman kontrol tanpa perlakuan (Gambar 5; Lampiran 2). Keparahan penyakit dari minggu ke 1-8 masing-masing sebesar 58.1% pada perlakuan TP+EDP, 0-58.5% pada perlakuan TP, 0-61.3% pada perlakuan EDP dan 0-75.8% pada tanaman kontrol tanpa perlakuan.
Gambar 5 Perkembangan keparahan penyakit tanaman dari minggu ke 1- 8. Rendahnya keparahan penyakit tanaman perlakuan disebabkan oleh adanya tanaman pinggir yang berfungsi sebagai tempat menghilangkan BCMV yang terbawa pada stilet kutudaun. Indra kutudaun hanya dapat membedakan warna tanah dan hijau daun dan perilaku kutudaun yang menusuk-nusukkan stiletnya saat mencari inang yang sesuai (Hooks dan Fereres, 2006; Fereres, 2000). Oleh karena jagung ditanam 4 minggu lebih awal dari kacang panjang, maka kutudaun lebih dulu mengenali warna hijau daun jagung, sehingga jagung lebih dulu didatangi kutudaun bersayap. Menurut Ingwell et al. (2012), kutudaun yang mengandung virus, akan tertarik pada tanaman sehat, sedangkan kutudaun yang tidak mengandung virus akan lebih tertarik pada tanaman yang terinfeksi virus. Dalam penelitian ini kutudaun makan pada tanaman sakit sampai bersayap, sehingga di lapangan kutudaun langsung terbang mencari inang sehat (jagung) atau tanaman kacang panjang (kontrol). Hal ini menjelaskan bahwa pada tanaman yang diberi perlakuan tanaman pinggir menunjukkan kejadian dan keparahan penyakit yang nyata lebih rendah dibandingkan kontrol.
EDP dilaporkan mampu menginduksi ketahanan sistemik terhadap infeksi CMV pada cabai (Hersanti 2007) dan ekstrak C. aculeatum menyebabkan tembakau imun terhadap TMV (Verma et al, 1996). Namun perlakuan EDP menunjukkan kejadian dan keparahan penyakit diantara perlakuan kontrol dan perlakuan TP+EDP dan TP. Hal ini menunjukkan EDP di lapangan tidak seefektif di rumah kaca dalam menekan infeksi BCMV (kejadian dan keparahan penyakit), padahal EDP sebelumnya dilaporkan efektif menekan BCMV yang ditularkan
10
secara mekanis sampai 100% di rumah kaca (Kurnianingsih 2010). Faktor lingkungan dan cara penularan BCMV diduga mempengaruhi keefektifan EDP dalam menekan BCMV.
Dalam penelitian ini TP cukup mampu menekan infeksi BCMV melalui kutudaun, dan keefektifannya semakin tinggi didalam menekan BCMV jika dikombinasikan dengan ekstrak daun pagoda (TP+EDP). Menurut Hooks dan Fereres (2006) mekanisme tanaman pinggir dalam menekan infeksi virus tular kutudaun secara non-persisten karena tanaman pinggir berfungsi (1) sebagai tempat penampung virus (virus-sink hypothesis), (2) sebagai penghalang fisik (physical barrier), (3) sebagai kamuflase atau menutupi tanaman inang utama (camouflaging or masking the host plant), dan (4) sebagai tanaman perangkap (trap crop).
Pengaruh Perlakuan Terhadap Akumulasi BCMV
NAE merupakan gambaran kuantitatif virus yang menginfeksi tanaman. Akumulasi BCMV berdasarkan NAE sampel pada 4 MSP berkorelasi positif dengan keparahan penyakit. Pada 4 MSP keparahan semua tanaman perlakuan hanya berkisar 18.3% dengan gejala yang sangat ringan, sedangkan keparahan tanaman kontrol sekitar 30% (Gambar 6, Lampiran 2).
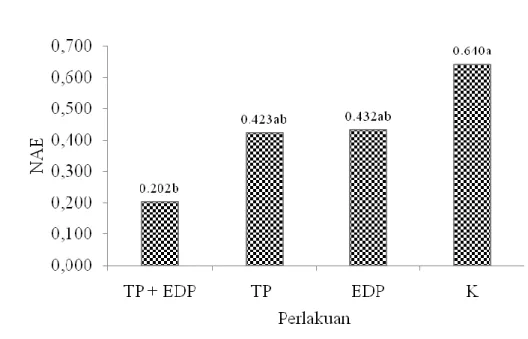
Perlakuan TP+EDP menunjukkan NAE yang nyata paling rendah dibandingkan NAE kontrol tanpa perlakuan, namun tidak berbeda nyata dengan perlakuan TP dan EDP. Diantara semua perlakuan yang diuji, perlakuan TP+EDP menunjukkan tidak terdeteksi positif BCMV (Gambar 6, Lampiran 3 dan 4). Sedangkan NAE perlakuan TP dan EDP tidak berbeda nyata dengan NAE kontrol. Walaupun perlakuan TP+EDP menunjukkan NAE yang tidak berbeda nyata dengan NAE perlakuan tunggal TP dan EDP, namun kombinasi keduanya meningkatkan efektifitas pengendalian dan mampu melindungi tanaman dari infeksi BCMV (BCMV tidak terdeteksi), jika dibandingkan dengan perlakuan tunggal TP dan EDP (keduanya positif terdeteksi BCMV). Di lapangan tidak adanya sumber virus di pertanaman lebih penting dibandingkan ada tanaman terinfeksi virus yang dapat menjadi sumber penularan dan penyebaran virus oleh serangga. TP dan EDP mampu menekan infeksi dan keparahan BCMV, namun pada kedua perlakuan, BCMV masih dapat terdeteksi. Sehingga aplikasi kombinasi kedua perlakuan merupakan perlakuan terbaik yang saling mendukung dan meningkatkan keefektifan pengendalian BCMV. Perlakuan TP+EDP menunjukkan kejadian dan keparahan penyakit yang nyata lebih rendah dibandingkan kontrol. Hasil deteksi serologi juga menunjukkan pada perlakuan ini BCMV tidak terdeteksi. Oleh karena itu, gejala dan keparahan yang teramati menunjukkan bahwa tanaman perlakuan kemungkinan terinfeksi oleh virus selain BCMV. Pada umur 8 MSP, gejala yang terlihat hanya pada pucuk tanaman yang tidak tertutupi oleh tanaman jagung.
Gambar 6 Rata-rata NAE BCMV dari tanaman uji. NAE K(-):0.190.
NAE BCMV menunjukkan lebih rendah dibandingkan dengan NAE inokulum awal (2.507). Menurut Damayanti (2013, komunikasi pribadi), ada virus lain yang berasosiasi dengan penyakit mosaik kuning di lapangan yaitu CMV dan
Geminivirus yang menginfeksi kacang panjang secara tunggal maupun ganda
dengan BCMV. Infeksi campuran atau ganda virus di lapangan merupakan kejadian yang umum terjadi secara alami. Infeksi campuran beberapa virus yang berbeda dapat menekan (antagonistik) atau meningkatkan konsentrasi virus (sinergistik) yang menginfeksi secara bersama (Syller, 2012), seperti infeksi campuran antara Cauliflower mosaic caulimovirus (CaMV) dan Turnip mosaic
potyvirus (TuMV) pada brassica (Martin dan Elena, 2009) dan antara TMV dan
PVX pada tomat (Bolagun et al. 2002).
Pengaruh Perlakuan terhadap Nilai AUDPC dan Penghambatan Penyakit dan Virus
Nilai AUDPC perlakuan TP+EDP dan TP secara nyata lebih rendah dibandingkan perlakuan EDP dan kontrol. AUDPC perlakuan EDP lebih rendah dibandingkan kontrol, namun secara statistik tidak berbeda nyata (Tabel 2).
Tabel 2 Pengaruh perlakuan terhadap AUDPC, penghambatan penyakit dan virus pada 4 MSP.
Perlakuana AUDPCb Penghambatan virus (%) Penghambatan Penyakit (%) TP+EDP 16.85 ± 5.85bc 68.43 57.12 TP 15.15 ± 4.21c 33.91 61.45 EDP 28.00 ± 11.5ab 32.50 28.75 K 39.30 ± 18.70a 00.00 00.00
a TP+EDP= Tanaman pinggir + ekstrak daun pagoda, TP= Tanaman pinggir, EDP= Ekstrak daun pagoda, K= Kontrol
b Angka yang diikuti huruf yang berbeda pada kolom yang sama menunjukkan hasil berbeda nyata (uji selang berganda Duncan α = 5%)
12
Penghambatan penyakit tertinggi ditunjukkan oleh perlakuan TP (61.45%) dan penghambatan virus tertinggi ditunjukkan oleh perlakuan TP+EDP (68.43%), sedangkan perlakuan EDP saja hanya mampu menekan penyakit dan virus sebesar 28.75% dan 32.50%. Hal ini menunjukkan bahwa perlakuan tunggal TP cukup mampu menghambat penularan BCMV melalui kutudaun karena kutudaun tidak dapat langsung menularkan BCMV ke tanaman kacang panjang karena terhalang tanaman pinggir. Namun perlakuan TP saja tidak sepenuhnya mampu menghambat virus yang berhasil ditularkan oleh kutudaun (kutudaun bervirus yang bisa masuk ke pertanaman tanpa melewati TP). Pertumbuhan TP yang bervariasi ketinggiannya memungkinkan adanya kutudaun yang berhasil melewati TP dan menularkan virus.
Pada perlakuan EDP menunjukkan kurang mampu menekan penyakit dan virus di lapangan jika dibandingkan perlakuan TP+EDP dan TP. Sehingga diantara perlakuan uji, perlakuan paling baik dalam menekan BCMV di lapangan ditunjukkan oleh perlakuan kombinasi TP+EDP. TP menghalangi penularan BCMV secara langsung ke tanaman kacang panjang dan EDP meningkatkan penghambatan BCMV yang terbawa kutudaun, sehingga tidak satupun tanaman terdeteksi positif BCMV pada perlakuan TP+EDP, walaupun tanaman menunjukkan gejala terinfeksi virus. Hal ini menjelaskan bahwa BCMV dapat dikendalikan dengan perlakuan TP+EDP, namun karena adanya infeksi campuran yang terjadi secara alami di lapangan menyebabkan munculnya gejala yang berbeda dari gejala infeksi BCMV yang teramati.
Keefektifan TP jagung dan EDP dalam menekan BCMV yang ditularkan melalui serangga pada penelitian ini tidak seefektif di rumah kaca seperti yang dilaporkan Suryadi et al. (2008) dan Kurnianingsih (2010) pada perlakuan tunggal. Hal ini menunjukkan bahwa di lapangan banyak faktor yang mempengaruhi keefektifan pengendalian virus seperti faktor lingkungan, cara penularan, adanya infeksi patogen lain (virus, fungi) serta serangga hama lainnya.
KESIMPULAN
Penggunaan tanaman pinggir dan ekstrak daun pagoda (Clerodendrum
japonicum) secara kombinasi (TP+EDP) cukup efektif dalam menekan kejadian
dan keparahan BCMV pada tanaman kacang panjang di lapangan dibandingkan perlakuan tunggal dan kontrol.
SARAN
Perlu dilakukan kajian tentang pengendalian virus lain yang ditularkan serangga secara persisten yang berasosiasi dengan penyakit mosaik kuning kacang panjang di lapangan. Hal ini untuk dapat mengatasi infeksi dan penularan virus-virus tular serangga yang berasosiasi dengan penyakit mosaik kuning yang berbeda sifat penularannya.
14
DAFTAR PUSTAKA
[BPS] Badan Pusat Statistik. 2012. Produksi sayuran di Indonesia [internet]. Jakarta [ID]: Badan Pusat Statistik; [diunduh 2012 Desember 29]. Tersedia pada: http://www.bps.go.id /tab_sub/view.php.
Adijaya IN, Yasa MR, Sukadana M. 2005. Respon kacang panjang terhadap pemupukan organik dan anorganik di lokasi Prima Tani lahan kering Kecamatan Gerokgak,Kabupaten Buleleng, Bali [internet]. Bali [ID]: Balai Pengkajian Teknologi Pertanian Bali; [diunduh 2011 Okt 11]. Tersedia pada: pada: http://ntb.litbang.deptan.go.id/ind/2006/TPH/responkcpanjang. doc.
Agrios GN. 2005. Plant Pathology. Ed Ke-5. New York (US): Academic Press. Balogun OS, Xu L, Teraoka T, Hesokawa D. 2002. Effect of single and double
infectious with Potato Virus X and Tobacco mosaic virus on disease development, Plant growth, and virus accumulation in tomato. Fitopatol,
bras 7(3):241-248.
Blackman RL, Eastop VF. 2000. Aphids on the World Crop: An Identification and
Information Guide. London (UK): The Natural History Museum.
Damayanti TA, Alabi OJ, Naidu RA, Rauf N. 2009. Severe outbreak of a yellow mosaic disease on the yard long bean in Bogor, West Java. Hayati J Biosci. 16(2):78-82.
Fereres A. 2000. Barrier crops as a cultural control measure of non-persistently transmitted Aphid-borne viruses. Virus Res 71: 221-231.
Haryanto E, Suhartini T, Rahayu E. 2007. Budi Daya Kacang Panjang. Ed ke-14. Jakarta (ID): Penebar Swadaya.
Hersanti. 2007. Aktifitas peroksidase dan kandungan asam salisilat dalam tanaman cabai merah yang diinduksi ketahanannya terhadap Cucumbar
mosaic virus oleh ekstrak daun C. paniculatum. J Agrikultura 18(1):26-32.
Hooks, CRR, Fereres A. 2006. Protecting crops from non-persistently aphid-transmitted viruses : A review on the use of barrier plants as a management tool. Virus Res 120:1-6.
Ingwell LL, Eigenbrode SD, Bosque-Perez NA. 2012. Plant viruses alter insect behavior to enhance their spread. Scientific Reports (2:578):1-6.
Kurnianingsih L. 2010. Potensi lima ekstrak tumbuhan dalam menekan infeksi virus mosaik pada tanaman kacang panjang (Vigna unguiculata subsp.
sesquipedalis) [skripsi]. Bogor (ID) : Fakultas Pertanian, Institut Pertanian
Bogor.
Martin S, Elena FS. 2009. Application of game theory to the interaction between plant viruses during mix infections. J Gen Virol 90: 2815-2820.
Setyastuti L. 2008. Tingkat ketahanan sembilan kultivar kacang panjang terhadap infeksi Bean common mosaic virus (BCMV) [skripsi]. Bogor (ID): Fakultas Pertanian. Institut Pertanian Bogor.
Shiner, Finney. 1977. Di dalam: Strange RN. 2003. Introduction to Plant
mengendalikan penyakit mosaik pada tanaman kacang panjang (Vigna
sinensis L.) [PKM]. Bogor (ID): Fakultas Pertanian, Institut Pertanian
Bogor.
Susetio H. 2011. Penyakit mosaik kuning kacang panjang: respons kultivar kacang panjang (Vigna sinensis L.) dan efisiensi penularan melalui kutudaun (Aphis craccivora Koch.) [skripsi]. Bogor (ID): Fakultas Pertanian, Institut Pertanian Bogor.
Syller J. 2012. Facilitative and antagonistic interactions between plant viruses in mixed infection. Mol Plant Pathol 13(2):204-216.
Udayashankar AC, Nayaka SC, Kumar HB, Mortensen CN, Shetty HS, Prakash HS. 2010. Establishing inoculum threshold levels for Bean common mosaic
virus strain Blackeye cowpea mosaic infection in cowpea seed. African J Biotechnol 9(53):8958-8969.
Verma HN, Baranwal VK, Srisavasta S. 1996. Antiviral substances of plant origin. Di dalam: Hadidi A, Khetarpal RK, Koganezawa H, editor. 1998.
16
Lampiran 1 Kejadian penyakit pada minggu ke 1 – 8
Perlakuana Kejadian Penyakit
b
(MSPc) (%)
1 2 3 4 5 6 7 8
TP+EDP 0.0 ± 0.0 a 2.6 ± 5.3 b 23.7 ± 9.1 b 37.4 ± 5.5 b 44.8 ± 4.8 a 54.1 ± 7.4 b 62.9 ± 12.6b 72.6 ± 14.9a TP 0.0 ± 0.0 a 2.6 ± 2.2 b 21.9 ± 7.1 b 36.3 ± 3.4 b 45.2 ± 6.9 a 55.2 ± 7.1 b 60.4 ± 8.8 b 71.1 ± 9.0 a EDP 0.0 ± 0.0 a 15.6 ± 11.2ab 32.9 ± 9.9ab 40.4 ± 8.1 b 46.3 ± 6.5 a 57.4 ± 7.5 b 65.2 ± 7.3 ab 74.1 ± 8.9 a K 0.0 ± 0.0 a 24.8 ± 23.5a 43.3 ± 13.2a 53.3 ± 9.2 a 62.3 ±15.0a 66.7 ± 4.7 a 74.8 ± 5.4 a 77.8 ± 6.9 a a
TP+EDP= Tanaman pinggir + ekstrak daun pagoda. TP= Tanaman pinggir. EDP= Ekstrak daun pagoda. K=kontrol.
b Angka yang diikuti huruf yang berbeda pada kolom yang sama menunjukkan hasil berbeda nyata (uji selang berganda Duncan α = 5%). c Minggu setelah penularan.
Lampiran 2 Keparahan penyakit pada dari minggu ke 1-8
Perlakuana Keparahan Penyakit
b (MSPc) (%) 1 2 3 4 5 6 7 8 TP+EDP 0.0 ± 0.0 a 0.6 ± 1.3 b 7.1 ± 3.2 b 18.3 ± 4.3cb 26.3 ± 3.9 b 36.3 ± 3.4 b 44.8 ± 4.0 b 58.1 ± 8.0 b TP 0.0 ± 0.0 a 0.7 ± 0.7 b 6.5 ± 2.3 b 15.9 ± 3.5 c 24.5 ± 4.5 b 35.6 ± 5.5 b 44.0 ± 5.5 b 58.5 ± 6.9 b EDP 0.0 ± 0.0 a 4.1 ± 3.0 ab 12.7 ± 5.6 ab 22.4 ± 6.2 b 29.5 ± 5.2 ab 39.9 ± 6.6 b 46.7 ± 6.6 b 61.3 ± 5.5 b K 0.0 ± 0.0 a 7.5 ± 6.3 a 16.5 ± 8.7 a 30.6 ± 8.5 a 35.1 ± 9.0 a 49.4 ± 8.9 a 55.2 ± 7.3 a 75.8 ± 15.5a a TP+EDP= Tanaman pinggir + ekstrak daun pagoda. TP= Tanaman pinggir. EDP= Ekstrak daun pagoda. K=kontrol.
b Angka yang diikuti huruf yang berbeda pada kolom yang sama menunjukkan hasil berbeda nyata (uji selang berganda Duncan α = 5%). c
Minggu setelah penularan.
1
18
Lampiran 3 Rata-rata nilai absorban ELISA
Perlakuana NAEb Keteranganc
TP+EDP 0.202 ± 0.086 b -
TP 0.423 ± 0.306 ab +
EDP 0.432 ± 0.192 ab +
K 0.640 ± 0.248 a +
a TP+EDP= Tanaman pinggir + ekstrak daun pagoda, TP= Tanaman pinggir, EDP= Ekstrak daun pagoda, K=kontrol. NAE K (-) = 0.190.
b
Angka yang diikuti huruf yang berbeda pada kolom yang sama menunjukkan hasil berbeda nyata (uji selang berganda Duncan α = 5%).
c Sampel positif BCMV jika NAE sampel uji nilainya 2 x NAE kontrol (-). Lampiran 4 NAE sampel komposit pada 4 MSP
Perlakuan NAE Keterangana
Bufer 0.174 - Kontrol (-) 0.190 - Kontrol (+) 1.096 + TP + EDP 1 0.138 - TP + EDP 2 0.313 - TP + EDP 3 0.301 - TP + EDP 4 0.198 - TP + EDP 5 0.133 - TP + EDP 6 0.127 - TP 1 0.233 - TP 2 0.647 + TP 3 0.333 - TP 4 0.936 + TP 5 0.245 - TP 6 0.142 - EDP 1 0.303 - EDP 2 0.779 + EDP 3 0.444 + EDP 4 0.302 - EDP 5 0.497 + EDP 6 0.269 - K 1 0.544 + K 2 1.006 + K 3 0.711 + K 4 0.417 + K 5 0.809 + K 6 0.354 -
Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 2115 705 3.97 0.023
Error 20 3547 177
Total terkoreksi 23 5662
Lampiran 6 Hasil analisis ragam kejadian penyakit minggu ke 3 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 1750 583 5.73 0.005
Error 20 2036 102
Total terkoreksi 23 3787
Lampiran 7 Hasil analisis ragam kejadian penyakit minggu ke 4 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 1107.9 369.3 7.67 0.001
Error 20 962.9 48.1
Total terkoreksi 23 2070.8
Lampiran 8 Hasil analisis ragam kejadian penyakit minggu ke 5 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 237.6 79.2 1.82 0.176
Error 20 870.8 43.5
Total terkoreksi 23 1108.4
Lampiran 9 Hasil analisis ragam kejadian penyakit minggu ke 6 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 590.1 196.7 4.31 0.017
Error 20 913.5 45.7
Total terkoreksi 23 1503.7
Lampiran 10 Hasil analisis ragam kejadian penyakit minggu ke 7 pada taraf α=5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 715.2 238.4 2.99 0.055
Error 20 1594.3 79.7
20
Lampiran 11 Hasil analisis ragam kejadian penyakit minggu ke 8 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 147 49 0.45 0.718
Error 20 2166 108
Total terkoreksi 23 2314
Lampiran 12 Hasil analisis ragam keparahan penyakit minggu ke 2 pada taraf α=5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 3053 1018 4.96 0.010
Error 20 4103 205
Total terkoreksi 23 7156
Lampiran 13 Hasil analisis ragam keparahan penyakit minggu ke 3 pada taraf α=5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 6519 2173 4.43 0.015
Error 20 9808 490
Total terkoreksi 23 16327
Lampiran 14 Hasil analisis ragam keparahan penyakit minggu ke 4 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 12017 4006 7.11 0.002
Error 20 11266 563
Total terkoreksi 23 23283
Lampiran 15 Hasil analisis ragam keparahan penyakit minggu ke 5 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 6199 2066 3.62 0.031
Error 20 11417 571
Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 11580 3860 5.88 0.005
Error 20 13121 656
Total terkoreksi 23 24701
Lampiran 17 Hasil analisis ragam keparahan penyakit minggu ke 7 pada taraf α =5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 7607 2536 4.42 0.015
Error 20 11464 573
Total terkoreksi 23 19071
Lampiran 18 Hasil analisis ragam keparahan penyakit minggu ke 8 pada taraf α=5% Sumber keragaman Derajat bebas Jumlah kuadrat Kuadrat
tengah F hitung Nilai P
Perlakuan 3 1268.4 422.8 4.47 0.015
Error 20 1890.6 94.5
RIWAYAT HIDUP
Penulis dilahirkan di Kabupaten Kuantan Singingi, Kota Baserah, Riau pada tanggal 02 Februari 1990, dari pasangan Bapak Taslim dan Ibu Radilis S.Pd. Penulis merupakan anak pertama dari 2 bersaudara. Tahun 2008 penulis lulus dari SMA Negeri 1 Kuantan Hilir dan pada tahun yang sama penulis diterima di Institut Pertanian Bogor, Departemen Proteksi Tanaman melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama menempuh pendidikan di IPB, penulis aktif dalam unit kegiatan mahasiswa pada Tahap Persiapan Bersama (TPB) tahun 2008, unit kegiatan Himpunan Mahasiswa Proteksi Tanaman, unit kegiatan Keluarga Mahasiswa Riau Bogor dan Keluarga Mahasiswa Kuantan Singingi IPB pada tahun 2010-2012.