i PROPOSAL
PENELITIAN KERJA SAMA ANTAR PERGURUAN TINGGI (PAKERTI) DANA ITS TAHUN 2020
SINTESIS BIOKOMPOSIT BASIS MIKROKRISTALIN SELULOSA LIMBAH PERTANIAN DAN Zn-ZEOLIT SEBAGAI MATERIAL PACKAGING PANGAN
AKTIF
Tim Peneliti:
Prof. Dr. Didik Prasetyoko, M.Sc. (Kimia/FSAD/ITS) Dra. Ratna Ediati, MS., Ph.D (Kimia/FSAD/ITS)
Suprapto, Ph.D (Kimia/FSAD/ITS)
Susanti Dhini Anggraini, M.Si (Teknik Industri/FT/Unirow)
DIREKTORAT PENELITIAN DAN PENGABDIAN KEPADA MASYARAKAT INSTITUT TEKNOLOGI SEPULUH NOPEMBER
SURABAYA
ii DAFTAR ISI COVER PROPOSAL ... i DAFTAR ISI ... ii DAFTAR TABEL ... iv DAFTAR GAMBAR ... v BAB I. RINGKASAN ... 1
BAB II. PENDAHULUAN ... 2
2.1 Latar belakang ... 2
2.2 Perumusan dan Pembatasan Masalah ... 3
2.3 Tujuan ... 4
2.4 Relevansi ... 4
2.5 Luaran yang ditargetkan ... 4
BAB III. TINJAUAN PUSTAKA ... 6
3.1 Lada ... 6
3.2 Kemiri Sunan ... 7
3.3 Selulosa ... 8
3.4 Mikrokristalin selulosa ... 9
3.4.1 Mekanisme hidrolisis selulosa menjadi mikrokristalin selulosa ... 11
3.5 Kemasan aktif ... 12
3.6 Roadmap penelitian ... 13
3.6.1. Perumusan Topik Penelitian ... 14
3.6.2 Keterkaitan road map penelitian ... 15
3.7 Studi Pendahuluan ... 16
BAB IV. METODE ... 17
4.1 Metodologi ... 17
4.2 Alat dan Bahan ... 17
4.2 Prosedur ... 18
4.2.1 Preparasi limbah ... 18
4.2.2 Isolasi selulosa dari limbah ... 18
4.2.3 Isolasi selulosa dari mikrokristalin selulosa dengan hidrolisis asam ... 18
4.2.4 Karakterisasi Selulosa dan MCC ... 18
4.2.5 Sintesis Zn-Zeolit A ... 19
iii
4.2.7 Karakterisasi material biokomposit aktif ... 20
4.3 Organisasi tim peneliti ... 21
BAB V. JADWAL ... 22
5.1 Jadwal Penelitian ... 22
5.2 Anggaran Biaya ... 22
5.3 Justifikasi anggaran (Rincian Anggaran Biaya) ... 22
BAB VI. DAFTAR PUSTAKA ... 25
BAB VII. LAMPIRAN ... 31
7.1 Tim biodata peneliti ... 31
iv
DAFTAR TABEL
Tabel 1. Selulosa yang telah diisolasi dari limbah pertanian. ... 9 Tabel 2. Sifat fisikokimia dari mikrokristalin selulosa yang disintesis, komersial dan referen. . ... 16 Tabel 3. Variasi dalam pembuatan biokomposit... 20
v
DAFTAR GAMBAR
Gambar 1. Limbah pengolahan lada. ... 7
Gambar 2. Biji kemiri segar (a), kering dalam cangkang (b) dan kulit buah (c). ... 8
Gambar 3. Depolimerisasi selulosa menjadi mikrokristalin selulosa (Trache et al., 2016). .... 10
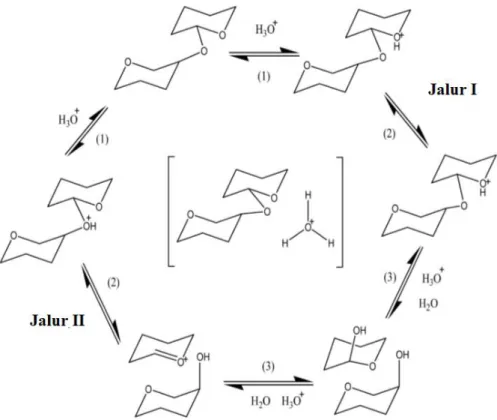
Gambar 4. Mekanisme hidrolisis asam pada ikatan glikosidik (Philipp et al., 1979). ... 12
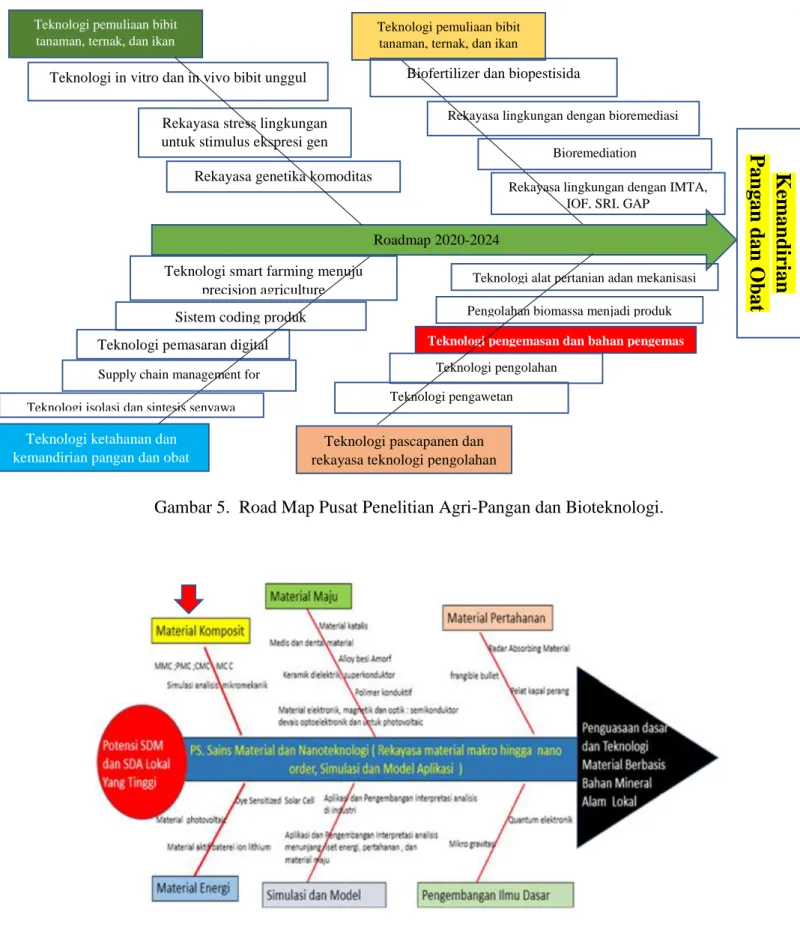
Gambar 5. Road Map Pusat Penelitian Agri-Pangan dan Bioteknologi. ... 15
Gambar 6. Road map riset Laboratorium Kimia Material dan Energi Kimia ITS. ... 15
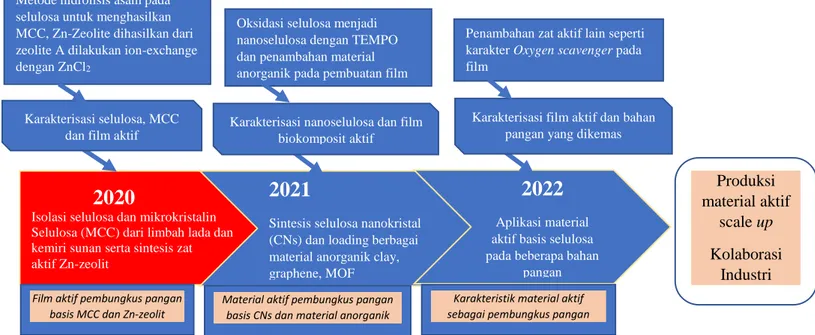
Gambar 7. Road map riset tentang material aktif packaging basis selulosa. ... 16
1
BAB I. RINGKASAN
Bioterorisme pangan telah menjadi perhatian utama pada era perdagangan global saat ini. Kemasan fungsional adalah inovasi yang diperlukan untuk mengakomodasi berbagai kebutuhan konsumen. Istilah kemasan aktif telah menjadi solusi untuk dikembangkan agar kepercayaan konsumen terhadap produk pangan semakin tinggi. Pengembangan material aktif sangat bervariasi tergantung fungsionalitas yang akan ditawarkan, serta bahan baku yang bersifat alami. Selulosa menjadi sumber utama yang dikembangkan pada teknologi active packaging, sebab ketersedian bahannya yang sangat melimpah. Namun pencarian sumber baru selulosa terus dilakukan oleh peneliti dengan berbagai alasan penting yang salah satunya adalah pemanfaatan limbah. Limbah pengolahan merica dan kulit kemiri sunan termasuk limbah pertanian yang melimpah di Indonesia, dan belum pernah dilaporkan sebelumnya diseluruh dunia sebagai sumber selulosa. Dalam proses aplikasinya, selulosa dihidrolisis menjadi mikrokristalin selulosa (MCC), dimana MCC berbentuk serbuk kristalin yang terdiri atas partikel berpori dan memiliki derajat polimerisasi ≤ 350, lebih baik jika diaplikasikan dalam pembuatan packaging pangan. Sifat fungsional yang akan dikembangkan adalah antibakteri. Hal ini dilakukan agar bahan pangan memiliki umur simpan yang lebih panjang dan menghindari kontaminan monomer plastik sintetik. Kemasan yang dikembangkan pada penelitian ini adalah material biokomposit aktif basis MCC limbah lada dan kulit kemiri dan peningkatan antibakteri biokomposit melalui penambahan Zn-zeolit A dimana zeolit A dilakukan modifikasi ukuran partikel (nanopartikel) yang dikombinasi dengan logam Zn.
Penelitian sintesis material aktif basis mikrokristalin selulosa dan Zn-zeolit A dirancang selama 1 tahun dengan proses isolasi dan karakterisasi selulosa dari 2 jenis limbah pertanian yang belum pernah dilaporkan sebelumnya yakni limbah lada dan kulit kemiri sunan. Selulosa yang dihasilkan dikonversi menjadi mikrokristalin selulosa dengan metode hidrolisis asam. Agen aktif yang ditambahkan terhadap biokomposit yakni Zn-zeolit A nanopartikel yang bertindak sebagai antibakteri. Selulosa dan MCC yang berhasil diiolasi dikarakterisasi menggunakn FT-IR, XRD, FT-Raman, SEM dan TGA-DSC. Selain itu, uji kndungan lignoselulosik pada selulosa dari kedua limbah dilakukan. Uji fisikokimia MCC yang dihasilkan juga dilakukan dan dibandingkan dengan MCC komersil (Avicel PH 101). Uji fisikokimia yang dilakukan yakni kadar air, kadar abu, densitas, water/oil holding capacity, pH dan indeks swelling. Biokomposit diformulasikan dengan mengkombinasi PLA, MCC dan Zn-zeolit A dengan pemlastis PEG. Material biokomposit yang dihasilkan dikarakterisasi termal dengan TGA-DSC, uji tarik, Water Vapor Permeability, ketebalan film dan uji antibakteri. Penelitian ini akan dilakukan selama 8 bulan dengan menargetkan publikasi jurnal internasional bereputasi Q2 “Journal of polymer research”. Penelitian ini diharapkan menghasilkan material aktif yang dapat digunakan sebagai kemasan pangan yang bersifat biodegradable.
2
BAB II. PENDAHULUAN
2.1 Latar belakang
Baru-baru ini, biomaterial sedang marak dikembangkan untuk mengurangi ketergantungan pada bahan bakar fosil [1,2]. Biomaterial lebih bersifat ramah lingkungan, mudah terdegradasi dan mengurangi penggunaan komposit berbasis minyak bumi karena bahan tersebut tidak dapat terurai secara hayati. Industri kemasan umumnya melirik komponen biopolimer komposit sebagai bahan baku yang bersifat aman dan ramah lingkungan [3–5]. Pencarian sumber biopolimer untuk kebutuhan biokomposit terus digalakkan untuk mendapatkan sumber yang sangat potensial dan tidak bertumbukan dengan kebutuhan pangan. Lignoselulosa memiliki potensi yang baik untuk tujuan ini karena mengandung serat selulosa, yang berlimpah, terbarukan, memiliki kekuatan tarik tinggi, dan menjadi produk sampingan yang relatif murah. Selulosa adalah biopolimer alami terbarukan yang jumlahnya sangat banyak [6,7]. Sumber selulosa yang sangat potensial dan melimpah adalah limbah pertanian [8]. Limbah pertanian adalah jenis limbah yang umumnya belum termanfaatkan dengan baik dan penangannya masih dengan cara pembakaran sehingga dapat menyebabkan polusi udara. Beberapa limbah pertanian yang telah digunakan sebagai sumber selulosa antara lain batang kapas [9], jerami [10], sekam padi dan kulit kacang [11], tandan kosong sawit [12,13], Daun sawit [14,15], Rami [16], kulit jeruk [17], kulit jagung dan jerami padi [18], kulit tomat [19], limbah teh [20], kulit Ensete glaucum (Roxb.) [21], limbah tebu [9,22], kulit biji sagu [23], limbah kulit nanas [24]. Limbah merica dan kulit kemiri sunan adalah limbah yang sangat potensial digunakan sebagai sumber selulosa karena dari uji pendahuluan kandungan selulosa berkisar 50-67% setelah proses purifikasi. Berdasarkan studi literatur, sampai saat ini kedua limbah tersebut belum pernah dimanfaatkan sebagai sumber selulosa.
Aplikasi selulosa pada biokomposit kurang banyak diminati, hal ini dikarenakan sifat dari selulosa yang mempunyai daya campur dengan polimer lain yang kurang baik. Oleh karena itu perlu adanya modifikasi selulosa menjadi mikro kristalin selulosa (MCC). Mikrokristalin selulosa merupakan α-selulosa yang terdepolimerisasi sebagian dan dimurnikan sampai berwarna putih, tidak berbau, tidak berasa, memiliki derajat polimerisasi ≤ 350, dan berbentuk serbuk kristalin yang terdiri atas partikel berpori [25]. Mikrokristalin selulosa dibuat dengan cara hidrolisis terkontrol α-selulosa, dengan larutan asam mineral encer pada suhu tinggi kemudian dicuci dengan air sampai bebas asam dikeringkan dan dihaluskan secara mekanis. Mikrokristalin selulosa menunjukkan sifat yang mudah mengalir dan merupakan bahan yang
3
dapat bertindak sebagai filler-binder disintegrant [26]. Hingga saat ini, pemanfaatan MCC telah banyak diaplikasikan pada pembuatan material packaging [20,26–33].
Inovasi kemasan aktif penting untuk dikembangakn. Kerusakan bahan pangan dapat terjadi melalui reaksi oksidasi dan kontaminasi bakteri sehingga dibutuhkan agen yang dapat bertindak secara indirect untuk pencegahan tersebut. Kemasan pangan aktif sangat dibutuhkan untuk menanggulangi hal tersebut. Penambahan agen antibakteri secara langsung dalam pengolahan tradisional kerap dilakukan, namun metode seperti ini terkadang tidak diijinkan akibat kadar komponen kimia yang tidak dapat dikendalikan [34,35]. Berbagai inovasi pengendalian bakteri sebagai cemaran patogen kedalam makanan kemasan telah berkembang pesat. Sebab penggunaan agen antimikroba basis chemical sangat mengkhawatirkan bagi kesehatan. Pada penelitian ini mengembangkan material zeolit sebagai agen antibakteri pada biokomposit. Zeolit umumnya diaplikasikan sebagai katalis reaksi kimia, namun laporan penelitian terbaru menunjukkan potensi zeolit sebagai agen antibakteri. Kenyó et al., [36] melaporkan bahwa untuk meningkatkan sifat antibakteri zeolit harus dilakukan proses pertukaran ion yaitu ion perak (Ag+). Mihaly-kozmuta et al., [37] melaporkan bahwa Ag-Zeolit menghambat pertumbuhan Escherichia coli, Bacillus subtilis, dan Staphylococcus aureus. Sedangkan Demirci et al., [38] melaporkan bahwa zeolit A dan X terimpregnasi ion perak, Cu dan Zn mampu menghambat pertumbuhan E. coli, Pseudomonas aeruginosa, dan S. aureus. Bahkan Faujasit terdoping ion perak menunjukkan antibakteri dan jamur [39]. Aktivitas antibakteri zeolit (Ag-Zeolit dan Zeolit/Ag) yang tinggi menunjukkan potensi aplikasi dalam plastik biokomposit sebagai agen antibakteri. Pada penelitian ini akan digunakan zeolit A dan logam Zn sebagai agen antibakteri dengan memodifikasi ukuran partikel pada zeolit menjadi nanopartikel untuk meningkatkan kinerja dari agen tersebut dan zeolit disintesis dari material alam yakni kaolin.
2.2 Perumusan dan Pembatasan Masalah
Perkembangan riset material biokomposit sangat pesat yang dimulai dari pencarian sumber biopolymer sampai pada peningkatan sifat fungsional. Limbah pengolahan lada dan kemiri adalah limbah organik yang sangat melimpah di Indonesia dan berdasarkan studi literatur belum pernah dilaporkan sebagai sumber selulosa. Berdasarkan uji pendahuluan, kedua limbah tersebut menunjukkan limbah potensial karena kandungan selulosa syang tinggi mencapai sekitar 55-67% setelah proses purifikasi. Selulosa yang dihasilkan dikonversi menjadi MCC untuk meningkatkan sifat kristalinitas dari selulosa agar memiliki karakter yang baik saat dijadikan biokomposit. Riset tentang biokompit sebagai bioplastik aktif secara nasional belum
4
menunjukkan perkembangan seperti dikawasan Eropa. Sehingga dalam penelitian ini merujuk pada review internasional dan menunjukkan bahwa penggunaan Zeolit A merupakan salah satu agen antibakteri pada food packaging. Zeolit A memiliki keunggulan dari zeolit tipe lainnya karena disintesis rendah Si. Kandungan Al yang tinggi memberikan sifat asam pada lingkungan pori sehingga meningkatkan laju deaktivasi mikroba yang terperangkap. Pada penelitian ini zeolit disintesis dari mineral alam yakni kaolin. Modifikasi ukuran zeolit menjadi nanopartikel juga dilakukan dan zeolit dikombinasi dengan logam Zn untuk meningkatkan sifat antibakteri. Zn sebagai logam antibakteri yang secara ekonomi memiliki nilai ekonomi rendah, sehingga sangat potensial digunakan. Biokomposit memiliki sifat biodegradable sehingga pada pembuatannya perlu dimodifikasi melalui peningkatan sifat hidrofobisitas dan blending dengan polimer sintetik.
2.3 Tujuan
Tujuan dari penelitian ini adalah
1. Memanfaatkan limbah pertanian seperti limbah pengolahan lada dan kemiri sunan sebagai sumber selulosa.
2. Melakukan konversi selulosa menjadi mikrokristalin selulosa sebagai biomaterial aktif. 3. Memanfaatkan Zn-zeolit A sebagai agen antibakteri efektif pada plastik biokomposit yang
bersifat asam, dimana zeolit A disintesis dari mineral alam yakni kaolin.
4. Menghasilkan material biokomposit aktif MCC/PLA/Zn-zeolit tinggi hidrofobisitas dan memiliki karakter termal yang baik yang dikombinasikan dengan PLA.
2.4 Relevansi
Penelitian ini akan memberikan hasil berupa biokomposit basis mikrokristalin selulosa dan Zn-zeolit A sebagai material aktif untuk packaging pangan. Penelitian ini sesuai dengan road map pusat Agri-Pangan dan Bioteknologi LPPM ITS terkait “teknologi pengemasan dan bahan pengemas”. Selain itu, penelitian ini juga in-line dengan road map riset Laboratorium Kimia Material dan Energi ITS. Penelitian akan memberikan kontribusi berarti bagi pengembangan IPTEK dalam bidang pengembangan material packaging. Studi isolasi MCC dari kedua limbah tersebut dilakukan optimasi untuk menghasilkan MCC dalam jumlah optimum.
2.5 Luaran yang ditargetkan
Target dari penelitian ini adalah
1. Publikasi dalam jurnal internasional terindex scopus yaitu di jurnal “Journal of Polymer Research” dengan impact factor 1.823 (Q2),
2. Seminar internasional “5th International Conference of Chemical Engineering & Industrial Biotechnology”
5
Hasil penelitian ini diharapkan dapat memberikan informasi terkait sumber selulosa terbaru dengan memanfaatkan limbah pertanian seperti limbah pengolahan lada dan kulit buah kemiri sunan yang belum dimanfaatkan dengan baik sampai saat ini dan selulosa ini dapat dimanfaatkan dalam pembuatan kemasan biodegradable. Selain itu, material biodegradable ini dikembangkan menjadi material aktif yang memiliki karakter antibakteri dengan memanfaatkan Zn-zeolit A sebagai material anorganik yang bertindak sebagai agen antibakteri agar bahan pangan memiliki umur simpan yang panjang, menghindari loss nutrition serta kontaminan monomer kemasan plastik sintetik. Peningkatan jumlah plastik di Indonesia yang diproduksi dari material ini maka dapat mengurangi penggunaan plastik sintetik yang ada.
6
BAB III. TINJAUAN PUSTAKA
3.1 Lada
Indonesia merupakan produsen dan eksportir utama lada di dunia dan termasuk dalam lima besar negara produsen lada di dunia khususnya lada hitam dan lada putih, dan pada tahun 2018 Indonesia berada di peringkat keempat dalam hal produksi lada dunia. Kedudukan lada sebagai komoditi ekspor hasil perkebunan cukup penting, yaitu nomor enam setelah karet, kelapa sawit, kakao, kopi dan kelapa. Lada juga dikenal dengan nama King of Spices (Raja Rempah) untuk golongan komoditas rempah-rempah. Kontribusi lada Indonesia di pasar dunia pada 2019 adalah sebesar 17 persen dari produksi lada dunia dan merupakan produsen lada terbesar kedua di dunia setelah Vietnam [40]. Berdasarkan peran dan potensi ekonomi komoditas lada di atas, dapat dikatakan bahwa lada merupakan salah satu komoditas unggulan dan mempunyai potensi yang besar dalam pertumbuhan ekonomi Indonesia. Hal ini antara lain juga didasari oleh besarnya potensi dan peluang ke depan yang dimiliki Indonesia dalam perdagangan lada di pasar internasional.
Prospek komoditas lada Indonesia juga dapat dilihat dari potensi pasar domestik yang cukup besar, yaitu dengan semakin berkembangnya industri makanan yang menggunakan bumbu dari lada dan industri kesehatan yang menggunakan lada sebagai obat serta meningkatnya preferensi masyarakat dalam menggunakan lada sebagai penyedap makanan. Daerah sebagai penghasil lada terbesar di Indonesia antara lain Provinsi Bangka, Provinsi Bengkulu, Provinsi Kalimantan Timur, Provinsi Kalimantan Barat, Provinsi Sulawesi Tenggara, Provinsi Sulawesi Selatan. Dilihat dari luas lahan tenaman lada di seluruh Indonesia, pada tahun 2019 Indonesia memiliki luas lahan perkebunan lada sebesar 172.615 Ha dengan produksi sekitar 91.941 ton yang tersebar di 29 provinsi dan hampir seluruhnya dikelola oleh rakyat 99,90% dengan melibatkan sekitar 298.913 KK petani di lapangan [40].
Seiring dengan meningkatnya jumlah lada di Indonesia akan menyebabkan jumlah limbah yang meningkat pula. Sampai saat ini, belum terdapat data yang melaporkan terkait pemanfaatan limbah pengolahan lada sebagai sumber selulosa. Limbah pengolahan lada berupa tangkai lada yang diperoleh dari perontokan biji lada. Limbah tangkai lada hanya dibakar dan menyebabkan polusi udara. Limbah lada yang digunakan pada penelitian ini ditunjukkan pada Gambar 1.
7
Gambar 1. Limbah pengolahan lada.
3.2 Kemiri Sunan
Kemiri Sunan (Reutealis trisperma (Blanco) Airy Shaw), tanaman penghasil minyak nabati berpotensi sebagai bahan bakar nabati. Kemiri sunan bersifat non-edible, tidak bisa dikonsumsi seperti halnya kemiri bumbu. Tanaman ini dapat menghasilkan 50 kg biji kering per pohon per tahun dengan kadar minyak 50-56 persen. Suatu potensi yang sangat menjanjikan. Dengan kadar minyak dan potensi produksi seperti ini berarti dalam satu hektar dengan populasi 100 pohon dapat menghasilkan 5 ton biji kering, setara dengan 2,5 ton minyak, lebih tinggi dibanding potensi produksi yang dihasilkan kelapa sawit. Kemiri sunan dapat ditemukan pada ketinggian hingga 1000 m di atas permukaan laut. Tanaman kemiri sunan tergolong tanaman menahun tinggi > 15 meter dengan mahkota yang sangat rindang, kanovi daun lebar, struktur daun sangat rapat, ranting yang banyak, dan memiliki perakaran yang dalam, tanaman berumur panjang lebih dari 30 tahun usianya, tanaman ini dapat tumbuh di lahan datar, bergelombang, bertebing curam, lahan kritis (Oetami, 2012) dan buah kemiri sunan beracun terutama bijinya, sehingga tumbuhan ini baik untuk pohon peneduh, konservasi alam dan bahan bakar nabati biodiesel. Tanaman ini bisa tumbuh optimal sampai pada ketinggian maksimal 1.000 m dpl, dengan suhu 18,7 – 26,2°C pada pH 5,4 – 7,1 [41].
Kemiri sunan merupakan pohon dengan kanopi lebar, rapat, mampu menahan butiran air hujan sehingga tidak langsung menimpa tanah dan berakar tungggang, menyebar ke dalam ke samping yang berfungsi meningkatkan penyerapan air tanah dan mencegah longsor sehingga sangat baik sebagai tanaman konservasi untuk mencegah erosi dan bahan bakar biodiesel. Sampai saat ini, kemiri sunan telah dimanfaatkan minyaknya untuk dikonversi menjadi biodiesel [42,43] dan sedang digalakkan kedepannya untuk menghasilkan bodiesel skala besar. Pohon kemiri telah dibudidayakan diberbagai daerah di Indonesia antara lain di wilayah Jawa,
8
Nusa Tenggara, Sulawesi dan Papua. Sampai saat ini kulit buah dari kemiri sunan belum dimanfaatkan, hanya dibiarkan menjadi limbah atau dibakar [41]. Biji kemiri segar, kering dalam cangkang dan kulit buah ditunjukkan pada Gambar 2.
Gambar 2. Biji kemiri segar (a), kering dalam cangkang (b) dan kulit buah (c).
3.3 Selulosa
Serat pangan terdiri atas komponen serat yang larut, dan yang tidak larut. Contoh serat yang tidak larut air yaitu selulosa, hemiselulosa, dan lignin, sedangkan yang larut air yaitu pektin, gum, sebagian hemiselulosa, glukan dan mukilase. Selulosa adalah suatu polimer linier panjang (C6H10O5)n yang dibentuk oleh lebih 100-2000 molekul D-glukosa dengan ikatan
1,4-ß-glikosidik. Selulosa banyak terdapat pada dinding sel tumbuhan. Hemiselulosa adalah polimer bercabang beragam dari molekul heksosa, pentosa, dan asam uronat. Lignin, merupakan zat pengikat antara molekul-molekul selulosa. Serat larut air, seperti pektin adalah polimer yang terbentuk dari ramnosa dan asam galakturonat. Adapun gum, senyawa karboksimetil selulosa atau biasa disebut CMC adalah suatu polimer turunan selulosa yang disusun oleh molekul glukosa, galaktosa, manosa, arabinosa, ramnosa, dan asam uronat. Mukilase banyak terdapat pada bebijian dan akar, sedangkan glukan banyak terdapat pada serelia [22].
Selulosa adalah senyawa seperti serabut, tidak larut dalam air dan ditemukan di dalam sel pelindung tanaman, terutama pada tangkai, batang, dahan semua bagian berkayu dari jaringan tumbuhan [44]. Senyawa ini termasuk suatu polisakarida yang tak larut dalam air dan merupakan zat pembentuk kulit sel tanaman. Selulosa terdapat lebih dari 50% dalam kayu, berwarna putih, mempunyai kulit tarik yang besar. Selain terdapat dalam kayu, selulosa juga terkandung dalam beberapa tanaman lain seperti pelepah pohon pisang dan sekam padi [45]. Selulosa tidak pernah ditemukan dalam keadaan murni di alam, tetapi selalu berasosiasi dengan polisakarida lain seperti lignin, pektin, hemiselulosa, dan xilan. Selulosa membentuk komponen serat dari dinding sel tumbuhan. Molekul selulosa merupakan rantai-rantai atau mikrofibril dan D-glukosa sampai sebanyak 14.000 satuan yang terdapat berkas-bekas terpuntir
9
mirip tali yang terikat satu sama lain oleh ikatan hidrogen [46]. Kebanyakan selulosa berasosiasi dengan lignin sehingga sering disebut sebagai lignoselulosa. Selulosa mempunyai rumus kimia (C6H10O5) dan berat molekul 162. Beberapa sumber selulosa dari limbah pertanian
yang telah dilaporkan sebelumnya ditunjukkan pada Tabel 1. Limbah meica dan kemiri sunan akan digunakan pada penelitian ini.
Tabel 1. Selulosa yang telah diisolasi dari limbah pertanian.
No. Sumber Referensi
1. Batang kapas [9]
2. Jerami [10]
3. Sekam padi [11]
4. Kulit kacang [11]
5. Tandan kosong sawit [12,13]
6. Daun sawit [14,15] 7. Rami [16] 8. Kulit jeruk [17] 9. Kulit jagung [18] 10. Jerami padi [18] 11. Kulit tomat [19] 12. Limbah teh [20]
13. Kulit Ensete glaucum (Roxb.) [21]
14. Limbah tebu [9,22]
15. Kulit biji sagu [23]
16. Limbah kulit nanas [24]
17. Limbah merica Pada penelitian ini
18. Kulit kemiri sunan Pada penelitian ini
3.4 Mikrokristalin selulosa
Molekul selulosa mikrokristalin terdiri dari rantai sekitar 250 molekul glukosa. Mikrokristalin selulosa adalah stabilizer makanan terbentuk dari komponen alami yang digunakan dalam produk makanan. Jumlah efektif dari komponen alami yang disediakan untuk produk makanan untuk menjaga stabilitas fisik selama masa simpannya John [47]. Selulosa dapat larut segera dalam asam pekat, pelarutan dalam asam pekat mengakibatkan pemecahan rantai selulosa secara hidrolitik [21]. Mikrokristal Selulosa merupakan selulosa yang mengalami proses hidrolisis sebagian dan umumnya memiliki diameter 1-100 µm dengan persentase kristalin sebesar 55% - 85% [48]. Mikrokristalin selulosa dapat dihasilkan dengan mereaksikan selulosa di dalam larutan asam mineral yang mendidih selama waktu tertentu sampai batas derajat polimerisasi (level-off DP) tercapai [18]. Proses tersebut bertujuan untuk
10
menurunkan berat molekul, derajat polimerisasi, dan panjang rantai selulosa sehingga membentuk mikrokristalin [20]. Produksi mikrokristal selulosa menggunakan cara hidrolisis asam di bawah kendali waktu dan suhu yang dapat menghilangkan bagian amorf selulosa hingga membentuk kristal selulosa.
Pembuatan mikrokristalin selulosa perlu dilakukan isolasi selulosa terlebih dahulu untuk memperoleh selulosa murni. Proses yang dilakukan meliputi, proses delignifikasi, bleaching dan hidrolisis untuk memperoleh mikrokristalin selulosa sesuai persyaratan. Proses delignifikasi bertujuan untuk melarutkan kandungan lignin dalam kayu sehingga mempermudah pemisahan lignin dengan serat [49]. Tahapan isolasi selulosa menggunakan bleaching agent untuk menghilangkan lignin maupun hemiselulosa yang masih tersisa pada serat karena warna kecoklatan pada serat berasal dari lignin maka dari itu perlu dilakukan proses bleaching. Proses bleaching biasanya digunakan bahan kimia H2O2 dan NaOCl untuk
mengilangkan komponen berwarna atau mengubahnya menjadi zat yang tidak berwarna [50].
Gambar 3. Depolimerisasi selulosa menjadi mikrokristalin selulosa [1].
Kristal selulosa merupakan blok kristal yang berdampingan dengan blok amorf secara acak di sepanjang serat selulosa. Menghilangkan blok amorf mempengaruhi struktur dan kristalinitas serat selain itu, stabilitas suhu dan morfologi permukaan serat akan terpengaruh oleh hilangnya bagian amorf [51]. Pada dinding sel tanaman hidup, mikrokristal selulosa memainkan peran utama dalam struktur dinding sel serta memberikan kekuatan yang kokoh. Depolimerisasi selulosa menjadi mikrokristal selulosa melalui hidrolisis asam disajikan pada Gambar 3. Mikrokristalin selulosa adalah bahan tambahan penting di bidang farmasi, makanan, kosmetik, dan industri lainnya [52]. Bahkan, akhir-akhir ini MCC telah banyak dikembangkan
11
dalam packaging pangan. Mikrokristalin selulosa di pasaran dikenal dengan Avicel, banyak jenis Avicel misalnya Avicel PH 101 yang digunakan dalam penelitian ini. Avicel PH 101 merupakan nama dagang dari mikrokristalin selulosa (MCC). Kombinasi MCC dengan polimer lain seperti PVA, PLA, HDPE, LDPE telah dilaporkan oleh banyak peneliti [27,29,30]. MCC dapat mengubah performa dari film dengan meningkatkan tensile strength dan elongation at break pada film [30,33,53].
3.4.1 Mekanisme hidrolisis selulosa menjadi mikrokristalin selulosa
Mikrokristalin selulosa didapatkan dari hidrolisis selulosa menggunakan mineral asam. Selulosa mengandung -1,4-ikatan glikosidik yang mengikat unit hydroglucopyranose ke dalam rantai panjang. Selulosa pecah menjadi glukosa dan mereduksi gula (oligosakarida) tanpa
pembentukan produk dehidrasi yang sangat besar, misalnya asam levulinat serta 5-hidroksimetilfurfural. Saat selulosa dilarutkan dalam larutan asam seperti HCl, selulosa
menjadi larut dalam media reaksi. H+ bergerak menuju ikatan glikosidik sementara Cl−
melemahkan ikatan glikosidik untuk memfasilitasi proses hidrolisis. Saat ikatan glikosidik putus, struktur ikatan-H pada selulosa mulai terbuka. Dari reaksi ini, glukosa dan gula reduksi diproduksi dengan hasil yang sama atau lebih tinggi. Ion hidronium (H3O+) akan dibentuk
dengan protonasi dari asam selama degradasi glukosa dan hidrolisis selulosa [54].
Berdasarkan Gambar 4, protonasi oksigen glikosidik terjadi di jalur I sedangkan protonasi oksigen piran terjadi pada jalur II. Protonasi parsial dari kedua atom oksigen terjadi selama pembatasan konformasi rantai selulosa sepanjang ikatan glikosidik. Selama hidrolisis asam, pembentukan karbokation melalui langkah unimolekular adalah salah satu hal yang penting langkah-langkahnya, dapat melalui siklus di jalur I atau jalur II dari mekanisme tersebut. Pengetahuan ilmiah pertama untuk hidrolisis asam selulosa dengan asam sulfat dikenal sebagai proses Scholler, yang ditemukan pada 1920-an, sedangkan proses Berglus disebut penggunaan asam klorida dalam hidrolisis selulosa. Li dan Zhao [55] melaporkan bahwa asam fosfat kurang efektif untuk hidrolisis asam sedangkan asam nitrat dan asam klorida memiliki kesamaan perilaku terhadap asam sulfat tanpa pretreatment. Asam kuat memiliki potensi dalam protonasi oksigen glikosidik karena nilai pKa yang lebih rendah dibandingkan dengan asam lemah sebagai oksigen glikosidik adalah basa lemah. Untuk hidrolisis asam yang lebih baik dalam prosesnya, kekuatan keasaman menggambarkan peranan yang penting [56].
12
Gambar 4. Mekanisme hidrolisis asam pada ikatan glikosidik.
3.5 Kemasan aktif
Kemasan aktif memiliki karakter yang tidak seperti bahan kemasan makanan konvensional, sistem kemasan makanan aktif memiliki karakter inhibisi terhadap oksigen [57], mengadsorb kelembaban [58], penghasil CO2 [59], peredam etilen [60], antimikroba [61] atau
agen antijamur [62]. Ahmed et al., [63] melaporkan bahwa kemasan makanan aktif juga tergantung pada komponen fungsional yang terdapat dalam matriks, bahan pengemas dapat memiliki aktivitas intrinsiknya, seperti karakter antioksidan, antimikroba, dan antijamur pada makanan yang dikemas.
Kemasan antibakteri memiliki agen antimikroba yang terkandung dalam kemasan untuk menginhibisi tumbuhnya mikroba dan kontaminasi selama penyimpanan dan transportasi. Beberapa peneliti telah melaporkan beberapa agen aktibakteri yang telah digabungkan dalam kemasan antara lain essential oils, polikation, kitosan dan perak [63] untuk meningkatkan keamanan makanan yang terkemas terhadap mikroba dan jamur. Akhir akhir ini sedang marak dikembangkan material anorganik berpori digunakan sebagai support antibakteri yang digabung dengan metal [62]. Salah satu material berpori yang sedang marak dikembangkan adalah zeolit.
Zeolit terdiri dari silikon, aluminium, dan oksigen dalam framework dengan kation, air di dalam pori-pori, pada dasarnya adalah silikat alumina nanopori. Silika adalah tetrahedronin reguler yang netral di mana muatan positif ion silikon seimbang dengan oksigen. Namun
13
tedapat muatan negatif yang tidak seimbang dalam struktur alumina. Oleh karena itu, struktur total zeolit memiliki muatan negatif, dan muatan ini diseimbangkan dengan kation (terutama oleh Na+ atau K+). Kation ini dapat ditukar dalam larutan dengan ion positif yang diinginkan seperti logam berat atau ion amonium [38]. Kapasitas pertukaran kation tergantung pada rasio silika/alumina dalam struktur. Secara umum, zeolit dengan rasio silika/alumina (Si/ Al) yang rendah memiliki kapasitas pertukaran ion yang lebih tinggi. Menurut rasio Si/Al, ada beberapa jenis zeolit alam dan sintetik termasuk zeolit-β, zeolit-A, zeolit-X, dan zeolit-Y, yang merupakan adsorben komersial paling umum. Rumus umum zeolit ditunjukkan dalam persamaan sebagai Mx/n[(AlO2)x(SiO2)y]·zH2O di mana M berarti kation [64]. Zeolit telah
banyak digunakan dalam berbagai aplikasi tidak hanya sebagai katalis, hal ini dikarenakan zeolit memiliki karakter struktur yang baik, pengikatan reversibel dengan molekul kecil, selektivitas bentuk dan ukuran, dan kemampuan zeolit berperilaku seperti metaloenzim. Selain sifat-sifat tersebut zeolit juga tidak beraroma, tidak berbau, dan tidak berbahaya, karakteristik antimikroba dapat diperoleh melalui proses pertukaran ion. Ion yang paling umum digunakan dalam proses pertukaran adalah perak karena stabilitas dan spektrum luas dari efek antibakteri [65]. Telah dilaporkan bahwa perak yang digabungkan dengan zeolit ditemukan bersifat antibakteri terhadap Escherichia coli, Bacillus subtilis dan Staphylococcus aureus [66]. Selanjutnya, zeolit tipe X juga telah digabung dengan perak untuk memiliki efek bakterial terhadap E. coli, Pseudomonas aeruginosa dan S. aureus [67]. Terlepas dari zeolit sintetis, zeolit alami juga telah dibuat antibakteri melalui proses pertukaran kation. Zeolit faujasit yang diolah dengan perak telah diproduksi, dan sifat antimikrobanya telah diperiksa terhadap bakteri dan ragi. Selain itu, logam berat lainnya, terutama seng, tembaga, nikel, merkuri, timah, timah, bismut, kadmium, kromium, dan talium telah digunakan dalam prosedur pertukaran ion untuk membuat zeolit alami dan antimikroba sintetis [68]. Beberapa peneliti yang telah mengembangkan zeolit sebagai agen antibakteri dalam film yaitu Demirci et al., [69], Shing et al.,[70], Mihaly-Cozmuta et al., [71], Kenyó et al., [36] and Youssef et al., [65]
3.6 Roadmap penelitian
Penelitian ini sesuai dengan road map riset di salah satu pusat riset di LPPM ITS yaitu pusat penelitian Agri-Pangan dan Bioteknologi terkait “Teknologi Pengemasan dan bahan pengemas” (Gambar 5) dan road map riset di Laboratorium Kimia Material dan Energi ITS (Gambar 6). Kegiatan riset pada pendaan ini dapat ditunjukkan pada Gambar 7. Penelitian ini fokus pada pemanfaatan limbah pertanian seperti limbah lada dan kemiri sunan sebagai sumber
14
selulosa yang kemudian dihidrolisis menjadi MCC. Material aktif diproses dengan mengkombinasikan PLA dan Zn-zeolit A. Zn-zeolit A nanopartikel sebagai agen antibakteri.
3.6.1. Perumusan Topik Penelitian
Isu Strategis Konsep
Pemikiran/Rasional
Pemecahan Masalah Topik Riset yang Diperlukan
Peningkatan jumlah limbah kemasan plastik sintetik dan bioterorisme pangan. Bioterorisme pangan merupakan pelepasan cemaran virus, bakteri dan jamur yang dapat merusak pangan dan membahayakan konsumen.
Regulasi pemerintah yang kurang tepat menyebabkan produksi kemasan berbahan plastik sintetik terus
meningkat sehingga kerusakan lingkungan akibat
penumpukan dan sulitnya terdegradasi telah menjadi masalah utama di Indonesia. Selain itu, penggunaan plastik sintetik sebagai kemasan pangan pda kondisi dan waktu tertentu akan melepaskan monomer yang bersifat toksik. Pengembangan bahan pangan harus sejalan dengan
berkembangnya inovasi kemasan. Inovasi kemasan aktif diperlukan untuk meningkatkan shelf life dari bahan pangan.
Diperlukan produksi material biokomposit basis biopolimer. Indonesia merupakan negara agraris yang dapat memanfaatkan limbah pertanian sebagai sumber produksi kemasan pangan. Salah satu sumber alami melimpah yang dapat dijadikan sumber bahan pengemas yakni selulosa. Limbah pertanian sangat cocok dijadikan sumber selulosa karena umumnya
penanggulangan limbah pertanian hanya dengan proses pembakaran limbah yang
menyebabkan polusi. Perkembangan bahan pengemas sedang marak dikembangkan, tidak hanya sifat biodegradable dari bahan yang
digunakan akan tetapi juga memiliki sisi aktif seperti sifat antibakteri yang dapat
memperpanjang umur simpan bahan pangan.
1. Isolasi dan karakterisasi selulosa dan mikrokristalin selulosa dari limbah pertanian seperti limbah lada dan kulit kemiri sunan yang belum pernah dilaporkan
2. Sintesis plastik biokomposit basis mikrokristalin selulosa dan penambahan zat aktif seperti zat antibakteri basis zeolit.
3. Sintesis plastik biokomposit basis nanokristalin selulosa dan melakukan variasi zat aktif yang lainnya
4. Identifikasi karakteristik film biokomposit terbaik dan uji self life.
15 3.6.2 Keterkaitan road map penelitian
Gambar 5. Road Map Pusat Penelitian Agri-Pangan dan Bioteknologi.
Gambar 6. Road map riset Laboratorium Kimia Material dan Energi Kimia ITS. Teknologi pemasaran digital
Roadmap 2020-2024
Kem
a
ndi
ri
a
n
P
a
ng
a
n d
a
n Ob
a
t
Teknologi pemuliaan bibit tanaman, ternak, dan ikan
Teknologi in vitro dan in vivo bibit unggul
Rekayasa stress lingkungan untuk stimulus ekspresi gen
Rekayasa genetika komoditas
Teknologi pemuliaan bibit tanaman, ternak, dan ikan
Biofertilizer dan biopestisida
Rekayasa lingkungan dengan bioremediasi
Bioremediation
Rekayasa lingkungan dengan IMTA, IOF, SRI, GAP
Teknologi pengemasan dan bahan pengemas
Teknologi pengolahan
Pengolahan biomassa menjadi produk komersial
Sistem coding produk
Teknologi smart farming menuju
precision agriculture Teknologi alat pertanian adan mekanisasi
Teknologi pengawetan Supply chain management for
Agrifood
Teknologi pascapanen dan rekayasa teknologi pengolahan
pangan
Teknologi isolasi dan sintesis senyawa
Teknologi ketahanan dan kemandirian pangan dan obat
16
Gambar 7. Road map riset tentang material aktif packaging basis selulosa.
3.7 Studi Pendahuluan
Studi pendahuluan yang telah dilakukan dalam penelitian ini yakni sintesis mikrokristalin selulosa dari limbah industri lada (Industrial Pepper Waste/IPW). Tiga tahapan proses isolasi selulosa meliputi alkalisasi, hidrolisis asam dan re-alkalisasi menggunakan autoclave. Isolasi selulosa telah berhasil dilakukan dengan yield 67.9 ± 0.8%. Selanjutnya mikrokristalin selulosa disintesis melalui hidrolisis selulosa menggunakan HCl 3,5 N pada temperatur 70 ℃ selama 2 jam. Optimum yield serta kristalinitas mikrokristalin selulosa yang diperoleh sebesar 86% dan 78.9%. Sifat fisikokimia dari mikrokristalin selulosa yang disintesis (IPW-MCC), komersial (C-MCC) dan referen (E. glaucum MCC) ditampilkan pada Tabel 2. IPW-MCC telah berhasil disintesis dan memiliki sifat fisikokimia yang sesuai dengan standar (komersial) dan referen.
Tabel 2. Sifat fisikokimia dari mikrokristalin selulosa yang disintesis, komersial dan referen
a Pachuau et al., (2019).
Parameter IPW-MCC C-MCC E. glaucum MCCa
Kelembaban (%) 5.30 ± 0.20 5.15 ± 0.30 5.75 ± 0.15
Konten abu (%) 0.13 ± 0.03 0.15 ± 0.01 0.11 ± 0.02
Densitas (g/cm3) 1.412 ± 0.02 1.398 ± 0.02 1.478 ± 0.03
pH 5.90 ± 0.03 6,05 ± 0.02 5.34 ± 0.01
Kapasitas penahanan air 6.75 ± 0.05 2.64 ± 00.4 -
Kapasitas penahanan minyak
5.10 ± 0.03 2.73 ± 0.03 -
Index swelling 1.625 ± 0.29 1.267 ± 0.25 1.833 ± 0.47
2020
Isolasi selulosa dan mikrokristalin Selulosa (MCC) dari limbah lada dan kemiri sunan serta sintesis zat aktif Zn-zeolit
2021
Sintesis selulosa nanokristal (CNs) dan loading berbagai material anorganik clay, graphene, MOF
2022
Aplikasi material aktif basis selulosa pada beberapa bahan
pangan
Film aktif pembungkus pangan basis MCC dan Zn-zeolit
Material aktif pembungkus pangan basis CNs dan material anorganik
Karakteristik material aktif sebagai pembungkus pangan
Karakterisasi selulosa, MCC dan film aktif
Karakterisasi nanoselulosa dan film biokomposit aktif
Karakterisasi film aktif dan bahan pangan yang dikemas
Produksi material aktif
scale up Kolaborasi
Industri
Metode hidrolisis asam pada selulosa untuk menghasilkan MCC, Zn-Zeolite dihasilkan dari zeolite A dilakukan ion-exchange dengan ZnCl2
Oksidasi selulosa menjadi nanoselulosa dengan TEMPO dan penambahan material anorganik pada pembuatan film
Penambahan zat aktif lain seperti karakter Oxygen scavenger pada film
17
BAB IV. METODE
4.1 Metodologi
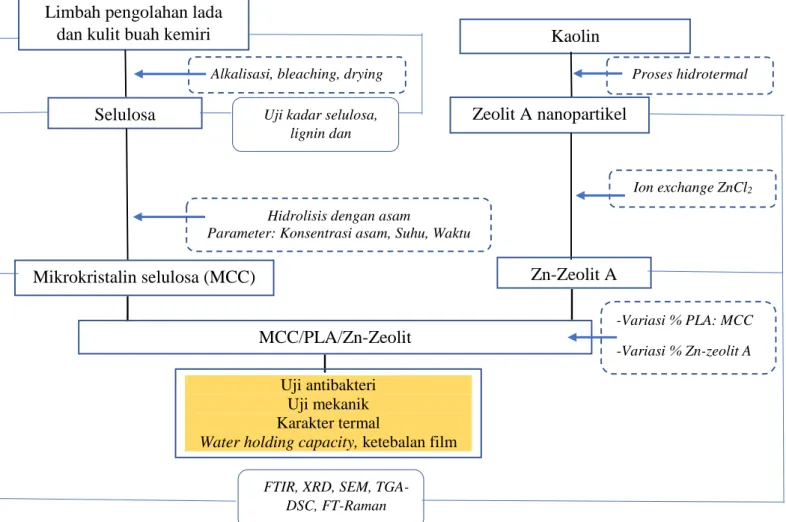
Penelitian ini terdiri dari empat tahap utama, yaitu isolasi selulosa dari limbah kulit buah kemiri sunan, hidrolisis selulosa menjadi mikrokristalin selulosa dengan HCl, sintesis zat antibakteri Zn-zeolit A dan pembuatan film packaging. Skema/alur kerja penelitian Pakerti ditunjukkan pada Gambar 7.
Gambar 8. Skema kerja penelitian. 4.2 Alat dan Bahan
Bahan utama yang digunakan pada penelitian ini adalah limbah pengolahan lada dan kulit buah kemiri sunan. Semua bahan yang digunakan dalam pekerjaan ini bersifat pure analisis. Beberapa bahan kimia yang digunakan yakni sodium hidroksida (NaOH, ≥99%), asam klorida (HCl, ≥37%), hidrogen peroksida (H2O2), Avicel PH 101 (Sigma-Aldrich). Avicel PH 101 (merek komersial selulosa mikrokristalin) digunakan untuk membandingkan dengan MCC yang dihasilkan.
Limbah pengolahan lada dan kulit buah kemiri
Selulosa
Alkalisasi, bleaching, drying
Hidrolisis dengan asam
Parameter: Konsentrasi asam, Suhu, Waktu
Mikrokristalin selulosa (MCC) Kaolin Zeolit A nanopartikel Proses hidrotermal Zn-Zeolit A Ion exchange ZnCl2 MCC/PLA/Zn-Zeolit -Variasi % PLA: MCC -Variasi % Zn-zeolit A Uji antibakteri Uji mekanik Karakter termal
Water holding capacity, ketebalan film
FTIR, XRD, SEM, TGA-DSC, FT-Raman Uji kadar selulosa,
lignin dan hemiselulosa
18
Peralatan yang digunakan antara lain peralatan gelas, timbangan analitik, reaktor autoclave, furnace, oven, sonikator, stirer, pompa vakum, FT-IR, FT-Raman, XRD, SEM, Universal Testing Machine dan TGA-DSC.
4.2 Prosedur
4.2.1 Preparasi limbah
Proses pengolahan limbah diawali dengan limbah dipisahkan dari bagian yang tidak diinginkan dan direndam dalam air deionisasi selama 4 jam pada 80°C sambil distirer. Setelah proses ini selesai, limbah disaring, dikeringkan dalam oven pada suhu 100°C selama 24 jam dan kemudian dipotong kecil-kecil. Limbah kering itu digiling menjadi bubuk.
4.2.2 Isolasi selulosa dari limbah
Isolasi selulosa dilakukan berdasarkan metode yang dilaporkan oleh Collazo-Bigliardi et al., [18]; Zhao et al., [20] dan Prado et al., [24] dengan sedikit modifikasi. 5% NaOH ditambahkan ke sampel dan diaduk konstan pada 90°C selama 2 jam untuk mendapatkan campuran yang homogen. Rasio sampel terhadap larutan natrium hidroksida adalah 1:20 (b/v). Kemudian, disaring dan dicuci beberapa kali dengan air deionisasi sampai pH netral. Untuk menghilangkan hemiselulosa residu dan lignin, 1 g residu netral limbah ditambahkan dengan 40 mL campuran 16% (v/v) H2O2 dan 5% NaOH pada suhu 55°C selama 90 menit, sambil diaduk. Setelah ini, campuran didinginkan pada suhu kamar dan disaring. Hasilnya dicuci dengan air deionisasi sampai pH 6. Untuk memastikan bahwa lignin dan hemiselulosa telah dihilangkan. Proses alkalisasi dilakukan lagi. Sampel diperlakukan dengan NaOH seperti di atas dalam autoklaf pada 90°C selama 1 jam, disaring dan kemudian dicuci dengan air deionisasi sampai pH netral. Residu netral yang diperoleh adalah selulosa dan dikeringkan pada suhu 60°C sampai massa konstan.
4.2.3 Isolasi selulosa dari mikrokristalin selulosa dengan hidrolisis asam
Selulosa yang diisolasi dari limbah dihidrolisis dengan asam klorida untuk menghasilkan MCC. MCC dipreparasi sesuai dengan yang telah dilaporkan oleh Hussin et al., [14] dan Zhao et al., [20] dengan sedikit modifikasi. Selulosa ditambahkan HCl (2,5-4,5 N), raasio selulosa terhadap HCl (1:20, b/v) dilakukan. Campuran diaduk selama 60-180 menit pada suhu 50-80°C. Mikrokristalin selulosa disaring dan dicuci dengan air suling sampai pH netral. MCC dikeringkan pada 60°C selama 24 jam dan disimpan untuk diproses lebih lanjut.
4.2.4 Karakterisasi Selulosa dan MCC
Selulosa dan MCC yang dihasilkan dilakukan uji kandungan lignoselulosik dan dikarakterisasi dengan berbagai instrumen. FT-IR digunakan untuk mengetahui karakter
19
seluloa dan MCC yang terbentuk melalui pendekatan gugs fungsi. SEM digunakan untuk mengetahui karakter morfologi dari selulosa dan MCC dr kedua jenis limbah. Selain itu, analisis fasa dan kristalinitas dari sampel dilakukan karakterisasi menggunakan XRD yang dikonfirmasi dengan FT-Raman. Karakter termal dari selulosa dan MCC dikarakterisasi menggunakan TGA-DSC. Selain itu, untuk mengetahui karakteristik MCC yang dihasilkan perlu dilakukan uji sifat fisikokimia seperti kadar air, pH, abu, densitas, water holding capacity dan oil holding capacity dan indeks swelling.
4.2.5 Sintesis Zn-Zeolit A
Zeolit NaA nanopartikel disintesis dari kaolin dengan metode tanpa templat dan suhu kristalisasi yang rendah. Tahap awal dimulai dengan proses metakaolinisasi kaolin melalui kalsinasi pada suhu 600°C selama 2 jam untuk membentuk fase metakaolin yang bersifat lebih aktif, kemudian dilanjutkan dengan tahap sintesis. Penyiapan mother liquor dilakukan dengan pembuatan masing-masing sebanyak 500 mL NaOH dengan dengan konsentrasi 1M, 2M, 3M, 4M, dan 5M dengan cara melarutkan padatan NaOH menggunakan air deionisasi. Metakaolin ditambahkan pada larutan alkalin masing-masing konsentrasi dengan rasio solid/liquid 1,0 g/25 mL sambil dilakukan pengadukan selama 3 hari pada suhu ruang. Hasil sintesis disaring dengan menggunakan penyaring Buchner dan filtrat yang diperoleh ditampung sebagai mother liquor tahap 1. Padatan yang diperoleh dicuci dengan air deionisasi sebanyak 3 kali kemudian dikeringkan dengan oven pada suhu 100°C selama 24 jam. Prosedur ini diulangi sampai penggunaan mother liquor tahap 5. Zeolit NaA yang dihasilkan kemudian dilanjutkan proses ion exchange dengan ZnCl2 untuk menghasilkan Zn-Zeolit A dengan proses refluks. Zn-zeolite
A yang dihasilkan kemudian dikarakterisasi dengan FT-IR, XRD dan SEM.
4.2.6 Preparasi material biokomposit
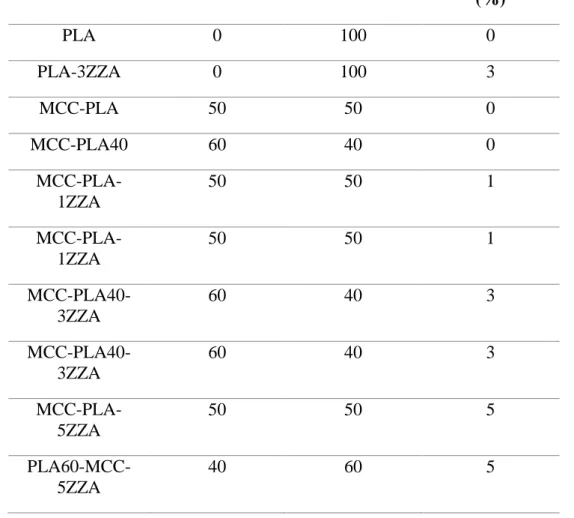
Mikrokristalin selulosa dibuat dengan melarutkan MCC dalam 100 mL air deionisasi pada 70°C di bawah pengadukan magnetik dan dilanjutkan dengan sonikasi. Demikian pula, larutan PLA dibuat dengan menambahkan PLA ke 100 ml air terdeionisasi pada 70°C dan diaduk hingga larut sempurna. Kemudian variasi PLA: MCC (sesuai Tabel 3) disiapkan dengan mencampur secara mekanis larutan kedua polimer dan disimpan di bawah pengadukan mekanis selama 4 jam. Setelah itu PEG sebanyak 5% terhadap PLA sebagai pemlastis ditambahkan. Campuran diaduk selama 1 jam. MCC/PLA yang telah disiapkan dicampur secara mekanis dengan Zn-zeolit A (1%, 3% dan 5% b/v) diikuti dengan sonikasi untuk 1 jam pada suhu kamar. MCC/PLA/Zn-zeolit A homogen dituangkan ke dalam cawan Teflon untuk diuapkan.
20
Tabel 3. Variasi dalam pembuatan biokomposit.
Sampel MCC (%) PLA (%) Zn-Zeolit A
(%) PLA 0 100 0 PLA-3ZZA 0 100 3 MCC-PLA 50 50 0 MCC-PLA40 60 40 0 MCC-PLA-1ZZA 50 50 1 MCC-PLA-1ZZA 50 50 1 MCC-PLA40-3ZZA 60 40 3 MCC-PLA40-3ZZA 60 40 3 MCC-PLA-5ZZA 50 50 5 PLA60-MCC-5ZZA 40 60 5
4.2.7 Karakterisasi material biokomposit aktif
Material biokomposit yang dihasilkan dikarakterisasi secara termal dengan TGA-DSC dan dilakukan uji tarik menggunakan Universal Testing Machine. Selain itu karakteristik ketebalan dan water vapor permeability dari material juga diuji. Untuk menguji karakter aktif dari biokomposit, uji antibakteri dilakukan antara lain terhadap bakteri Escherichia coli, Bacillus subtilis, dan Staphylococcus aureus.
21 4.3 Organisasi tim peneliti
No Nama/NIDN Institusi Asal Alokasi Waktu (jam/minggu) Uraian Tugas 1 Prof. Dr. Didik Prasetyoko, M.Sc/ 0016067108 Kimia FSAD ITS
10 - Peneliti Utama melakukan studi literatur, merancang pekerjaan, mengkoordinasi pekerjaan.
- Memonitor aktivitas pekerjaan di laboratorium - Sintesis zeolit dan Zn-zeolit
serta karakterisasinya - Menulis publikasi ilmiah 2 Dra Ratna Ediati, MS.,
Ph.D/0022066013
Kimia FSAD ITS
8 - Sintesis film aktif dan karakterisasinya
- Analisis data, diskusi hasil, menyimpulkan hasil penelitian dan turut
membantu dalam penulisan publikasi di jurnal ilmiah 3. Suprapto,
Ph.D/0019097206
Kimia FSAD ITS
8 - Analisis hasil karakterisasi material aktif (uji termal, uji tarik, uji antibakteri, WVP) - Turut membantu dalam
penulisan publikasi di jurnal ilmiah 4. Susanti Dhini Anggraini, M.Si/0723128804 Teknik Industri FT Unirow
8 - Isolasi selulosa dan MCC serta karakterisasinya - Analisis data, diskusi hasil,
menyimpulkan hasil penelitian dan menulis publikasi di jurnal ilmiah 5. Dr. Hasliza bahruji Universiti
Brunei Darussalam - - Menyediakan laboratorium untuk karakterisasi 6. Holilah/ 01211960010005 Mahasiswa S3 20 - Melaksanakan penelitian disertasi 7. Asranudin/0121196001 0005 Mahasiswa S3 20 - Melaksanakan penelitian disertasi
22
BAB V. JADWAL 5.1 Jadwal Penelitian
Jadwal penelitian pembuatan material packaging aktif ini dilakukan kurang lebih selama 8 bulan, secara rinci ditunjukkan pada Tabel dibawah ini:
No Uraian Bulan ke
1 2 3 4 6 7 8
1 Pengambilan bahan baku limbah pengolahan merica dan kulit kemiri
2 Pengadaan bahan-bahan habis pakai 3 Isolasi selulosa dari limbah pertanian 4 Karakterisasi selulosa
5 Hidrolisis selulosa menjadi mikrokristalin selulosa (MCC)
s6 Karakterisasi MCC
7 Sintesis dan karakterisasi Zn-zeolit 8 Pembuatan film biokomposit 9 Karakterisasi film aktif 10 Seminar Internasional
11 Laporan Kemajuan dan monitoring
12 Submit artikel ilmiah ke jurnal internasional 13 Laporan Akhir Penelitian
5.2 Anggaran Biaya
No Kegiatan Biaya (Rp)
1. Belanja Honorarium 4.800.000
1 Belanja Bahan 11.200.000
2 Belanja Barang non
Operasional Lainnnya 28.600.000
3 Biaya Perjalanan Lainnya 5.000.000
4 Belanja lain lain 400.000
Jumlah total 50.000.000
5.3 Justifikasi anggaran (Rincian Anggaran Biaya)
1. Belanja Honorarium Item Honorarium
Volume Satuan Honor/Jam
(Rp) Total (Rp)
Tenaga administrasi 8 OB 300.000 2.400.000
Pembantu peneliti 98 OJ 25.000 2.400.000
23 3. Belanja Barang Non Operasional Lainnya
Item Barang Volume Satuan Harga Satuan (Rp) Total (Rp)
FTIR 15 sampel 100.000 1.500.000
XRD 15 sampel 100.000 1.500.000
SEM 10 sampel 500.000 5.000.000
TGA-DSC 15 sampel 350.000 5.250.000
Uji tarik 10 sampel 500.000 5.000.000
Uji antibakteri 10 sampel 300.000 3.000.000
Uji kadar selulosa, hemiselulosa
dan lignin 5 sampel 250.000 1.250.000
FT-Raman 2 sampel 550.000 1.100.000
Biaya Internasional Seminar 1 unit 5.000.000 5.000.000
Sub Total 3 (Rp) 28.600.000
4. Belanja Perjalanan Lainnya
Item Perjalanan Volume Satuan BiayaSatuan (Rp) Total (Rp)
Tiket perjalanan seminar 1 OK 2.000.000 2.000.000
Penginapan di seminar 3 OH 500.000 1.500.000
Transportasi lokal
Tuban-Surabaya 3 OH 500.000 1.500.000
Sub Total 4 (Rp) 5.000.000
5. Belanja Lain-lain 2. Belanja Bahan
Item Bahan Volume Satuan Harga satuan (Rp) Total (Rp)
NaOH 1 Kg 1.500.000 1.500.000
HCl 1 L 1.250.000 1.250.000
NaOCl 1 250mL 1.150.000 1.150.000
H2O2 1 L 2.250.000 2.250.000
Air Deionisasi 20 L 5.000 100.000
Kertas saring 10 Lembar 20.000 200.000
PLA 1 Kg 1.850.000 1.850.000
PEG 1 L 1600000 1.600.000
ZnCl2 1 500g 1300000 1.300.000
24
Item Volume Satuan Biaya Satuan (Rp) Total (Rp)
Cetak laporan kemajuan dan akhir 1 8 50.000 400.000
Sub Total 5 (Rp) 400.000
25
BAB VI. DAFTAR PUSTAKA
[1] D. Trache, M.H. Hussin, C.T. Hui Chuin, S. Sabar, M.R.N. Fazita, O.F.A. Taiwo, T.M. Hassan, M.K.M. Haafiz, Microcrystalline cellulose: Isolation, characterization and bio-composites application—A review, Int. J. Biol. Macromol. 93 (2016) 789–804. https://doi.org/10.1016/j.ijbiomac.2016.09.056.
[2] S.M.L. Rosa, N. Rehman, M.I.G. De Miranda, S.M.B. Nachtigall, C.I.D. Bica, Chlorine-free extraction of cellulose from rice husk and whisker isolation, Carbohydr. Polym. 87 (2012) 1131–1138. https://doi.org/10.1016/j.carbpol.2011.08.084.
[3] J.W. Rhim, H.M. Park, C.S. Ha, Bio-nanocomposites for food packaging applications,
Prog. Polym. Sci. 38 (2013) 1629–1652.
https://doi.org/10.1016/j.progpolymsci.2013.05.008.
[4] A.M. Youssef, S.M. El-Sayed, Bionanocomposites materials for food packaging applications: Concepts and future outlook, Carbohydr. Polym. 193 (2018) 19–27. https://doi.org/10.1016/j.carbpol.2018.03.088.
[5] H. Namazi, A. Dadkhah, Convenient method for preparation of hydrophobically modified starch nanocrystals with using fatty acids, Carbohydr. Polym. 79 (2010) 731– 737. https://doi.org/10.1016/j.carbpol.2009.09.033.
[6] A. Haque, D. Mondal, I. Khan, M.A. Usmani, A.H. Bhat, U. Gazal, Fabrication of composites reinforced with lignocellulosic materials from agricultural biomass, in: Lignocellul. Fibre Biomass-Based Compos. Mater. Process. Prop. Appl., Elsevier Inc., 2017: pp. 179–191. https://doi.org/10.1016/B978-0-08-100959-8.00010-X.
[7] P. Kumar, D.M. Barrett, M.J. Delwiche, P. Stroeve, Methods for pretreatment of lignocellulosic biomass for efficient hydrolysis and biofuel production, Ind. Eng. Chem. Res. 48 (2009) 3713–3729. https://doi.org/10.1021/ie801542g.
[8] A. Merci, R.G. Marim, A. Urbano, S. Mali, Films based on cassava starch reinforced with soybean hulls or microcrystalline cellulose from soybean hulls, Food Packag. Shelf Life. 20 (2019). https://doi.org/10.1016/j.fpsl.2019.100321.
[9] M. El-Sakhawy, M.L. Hassan, Physical and mechanical properties of microcrystalline cellulose prepared from agricultural residues, Carbohydr. Polym. 67 (2007) 1–10. https://doi.org/10.1016/j.carbpol.2006.04.009.
[10] A.M. Bochek, I.L. Shevchuk, V.N. Lavrent’ev, Fabrication of microcrystalline and powdered cellulose from short flax fiber and flax straw, Russ. J. Appl. Chem. 76 (2003) 1679–1682. https://doi.org/10.1023/B:RJAC.0000015737.07117.12.
[11] A.M. Adel, Z.H. Abd El-Wahab, A.A. Ibrahim, M.T. Al-Shemy, Characterization of microcrystalline cellulose prepared from lignocellulosic materials. Part II: Physicochemical properties, Carbohydr. Polym. 83 (2011) 676–687. https://doi.org/10.1016/j.carbpol.2010.08.039.
[12] M.K. Mohamad Haafiz, S.J. Eichhorn, A. Hassan, M. Jawaid, Isolation and characterization of microcrystalline cellulose from oil palm biomass residue, Carbohydr. Polym. 93 (2013) 628–634. https://doi.org/10.1016/j.carbpol.2013.01.035.
26
microcrystalline cellulose from oil palm fibres for food applications, Carbohydr. Polym. 148 (2016) 11–20. https://doi.org/10.1016/j.carbpol.2016.04.055.
[14] M.H. Hussin, N.A. Pohan, Z.N. Garba, M.J. Kassim, A.A. Rahim, N. Brosse, M. Yemloul, M.R.N. Fazita, M.K.M. Haafiz, Physicochemical of microcrystalline cellulose from oil palm fronds as potential methylene blue adsorbents, Int. J. Biol. Macromol. 92 (2016) 11–19. https://doi.org/10.1016/j.ijbiomac.2016.06.094.
[15] A.F. Owolabi, M.K.M. Haafiz, M.S. Hossain, M.H. Hussin, M.R.N. Fazita, Influence of alkaline hydrogen peroxide pre-hydrolysis on the isolation of microcrystalline cellulose from oil palm fronds, Int. J. Biol. Macromol. 95 (2017) 1228–1234. https://doi.org/10.1016/j.ijbiomac.2016.11.016.
[16] S.M.A.S. Keshk, M.A. Haija, A new method for producing microcrystalline cellulose from Gluconacetobacter xylinus and kenaf, Carbohydr. Polym. 84 (2011) 1301–1305. https://doi.org/10.1016/j.carbpol.2011.01.024.
[17] P.M. Ejikeme, Investigation of the physicochemical properties of microcrystalline cellulose from agricultural wastes I: Orange mesocarp, Cellulose. 15 (2008) 141–147. https://doi.org/10.1007/s10570-007-9147-7.
[18] S. Collazo-Bigliardi, R. Ortega-Toro, A. Chiralt Boix, Isolation and characterisation of microcrystalline cellulose and cellulose nanocrystals from coffee husk and comparative study with rice husk, Carbohydr. Polym. 191 (2018) 205–215. https://doi.org/10.1016/j.carbpol.2018.03.022.
[19] Y. Liu, A. Liu, S.A. Ibrahim, H. Yang, W. Huang, Isolation and characterization of microcrystalline cellulose from pomelo peel, Int. J. Biol. Macromol. 111 (2018) 717– 721. https://doi.org/10.1016/j.ijbiomac.2018.01.098.
[20] T. Zhao, Z. Chen, X. Lin, Z. Ren, B. Li, Y. Zhang, Preparation and characterization of microcrystalline cellulose (MCC) from tea waste, Carbohydr. Polym. 184 (2018) 164– 170. https://doi.org/10.1016/j.carbpol.2017.12.024.
[21] L. Pachuau, R.S. Dutta, L. Hauzel, T.B. Devi, D. Deka, Evaluation of novel microcrystalline cellulose from Ensete glaucum (Roxb.) Cheesman biomass as sustainable drug delivery biomaterial, Carbohydr. Polym. 206 (2019) 336–343. https://doi.org/10.1016/j.carbpol.2018.11.013.
[22] R. Katakojwala, S.V. Mohan, Microcrystalline cellulose production from sugarcane bagasse: Sustainable process development, J. Clean. Prod. (2019) 119342. https://doi.org/10.1016/j.jclepro.2019.119342.
[23] S. Naduparambath, J. T.V., V. Shaniba, S. M.P., A.K. Balan, E. Purushothaman, Isolation and characterisation of cellulose nanocrystals from sago seed shells, Carbohydr. Polym. 180 (2018) 13–20. https://doi.org/10.1016/j.carbpol.2017.09.088. [24] K.S. Prado, M.A.S. Spinacé, Isolation and characterization of cellulose nanocrystals
from pineapple crown waste and their potential uses, Int. J. Biol. Macromol. 122 (2019) 410–416. https://doi.org/10.1016/j.ijbiomac.2018.10.187.
[25] L.K. Kian, M. Jawaid, H. Ariffin, O.Y. Alothman, Isolation and characterization of microcrystalline cellulose from roselle fibers, Int. J. Biol. Macromol. 103 (2017) 931– 940. https://doi.org/10.1016/j.ijbiomac.2017.05.135.
27
Mateo, Improvement on the properties of microcrystalline cellulose/polylactic acid composites by using activated biochar, J. Clean. Prod. 252 (2020) 119898. https://doi.org/10.1016/j.jclepro.2019.119898.
[27] R.D. Kale, V.G. Gorade, N. Madye, B. Chaudhary, P.S. Bangde, P.P. Dandekar, Preparation and characterization of biocomposite packaging film from poly(lactic acid) and acylated microcrystalline cellulose using rice bran oil, Int. J. Biol. Macromol. 118 (2018) 1090–1102. https://doi.org/10.1016/j.ijbiomac.2018.06.076.
[28] S. Ummartyotin, C. Pechyen, Microcrystalline-cellulose and polypropylene based composite: A simple, selective and effective material for microwavable packaging, Carbohydr. Polym. 142 (2016) 133–140. https://doi.org/10.1016/j.carbpol.2016.01.020. [29] B.Y. Alashwal, M. Saad Bala, A. Gupta, S. Sharma, P. Mishra, Improved properties of keratin-based bioplastic film blended with microcrystalline cellulose: A comparative
analysis, J. King Saud Univ. - Sci. 32 (2020) 853–857.
https://doi.org/10.1016/j.jksus.2019.03.006.
[30] S. Mohan Bhasney, K. Mondal, A. Kumar, V. Katiyar, Effect of microcrystalline cellulose [MCC] fibres on the morphological and crystalline behaviour of high density polyethylene [HDPE]/polylactic acid [PLA] blends, Compos. Sci. Technol. 187 (2020) 107941. https://doi.org/10.1016/j.compscitech.2019.107941.
[31] X. Kong, S. Zhang, Y. Wang, Y. Liu, R. Li, X. Ren, T.S. Huang, Antibacterial polyvinyl alcohol films incorporated with N-halamine grafted oxidized microcrystalline cellulose, Compos. Commun. 15 (2019) 25–29. https://doi.org/10.1016/j.coco.2019.06.005. [32] S.M. Vasquez Mejia, A. de Francisco, B.M. Bohrer, Replacing starch in beef emulsion
models with β-glucan, microcrystalline cellulose, or a combination of β-glucan and
microcrystalline cellulose, Meat Sci. 153 (2019) 58–65.
https://doi.org/10.1016/j.meatsci.2019.03.012.
[33] S. Mohan Bhasney, A. Kumar, V. Katiyar, Microcrystalline cellulose, polylactic acid and polypropylene biocomposites and its morphological, mechanical, thermal and rheological properties, Compos. Part B Eng. 184 (2020) 107717. https://doi.org/10.1016/j.compositesb.2019.107717.
[34] A.A. Hamid, H.A. Abdulmumeen, A.N. Risikat, A.R. Sururah, Composition and bioactivities of Essential Oils View project Review on Antioxidants View project Food: Its preservatives, additives and applications, Ijcbs. 1 (2012) 36–47. https://doi.org/10.13140/2.1.1623.5208.
[35] M.M. Tajkarimi, S.A. Ibrahim, D.O. Cliver, Antimicrobial herb and spice compounds
in food, Food Control. 21 (2010) 1199–1218.
https://doi.org/10.1016/j.foodcont.2010.02.003.
[36] C. Kenyó, K. Renner, J. Móczó, E. Fekete, C. Kröhnke, B. Pukánszky, Hips/zeolite hybrid composites as active packaging materials: Structure and functional properties, Eur. Polym. J. 103 (2018) 88–94. https://doi.org/10.1016/j.eurpolymj.2018.01.013. [37] A. Mihaly-Cozmuta, A. Peter, G. Craciun, A. Falup, L. Mihaly-Cozmuta, C. Nicula, A.
Vulpoi, M. Baia, Preparation and characterization of active cellulose-based papers modified with TiO2, Ag and zeolite nanocomposites for bread packaging application, Cellulose. 24 (2017) 3911–3928. https://doi.org/10.1007/s10570-017-1383-x.
28
[38] S. Demirci, Z. Ustaoǧlu, G.A. Yilmazer, F. Sahin, N. Baç, Antimicrobial properties of zeolite-X and zeolite-A ion-exchanged with silver, copper, and zinc against a broad range of microorganisms, Appl. Biochem. Biotechnol. 172 (2014) 1652–1662. https://doi.org/10.1007/s12010-013-0647-7.
[39] P. Dutta, B. Wang, Zeolite-supported silver as antimicrobial agents, Coord. Chem. Rev. 383 (2019) 1–29. https://doi.org/10.1016/j.ccr.2018.12.014.
[40] Direktorat Jenderal Perkebunan., (2019). Statistik Perkebunan Lada.
[41] Oetami.T.P., (2020). Wawancara tentang Kemiri Sunan, PT. Agrindo, Gresik.
[42] H. Holilah, D. Prasetyoko, T.P. Oetami, E.B. Santosa, Y.M. Zein, H. Bahruji, H. Fansuri, R. Ediati, J. Juwari, The potential of Reutealis trisperma seed as a new non-edible source for biodiesel production, Biomass Convers. Biorefinery. 5 (2015) 347– 353. https://doi.org/10.1007/s13399-014-0150-6.
[43] K. Kusmiyati, D. Prasetyoko, S. Murwani, M. Nur Fadhilah, T.P. Oetami, H. Hadiyanto, W. Widayat, A. Budiman, A. Roesyadi, Biodiesel Production from Reutealis Trisperma Oil Using KOH Impregnated Eggshell as a Heterogeneous Catalyst, Energies. 12 (2019) 3714. https://doi.org/10.3390/en12193714.
[44] J.M. Rieland, B.J. Love, Ionic liquids: A milestone on the pathway to greener recycling of cellulose from biomass, Resour. Conserv. Recycl. 155 (2020) 104678. https://doi.org/10.1016/j.resconrec.2019.104678.
[45] A.H. Bhat, I. Khan, M.A. Usmani, R. Umapathi, S.M.Z. Al-Kindy, Cellulose an ageless renewable green nanomaterial for medical applications: An overview of ionic liquids in extraction, separation and dissolution of cellulose, Int. J. Biol. Macromol. 129 (2019) 750–777. https://doi.org/10.1016/j.ijbiomac.2018.12.190.
[46] S. Coseri, Cellulose: To depolymerize… or not to?, Biotechnol. Adv. 35 (2017) 251– 266. https://doi.org/10.1016/j.biotechadv.2017.01.002.
[47] J. Nsor-Atindana, M. Chen, H.D. Goff, F. Zhong, H.R. Sharif, Y. Li, Functionality and nutritional aspects of microcrystalline cellulose in food, Carbohydr. Polym. 172 (2017) 159–174. https://doi.org/10.1016/j.carbpol.2017.04.021.
[48] L. Brinchi, F. Cotana, E. Fortunati, J.M. Kenny, Production of nanocrystalline cellulose from lignocellulosic biomass: Technology and applications, Carbohydr. Polym. 94 (2013) 154–169. https://doi.org/10.1016/j.carbpol.2013.01.033.
[49] M.S. Jahan, A. Saeed, Z. He, Y. Ni, Jute as raw material for the preparation of
microcrystalline cellulose, Cellulose. 18 (2011) 451–459.
https://doi.org/10.1007/s10570-010-9481-z.
[50] H.K. Singh, T. Patil, S.K. Vineeth, S. Das, A. Pramanik, S.T. Mhaske, Isolation of microcrystalline cellulose from corn stover with emphasis on its constituents: Corn
cover and corn cob, Mater. Today Proc. (2019).
https://doi.org/10.1016/j.matpr.2019.12.065.
[51] F. Potůček, M. Milichovský, Kraft Pulp Bleaching with Hydrogen Peroxide and Peracetic Acid*, n.d.
[52] K. Das, D. Ray, • N R Bandyopadhyay, Study of the Properties of Microcrystalline Cellulose Particles from Different Renewable Resources by XRD, FTIR,
29
Nanoindentation, TGA and SEM, (n.d.). https://doi.org/10.1007/s10924-010-0167-2. [53] L. Xiao, Y. Mai, F. He, L. Yu, L. Zhang, H. Tang, G. Yang, Bio-based green composites
with high performance from poly(lactic acid) and surface-modified microcrystalline
cellulose, J. Mater. Chem. 22 (2012) 15732–15739.
https://doi.org/10.1039/c2jm32373g.
[54] R. Rinaldi, F. Schüth, Acid hydrolysis of cellulose as the entry point into biorefinery
schemes, ChemSusChem. 2 (2009) 1096–1107.
https://doi.org/10.1002/cssc.200900188.
[55] C. Li, Z.K. Zhao, Efficient acid-catalyzed hydrolysis of cellulose in ionic liquid, Adv. Synth. Catal. 349 (2007) 1847–1850. https://doi.org/10.1002/adsc.200700259.
[56] M. Karim, Z. Chowdhury, S. Hamid, M. Ali, Statistical Optimization for Acid Hydrolysis of Microcrystalline Cellulose and Its Physiochemical Characterization by Using Metal Ion Catalyst, Materials (Basel). 7 (2014) 6982–6999. https://doi.org/10.3390/ma7106982.
[57] A. Dey, S. Neogi, Oxygen scavengers for food packaging applications: A review, Trends Food Sci. Technol. 90 (2019) 26–34. https://doi.org/10.1016/j.tifs.2019.05.013.
[58] R. Gaikwad, A. Bansode, A. Urakawa, High-pressure advantages in stoichiometric hydrogenation of carbon dioxide to methanol, J. Catal. 343 (2016) 127–132. https://doi.org/10.1016/j.jcat.2016.02.005.
[59] D.S. Lee, Carbon dioxide absorbers for food packaging applications, Trends Food Sci. Technol. 57 (2016) 146–155. https://doi.org/10.1016/j.tifs.2016.09.014.
[60] I. Majid, G. Ahmad Nayik, S. Mohammad Dar, V. Nanda, Novel food packaging technologies: Innovations and future prospective, J. Saudi Soc. Agric. Sci. 17 (2018) 454–462. https://doi.org/10.1016/j.jssas.2016.11.003.
[61] G.F. El Fawal, A.M. Omer, T.M. Tamer, Evaluation of antimicrobial and antioxidant activities for cellulose acetate films incorporated with Rosemary and Aloe Vera essential oils, J. Food Sci. Technol. 56 (2019) 1510–1518. https://doi.org/10.1007/s13197-019-03642-8.
[62] P. Dutta, B. Wang, Zeolite-supported silver as antimicrobial agents, Coord. Chem. Rev. 383 (2019) 1–29. https://doi.org/10.1016/j.ccr.2018.12.014.
[63] I. Ahmed, H. Lin, L. Zou, A.L. Brody, Z. Li, I.M. Qazi, T.R. Pavase, L. Lv, A comprehensive review on the application of active packaging technologies to muscle
foods, Food Control. 82 (2017) 163–178.
https://doi.org/10.1016/j.foodcont.2017.06.009.
[64] C. Kenyó, K. Renner, J. Móczó, E. Fekete, C. Kröhnke, B. Pukánszky, Hips/zeolite hybrid composites as active packaging materials: Structure and functional properties, Eur. Polym. J. (2018). https://doi.org/10.1016/j.eurpolymj.2018.01.013.
[65] H.F. Youssef, M.E. El-Naggar, F.K. Fouda, A.M. Youssef, Antimicrobial packaging film based on biodegradable CMC/PVA-zeolite doped with noble metal cations, Food Packag. Shelf Life. 22 (2019) 100378. https://doi.org/10.1016/j.fpsl.2019.100378. [66] J. Milenkovic, J. Hrenovic, D. Matijasevic, M. Niksic, N. Rajic, Bactericidal activity of
30
https://doi.org/10.1007/s11356-017-9643-8.
[67] B. Kwakye-Awuah, C. Williams, M.A. Kenward, I. Radecka, Antimicrobial action and efficiency of silver-loaded zeolite X, J. Appl. Microbiol. 104 (2008) 1516–1524. https://doi.org/10.1111/j.1365-2672.2007.03673.x.
[68] L. Ferreira, A.M. Fonseca, G. Botelho, C.A. Aguiar, I.C. Neves, Antimicrobial activity of faujasite zeolites doped with silver, Microporous Mesoporous Mater. 160 (2012) 126–132. https://doi.org/10.1016/j.micromeso.2012.05.006.
[69] S. Demirci, Z. Ustaoǧlu, G.A. Yilmazer, F. Sahin, N. Baç, Antimicrobial properties of zeolite-X and zeolite-A ion-exchanged with silver, copper, and zinc against a broad range of microorganisms, Appl. Biochem. Biotechnol. 172 (2014) 1652–1662. https://doi.org/10.1007/s12010-013-0647-7.
[70] S. Singh, M. ho Lee, I. Park, Y.J. Shin, Y.S. Lee, Antimicrobial properties of polypropylene films containing AgSiO2, AgZn and AgZ for returnable packaging in seafood distribution, J. Food Meas. Charact. 10 (2016) 781–793. https://doi.org/10.1007/s11694-016-9363-7.
[71] A. Mihaly-Cozmuta Anca Peter Grigore Craciun Anca Falup Leonard Mihaly-Cozmuta Camelia Nicula Adriana Vulpoi Monica Baia, Preparation and characterization of active cellulose-based papers modified with TiO 2 , Ag and zeolite nanocomposites for bread packaging application, Cellulose. 24 (n.d.). https://doi.org/10.1007/s10570-017-1383-x.
31
BAB VII. LAMPIRAN 7.1 Tim biodata peneliti
Ketua
a. Nama Lengkap : Prof. Dr. Didik Prasetyoko, S.Si., M. Sc
b. NIP/NIDN : 19710616 1997031 002/0016067108
c. Fungsional/Pangkat/Gol. : Profesor / Pembina Utama Madya / IVd d. Bidang Keahlian : Sintesis advanced material dan Energi e. Departemen/Fakultas : Departemen Kimia / Fakultas Sains dan
Analitika Data
f. Alamat Rumah dan No. Telp. : Perumahan Dosen ITS Blok U No. 100 085646162520
g. Riwayat penelitian :
No. Tahun Judul penelitian
Pendanaan
Sumber Jml (Juta Rp)
1.
2018-2020
Produksi Biofuel dari Minyak Kemiri Sunan Melalui Reaksi Deoksigenasi Menggunakan Katalis Logam/ZSM-5 Hierarki Ketua Ristekdikti 180 2. 2017-2019
Synthesis of Faujasite Material from Kaolin Bangka Belitung and Its
Application for Esterification (Penelitian Dasar)
Ketua Ristekdikti
360
h. Publikasi :
No. Judul Artikel Ilmiah Volume / No /
Tahun Nama Jurnal
1.
Size tunable mesoporous carbon microspheres using Pluronic F127 and gelatin as co-template for removal of ibuprofen
711/135066/2020 Science of The Total Environment
(Elsevier)
2.
Direct Synthesis of Sodalite from
Indonesian Kaolin for
Adsorption of Pb2+ Solution, Kinetics, and Isotherm Approach.
14/3/2019 Bulletin of Chemical Reaction Engineering & Catalysis.


![Gambar 3. Depolimerisasi selulosa menjadi mikrokristalin selulosa [1].](https://thumb-ap.123doks.com/thumbv2/123dok/4523900.3279869/15.892.251.714.520.813/gambar-depolimerisasi-selulosa-menjadi-mikrokristalin-selulosa.webp)