Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN
PEROKSIDA
SKRIPSI
Diajukan untuk Memenuhi Sebagian dari Syarat Untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Konsentrasi Kimia Material
Oleh:
KARTIKO CHAHYO LAKSONO 1006767
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PENDIDIKAN INDONESIA
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN
PEROKSIDA
Oleh
Kartiko Chahyo Laksono
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Kartiko Chahyo Laksono 2014 Universitas Pendidikan Indonesia
Oktober 2014
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
Skripsi ini tidak boleh diperbanyak seluruh atau sebagian,
Dengan dicetak ulang, difoto kopi, atau cara lainnya tanpa ijin dari penulis
KARTIKO CHAHYO LAKSONO
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN
PEROKSIDA
DISETUJUI DAN DISAHKAN OLEH PEMBIMBING :
Pembimbing I
Galuh Yuliani, M.Si., Ph.D. NIP. 198007252001122001
Pembimbing II
Dr. Agus Setiabudi, M.Si NIP. 196808031992031002
Mengetahui,
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
ABSTRAK
Batubara berpotensi digunakan sebagai adsorben bagi ion logam dalam larutan, karena memiliki karakteristik mirip dengan karbon aktif. Beberapa penelitian telah melaporkan penggunaan batubara peringkat rendah dari Indonesia sebagai adsorben bagi logam beracun dan senyawa organik. Namun Kapasitas adsorpsi batubara peringkat rendah masih rendah dibandingkan dengan adsorben lain terutama bila dibandingkan dengan karbon aktif. Pada penelitian ini batubara peringkat rendah asal Indonesia telah di modifikasi menggunakan hidrogen peroksida, dan diaplikasikan pada proses adsorpsi ion logam kromium (Cr3+) dan kobalt (Co2+). Modifikasi batubara peringkat rendah menggunakan hidrogen peroksida bertujuan untuk meningkatkan kadar oksigen yang merupakan gugus aktif pada proses penjerapan ion logam. Batubara peringkat rendah hasil modifikasi menggunakan hidrogen peroksida 20% dikarakterisasi dengan menggunakan FTIR, analisis luas permukaan, dan analisis ultimat. Dari hasil pengujian FTIR, terdapat peningkatan puncak serapan pada 1.442,7 cm-1 dan 3.317,3 cm-1 yang menandakan adanya peningkatan gugus C–O–H (karboksilat) dan O–H (hidroksil). Luas permukaan batubara setelah modifikasi meningkat menjadi 8,651 m2/g dari luas permukaan mula-mula sebesar 3,658 m2/g. Dari hasil pengujian ultimat, terdapat peningkatan kadar oksigen dari 7,39 menjadi 8,77%. Uji adsorpsi dilakukan menggunakan teknik batch test dengan larutan ion logam Cr3+ dan Co2+ sebagai larutan model. Konsentrasi ion logam ditentukan menggunakan spektroskopi serapan atom pada panjang gelombang 357,9 nm untuk logam Cr3+ dan 240,7 nm untuk logam Co2+. Kapasitas adsorpsi maksimum ditentukan menggunakan model isotherm adsorpsi Langmuir dan Freundlich. Plot data eksperimen adsorpsi batubara dan batubara termodifikasi terhadap ion logam mengikuti model isotherm Langmuir untuk logam Cr3+ dengan koefisien korelasi (R2) sebesar 0,99 dan 0,98. Kapasitas adsorpsi batubara meningkat setelah modifikasi dari 0,243 menjadi 0,535 mg/g untuk ion logam Cr3+ dan 0,018 menjadi sebesar 0,058 mg/g untuk ion logam Co2+. Dapat disimpulkan bahwa modifikasi batubara menggunakan hidrogen peroksida 20% dapat meningkatkan kemampuan adsorpsinya terhadap ion logam Cr3+ dan Co2+.
Kata kunci : Adsorpsi, Batubara Peringkat Rendah, Hidrogen Peroksida 20%,
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
ABSTRACT
Coal have the potential to use as adsorbent for the metal ion in the solvent because
its have characteristic like activated carbon’s have. Some of the researchers had
reported the use of low-rank coal from Indonesia as the adsorbent for toxic metal ion and some of organic compound, but the adsorption capacity of low-rank coal was still lower than the activated carbon. In this research, the low-rank coal from Indonesia had been modified using hydrogen peroxide, and applied in the adsorption process of metal ion chromium (Cr3+) and cobalt (Co2+). The modification of low-rank coal using hydrogen peroxide aims to increase the amount of oxygen which have a role as the active group in the adsorption process. The low-rank coals which had been modificated using hydrogen peroxide 20% were characterized using FTIR, surface area analysis, and ultimate analysis. From the FTIR analysis, it showed the increasing peak on 1442,7 cm-1 and 3317,3 cm-1 which showed the increase of C-O-H (carboxylic) and O-H (Hydroxyl) group. The surface area of the coal after the modification was increased from 3,658 to 8,651 m2/g. From ultimate analysis, it showed the increased amount of oxygen from 7,39 to 8,77 %. The adsorption test was measured using batch test technique with metal ion solution of Cr3+ and Co2+ as the solution models. The metal ion concentrations were measured using atomic absorption spectroscopy in the wave length 357,9 nm and 240,7 nm respectively for Cr3+ and Co2+. The maximum adsorption capacity was measured using Langmuir and Freundlich isotherm adsorption model. Data plot experiment of the coal and modificated coal adsorption to the metal ion were followed Langmuir isotherm model for Cr3+ with correlation coefficient (R2) about 0,99 and 0,98. The coal adsorption capacity increased after it had been modificated from 0,243 to 0,535 mg/g for Cr3+ and from 0,018 to 0,058 mg/g for Co2+. This research could be conclude that the modification of the low-rank coal using hydrogen peroxide 20% could increased the adsorption ability to metal ion Cr3+ and Co2+.
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
DAFTAR ISI
ABSTRAK i
KATA PENGANTAR iii
UCAPAN TERIMA KASIH iv
DAFTAR ISI v
DAFTAR GAMBAR viii
DAFTAR TABEL x
DAFTAR LAMPIRAN xi
BAB I PENDAHULUAN 1
1.1 Latar Belakang Penelitian 1
1.2 Rumusan Masalah Penelitian 3
1.3 Batasan Masalah Penelitian 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 3
BAB II TINJAUAN PUSTAKA 5
2.1 Batubara 5
2.1.1 Jenis-Jenis Batubara 6
2.1.2 Sifat-Sifat Batubara 7
2.2 Logam Berat 9
2.3 Adsorpsi dan Adsorben 12
2.4 Adsorpsi Isoterm 15
2.5 Pengujian Adsorpsi Ion Logam Co2+ dan Cr3+ Menggunakan Berbagai Adsorben 17
2.6 Karakterisasi 19
2.6.1 Analisis Nilai Kalor (Calorific Value, CV) 19
2.6.2 Analisis Proksimat 20
2.6.2.1 Kandungan Air (Moisture Content) 21
2.6.2.2 Kandungan Abu (Ash Content) 22
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
2.6.2.4 Kandungan Fixed Carbon 24
2.6.3 Analisis Ultimat 24
2.6.4 Surface Area Analyzer 25
2.6.5 Spektroskopi Fourier Transform Infra Red (FTIR) 26
2.6.6 Spektrofotometri Serapan Atom 29
BAB III METODA PENELITIAN 31
3.1 Tempat Penelitian 31
3.2 Alat dan Bahan 31
3.2.1 Alat 31
3.2.2 bahan 31
3.3 Desain Penelitian 31
3.4 Prosedur Penelitian 33
3.4.1 Karakterisasi Batubara Peringkat Rendah 33
3.4.1.1 Analisis Proksimat 33
3.4.1.2 Analisis FTIR 34
3.4.1.3 Analisis Spektroskopi Serapan Atom (SSA) 34
3.4.2 Preparasi Larutan Sintetis Logam Cr3+ dan Co2+ 35
3.5 Studi Adsorpsi 35
3.5.1 Penentuan Waktu Optimum Adsorpsi Batubara dan Batubara Termodifikasi Hidrogen Peroksida 36
3.5.2 Uji Pengaruh Massa Batubara dan Batubara Termodifikasi Hidrogen Peroksida 36
BAB IV HASIL DAN PEMBAHASAN 38
4.1 Karakterisasi Batubara dan Batubara Termodifikasi Hidrogen peroksida 38
4.1.1 Analisis Proksimat-Ultimat 38
4.1.2 Analisis FTIR 39
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
Pengaruh Waktu 42
4.3 Uji Batubara dan Batubara Termodifikasi Terhadap Pengaruh Massa 43
4.4 Oksidasi Batubara Menggunakan Hidrogen Peroksida 48
4.5 Mekanisme Adsorpsi 51
BAB V KESIMPULAN 53
5.1 Kesimpulan 53
5.2 Saran 54
DAFTAR PUSTAKA 55
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB I PENDAHULUAN
1.1 Latar Belakang Penelitian
Limbah logam berat yang banyak dibuang oleh berbagai industri dapat membahayakan kesehatan manusia dan dapat terakumulasi dalam sungai ataupun lahan tanah. Menurut Suganda et.al., (2002) dan Andarani
et.al., (2009), dalam penelitiannya menjelaskan total area lahan yang
tercemar aliran limbah pabrik tekstil yang mencemari sungai atau tanah khususnya logam berat adalah Cu, Zn, Pb, Cd, Co, Ni, dan Cr. Penghilangan logam berat dari limbah cair dapat dilakukan menggunakan beberapa metode seperti pertukaran ion konvensional, adsorpsi, presipitasi kimia, dan filtrasi membran. Salah satu metode yang banyak digunakan adalah adsorpsi. Adsorpsi merupakan suatu proses atau fenomena
penimbunan atau penghimpunan solute pada permukaan dari dua fasa yang teradsorpsi disebut adsorbat (solute dan fasa pengadsorpsi disebut
adsorben) (Treyball, 1981). Banyak penelitian yang mejelaskan bahwa logam berat dapat dihilangkan/diminimalisir menggunakan adsorben-adsorben seperti Karbon Aktif, Batubara muda (Pehlivan et al., 2007), zat arang alami (Spruce wood, Pine bark, cork, dan Peat) (Hanzlik, 2004),
Coconut husk (Olayinka, 2009) dan lain-lain.
2
Batubara merupakan senyawa hidrokarbon yang struktur kimianya sangat kompleks. Rumusan struktur kimia batubara menurut Solamon (1998) terdiri dari kluster aromatik yang berupa kelompok fungsional alifatik yang mungkin berikatan dengan unsur O, N, atau S, kelompok fasa mobile, dan senyawa penyambung (bridges) (Bindar et al., 2007). Dilaporkan dari beberapa literatur sisi aktif yang dimiliki batubara muda merupakan gugus karboksilat yang dapat mengalami reaksi pertukaran kation dengan ion logam. (Yuliani, 2012 dan Pehlivan et al., 2007).
Pada penelitian sebelumnya oleh E.Pehlivan dan G.Arsalan tahun 2007, batubara muda di daerah Turki dengan modifikasi penambahan NaNO3 yang digunakan untuk mengadsorpsi logam berat seperti Nikel (Ni), Tembaga (Cu), dan Timbal (Pb) dapat meningkatkan kapasitas adsorpsinya. Kapasitas adsorpsi batubara muda terhadap logam tersebut sebesar 18,9 mg/g untuk logam Cu2+; 68,5 mg/g untuk logam Pb2+; dan 12,0 mg/g untuk logam Ni2+. Kapasitas adsorpsi batubara muda lebih besar dari karbon aktif sebesar 7,2 mg/g untuk Cu2+; 62,3 mg/g untuk Pb2+; dan 5,4 mg/g untuk Ni2+ (Pehlivan et al., 2007).
Batubara muda termodifikasi hidrogen peroksida telah digunakan untuk adsorpsi methilene blue. Modifikasi batubara muda menggunakan hidrogen peroksida dapat meningkatkan kadar oksigen dan meningkatkan kapasitas adsorpsi dari batubara. Pada poses modifikasi menggunakan hidrogen peroksida diperoleh konsentrasi maksimum hidrogen peroksida yaitu 20% dan waktu optimum pengadukan yaitu 30 menit. Kapasitas adsorpsi maksimum terhadapat zat warna metilene blue dari batubara muda termodifikasi meningkat 100% dibandingkan dengan batubara muda tanpa modifikasi yaitu 51,81 menjadi 103,09 mg/g (Novyana, 2012).
3
1.2 Rumusan Masalah Penelitian
Berdasarkan uraian yang telah dikemukakan di atas, maka rumusan masalah dalam penelitian ini adalah:
1. Bagaimana karakterisasi batubara dan batubara hasil modifikasi menggunakan hidrogen peroksida 20% ?
2. Bagaimana kinerja batubara dan batubara hasil modifikasi menggunakan hidrogen peroksida 20% dalam proses adsorpsi logam Cr3+ dan Co2+ ?
1.3 Batasan Masalah Penelitian
Berdasarkan uraian yang telah dikemukakan di atas, maka pembatasan masalah dalam penelitian ini adalah:
1. Batubara peringkat rendah yang digunakan berasal dari daerah Indonesia yang dimodifikasi menggunakan hidrogen peroksida
20%.
2. Variasi waktu selama percobaan dibatasi pada waktu 20; 40; 60; 120; dan 240 menit.
3. Variasi massa batubara dan batubara termodifikasi dengan berat 0,5; 1,0; 1,5; 2,0; 2,5; dan 3,0 g.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengkarakterisasi batubara dan batubara hasil modifikasi menggunakan hidrogen peroksida 20%.
2. Mengetahui pengaruh waktu dan berat batubara hasil modifikasi menggunakan hidrogen peroksida terhadap adsorpsi ion logam.
4
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB III
METODA PENELITIAN
3.1 Tempat Penelitian
Penelitian ini dilaksanakan di laboratorium Riset, karakterisasi FTIR, dan pengujian SSA dilakukan di laboratorium Kimia Instrumen, Jurusan Pendidikan Kimia, FPMIPA Universitas Pendidikan Indonesia (UPI). Analisis luas permukaan dilakukan di laboratoium pengujian Institut Teknologi Bandung (ITB). Analisis proksimat, analisis ultimat, dan nilai kalori dilakukan di laboratorium pengujian Pusat Penelitian dan Pengembangan Teknologi Mineral dan Batubara (tekMIRA).
3.2 Alat dan Bahan 3.2.1 Alat
Alat-alat yang digunakan adalah : alat-alat gelas, neraca analitik, neraca teknis, magnetic stirrer, mechanics stirrer, lumpang alu,
thermometer, crusher, dan alat-alat analisis berupa pH-meter, FTIR
Shimadzu 8400, Spektrometer Serapan Atom (SSA) Perkin Element
AAnalist 100, Surface Area Analyzer, dan instrumen analisis unsur
(Karbon, Hidrogen, Oksigen, Nitrogen, Sulfur).
3.2.2 Bahan
Bahan-bahan yang digunakan adalah : Batubara peringkat rendah di daerah Indonesia, H2O2 20% (PT. Brataco Chemical), aquadest, padatan Cr(NO3)3. 9H2O (merck), padatan Co(NO3)2.6H2O (merck), larutan HNO3 65% (merck) dan kertas saring Whatman.
32
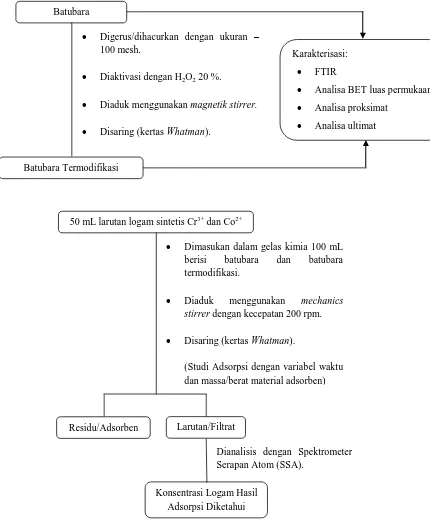
[image:16.595.137.567.182.707.2]Desain penelitian dilakukan mengikuti alur penelitian seperti ditunjukan pada Gambar 3.1.
Gambar 3.1. Tahapan Secara Umum Penelitian Larutan/Filtrat
Konsentrasi Logam Hasil Adsorpsi Diketahui
Dianalisis dengan Spektrometer Serapan Atom (SSA).
Residu/Adsorben
50 mL larutan logam sintetis Cr3+ dan Co2+
Dimasukan dalam gelas kimia 100 mL berisi batubara dan batubara termodifikasi.
Diaduk menggunakan mechanics stirrer dengan kecepatan 200 rpm.
Disaring (kertas Whatman).
(Studi Adsorpsi dengan variabel waktu dan massa/berat material adsorben)
Karakterisasi: FTIR
Analisa BET luas permukaan Analisa proksimat
Analisa ultimat Batubara
Digerus/dihacurkan dengan ukuran – 100 mesh.
Diaktivasi dengan H2O2 20 %.
Diaduk menggunakan magnetik stirrer.
Disaring (kertas Whatman).
33
3.4 Prosedur Penelitian
3.4.1 Karakterisasi Batubara Peringkat Rendah
Batubara yang ukurannya sudah kecil/ kasar di haluskan kembali menggunakan crusher kemudian adsorben diayak menggunakan saringan dengan ukuran 100 mesh. Kemudian dilakukan analisis awal nilai kalori, analisis proksimat, analisis ultimat, FTIR, dan BET surface area.
Seberat 40 gram batubara ukuran 100 mesh ditimbang lalu dimasukan dalam gelas kimia 500 ml. kemudian tambahkan larutan H2O2 20% kedalam gelas kimia berisi batubara. Lalu diaduk menggunakan
magnetic Stirrer hingga homogen. Proses pengadukan dilakukan selama ½
jam. Setelah proses pengadukan selesai, campuran disaring menggunakan kertas saring whatman berukuran 42 dan diambil residunya, kemudian keringkan dengan cara diangin-angin. Batubara hasil modifikasi H2O2 20% kemudian dilakukan analisis nilai kalori, analisis proksimat, analisis ultimat, FTIR, dan BET surface area.
3.4.1.1Analisis Proksimat
Analisis proksimat menggunakan instrument TGA ini digunakan untuk diantaranya analisis kandungan air total (total moisture), analisi air bawaan (moisture inherent), analisa kandungan abu, penentuan volatile
matter, penentuan karbon tertambat (fixed carbon) dalam satu waktu
dengan kata lain analisis proksimat secara otomatis tidak manual.
Pastikan instrument TGA siap untuk menganalisis sampel. Pada menu utama klik F5 analyzer pada toolbar (jika sebelumnya data sampel belum dimasukan, maka akan ditampilkan menu sampel login. Furnace akan segera membuka, tempatkan sejumlah crucible kosong yang akan digunakan untuk analisa pada lubang-lubang carousel, ditambah satu
34
lubang kecil. Tekan tombol actuator (pada panel depan analyzer), furnace akan menutup dan sistem akan menginisialisasi dan menimbang semua
crucible. Setelah selesai, furnace akan membuka kembali dan carousel
akan menuju ke posisi crucible yang pertama, sistem siap menimbang sampel. Masukkan sampel sebanyak 1 scope ke dalam crucible pertama, tepat didepan instrument (1 scope = ±1 gram). Tekan tombol actuator,
carousel akan berputar dan berhenti pada posisi crucible berikutnya.
Setelah pengisian crucible yang terakhir, penekanan tombol actuator akan memulai analisis secara otomatis. Untuk step volatile matter diperlukan
crucible cover, jika sudah sampai pada step ini maka cover akan membuka
dan mempersilahkan operator memasang crucible cover. Jika step ini selesai maka operator harus mengambil crucible cover.
3.4.1.2Analisis FTIR
Analisis FTIR menggunakan instrumen FTIR 8400 Shimadzu Hyper IR berguna untuk mengidentifikasi keberadaan gugus fungsi pada
material.
Sedikit sampel Batubara (± 1 mg), kemudian ditambahkan bubuk KBr murni (± 100 mg) dan digerus hingga rata dengan bantuan alat lumpang-alu. Campuran ini kemudian ditempatkan dalam cetakan dan ditekan dengan menggunakan alat tekanan mekanik. Tekanan ini dipertahankan beberapa menit, kemudian sampel (pelet KBr yang terbentuk) diambil dan kemudian ditempatkan dalam tempat sampel pada alat Spektroskopi Inframerah untuk dianalisis.
3.4.1.3Pengujian Spektroskopi Serapan Atom (SSA)
35
radiasi, dan radiasi yang berasal dari nyala api. Detektor akan menolak arah searah arus (DC) dari emisi nyala dan hanya mengukur arus bolak-balik dari sumber radiasi atau sampel.
Kurva kalibrasi disiapkan dengan mengencerkan larutan induk, untuk larutan logam Cr(NO3)3. 9H2O deret kurva standar dibuat dari 4 ppm, 8 ppm, 12 ppm, 16 ppm, 20 ppm, 24 ppm dan 28 ppm. Sedangkan untuk larutan logam Co(NO3)2.6H2O deret kurva dibuat dari 7 ppm, 14 ppm, 21 ppm, 28 ppm, dan 35 ppm. Pengukuran konsentrasi logam diukur menggunakan instrument Spektrometer Serapan Atom (SSA).
3.4.2 Preparasi Larutan Sintetis Logam Cr3+ dan Co2+
Larutan model yang digunakan adalah larutan logam Cr(NO3)3. 9H2O dan Co(NO3)2.6H2O. Larutan induk disiapkan dengan konsentrasi 1000 ppm dengan pH awal dibuat pada pH 3,8 - 4. Larutan kerja 25 ppm
disiapkan dengan mengencerkan larutan induk 1000 ppm. Pengukuran konsentrasi logam diukur menggunakan instrument Spektrometer Serapan
Atom (SSA).
3.5 Studi Adsorpsi
36
3.5.1 Penentuan Waktu Optimum Adsorpsi Batubara dan Batubara Termodifikasi Hidrogen Peroksida
Sebanyak 50 mL larutan limbah logam sintetik dengan konsentrasi 25 ppm dimasukan dalam wadah yang berisi batubara dan batubara termodifikasi hidrogen peroksida seberat 1 gram. Kemudian campuran tersebut diaduk menggunakan mechanics stirrer, dilakukan berulang-ulang dengan variasi waktu 20 – 240 menit. Setelah itu campuran disaring menggunakan kertas saring whatman, lalu larutan/filtrat diuji pH. Filtrat yang diperoleh dianalisis menggunakan Spektrometer Serapan Atom (SSA).
[image:20.595.249.386.178.339.2]3.5.2 Uji Pengaruh Massa Batubara dan Batubara Termodifikasi Hidrogen Peroksida
Gambar 3.2 Rangkaian Alat Adsorpsi Batch: (1).Beaker glass; (2). Pengaduk; (3). Tombol on/off;
37
Sebanyak 50 mL larutan limbah sintetik dengan konsentrasi 25 ppm dimasukan dalam wadah yang berisis batubara termodifikasi hidrogen peroksida yang telah ditimbang dengan variasi berat : 0,5 ; 1 ; 1,5 ; 2 ; 2,5; dan 3 gram. kemudian campuran tersebut diaduk menggunakan mechanics
stirrer pada waktu optimum adsorpsi. Setelah itu campuran disaring
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang sudah dilakukan, maka dapat disimpulkan bahwa:
1. Oksidasi menggunakan H2O2 20% pada batubara dapat meningkatkan kadar senyawa oksigen dan meningkatkan kapasitas adsorpsi pada batubara. Hal ini dapat terlihat dari analisis ultimat yang meperlihatkan peningkatan kadar oksigen dari 7,39 meningkat menjadi 8,77%. Hal ini dibuktikan pula dari analisis FTIR yang meningkatkan sisi aktif dari batu bara yaitu gugus C-O-H tekuk kedalam pada serapan 1440,7 cm-1 dengan diperkuat adanya ikatan O-H pada serapan 3317,3 cm-1 yang diperkirakan adanya gugus karboksilat yang merupakan gugus penjerap ion logam berat.
54
5.2 Saran
Laksono, Kartiko Chahyo. 2014
ADSORPSI ION LOGAM KROMIUM DAN KOBALT MENGGUNAKAN BATUBARA PERINGKAT RENDAH TERMODIFIKASI HIDROGEN PEROKSIDA
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
DAFTAR PUSTAKA
Andarani, P., & Roosmini, D. (2009). “Heavy Metal (Cu, Cr, and Zn) Pollution Profiles In Surface Water And Sendiments Around Tetile Industri PT. X”. Jurnal Teknik. EM7, 1-12.
Billah, M. (2010). “Kemampuan Batubara dalam Menurunkan Kadar Logam Cr2+ dan Fe2+ dalam Limbah Indutri Baja”. Jurnal Penelitian Ilmu Teknik 10. (1). 48-56.
Bindar Y., Riza A., Susanto H., Sasongko D., (2007). “Metoda Dekomposisi Batubara Berdasarkan Neraca Elemen dan Teori Devolatilisasi dari Data Analisa Proksimat dan Ultimat”. Jurnal Teknik Kimia Indonesia. 6 (1): 549-562.
Chrisman, A. (2008). “Preparasi Karbon Aktif”. FT UI Jakarta: tidak diterbitkan.
Dee, P, R,. (2012). “Modifikasi Bentonit Terpilar Al dengan Kitosan Untuk
Adsorpsi Ion Logam Berat”. Skripsi Sarjana Pada FMIPA UI Jakarta: tidak
diterbitkan.
Erden, E,. Karapinar, N,. Donat, R,. (2004). “The Removal Of Heavy Metal Cations by Natural Zeolites”. Journal of Colloid and interface Science.
280. 3009-314.
Erna Komariah W. (2012). “Peningkatan Kualitas Batubara Indonesia Peringkat Rendah Melalui Penghilangan Moisture dengan Pemanasan Gelombang
Mikro”. Tesis Megister Teknik pada Pasca Sarjana UI Jakarta: tidak
56
Estiatym, L.M. (2012). “Kesetimbangan dan Kinetika Adsorpsi Ion Cu2+ Pada Zeolite-H”. 22 (2): 115-129.
Grandistin G.G,. (2014). “Karakterisasi dan Uji Adsorpsi Batubara Muda
Termodifikasi Hidrogen Peroksida menggunakan Metoda Kontinyu
Terhadap Metilen Blue”. Skripsi Sarjana pada FPMIPA UPI Bandung:
tidak diterbitkan.
Hanzlik, P., Jehlicka, J., Weishauptova, Z., Sebek, O. (2004). “Adsorption of Copper, Cadmium and Silver From Aqueous Solutions Onto Natural Carbonaceous Materials”. Journal Plant Soil Environ. 50. 257-264.
Hendayana. S. (1994). “Kimia Analitik Instrumen”. Semarang: IKIP Semarang
Press.
John. D. (1994). “Kamus Kimia Lengkap”. English: Oford Univerxity press.
Mudzakir, A. et al. (2008). “Praktikum Kimia Anorganik”. Bandung: FPMIPA Universitas Pendidikan Indonesia.
Majari Magazine,. (2008). ”Laporan Khusus: Puslitbang tekMIRA (Bagian 2)”. Tersedia: [Online] http://majarimagazine.com/2008/06/laporan-khusus-puslitbang-tekmira-bagian-2/ (12 Juli 2014).
57
Olayinka, O.K., Oyedeji, O.A., & Oyeyiola, O.A. (2009). “Removal of Chromium and Nickel Ions from Aqueous Solution by Adsorption on Modified Coconut Husk”. Journal Of Envirinmental Science and Technology. 3.
286-293.
Orchin, M, Reggel L. (1947). “Aromatic Cyledehydrogenation”. J. Am. Chem.
Soc., 69, 505-509.
Patri, N,. (2012).“Adsorpsi Ion Cr(III) dan Cr(VI) Menggunakan Bentonit
Temodifikasi Oksida Besi”. Skripsi Sarjana pada FMIPA IPB Bogor: tidak
diterbitkan.
Pehlivan, E. & Arslan, G. (2007). “Removal of Metal Ions Using Lignite in Aqueous Solution - Low Cost Biosorbents”. Journal Fuel Processing
Technology 88. 99-106.
Purnamasari, Y, (2000). “ Pembuatan Briket Dari Batubara Kualitas Rendah Dengan Proses Non Karbonisasi Dengan Menambahkan MgO dan MgCl2”,
UPN”veteran”: Jawa Timur.
Purwaningsih, D. (2009). “Adsoprsi <ulti Logam Ag(I), Pb(II), Cr(III), Cu(II) dan Ni(II) pada Hibrida Etilendiamino-Silika dari Abu Sekam Padi”. Jurnal Penelitian Saintek, Vol. 14. No.1, April 2009: 59-76.
Sandstorm, Donald W., and Heber E. K. (1979). “Waste Water Treatment”. Prentice-hall, Inc. Englewood Cliffs, N.J. 07632: USA.
Setiabudi, A, et al. (2012). “Karakterisasi Material; Prinsip dan Aplikasi dalam
58
Suardana, I, N,. (2008). “Optimasi Daya Adsorpsi Zeolit Terhadap Ion Kromium (III)”. Jurnal Penelitian dan Pengembangan Sains & Humaniora. 2. (1). 17-33.
Suganda, H., Setyorini, D., Kusnadi, H., Saripin, I., & Kurnia, U. (2002).
“Evaluation Of The Pollution Of Liquid Waste Textile Industri On The Sustainability Of Rice Field”. Jurnal Lahan Pertanian. 20, (5), 202-220.
Wang, Haihui, Bogdan Z. Dlugogorski & Eric kennedy. (2003). “Coal Oxidation at Low Temperature : Oxygen Consumtion, Oxidation Product Reaction
Mechanism and Kinetic Modeling”. Progress in Energy and Combustion
Science, 29. 487-513.
Yuliani, G., Ying Qi, Andrew F.A. Hoadley, Alan L., Chaff, and Gil Garnier.
(2012). “Lignite Clean up of Magnesium Bisulphate Pulp Mill Effluent as a
Proxy for Aqueous Discharge from a Lingo-Cellulosic Biorefinery”.
Scivers Science Direct, Biomass and Bioenergy. 2012, 38, 411-418.
Zakaria, A. (2011). “Adsorpsi Cu (II) Menggunakan Zeolite Sintesis Dari Abu
Terbang Batubara”. Tesis Megister Sains pada PascaSarjana IPB Bogor: