3.
METODOLOGI3.1. Waktu dan Tempat
Penelitian dilaksanakan pada bulan Februari hingga bulan Maret 2009 dan bertempat di Laboratorium Pengolahan Hasil Perairan, Laboratorium Mikrobiologi Hasil Perairan, Laboratorium Biokimia Hasil Perairan, Departemen Teknologi Hasil Perairan dan Laboratorium Kimia Pangan, Departemen Teknologi Pangan Institut Pertanian Bogor.
3.2. Alat dan Bahan
Bahan dan alat yang digunakan dalam penelitian ini antara lain : 3.2.1. Alat
Alat yang digunakan untuk pembuatan petis kupang adalah rancak
(alat berbentuk tabung yang terbuat dari bambu, garis tengah 50 cm dan tinggi 1 m), caruk (alat yang berbentuk seperti alat penangkap serangga atau serok ikan
dan biasanya terbuat dari jala bekas, umumnya memiliki garis tengah sekitar 25 - 30 cm), gelas ukur, timbangan, panci, wajan, pisau, baskom, toples kaca, talenan, kompor, pengaduk kayu. Peralatan analisis mutu produk terdiri dari labu destruksi, erlenmeyer, soxhlet, kapas, selongsongan, oven, cawan porselen, desikator, bunsen, tanur listrik, labu destilasi, aw-meter (Shibaura wa-360), viscometer (Brookfield LV).
3.2.2. Bahan
Bahan baku untuk pembuatan petis kupang berupa cairan hasil rebusan kupang putih (Corbula faba Hinds) yang diperoleh dari pengusaha petis Ibu Eris,
Kraton, Pasuruan Jawa Timur. Bahan-bahan pelengkap lainnya terdiri dari tepung terigu, tepung tapioka, tepung beras, air tajin, gula merah, garam, cereh (kaldu
kupang pekat), cabe rawit dan bawang putih sedangkan bahan untuk analisis fisika kimia terdiri dari akuades, HCl, NaOH, H2SO4 pekat, HNO3, tablet Kjeltab, pelarut heksana, H3BO3, HClO4 dan metil merah.
3.3. Tahapan Penelitian
Metode penelitian dibagi menjadi 3 tahap yaitu, analisis fisika-kimia
ladon, pencarian jenis pati yang tepat dan penentuan konsentrasi pati yang sesuai.
Petis kupang dikarakteristik fisika-kimia setelah diperoleh konsentrasi pati terpilih, kemudian dibandingkan dengan petis kupang komersial, petis kupang kontrol (tanpa penambahan pati), dan petis menurut standar mutu SNI 01-2346-2006. Berikut merupakan penjelasan penelitian dari berbagai tahapnya :
3.2.1. Analisis fisika-kimia ladon
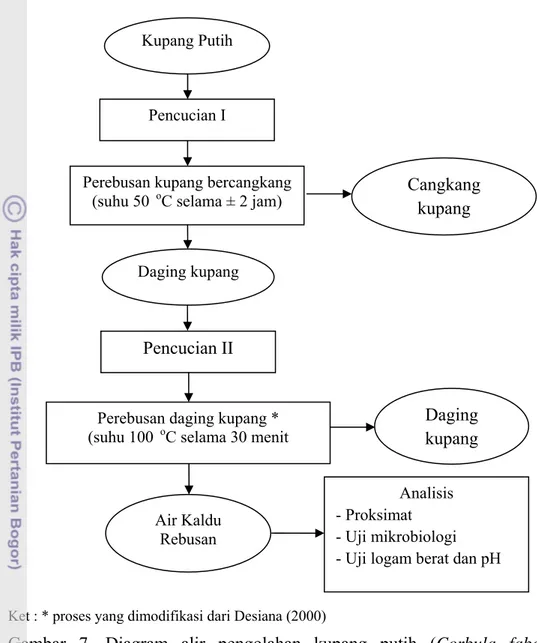
Kupang putih diperoleh dari nelayan kupang di daerah Kraton, Pasuruan. Nelayan menangkap kupang putih dengan cara menggeruk dasar perairan dengan alat penggeruk. Kupang yang telah didapatkan, dibersihkan dari lumpur dan kotoran yang menempel dengan dicuci menggunakan air sungai dan dicuci kembali dengan air PAM agar lebih bersih. Kupang yang telah dicuci, direbus pada air mendidih (suhu ± 100 oC) selama lebih kurang 2 jam. Perebusan kupang bertujuan untuk mempermudah pelepasan dan pemisahan antara daging kupang dan cangkang kupang. Kupang disaring untuk memisahkan daging dan cangkang setelah perebusan pertama selesai, kemudian dilakukan pencucian kedua. Pencucian kupang yang kedua dilakukan dengan cara yang sama seperti pencucian pertama. Daging kupang yang telah dicuci, direbus pada suhu 50 oC selama lebih kurang 30 menit. Setelah itu, daging kupang dipisahkan dari air rebusannya. Air hasil perebusan kedua dapat digunakan untuk pembuatan petis, sedangkan air hasil perebusan pertama tidak dapat digunakan karena kulit kupang belum terbuka. Diagram alir pengolahan kupang putih (Corbula faba Hinds)
untuk mendapatkan air kaldu rebusan dapat dilihat pada Gambar 7.
Penelitian tahap awal adalah melakukan analisis fisika-kimia terhadap
ladon yang meliputi analisis proksimat (kadar air, abu, protein, dan lemak), uji
derajat keasaman (pH), uji mikrobiologi, dan uji logam berat. Tujuan dari analisis ini adalah untuk mengetahui kandungan kimia awal kaldu kupang (ladon)
Ket : * proses yang dimodifikasi dari Desiana (2000)
Gambar 7. Diagram alir pengolahan kupang putih (Corbula faba Hinds)
(Desiana 2000).
3.2.2. Penentuan jenis pati yang tepat
Tahap formulasi bahan tambahan dan bahan utama dilakukan untuk menentukan jenis pati yang tepat. Formulasi bertujuan memberi pedoman dalam penentuan komposisi bahan agar kandungan nutrisi produk sesuai dengan ketentuan SNI serta memberikan karakteristik produk terbaik. Penentuan formulasi dilakukan dengan metode trial and error hingga didapatkan
karakteristik formulasi yang layak untuk dilakukan uji organoleptik. Adapun komposisi formula yang digunakan dapat dilihat pada Tabel 12.
Kupang Putih
Pencucian I
Perebusan kupang bercangkang
(suhu 50 oC selama ± 2 jam) Cangkang
kupang Daging kupang Daging kupang Air Kaldu Rebusan Pencucian II
Perebusan daging kupang * (suhu 100 oC selama 30 menit
Analisis - Proksimat - Uji mikrobiologi - Uji logam berat dan pH
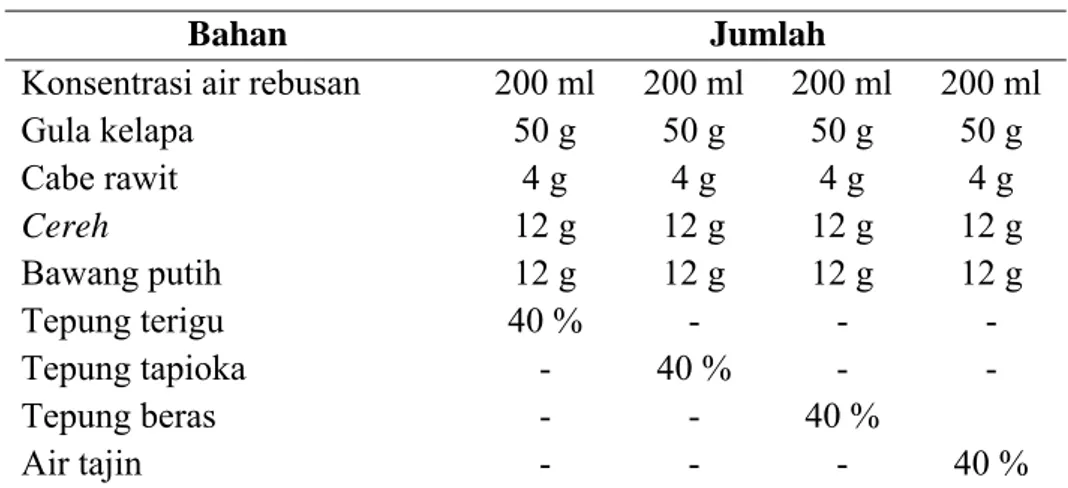
Tabel 12. Uji coba pembuatan petis dengan penambahan tepung terigu, tepung tapioka, tepung beras, dan air tajin.
Bahan Jumlah
Konsentrasi air rebusan 200 ml 200 ml 200 ml 200 ml
Gula kelapa 50 g 50 g 50 g 50 g Cabe rawit 4 g 4 g 4 g 4 g Cereh 12 g 12 g 12 g 12 g Bawang putih 12 g 12 g 12 g 12 g Tepung terigu 40 % - - - Tepung tapioka - 40 % - - Tepung beras - - 40 % Air tajin - - - 40 %
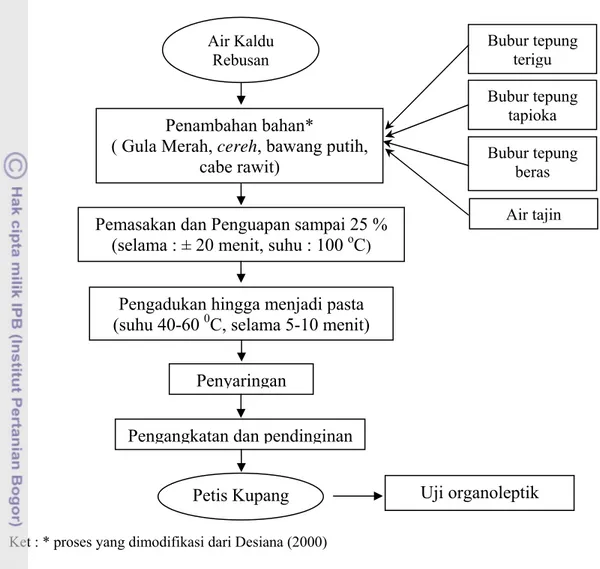
Air kaldu rebusan kupang yang diperoleh pada tahap pertama, kemudian dilakukan penambahan bahan-bahan seperti, gula merah, cabe rawit, cereh, bawang putih dan pati-patian. Bahan pengisi (pati-patian) dibuat dalam bentuk bubur, yaitu dengan melarutkan tepung-tepungan ke dalam air panas dengan perbandingan 1:3 atau 50 g tepung ke dalam 150 ml air. Campuran bahan-bahan dimasak dan diuapkan pada suhu 100 oC selama ± 20 menit hingga volume air kaldu menyusut sebanyak 25% dari volume awalnya. Setelah itu, larutan kaldu diaduk hingga menjadi pasta pada suhu 40-60 oC selama ± 5-10 menit. Sebelum dilakukan pengangkatan dan pendinginan, kaldu kupang disaring untuk memisahkan kotoran-kotoran yang dihasilkan dari penambahan bahan. Diagram alir pembuatan petis kupang dengan penambahan pati-patian disajikan pada Gambar 8.
Pati terpilih ditentukan secara organoleptik dengan uji organoleptik skala hedonik. Parameter yang diuji meliputi aroma, rasa, penampakan, dan tekstur. Data yang diperoleh dari hasil uji organoleptik kemudian dianalisis dengan menggunakan uji Kruskal Wallis dan jika hasil analisis ragam berbeda nyata,
dilanjutkan dengan uji lanjut Multiple Comparison. Tahap selanjutnya merupakan
Uji organoleptik Pemasakan dan Penguapan sampai 25 %
(selama : ± 20 menit, suhu : 100 oC)
Pengadukan hingga menjadi pasta (suhu 40-60 0C, selama 5-10 menit)
Penyaringan Penambahan bahan* Bubur tepung terigu Bubur tepung tapioka Bubur tepung beras Air tajin
( Gula Merah, cereh, bawang putih,
cabe rawit)
Pengangkatan dan pendinginan Petis Kupang
Air Kaldu Rebusan
Ket : * proses yang dimodifikasi dari Desiana (2000)
Gambar 8. Diagram alir pembuatan petis Kupang Putih (Corbula faba Hinds)
3.2.3. Pencarian konsentrasi pati yang sesuai
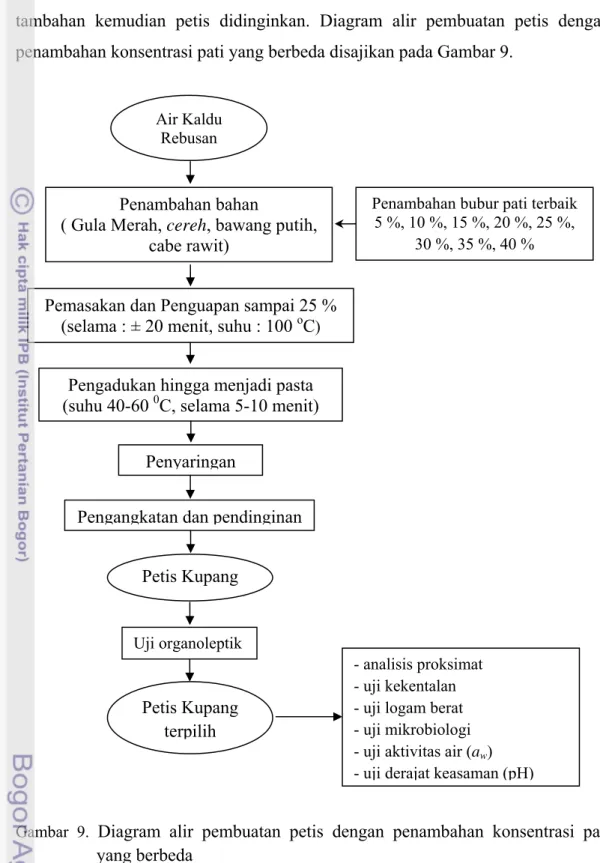
Tahap selanjutnya, jenis pati terbaik dicampur dengan air kaldu rebusan dan bumbu-bumbu. Bubur pati yang ditambahkan sebanyak 40 % dari konsentrasi air rebusan kupang. Penambahan pati berdasarkan pada ketentuan standar mutu petis SNI 01-2346-2006 yang mencantumkan bahwa kadar karbohidrat maksimal 40 %, sehingga perlakuan konsentrasi bubur pati yang ditambahkan sebesar 5 %, 10 %, 15 %, 20 %, 25 %, 30 %, 35 %, dan 40 % (v/v) dari berat air kaldu rebusan. Campuran bahan-bahan kemudian dimasak dan diuapkan hingga volume air kaldu menyusut sebanyak 25 % dari berat awalnya. Pemasakan dilakukan pada suhu 100 0C selama 20 menit dan setelah agak kental adonan diaduk selama 5-10 menit (suhu 40-60 0C). Adonan petis disaring untuk menghilangkan kotoran dari bahan
tambahan kemudian petis didinginkan. Diagram alir pembuatan petis dengan penambahan konsentrasi pati yang berbeda disajikan pada Gambar 9.
Air Kaldu Rebusan
Gambar 9. Diagram alir pembuatan petis dengan penambahan konsentrasi pati
yang berbeda
Konsentrasi tepung terbaik ditentukan secara organoleptik dengan uji organoleptik skala hedonik. Parameter yang diuji dalam uji hedonik meliputi penampakan, aroma, rasa dan konsistensi. Setelah didapatkan petis kupang dengan konsentrasi pati terpilih, petis dianalisis karakteristiknya yang meliputi,
Penambahan bubur pati terbaik 5 %, 10 %, 15 %, 20 %, 25 %,
30 %, 35 %, 40 %
Penambahan bahan
( Gula Merah, cereh, bawang putih,
cabe rawit)
Pemasakan dan Penguapan sampai 25 % a : ± 20 menit, suhu : 100 oC)
(selam
Pengadukan hingga menjadi pasta suhu 40-60 0C, selama 5-10 menit
( )
Penyaringan
- analisis proksimat - uji kekentalan - uji logam berat - uji mikrobiologi - uji aktivitas air (aw) - uji derajat keasaman (pH)
Pengangkatan dan pendinginan Petis Kupang
Uji organoleptik
Petis Kupang terpilih
analisis proksimat, analisis derajat keasaman (pH), analisis aktivitas air (aw), analisis viskositas uji mikrobiologi (kapang).
3.4.Pengujian
Prosedur pengujian ada dua cara, yaitu secara subyektif dan secara obyektif. Analisis secara obyektif yaitu analisis kimia yang meliputi uji proksimat (kadar karbohidrat, kadar lemak, kadar protein, kadar air, kadar abu, kekentalan), derajat keasaman (pH), aktivitas air (aw), dan analisis biologi yaitu uji mikroba kapang (Total Plate Count), sedangkan analisis secara subyektif yaitu uji
organoleptik dengan parameter warna, penampakan, bau/aroma, tekstur dan rasa, dan dilanjutkan dengan perhitungan dengan metode different test dengan Multiple
Comparison (Larmond 1970).
3.4.1. Uji Organoleptik
Metode yang digunakan untuk uji organoleptik menggunakan score sheet
berdasarkan SNI-01-2346-2006. Pengujian organoleptik merupakan pengujian yang bersifat subjektif dengan menggunakan indera yang ditujukan pada penampakan, bau, konsistensi cairan, rasa dan warna. Data yang diperoleh diuji dengan menggunakan uji statistik non parametrik Kruskal Wallis, sedangkan uji
lanjutan digunakan Multiple Comparison.
3.4.2. Analisis Kimia
3.4.2.1. Kadar Lemak (Apriyantono 1989).
Kadar lemak ditentukan dengan menggunakan metode Rose-Gottlieb.
Metode Rose-Gottlieb digunakan untuk menentukan bahan yang berbentuk cair atau pasta. Cara kerja metode ini adalah sebagai berikut:
1. Sampel ditimbang 4-5 g dalam tabung ekstraksi, kemudian
ditambahkan 1,5 ml amonia 35 % (v/v), campur merata lalu ditambahkan 7 ml air hangat.
2. Campuran dipanaskan pada suhu 60-70 oC selama 15 menit, lalu ditambahkan 10 ml etanol, dikocok dan dibiarkan dingin.
3. Dalam tabung, ditambahkan 25 ml dietil eter, kocok merata selama 1 menit, biarkan dingin, kemudian ditambahkan 35 ml petroleum eter,
kocok merata selama 30 detik atau hingga lapisan eter jernih dan seluruhnya terpisah dari lapisan aqueous.
4. Dekantasi lapisan eter sebanyak mungkin, masukkan ke dalam labu 150 ml lalu ditambahkan 10 ml pelarut eter campuran ke dalam tabung dan tanpa pengocokan, pindahkan pelarut ke dalam labu.
5. Bagian luar tabung dicuci dengan pelarut eter campuran, masukkan cucian ke dalam tabung dan hilangkan pelarut yang ada dalam labu dengan cara distilasi.
6. Keringkan residu lemak dalam oven 100 ± 2 oC selama 1 jam, lalu tempatkan labu dalam desikator sampai dingin sedikitnya selama 30 menit, kemudian ditimbang
Perhitungan kadar lemak pada kupang putih (Corbula faba Hinds) :
% Lemak = W2 – (W3+W4) x 100 % W1
Keterangan : W1 = Berat sampel (g)
W2 = Berat labu + ekstrak (g)
W3 = Berat labu sesudah penghilangan lemak (g). W4 = Berat residu yang terekstrak dalam blanko (g) 3.4.2.2. Kadar Protein (Apriyantono 1989).
Penentuan kadar protein dilakukan dengan metode kjeldahl-mikro sebagai berikut :
1. Sampel ditimbang sebanyak 1 g dan dimasukkan ke dalam labu Kjeldahl 30 ml. kemudian ditambah H2SO4 dan selenium.
2. Sampel didihkan selama 2 jam sampai cairan menjadi jernih (hijau bening) lalu didinginkan dan ditambah air suling atau diencerkan sebanyak 100 ml.
3. Isi labu dipindahkan ke dalam alat destilasi sebanyak 10 ml, ditambah 10 ml NaOH, lalu didestilasi.
4. Destilat ditampung dalam erlenmeyer 125 ml yang berisi 25 ml H3BO3 hingga cairan berwarna biru.
5. Hasil destilasi kemudian dititrasi dengan HCl hingga terjadi perubahan warna merah.
Perhitungan kadar protein pada kupang putih (Corbula faba Hinds) :
% Nitrogen = (ml HCl kupang– ml HCl blanko)x 0.1 N HCl x 14 x 100 % mg kupang putih (Corbula faba Hinds)
% Kadar Protein = % Nitrogen x 6,25 3.4.2.3. Kadar Abu (Apriyantono 1989).
Kadar abu ditentukan dengan prosedur sebagai berikut :
1. Sampel sebanyak 5 gram dimasukkan ke dalam cawan pengabuan yang telah ditimbang dan dibakar di dalam tanur serta didinginkan dalam desikator.
2. Cawan yang berisi sampel dimasukkan ke dalam tanur pengabuan dan dibakar sampai didapat abu yang berwarna keabu-abuan selama 8 jam pada suhu 550 oC.
3. Cawan yang berisi abu tersebut didinginkan dalam desikator dan kemudian ditimbang.
Perhitungan kadar abu pada kupang putih (Corbula faba Hinds) :
% 100 % x A B A C KadarAbu − − =
Keterangan : A = Berat cawan abu porselen kosong (gram)
B = Berat cawan abu porselen dengan daging kupang putih (Corbula faba Hinds) (gram)
C = Berat cawan abu porselen dengan daging kupang putih (Corbula faba Hinds) setelah dikeringkan (gram).
3.4.2.4. Uji Kadar Air (Apriyantono 1989).
Prosedur penentuan kadar air adalah sebagai berikut :
1. Sampel yang sudah homogen ditimbang 5 gram dan diletakkan dalam cawan kosong yang sudah ditimbang beratnya, dimana cawan dan tutupnya sudah dikeringkan di dalam oven serta didinginkan dalam desikator.
2. Cawan yang berisi sampel kemudian ditutup dan dimasukkan ke dalam oven dengan suhu 100-102 oC selama 16 jam.
3. Cawan lalu didinginkan di dalam desikator dan setelah dingin cawan ditimbang.
Perhitungan kadar air pada kupang putih (Corbula faba Hinds) :
% 100 % x A B C B KadarAir − − =
Keterangan : A = Berat cawan kosong (gram)
B = Berat cawan dengan kupang putih (Corbula faba Hinds) (gram)
C = Berat cawan dengan daging ikan setelah dikeringkan (gram).
3.4.2.5. Kadar Karbohidrat (Apriyantono 1989).
Analisis kadar karbohidrat dilakukan secara by difference, yaitu dengan menggunakan rumus:
K. karbohidrat = 100 % - ( K. lemak – K. protein – K. air – K. abu)
3.4.2.6. Derajat Keasaman (pH) (AOAC 1995).
Untuk pengukuran pH dilakukan dengan menggunakan pH meter dengan cara mula-mula pH meter dinyalakan lalu dikalibrasi dengan larutan buffer pH 4 dan kemudian buffer pH 7.
Sampel ditimbang sebanyak 5 gram dan diencerkan dengan perbandingan petis kupang : air aquades (1:5) kemudian dihomogenkan dengan menggunakan mixer, setelah homogen sampel diukur dengan menggunakan pH meter yang telah dikalibrasi. Nilai yang diperoleh dari hasil pembacaan pada pH meter selama satu menit atau sampai angka digital yang menunjukkan nilai pH tidak berubah/konstans.
3.4.2.7. Aktivitas Air (aw) (Muchtadi 1984).
Analisis nilai aktivitas air (aw) menggunakan alat aw-meter Shibaura
Wa-360. Cara kerjanya sebagai berikut :
Sampel yang telah dihaluskan dan dihomogenkan dimasukkan ke dalam
aw-meter. Sebelum digunakan aw-meter harus dikalibrasi dengan menggunakan
barium klorida. Proses kalibrasi dilakukan selama 1 jam sampai tanda kompleted tertera pada alat aw-meter, kemudian ditekan tombol start setelah itu baru sampel
dalam alat aw-meter maka tombol start ditekan kembali sampai tanda kompleted
tertera kembali. Koreksi diberikan terhadap perbedaan suhu pengukuran dan suhu standar dengan mengalikan faktor koreksi yang terdapat dalam manual alat.
3.4.2.8 Uji TPC (Total Plate Count ) (Fardiaz 1992).
Pengukuran total mikroba dilakukan dengan uji mikroba secara aseptis, pada produk petis kupang ini dilakukan pengukuran total mikroba kapang, karena pada petis kupang mikroba yang paling banyak tumbuh adalah kapang.
Prosedur pengukuran total mikroba sebagai berikut:
Sampel diambil sebanyak 10 ml, kemudian sampel dimasukkan ke dalam labu erlenmeyer yang telah berisi larutan NaCl fisiologis sebanyak 90 ml dan diaduk sampai homogen (larutan dengan pengenceran 10-1), kemudian dilakukan pengenceran bertingkat 10-2, 10-3, 10-4 dan 10-5 dan masing-masing dituang sebanyak 1 ml ke dalam cawan petri dan dilakukan secara duplo. PCA dibiarkan hingga agar memadat dan diinkubasi selama 2 hari.
Perhitungan :
Koloni per ml atau per gram = Jumlah koloni per cawan x 1/ Faktor Pengencer 3.4.2.9 Penentuan kandungan logam berat (AOAC 2000)
Penentuan kandungan logam berat terbagi atas beberapa tahap. Tahap-tahap tersebut adalah destruksi, pembacaan absorbans contoh, dan perhitungan kandungan logam berat.
Metode analisis dilakukan berdasarkan Association of Official Analitical
Chemis (AOAC), edisi 14 tahun 1984 yang diadopsi menjadi SNI-2364-1991
untuk merkuri (Hg) dan SNI-2362-1991 untuk kadmium (Cd) dan timbal (Pb) : a. Tahap destruksi
Ke dalam labu alas bulat 250 ml dimasukkan 5 gram sampel, berturut-turut ditambahkan 20 ml HCl 37 % dan 10 ml HNO3 65 %. Kemudian dipanaskan dengan api spiritus selama 20 menit. setelah 20 menit api spiritus sementara dimatikan, kemudian dtambahkan H2O2 30 % dan dipanaskan lagi selama 10 menit atau sampai larutan menjadi jernih. Setelah dingin larutan dipindahkan ke dalam labu takar 100 ml kemudian ditambahkan aquades sampai tanda tera.
b. Pembacaan absorbans
Pembacaan absorbans logam berat merkuri dilakukan dengan spektrofotometer penyerapan atom tanpa nyala, sedangkan kadmium dan plumbum ditentukan dengan nyala asetilen.
Absorbans Untuk Logam Berat Merkuri (Hg)
Mercury Hydride System (MHS-10) dirangkai dengan alat AAS.
Kemudian AAS diaktifkan dan ditunggu selama 15 menit, kondisi optimum AAS dicari dengan mengatur posisi Hg, kedudukan sel absorbans, panjang gelombang, dan mengalirkan gas nitrogen (N2) ke dalam sistem.
• Pembacaan Absorbans Larutan Standar Merkuri
Ke dalam tabung A dimasukkan 10 ml larutan standar. Tabung B diisi dengan reduktor standar. Tabung C ditekan untuk memompa reduktor sehingga mengalir ke tabung A dan mereduksi larutan standar agar terbentuk kabut uap merkuri yang selanjutnya kabut uap tersebut didorong oleh gas N2 menuju sel absorbans. Di dalam sel absorbans uap Hg menyerap sinar dari lampu Hg pada panjang gelombang 253,7 nm. Nilai absorbans langsung dapat dibaca (pada digital display). Dibuat kurva absorbans vs konsentrasi sehingga didapat garis standar dengan persamaan garis Y= a+ bx (linier), dimana a adalah intersept yaitu jarak antara titik potong garis pada sumbu Y dengan titik pusat (0,0) dan b adalah kemiringan garis (slope).
• Pembacaan Absorbans Contoh
Dengan cara yang sama seperti absorbans standar, dilakukan pembacaan absorbans contoh dengan memasukkan contoh ke dalam tabung A dan reduktor contoh (daging) ke dalam tabung B. Absorbans Untuk Logam Berat Kadmium (Cd) dan Timbal (Pb) Pembacaan absorbans larutan standar dan absorbans contoh pada logam berat Cd dan Pb pada prinsipnya sama dengan pembacaan absorbans pada
analisis merkuri. Pada pembacaan absorbans logam berat Cd dan Pb menggunakan panjang gelombang 228,8 nm dan 283,3 nm. Untuk menghasilkan nyala api digunakan gas asetilen.
c. Perhitungan
Kadar logam berat sampel dihitung dengan memasukkan harga absorban contoh ke dalam persamaan garis standar.
Y = a + bx
Dimana nilai absorbans sebagai Y sedang a dan b dari persamaan garis standar, maka diperoleh harga x yang merupakan konsentrasi contoh. Hasil perhitungan dinyatakan dengan ppm.
ppm = (Ac - Ab) – a x 100
b x berat contoh (gr) x 1000
dimana : Ac = absorban contoh
Ab = absorban blanko
a = intersept dari persamaan regresi standar b = slop dari persamaan regresi standar
3.4.2.10 Uji viskositas (Marine Colloids FMC, Corp 1977 dalam Mukti 1987) Spindel terlebih dahulu dipanaskan pada suhu 75 oC kemudian dipasangkan ke alat ukur viscometer brookfield. Posisi spindel dalam larutan
panas diatur sampai tepat, viscometer dihidupkan dan suhu larutan diukur. Ketika suhu larutan mencapai suhu 75 oC, termometer dikeluarkan dan nilai viskositas diketahui dengan pembacaan viscometer pada skala 1 sampai 100. Pembacaan dilakukan setelah satu menit putaran penuh. Hasil bacaan digandakan sesuai dengan spindel yang digunakan dengan kecepatan 60 rpm. Hal ini berfungsi untuk menyatakan viskositas mutlak dalam satuan centipoise (cps).
3.5 Analisis Data
Pengujian organoleptik dilaksanakan dengan melibatkan 35 orang panelis secara deskriptif dengan menggunakan score sheet. Analisis data organoleptik
menggunakan statistik non-parametrik dengan metode Kruskal-Wallis dengan uji lanjut Multiple Comparison (Steel dan Torrie, 1989).
Rancangan percobaan yang digunakan pada analisis data penelitian ini adalah model rancangan acak lengkap (RAL). Asumsi yang digunakan dalam menggunakan rancangan percobaan ini adalah pengaruh perlakuan dan lingkungan bersifat aditif, ragam galat percobaan homogen, galat percobaan menyebar normal dan galat percobaan saling bebas. Nilai rata-rata dihitung menggunakan rumus berikut (Walpole 1975):
X = Nilai rata-rata N = Jumlah data Xi = Nilai X ke-i n Xi X n i
∑
= = 1Analisis pengaruh penambahan flavor udang windu (Penaeus monodon)
terhadap kandungan proksimat serta komposisi asam lemak ikan dilakukan melalui uji ragam (ANOVA) single factorial.
Persamaan umum model rancangan tersebut sebagai berikut: Yij = µ + σi + εij
Keterangan:
Yij = nilai pengamatan untuk perlakuan ke-i, ulangan ke-j µ = nilai tengah populasi
σi = pengaruh perlakuan pada taraf ke-i
εij = galat percobaan pada perlakuan ke-i, ulangan ke-j Hipotesis yang digunakan :
Ho : µi = µj H1 : µi ≠ µj
Apabila Fhit > Ftab maka tolak Ho artinya terdapat perlakuan yang berbeda nyata pengaruhnya terhadap produk petis kupang putih (Corbula faba Hinds).
Apabila Fhit < Ftab maka gagal tolak Ho artinya tidak terdapat perlakuan yang berbeda nyata pengaruhnya terhadap produk petis kupang putih (Corbula faba Hinds).