PENAPISAN AWAL KOMPONEN BIOAKTIF
DARI KIJING TAIWAN (Anodonta woodiana Lea.)
SEBAGAI SENYAWA ANTIOKSIDAN
Oleh:
Eka Ayuningrat C34104040
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea.) sebagai Senyawa Antioksidan adalah hasil karya saya sendiri dan belum pernah diajukan kepada perguruan tinggi manapun. Sumber informasi atau kutipan dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi.
Bogor, Januari 2009 Eka Ayuningrat
RINGKASAN
EKA AYUNINGRAT. C34104040. Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea.) sebagai Senyawa Antioksidan. Dibawah bimbingan ELLA SALAMAH dan SRI PURWANINGSIH.
Kijing Taiwan (Anodonta woodiana Lea) merupakan kerang-kerangan yang hidup di danau atau sungai. Tingkat reproduksinya yang tinggi menjadikan kijing Taiwan sangat potensial jika dibudidayakan. Kijing Taiwan sebenarnya telah lama dimanfaatkan oleh bangsa Cina sebagai obat untuk berbagai macam penyakit, membersihkan racun dalam tubuh, memperlancar sirkulasi darah, menambah energi, dan memperkuat daya tahan tubuh. Berbagai khasiat yang terdapat pada kijing Taiwan mendorong penelitian tentang kandungan bioaktif sebagai antioksidan yang terdapat di dalamnya.
Penelitian dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan utama. Penelitian pendahuluan dilakukan untuk menentukan jenis pelarut yang efektif untuk dapat mengekstrak senyawa antioksidan dari kijing Taiwan. Metode ekstraksi yang dilakukan adalah ekstraksi bertingkat untuk memisahkan ekstrak berdasarkan sifat kepolarannya. Pengujian antioksidan dilakukan dengan metode 1,1-diphenyl-2-picrylhydrazil (DPPH). Penelitian utama dilakukan untuk menentukan waktu maserasi paling optimal untuk mendapatkan ekstrak dengan sifat antioksidan paling tinggi. Pengujian ini dilanjutkan dengan penghitungan bilangan peroksida emulsi minyak dan uji fitokimia.
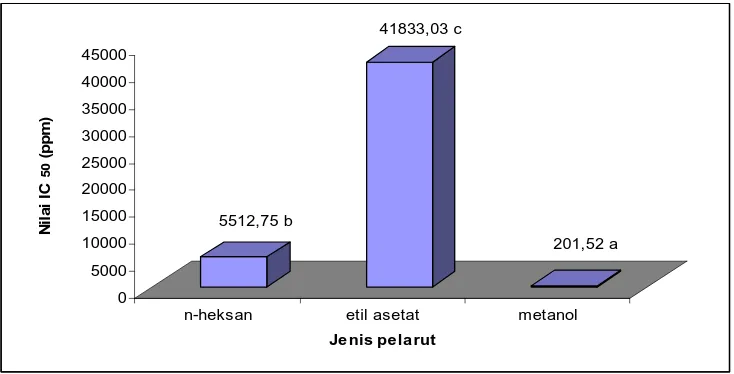
Jenis pelarut terbaik berdasarkan penelitian pendahuluan adalah metanol karena mempunyai nilai IC50 sebesar 201,52 ppm. Nilai tersebut menunjukkan bahwa pada konsentrasi sebesar 201,52 ppm, ekstrak kijing Taiwan mampu mereduksi radikal bebas (DPPH) sebanyak 50%, artinya ekstrak tersebut bersifat antioksidan. Hasil uji ekstrak dari maserasi dengan pelarut n-heksan dan etil asetat menunjukkan tidak bersifat sebagai antioksidan. Tahap penelitian utama dilakukan maserasi dengan pelarut metanol selama 24 jam, 48 jam, dan 72 jam. Hasil uji efek antioksidan paling tinggi diperoleh dari maserasi selama 72 jam dengan nilai IC50 sebesar 166,64 ppm. Pengujian penghitungan bilangan peroksida dilakukan menggunakan ekstrak dari hasil terbaik, yaitu maserasi kijing Taiwan dengan metanol selama 72 jam.
Bilangan peroksida dihitung dari emulsi minyak dengan tambahan ekstrak yang telah disimpan di inkubator suhu 36,9oC selama tujuh hari. Ekstrak yang ditambahkan pada emulsi minyak adalah sebesar 0 ppm, 2000 ppm, 3000 ppm, dan 4000 ppm. Hasil terbaik yang diperoleh adalah dari penambahan ekstrak
sebanyak 4000 ppm. Bilangan peroksida yang dihasilkan adalah sebesar 2,38 Meq/kg bahan. Bilangan peroksida yang terbentuk masih di bawah ambang
PENAPISAN AWAL KOMPONEN BIOAKTIF
DARI KIJING TAIWAN (Anodonta woodiana Lea.)
SEBAGAI SENYAWA ANTIOKSIDAN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh:
Eka Ayuningrat C34104040
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Judul Skripsi : PENAPISAN AWAL KOMPONEN BIOAKTIF DARI KIJING TAIWAN (Anodonta woodiana Lea.) SEBAGAI SENYAWA ANTIOKSIDAN
Nama : Eka Ayuningrat NRP : C34104040
Menyetujui, Komisi Pembimbing
Pembimbing I Pembimbing II
Dra. Ella Salamah, M.Si Dr. Ir. Sri Purwaningsih, M.Si
NIP. 131 788 597 NIP. 131 878 935
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Prof. Dr. Ir. Indra Jaya, M.Sc NIP. 131 578 799
KATA PENGANTAR
Puji syukur kehadirat Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga penelitian dengan judul Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea) sebagai Senyawa Antioksidan ini dapat diselesaikan oleh penulis. Adapun tujuan dari penyusunan skripsi ini adalah sebagai syarat kelulusan pada program sarjana Fakultas
Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis menyadari banyak kekurangsempurnaan dalam penulisan, karena itu
segala bentuk kritik dan saran yang membangun sangat diharapkan guna
tercapainya hasil yang lebih baik. Semoga bermanfaat.
Bogor, Januari 2009
UCAPAN TERIMA KASIH
Puji syukur kehadirat Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga penulis mampu menyelesaikan pendidikan di Institut
Pertanian Bogor ini dengan baik. Penulis mengucapkan terima kasih kepada
seluruh pihak yang telah membantu penyelesaian skripsi ini, diantaranya kepada:
1. Ibu Dra. Ella Salamah, M.Si dan Ibu Dr. Ir. Sri Purwaningsih, M.Si sebagai
komisi pembimbing atas segala masukan, kritik, arahan, motivasi, dan
bimbingan yang telah diberikan.
2. Bapak Dr. Ir. Bustami Ibrahim, M.Sc dan Ibu Ir. Anna C. Erungan, MS
sebagai penguji atas semua kritik, saran, dan masukan yang telah diberikan.
3. Bapak Ir. Djoko Poernomo, B.Sc selaku pembimbing akademik atas semua
bantuan dan dorongan semangat.
4. Ibu dan Bapak yang telah memberikan semuanya, semoga selalu berada
dalam lindungan Allah SWT dan selalu sehat wal’afiat.
5. Adik-adikku (Ichwan, Husein, dan Ghofur), juga kepada Shifa dan Afi atas
segala keceriaan dalam hidup.
6. Mbah Putri, Mbah Kakung, Mbak Anik, Mas Ipul, Bulik Puk, dan semua
anggota keluarga besar di Blitar, Bogor, Pondok Gede, dan Surabaya atas
doa dan dukungannya.
7. Ika, Nia, Dilla, Sereli. Jaga persahabatan kita karena persahabatan itu abadi.
8. Sahabat-sahabatku di THP 41: Anang, An’im, Amelia, Estrid, Yanti, Tyas,
Enif, Ulfah, Nuzul, Windhyka, Glory, Gilang, Yudha, Rijan, Masikah,
Wisnu, Erlangga, Yugha, Dede, Santi, Luh Putu Ari, Vika, Vera, Ima, Indah,
Andi, Andika, Alim, Yudha, Rijal, dan teman-teman lain yang tidak bisa
disebutkan satu persatu. Juga kepada rekan-rekan THP 39, 40, 42, dan 43
yang pernah mengisi hari-hari yang telah lewat.
9. Teman-teman di Blitar (Lailatul, Rahma, Irma, Tika, Lia, Diah, Sofwan,
Bayu, Radith, Iqbal, dan semuanya) yang mengajari tentang arti hidup yang
lebih baik dan cara mendewasakan diri.
10. Para penghuni Kawah Kelud dan Pondok An-Nur, untuk semua kenangan
11. Bu Ema, Mbak Icha, Om Zacky, Mas Ipul, Umi atas semua bantuan dan
suntikan semangat selama berjuang di THP.
12. Pak Nurwanto di PAU, Mbak Ina, Mbak Nunuk, Mbak Titis, Endi di
Biofarmaka atas bantuan dan saran yang sangat membantu selesainya skripsi
ini.
13. Basuki Sulistyana atas dukungan, perhatian, dan semua hal yang pernah
terkorbankan.
14. Semua pihak yang telah membantu penulis dari awal sampai sekarang yang
tidak bisa disebutkan satu per satu.
Kesempurnaan skripsi ini tidak terlepas dari segala kritik dan saran yang
membangun dari semua pihak. Semoga skripsi ini dapat bermanfaat bagi penulis
RIWAYAT HIDUP
Penulis dilahirkan di Blitar, 13 Juni 1986 dari ayah
M. Ghufron dan ibu Sri Eko Martiningsih. Penulis merupakan
anak pertama dari empat bersaudara. Tahun 2004 penulis
menyelesaikan pendidikan di SMA Negeri I Blitar dan pada
tahun yang sama lulus seleksi masuk IPB melalui jalur
Undangan Seleksi Masuk IPB pada Program Studi Teknologi
Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan.
Selama menjadi mahasiswa, penulis aktif dalam organisasi
HIMASILKAN sebagai staff Hubungan Luar dan Komunikasi (Hublukom) pada
tahun 2005/2006, staff Pengabdian Mahasiswa dan Masyarakat (PMM) pada
tahun 2006/2007, dan bendahara pada tahun 2007/2008. Penulis juga menjadi
koordinator asisten mata kuliah Teknologi Pengolahan Tradisional Hasil
Perikanan tahun ajaran 2007/2008 dan mata kuliah Biotoksikologi Hasil Perairan
tahun ajaran 2008/2009. Pada tahun 2008 penulis menjuarai Kompetisi Pemikiran
Kritis Mahasiswa (KPKM) tingkat nasional bidang perekonomian sebagai juara II,
dengan judul karya tulis Tantangan dalam Meningkatkan Standar Kualitas Udang
Ekspor Indonesia melalui Traceability System.
Penulis menyelesaikan studi di Institut Pertanian Bogor dengan
DAFTAR ISI
Halaman
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujuan ... 2
2. TINJAUAN PUSTAKA ... 3
2.1. Kijing Taiwan (Anodonta woodiana Lea) ... 3
2.2. Penapisan Komponen Bioaktif ... 5
2.3. Radikal Bebas ... 9
2.4. Antioksidan ... 10
3. METODOLOGI ... 14
3.1. Waktu dan Tempat ... 14
3.2. Alat dan Bahan ... 14
3.3. Tahapan Penelitian ... 14
3.3.1. Penelitian Pendahuluan ... 15
3.3.1.1. Ekstraksi Senyawa Bioaktif ... 15
3.3.1.2. Uji Antioksidan (DPPH) ... 17
3.3.2. Penelitian Utama ... 17
3.3.2.1. Uji Antioksidan (DPPH) ... 17
3.3.2.2. Evaluasi Aktivitas Antioksidan (Penentuan Bilangan Peroksida) ... 18
3.3.3. Fitokimia ... 19
3.3.3.1. Uji Alkaloid ... 19
3.3.3.2. Uji Triterpenoid/steroid ... 19
3.3.3.3. Uji Flavonoid ... 20
3.3.4. Rancangan Percobaan dan Analisis Data ... 20
4. HASIL DAN PEMBAHASAN ... 22
4.1. Penelitian Pendahuluan ... 22
4.1.1. Ekstraksi Senyawa Bioaktif ... 22
4.1.2. Penentuan Jenis Pelarut dengan Uji Antioksidan Metode DPPH ... 22
PENAPISAN AWAL KOMPONEN BIOAKTIF
DARI KIJING TAIWAN (Anodonta woodiana Lea.)
SEBAGAI SENYAWA ANTIOKSIDAN
Oleh:
Eka Ayuningrat C34104040
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea.) sebagai Senyawa Antioksidan adalah hasil karya saya sendiri dan belum pernah diajukan kepada perguruan tinggi manapun. Sumber informasi atau kutipan dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi.
Bogor, Januari 2009 Eka Ayuningrat
RINGKASAN
EKA AYUNINGRAT. C34104040. Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea.) sebagai Senyawa Antioksidan. Dibawah bimbingan ELLA SALAMAH dan SRI PURWANINGSIH.
Kijing Taiwan (Anodonta woodiana Lea) merupakan kerang-kerangan yang hidup di danau atau sungai. Tingkat reproduksinya yang tinggi menjadikan kijing Taiwan sangat potensial jika dibudidayakan. Kijing Taiwan sebenarnya telah lama dimanfaatkan oleh bangsa Cina sebagai obat untuk berbagai macam penyakit, membersihkan racun dalam tubuh, memperlancar sirkulasi darah, menambah energi, dan memperkuat daya tahan tubuh. Berbagai khasiat yang terdapat pada kijing Taiwan mendorong penelitian tentang kandungan bioaktif sebagai antioksidan yang terdapat di dalamnya.
Penelitian dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan utama. Penelitian pendahuluan dilakukan untuk menentukan jenis pelarut yang efektif untuk dapat mengekstrak senyawa antioksidan dari kijing Taiwan. Metode ekstraksi yang dilakukan adalah ekstraksi bertingkat untuk memisahkan ekstrak berdasarkan sifat kepolarannya. Pengujian antioksidan dilakukan dengan metode 1,1-diphenyl-2-picrylhydrazil (DPPH). Penelitian utama dilakukan untuk menentukan waktu maserasi paling optimal untuk mendapatkan ekstrak dengan sifat antioksidan paling tinggi. Pengujian ini dilanjutkan dengan penghitungan bilangan peroksida emulsi minyak dan uji fitokimia.
Jenis pelarut terbaik berdasarkan penelitian pendahuluan adalah metanol karena mempunyai nilai IC50 sebesar 201,52 ppm. Nilai tersebut menunjukkan bahwa pada konsentrasi sebesar 201,52 ppm, ekstrak kijing Taiwan mampu mereduksi radikal bebas (DPPH) sebanyak 50%, artinya ekstrak tersebut bersifat antioksidan. Hasil uji ekstrak dari maserasi dengan pelarut n-heksan dan etil asetat menunjukkan tidak bersifat sebagai antioksidan. Tahap penelitian utama dilakukan maserasi dengan pelarut metanol selama 24 jam, 48 jam, dan 72 jam. Hasil uji efek antioksidan paling tinggi diperoleh dari maserasi selama 72 jam dengan nilai IC50 sebesar 166,64 ppm. Pengujian penghitungan bilangan peroksida dilakukan menggunakan ekstrak dari hasil terbaik, yaitu maserasi kijing Taiwan dengan metanol selama 72 jam.
Bilangan peroksida dihitung dari emulsi minyak dengan tambahan ekstrak yang telah disimpan di inkubator suhu 36,9oC selama tujuh hari. Ekstrak yang ditambahkan pada emulsi minyak adalah sebesar 0 ppm, 2000 ppm, 3000 ppm, dan 4000 ppm. Hasil terbaik yang diperoleh adalah dari penambahan ekstrak
sebanyak 4000 ppm. Bilangan peroksida yang dihasilkan adalah sebesar 2,38 Meq/kg bahan. Bilangan peroksida yang terbentuk masih di bawah ambang
PENAPISAN AWAL KOMPONEN BIOAKTIF
DARI KIJING TAIWAN (Anodonta woodiana Lea.)
SEBAGAI SENYAWA ANTIOKSIDAN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh:
Eka Ayuningrat C34104040
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Judul Skripsi : PENAPISAN AWAL KOMPONEN BIOAKTIF DARI KIJING TAIWAN (Anodonta woodiana Lea.) SEBAGAI SENYAWA ANTIOKSIDAN
Nama : Eka Ayuningrat NRP : C34104040
Menyetujui, Komisi Pembimbing
Pembimbing I Pembimbing II
Dra. Ella Salamah, M.Si Dr. Ir. Sri Purwaningsih, M.Si
NIP. 131 788 597 NIP. 131 878 935
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Prof. Dr. Ir. Indra Jaya, M.Sc NIP. 131 578 799
KATA PENGANTAR
Puji syukur kehadirat Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga penelitian dengan judul Penapisan Awal Komponen Bioaktif dari Kijing Taiwan (Anodonta woodiana Lea) sebagai Senyawa Antioksidan ini dapat diselesaikan oleh penulis. Adapun tujuan dari penyusunan skripsi ini adalah sebagai syarat kelulusan pada program sarjana Fakultas
Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis menyadari banyak kekurangsempurnaan dalam penulisan, karena itu
segala bentuk kritik dan saran yang membangun sangat diharapkan guna
tercapainya hasil yang lebih baik. Semoga bermanfaat.
Bogor, Januari 2009
UCAPAN TERIMA KASIH
Puji syukur kehadirat Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga penulis mampu menyelesaikan pendidikan di Institut
Pertanian Bogor ini dengan baik. Penulis mengucapkan terima kasih kepada
seluruh pihak yang telah membantu penyelesaian skripsi ini, diantaranya kepada:
1. Ibu Dra. Ella Salamah, M.Si dan Ibu Dr. Ir. Sri Purwaningsih, M.Si sebagai
komisi pembimbing atas segala masukan, kritik, arahan, motivasi, dan
bimbingan yang telah diberikan.
2. Bapak Dr. Ir. Bustami Ibrahim, M.Sc dan Ibu Ir. Anna C. Erungan, MS
sebagai penguji atas semua kritik, saran, dan masukan yang telah diberikan.
3. Bapak Ir. Djoko Poernomo, B.Sc selaku pembimbing akademik atas semua
bantuan dan dorongan semangat.
4. Ibu dan Bapak yang telah memberikan semuanya, semoga selalu berada
dalam lindungan Allah SWT dan selalu sehat wal’afiat.
5. Adik-adikku (Ichwan, Husein, dan Ghofur), juga kepada Shifa dan Afi atas
segala keceriaan dalam hidup.
6. Mbah Putri, Mbah Kakung, Mbak Anik, Mas Ipul, Bulik Puk, dan semua
anggota keluarga besar di Blitar, Bogor, Pondok Gede, dan Surabaya atas
doa dan dukungannya.
7. Ika, Nia, Dilla, Sereli. Jaga persahabatan kita karena persahabatan itu abadi.
8. Sahabat-sahabatku di THP 41: Anang, An’im, Amelia, Estrid, Yanti, Tyas,
Enif, Ulfah, Nuzul, Windhyka, Glory, Gilang, Yudha, Rijan, Masikah,
Wisnu, Erlangga, Yugha, Dede, Santi, Luh Putu Ari, Vika, Vera, Ima, Indah,
Andi, Andika, Alim, Yudha, Rijal, dan teman-teman lain yang tidak bisa
disebutkan satu persatu. Juga kepada rekan-rekan THP 39, 40, 42, dan 43
yang pernah mengisi hari-hari yang telah lewat.
9. Teman-teman di Blitar (Lailatul, Rahma, Irma, Tika, Lia, Diah, Sofwan,
Bayu, Radith, Iqbal, dan semuanya) yang mengajari tentang arti hidup yang
lebih baik dan cara mendewasakan diri.
10. Para penghuni Kawah Kelud dan Pondok An-Nur, untuk semua kenangan
11. Bu Ema, Mbak Icha, Om Zacky, Mas Ipul, Umi atas semua bantuan dan
suntikan semangat selama berjuang di THP.
12. Pak Nurwanto di PAU, Mbak Ina, Mbak Nunuk, Mbak Titis, Endi di
Biofarmaka atas bantuan dan saran yang sangat membantu selesainya skripsi
ini.
13. Basuki Sulistyana atas dukungan, perhatian, dan semua hal yang pernah
terkorbankan.
14. Semua pihak yang telah membantu penulis dari awal sampai sekarang yang
tidak bisa disebutkan satu per satu.
Kesempurnaan skripsi ini tidak terlepas dari segala kritik dan saran yang
membangun dari semua pihak. Semoga skripsi ini dapat bermanfaat bagi penulis
RIWAYAT HIDUP
Penulis dilahirkan di Blitar, 13 Juni 1986 dari ayah
M. Ghufron dan ibu Sri Eko Martiningsih. Penulis merupakan
anak pertama dari empat bersaudara. Tahun 2004 penulis
menyelesaikan pendidikan di SMA Negeri I Blitar dan pada
tahun yang sama lulus seleksi masuk IPB melalui jalur
Undangan Seleksi Masuk IPB pada Program Studi Teknologi
Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan.
Selama menjadi mahasiswa, penulis aktif dalam organisasi
HIMASILKAN sebagai staff Hubungan Luar dan Komunikasi (Hublukom) pada
tahun 2005/2006, staff Pengabdian Mahasiswa dan Masyarakat (PMM) pada
tahun 2006/2007, dan bendahara pada tahun 2007/2008. Penulis juga menjadi
koordinator asisten mata kuliah Teknologi Pengolahan Tradisional Hasil
Perikanan tahun ajaran 2007/2008 dan mata kuliah Biotoksikologi Hasil Perairan
tahun ajaran 2008/2009. Pada tahun 2008 penulis menjuarai Kompetisi Pemikiran
Kritis Mahasiswa (KPKM) tingkat nasional bidang perekonomian sebagai juara II,
dengan judul karya tulis Tantangan dalam Meningkatkan Standar Kualitas Udang
Ekspor Indonesia melalui Traceability System.
Penulis menyelesaikan studi di Institut Pertanian Bogor dengan
DAFTAR ISI
Halaman
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
1. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujuan ... 2
2. TINJAUAN PUSTAKA ... 3
2.1. Kijing Taiwan (Anodonta woodiana Lea) ... 3
2.2. Penapisan Komponen Bioaktif ... 5
2.3. Radikal Bebas ... 9
2.4. Antioksidan ... 10
3. METODOLOGI ... 14
3.1. Waktu dan Tempat ... 14
3.2. Alat dan Bahan ... 14
3.3. Tahapan Penelitian ... 14
3.3.1. Penelitian Pendahuluan ... 15
3.3.1.1. Ekstraksi Senyawa Bioaktif ... 15
3.3.1.2. Uji Antioksidan (DPPH) ... 17
3.3.2. Penelitian Utama ... 17
3.3.2.1. Uji Antioksidan (DPPH) ... 17
3.3.2.2. Evaluasi Aktivitas Antioksidan (Penentuan Bilangan Peroksida) ... 18
3.3.3. Fitokimia ... 19
3.3.3.1. Uji Alkaloid ... 19
3.3.3.2. Uji Triterpenoid/steroid ... 19
3.3.3.3. Uji Flavonoid ... 20
3.3.4. Rancangan Percobaan dan Analisis Data ... 20
4. HASIL DAN PEMBAHASAN ... 22
4.1. Penelitian Pendahuluan ... 22
4.1.1. Ekstraksi Senyawa Bioaktif ... 22
4.1.2. Penentuan Jenis Pelarut dengan Uji Antioksidan Metode DPPH ... 22
4.2. Penelitian Utama ... 25
4.2.1. Penentuan Waktu Maserasi dengan Uji Antioksidan Metode DPPH ... 25
4.2.2. Evaluasi Aktivitas Antioksidan dengan Pengukuran Bilangan Peroksida ... 28
4.3. Hasil Uji Fitokimia ... 30
5. KESIMPULAN DAN SARAN ... 33
5.1. Kesimpulan ... 33
5.2. Saran ... ... 33
DAFTAR PUSTAKA ... 34
DAFTAR TABEL
No. Teks
Halaman
1 Kandungan gizi kijing Taiwan per 100 g bahan ... 4
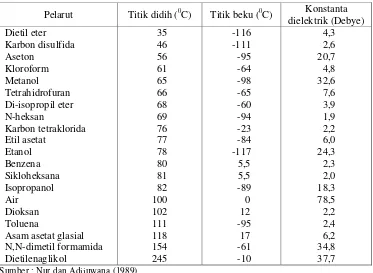
2 Beberapa pelarut organik dan sifat fisiknya ... 6
3 Pembagian panjang gelombang sinar tampak ... 13
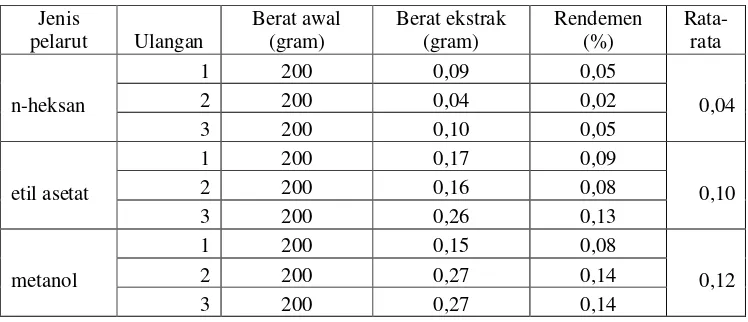
4 Data rendemen ekstrak kijing Taiwan pada berbagai pelarut ... 23
5 Data rendemen ekstrak kijing Taiwan pada berbagai
waktu maserasi ... 26
6 Hasil uji fitokimia ekstrak kijing Taiwan dengan maserasi
metanol selama 72 jam ... 31
DAFTAR GAMBAR
No. Teks Halaman
1 Anatomi bivalvia secara umum ... 3
2 Reaksi penghambatan antioksidan primer terhadap radikal lipid ... 11
3 Struktur awal DPPH dan DPPH tereduksi ... 12
4 Struktur umum kelompok senyawa yang mempunyai
aktivitas antioksidan ... 13
5 Tahapan proses ekstraksi ... 16
6 Kijing Taiwan (Anodonta woodiana Lea.) yang digunakan
dalam penelitian ... 22
7 Grafik hasil uji antioksidan dengan metode DPPH terhadap ekstrak kijing Taiwan berdasarkan jenis pelarut ... 24
8 Grafik hasil uji antioksidan dengan metode DPPH terhadap ekstrak kijing Taiwan berdasarkan waktu maserasi ... 27
9 Bilangan peroksida pada emulsi minyak dengan penambahan
ekstrak kijing Taiwan ... 29
10 Hasil uji fitokimia (alkaloid, flavonoid, dan steroid)
terhadap ekstrak kijing Taiwan dari maserasi dengan metanol
selama 72 jam ... 31
DAFTAR LAMPIRAN
No.
Halaman 1 Urutan proses ekstraksi kijing Taiwan (Anodonta woodiana Lea.) ... 38
2 Contoh perhitungan nilai rendemen ekstrak kijing Taiwan ... 39
3 Analisis sidik ragam rendemen ekstrak kijing Taiwan
berdasarkan jenis pelarut ... 40
4 Hasil uji Duncan terhadap rendemen ekstrak kijing Taiwan
berdasarkan jenis pelarut ... 40
5 Uji aktivitas antioksidan dengan DPPH terhadap perlakuan
jenis pelarut ... 41
6 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan pelarut n-heksan ... 43
7 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan pelarut etil asetat ... 44
8 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan pelarut metanol ... 45
9 Contoh perhitungan nilai IC50 ... 46
10 Analisis sidik ragam perlakuan jenis pelarut
(transformasi logaritma) ... 47
11 Hasil uji Duncan terhadap perlakuan jenis pelarut
(transformasi logaritma) ... 47
12 Analisis sidik ragam rendemen ekstrak kijing Taiwan
berdasarkan waktu maserasi ... 48
13 Uji aktivitas antioksidan dengan DPPH terhadap perlakuan
waktu maserasi ... 49
14 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan waktu maserasi 24 jam ... 51
15 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan waktu maserasi 48 jam ... 52
16 Kurva aktivitas antioksidan ekstrak kijing Taiwan
dengan waktu maserasi 72 jam ... 53
17 Analisis sidik ragam perlakuan waktu maserasi ... 54
18 Hasil uji Duncan terhadap perlakuan waktu maserasi ... 54
19 Contoh perhitungan bilangan peroksida emulsi minyak
20 Analisis sidik ragam terhadap bilangan peroksida sampel minyak dengan penambahan ekstrak kijing Taiwan ... 56
21 Hasil uji Duncan terhadap bilangan peroksida sampel minyak
dengan penambahan ekstrak kijing Taiwan ... 56
1. PENDAHULUAN
1.1. Latar Belakang
Indonesia sebagai negara kepulauan memiliki keanekaragaman
sumberdaya perairan yang sangat melimpah. Wilayah perairan yang sangat luas
mampu menyediakan berbagai jenis ikan, karang, rumput laut, kerang-kerangan,
dan sumberdaya lain yang masih sangat potensial. Salah satu sumberdaya yang
belum dimanfaatkan secara optimal adalah kerang-kerangan.
Kijing Taiwan (Anodonta woodiana Lea) merupakan kerang-kerangan
yang hidup di danau atau sungai. Kerang jenis ini mempunyai keistimewaan,
yaitu dapat mengatur tingkat metabolisme O2 dengan baik sehingga masih bisa
hidup pada keadaan perairan yang berkadar O2 rendah (Soeseno 1984). Kijing
Taiwan juga mampu berkembang biak dengan cepat. Sekali memijah kijing
Taiwan mampu menghasilkan telur sebanyak 369.227 – 458.000 butir telur.
Kenyataan ini menunjukkan bahwa kijing Taiwan sangat potensial untuk
dibudidayakan (Suwignyo et al 1981).
Kerang ini sebenarnya bukan kerang asli dari Indonesia, diduga bahwa
kijing Taiwan masuk ke Indonesia melalui ikan nila atau ikan mola yang dibawa
dari Taiwan sekitar tahun 1960 sampai 1970. Nama kijing Taiwan akhirnya
diambil dari daerah asal tersebut (Hasim 2008).
Kijing Taiwan mempunyai berbagai manfaat. Kerang ini bersifat filter
feeder karena hidupnya yang berada di dasar perairan tergenang atau mengalir.
Makanannya berupa detritus membuatnya menjadi biofilter perairan yang efektif
sehingga dapat membantu dalam usaha penjernihan air (Suwignyo et al. 1981).
Menurut Liu et al (2008), Kijing Taiwan sebenarnya telah lama dimanfaatkan
oleh bangsa Cina sebagai obat untuk berbagai macam penyakit, seperti lever dan
diabetes. Bahkan dalam Kamus Obat-obatan Tradisional Cina (Zhong Yao Da Ci
Dian), kerang Anodonta woodiana mempunyai khasiat untuk membersihkan
racun dalam tubuh, memperlancar sirkulasi darah, menambah energi, dan
memperkuat daya tahan tubuh.
Penyebaran kijing Taiwan di Indonesia sudah cukup luas. Usaha
terdapat di Bogor, Cianjur, Yogyakarta, dan Jawa Tengah. Konsumsi kijing
Taiwan di daerah-daerah tersebut terus meningkat walaupun pemanfaatannya
masih terbatas untuk konsumsi (Suwignyo et al 1981).
Berbagai penelitian mengenai manfaat kijing Taiwan membuka wawasan
yang lebih luas tentang kandungan komponen bioaktif yang terdapat di dalamnya.
Kenyataan bahwa kijing Taiwan mampu memberikan efek menyehatkan bila
dikonsumsi memberikan dugaan bahwa terdapat suatu komponen yang bersifat
antioksidan. Antioksidan sendiri merupakan suatu zat yang dapat menangkal
pengaruh radikal bebas yang bila masuk ke dalam tubuh dapat menyebabkan
kerusakan. Pengaruh negatif yang diakibatkan oleh radikal bebas diantaranya
penuaan dini, jantung koroner, kanker (Muchtadi 2000). Senyawa-senyawa aktif
dari kijing Taiwan yang diperoleh dari hasil penelitian ini diharapkan dapat
dimanfaatkan dalam bidang farmasi, pangan, industri, dan lain-lain.
1.2. Tujuan
Tujuan utama dari penelitian ini adalah untuk membuktikan adanya
komponen antioksidan pada kijing Taiwan (Anodonta woodiana Lea) melalui
ekstraksi bertingkat dengan pelarut polar, semi polar, dan nonpolar, sedangkan
tujuan khusus yang ingin dicapai antara lain:
1) Menentukan jenis pelarut yang dapat menghasilkan ekstrak dengan aktivitas
antioksidan terbaik.
2) Menentukan waktu maserasi yang paling optimal yang dapat menghasilkan
ekstrak dengan aktivitas antioksidan terbaik.
3) Mengaplikasikan ekstrak terbaik pada emulsi minyak dan menentukan jumlah
optimal ekstrak yang dapat menghambat pembentukan peroksida.
4) Mengetahui jenis dan sifat komponen bioaktif yang terdapat pada kijing
2. TINJAUAN PUSTAKA
2.1. Kijing Taiwan (Anodonta woodiana Lea)
Kerang jenis Anodonta woodiana ini berasal dari Taiwan, oleh karena
itulah ia dikenal juga dengan sebutan kerang atau kijing taiwan. Kerang ini
masuk ke Indonesia tanpa sengaja karena ikut terbawa saat Indonesia mengimpor
ikan mola (Hypophthalmichtys molitrix) dari Taiwan sekitar akhir 1960-an hingga
awal 1970-an (Hasim 2008).
Kijing Taiwan dapat hidup di beberapa ekosistem perairan tawar karena
memiliki kemampuan menyedot air dan menyaring partikel dalam air 40 L per
hari per ekor. Pertumbuhan kijing Taiwan cepat pada habitat air yang
menggenang. Bahkan pada beberapa perairan, kijing Taiwan terjaga
kontinuitasnya walaupun tidak dibudidayakan dengan sengaja (BPPT 2008).
Anatomi kijing Taiwan disajikan dalam gambar bivalvia secara umum seperti
yang disajikan pada Gambar 1.
Berikut ini merupakan klasifikasi kijing Taiwan menurut Parker dan
Haswell (1960) diacu dalam Suwignyo et al. (1981):
Kingdom : Animalia
Phylum : Mollusca
Kelas : Lamellibranchiata
Ordo : Eulamellibranchiata
Famili : Unionidae
Genus : Anodonta
Spesies : Anodonta woodiana Lea.
Kandungan gizi kijing Taiwan cukup tinggi. Pemanfaatannya sebagai
bahan makanan dapat dijadikan sebagai alternatif sumber protein dan zat besi
karena jumlahnya yang tinggi. Kandungan asam aminonya cukup lengkap, yang
tertinggi adalah asam glutamat yang mencapai 1020 mg/100 g bahan. Kijing
Taiwan juga mempunyai asam amino pembatas yaitu valine dengan nilai sebesar
287 mg/100 g bahan (Suwignyo et al 1981). Kandungan gizi kijing taiwan secara
lengkap dapat dilihat pada Tabel 1.
Tabel 1. Kandungan gizi kijing Taiwan per 100 g bahan
Komposisi kimia Kadar
Kijing Taiwan mempunyai cangkang yang simetri bilateral dan terdiri dari
dua buah keping pada bagian kanan dan kiri. Kedua keping cangkang kerang ini
cembung berwarna hijau kebiru-biruan dan kecoklat-coklatan. Cangkang terdiri
berupa kristal kalsium karbonat dan lapisan dalam sebagai lapisan mutiara yang
mengandung kalsium karbonat dan dapat memantulkan cahaya. Pada bagian
dorsal cangkang terdapat hinge-ligament yang merupakan tempat pertautan dari
kedua cangkang dan pada bagian anterior ligament terdapat penonjolan yang
disebut umbo. Sekeliling umbo terdapat garis pertumbuhan tahunan yang
kelihatan nyata (BPPT 2008).
Hewan ini tergolong filter feeder yaitu jenis hewan yang mendapatkan
makanan dengan jalan menyaring air yang masuk ke dalam tubuhnya. Volume air
yang dapat disaring oleh kijing Taiwan adalah 2,5 liter per individu dewasa per
jam. Makanan yang masuk bersama air tadi digerakkan, diperas, lalu dicerna
dengan bantuan cilia (rambut getar) pada tubuhnya. Cilia mampu bergerak 2-20
kali per detik. Makanan yang masuk dapat berupa zooplankton, fitoplankton,
bakteri, flagellata, protozoa, detritus, alga, dan berbagai zat yang tersuspensi
dalam perairan tempat tinggalnya. Alat pencernaannya berturut-turut terdiri dari
mulut yang tidak berahang atau bergigi, sepasang labial palps yang bercilia,
esofagus, lambung, usus, rektum, dan anus. Dalam tubuh kerang terdapat pula hati
yang menyelubungi dinding lambung, ginjal, pembuluh darah, dan pembuluh urat
saraf (Hasim 2008).
Lingkungan yang cocok untuk habitat kijing Taiwan adalah dasar perairan
yang berupa lumpur dengan pasir atau sedimen yang membentuk lapisan tanah
yang tidak padat. Suhu perairan yang optimal harus berkisar antara 11-29°C
dengan derajat keasaman (pH) antara 4,8 sampai 9,8. Umumnya kijing dapat
mengatur tingkat metabolisme oksigen dengan baik sehingga masih dapat hidup
pada keadaan di mana kadar oksigen dalam air sangat sedikit (BPPT 2008).
2.2. Penapisan Komponen Bioaktif
Penapisan merupakan pemisahan suatu bahan dari zat-zat pencemar atau
endapan. Penapisan juga dapat diartikan sebagai proses pemisahan bahan
berdasarkan perbedaan ukuran atau sifat (KBBI 1990). Proses penapisan
dilakukan untuk mendapatkan ekstrak dari hewan atau tumbuhan yang selanjutnya
dapat dianalisis kandungannya. Penapisan mempunyai pengertian yang sedikit
berbeda dengan ekstraksi. Ekstraksi merupakan suatu proses yang secara selektif
dilakukan dengan tujuan untuk memperoleh ekstrak murni atau ekstrak yang
hanya terdiri dari satu komponen tunggal, sedangkan proses penapisan dilakukan
untuk mendapatkan ekstrak yang lebih kasar. Secara umum proses penapisan
lebih sederhana daripada ekstraksi. Namun dalam banyak sumber, semua
prosedur untuk menarik kaomponen aktif dari suatu bahan sampai diperoleh
ekstrak disebut dengan ekstraksi (Achmadi 1992).
Teknik ekstraksi didasarkan pada kenyataan bahwa jika suatu zat dapat
larut dalam dua fase yang tidak tercampur, maka zat itu dapat dialihkan dari fase
yang satu ke fase yang lain dengan mengocoknya bersamaan. Pemilihan pelarut
yang digunakan tergantung pada sifat zat yang dilarutkan, karena setiap zat
memiliki kelarutan yang berbeda dalam pelarut yang berlainan (Achmadi 1992).
Sifat-sifat pelarut yang dapat dijadikan acuan pemilihan pelarut dapat dilihat pada
Tabel 2.
Tabel 2. Beberapa pelarut organik dan sifat fisiknya
Pelarut Titik didih (0C) Titik beku (0C) Konstanta Sumber : Nur dan Adijuwana (1989)
Gaya yang bekerja dalam proses ekstraksi adalah akibat adanya perbedaan
konsentrasi antara larutan di dalam sel dengan cairan ekstraksi yang berada di luar
protoplasma membengkak dan bahan kandungan sel akan terlarut sesuai
kelarutannya (Voight 1994).
Metode ekstraksi berdasarkan jenis pelarutnya dapat dilakukan dengan dua
cara yaitu aqueous phase dan organic phase. Cara aqueous phase dilakukan
dengan menggunakan air, sedangkan cara organic phase dilakukan dengan pelarut
organik. Prinsip ekstraksi menggunakan pelarut organik adalah bahan yang akan
diekstrak kontak langsung dengan pelarut pada waktu tertentu, kemudian diikuti
dengan pemisahan bahan yang diekstrak. Hal-hal yang harus dipertimbangkan
saat memilih pelarut antara lain (Achmadi 1992) :
1) Pelarut polar akan melarutkan senyawa polar dan pelarut non polar akan
melarutkan senyawa non polar.
2) Pelarut organik cenderung melarutkan senyawa organik.
3) Air cenderung melarutkan senyawa organik dan garam dari asam maupun
basa organik.
4) Asam-asam organik yang larut dalam pelarut organik dapat diekstraksi
dengan menggunakan basa (NaOH, Na2CO3, dan NaHCO3).
Metode ekstraksi juga dikelompokkan berdasarkan tingkat kesulitannya,
yaitu ekstraksi sederhana dan ekstraksi khusus (Harborne 1987). Ekstraksi
sederhana terdiri atas:
1) Maserasi, yaitu metode ekstraksi dengan cara merendam sampel dalam
pelarut dengan atau tanpa pengadukan.
2) Perkolasi, yaitu metode ekstraksi secara berkesinambungan.
3) Reperkolasi, yaitu perkolasi dimana hasil perkolasi digunakan untuk
melarutkan sampel di dalam perkolator sampai senyawa kimianya terlarutkan.
4) Diakolasi, yaitu perkolasi dengan penambahan tekanan udara.
Ekstraksi khusus terdiri atas:
1) Soxhletasi, yaitu metode ekstraksi secara berkesinambungan untuk
melarutkan sampel kering dengan menggunakan pelarut bervariasi.
2) Arus balik, yaitu metode ekstraksi secara berkesinambungan dimana sampel
dan pelarut saling bertemu melalui gerakan aliran yang berlawanan.
3) Ultrasonik, yaitu metode ekstraksi dengan alat yang menghasilkan frekuensi
Sifat penting yang harus diperhatikan dalam pemilihan pelarut adalah
kepolaran senyawa yang dilihat dari gugus polarnya (seperti gugus OH, COOH,
dan lain-lain). Derajat polaritas tergantung pada tetapan dielektrik, makin besar
tetapan dielektrik semakin polar pelarut tersebut. Bahan-bahan jenis tertentu
memerlukan metode ekstraksi bertingkat. Ekstraksi bertingkat dilakukan secara
berturut-turut dimulai dengan pelarut nonpolar (heksan) lalu dengan pelarut yang
kepolarannya menengah (etilasetat atau dietileter), kemudian dengan pelarut polar
(metanol atau etanol). Dengan demikian akan diperoleh ekstrak awal (crude
extract) yang berturut-turut mengandung senyawa nonpolar, kepolaran menengah,
dan polar (Nur dan Adijuwana 1989).
Pelarut nonpolar merupakan salah satu pelarut yang dikenal efektif
terhadap alkaloid dalam bentuk basa dan terpenoid dari bahan. Pelarut nonpolar
juga dapat mengekstrak senyawa kimia seperti lilin, lemak, dan minyak yang
mudah menguap. Pelarut semi polar mampu mengekstrak senyawa fenol,
terpenoid, alkaloid, aglikon, dan glikosida. Pelarut yang bersifat polar, mampu
mengekstrak senyawa alkaloid kuartener, komponen fenolik, karotenoid, tanin,
gula, asam amino, dan glikosida (Harborne 1987). Metanol, sebagai senyawa
polar, dapat disebut sebagai pelarut universal karena selain mampu mengekstrak
komponen polar, dapat juga mengekstrak komponen nonpolar seperti lilin dan
lemak (Houghton dan Raman 1998).
Proses ekstraksi terdiri dari beberapa tahap yaitu penghancuran bahan,
penimbangan, perendaman dengan pelarut, penyaringan, dan pemisahan.
Penghancuran bertujuan untuk mempermudah pengadukan dan kontak bahan
dengan pelarutnya pada saat proses pelarutnya. Bahan ditimbang untuk
mengetahui berat awal bahan sehingga dapat ditentukan rendemen yang
dihasilkan. Bahan yang telah ditimbang kemudian direndam dalam pelarut yang
sesuai. Proses perendaman yang dilakukan disebut maserasi. Tahap selanjutnya
adalah tahap pemisahan yang terdiri dari penyaringan dan evaporasi. Penyaringan
dilakukan untuk memisahkan residu bahan dan pelarut yang telah mengandung
senyawa bioaktif. Pemisahkan pelarut dengan senyawa bioaktif yang terikat
dilakukan evaporasi sehingga pelarut akan menguap dan diperoleh senyawa hasil
antara lain kondisi alamiah senyawa tersebut, metode ekstraksi yang digunakan,
ukuran partikel sample, kondisi dan waktu penyimpanan, lama waktu ekstraksi,
dan perbandingan jumlah pelarut terhadap jumlah sampel (Darusman et al 1995).
2.3. Radikal Bebas
Radikal bebas merupakan struktur kimia yang mempunyai satu elektron
yang tidak berpasangan pada orbit luarnya. Energi yang dihasilkan oleh
konfigurasi yang tidak stabil dan sangat reaktif tersebut dilepaskan melalui reaksi
dengan molekul didekatnya sehingga terjadi perpindahan elektron dari molekul
donor ke molekul radikal untuk menjadikan radikal tersebut stabil. Radikal bebas
kemudian memulai reaksi autotokatalitik dimana molekul yang bereaksi dengan
radikal bebas dengan sendirinya berubah menjadi radikal bebas untuk menambah
rantai kerusakan. Radikal bebas sangat berbahaya bagi makhluk hidup karena
apabila reaksi ini terjadi di dalam tubuh, maka akan menimbulkan berbagai
kerusakan yang menjadi penyebab penyakit (BlueFame Forums 2008).
Senyawa radikal yang terdapat dalam tubuh (prooksidan) dapat berasal
dari luar tubuh (eksogen) atau terbentuk di dalam tubuh (endogen) dari hasil
metabolisme zat gizi secara normal (Muchtadi 2000). Secara eksogen, senyawa
radikal antara lain berasal dari polutan, makanan atau minuman, radiasi, ozon, dan
pestisida (Supari 1996). Penjelasan mengenai sumber radikal bebas endogen
sangat bervariasi. Sumber radikal endogen dapat melewati autoksidasi, oksidasi
enzimatik, fagositosis dalam respirasi, transpor elektron di mitokondria, oksidasi
ion-ion logam transisi, atau melalui ischemic. Autoksidasi adalah senyawa yang
mengandung ikatan rangkap, hidrogen alilik, benzilik atau tersier yang rentan
terhadap oksidasi oleh udara. Oksidasi enzimatik menghasilkan oksidan asam
hipoklorit, di mana sekitar 70-90 % konsumsi O2 oleh sel fagosit diubah menjadi
superoksida. Sumber eksogenus radikal bebas, berasal dari luar sistem tubuh,
diantaranya sinar UV. Sinar UV B merangsang melanosit memproduksi melanin
berlebihan dalam kulit, yang tidak hanya membuat kulit lebih gelap, melainkan
juga berbintik hitam. Pemaparan berlebihan dari sinar ultra violet ini bahkan
dapat menyebabkan kulit terbakar sampai kanker kulit. Sinar UVA dapat merusak
kulit dengan menembus lapisan basal yang menimbulkan kerutan sehingga kulit
Radikal bebas juga dapat menyebabkan oksidasi DNA sehingga DNA
termutasi dan menimbulkan kanker. Oksigen reaktif dapat meningkatkan kadar
LDL (Low Density Lipoprotein) yang kemudian menjadi penyebab penimbunan
kolesterol pada dinding pembuluh darah. Akibatnya timbullah aterosklerosis atau
lebih dikenal dengan penyakit jantung koroner. Penurunan suplai darah atau
ischemic karena penyumbatan pembuluh darah menurut patologi juga dikarenakan
radikal bebas. Senyawa radikal juga memicu terjadinya penuaan dini akibat
rusaknya sel-sel jaringan tubuh serta dapat menimbulkan penyakit autoimun.
Lipid yang seharusnya menjaga kulit agar tetap segar berubah menjadi lipid
peroksida karena bereaksi dengan radikal bebas sehingga mempercepat penuaan
(Muchtadi 2000).
2.4. Antioksidan
Antioksidan adalah zat yang dapat melawan pengaruh bahaya dari radikal
bebas atau Reactive Oxygen Species (ROS) yang terbentuk sebagai hasil dari
metabolisme oksidatif yaitu hasil dari reaksi-reaksi kimia dan proses metabolik
yang terjadi di dalam tubuh (Sauriasari 2006). Senyawa antioksidan dapat
berfungsi sebagai penangkap radikal bebas, pembentuk kompleks dengan
logam-logam prooksidan dan berfungsi sebagai senyawa pereduksi. Antioksidan dapat
menangkap radikal bebas sehingga menghambat mekanisme oksidatif yang
merupakan penyebab penyakit-penyakit degeneratif seperti penyakit jantung,
kanker, katarak, disfungsi otak, dan artritis (Sofia 2008).
Berbagai sumber nutrisi yang mengandung antioksidan diantaranya adalah
semua biji-bijian, buah-buahan dan sayuran, hati, tiram, unggas, kerang, ikan,
susu dan daging. Vitamin E alami dapat ditemukan pada wheat germ (gandum),
minyak sayur, sayuran berdaun hijau, kuning telur dan kacang-kacangan. Vitamin
C alami dapat ditemukan pada buah sitrus, tomat, melon, kubis, jambu biji,
strawberry, dan sebagainya. Beta karoten (pro-vitamin A) yang merupakan
antioksidan penting dari karotenoid banyak dijumpai pada buah apricot, wortel,
blewah, bit, daun singkong, daun bayam dan ubi merah. Sumber antioksidan
terbaik, tentunya berasal dari makanan alami. Namun tidak ada salahnya untuk
perawatan kesehatan, karena makanan yang dimakan belum tentu mengandung
komponen yang dibutuhkan secara lengkap (Sofia 2008).
Antioksidan dapat digolongkan menjadi antioksidan primer (
chain-breaking antioxidant) dan antioksidan sekunder (preventive antioxidant).
Antioksidan primer dapat bereaksi dengan radikal lipid dan mengubahnya menjadi
bentuk yang lebih stabil. Sebuah senyawa dapat disebut sebagai antioksidan
primer bila senyawa tersebut dapat mendonorkan atom hidrogennya dengan cepat
ke radikal lipid dan radikal antioksidan yang dihasilkan lebih stabil dari radikal
lipid atau dapat diubah menjadi produk lain yang lebih stabil. Senyawa yang
termasuk dalam kelompok antioksidan primer adalah vitamin E (tokoferol),
vitamin C (asam askorbat), β-karoten, glutation, dan sistein (Sauriasari 2006).
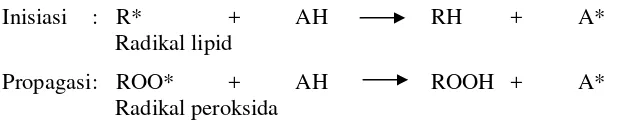
Contoh yang disajikan pada Gambar 2 di bawah ini merupakan mekanisme
pengikatan radikal bebas oleh antioksidan pada oksidasi lemak.
Inisiasi : R* + AH RH + A*
Radikal lipid
Propagasi : ROO* + AH ROOH + A*
Radikal peroksida
Gambar 2. Reaksi penghambatan antioksidan primer terhadap radikal lipid Sumber: Gordon (1990)
Penambahan antioksidan (AH) primer dalam konsentrasi rendah pada lipid
dapat menghambat atau mencegah reaksi autooksidasi. Proses autooksidasi lipid
pada tahap inisiasi akan menghasilkan radikal lipid (R*) bila lipid kontak dengan
panas, cahaya, ion metal, dan oksigen. Radikal antioksidan yang terbentuk (A*)
relatif stabil dan tidak mempunyai cukup energi untuk dapat bereaksi dengan
molekul lipid lain membentuk radikal lipid baru. Tahap propagasi terjadi ketika
radikal lipid dari tahap inisiasi kontak dengan oksigen membentuk radikal
peroksida (ROO*). Tahap terakhir yaitu terminasi, dimana hidroperoksida
(ROOH) yang sangat tidak stabil terpecah menjadi senyawa organik berantai
pendek seperti keton, aldehid, alkohol, dan asam (Gordon 1990).
Antioksidan sekunder berfungsi sebagai antioksidan pencegah, yaitu
menurunkan kecepatan inisiasi dengan berbagai mekanisme, seperti melalui
menjadi produk-produk nonradikal. Contoh antioksidan sekunder antara lain
turunan-turunan asam fosfat, senyawa karoten, sterol, fosfolipid, dan
produk-produk reaksi maillard. Tujuan dasar dari antioksidan sekunder adalah mencegah
terjadinya radikal yang paling berbahaya yaitu radikal hidroksil (BlueFame
Forums 2008).
Beberapa metode pengukuran aktivitas antioksidan yang dapat digunakan
antara lain metode DPPH dan metode uji aktivitas kemampuan mereduksi.
Pengujian dengan DPPH merupakan salah satu metode yang sederhana dengan
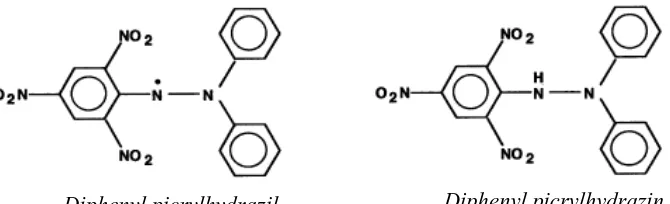
menggunakan 1,1-diphenyl-2-picrylhydrazil (DPPH) sebagai senyawa pendeteksi.
DPPH merupakan senyawa radikal bebas yang bersifat stabil sehingga dapat
bereaksi dengan atom hidrogen yang berasal dari suatu antioksidan. Hasil reaksi
tersebut berupa DPPH tereduksi (1,1-diphenyl-2-picrylhydrazin) yang tidak
reaktif lagi karena telah mendapat donor hidrogen (Molyneux 2004). Struktur
DPPH dan DPPH tereduksi hasil reaksi dengan antioksidan dapat dilihat pada
Gambar 3.
Diphenylpicrylhydrazil Diphenylpicrylhydrazin
Gambar 3. Struktur awal DPPH dan DPPH tereduksi
Pengukuran kapasitas antioksidan dengan metode DPPH menggunakan
spektrofotometer dengan panjang gelombang 517 nm. Larutan DPPH berwarna
ungu gelap, ketika ditambahkan senyawa antioksidan maka warna larutan akan
berubah menjadi kuning cerah. Penurunan absorbansi, yang ditunjukkan dengan
berkurangnya warna ungu, menunjukkan adanya aktivitas scavenging (aktivitas
antioksidan). Metode aktivitas kemampuan mereduksi digunakan untuk
menentukan antioksidan total pada sampel. Aktivitas antioksidan diukur sebagai
kemampuan mereduksi kalium ferri sianida. Absorbansi yang tinggi
bawah ini menampilkan pembagian warna dalam spektrum cahaya tampak
berdasarkan panjang gelombangnya.
Tabel 3. Pembagian panjang gelombang sinar tampak
Panjang gelombang
(nm) Warna Warna komplementer
400 – 435
Keterangan : warna komplementer merupakan warna larutan yang terlihat (warna yang diteruskan atau dipantulkan)
Sumber : Sudarmadji et al (2007)
Beberapa senyawa yang telah diketahui efektivitasnya sebagai antioksidan
antara lain alkaloid, flavonoid, saponin, dan steroid. Struktur dari kelompok
senyawa tersebut dapat dilihat pada Gambar 4.
Alkaloid Flavonoid
Steroid Saponin
3. METODOLOGI
3.1. Waktu dan Tempat
Penelitian tentang penapisan awal komponen bioaktif dari kijing Taiwan
(Anodonta woodiana Lea) sebagai senyawa antioksidan ini dilaksanakan pada
bulan Agustus sampai November 2008 di Laboratorium Pananganan Bahan Baku
Hasil Perairan, Laboratorium Biokimia Hasil Perairan, Departemen Teknologi
Hasil Perairan, Laboratorium Pusat Antar Universitas Pangan dan Gizi, Institut
Pertanian Bogor, serta Laboratorium Basah Pusat Studi Biofarmaka, Institut
Pertanian Bogor.
3.2. Alat dan Bahan
Alat-alat yang digunakan antara lain cool box, pisau, talenan, timbangan,
kertas label, aluminium foil, corong kaca, labu erlenmeyer, gelas piala, tabung
reaksi, buret, rak tabung reaksi, plastik tahan panas, pinggan porselin, oven,
penjepit, desikator, kompor listrik, pipet tetes, sudip, bulp, kain blacu, saringan
whatman, freezer, vakum evaporator, magnetic stirrer, hot plate,
spektrofotometer, botol steril, botol uji fitokimia dan lempeng tetes.
Bahan utama yang digunakan pada penelitian ini adalah kijing Taiwan
(Anodonta woodiana Lea). Bahan tambahan lain yang digunakan antara lain es
curai, pelarut (n-heksan, etil asetat dan metanol), radikal bebas DPPH
(1,1-diphenyl-2-picrylhydrazil), H2SO4 2 M, HCl 1,57%, KI, pereaksi Mayer,
pereaksi Dragendorff, pereaksi Wagner, eter, anhidrida asetat, H2SO4 pekat,
serbuk magnesium, NaOH 1 N, FeCl3 1%, aquades, minyak kelapa, asam asetat
glasial, kloroform, dan natrium tiosulfat (Na2S2O3).
3.3. Tahapan Penelitian
Rangkaian kegiatan penelitian ini dibagi menjadi dua tahap. Tahap
pertama merupakan penelitian pendahuluan yang meliputi ekstraksi senyawa
bioaktif dan penentuan ekstrak terbaik berdasarkan jenis pelarut dengan uji
antioksidan dengan metode DPPH (1,1-diphenyl-2-picrylhydrazil). Tahap kedua
merupakan penelitian utama berupa penentuan ekstrak terbaik berdasarkan waktu
dan sistem emulsinya, evaluasi aktivitas antioksidan kijing Taiwan dalam
mencegah proses ketengikan pada emulsi minyak kelapa dengan mengukur
bilangan peroksida serta analisis fitokimia sampel terpilih.
3.3.1. Penelitian Pendahuluan
Penelitian pendahuluan meliputi ekstraksi senyawa bioaktif dan penentuan
ekstrak terbaik berdasarkan jenis pelarut dengan uji antioksidan dengan DPPH.
Tujuan yang ingin dicapai adalah menentukan jenis pelarut terbaik yang
menghasilkan ekstrak dengan sifat antioksidan yang paling tinggi.
3.3.1.1. Ekstraksi Senyawa Bioaktif (Darusman et al 1995.)
Proses ekstraksi kijing Taiwan (Anodonta woodiana Lea) meliputi
penghancuran sampel, maserasi, penyaringan dan evaporasi. Kerang dipisahkan
dengan cangkangnya, dicuci dan dicacah dengan pisau. Sampel kemudian
ditimbang, dimasukkan dalam erlenmeyer dan dimaserasi dengan pelarut dengan
perbandingan sampel : pelarut 1:2 (b/v). Pelarut yang digunakan secara
berturut-turut yaitu n-heksan, etil asetat dan metanol.
Waktu perendaman yang digunakan dalam penelitian pendahuluan ini
adalah masing-masing selama 24 jam untuk tiap pelarut. Tahap pertama, sampel
dimaserasi dengan n-heksan selama 24 jam pada suhu ruang. Sampel lalu disaring
dengan kain blacu sebagai saringan kasar, dilanjutkan dengan kertas saring
whatman untuk pemisahkan filtrat dengan ampasnya. Filtrat yang diperoleh
disebut filtrat n-heksan. Ampas selanjutnya dimaserasi dengan pelarut etil asetat
selama 24 jam kemudian disaring sehingga diperoleh filtrat etil asetat. Ampas
yang diperoleh dimaserasi kembali dengan pelarut metanol selama 24 jam lalu
disaring sehingga diperoleh ekstrak metanol.
Filtrat n-heksan, etil asetat dan metanol yang diperoleh selanjutnya
dievaporasi dengan vacum evaporator pada suhu antara 30oC – 40oC sehingga
diperoleh ekstrak kasar n-heksan, etil asetat dan metanol. Penggunaan suhu
tersebut dimaksudkan untuk menjaga kestabilan aktivitas antioksidan pada
ekstrak, karena dikhawatirkan akan rusak pada suhu tinggi. Tahapan proses
Gambar 5. Tahapan proses ekstraksi
(Quinn 1988 diacu dalam Darusman et al 1995) Keterangan: Produk
Proses Pemisahan daging dari cangkang
Penimbangan Pencacahan Pencucian
Maserasi dengan n-heksan
Penyaringan
Evaporasi
Evaporasi
Penyaringan
Evaporasi Maserasi dengan etil asetat
Maserasi dengan metanol Penyaringan
Kijing Taiwan (Anodonta woodiana Lea.)
Filtrat n-heksan
Ekstrak kasar n-heksan
Ampas
Filtrat etil asetat
Ekstrak kasar etil asetat
Ampas
Filtrat metanol Ampas
3.3.1.2. Uji Antioksidan (DPPH) (Molyneux 2004).
Ekstrak kijing Taiwan yang berasal dari proses maserasi dengan n-heksan,
etil asetat, dan metanol dilarutkan dengan metanol pro analisis dengan
konsentrasi 50, 100, 250, 500, dan 1000 ppm. Larutan pereaksi DPPH yang
digunakan dibuat dengan melarutkan DPPH dalam metanol pro analisis dengan
konsentrasi 400 ppm, yang dibuat segar dan dijaga pada suhu rendah serta
terlindung dari cahaya. Sebanyak 4 ml larutan uji atau pembanding direaksikan
dengan 1 ml larutan DPPH, lalu diukur absorbansinya pada panjang gelombang
516 nm. Larutan standar dibuat dengan mencampur 4 ml metanol pro analisis
dengan 1 ml DPPH. Persen peredaman dihitung dengan persamaan regresi
terhadap konsentrasi larutan uji, mengikuti persamaan Y = aLn(x) + b, dengan Y
menyatakan nilai IC (inhibitor concentration) yang dicari, yaitu sebesar 50 dan X
menyatakan nilai dari IC50. Nilai IC50 menyatakan konsentrasi larutan sampel
yang dibutuhkan untuk mereduksi DPPH sebesar 50% (Molyneux 2004).
3.3.2. Penelitian Utama
Penelitian utama bertujuan untuk menetukan waktu maserasi terbaik yang
dapat menghasilkan ekstrak dengan sifat antioksidan paling tinggi. Selain itu,
juga untuk menentukan konsentrasi ekstrak terpilih yang paling optimal untuk
penghambatan pembentukan peroksida pada emulsi minyak, serta untuk
mengetahui komponen bioaktif dengan uji fitokimia.
3.3.2.1. Uji Antioksidan (DPPH) (Molyneux 2004).
Uji antioksidan dengan DPPH pada penelitian pendahuluan akan
menghasilkan satu ekstrak terbaik berdasarkan jenis pelarut. Ekstrak terbaik
tersebut selanjutnya dimodifikasi tu diberi perlakuan pada waktu maserasinya,
yaitu selama 24 jam, 48 jam, dan 72 jam. Ekstrak yang didapatkan dari berbagai
waktu maserasi tersebut diuji DPPH kembali untuk menentukan waktu maserasi
yang terbaik. Metode pengujian dengan DPPH sama dengan pengujian pada
tahap penelitian pendahuluan berdasarkan (Molyneux 2004). Ekstrak yang
mempunyai sifat antioksidan terbaik selanjutnya digunakan pada tahap aplikasi
3.3.2.2. Evaluasi aktivitas antioksidan (penentuan bilangan peroksida)
Penentuan aktivitas antioksidan dari ekstrak kijing Taiwan diterapkan pada
emulsi minyak. Antioksidan berfungsi untuk menghambat pembentukan
peroksida pada minyak. Pengujian ini dilakukan melalui pembuatan minyak
kelapa dan sistem emulsinya yang dilanjutkan dengan evaluasi aktivitas
antioksidan dengan penentuan bilangan peroksida.
a) Pembuatan minyak kelapa dan sistem emulsinya (Santoso et al 2004)
Minyak yang digunakan dalam penelitian dibuat dari parutan kelapa yang
diperas untuk diambil santan kentalnya. Santan kental tersebut dipanaskan
dengan cara direbus untuk memisahkan komponen minyak yang terkandung di
dalamnya, kemudian dilakukan penyaringan untuk memisahkan minyak dan
ampas parutan kelapa. Filtrat yang dihasilkan kemudian disaring lagi dengan
kertas whatman agar diperoleh minyak kelapa yang bening. Sistem emulsi
minyak dibuat dengan mengacu pada metode Santoso et al (2004) yang
dimodifikasi, yaitu dengan menghomogenkan 3% minyak kelapa dan 97% air
yang mengandung 0,3% Tween 20.
b) Penentuan bilangan peroksida
Peroksida merupakan hasil reaksi antara lemak tidak jenuh dengan
oksigen. Bilangan peroksida ditentukan berdasarkan jumlah iodin yang
dibebaskan setelah lemak atau minyak ditambahkan alkali iodida. Peroksida yang
terbentuk dalam minyak atau lemak berikatan dengan alkali sehingga iod
terbebaskan. Iod ini ditangkap dengan natrium thuosulfat yang selanjutnya
ditentukan jumlahnya dengan titrasi (Winarno 1996). Bilangan peroksida adalah
nilai terpenting untuk menentukan derajat kerusakan pada minyak atau lemak
(Ketaren 1986).
Sistem emulsi lemak ditambahkan ekstrak kijing Taiwan terbaik dari tahap
sebelumnya sebanyak 0 ppm (tanpa penambahan ekstrak), 2000 ppm, 3000 ppm,
dan 4000 ppm yang selanjutnya disebut sampel minyak. Sampel minyak
selanjutnya disimpan selama tujuh hari dalam inkubator bersuhu 36,9oC untuk
mempercepat oksidasi. Sampel minyak kemudian ditimbang sebanyak 5 gram di
dalam labu erlenmeyer, kemudian ditambahkan 30 ml pelarut yang terdiri dari
ditambahkan 0,5 ml larutan KI jenuh dan didiamkan 15 menit dalam ruang gelap
sambil dikocok. Iod yang terbentuk dititrasi dengan larutan Na2S2O3 0,01 N
dengan indikator pati 1%. Titrasi dihentikan saat larutan sampel menjadi tidak
berwarna. Hasil pengurangan volume akhir terhadap volume awal larutan
Na2S2O3 0,01 N yang ditunjukan oleh skala pada burret, merupakan volume total
larutan Na2S2O3 0,01 N yang digunakan untuk titrasi sampel. Cara yang sama
dibuat juga untuk penerapan blanko. Nilai bilangan peroksida dinyatakan dengan
miliequivalen per 1 kg minyak atau lemak (Ketaren 1986), yaitu dengan rumus :
miliequivalen / kg bahan = (a - b) x N x 1000 G
Keterangan :
a = jumlah ml larutan Na2S2O3 untuk titrasi sampel b = jumlah ml larutan Na2S2O3 untuk titrasi blanko N = normalitas larutan Na2S2O3
G = berat sampel (g)
3.3.3. Fitokimia (Harborne 1987)
Penentuan kelompok bioaktif yang terdapat dalam ekstrak kijing Taiwan
terpilih dilakukan terhadap tiga jenis senyawa, yaitu alkaloid, triterpenoid/steroid,
dan flavonoid. Menurut Darusman et al (1995), komponen bioaktif yang secara
umum dan dominan terdapat pada jenis kerang-kerangan adalah alkaloid,
triterpenoid/steroid, dan flavonoid.
3.3.3.1. Uji alkaloid (Harborne 1987)
Satu gram sampel dilarutkan dalam 1,52% HCl dan larutan dibagi
dalam tiga tabung reaksi. Tabung 1 ditambah 0,5 larutan asam encer
sebagai pembanding, tabung 2 ditambah pereaksi Dragendorff, dan tabung
3 ditambah pereaksi Mayer. Terbentuknya endapan jingga pada tabung 2
dan endapan kekuningan pada tabung 3 menunjukkan adanya alkaloid.
3.3.3.2. Uji triterpenoid/steroid (Harborne 1987)
Ekstrak dilarutkan dalam 0,5 ml kloroform dan ditambahkan 0,5 ml
asam asetat anhidrat. Larutan selanjutnya ditetesi dengan 12 ml H2SO4
perbatasan dua pelarut menunjukkan adanya triterpen, sedangkan warna
hijau kebiruan menunjukkan adanya sterol.
3.3.3.3. Uji flavonoid (Harborne 1987)
Sebanyak sampel ditambah serbuk magnesium 0,1 mg dan 0,4 ml
amil alkohol (campuran asam klorida 37% dan etanol 95% dengan volume
sama) dan 4 ml alkohol kemudian campuaran dikocok. Terbentuknya
warna merah, kuning atau jingga pada lapisan amil alkohol menunjukkan
adanya flavonoid.
3.3.4. Rancangan Percobaan dan Analisis Data (Steel dan Torrie 1980)
Analisis data dilakukan terhadap hasil pada tahap penelitian pendahuluan
dan penelitian utama. Tahapan penelitian pendahuluan bertujuan untuk
menentukan ekstrak terbaik dari kijing Taiwan berdasarkan jenis pelarut. Faktor
yang digunakan adalah jenis pelarut dengan tiga taraf yaitu n-heksan (pelarut
polar), etil asetat (pelarut semi polar), dan metanol (pelarut nonpolar). Analisis
data dilakukan terhadap hasil dari nilai IC50 yang menunjukkan kemampuan
komponen antioksidan dalam menangkap radikal bebas (dalam pengujian ini
radikal bebas yang digunakan adalah 1,1-diphenyl-2-picrylhydrazil (DPPH)).
Nilai IC50 menyatakan konsentrasi ekstrak yang dibutuhkan untuk mereduksi
DPPH sebesar 50% (Molyneux 2004).
Penelitian utama dilakukan untuk menentukan ekstrak terbaik dari kijing
Taiwan berdasarkan waktu maserasi. Faktor yang digunakan dalam penelitian ini
adalah waktu maserasi dengan tiga taraf yaitu 24 jam, 48 jam, dan 72 jam.
Analisis data juga dilakukan terhadap hasil dari nilai IC50 yang menunjukkan
kemampuan komponen antioksidan dalam menangkap radikal bebas. Tahapan
aplikasi terhadap emulsi minyak bertujuan untuk menentukan seberapa besar
konsentrasi ekstrak terpilih yang mampu menghambat pembentukan peroksida
dalam sistem emulsi minyak. Faktor yang digunakan adalah konsentrasi ekstrak
dengan empat taraf yaitu 0 ppm, 2000 ppm, 3000 ppm, dan 4000 ppm.
Semua perlakuan pada penelitian ini dilakukan sebanyak tiga kali ulangan.
Rancangan yang digunakan untuk semua analisis data adalah Rancangan Acak
Lengkap (RAL) dengan model:
Keterangan :
Yij = Respon pengaruh konsentrasi pada taraf i ulangan ke-j = Pengaruh rata-rata umum
αi = Pengaruh konsentrasi pada taraf i
εij = Pengaruh acak (galat percobaan) pada konsentrasi taraf i ulangan ke-j i = n-heksan, etil asetat, metanol (penelitian pendahuluan)
= 24 jam, 48 jam, 72 jam (penentuan waktu maserasi)
= 0 ppm, 2000 ppm, 3000 ppm, dan 4000 ppm (penentuan konsentrasi ekstrak terpilih)
Hipotesis
• Penelitian pendahuluan (penentuan jenis pelarut )
Ho = Jenis pelarut tidak mempengaruhi aktivitas antioksidan ekstrak kijing Taiwan
H1 = Jenis pelarut memengparuhi aktivitas antioksidan ekstrak kijing Taiwan
• Penelitian utama Penentuan waktu maserasi:
Ho = Waktu maserasi tidak mempengaruhi aktivitas antioksidan ekstrak kijing Taiwan
H1 = Waktu maserasi mempengaruhi aktivitas antioksidan ekstrak kijing Taiwan
Penentuan konsentrasi ekstrak terpilih:
Ho = Konsentrasi ekstrak tidak mempengaruhi aktivitas antioksidan ekstrak kijing Taiwan
H1 = Konsentrasi ekstrak mempengaruhi aktivitas antioksidan ekstrak kijing Taiwan
Jika hasil dari pengujian menunjukkan adanya pengaruh yang berbeda
nyata pada selang 95% (α=0,05) maka dilakukan uji lanjut Duncan. Rumus uji
Rр = nilai kritikal untuk perlakuan yang dibandingkan p = perlakuan
dbs = derajat bebas
kts = jumlah kuadrat tengah
4. HASIL DAN PEMBAHASAN
4.1. Penelitian Pendahuluan
Penelitian pendahuluan ini meliputi ekstraksi senyawa bioaktif dan
penentuan ekstrak terbaik berdasarkan jenis pelarut dengan uji DPPH yang
selanjutnya akan digunakan pada penelitian utama. Hasil ekstraksi dari kijing
Taiwan (Anodonta woodiana Lea.) dinyatakan dalam persentase rendemen.
4.1.1. Ekstraksi Senyawa Bioaktif
Proses ekstraksi kijing Taiwan (Anodonta woodiana Lea.) meliputi
penghancuran sampel, maserasi, penyaringan dan evaporasi. Sampel kijing
Taiwan dibuka cangkangnya dengan bantuan pisau, kemudian diambil daging dan
seluruh organnya. Tahapan maserasi merupakan perendaman daging kijing
Taiwan dalam pelarut tanpa pengadukan. Metode ekstraksi yang digunakan
adalah ekstraksi bertingkat yang dilakukan secara berturut-turut dimulai dengan
pelarut nonpolar (n-heksan), pelarut yang kepolarannya menengah (etil asetat),
dan pelarut polar (metanol). Hasil ekstraksi kijing Taiwan yang dinyatakan dalam
persen rendemen dapat dilihat pada Tabel 3.
Kijing Taiwan yang digunakan pada penelitian ini diperoleh dari Situ
Gede, Bogor. Sampel diambil pada awal bulan September 2008. Ukuran kijing
Taiwan yang diperoleh bervariasi, antara 7 cm – 12 cm. Kondisi sampel pada saat
akan dipreparasi adalah masih hidup, sehingga ekstraksi yang dilakukan adalah
terhadap sampel segar. Kijing Taiwan yang diperoleh disajikan dalam Gambar 6.