PENAPISAN SENYAWA BIOAKTIF SPONS Aaptos
aaptos DAN Petrosia sp. DARI LOKASI YANG
BERBEDA
MEUTIA SAMIRA ISMET
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Penapisan Senyawa Bioaktif Spons Aaptos aaptos dan Petrosia sp. dari Lokasi yang Berbeda adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, April 2007
ABSTRAK
MEUTIA SAMIRA ISMET. Penapisan Senyawa Bioaktif Spons Aaptos aaptos dan Petrosia sp. dari Lokasi yang Berbeda. Dibimbing oleh Dedi Soedharma dan Hefni Effendi.
Spons Aaptos aaptos dan Petrosia sp. diketahui memiliki potensi bioaktivitas yang tinggi. Perbedaan habitat spons dapat berpengaruh terhadap potensi tersebut. Penelitian ini bertujuan untuk melakukan penapisan senyawa bioaktif kedua jenis spons tersebut, menganalisa kandungan senyawa ekstrak kasar spons dan bioaktivitas antibakteri masing-masing senyawa, melihat pengaruh lingkungan terhadap aktivitas senyawa, serta melihat kaitan biomassa sel spons dan isolat bakteri terhadap bioaktivitas senyawa ekstrak kasar kedua jenis spons tersebut.
Sampel spons diambil dari dua lokasi (Barat dan Selatan P. Pari) dengan kondisi substrat yang berbeda, yaitu pasir berlumpur dan karang. Bioaktivitas sampel spons dianalisa dengan metode difusi agar terhadap Escheria coli, Staphylococcus aureus, dan Aeromonas hydrophilla (Ah), serta uji toksisitas terhadap Artemia salina (As). Kandungan senyawa ekstrak kasar kedua spons difraksinasi dan dianalisa menggunakan Kromatografi Lapis Tipis (TLC). Aktivitas antibakteri kandungan senyawa hasil TLC dianalisa dengan metode bioautografi terhadap (Ah). Penentuan biomassa dan struktur sel spons dilakukan dengan pengamatan histologi dan pemisahan fraksi sel menggunakan sentrifugasi. Analisa data dilakukan secara deskriptif (kualitatif) untuk menapis senyawa bioaktif kedua jenis spons, melihat pengaruh lingkungan dan kaitan biomassa serta isolat bakteri simbion terhadap bioaktivitas senyawa ekstrak kasar kedua jenis spons. Analisa korelatif dilakukan untuk melihat hubungan antara bioaktivitas antibakteri dan toksisitas terhadap (As)senyawa ekstrak kasar spons Aaptos aaptos dan Petrosia sp.
Tingkat bioaktivitas kedua jenis spons yang berasal dari alam memiliki kisaran yang beragam untuk tiap habitat pada masing-masing lokasi pengambilan sampel. Sampel hasil transplantasi spons Aaptos aaptos memiliki tingkat bioaktivitas yang cenderung sama, semetara spons Petrosia sp. hasil transplantasi menunjukkan tingkat bioaktivitas yang tidak seragam. Tidak terdapat korelasi antara tingkat bioaktivitas antibakteri senyawa ekstrak kasar spons dengan toksisitasnya terhadap (As).
Hasil Kromatografi Lapis Tipis (TLC), di bawah sinar uv pada 254 dan 365 nm, terhadap kedua jenis spons menunjukkan bahwa fraksi organik Aaptos aaptos mengandung 6 senyawa yang terpisah. Sementara hasil TLC pada spons
Petrosia sp. menunjukkan bahwa fraksi organiknya mengandung 3 senyawa
terpisah, dan 4 senyawa dari fraksi semi organik.
ABSTRACT
MEUTIA SAMIRA ISMET. Screening of Bioactive Compounds of Aaptos aaptos
dan Petrosia sp. Sponges from Different Location. Supervised by Dedi
Soedharma dan Hefni Effendi.
Aaptos aaptos and Petrosia sp. sponges are known for their high potential of bioactive compounds. Differences in sponge habitat may influence the sponge bioactivity. The objectives of this research were to screen the bioactive compound of those two sponges species, to analyze sponge raw extract compounds and the antibacterial activity of bioactive compounds, to determine the environmental effect on sponges bioactivity, and to observe the correlation of sponge’s cell biomass and bacteria-associated isolates on sponges raw extracts bioactivity.
Sponge samples were taken from two locations (West- and South- side of Pari Island) with different substrate condition (muddy-sand and rubble). Sponges bioactivity was analyzed using agar diffusion method against Escherichia coli; Staphylococcus aureus; and Aeromonas hydrophylla; meanwhile the toxicity was examined against the Artemia salina. The compound of both sponges raw extract was fractionated and analyzed using Thin Layer Chromatography (TLC). Antibacterial activity of TLC results of raw compounds was analyzed using bioautography method against Aeromonas hydrophilla. Sponges cell biomass and cell structure determinations used histological observation and centrifugal cell fractionation. Data analyses were done qualitatively (descriptive) on both sponges bioactive compound screening, to determine the environmental effects and correlation of sponges biomass and bacteria-associated isolates on sponges raw extract bioactivity. Whilst the Correlation Analysis was done to examine the correlation between antibacteria and toxicity bioactivity of both sponges raw extract.
The Aaptos aaptos and Petrosia sp. from natural habitat denoted a varied range of bioactivity for each habitat in different location (West- and South- side of Pari Island). Transplanted samples of Aaptos aaptos showed relative similar bioactivity, which was contrary with the transplanted Petrosia sp. There was no correlation between antibacterial bioactivity and toxicity of the sponge raw extract.
TLC results, under uv light (254 and 365 nm), pointed out that the organic fraction of Aaptos aaptos produced 6 different compounds; whilst there were only 3 different compounds from the Petrosia sp. organic fraction and 4 compounds from its semi-organic fraction.
Aaptos aaptos has soft body, with skeleton-forming fraction up to 55.9%, sponge cell 14.2%, and bacterial fraction 29.9%. It also contains 8 identified symbiotic-bacterial isolates: Bacillus sp. (3 isolates), Staphylococcus sp., Acinetobacter haemolyticus (2 isolates), Xenorhabdus nemathophillus, dan Vibrio algynolyticus. Meanwhile, Petrosia sp. sponge has rigid body with dominant skeleton-forming fraction (68.6%), hence, it has a lesser amount of sponge cell and bacterial fraction (19.7 % and 11.7%). There were no symbiotic-bacteria isolated from Petrosia sp. Nevertheless, two unidentified fungi-associated sponge were isolated from this sponge. It was concluded that sponges morphology and symbiotic-bacteria could influence sponges bioactive compounds and its activity, as well as the sponges’ habitat.
PENAPISAN SENYAWA BIOAKTIF SPONS Aaptos
aaptos DAN Petrosia sp. DARI LOKASI YANG
BERBEDA
MEUTIA SAMIRA ISMET
Tesis
Sebagai salah satu syarat memperoleh gelar
Magister Sains pada
Departemen Ilmu Kelautan
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
Judul Penelitian : Penapisan Senyawa Bioaktif Spons Aaptos aaptos dan Petrosia sp. dari Lokasi yang Berbeda
Nama Mahasiswa : Meutia Samira Ismet
NRP : C651040131
Program Studi : Ilmu Kelautan (IKL)
Menyetujui,
Komisi Pembimbing,
Prof. Ir. Dr. Dedi Soedharma, DEA. Dr. Ir. Hefni Effendi, MPhil.
Ketua Anggota
Mengetahui,
Ketua Program Studi Ilmu Kelautan Dekan Sekolah Pasca Sarjana IPB
Dr. Ir. Djisman Manurung, MSc. Dr. Ir Khairil Anwar Notodiputro, MS.
PRAKATA
Puji syukur Penulis panjatkan kepada Allah SWT atas segala karunia-Nya
sehingga penelitian dan penulisan tesis ini dapat diselesaikan dengan baik.
Penulis mengucapkan terima kasih kepada berbagai pihak yang telah
membantu proses penyelesaian karya ilmiah ini, antara lain:
1. Komisi pembimbing, Prof. Dr. Ir. Dedi Soedharma, DEA dan Dr. Ir. Hefni
Effendi, Mphil., yang telah memberi banyak masukan pada kegiatan
penelitian dan penulisan tesis ini.
2. Dr. Ir.Yulin Lestari, sebagai penguji luar komisi.
3. Proyek Hibah Pasca VII, yang diketuai Prof. Dr. Dedi Soedharma, DEA,
yang telah menyediakan sebagian dana untuk penelitian yang penulis
lakukan dan penyedia fasilitas penelitian, yaitu Lab. Mikrobiologi dan Lab.
Lingkungan PPLH-IPB, Lab. Mikrobiologi-Departemen Biologi IPB, Lab.
Kimia Analitik – Departemen Kimia IPB, Lab. Mikrobiologi dan Biokimia
serta Lab. Mikrobiologi dan Bioteknologi Pusat Studi Ilmu Hayat dan
Bioteknologi (PSIHB)-IPB
4. Laboran dan staf laboratorium (Mbak Heni, Pak Iwa, Bu Ika, staf
Lab.Lingkungan-PPLH dan Kimia Analitik- Dept. Kimia IPB) serta kepada
tim mahasiswa peneliti Hibah Pasca VII yang telah banyak membantu
dalam penelitian ini.
5. Abu, mama, adi dan mami Lisdar sekeluarga, bunda Mar, om Adek dan
keluarga besar atas doa, kasih sayang dan dukungannya.
6. Rekan-rekan sepenelitian (terutama Ubun dan Mbak Niet) dan
teman-teman IKL angkatan 2004 atas dukungannya, terutama kepada Iwan dan
Denti yang telah membantu dalam penelitian ini, juga kepada
teman-teman yang tidak dapat disebutkan satu persatu, atas keceriaan dan
semangatnya.
Penulis menyadari bahwa masih banyak kekurangan dalam karya ilmiah
ini. Namun penulis berharap semoga karya ilmiah ini dapat bermanfaat bagi kita
semua.
Bogor, April 2007
RIWAYAT HIDUP
Penulis dilahirkan di Kairo pada tanggal 25 Maret 1980, merupakan anak
pertama dari dua bersaudara, putri dari pasangan Ismet Yunus dan Asmawita
A.Manaf.
Penulis menyelesaikan pendidikan Sarjana Sains dari Departemen
Biologi-Institut Pertanian Bogor, pada tahun 2003. Kemudian masuk sebagai mahasiswa
Magister Sains di Sekolah Pasca – Sarjana IPB, program studi Ilmu Kelautan
pada tahun 2004. Selain itu, penulis juga bekerja sebagai Asisten Dosen dan
terdaftar sebagai staf Honorer laboratorium Biologi Laut, Departemen Ilmu dan
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN... xi
PENDAHULUAN Latar Belakang ... 1
Perumusan Masalah ... 2
Tujuan Penelitian ... 3
TINJAUAN PUSTAKA Morfologi Spons ... 4
Metabolit Sekunder ... 9
Produk Alami dan Mikroba Simbion Spons ... 10
BAHAN DAN METODE Waktu dan Tempat Penelitian ... 16
Bahan dan Alat ... 16
Metode Kerja ... 17
Diagram Alir Penelitian ... 22
HASIL PENELITIAN Bioaktivitas Senyawa Ekstrak Kasar dan Pengaruh Lingkungan ... 23
Analisa Kandungan dan Aktivitas Antimikrob Fraksi Senyawa Ekstrak Kasar Spons ... 29
Bakteri Simbion dan Biomassa Sel Spons ... 33
PEMBAHASAN Bioaktivitas Senyawa Ektrak Kasar Dan Pengaruh Lingkungan ... 38
Kandungan dan Aktivitas Antimikrob Fraksi Senyawa Ekstrak Kasar Spons ... 42
Bakteri Simbion dan Biomassa Sel Spons ... 46
KESIMPULAN ... 53
SARAN ... 55
DAFTAR PUSTAKA ... 56
DAFTAR TABEL
Halaman
1 Senyawa bioaktif yang dihasilkan spons laut ... 12
2 Bioaktivitas senyawa ekstrak kasar spons Aaptos aaptos
terhadap beberapa organisme target ... 24
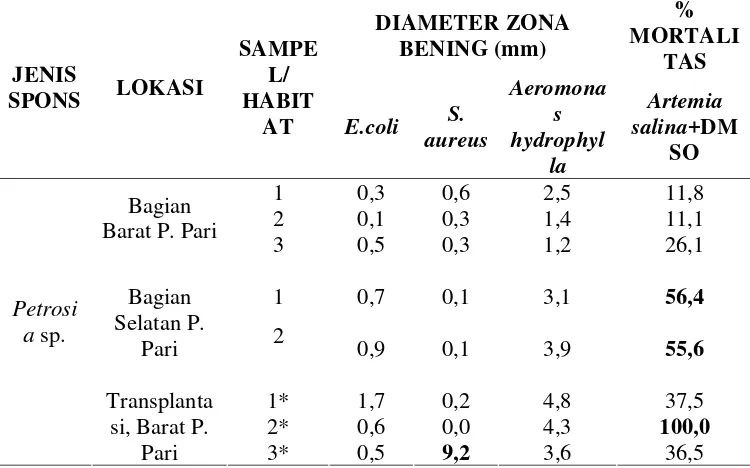
3 Bioaktivitas senyawa ekstrak kasar spons Petrosia sp.
terhadap beberapa organisme target ... 26
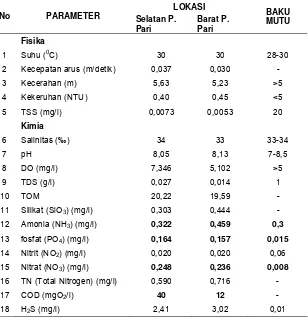
4 Nilai parameter lingkungan di kedua lokasi pengambilan
sampel beserta baku mutunya ... 28
5 Nilai rendemen ekstrak kasar spons Aaptos aaptos dan
Petrosia sp. dari bagian Barat dan Selatan P.Pari ... 29
6 Nilai Rf kandungan senyawa ekstrak kasar hasil fraksinasi
di bawah sinar uv (254 dan 365 nm) ... 31
7 Morfologi bakteri simbion yang berhasil diisolasi
dari spons Aaptos aaptos ... 33
DAFTAR GAMBAR
Halaman
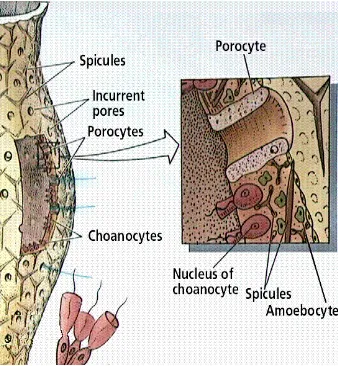
1 Struktur organisasi tubuh spons ... 7
2 Spons laut Aaptos aaptos ... 8
3 Spons laut Petrosia sp. ... 8
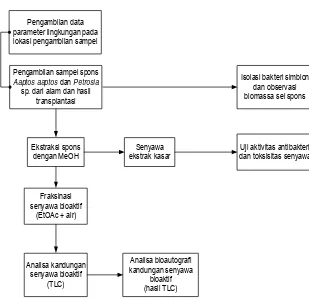
4 Diagram alir penelitian ... 22
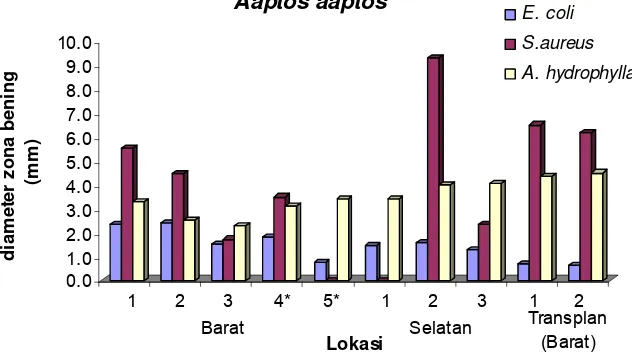
5 Bioaktivitas antibakteri senyawa ekstrak kasar spons Aaptos aaptos terhadap bakteri target ... 24
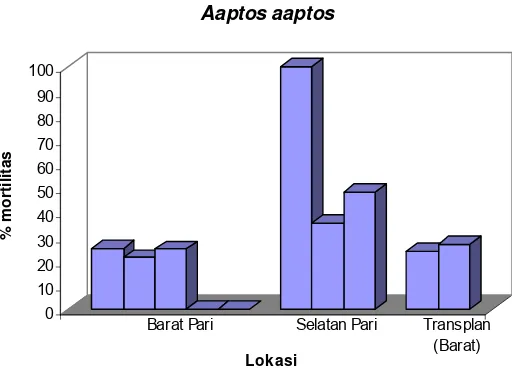
6 Toksisitas spons Aaptos aaptos terhadap Artemia salina ... 25
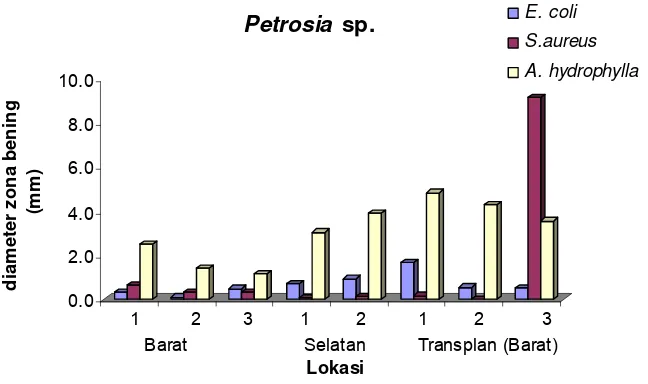
7 Bioaktivitas antibakteri senyawa ekstrak kasar spons Petrosia sp. terhadap bakteri target ... 27
8 Toksisitas spons Petrosia sp.terhadap Artemia salina ... 27
9 Fraksinasi ekstrak kasar spons ... 30
10 Hasil TLC spons Aaptos aaptos dan Petrosia sp. ... 31
11 Bioautografi fraksi organik spons Aaptos aaptos terhadap Aeromonas hydrophylla ... 32
12 Bioautografi fraksi organik spons Petrosia sp.terhadap Aeromonas hydrophylla ... 32
13 Bioautografi fraksi semi-organik spons Petrosia sp. terhadap Aeromonas hydrophylla ... 33
14 Isolat fungi simbion spons Petrosiasp. ... 34
15 Struktur sel spons Aaptos aaptos ... 35
16 Struktur sel spons Petrosia sp. ... 36
17 Distribusi fraksi sel spons setelahsentrifugasi ... 37
18 Alur penelitian dan pengembangan produk senyawa bioaktif dari spons ... 45
19 Peta Pulau Pari ... 66
DAFTAR LAMPIRAN
Halaman
1 Struktur taksonomi spons Aaptos aaptos
dan Petrosia sp. ... 66
2 Peta lokasi pengambilan sampel (Pulau Pari) ... 66
3 Sifat morfologi dan fisiologi bakteri simbion
yang berhasil diisolasi dari spons Aaptos aaptos... 67
PENDAHULUAN
Latar Belakang
Perkembangan dunia pengobatan yang semakin pesat telah memunculkan
beragam jenis obat-obatan baru. Penelitian untuk menemukan sumber metabolit
sekunder yang dapat digunakan sebagai bahan berbagai macam jenis obat juga
terus dilakukan. Sejak satu dekade terakhir ini, perhatian dunia pengobatan mulai
terarah ke bermacam organisme laut sebagai sumber daya yang sangat
potensial. Berbagai penelitian menunjukkan bahwa organisme laut memiliki
potensi yang sangat besar dalam menghasilkan senyawa-senyawa aktif yang
dapat digunakan sebagai bahan baku obat-obatan. Beberapa organisme laut
yang diketahui dapat menghasilkan senyawa aktif antara lain adalah spons,
moluska, bryozoa, tunikata dan lain-lain. Organisme-organisme ini diketahui
dapat menghasilkan sejumlah besar produk laut yang bersifat alami, juga mampu
menunjukkan keragaman senyawa kimia yang sangat besar. Senyawa-senyawa
kimia yang diketahui dapat dihasilkan oleh organisme tersebut antara lain adalah
senyawa alkaloid, peptida, terpena, poliketida dan beragam senyawa lainnya.
Lebih jauh lagi, diketahui bahwa dari 13 produk alami laut (atau produk analog
yang dihasilkan darinya) merupakan senyawa obat-obatan jenis baru, dan bahwa
12 senyawa tersebut berasal dari invertebrata laut (Thakur & Müller 2004).
Spons adalah hewan metazoa multiseluler yang tergolong ke dalam filum
Porifera, yang memiliki perbedaan struktur dengan metazoan lainnya. Hal ini
disebabkan seluruh tubuh spons terbentuk dari sistem pori, saluran dan
ruang-ruang sehingga air dapat dengan mudah mengalir keluar dan masuk secara terus
menerus. Sebagian besar spons hidup di laut, hanya beberapa spesies saja yang
dapat hidup di air tawar (Kozloff 1990). Hewan ini mencari makan dengan
mengisap dan menyaring air yang melalui seluruh permukaan tubuhnya secara
aktif (Romimohtarto & Juwana 1999). Spons terdiri dari 850 jenis, yang dapat
dibagi menjadi tiga kelas besar, yaitu Calcarea, Demospongiae dan
Hexactinellida. Spons juga diketahui memiliki ekologi habitat yang sangat luas.
Organisme sederhana ini diketahui dapat hidup pada kedalaman dan kondisi
perairan yang beragam. Para peneliti menemukan bahwa spons menghasilkan
metabolit sekunder sebagai mekanisme perlindungan diri. Penelitian juga
mengungkapkan bahwa metabolit sekunder ini tidak hanya berperan dalam
organisme terhadap lingkungannya (Thakur & Müller 2004). Adaptasi tersebut
dapat sebagai mekanisme pertahanan diri terhadap predator, keadaan
lingkungan yang menuntut kompetisi akan nutrisi, maupun mekanisme
pertahanan terhadap kondisi lingkungan yang terpolusi limbah organik (Thakur &
Müller 2004).
Keragaman metabolit sekunder yang dihasilkan spons telah banyak diteliti
dan dimanfaatkan untuk menemukan senyawa-senyawa aktif yang berguna bagi
dunia pengobatan. Senyawa-senyawa tersebut dapat berupa turunan asam
amino dan nukleosida, makrolida, porphirine, terpenoid, gugus alifatik peroksida
dan sterol. Obat-obat yang diketahui dihasilkan oleh spons antara lain adalah
discodermolide, topsentin, manzamine A, plakortolide, dan berbagai senyawa
lainnya yang diketahui bersifat sebagai antikanker, antifungal, anti-inflamasi, anti
HIV, penghambat aktivitas enzim dan sifat-sifat lainnya (Higa et al. 1994;
Kobayashi & Kitogawa 1994; Sennett et al. 2002; Proksch et al. 2003; Thakur &
Müller 2004; Anonim 2005; Hadas et al. 2005; Zheng et al. 2005).
Perumusan Masalah
Perkembangan dunia pengobatan dan ilmu pengetahuan yang semakin
pesat memacu eksplorasi terhadap sumber senyawa bioaktif dari organisme laut.
Spons merupakan salah satu organisme laut yang memiliki banyak potensi
sebagai sumber senyawa bioaktif. Tingginya keragaman jenis spons dan masih
sedikitnya informasi yang tersedia mengenai potensi organisme ini, memacu
berbagai penelitian mengenai potensi yang dikandungnya, selain mengenai
reproduksi dan mekanisme hidup spons.
Indonesia sebagai negara maritim yang memiliki tingkat keragaman
organisme laut yang tinggi, termasuk spons, mempunyai potensi yang sangat
besar untuk mengembangkan berbagai senyawa bioaktif. Hal ini telah disadari
oleh banyak peneliti, sehingga penelitian mengenai potensi spons Indonesia
semakin banyak dilakukan dewasa ini. Namun demikian, perbedaan kualitas
lingkungan perairan sebagai habitat organisme dapat mempengaruhi
metabolisme organisme tersebut, termasuk spons. Oleh karena itu, perlu
dilakukan suatu penelitian mengenai pengaruh lingkungan terhadap potensi
senyawa bioaktif yang dikandung oleh spons.
Penelitian awal yang pernah dilakukan oleh Tim Hibah Pasca (IPB 2005)
memiliki jumlah jenis dan kelimpahan spons yang tinggi. Spons yang ditemukan
dalam jumlah dan kelimpahan yang dominan diantaranya adalah Aaptos aaptos
dan Petrosia sp. Penelitian yang dilakukan oleh Kardono (2006) dan Susanna
(2006) juga menunjukkan bahwa kedua jenis spons ini memiliki kecenderungan
peningkatan jumlah dan kelimpahan seiring pertambahan kedalaman. Kedua
jenis spons ini juga memiliki potensi sebagai senyawa antibakteri.
Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Melakukan penapisan senyawa bioaktif dari spons Aaptos aaptos dan
Petrosia sp.
2. Menganalisa kandungan senyawa ekstrak kasar spons Aaptos aaptos
dan Petrosia sp. (fraksi organik dan semi organik), dan bioaktivitas
antibakteri masing-masing senyawa
3. Melihat pengaruh perbedaan lingkungan terhadap tingkat bioaktivitas
(antimikroba dan toksisitas) senyawa dari spons jenis Aaptos aaptos dan
Petrosia sp.
4. Melihat kaitan biomassa sel spons dan isolat bakteri terhadap bioaktivitas
senyawa ekstrak kasar spons Aaptos aaptos dan Petrosia sp.
Analisis ini diharapkan dapat memberikan informasi senyawa yang dapat
TINJAUAN PUSTAKA
Morfologi Spons
Spons adalah hewan yang termasuk Filum Porifera. Filum Porifera terdiri
dari tiga kelas, yaitu: Calcarea, Demospongiae, dan Hexactinellida (Haywood &
Wells 1989; Sara 1992; Rachmaniar 1996; Romimohtarto & Juwana 1999),
sedangkan menurut Warren (1982), Kozloff (1990), Harrison dan De Vos (1991),
Pechenik (1991), Ruppert dan Barnes (1991), Filum Porifera terdiri dari empat
kelas, yaitu: Calcarea, Demospongiae, Hexactinellida, dan Sclerospongia.
Kelas Calcarea adalah kelas spons yang semuanya hidup di laut. Spons ini
mempunyai struktur sederhana dibandingkan yang lainnya. Spikulanya terdiri dari
kalsium karbonat dalam bentuk calcite. Kelas Demospongiae adalah kelompok
spons yang paling dominan di antara Porifera masa kini. Jenis ini tersebar luas
di alam, serta jumlah jenis maupun organismenya sangat banyak. Mereka sering
berbentuk masif dan berwarna cerah dengan sistem saluran yang rumit,
dihubungkan dengan kamar-kamar bercambuk kecil yang bundar. Spikulanya
ada yang terdiri dari silikat dan ada beberapa (Dictyoceratida, Dendroceratida
dan Verongida) spikulanya hanya terdiri serat spongin, serat kollagen atau tanpa
spikula. Kelas Hexactinellida merupakan spons gelas. Mereka kebanyakan hidup
di laut dalam dan tersebar luas. Spikulanya terdiri dari silikat dan tidak
mengandung spongin (Warren 1982; Kozloff 1990; Brusca & Brusca 1990;
Ruppert & Barnes 1991; Romimohtarto & Juwana 1999). Kelas Sclerospongia
merupakan spons yang kebanyakan hidup pada perairan dalam di terumbu
karang atau pada gua-gua, celah-celah batuan bawah laut atau terowongan
diterumbu karang. Semua jenis ini adalah bertipe leuconoid yang kompleks yang
mempunyai spikula silikat dan serat spongin. Elemen-elemen ini dikelilingi oleh
jaringan hidup yang terdapat pada rangka basal kalsium karbonat yang kokoh
atau pada rongga yang ditutupi oleh kalsium karbonat (Warren 1982; Kozloff
1990; Harrison & De Vos 1991; Pechenik 1991; Ruppert & Barnes 1991).
Morfologi luar spons laut sangat dipengaruhi oleh faktor fisik, kimiawi, dan
biologis lingkungannya. Spesimen yang berada di lingkungan yang terbuka dan
berombak besar cenderung pendek pertumbuhannya atau juga merambat.
Sebaliknya spesimen dari jenis yang sama pada lingkungan yang terlindung atau
tegak dan tinggi. Pada perairan yang lebih dalam spons cenderung memiliki
tubuh yang lebih simetris dan lebih besar sebagai akibat dari lingkungan yang
lebih stabil apabila dibandingkan dengan jenis yang sama yang hidup pada
perairan yang dangkal (Bergquist 1978).
Spons dapat berbentuk sederhana seperti tabung dengan dinding tipis,
atau masif bentuknya dan agak tidak teratur. Banyak spons juga terdiri dari
segumpal jaringan yang tak tentu bentuknya, menempel dan membuat kerak
pada batu, cangkang, tonggak, atau tumbuh-tumbuhan. Kelompok spons lain
mempunyai bentuk lebih teratur dan melekat pada dasar perairan melalui
sekumpulan spikula. Bentuk-bentuk yang dimiliki spons dapat beragam.
Beberapa jenis bercabang seperti pohon, lainnya berbentuk seperti sarung tinju,
seperti cawan atau seperti kubah. Ukuran spons juga beragam, mulai dari jenis
berukuran sebesar kepala jarum pentul, sampai ke jenis yang ukuran garis
tengahnya 0.9 m dan tebalnya 30.5 cm. Jenis-jenis spons tertentu nampak
berbulu getar karena spikulanya menyembul keluar dari badannya
(Romimohtarto & Juwana 1999).
Banyak spons berwarna putih atau abu-abu, tetapi lainnya berwarna
kuning, oranye, merah, atau hijau. Spons yang berwarna hijau biasanya
disebabkan oleh adanya alga simbiotik yang disebut zoochlorellae yang terdapat
didalamnya (Romimohtarto & Juwana 1999). Warna spons tersebut sebagian
dipengaruhi oleh fotosintesa mikrosimbionnya. Mikrosimbion spons umumnya
adalah cyanophyta (cyanobacteria dan eukariot alga seperti dinoflagellata atau
zooxanthella). Beberapa spons memiliki warna yang berbeda walaupun termasuk
dalam jenis yang sama. Beberapa spons juga memiliki warna dalam tubuh yang
berbeda dengan pigmentasi luar tubuhnya. Spons yang hidup di lingkungan yang
gelap akan berbeda warnanya dengan spons sejenis yang hidup pada
lingkungan yang cerah (Wilkinson 1980).
Secara umum spons terdiri dari beberapa jenis sel yang menyusun struktur
tubuh dan biomassanya. Sel-sel tersebut memiliki fungsi yang berperan dalam
organisasi tubuh spons. Dinding tubuh spons terorganisasi secara sederhana.
Lapisan luar dinding tubuh disusun oleh sel-sel pipih yang menyerupai sel epitel
pada hewan lain, yang disebut pinacocytes, membentuk lapisan pinacoderm.
Perbedaan sel ini dengan sel epitel hewan lainnya adalah tidak adanya basal
lamina dan saluran interseluler, serta dapat berkontraksi atau menyusut,
menghasilkan material seksresi yang dapat melekatkan spons ke substratnya.
Pada dinding tubuh spons juga terdapat pori-pori yang dibentuk oleh porocyte,
yaitu sel berbentuk cincin yang berkembang dari permukaan luar ke bagian
spongocoel. Sel-sel ini dapat membuka dan menutup dengan adanya kontraksi.
Pada bagian dalam pinacoderm terdapat mesohyl, yang terdiri dari matriks
protein bergelatin yang mengandung skeleton dan sel-sel amoeboid. Lapisan ini
berfungsi seperti jaringan ikat pada metazoa lainnya. Skeleton spons
demospongia terbentuk dari spikula bersilika dan serat protein spongin. Materi
inilah yang membentuk dan menyokong bangun tubuh spons. Spikula spons
memiliki jenis yang beragam, sehingga dijadikan dasar untuk identifikasi spons.
Secara umum, spikula terbagi menjadi megascleres (spikula berukuran besar
dan merupakan elemen penyokong utama dalam skeleton) dan microscleres
(spikula berukuran kecil). Spikula berada di dalam mesohyl, namun sering juga
ditemukan pada lapisan pinacoderm. Sementara itu, serat spongin merupakan
serat protein yang menyerupai kolagen. Spons dengan serat spongin yang
berlimpah, biasanya memiliki morfologi yang keras dan padat (kasar). Selain itu,
pada banyak spesies, seringkali sebagian atau keseluruhan spikula bersilika
ditutupi oleh serat spongin ini, sehingga menjadi lebih kaku.
Sel-sel amoeboid dapat ditemukan pada mesohyl, dan tersusun dari
beberapa jenis sel. Archaeocyt adalah sel berukuran besar dengan nukleus yang
besar pula. Sel ini merupakan sel fagositosis dan berperan dalam digesti
makanan. Sel ini juga bersifat totipotent (dapat berubah fungsi), sehingga dapat
berubah fungsi menjadi sel lain yang dibutuhkan oleh spons. Sel-sel tetap yang
disebut dengan collencytes, berfungsi mensekresikan jaringan kolagen yang
menyebar pada dinding tubuh spons.
Spikula pembentuk skeleton dihasilkan oleh sel-sel sclerocyte yang bersifat
amoeboid. Sementara jaringan spongin merupakan hasil sekresi sel-sel
spongocytes.
Choanocytes, adalah lapisan sel yang terdapat pada bagian dalam
mesohyl, sejajar dengan spongocoel. Sel ini memiliki struktur yang menyerupai
protozoa choanoflagelata. Choanocyte berbentuk bulat, dengan satu ujungnya
terhubung ke mesohyl. Sisi berlawanan dengan bagian tersebut memiliki flagella
yang dikelilingi oleh mikrovilli. Sel choanocyte berperan dalam pergerakan air
dalam tubuh spons dan untuk menyediakan makanan (Rupert & Barnes 1994).
Gambar 1 Struktur organisasi tubuh spons (sumber: www.maricopa.edu)
Selain sel-sel yang telah disebutkan di atas, spons juga bersimbiosis
dengan beberapa mikroorganisme, seperti bakteri. Menurut Friedrich et al. (2001, diacu dalam Thakur & Mϋller 2004), diperkirakan sekitar 40% biomassa beberapa spons disusun oleh komunitas bakteri. Bakteri-bakteri tersebut
merupakan simbion dalam tubuh spons. Beberapa penelitian menunjukkan
bahwa simbion-simbion tersebut memiliki peranan dalam produksi senyawa
bioaktif yang berfungsi dalam adaptasi ekologi spons (Faulkner et al. 1994;
Kobayashi & Kitagawa 1994; Guyot 2000; Proksch et al. 2003; Rahe 2004;
Thakur & Mϋller 2004; dan Zheng et al. 2004).
Proses interaksi antara spons dan mikroba simbionnya belum sepenuhnya
diketahui. Beberapa teori mengemukakan bahwa proses rekrutmen mikroba
simbion dilakukan spons pada saat proses filter feeder, dan masuk ke dalam
mesohyl. Namun beberapa penelitian menunjukkan bahwa selain mikroba
episimbion yang melekat pada bagian permukaan spons selama masa
pertumbuhan (Carpenter 2002; Chelossi et al. 2004), beberapa bakteri dan
khamir (fungi) diturunkan secara genetis dalam tubuh spons (Maldonado et al.
2005; Oren et al. 2005; Steindler et al. 2005). Mikroba simbion spons, selain
berperan dalam produksi senyawa bioaktif, juga memiliki peran menjaga
kestabilan pertumbuhan dan kesehatan spons. Simbion-simbion tersebut
memiliki peran penting dalam penyediaan energi dan nutrisi (Carpenter 2002;
Steindler 2002,2005), menghambat mikroba patogen (Faulkner et al. 1994), serta
sebagai pelindung terhadap radiasi sinar uv dan penghasil enzim antioksidan
Gambar 2 Spons laut Aaptos aaptos.
Spons Aaptos aaptos dapat ditemukan di Kepulauan Seribu, yaitu di Pulau
Lancang, Pulau Pari dan Pulau Pramuka, yang memiliki kondisi lingkungan yang
cukup berbeda (IPB 2005). Spons ini termasuk ke dalam famili Suberitidae,
Schmidt 1870, dengan morfologi yang masif. Spons genus Aaptos Gray,1867
(diacu dalam Hooper 2000), memiliki morfologi yang berbentuk
spherical/subspherical (bundar/agak bundar), soliter, dengan permukaan yang
halus atau berserabut, dan skeleton radial. Saluran spikula pada spons genus ini
mengarah keluar dari bagian tengah spons secara bervariasi. Korteksnya yang
tipis mengandung kolagen, barisan dua jenis spikula berukuran kecil, dan
spikula berukuran sedang pada bagian saluran ektosomal plumose. Spikula
primer spons genus Aaptos biasanya berupa strongyloxea, spikula yang
berukuran sedang berbentuk lurus atau melengkung atau subtylostyle,
sementara spikula ektosomal dapat berupa style, subtylostyle, dan/atau tylostyle
yang lebih kecil. Pada beberapa spesies dapat juga ditemukan oxea
(Kelly-Borges & Bergquist 1994, diacu dalam Hooper 2000).
Gambar 3 Spons laut Petrosia sp., berbentuk lembaran: (a) melekat pada substrat karang; (b) dengan makrofauna pada permukaannya (berwarna putih).
Spons Petrosia sp. juga dapat ditemukan di Kepulauan Seribu, antara lain
di Pulau Pramuka dan Pulau Pari (IPB 2005). Spons ini termasuk ke dalam famili
yang sama dengan Xestospongia, yaitu Petrosiidae, Van Soest 1980. Skeleton
ektosomal spesies ini berupa potongan spikula yang seragam (isotropic),
dengan skeleton choanosomal yang tersusun atas saluran spikula yang padat
dan terikat dengan sedikit spongin, sehingga membentuk tekstur yang keras.
Spesies ini memiliki sekitar 2 jenis ukuran oxeote atau spikula strongylote
(Bergquist & Warne 1980; van Soest 1980, diacu dalam Hooper 2000). Skema
taksonomi spons Aaptos aaptos dan Petrosia sp. dapat dilihat pada Lampiran 1.
Penelitian yang dilakukan Susanna (2006) menunjukkan bahwa kedua
jenis spons (Aaptos aaptos dan Petrosia sp.) memiliki jumlah dan kelimpahan
jenis yang semakin meningkat seiring bertambahnya kedalaman. Hal ini
dikatakan terkait dengan kondisi lingkungan perairan yang semakin kondusif
seiring bertambahnya kedalaman. Susanna (2006) juga menyatakan bahwa
spons jenis Aaptos aaptos (yang diidentifikasi awal sebagai Xestospongia sp.2)
dan Petrosia sp. merupakan jenis yang dominan ditemukan pada perairan
Kepulauan Seribu (P. Lancang, P. Pari dan P. Pramuka).
Metabolit Sekunder
Secara ekologis, spons terdapat pada beragam kondisi habitat. Ini
menimbulkan pertanyaan mengenai mekanisme adaptasi spons, yang
merupakan hewan sederhana, terhadap kondisi lingkungan habitat.
Penelitian-penelitian yang dilakukan menunjukkan bahwa spons memiliki pertahanan diri
secara kimiawi (metabolit sekunder). Senyawa-senyawa kimiawi tersebut
bermanfaat untuk mempertahankan diri dari tekanan kompetitor, reaksi
antagonisme, infeksi maupun predasi oleh organisme laut lainnya.
Spons menghasilkan dua jenis metabolit selama masa pertumbuhan dan
perkembangannya, yaitu metabolit primer dan metabolit sekunder. Metabolit
primer adalah metabolit yang dibentuk selama masa pertumbuhan dan
digunakan dalam proses-proses metabolisme esensial bagi organisme. Produksi
metabolit ini hampir serupa pada semua organisme, melibatkan proses
anabolisme dan katabolisme, contohnya lintasan pembentukan glukosa.
Sementara itu, metabolisme sekunder adalah komponen senyawa yang
diproduksi pada saat kebutuhan metabolisme primer sudah terpenuhi dan
lingkungan(Torssell 1983). Karakteristik senyawa metabolit sekunder adalah
(Crueger & Crueger 1982; Madigan et al. 2000):
a. Masing-masing senyawa metabolit sekunder dihasilkan oleh beberapa
organisme tertentu saja.
b. Metabolit sekunder bukanlah merupakan senyawa yang esensial bagi
pertumbuhan dan reproduksi.
c. Pembentukan senyawa metabolit sekunder sangat dipengaruhi oleh kondisi
lingkungan organisme.
d. Beberapa senyawa metabolit sekunder yang dihasilkan organisme
merupakan kelompok senyawa yang berkerabat (memiliki kesamaan
struktur).
e. Beberapa organisme membentuk berbagai substansi yang berbeda
sebagai metabolit sekundernya.
f. Regulasi biosintesis metabolit sekunder sangat berbeda dengan metabolit
primer.
g. Produksi metabolit sekunder seringkali dapat terjadi secara berlebihan jika
terkait dengan produksi metabolit primer.
h. Produk metabolit sekunder dapat berasal dari hasil samping produk
metabolit primer, atau disebut juga berasal dari beberapa produk
intermedia yang terakumulasi selama metabolisme primer.
Metabolit sekunder yang dihasilkan oleh spons memiliki keragaman yang
sangat tinggi. Senyawa-senyawa tersebut antara lain adalah derivat asam amino,
dan nukleosida hingga makrolida, porphyrine, terpenoid hingga ikatan alifatik
peroksida, dan sterol. Beberapa penelitian menunjukkan bahwa spons kaya akan
terpenoid dan steroid, yang diduga berfungsi sebagai antipredasi dan kontrol
terhadap kompetisi ruang serta pertumbuhan epibion yang berlebih (Bakus et
al.1986, diacu dalam Thakur & Müller 2004).
Produk Alami dan Mikroba Simbion Spons
Kategori Produk Alam Laut
Produk alam laut dikelompokkan atas: (1) sumber biokimia yang mudah
untuk mendapatkan dalam jumlah yang besar dan barangkali dapat dirubah ke
bahan-bahan yang lebih berharga; (2) senyawa bioaktif yang termasuk (a)
senyawa aktif secara farmakologi dan (d) senyawa sitotoksik dan antitumor; (3)
Racun laut (Kobayashi & Rachmaniar 1998).
Senyawa Bioaktif Spons
Selama beberapa abad (sejak dua abad yang lalu) telah diketahui bahwa
spons memiliki potensi bioaktif yang besar. Richter pada tahun 1907 (diacu
dalam Thakur & Müller 2004) menemukan bahwa spons mandi yang dibakar
ditemukan senyawa iodine. Sementara yang pertama kali mencari produk
senyawa alami spons secara sistematis adalah Bergman dan Fenney (1951,
diacu dalam Thakur & Müller 2004), yang berhasil mengisolasi 3 nukleosida dari
spons Karibia Chryptotethya crypta Laubenfels, 1949. Sejak itu bermacam
senyawa obat-obatan telah ditemukan dari produk alami spons atau pun
analognya. Tabel 1 menunjukkan beragam senyawa bioaktif yang telah
ditemukan dari spons.
Senyawa antibakteri telah diisolasi dari spons laut jenis: Discodermia
kiiensis, Cliona celata, Lanthella basta, Lanthella crardis, Psammaplysila
purpurea, Agelas sceptrum, Phakelia flabellata. Senyawa antijamur telah diisolasi
dari spons laut jenis: Jaspis sp., Jaspis johnstoni, Geodia sp. Senyawa anti
tumor/anti kanker telah diisolasi dari spons laut jenis: Aplysina fistularis, A.
aerophoba. Senyawa antivirus telah diisolasi dari spons laut jenis: Cryptotethya
crypta, Ircinia variabilis. Senyawa sitotoksik diisolasi dari spons laut jenis:
Axinella cannabina, Epipolasis kuslumotoensis, Spongia officinalis, Igernella
notabilis, Tedania ignis, Axinella verrucosa, Ircinia sp. Senyawa antienzim
tertentu telah diisolasi dari spons laut jenis: Psammaplysilla purea (Ireland et al.
1989; Munro et al. 1989).
Spons juga diketahui memiliki mikroba simbion yang berasosiasi dalam
jumlah yang sangat besar. Mikroba ini diketahui hidup di permukaan tubuh dan
dalam matriks tubuh spons. Pada proses pengambilan makanan, mikroba dari
lingkungan perairan sekitarnya ikut tersaring dan masuk ke dalam tubuh spons.
Diduga sebagian besar mikroba ini tetap hidup dalam tubuh spons tersebut.
Dugaan ini diperkuat oleh fenomena bahwa kepadatan mikroba simbion
berubah seiring variasi perubahan lingkungan (Thakur 2001, diacu dalam Thakur
& Müller 2004). Jumlah mikroba simbion yang berasosiasi dengan spons
diperkirakan mencapai 40% biomassa spons. Oleh karena itu, beberapa
penelitian berusaha membuktikan bahwa senyawa aktif dan antimikroba yang
spons. Beberapa senyawa bioaktif spons yang diketahui dihasilkan oleh mikroba
simbion adalah senyawa norharman (senyawa β-carboline dari kelompok
alkaloid), yang memiliki aktivitas antibakterial, dari bakteri simbion pada spons
Hymeniacidon perleve (Zheng et al. 2004), senyawa decalactone baru dari fungi
simbion pada spons Xestospongia exigua (Proksch et al. 2003), 2-metil
thio-1,4-naftoquinon dari bakteri simbion pada Dysidea avarai, sorbilactone A dari fungi
Penicillium chrisogenum pada spons Ircinia fasciculate, dan banyak senyawa
lainnya (Thakur & Müller 2004).
Spons Aaptos aaptos dapat menghasilkan metabolit sekunder yang
mengandung senyawa bioaktif potensial, seperti senyawa dari golongan alkaloid
(aaptamine dan demethyloxyaaptamine), homarine dan senyawa lainnya.
Senyawa-senyawa tersebut telah dibuktikan memiliki aktivitas sebagai
anti-tumor, sehingga potensial sebagai sumber obat-obatan baru (Pelletier et al.
1987; Bergquist 1991, diacu dalam Miller et al. 1998; Granato et al. 2000).
Sementara itu, spons Petrosia sp. diketahui mengandung senyawa bioaktif yang
termasuk kedalam kelompok poliasetilen dan dari kelompok sterol.
Senyawa-senyawa tersebut telah dibukstikan potensial sebagai antibakteri, antifungi,
antifouling dan lain-lain (Young et al.1999; Kim et al. 2002; Sarma et al. 2005;
www.cas.muohio.edu).
Tabel 1 Senyawa bioaktif yang dihasilkan spons laut Aktivitas
Farmakologi Senyawa bioaktif Jenis spons
Sitotoksik Asam 3,6 epoksieikosa- Hymeniacidon hauraki
3 ,5,8,1 1,14,17-heksaenoat
Reidispongiolid A dan B Reidispongia coerulea
Superstolida A dan B Neosiphnia sperstes
Swinhol ida A Theonella swinhoet
Arenastatin A Dysidea arenaria
Fakeliastatin Phakelia costata
Diskodermin E-H Discodermia kiiensis
Ingenamin, ingamin A dan B, Xestospongia ingens
Madangamin A
8-hidrosimanzamin A Pachypellina sp. Glisinililimakuinon A Fasciospongia rimosa
Vaskulin Cribrocalina vasculum
Latrunkulin S, neolaulimalida, Fasciospongia rimosa
Tabel 1 Senyawa bioaktif yang dihasilkan spons laut * (Lanjutan)
Aktivitas
Farmakologi Senyawa bioaktif Jenis spons
Sitotoksik Leukasandrolida Leucasandra caveolata
Altohirtin A-C, 5-deasctil- Hyrtos alium
Altohirtin
Halisilindramida A Halichondria caveolata
Antitumor Agelasfin (AGL) Agelas muritianus
Antileukemia Kurasin A Lingbya majuscula
Amfidinolid B1, B2, B3, N, Q. Amphidinium sp. Triangulin A-H, asam Pellina triagulata
Triangulinat
Anti HIV 1 Trikendiol Trikentrion loeve
Antimikroba Hormotamnim Hormothamnion Enteromorphoides
Diskodermin E-H Discodermia kiiensis
Antibakteri Lokisterolamin A dan B Corticium sp.
Antijamur Asam kortikatat A,B,C Petrosia corticata
Leukasandrolida Leucasandra caveolata
Halisilindramida Halichondria cylindrica
Imunomodulato Agelasfln 10 dan 12 Agelas muritianus
Antiinflamasi Manualida Luffariella variabilis
Belum Halisiklamina A Haliclona sp. (masih dalam BastadinA. dan B Ianthella basta
penelitian) Asam manadat A dan B Placortis sp.
Klatirimin Clathria basilana
Halisiklamina B Xestrospongia sp.
Keterangan: angka dalam kurung pada kolom kedua adalah jumlah jenis/genus * menurut Soediro (1999)
Ekstrak Kasar dan Fraksi
Produk senyawa organik spons laut yang memiliki potensi sebagai
senyawa bioaktif mencakup lebih dari 50% penemuan senyawa organik potensial
dari laut (Hunt & Vincent 2006). Pengisolasian senyawa organik potensial ini
dilakukan dengan mengekstrak organisme spons dengan pelarut yang dipilih
berdasarkan kesamaan tingkat polaritas senyawa yang diinginkan. Pada saat
ekstraksi, senyawa ekstrak kasar (campuran) dari organisme spons akan tertarik
keluar oleh pelarut pengekstrak, sehingga dapat dilakukan pengujian untuk
Hasil ekstraksi tersebut kemudian dapat difraksinasi untuk mendapatkan
senyawa organik yang terpisah dari fraksi air yang mengandung ion. Cara ini
merupakan awal dari pemurnian senyawa organik yang diinginkan (Smart 2002).
Proses ini menggunakan dua pelarut yang berbeda berdasarkan teori like dislike
polarity, sehingga didapatkan dua fraksi terpisah yang berbeda, yaitu fraksi
organik dan ionik dari ekstrak.
Isolasi dan identifikasi komponen-komponen senyawa organik yang
memiliki potensi sebagai senyawa bioaktif dapat dilakukan dengan cara
kromatografi. Kromatografi merupakan metode pemisahan senyawa untuk
memurnikan dan mengidentifikasi komponen-komponennya. Metode ini
berdasarkan distribusi komponen yang berbeda dari suatu campuran antara fase
bergerak dan fase diam pada suatu lempengan tipis. Pada kromatografi lapis
tipis (Thin Layer Chromatography/TLC), fase diamnya berupa lapisan tipis yang
melekat pada suatu material (dapat berupa gelas, plastik atau lembaran metal),
yang memungkinkan fase bergerak dapat bergerak ke atas secara kapilari.
Proses pemisahan senyawa berdasarkan prinsip bahwa tiap komponen dalam
campuran senyawa memiliki perbedaan polaritas dan akan terserap oleh fase
diamnya (misalnya gel silika), demikian pula pelarut (adsorbent) dan zat terlarut
(dissolve) yang berada pada fase gerak, akan bergerak pada tingkatan yang
berbeda. Oleh karena itu, tiap komponen dalam campuran senyawa akan tertarik
oleh pelarut fase gerak pada tingkatan yang berbeda di sepanjang plat
kromatografi.
Hasil pemisahan senyawa akan menunjukkan spot-spot yang terpisah
sepanjang plat TLC berdasarkan tingkat polaritasnya. Spot-spot ini kemudian
dilihat dan ditandai di bawah sinar uv. Faktor retardasi (Rf) dari tiap spot
komponen yang terpisah dapat dikalkulasi dengan mengukur jarak dari titik awal
sampel ke tengah spot yang sudah terpisah. Rf ini dapat merupakan langkah
awal untuk memperkirakan jenis (identifikasi awal) komponen senyawa organik
yang telah terpisah (Smart 2002; Furniss et al. 2004).
Spons laut menghasilkan ekstrak kasar dan fraksi organik yang bersifat
antibakteri, antijamur, antibiofouling dan ichtyotoksik. Bioaktivitas antibakteri
ekstrak kasar spons laut terdapat pada beberapa jenis, seperti: Halichondria sp,
Callyspongia pseudoreticulata, Callyspongia sp. dan Auletta sp. (Suryati et al.
bakteri Staphylococcus aures, Bacillus subtilis dan Vibrio cholerae Eltor
(Rachmaniar 1994, 1995, 1996, 1997).
Bioaktivitas antijamur ekstrak kasar spons laut terdapat pada beberapa
jenis, seperti: Auletta spp., yang aktif terhadap jamur Aspergillus fumigatus,
spons Clathria spp., yang aktif terhadap Aspergillus spp., Aspergillus fumigatus
dan Fusarium spp., spons Theonella cylindrica, yang aktif terhadap Aspergillus
spp., Aspergillus fumigatus, Fusarium spp. dan Fusarium solani (Muliani et al.
1998).
Bioaktivitas antibiofouling ekstrak kasar spons laut terdapat pada
beberapa jenis, seperti: Asterospus sarasinorum, Callyspongia sp., Clathria sp.,
Clathria jaspis, yang keaktifannya tinggi terhadap teritip (Balanus amphirit);
Echynodicum sp., Gelliodes sp., Pericarax sp., Xestopongia sp., yang
keaktifannya rendah terhadap teritip (Balanus amphirit)(Suryati et al. 1999).
Bioaktivitas ichtyotoksik (toksisitas terhadap biota ikan) ekstrak kasar
spons laut terdapat pada beberapa jenis, seperti: Auletta spp., Callyspongia sp.,
Callyspongia pseudoreticulata, yang toksik terhadap nener bandeng (Chanos
chanos) (Parenrengi et al. 1999).
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan selama kurang lebih 6 bulan yang dimulai dari
bulan September sampai Desember 2006. Pengamatan dan pengambilan
sampel spons dilakukan di sekitar perairan terumbu karang Pulau Pari, yaitu
pada bagian Barat (1060 35’ 712” BT dan 050 52’ 055” LS) dan Selatan (1060
36’ 761” BT dan 050 52’ 244” LS) Pulau Pari, Kepulauan Seribu, DKI Jakarta.
Sementara sampel spons hasil transplantasi diambil dari kegiatan transplantasi
spons Hibah Pasca di perairan yang sama (bagian Barat Pulau Pari).
Selama pengamatan, juga dilakukan pengukuran beberapa parameter
lingkungan, yaitu suhu, salinitas, pasang surut dan parameter kualitas air
lingkungan.
Sampel spons yang diambil, selanjutnya dianalisis di Laboratorium
Mikrobiologi, Pusat Penelitian Lingkungan Hidup (PPLH)-IPB.
Bahan dan Alat
Ekstraksi, Fraksinasi dan Uji Bioaktivitas (Skrining Senyawa Bioaktif)
Ektraksi adalah suatu teknik untuk memisahkan dan mengisolasi suatu
senyawa dari suatu larutan campuran atau padatan. Ekstraksi padatan
dilakukan untuk mengambil produk natural dari jaringan makhluk hidup, dengan
perendaman jaringan pada suatu pelarut yang memiliki kesamaan tingkat
polaritas dengan senyawa yang diinginkan. Alat dan bahan yang digunakan
untuk ekstraksi adalah jaringan spons Aaptos aaptos dan Petrosia sp. yang
dipreservasi dalam metanol teknis, pelarut MeOH (metanol) p.a (Richelle-Maurer
& Braekman 2001; Kelly et al. 2003), erlenmeyer, tabung Buchner, vaccum
pump, rotary evaporator, alat freeze drying, kertas saring Whattman 9 mm
ukuran 40, dan tabung sampel.
Fraksinasi adalah suatu teknik untuk memisahkan komponen organik dan
ionik (larut dalam air) dalam suatu senyawa campuran menjadi dua fraksi
berbeda. Metode ini dapat dilakukan dengan mencampur dua jenis pelarut yang
berbeda, dengan komponen senyawa yang ingin dipisahkan. Alat dan bahan
yang digunakan adalah hasil ekstrak kasar sampel spons Aaptos aaptos dan
Petrosia sp. yang telah dikristalisasi, pelarut EtOAc (etil asetat), pelarut air,
Uji bioaktivitas dilakukan untuk melihat potensi ekstrak kasar senyawa
organik sampel spons Aaptos aaptos dan Petrosia sp. dari lingkungan yang
berbeda. Alat dan bahan yang digunakan adalah: senyawa organik hasil
ekstrak kasar spons Aaptos aaptos dan Petrosia sp., dengan konsentrasi 25
mg/ml MeOH (Richelle-Maurer & Braekman 2001); bakteri target
(Staphylococcus aureus, Aeromonas sp., dan Escherichia coli) dan antibiotik
pembanding Amphisilin trihidrat untuk uji anti bakteria senyawa, Artemia
salina (untuk uji toksisitas), cawan petri, pipet mikro, pipet tetes, kertas
cakram (diameter 6 mm), media Tryptic Soy Broth (TSB) dan Tryptic Soy Agar
(TSA), DMSO (dimetil sulfooksida), jarum ose, shaker, inkubator, batang
sebar, air laut.
Isolasi Senyawa Bioaktif
Isolasi senyawa bioaktif dilakukan terlebih dahulu dengan mengekstrak
sampel spons menggunakan metanol. Senyawa bioaktif yang didapatkan lalu di
fraksinasi menggunakan metanol (MeOH) dan etil asetat (EtOAc). Analisa
kandungan senyawa bioaktif dilakukan menggunakan DCM (diklorometana) dan
MeOH (10:1, v/v) pada gel silika kromatografi lapis tipis (TLC) 25 TLC Aluminium Sheets Silica Gel 60F254 Merck, yang lalu diikuti oleh deteksi
spektrofotometri pada gelombang 254 dan 365 nm (Zheng et al. 2005).
Uji bioaktivitas senyawa bioaktif (bioautografi) menggunakan bioindikator
bakteri uji A hydrophilla, media TSA (triptic Soy Agar Difco). Gel silica TLC yang sudah mengandung senyawa terpisah kemudian diuji dengan melapisi media
yang mengandung bakteri, untuk melihat aktivitas antimikrob senyawa hasil
fraksinasi.
Metode Kerja
Konsentrasi dan Bioaktivitas Antibakteri Ekstrak Kasar dan Fraksi
Pengambilan Sampel. Semua sampel yang akan digunakan dalam analisis pada penelitian ini diambil dari dua lokasi, yaitu bagian Barat (1060
35’ 712” BT dan 050 52’ 055” LS) dan Selatan (1060 36’ 761” BT dan 050 52’
244” LS) P.Pari. Pengambilan sampel dilakukan pada kedalaman 7 m dengan
menggunakan peralatan SCUBA DIVING SET. Sementara sampel hasil transplantasi diambil dari rak transplantasi di bagian Barat P. Pari, juga pada
kedalaman yang sama (7 m). Transplantasi dilakukan dengan mengikat
yang telah berusia 3 bulan, kemudian diambil untuk dianalisis. Beberapa
individu spons diambil pada setiap habitat di kedua lokasi (untuk sampel
alam) dan pada rak transplantasi untuk diekstraksi, yang ekstraksinya
terpisah setiap sampel, untuk kemudian dilakukan penapisan senyawa bioaktif
ekstrak kasarnya. Sampel untuk setiap habitat diperlakukan sebanyak tiga kali
ulangan. Sampel masing-masing spons dengan bobot yang memadai juga
diambil untuk analisis fraksinasi. Setelah preparasi dengan menyemprotkan
metanol (MeOH) teknis, sampel-sampel tersebut disimpan pada suhu -20°C.
Selain itu, masing-masing spons juga diambil dalam jumlah kecil dalam
keadaan segar dan preparasi formalin 4%, dengan tujuan mengisolasi bakteri
simbion dan analisa biomassa sel spons.
Ekstraksi. Ekstraksi dilakukan dengan metode maserasi menurut petunjuk Richelle-Maurer dan Braekman (2001) dan Kelly et al. (2003). Metode tersebut
adalah sebagai berikut: spons laut ditimbang sebanyak 25 gr, setelah ditimbang,
dipotong kecil-kecil, lalu dipindahkan ke dalam beaker glass 100 ml dan
ditambahkan 25 ml metanol p.a., kemudian diaduk-aduk hingga metanol
meresap ke dalam sampel. Beaker glass ditutup plastik dan disimpan selama 24
jam dalam suhu kamar. Kegiatan ini dilakukan sebanyak dua kali, sehingga
volume pelarut mencapai 50 ml. Setelah 24 jam, suspensi pekat disaring dengan
kertas saring untuk memisahkan cairan dengan endapannya. Cairan ditampung
di dalam labu takar 50 ml (ekstrak). Setelah dilakukan pengeringan ekstrak
larutan menggunakan evaporator rotavapor, lalu dilanjutkan dengan kristalisasi
menggunakan metode freeze drying, ekstrak kasar dipindahkan ke dalam
botol-botol kecil dan ditutup rapat, kemudian ditimbang untuk mengetahui
konsentrasinya. Ekstrak disimpan di dalam lemari pendingin untuk dilakukan
pengujian bioaktivitasnya.
Fraksinasi. Fraksinasi didasarkan pada prosedur fraksinasi menurut Parenrengi (1999). Prosedur fraksinasinya adalah sbb: (1) ekstraksi dengan
metanol (500 g spons segar dihaluskan dengan blender dan diekstraksi secara
maserasi dengan menggunakan pelarut metanol 500 ml selama 3 x 24 jam,
kemudian ekstrak kasar yang dihasilkan dihilangkan kadar airnya dengan
menggunakan vaccum rotary evaporator; (2) ekstraksi dengan etil asetat (ekstrak
secara pelan-pelan, kemudian diekstraksi menggunakan pelarut etil asetat
sehingga didapatkan dua fraksi, yakni larutan organik dan lapisan air).
Metode ini dilakukan dalam sebuah tabung separasi. Pelarut organik
(EtOAc) dan air dicampur sedemikan rupa dengan komponen campuran yang
ingin dipisahkan, lalu didiamkan beberapa waktu sampai membentuk dua lapisan
larutan fraksi yang berbeda. Kemudian lapisan paling bawah, yaitu fraksi air
(karena pelarut organik yang digunakan memiliki berat jenis yang lebih rendah
daripada air), dikeluarkan dari tabung, dan dipisahkan dari fraksi organik. Jenis
komponen organik dan ionik akan terpisah pada masing-masing fraksi.
Isolasi Bakteri simbion Spons. Sampel spons hidup dicuci dengan air laut steril untuk membuang bakteri non-simbion. Kemudian sekitar 0,5 g sampel
dikocok dengan air laut steril dan diinokulasi ke media padat (Sea Water
Complete agar + air laut steril). Setelah inkubasi selama ± 10 hari pada suhu
250C (Zheng et al. 2005), semua koloni dengan pigmentasi dan morfologi yang
berbeda, dipisahkan dan dibuat isolat murninya.
Uji bioaktivitas senyawa. Uji bioaktivitas terhadap senyawa hasil isolasi dilakukan dengan metode difusi agar menggunakan media TSA. Organisme
target (bakteri patogen) dikulturkan pada media tersebut dalam masing-masing
petri. Media yang telah disebar organisme target didiamkan selama 1 jam dalam
suhu kamar (280C). Kemudian ditengah-tengah media diletakan "paper disc" dan
diteteskan senyawa ekstrak kasar spons, yang telah dilarutkan sebanyak 25
mg/ml MeOH p.a (Richelle-Maurer & Braekman 2001), kurang lebih 20 µl
(0,04mg). Media yang telah diinokulasi dan ditotol dengan kertas cakram
diinkubasi pada 4 jam pada suhu 100C, untuk optimalisasi proses difusi,
kemudian diinkubasi selama 18 jam kemudian dihitung diameter hambatnya
terhadap organisme target. Sementara kista Artemia salina, dikultur pada air laut
steril selama 24 jam dengan suhu 280C dalam erlenmeyer, lalu diteteskan
ekstrak senyawa yang telah dilarutkan sebanyak 5 mg/ 20 µl DMSO (Effendi
2004), pada tabung reaksi yang berisi 2 ml air laut dan 10 individu Artemia salina
untuk melihat tingkat toksisitas senyawa (Richelle-Maurer & Braekman 2001).
Isolasi/identifikasi senyawa bioaktif sampel hasil fraksinasi
Isolasi dan identifikasi senyawa bioaktif sampel dilakukan dengan
terhadap senyawa organik dan semi organik dari hasil fraksinasi ekstrak kasar
spons Aaptos aaptos dan Petrosia sp. TLC dilakukan pada plat 25 TLC Aluminium sheets Silica Gel 60F254 produksi Merck. Sampel senyawa
organik diteteskan pada plat yang telah diberi tanda sebagai titik awal.
Kemudian plat direndam dalam eluen DCM:MeOH (10:1,v/v, yang telah
dioptimasi selama 2 jam) selama beberapa saat pada kotak kromatografi
(chamber). Setelah senyawa bergerak sampai garis batas, plat dikeluarkan
dan dikeringkan. Komponen senyawa organik yang terpisah akan berbentuk
spot-spot di sepanjang plat, kemudian dilihat dan ditandai di bawah sinar uv
dengan panjang gelombang 256 dan 365 nm (Zheng et al. 2005).
Analisa Aktivitas Antimikrob Senyawa Hasil Fraksinasi (Bioautografi)
Bahan yang digunakan adalah lapisan gel silica TLC yang mengandung
senyawa yang sudah difraksinasi. Lapisan gel tersebut disterilisasi menggunakan
sinar uv selama 30 menit, lalu diletakkan di atas agar nurien pada cawan petri.
Kemudian lapisan tersebut di lapisi oleh media agar nutrien cair yang
mengandung bakteri bioindikator A.hydrophylla dengan metode agar tuang,
kemudian diinkubasi pada suhu ruang selama 24 jam. Setelah masa inkubasi,
zona bening yang terbentuk diamati, untuk melihat spot komponen senyawa
organik yang dapat menghambat pertumbuhan bakteri (Zheng et al.2005).
Observasi Biomassa Sel Spons
Preparat histologi sampel spons yang telah dipreparasi dalam formalin
4% dilakukan untuk melihat susunan struktur jaringan spons. Selain itu, sampel
spons dipreparasi dalam formalin 3,5 - 4 % yang diencerkan dengan air laut yang
telah disaring dengan filter 0,2µm. Sampel spons kemudian dihancurkan dengan
menggunakan blender, kemudian suspensi sel diamati dibawah mikroskop fase
kontras untuk melihat tipe sel dan menghitung jumlah sel dengan memakai
haemasitometer.
Suspensi sel disentrifugasi untuk memisahkan biomassa sel spons dengan
bakteri simbion, serta fraksi bakteri, dengan dua kali proses sentrifugasi.(1)
Sentrifugasi pertama pada 1000 g selama 5 menit, untuk mendapatkan
supernatannya, (2) kemudian sentrifugasi pada 4000 g selama 10 menit untuk
mendapatkan pellet bakteri. Setelah masing hasil sentrifugasi disimpan dalam air
laut buatan yang dingin (cold artificial sea water) pengamatan jenis dan jumlah
Analisa Data
Analisa data pada penelitian ini sesuai dengan tahapan-tahapan yang
dilakukan, yaitu:
a. Penapisan senyawa bioaktif dianalisa dengan melihat besar zona bening
(zona hambat) terhadap bakteri indikator dan toksisitas terhadap Artemia
salina.
b. Kekuatan aktivitas (tingkat bioaktivitas) senyawa ekstrak berdasarkan
lingkungan hidup spons dianalisa secara deskriptif (kualitatif).
c. Hubungan bioaktivitas antibakteri dan toksisitas senyawa ekstrak spons
dianalisa dengan analisa korelatif, menggunakan program Minitab 1.3. d. Analisa kandungan senyawa hasil fraksinasi, serta kaitan bakteri simbion
dan biomassa sel spons dengan bioaktivitas spons dilakukan secara
DIAGRAM ALIR PENELITIAN
Pengambilan sampel spons
Aaptos aaptos dan Petrosia
sp. dari alam dan hasil transplantasi
Ekstraksi spons dengan MeOH
Senyawa ekstrak kasar
Fraksinasi senyawa bioaktif
(EtOAc + air)
Analisa kandungan senyawa bioaktif
(TLC)
Uji aktivitas antibakteri dan toksisitas senyawa
Analisa bioautografi kandungan senyawa
bioaktif (hasil TLC)
Isolasi bakteri simbion dan observasi biomassa sel spons Pengambilan data
parameter lingkungan pada lokasi pengambilan sampel
HASIL PENELITIAN
Hasil yang didapatkan dari penelitian ini mencakup beberapa aspek, yaitu
potensi bioaktivitas senyawa ekstrak kasar spons Aaptos aaptos dan Petrosia sp.
dari dua lokasi pengambilan sampel, pengaruh lingkungan terhadap kekuatan
bioaktivitas senyawa ekstrak kasar spons, kandungan fraksi senyawa ekstrak
kasar spons dan aktivitas antimikrob-nya, serta jenis isolat bakteri simbion dan
biomassa sel spons.
Bioaktivitas Senyawa Ekstrak Kasar Spons dan Pengaruh Lingkungan
Sampel spons Aaptos aaptos yang diambil dari beberapa habitat di bagian
Barat dan Selatan Pulau Pari, baik yang berasal dari alam maupun hasil
transplantasi, menunjukkan tingkat bioaktivitas yang beragam terhadap
organisme target (E. coli, S. aureus,A. hydrophylla, dan Artemia salina). Tabel 2
menunjukkan tingkat bioaktivitas ekstrak kasar spons Aaptos aaptos terhadap
beberapa organisme target.
Uji bioaktivitas antibakteri ekstrak kasar spons Aaptos aaptos terhadap
bakteri Gram (-) yang diwakili oleh bakteri E. coli menunjukkan tingkat aktivitas
yang cenderung rendah. Hal ini ditunjukkan oleh diameter zona hambat yang
kurang dari 3 mm. Sementara uji terhadap bakteri Gram (+) yang diwakili oleh
bakteri S. Aureus menunjukkan aktivitas yang sangat beragam, dari sangat
rendah (<0,1 mm) sampai tinggi (>5,5 mm). Kategori kekuatan bioaktivitas
antibakteri ditetapkan berdasarkan kontrol positif terhadap bakteri target,
memakai antibiotik ampisilin trihidrat (dengan zona hambat 2-3 mm).
Tingkat aktivitas yang paling tinggi terhadap S. aureus terlihat pada sampel
ekstrak spons Aaptos aaptos dari habitat 2 di lokasi Selatan P. Pari, yaitu
sebesar 9,3 mm. Bioaktivitas antibakteri senyawa ekstrak spons Aaptos aaptos
terhadap S. Aureus yang berasal dari alam (bagian Barat dan Selatan P. Pari)
sangat tidak seragam, berlawanan dengan bioaktivitas antibakteri dari hasil
transplantasi yang menunjukkan diameter zona hambat yang tidak terlalu jauh,
yaitu 6,5 dan 6,2 mm.
Uji bioaktivitas antibakteri ekstrak kasar Aaptos aaptos juga dilakukan
terhadap bakteri patogen Aeromonas hydrophylla. Bakteri ini adalah bakteri
Gram (-) berbentuk batang pendek, yang dikenal dapat menyebabkan penyakit
cenderung sensitif terhadap senyawa ekstrak kasar spons Aaptos aaptos. Hal ini
terlihat dari diameter zona hambat yang terbentuk di atas 1 mm, walaupun tidak
ada sampel ekstrak yang menunjukkan aktivitas tinggi (>5,5 mm). Gambar 5
menunjukkan grafik bioaktivitas antibakteri ekstrak kasar spons Aaptos aaptos
dari berbagai lokasi.
Tabel 2 Bioaktivitas senyawa ekstrak kasar spons Aaptos aaptos terhadap beberapa organisme target
* tanpa ulangan individu (hanya satu individu/habitat)
0.0
Gambar 5 Bioaktivitas antibakteri senyawa ekstrak kasar spons Aaptos aaptos terhadap bakteri target.
Tabel 2 menunjukkan bahwa spons Aaptos aaptos di bagian Barat dan
Selatan P. Pari lebih memiliki keragaman tingkat bioaktivitas terhadap ketiga
bakteri target. Sementara, spons hasil transplantasi memiliki zona hambat yang
DIAMETER ZONA BENING (mm) % MORTALITAS JENIS SPONS LOKASI SAMPEL/
nilainya hampir sama untuk masing-masing bakteri target, yaitu 0,7 mm terhadap
E. coli; 6,5 dan 6,2 mm terhadap S.aureus; serta 4,4 dan 4,5 mm terhadap A.
hydrophylla. Gambar 5 juga menunjukkan bahwa secara keseluruhan dapat
dikatakan bakteri S.aureus dan A.hydrophylla cenderung lebih sensitif terhadap
ekstrak kasar spons daripada bakteri E.coli.
Tabel 2 menunjukkan tingkat toksisitas spons Aaptos aaptos pada
konsentrasi 0,5 mg/20 μl DMSO, yang direfleksikan oleh persen mortalitas
Artemia salina. Hasil pengujian toksisitas menunjukkan bahwa pada konsentrasi
0,5 mg/20 μl DMSO, spons Aaptos aaptos menunjukkan bioaktivitas antibakteri
yang beragam dan tingkat toksisitas yang cenderung rendah pada berbagai
habitat di tiap lokasi, kecuali pada sampel yang berasal dari habitat 1 Selatan P.
Pari. Tingkat toksisitas dikatakan rendah jika pada dosis tersebut tidak
mengakibatkan kematian/mortilitas Artemia salina melebihi 50% atau tidak
mencapai LC50. Tingkat toksisitas spons Aaptos aaptos terhadap Artemia salina
ditunjukkan pada Gambar 6. Secara keseluruhan, Gambar 6 menunjukkan
bahwa spons dari bagian Selatan P. Pari memiliki toksisitas yang lebih tinggi
terhadap Artemia salina dibandingkan ekstrak kasar spons dari bagian Barat P.
Pari (untuk sampel alam dan hasil transplantasi).
0
Barat Pari Selatan Pari Transplan (Barat)
Gambar 6 Toksisitas spons Aaptos aaptos terhadap Artemia salina.
Spons Petrosia sp. memperlihatkan hasil uji bioaktivitas antibakteri yang
cenderung rendah (< 3 mm) terhadap E. coli dan S. aureus, kecuali pada sampel
dari hasil tranplantasi individu ketiga (sebesar 9,3 mm) terhadap S. aureus.
termasuk sedang (1,2 – 4,8 mm). Dengan demikian, dapat dikatakan bahwa
bakteri A.hydrophylla cenderung lebih sensitif terhadap ekstrak kasar spons
Petrosia sp. Sementara itu, tingkat toksisitas terhadap Artemia salina pada konsentrasi 0,5 mg/ 20 μl DMSO terlihat bervariasi. Sampel dari bagian Barat P. Pari cenderung memperlihatkan tingkat toksisitas yang rendah/sedang (dengan
mortilitas <30%) terhadap Artemia salina, sementara sampel dari bagian Selatan
P. Pari menunjukkan toksisitas yang cukup tinggi (mortilitas > 50%). Sampel dari
hasil transplantasi menunjukkan tingkat toksisitas dari sedang (mortilitas 36,5 %
dan 37,5%) sampai sangat tinggi (mortilitas 100%) pada sampel individu kedua.
Bioaktivitas spons Petrosia sp. dari berbagai lokasi terhadap organisme target
dapat dilihat pada Tabel 3, Gambar 7 dan 8.
Secara keseluruhan, terlihat dari Tabel 2 dan 3, bahwa bakteri target A.
hydrophylla cenderung sensitif terhadap senyawa ekstrak kasar spons Aaptos
aaptos dan Petrosia sp. Hal ini ditunjukkan oleh besar zona hambat yang
terbentuk dari semua sampel spons melebihi zona hambat yang dibentuk oleh
Ampisilin trihidrat (sebesar 2 mm). Sampel spons Aaptos aaptos dari semua
lokasi menunjukkan tingkat bioaktivitas dengan zona yang berkisar 2,3 – 4,5 mm,
sementara sampel Petrosia sp. membentuk zona hambat sebesar 1,2 – 4,8 mm.
Tabel 3 Bioaktivitas senyawa ekstrak kasar spons Petrosia sp. terhadap beberapa organisme target
• tanpa ulangan individu (hanya satu individu/ habitat)
0.0
Petrosia sp. E. coli
S.aureus
A. hydrophylla
Barat Selatan Transplan (Barat)
1 2 3 1 2 1 2 3
Gambar 7 Bioaktivitas antibakteri senyawa ekstrak kasar spons Petrosia sp. terhadap bakteri target.
Barat Pari Selatan Pari Transplan (Barat)
Gambar 8 Toksisitas spons Petrosia sp. terhadap Artemia salina.
Hasil pengujian semua sampel spons Aaptos aaptos dan Petrosia sp.
terhadap bakteri target (E. coli, S. aureus, A. hydrophylla) dan Artemia salina
menunjukkan bahwa tidak terlihat adanya hubungan tingkat bioaktivitas
antibakteri terhadap toksisitas senyawa ekstrak kasar pada kedua sampel. Ini
ditunjukkan dengan nilai P-value yang tidak signifikan (0,88 untuk E. coli, 0,33
untuk S. aureus, dan 0,14 untuk A. hydrophylla).
Hasil pengukuran parameter lingkungan menunjukkan bahwa kedua lokasi
pengambilan sampel (bagian Barat dan Selatan P. Pari) memiliki perbedaan
pengukuran COD yang menunjukkan perbedaan antara bagian Barat dan
Selatan P. Pari, yaitu 40 mg/l dan 12 mg/l air laut, sementara perairan yang tidak
tercemar biasanya memiliki nilai COD < 20 mg/l (Effendi 2003). Selain itu, lokasi
pengambilan sampel di bagian Barat P. Pari memiliki substrat yang cenderung
berlumpur dan berpasir, dengan sedikit karang. Sementara bagian Selatan P.
Pari memiliki substrat yang didominasi oleh karang (terumbu) dan arus yang
lebih kencang. Hal ini mempengaruhi faktor kecerahan lingkungan perairan di
masing-masing lokasi. Pengukuran parameter lingkungan yang lain tidak terlalu
jauh berbeda dan berada di bawah baku mutu kualitas lingkungan, kecuali untuk
parameter ammonia, fosfat, nitrat dan H2S yang berada di atas batas normal
perairan (Effendi 2003). Hasil pengukuran COD, ammonia, fosfat, nitrat dan H2S
(sulfida) mengindikasikan kedua perairan lokasi tersebut kemungkinan
mengalami kontaminasi limbah organik, atau merupakan perairan yang cukup
subur. Tabel 4 memperlihatkan hasil pengukuran parameter lingkungan di kedua
lokasi pengambilan sampel (bagian Barat dan Selatan P. Pari).
Tabel 4 Nilai parameter lingkungan di kedua lokasi pengambilan sampel beserta baku mutunya
LOKASI No PARAMETER Selatan P.