STABILISASI TEPUNG BEKATUL MELALUI METODE
PENGUKUSAN DAN PENGERINGAN RAK SERTA
PENDUGAAN UMUR SIMPANNYA
oleh :
Nova Dwi Swastika F34104041
2009
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
Nova Dwi Swastika. F34104041. Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak serta Pendugaan Umur Simpannya. Dibawah bimbingan Sugiarto dan Indah Yuliasih. 2009.
RINGKASAN
Bekatul merupakan hasil samping penggilingan padi. Menurut data BPS (2008) jumlah bekatul mencapai 4,8 juta ton. Bekatul dapat diolah menjadi berbagai produk, salah satunya adalah tepung bekatul. Tepung bekatul dapat digunakan sebagai bahan subtitusi roti, cookies, dan minuman berserat. Penurunan mutu bekatul dapat terjadi melalui proses hidrolisis dan oksidasi lemak. Permasalahan tersebut dapat diatasi melalui stabilisasi bekatul. Stabilisasi bekatul dapat dilakukan melalui pengukusan bahan dalam kurun waktu tertentu. Tujuan penelitian ini adalah mendapatkan kondisi stabilisasi dan pengeringan bekatul, karakteristik bekatul dan bekatul terstabilisasi, serta pendugaan umur simpannya.
Kondisi pengeringan bekatul segar yang konstan tercapai selama 4 jam dengan laju pengeringan sebesar 1 x 10-4 g/det hingga kadar airnya 5 %. Pengukusan bekatul dilakukan melalui 3 taraf waktu pengukusan yaitu 5, 10, dan 15 menit.
Tahap selanjutnya adalah karakterisasi bekatul dan bekatul terstabilisasi. Karakteristik bekatul segar meliputi kadar air 6,86 %, lemak 16,84 % (bk), abu 7,43 % (bk), protein 13,72 % (bk), serat 7,25 % (bk), karbohidrat by different 47,9 % (bk), dan TBA 0,68 mg malonaldehid/kg sampel, kelarutan 11,95 %, swelling power 5,96 %, sineresis 95,50 %, jumlah total koloni 1,65 x 106, dan tidak ditemukan koloni E. coli. Berdasarkan parameter uji kadar air, lemak, dan TBA terpilihlah bekatul dengan lama pengukusan 5 menit. Karakteristik bekatul terstabilisasi tersebut meliputi kadar air 5,61 %, lemak 14,23 % (bk), dan TBA 0,23 mg malonaldehid/kg sampel.
Bekatul terstabilisasi selama 5 menit digunakan sebagai sebagai bahan baku dalam penyimpanan dan pendugaan umur simpan. Produk dikemas dalam metalizzed dan disimpan pada suhu 35, 45, dan 50oC selama 8 minggu. Parameter mutu yang digunakan dalam penyimpanan bekatul terstabilisasi adalah kadar air, TBA, dan kecerahan warna. Selama penyimpanannya terjadi penurunan kadar air dan kecerahan warna, serta terjadi peningkatan nilai TBA.
Nova Dwi Swastika. F34104041. Bran Powder Stabilization through Steaming and Tray Dryer Method also Predicting the Shelf Life. Supervised by Sugiarto and Indah Yuliasih. 2009.
SUMMARY
Bran is side product from rice milling. According to BPS (2008), bran production reach at 4,8 million tons. Bran can be processed to be various product, one of them is bran powder. Bran powder can be used as brade substitution agent, cookies, and dietary drink. The decreasing of quality of bran can occure through hydroliytic and oxidation processes. The problem can be solved trough bran stabilization. It can be processed by steaming of the material in certain time. The purposes of this research are to get condition of stabilization and bran drying, bran characterization and stabilized bran, also to predict the packaging time.
Constant condition of drying of the fresh bran reached in 4 hours with the drying rate about 1 x 10-4 g/second untill the water level at 5 %. Steaming of the bran was carried out in 3 level of time; 5, 10, and 15 minutes.
The next step was characterizing the bran and stabilized bran. The characterization of fresh bran include water level 6,86 %, fat 16,84 % (db), ash 7,43 % (db), protein 13,72 % (db), crude fiber 7,25 % (db), carbohydrate by different 47,9 % (db), and TBA 0,68 mg malonaldehid/kg sample, solubility 11,95 %, swelling power 5,96 %, cyneresis 95,50 %, total colony number 1,65 x 106, and was not found E. Coli colony. Based on tested parameter water level, fat, and TBA were choosen bran with steaming at 5 minutes. The stabilized bran characterization include water level 5,61 %, fat 14,23 % (db), and TBA 0,23 mg malonaldehid/kg sample.
The bran that was stabilized at 5 minutes was used as the material to predict the storage and shelf life. The product packed in metalizzed and was storaged at tempeature 35, 45, and 50oC during 8 weeks. The quality parameter that was used in were water level, TBA, and brightness level. During the storage, it occured decreasing of water level and brightness level, also the increasing of TBA value.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
STABILISASI TEPUNG BEKATUL MELALUI METODE PENGUKUSAN DAN PENGERINGAN RAK SERTA
PENDUGAAN UMUR SIMPANNYA
SKRIPSI
Sebagai salah satu syarat memperoleh gelar Sarjana Teknologi Pertanian
pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
oleh :
Nova Dwi Swastika F34104041
Dilahirkan di Purworejo, 10 November 1986 Lulus : 4 Februari 2009
Disetujui, Maret 2009
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi yang berjudul
“Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak
serta Pendugaan Umur Simpannya”adalah karya asli saya dengan arahan dosen pembimbing dan rujukan literatur yang jelas.
Bogor, Maret 2009
Yang membuat pernyataan
i
RIWAYAT PENULIS
Penulis dilahirkan di Purworejo pada tanggal 10 November 1986. Menempuh pendidikan sekolah dasar di SD N Majir 2 dan lulus pada tahun 1998. Kemudian melanjutkan Sekolah Menengah Pertama di SLTP N 1 Kutoarjo pada tahun 1998 sampai 2001. Penulis menempuh pendidikan Sekolah Menengah Atas di SMA N 1 Purworejo selama 3 tahun yaitu pada tahun 2001- 2004. Pada tahun 2004 penulis diterima di Departemen Teknologi Industri Pertanian IPB melalui jalur Ujian Seleksi Masuk Mahasiswa (USMI).
Selama masa kuliah penulis aktif dalam organisasi Forum Bina Islami Fateta sebagai staf Pengembangan Sumber Daya Manusia selama 2 periode yaitu 2004/2005 dan 2005/2006. Pada tahun 2005 penulis tercatat sebagai staf departemen Pengabdian Masyarakat Badan Eksekutif Mahasiswa Fakultas Teknologi Pertanian (BEM FATETA) periode 2005/2006 dan periode 2006/2007 sebagai sekretaris departemen Kesejahteraan Mahasiswa. Tahun 2007 penulis melaksanakan Praktek Lapang di PT Garuda Food dengan judul “Mempelajari penambahan mesin filling terhadap efektifitas produksi”.
Selama menempuh studi di IPB, penulis pernah menjadi asisten praktikum matakuliah Teknologi Pengemasan, Distribusi, dan Transportasi (TPDT) pada semester 7, Teknik Penyimpanan dan Penggudangan (TPP) pada semester 8, dan Teknologi Pengendalian dan Pencemaran Industri (TPPI) pada semester 9.
Sebagai pelaksanaan tugas akhir, penulis melakukan penelitian berjudul
“Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak
ii
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT atas penyelesaian laporan skripsi. Skrispsi ini sebagai salah satu syarat mendapatkan gelar Sarjana Teknologi Pertanian pada Departemen Teknologi Industri Pertanian, Fakultas
Teknologi Pertanian, Institut Pertanian Bogor dengan judul “Stabilisasi Tepung
Bekatul melalui Metode Pengukusan dan Pengeringan Rak serta Pendugaan Umur
Simpannya”.
Penulis mengucapkan terimakasih kepada seluruh pihak yang telah membantu pelaksanaan, penelitian dan penyusunan laporan skripsi. Penulis mengucapkan terimakasih kepada :
1. Ir. Sugiarto, M.Si. sebagai dosen pembimbing I yang telah membimbing dan mengarahkan penulis hingga penyusunan skripsi.
2. Dr. Ir. Indah Yuliasih M.Si. sebagai dosen pembimbing II yang telah membantu, mengarahkan, dan memberikan informasi dalam penyelesaian skripsi ini.
3. Dr. Ir. M. Yani, M.Eng. sebagai dosen penguji yang telah mengarahkan dan memberikan masukan terhadap penyusunan skripsi ini.
4. Bapak, Ibu, dan keluarga yang telah memberikan doa, dukungan, dan kasih sayang kepada penulis.
5. Team Bekatul Menir atas kerjasama, dukungan, bantuan, dan perhatian selama proses penelitian dan penyusunan skrikpsi.
6. Laboran dan staf TIN yang telah membantu pelaksanaan penelitian, seminar, dan sidang skripsi.
7. Pak Tri Jauhari, Bu Cucun, dan Afifah crew yang telah menemani, mendukung, dan memberikan makna kekeluargaan.
8. Teman-teman TIN 41 untuk kebersamaan, persahabatan, dan kerjasamanya selama ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, namun penulis berharap laporan ini memberikan manfaat bagi pihak yang membutuhkan.
iii DAFTAR ISI
Halaman
RIWAYAT PENULIS... i
KATA PENGANTAR... ii
DAFTAR ISI... iii
DAFTAR TABEL... iv
DAFTAR GAMBAR... v
DAFTAR LAMPIRAN... vi
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. TUJUAN... 2
II. TINJAUAN PUSTAKA A. BEKATUL... 3
B. KETENGIKAN BEKATUL... 6
C. STABILISASI BEKATUL... 7
D. PENGERINGAN... 9
D. UMUR SIMPAN... 10
III. METODOLOGI A. BAHAN DAN ALAT... 12
B. METODE PENELITIAN... 12
IV. HASIL DAN PEMBAHASAN A. KONDISI PENGERINGAN... 17
B. KARAKTERISTIK BEKATUL DAN BEKATUL TERSTABILISASI... 20
C. PERUBAHAN MUTU SELAMA PENYIMPANAN... 26
D. PENDUGAAN UMUR SIMPAN PRODUK... 29
V. KESIMPULAN DAN SARAN ... 32
DAFTAR PUSTAKA………... 33
iv
DAFTAR TABEL
Halaman Tabel 1. Komposisi kimia bekatul pada kadar air 14 % ... 4 Tabel 2. Kadar air bekatul terstabilisasi setelah pengukusan dan
v
DAFTAR GAMBAR
Halaman
Gambar 1. Skema morfologi gabah kering (Champagne, 1994)... 3
Gambar 2. Skema proses penggilingan gabah kering (modifikasi Damardjati, 1983)...………...……. 4
Gambar 3. Mekanisme hidrolisis lemak menjadi gliserol dan asam lemak (Charley, 1983)... 6
Gambar 4. Kurva laju pengeringan dan kadar air selama pengeringan (McCabe, 1985)... 10
Gambar 5. Diagram alir pembuatan bekatul terstabilisasi... 14
Gambar 6. Laju pengeringan bekatul segar selama pengeringan... 17
Gambar 7. Hubungan kadar air bahan terhadap lama waktu pengeringan... 18
Gambar 8. Model perpindahan massa selama pengeringan (Himmelblau, 1986)... 19
Gambar 9. Hubungan antara suhu pemanasan dengan WRC... 24
Gambar 10. Hubungan antara suhu pemanasan dengan ORC... 25
Gambar 11. Hubungan antara lama penyimpanan (minggu) dengan kadar air produk (%)... 26
Gambar 12. Hubungan antara lama penyimpanan (minggu) dengan nilai TBA (mg malonaldehid/kg sampel)... 27
Gambar 13. Hubungan antara lama penyimpanan (minggu) dengan nilai kecerahan (L) produk... 28
Gambar 14. Regresi linear peningkatan nilai TBA bekatul terstabilisasi selama penyimpanan suhu 35, 45, dan 50oC... 29
STABILISASI TEPUNG BEKATUL MELALUI METODE
PENGUKUSAN DAN PENGERINGAN RAK SERTA
PENDUGAAN UMUR SIMPANNYA
oleh :
Nova Dwi Swastika F34104041
2009
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI PERTANIAN
Nova Dwi Swastika. F34104041. Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak serta Pendugaan Umur Simpannya. Dibawah bimbingan Sugiarto dan Indah Yuliasih. 2009.
RINGKASAN
Bekatul merupakan hasil samping penggilingan padi. Menurut data BPS (2008) jumlah bekatul mencapai 4,8 juta ton. Bekatul dapat diolah menjadi berbagai produk, salah satunya adalah tepung bekatul. Tepung bekatul dapat digunakan sebagai bahan subtitusi roti, cookies, dan minuman berserat. Penurunan mutu bekatul dapat terjadi melalui proses hidrolisis dan oksidasi lemak. Permasalahan tersebut dapat diatasi melalui stabilisasi bekatul. Stabilisasi bekatul dapat dilakukan melalui pengukusan bahan dalam kurun waktu tertentu. Tujuan penelitian ini adalah mendapatkan kondisi stabilisasi dan pengeringan bekatul, karakteristik bekatul dan bekatul terstabilisasi, serta pendugaan umur simpannya.
Kondisi pengeringan bekatul segar yang konstan tercapai selama 4 jam dengan laju pengeringan sebesar 1 x 10-4 g/det hingga kadar airnya 5 %. Pengukusan bekatul dilakukan melalui 3 taraf waktu pengukusan yaitu 5, 10, dan 15 menit.
Tahap selanjutnya adalah karakterisasi bekatul dan bekatul terstabilisasi. Karakteristik bekatul segar meliputi kadar air 6,86 %, lemak 16,84 % (bk), abu 7,43 % (bk), protein 13,72 % (bk), serat 7,25 % (bk), karbohidrat by different 47,9 % (bk), dan TBA 0,68 mg malonaldehid/kg sampel, kelarutan 11,95 %, swelling power 5,96 %, sineresis 95,50 %, jumlah total koloni 1,65 x 106, dan tidak ditemukan koloni E. coli. Berdasarkan parameter uji kadar air, lemak, dan TBA terpilihlah bekatul dengan lama pengukusan 5 menit. Karakteristik bekatul terstabilisasi tersebut meliputi kadar air 5,61 %, lemak 14,23 % (bk), dan TBA 0,23 mg malonaldehid/kg sampel.
Bekatul terstabilisasi selama 5 menit digunakan sebagai sebagai bahan baku dalam penyimpanan dan pendugaan umur simpan. Produk dikemas dalam metalizzed dan disimpan pada suhu 35, 45, dan 50oC selama 8 minggu. Parameter mutu yang digunakan dalam penyimpanan bekatul terstabilisasi adalah kadar air, TBA, dan kecerahan warna. Selama penyimpanannya terjadi penurunan kadar air dan kecerahan warna, serta terjadi peningkatan nilai TBA.
Nova Dwi Swastika. F34104041. Bran Powder Stabilization through Steaming and Tray Dryer Method also Predicting the Shelf Life. Supervised by Sugiarto and Indah Yuliasih. 2009.
SUMMARY
Bran is side product from rice milling. According to BPS (2008), bran production reach at 4,8 million tons. Bran can be processed to be various product, one of them is bran powder. Bran powder can be used as brade substitution agent, cookies, and dietary drink. The decreasing of quality of bran can occure through hydroliytic and oxidation processes. The problem can be solved trough bran stabilization. It can be processed by steaming of the material in certain time. The purposes of this research are to get condition of stabilization and bran drying, bran characterization and stabilized bran, also to predict the packaging time.
Constant condition of drying of the fresh bran reached in 4 hours with the drying rate about 1 x 10-4 g/second untill the water level at 5 %. Steaming of the bran was carried out in 3 level of time; 5, 10, and 15 minutes.
The next step was characterizing the bran and stabilized bran. The characterization of fresh bran include water level 6,86 %, fat 16,84 % (db), ash 7,43 % (db), protein 13,72 % (db), crude fiber 7,25 % (db), carbohydrate by different 47,9 % (db), and TBA 0,68 mg malonaldehid/kg sample, solubility 11,95 %, swelling power 5,96 %, cyneresis 95,50 %, total colony number 1,65 x 106, and was not found E. Coli colony. Based on tested parameter water level, fat, and TBA were choosen bran with steaming at 5 minutes. The stabilized bran characterization include water level 5,61 %, fat 14,23 % (db), and TBA 0,23 mg malonaldehid/kg sample.
The bran that was stabilized at 5 minutes was used as the material to predict the storage and shelf life. The product packed in metalizzed and was storaged at tempeature 35, 45, and 50oC during 8 weeks. The quality parameter that was used in were water level, TBA, and brightness level. During the storage, it occured decreasing of water level and brightness level, also the increasing of TBA value.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
STABILISASI TEPUNG BEKATUL MELALUI METODE PENGUKUSAN DAN PENGERINGAN RAK SERTA
PENDUGAAN UMUR SIMPANNYA
SKRIPSI
Sebagai salah satu syarat memperoleh gelar Sarjana Teknologi Pertanian
pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
oleh :
Nova Dwi Swastika F34104041
Dilahirkan di Purworejo, 10 November 1986 Lulus : 4 Februari 2009
Disetujui, Maret 2009
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi yang berjudul
“Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak
serta Pendugaan Umur Simpannya”adalah karya asli saya dengan arahan dosen pembimbing dan rujukan literatur yang jelas.
Bogor, Maret 2009
Yang membuat pernyataan
i
RIWAYAT PENULIS
Penulis dilahirkan di Purworejo pada tanggal 10 November 1986. Menempuh pendidikan sekolah dasar di SD N Majir 2 dan lulus pada tahun 1998. Kemudian melanjutkan Sekolah Menengah Pertama di SLTP N 1 Kutoarjo pada tahun 1998 sampai 2001. Penulis menempuh pendidikan Sekolah Menengah Atas di SMA N 1 Purworejo selama 3 tahun yaitu pada tahun 2001- 2004. Pada tahun 2004 penulis diterima di Departemen Teknologi Industri Pertanian IPB melalui jalur Ujian Seleksi Masuk Mahasiswa (USMI).
Selama masa kuliah penulis aktif dalam organisasi Forum Bina Islami Fateta sebagai staf Pengembangan Sumber Daya Manusia selama 2 periode yaitu 2004/2005 dan 2005/2006. Pada tahun 2005 penulis tercatat sebagai staf departemen Pengabdian Masyarakat Badan Eksekutif Mahasiswa Fakultas Teknologi Pertanian (BEM FATETA) periode 2005/2006 dan periode 2006/2007 sebagai sekretaris departemen Kesejahteraan Mahasiswa. Tahun 2007 penulis melaksanakan Praktek Lapang di PT Garuda Food dengan judul “Mempelajari penambahan mesin filling terhadap efektifitas produksi”.
Selama menempuh studi di IPB, penulis pernah menjadi asisten praktikum matakuliah Teknologi Pengemasan, Distribusi, dan Transportasi (TPDT) pada semester 7, Teknik Penyimpanan dan Penggudangan (TPP) pada semester 8, dan Teknologi Pengendalian dan Pencemaran Industri (TPPI) pada semester 9.
Sebagai pelaksanaan tugas akhir, penulis melakukan penelitian berjudul
“Stabilisasi Tepung Bekatul melalui Metode Pengukusan dan Pengeringan Rak
ii
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT atas penyelesaian laporan skripsi. Skrispsi ini sebagai salah satu syarat mendapatkan gelar Sarjana Teknologi Pertanian pada Departemen Teknologi Industri Pertanian, Fakultas
Teknologi Pertanian, Institut Pertanian Bogor dengan judul “Stabilisasi Tepung
Bekatul melalui Metode Pengukusan dan Pengeringan Rak serta Pendugaan Umur
Simpannya”.
Penulis mengucapkan terimakasih kepada seluruh pihak yang telah membantu pelaksanaan, penelitian dan penyusunan laporan skripsi. Penulis mengucapkan terimakasih kepada :
1. Ir. Sugiarto, M.Si. sebagai dosen pembimbing I yang telah membimbing dan mengarahkan penulis hingga penyusunan skripsi.
2. Dr. Ir. Indah Yuliasih M.Si. sebagai dosen pembimbing II yang telah membantu, mengarahkan, dan memberikan informasi dalam penyelesaian skripsi ini.
3. Dr. Ir. M. Yani, M.Eng. sebagai dosen penguji yang telah mengarahkan dan memberikan masukan terhadap penyusunan skripsi ini.
4. Bapak, Ibu, dan keluarga yang telah memberikan doa, dukungan, dan kasih sayang kepada penulis.
5. Team Bekatul Menir atas kerjasama, dukungan, bantuan, dan perhatian selama proses penelitian dan penyusunan skrikpsi.
6. Laboran dan staf TIN yang telah membantu pelaksanaan penelitian, seminar, dan sidang skripsi.
7. Pak Tri Jauhari, Bu Cucun, dan Afifah crew yang telah menemani, mendukung, dan memberikan makna kekeluargaan.
8. Teman-teman TIN 41 untuk kebersamaan, persahabatan, dan kerjasamanya selama ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, namun penulis berharap laporan ini memberikan manfaat bagi pihak yang membutuhkan.
iii DAFTAR ISI
Halaman
RIWAYAT PENULIS... i
KATA PENGANTAR... ii
DAFTAR ISI... iii
DAFTAR TABEL... iv
DAFTAR GAMBAR... v
DAFTAR LAMPIRAN... vi
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. TUJUAN... 2
II. TINJAUAN PUSTAKA A. BEKATUL... 3
B. KETENGIKAN BEKATUL... 6
C. STABILISASI BEKATUL... 7
D. PENGERINGAN... 9
D. UMUR SIMPAN... 10
III. METODOLOGI A. BAHAN DAN ALAT... 12
B. METODE PENELITIAN... 12
IV. HASIL DAN PEMBAHASAN A. KONDISI PENGERINGAN... 17
B. KARAKTERISTIK BEKATUL DAN BEKATUL TERSTABILISASI... 20
C. PERUBAHAN MUTU SELAMA PENYIMPANAN... 26
D. PENDUGAAN UMUR SIMPAN PRODUK... 29
V. KESIMPULAN DAN SARAN ... 32
DAFTAR PUSTAKA………... 33
iv
DAFTAR TABEL
Halaman Tabel 1. Komposisi kimia bekatul pada kadar air 14 % ... 4 Tabel 2. Kadar air bekatul terstabilisasi setelah pengukusan dan
v
DAFTAR GAMBAR
Halaman
Gambar 1. Skema morfologi gabah kering (Champagne, 1994)... 3
Gambar 2. Skema proses penggilingan gabah kering (modifikasi Damardjati, 1983)...………...……. 4
Gambar 3. Mekanisme hidrolisis lemak menjadi gliserol dan asam lemak (Charley, 1983)... 6
Gambar 4. Kurva laju pengeringan dan kadar air selama pengeringan (McCabe, 1985)... 10
Gambar 5. Diagram alir pembuatan bekatul terstabilisasi... 14
Gambar 6. Laju pengeringan bekatul segar selama pengeringan... 17
Gambar 7. Hubungan kadar air bahan terhadap lama waktu pengeringan... 18
Gambar 8. Model perpindahan massa selama pengeringan (Himmelblau, 1986)... 19
Gambar 9. Hubungan antara suhu pemanasan dengan WRC... 24
Gambar 10. Hubungan antara suhu pemanasan dengan ORC... 25
Gambar 11. Hubungan antara lama penyimpanan (minggu) dengan kadar air produk (%)... 26
Gambar 12. Hubungan antara lama penyimpanan (minggu) dengan nilai TBA (mg malonaldehid/kg sampel)... 27
Gambar 13. Hubungan antara lama penyimpanan (minggu) dengan nilai kecerahan (L) produk... 28
Gambar 14. Regresi linear peningkatan nilai TBA bekatul terstabilisasi selama penyimpanan suhu 35, 45, dan 50oC... 29
vi LAMPIRAN
Halaman
Lampiran 1. Prosedur analisa sifat fisikokimia dan mikrobiologi bekatul... 37
Lampiran 2. Prosedur analisa sifat fungsional bekatul... 41
Lampiran 3. Pengeringan bekatul segar selama 6 jam……... 43
Lampiran 4. Nilai WRC dan ORC bekatul dan bekatul terstabilisasi... 44
Lampiran 5. Analisis ragam (Anova)... 46
Lampiran 6. Uji lanjut Duncan... 47
1 I. PENDAHULUAN
A. LATAR BELAKANG
Bekatul merupakan hasil samping penggilingan padi. Jumlah bekatul melimpah dan belum termanfaatkan secara luas. Jumlah bekatul diperkirakan sebesar 4.822.391,76 ton (BPS, 2008). Selama ini pemanfaatan bekatul terbatas sebagai pakan ternak. Kondisi tersebut menyebabkan nilai jual bekatul menjadi rendah.
Bekatul mempunyai kandungan gizi dan bioktif yang dapat dimanfaatkan sebagai bahan pangan fungsional. Pangan fungsional merupakan produk pangan yang diharapkan memberikan pengaruh terhadap kesehatan. Kandungan biokatif bekatul seperti asam ferulat, fenol, dan oryzanol dalam bekatul mampu menurunkan tekanan darah dan kolesterol. Selain itu, kandungan serat pangan bekatul mampu mempercepat waktu singgah makanan dalam proses pencernaan (Luh, 1991).
Bekatul dapat diolah lebih lanjut menjadi tepung bekatul. Tepung bekatul dapat digunakan sebagai bahan substitusi tepung terigu dalam pembuatan roti, cookies, dan breakfast sereal. Tepung bekatul juga dapat dijadikan minuman kesehatan yang mampu menurunkan kolesterol darah.
Pemanfaatan bekatul sebagai bahan pangan terbatas karena sifatnya yang mudah tengik. Ketengikan bekatul disebabkan adannya interaksi antara lemak bekatul (15-19,7 %) dengan enzim lipase dan lipoksigenase yang secara alami terdapat dalam bekatul maupun kontaminasi mikroba. Permasalahan tersebut dapat diatasi melalui proses stabilisasi bekatul (Champagne, 1994).
Metode stabilisasi yang digunakan dalam penelitian ini adalah pemanasan basah. Pemanasan dianggap aman dalam mempertahankan kandungan gizi bahan dan mampu menginaktifkan enzim dan membunuh mikroba patogen. Selain itu, pengukusan merupakan cara yang mudah dan relatif murah (Kuswanto, 2003).
2 penyimpanan. Oleh karena itu, perlu adanya proses pengeringan untuk menurunkan kadar air bahan.
B. TUJUAN
3 II. TINJAUAN PUSTAKA
A. BEKATUL
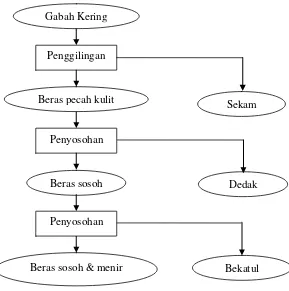
Bekatul merupakan hasil samping penggilingan beras. Bekatul terdiri atas lapisan pericarp, testa, dan lapisan aleurone. Selama peggilingan gabah kering dihasilkan sekam 20 %, 8 % bekatul, lembaga 2 %, dan beras sosoh 70 % (Orthoefer, 2001). Komponen penyusun gabah kering digambarkan sebagai berikut.
Gambar 1. Skema morfologi gabah kering (Champagne, 1994)
4 Gambar 2. Skema proses penggilingan gabah kering (modifikasi Damardjati,
1983)
5 Lemak bekatul tersusun atas asam lemak esensial seperti asam palmitat (asam lemak jenuh), serta oleat dan linoleat yang merupakan asam lemak tak jenuh. Karbohidrat penyusun bekatul adalah selulosa, hemiselulosa, dan pati dalam jumlah kecil (Champagne, 1994).
Bekatul mengandung komponen bioaktif yang bermanfaat bagi kesehatan. Komponen bioaktif tersebut adalah tokoferol (vitamin E), tokotrienol, oryzanol, dan asam pangamit. Tokoferol (vitamin E) berperan sebagai antioksidan dengan mencegah kerusakan dinding sel sehingga mampu mencegah hemolisis (kerapuhan) sel darah merah. Oryzanol merupakan fraksi tidak tersabunkan dari minyak bekatul yang dapat membantu sirkulasi darah dan memicu sekresi hormon (Kahlon et al., 1994).
Bekatul mempunyai sifat fungsional penurun kolesterol yang disebut efek hiperkolesterolemik. Mekanisme yang mendasari penurunan kolesterol adalah kemampuan serat diet menyerap lipid pada jalur gastrointestinal dan peningkatan ekskresi asam empedu (Kahlon et al., 1994). Selain itu, bekatul mampu menurunkan tekanan darah melalui penghambatan kerja enzim angiotensin i-converting enzyme (ACE), suatu enzim yang bertanggung jawab terhadap peningkatan tekanan darah (Ardiansyah, 2006).
Bekatul juga mengandung zat anti gizi dan enzim yang sangat merugikan. Zat anti gizi dapat menghambat metabolisme tubuh sedangkan keberadaan enzim menyebabkan ketengikan bekatul (Juliano, 1985). Menurut Luh (1991), zat anti gizi di dalam bekatul meliputi asam fitat, tripsin inhibitor, dan hemaglutinin. Zat anti gizi tersebut mempunyai aktivitas yang rendah dan dapat diinaktifkan melalui pemanasan.
6
B. KETENGIKAN BEKATUL
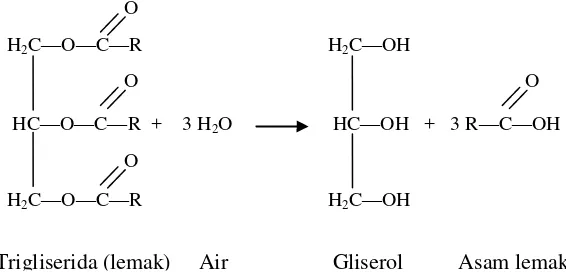
Menurut Champagne (1994), kandungan lemak bekatul yang tinggi (15-19,7 %) menjadi subyek kerusakan hidrolitik dan oksidatif. Kerusakan hidrolitik terjadi karena adanya air dalam bahan yang bereaksi dengan lemak bekatul. Mekanisme hidrolisis ditunjukkan seperti berikut.
Gambar 3. Mekanisme hidrolisis lemak menjadi gliserol dan asam lemak (Charley, 1982)
Kerusakan hidrolisis dan oksidatif dapat dipercepat oleh enzim lipase dan lipoksigenase yang secara alami terdapat dalam bekatul maupun dari aktivitas mikroba. Enzim lipase terletak pada lapisan testa sedangkan minyak bekatul terdapat pada lapisan aleuron dan endosperm (Champagne, 1994).
Aktivitas lipase berkaitan dengan suhu penyimpanan dan kelembaban. Pada suhu tinggi dan kondisi lembab, kandungan asam lemak bebas (FFA) meningkat 5-10 % per hari dan 70 % dalam sebulan. Aktivitas lipase mencapai optimal pada suhu 35-40oC. Suhu yang rendah dapat mengurangi aktivitas lipase. Aktivitas lipase tidak terjadi pada penyimpanan beku (Orthoefer, 2001).
Proses oksidasi dapat terjadi karena aktivitas enzimatik maupun non enzimatik. Oksidasi enzimatik terjadi akibat adanya enzim lipoksigenase, enzim yang ditemukan pada lapisan germ (embrio). Enzim lipoksigenase mengkatalis proses oksidasi asam lemak tak jenuh menjadi peroksida dengan bantuan radikal bebas dan oksigen. Peroksida merupakan senyawa yang labil dan akan terurai menjadi senyawa rantai karbon yang lebih pendek. Senyawa
7 karbon rantai pendek yang terbentuk meliputi asam lemak, aldehid, dan keton. Senyawa-senyawa tersebut bertanggung jawab dalam pembentukan off flavor tengik minyak bekatul (Charley, 1982).
Oksidasi nonenzimatik terjadi karena adanya radikal bebas (autooksidasi) dan fotooksidasi. Jalur radikal bebas tergantung pada molekul lemak yang berinteraksi dengan oksigen. Sedangkan jalur fotooksidasi terjadi melalui molekul fotosintesis (riboflavin, ion logam) yang menyerap cahaya. Oksigen hasil fotosintesis dapat bereaksi dengan asam lemak membentuk hidroperoksida (Champagne, 1994).
Kerusakan minyak bekatul dapat dideteksi melalui peningkatan nilai peroksida, penurunan nilai iodin, dan peningkatan nilai asam thiobarbiturat (Orthoefer, 2001). Nilai peroksida digunakan untuk mengetahui jumlah senyawa peroksida yang terbentuk, nilai iodin sebagai indikor seberapa banyak asam lemak tak jenuh yang telah terurai menjadi asam lemak bebas, dan asam thiobarbiturit sebagai indikator pembentukan aldehid hasil oksidasi lanjutan peroksida. Asam thiobarbiturat bereaksi dengan malonaldehid (senyawa aldehid) membentuk kromogen warna merah yang dapat ditentukan intensitas warnanya menggunakan spektrofotometer (Charley, 1982).
C. STABILISASI BEKATUL
Tujuan stabilisasi bekatul adalah membunuh mikroba dan mendestruksi enzim lipase. Untuk mendapatkan bekatul food grade dengan mutu tinggi, seluruh komponen penyebab kerusakan harus dihambat dan komponen kandungan bioaktifnya harus tetap dijaga (Champagne, 1994).
Metode stabilisasi dapat dilakukan dengan beberapa cara yaitu melalui pemanasan kering, pemanasan basah, pendinginan, modifikasi pH, dan perlakuan kimiawi (Orthoefer, 2001). Stabilisasi menggunakan panas kering dilakukan pada suhu 100-110oC. Beberapa metode yang termasuk dalam pemanasan kering adalah penyangraian, stationary dryer, dan fluid bed dryer (Sayre et al., 1982).
8 pada penyangraian tidak merata, kemungkinan terjadi kerusakan bahan, mikroba tidak terbasmi semuanya, dan enzim lipase tidak inaktif secara total (Juliano, 1985).
Drum berputar dan ekstrusi termasuk juga dalam metode pemanasan kering. Air yang terdapat dalam bahan digunakan sebagai media penghantar panas. Dalam pemanasan drum berputar, bekatul dipanaskan pada suhu 110-120oC selama 5 menit dengan tekanan 0,3-0,5 kg/cm. Pada proses ekstrusi, suhu pemasakan bekatul berkisar 130-140oC, densitas bekatul meningkat 0,3 %, dan kadar air menurun sebesar 5-8 % (Damardjati et al., 1990).
Proses pemanasan basah lebih efektif dibandingkan pemanasan kering. Inaktivasi enzim lipase dapat dilakukan pada suhu 100oC selama 3 menit. Pemanasan basah pada umumnya dilakukan dengan pengukusan selama 10-30 menit dilanjutkan dengan pengeringan bekatul hingga kadar air 3-12 % (Sayre et al., 1982).
Pemanasan basah dapat juga dilakukan dengan autoklaf. Autoklaf merupakan alat yang digunakan sebagai sterilisasi bahan. Mekanismenya melalui inaktivasi enzim dan membunuh mikroba pada suhu 121oC selama 15 menit. Pemanasan menggunakan autoklaf memberikan waktu pemanasan yang singkat dan lebih efektif membunuh mikroba dan menginaktivkan enzim, namun membutuhkan investasi yang mahal dan keterampilan yang tinggi (Winarno, 1992).
Metode stabilisasi yang lain adalah pendinginan, modifikasi pH, dan penambahan bahan kimia. Suhu rendah mampu mengurangi laju hidrolisis lipase. Modifikasi pH dilakukan pada nilai pH 4 yaitu dengan penambahan asam hidrokolik. Penggunakan bahan kimia dapat dilakukan dengan penambahan sodium metabisulfit. Ketiga metode ini jarang dilakukan dan tidak dikomersialkan (Orthoefer, 2001).
9
D. PENGERINGAN
Bekatul merupakan bahan yang bersifat higroskopis yaitu mudah menyerap maupun melepaskan air. Penyerapan air terjadi jika bekatul disimpan dalam ruangan dengan kelembaban tinggi, sedangkan penyimpanan pada kelembaban ruangan yang rendah menyebabkan bekatul kehilangan sejumlah air. Kondisi tersebut terus terjadi hingga bekatul mencapai kadar air kesetimbangan (Kuswanto, 2003).
Pengeringan merupakan penghilangan sejumlah air dari bahan melalui proses penguapan. Pengeringan melibatkan perpindahan panas dan massa secara bersamaan. Selama proses pengeringan, air dalam bahan akan dipindahkan ke permukaan bahan kemudian diuapkan jika RH (kelembaban) ruangan lebih rendah. Proses ini terjadi hingga keseimbangan kadar air bahan dengan RH lingkungannya tercapai (Kuswanto, 2003).
Kadar air bahan yang rendah dapat meningkatkan umur simpan bahan pangan. Jasad renik tidak dapat melakukan pembusukan dan pemecahan komponen bahan tanpa ketersediaan air yang cukup. Kadar air yang aman untuk penyimpanan bahan berkisar 13-14 %. Namun jika bahan disimpan dalam jangka waktu panjang, sebaiknya kadar air bahan barada dibawah 12 % (Singh, 2001).
10 Gambar 4. Kurva laju pengeringan dan kadar air selama pengeringan
(McCabe, 1985)
Selama proses pengeringan, kurva laju pengeringan akan membentuk garis linear yang menunjukkan penguapan air dalam bahan. Kurva laju pengeringan selanjutnya membentuk garis horizontal yang mengindikasikan bahwa laju pengeringan bahan telah konstan. Kondisi tersebut terjadi ketika suhu, kelembaban, dan kecepatan aliran udara yang melewati permukaan bahan dalam pengering tidak berubah. Pada waktu pengeringan tertentu, kurva laju pengeringan akan turun hingga nilainya 0. Kondisi tersebut tercapai ketika kadar air bahan sama dengan kandungan uap air dalam pengering (McCabe, 1985).
Bahan yang dikeringkan akan mengalami penurunan kadar air melalui mekanisme penguapan. Penurunan kadar air terus terjadi hingga kadar air bahan sama dengan kandungan uap air udara pengering. Setelah kondisi tersebut tercapai, kadar air bahan akan tetap. Kondisi ini ditunjukkan dengan garis horizontal pada kurva kadar air (McCabe, 1985).
E. UMUR SIMPAN
11 Floros (1993) menyatakan bahwa umur simpan produk dapat diduga melalui 2 metode yaitu Extended Storages Studies (ESS) dan Accelarated Storage Studies (ASS). ESS sering disebut sebagai metode konvensional yaitu penentuan masa kadaluarsa dengan menyimpan suatu produk pada kondisi normal.
Labuza (1982) menyatakan bahwa penilaian umur simpan dapat dilakukan pada kondisi dipercepat (accelerated shelf life test) yang mampu memprediksi umur simpan produk. Metode ini dilakukan dengan mengkondisikan bahan pangan pada suhu dan kelembaban relatif tinggi Penentuan umur simpan metode Arrhenius termasuk kedalam metode akselerasi ini.
Metode Arrhenius merupakan metode simulasi dalam menduga umur simpan produk. Penurunan mutu dengan metode simulasi memerlukan beberapa pengamatan yaitu adanya parameter kuantitatif. Parameter tersebut harus dapat mencerminkan keadaan mutu yang terjadi pada kondisi penyimpanan (Syarif dan Halid, 1993).
Syarif dan Halid (1993) menyatakan bahwa suhu merupakan faktor yang sangat berpengaruh terhadap perubahan mutu pangan. Suhu ruangan yang konstan akan lebih baik dari suhu penyimpanan yang berubah-ubah. Pendugaan laju penurunan mutu dapat dilakukan dengan persamaan Arrhenius berikut:
k = ko e -E/RT Keterangan:
k = konstanta penurunan mutu
ko = konstanta (tidak tergantung suhu) E = energi aktivasi
T = suhu mutlak (Kelvin)
12 III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan utama yang digunakan adalah bekatul varietas campuran Ciherang dan IR 64 yang diperoleh dari desa Cibatok, Ciampea, Bogor. Bahan pendukung yang digunakan untuk analisis adalah H2SO4 pekat (36 N), H2SO4 0,02 N, H2SO4 0,325 N, NaOH 1,25 N, HCl 4 M, indikator Mengsel, pereaksi TBA, minyak goreng, heksan, alkohol, aquades, garam fisiologis, agar PCA (Plate Count Agar), dan agar EMB (Eosine Methylene Blue).
Alat-alat yang digunakan meliputi kertas saring, batu didih, cawan porselin, cawan petri, mikrometer pipet, tip, oven, neraca analitik, desikator, penangas, tanur listrik, labu kjeldahl, soxhlet, autoklaf, freezer, quebec colony counter, colormeter, pipet, tabung ulir, tabung reaksi, labu erlenmeyer, labu ukur, gelas piala, gelas ukur, termometer, sudip, dan pengaduk.
B. METODE PENELITIAN
Penelitian ini dibagi menjadi beberapa tahap yaitu penentuan waktu pengeringan bekatul segar, karakterisasi bekatul segar, stabilisasi dan pengeringan bekatul, karakterisasi bekatul terstabilisasi, serta penyimpanan dan pendugaan umur simpan bekatul terstabilisasi dengan metode Arrhenius. 1. Penentuan waktu pengeringan bekatul segar
Bekatul sebagai bahan baku utama dalam penelitian ini mengandung lemak yang tinggi (15-19,7 %). Kandungan lemak yang tinggi dapat menyebabkan penurunan mutu produk berupa ketengikan. Ketengikan disebabkan oleh proses hidrolisis dan oksidasi lemak dalam bekatul. Keberadaan air yang berlebih dalam bahan menjadi faktor pemicu proses hidrolisis lemak. Oleh karena itu, perlu adanya proses pengeringan untuk mengurangi kadar air bahan.
13 bekatul. Pengeringan bekatul segar dilakukan selama 6 jam dengan selang waktu pengamatan setiap 30 menit.
2. Karakterisasi bekatul segar
Karakterisasi bekatul segar meliputi analisis fisikokimia dan fungsional. Analisis fisikokimia meliputi: kadar air, abu, protein, lemak, serat kasar, karbohidrat, TBA (Thiobarbituric Acid), dan warna. Analisis fungsional yang dilakukan adalah kelarutan dan swelling power, freeze thaw stability, water retention capacity (WRC), dan oil retention capacity (ORC). Pengujian mikroba juga dilakukan untuk mengetahui mikroba yang tumbuh pada bahan. Pengujian mikroba meliputi total mikroba metode TPC (Total Plate Count) dan uji bakteri Escherichia coli.
3. Stabilisasi dan pengeringan bekatul
Pembuatan tepung bekatul melalui 2 tahap yaitu pengukusan dan pengeringan produk. Pengukusan bertujuan untuk menginaktivasi enzim dan membunuh mikroba penyebab ketengikan lemak sedangkan pengeringan bertujuan untuk mengurangi kadar air produk sehingga umur simpannya menjadi lebih lama.
Waktu pengukusan yang digunakan terdiri atas 3 taraf perlakuan waktu yaitu 5, 10, dan 15 menit. Bahan dikukus dalam pengukus yang berdiameter 30 cm dengan tebal lapisan bahan + 1 cm. Bahan kemudian dikeringkan dalam tray dryer dengan loyang berukuran 26,5 x 26,5 cm dengan ketebalan + 1 cm. Lama waktu pengeringan tepung bekatul diperoleh dari pengeringan bekatul segar pada Tahap 1.
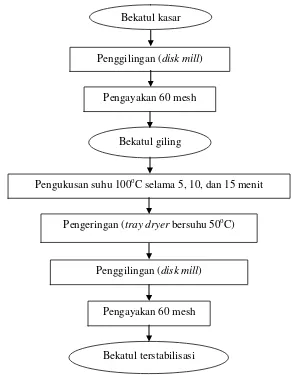
14 saringan 60 mesh. Diagram alir pembuatan tepung bekatul disajikan pada gambar berikut.
Gambar 5. Diagram alir pembuatan bekatul terstabilisasi
4. Karakterisasi bekatul terstabilisasi
Analisis yang dilakukan pada bekatul terstabilisasi meliputi fisiko kimia dan fungsional serta pengujian mikroba seperti halnya pada karakterisasi bekatul segar, yaitu kadar air, abu, protein, lemak, serat kasar, karbohidrat, TBA, warna, TPC, dan uji bakteri E. coli. Analisis fungsional yang dilakukan adalah kelarutan dan swelling power, freeze thaw stability, WRC, dan ORC.
Penggilingan (disk mill)
Pengayakan 60 mesh
Bekatul terstabilisasi Bekatul kasar
Penggilingan (disk mill)
Pengayakan 60 mesh
Pengukusan suhu 100oC selama 5, 10, dan 15 menit Bekatul giling
15 Produk dengan waktu pengukusan 5, 10, 15 menit kemudian dianalis secara statistik menggunakan analisis ragam (Anova). Uji lanjut Duncan digunakan untuk menganalisis hipotesis data yang berpengaruh nyata. Produk dengan waktu pengukusan terpilih akan diproduksi dan digunakan sebagai bahan baku pendugaan umur simpan dengan metode Arrhenius.
5. Penyimpanan dan pendugaan umur simpan bekatul terstabilisasi dengan metode Arrhenius
Selama penyimpanan produk dikemas dalam kemasan metallized yaitu campuran alumunium foil dengan plastik LDPE. Bobot bahan setiap kemasan sebesar 40 gram. Produk disimpan dalam suhu 35, 45, dan 55oC selama 2 bulan. Pengamatan dilakukan setiap satu minggu sekali.
Parameter uji yang dilakukan setiap minggunya adalah kadar air, TBA, dan warna. Pengujian yang dilakukan pada awal penyimpanan dan akhir penyimpanan adalah kadar air, TBA, warna, dan uji mikroba yang meliputi pengujian total mikroba (TPC) dan jumlah koloni E. coli.
16 Nilai regresi yang diperoleh dalam kurva hubungan 1/T dan ln k, digunakan untuk menentukan nilai konstanta penurunan mutu produk. Nilai konstanta penurunan mutu tersebut ditunjukkan seperti berikut.
k = ko.e –E/RT
Nilai ko menunjukkan konstanta penurunan mutu yang tidak tergantung pada suhu yang diperoleh dari ln nilai intersep persamaan regresi. Nilai k menyatakan konstanta penurunan mutu pada suhu penyimpanan tertentu, sedangkan E/R merupakan gradien yang diperoleh dari nilai regresi. Selanjutnya umur simpan produk dihitung berdasarkan persamaan berikut:
t = [Ao– At] k
Keterangan:
t = pendugaan waktu umur simpan produk Ao = nilai mutu awal produk
17 IV. HASIL DAN PEMBAHASAN
A. KONDISI PENGERINGAN
Pengeringan melibatkan pindah panas dan massa. Suhu pengeringan yang digunakan adalah 50oC. Pengeringan dibawah suhu 70oC dianjurkan untuk menghindari kerusakan nutrisi bahan terutama protein dan vitamin. Denaturasi protein terjadi pada suhu diatas 50oC (Singh, 2001). Denaturasi merupakan proses perubahan struktur molekul protein tanpa terjadinya pemecahan ikatan kovalen (Winarno, 1992).
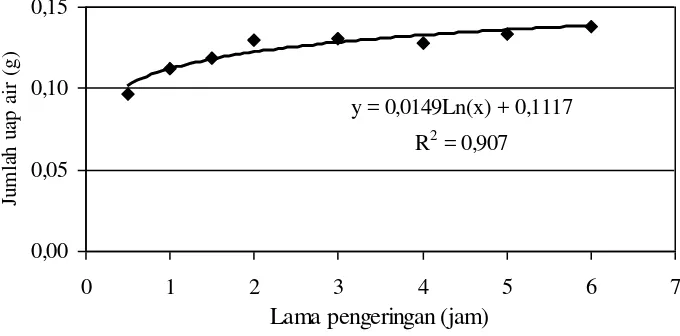
Sejumlah air yang terdapat dalam suatu bahan akan menguap selama pengeringan berlangsung. Banyaknya air yang menguap setiap waktunya menunjukkan besarnya laju pengeringan. Laju pengeringan bekatul segar ditunjukkan sebagai gambar berikut.
Gambar 6. Laju pengeringan bekatul segar selama pengeringan
Berdasarkan grafik diatas, penguapan air mulai konstan setelah 3 jam pengeringan. Kondisi tersebut menunjukkan laju pengeringan yang konstan telah tercapai. Menurut McCabe (1985), laju pengeringan konstan terjadi jika kecepatan penguapan air dari dalam bahan sama dengan kecepatan aliran panas udara pengering yang melalui permukaan bahan.
18
Penentuan lama waktu pengeringan bekatul berdasarkan pada laju pengeringan yang konstan dan kadar air yang diharapkan sebesar 5 %. Laju pengeringan yang konstan (Gambar 6) terjadi setelah 3 jam pengeringan sedangkan kadar air 5 % (Gambar 7) tercapai setelah 4 jam pengeringan. Oleh karena itu, lama waktu pengeringan bekatul yang digunakan adalah 4 jam.
Untuk mengetahui perubahan kadar air bekatul setelah pengukusan dan pengeringan, dilakukan pengujian kadar air pada kedua proses tersebut. Berikut disajikan kadar air bekatul terstabiliasi setelah pengukusan dan pengeringan pada setiap taraf waktu perlakuan pengukusan.
19 Setelah proses pengukusan, bekatul kemudian dikeringkan untuk menurunkan kadar air yang terserap selama pengukusan. Kadar air yang rendah bertujuan untuk menghambat proses hidrolisis lemak bekatul dan pertumbuhan mikroorganisme. Selama pengeringan bekatul, terjadi perpindahan massa dari bahan ke pengering. Berikut ini model perpindahan massa selama pengeringan.
Umpan = Produk + Uap air
Gambar 8. Model perpindahan massa selama pengeringan (Himmelblau, 1996)
Perhitungan banyaknya uap air bahan yang hilang selama pengeringan dan laju pengeringan bahan seperti pada pengukusan bekatul selama 5 menit berikut.
203,48 g 194,26 g Jumlah uap air selama 4 jam = 203,48 - 194,26 = 9,22 g
Laju pengeringan = 9,22 g/4 jam = 6,41 x 10-4 g/detik
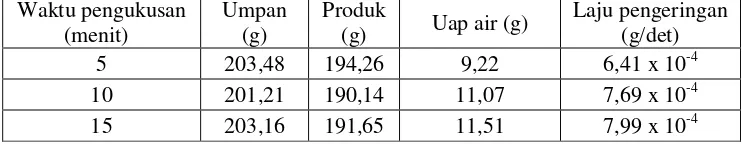
Hasil perhitungan laju pengeringan ketiga produk pengukusan ditampilkan pada tabel berikut.
20 Laju pengeringan bekatul segar selama 4 jam pengeringan sebesar 10-4 g/det. Berdasarkan laju pengeringan produk (Tabel 3), laju pengeringan terbesar ditunjukkan oleh pengukusan produk selama 15 menit yaitu 7,99 x 10-4 g/det. Perlakuan pengukusan bahan menyebabkan kenaikan laju pengeringan. Hal ini disebabkan oleh kandungan air yang berbeda pada bekatul segar dan bekatul terstabiliasi. Pengukusan menyebabkan peningkatan penyerapan uap air ke dalam bahan sehingga air yang diuapkan selama pengeringan meningkat dan laju pengeringan bahan pun menjadi lebih besar.
B. KARAKTERISTIK BEKATUL DAN BEKATUL TERSTABILISASI
Analisis yang dilakukan dalam karakterisasi bekatul dan bekatul terstabiliasi meliputi analisis fisikokimia, fungsional, dan mikrobiologi. Analisis tersebut digunakan untuk mengetahui perubahan yang terjadi selama stabilisasi dan pengeringan bekatul.
Hasil analisis sifat fisikokimia bekatul dan bekatul terstabiliasi secara rinci disajikan pada Tabel 4.
Tabel 4. Sifat fisikokimia bekatul dan bekatul terstabilisasi
21 Pengukusan dapat menarik sebagian udara dalam jaringan sehingga tekanan turgor sel berkurang. Hal ini menyebabkan jaringan bahan menjadi lunak. Penarikan udara akan mendegradasi sebagian dinding sel sehingga jaringan menjadi porous. Selama proses pengukusan, uap air pengukus terserap oleh bahan. Semakin lama bahan dikukus maka penyerapan uap air oleh bahan semakin meningkat.
Produk yang dikukus dapat menyerap air yang berasal dari uap air pengukus. Air tersebut harus dihilangkan untuk mencegah terjadinya hidrolisis lemak maupun pertumbuhan mikroorganisme. Pengeringan menyebabkan penurunan kadar air tepung bekatul. Nilai kadar air produk yang dikukus selama 5 menit 5,61 %, 10 menit 5,48 %, dan 15 menit 5,72 %.
Kadar protein bekatul segar sebesar 13,72 % (bk). Nilai tersebut lebih besar dari standar yaitu min 8 %. Metode protein kasar dalam perhitungan diperoleh dari semua nilia N (nitrogen) baik N penyusun protein maupun non protein. Kadar protein yang tinggi diduga berasal dari kontaminasi beras sosoh dan lembaga selama penggilingan dan terhitungnya nilai N non protein. Menurut Luh (1980), komponen N non protein yang terdapat dalam bekatul adalah guanin, adenin, xanthin, dan hipoxantihin.
Nilai protein bekatul terstabilisasi mengalami penurunan karena sebagian komponen protein diduga larut selama pengukusan. Menurut Luh (1980), komponen utama protein bekatul adalah albumin dan globulin. Albumin merupakan fraksi larut air dan globulin merupakan fraksi yang tidak larut air.
22 Abu merupakan bahan anorganik (mineral) dalam suatu bahan. Kadar abu bekatul yang dihasilkan dalam pengujian sebesar 7,43 % (bk) sedangkan nilai kadar abu produk berkisar antara 7,76-7,99 % (bk). Kandungan abu dalam bekatul tergantung pada kondisi tanah, lingkungan tumbuh, varietas padi, dan proses penggilingan. Pemanasan dapat membakar atau menghilangkan unsur organik bahan sedangkan kandungan mineralnya akan tetap. Oleh karena itu, proses pengukusan dan pengeringan bekatul tidak penurunan kadar serat. Pengukusan produk menyebabkan jaringan dinding sel menjadi lunak dan terlarut dalam air selama pengukusan sehingga kadar serat produk mengalami penurunan.
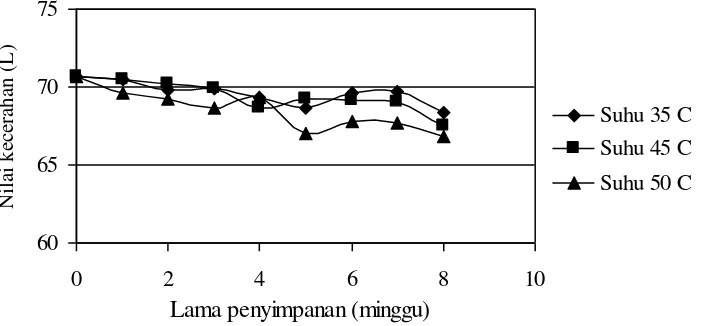
Warna merupakan parameter mutu yang dapat diamati secara langsung. Pengujian warna dilakukan menggunakan alat colormeter. Nilai kecerahan warna bekatul segar sebesar 71,70. Nilai kecerahan produk berkisar antara 64,94-65,48. Namun jika nilai kecerahan antar produk dibandingkan, maka produk yang dikukus selama 15 menit mempunyai tingkat kecerahan yang lebih tinggi dibandingkan pengukusan produk 5 dan 10 menit. Produk yang dikukus selama 15 menit memiliki kadar air terbesar yaitu 5,72 % (bb). Pengikatan air selama pengukusan menyebabkan warna bahan menjadi lebih mengkilab sehingga tingkat kecerahannya pun meningkat. Semakin banyak air yang terserap selama pengukusan maka nilai kecerahan bekatul semakin besar.
23 kandungan airnya yang rendah serta aktivitas enzim menurun karena adanya proses pengukusan bahan.
Selain analisis sifat fisikomia, dilakukan pula analisis sifat fungsional dan mikrobiologi bekatul dan bekatul terstabilisasi. Hasil pengujian tersebut disajikan pada Tabel 5.
Tabel 5. Sifat fungsional dan mikrobiologi bekatul dan bekatul terstabilisasi
Parameter Bekatul Bekatul terstabilisasi
5’ 10’ 15’ menunjukkan kemampuan bahan melarut dalam suatu pelarut. Nilai kelarutan yang kecil menunjukkan bahwa bekatul sulit larut dalam air. Proses stabilisasi melalui metode pengukusan dapat meningkatkan kelarutan bekatul. Nilai kelarutan produk yang telah dikukus berkisar antara 18,73-21,21 %. Pengukusan menyebabkan jaringan bahan mengalami kerusakan sehingga sebagian komponen bahan yang larut air keluar dari jaringan. Komponen yang berperan dalam kelarutan diduga berasal dari serat dan amilosa. Amilosa merupakan komponen pati yang larut dalam air. Menurut Luh (1980), selama penyosohan beras pecah kulit, sebagian pati yang berasal dari endosperm dan germ terikut dalam bekatul.
Swelling power merupakan kemampuan bahan untuk mengembang.
24 Freeze thaw stability merupakan stabilitas bahan untuk disimpan dalam kondisi beku dan dinyatakan sebagai % sineresis. Sineresis merupakan proses keluarnya air dari jaringan bahan setelah bahan diletakkan pada suhu ruang (25-30oC). Nilai pengujian bekatul segar sebesar 95,50 %. Penurunan nilai % sineresis produk (90,58-93,92 %) menunjukkan perbaikan sifat fungsional bekatul dalam mengikat air. Pengukusan pada dasarnya membuat jaringan menjadi porous sehingga air lebih banyak terikat oleh jaringan.
Nilai WRC (Water Retention Capacity) menunjukkan kemampuan bahan menyerap dan menahan air. Serat berperan penting dalam pengikatan air. Lama pengukusan menyebabkan kerusakan jaringan bahan sehingga pengikatan air meningkat. Nilai WRC disajikan pada gambar berikut.
Hasil pengujian menunjukkan peningkatan nilai WRC seiring dengan kenaikan suhu pemanasan. Pemanasan menyebabkan peningkatan energi kinetik air sehingga pengikatan air terhadap serat bekatul meningkat. Pengukusan menyebabkan komponen serat menjadi porous sehingga pengikatan air menjadi lebih besar. Mekanisme pengikatan air terjadi melalui ikatan hidrogen yang menghubungkan gugus hidroksil serat bekatul dan ion hidrogen dalam molekul air. Nilai WRC secara lengkap disajikan pada Lampiran 4.
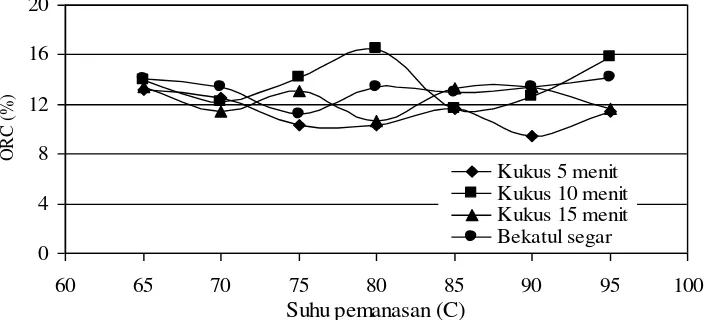
25 dilakukan oleh komponen serat bekatul. Pengujian dilakukan pada suhu pemanasan 65-95oC. Hasil pengujian ORC disajikan pada gambar berikut.
0
Gambar 10 menunjukkan bahwa pengikatan minyak oleh bekatul dan bekatul terstabilisasi relatif stabil pada setiap suhu pemanasan. Pengukusan mampu meningkatkan keporousan serat. Rongga serat yang porous dapat diisi oleh kompenen lain dari bahan yang dicampurkan ke dalam bekatul. Namun demikian, kemampuan serat mengikat minyak terbatas karena panjangnya rantai karbon minyak.
Uji total mikroorganisme menggunakan metode TPC (Total Plate Count) dilakukan untuk mengetahui jumlah mikroorganisme yang tumbuh secara keseluruhan (bakteri, kapang, maupun khamir). Hasil pengujian TPC menunjukkan nilai total mikroorganisme yang melebihi batas maksimal SNI 01-3549-1994 (mak 106) sedangkan produk pengukusan tidak menunjukkan adanya koloni. Tingginya jumlah mikroba dalam bahan dapat disebabkan oleh mikroba yang secara alami terdapat dalam bekatul maupun kontaminasi saat pengujian. Dengan adanya proses pengukusan akitivitas mikroorganisme dapat dihilangkan.
26 dapat dilakukan dengan penurunan kadar air bahan dan pengaturan oksigen melalui penggunaan kemasan.
C. PERUBAHAN MUTU SELAMA PENYIMPANAN
Pemilihan produk sebagai bahan baku penyimpanan berdasarkan pada tiga parameter uji yaitu kadar air, TBA, dan lemak. Produk yang dikukus selama 5 menit menjadi produk terpilih dengan kandungan air 5,61 %, TBA sebesar 0,23 mg malonaldehid/kg sampel, dan lemak 14,23 % (bk). Kandungan air yang rendah diperlukan selama penyimpanan untuk mencegah proses hidrolisis lemak. Nilai TBA sebagai indikator ketengikan minyak berguna untuk mengetahui efektivitas pemanasan terhadap proses stabilisasi enzim lipase. Penurunan nilai kadar lemak menunjukkan perubahan lemak menjadi asam lemak bebas yang selanjutnya teroksidasi membentuk senyawa aldehid yang berbau tengik.
Parameter uji yang digunakan dalam perubahan mutu selama penyimpanan adalah kadar air, TBA, dan kecerahan warna. Kadar air dan TBA merupakan parameter kimiawi yang berhubungan dengan ketengikan lemak bekatul, sedangkan kecerahan warna sebagai parameter fisik suatu bahan diterima atau ditolak konsumen.
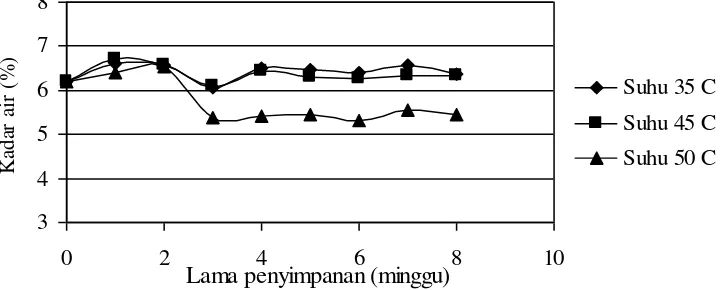
Perubahan kadar air bekatul pada ketiga suhu penyimpanan (35, 45, dan 50oC) selama 6 minggu penyimpanan disajikan pada gambar berikut.
3
27 Kadar air produk selama penyimpanan mengalami penurunan, terutama produk yang disimpan pada suhu 50oC. Kelembaban inkubator yang rendah, terjadinya permeabilitas kemasan, dan sifat bekatul yang higroskopis diduga menyebabkan penurunan kadar air produk.
Inkubator yang digunakan dalam penelitian tidak dilengkapi saluran udara masuk (inlet). Pemanasan menyebabkan ruang inkubator menjadi jenuh. Udara jenuh dalam inkubator dikeluarkan melalui saluran pembuangan (outlet) sehingga kelembaban ruang inkubator menjadi rendah. Hasil pengukuran kelembaban ruang inkubator pada suhu penyimpanan 35oC sebesar 12 %, suhu 45oC sebesar 7 %, dan 5 % pada inkubator suhu 50oC. Perpindahan uap air dari bahan menuju inkubator terus terjadi hingga kadar air bahan sama dengan uap air inkubator. Sifat higroskopis bekatul berperan dalam pelepasan uap air bahan. Selain itu, perpindahan air dalam bahan dipengaruhi oleh permeabilitas kemasan. Menurut Setyowati et al. (2000), peningkatan suhu penyimpanan menyebabkan permeabilitas kemasan semakin besar sehingga uap air produk dapat berdifusi keluar kemasan.
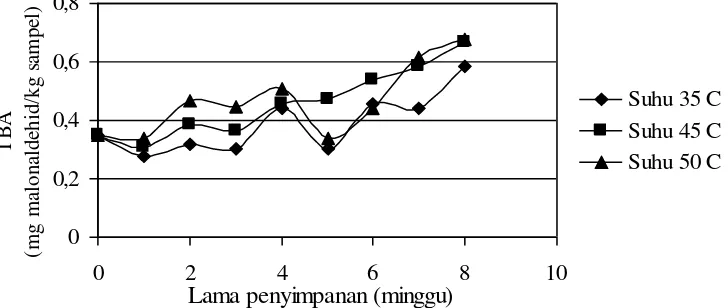
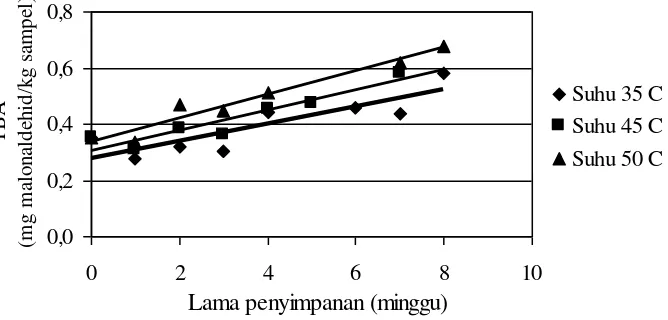
TBA merupakan indikator pembentukan aldehid hasil okidasi lanjutan peroksida dan hidroperoksida. Hasil pengujian TBA selama penyimpanan disajikan pada gambar berikut.
Gambar 12. Hubungan antara lama penyimpanan (minggu) dengan nilai TBA (mg malonaldehid/kg sampel)
28 Peningkatan suhu menyebabkan permeabilitas kemasan meningkat sehingga oksigen dari inkubator masuk ke dalam kemasan.
Warna merupakan indikator kerusakan produk pangan. Melalui penampakan warna, produk pangan dapat dideteksi perubahan mutunya. Kecerahan produk selama penyimpanan disajikan pada gambar berikut.
60
Gambar 13. Hubungan antara lama penyimpanan (minggu) dengan nilai kecerahan (L) produk
29
D. PENDUGAAN UMUR SIMPAN PRODUK
Selama proses penyimpanan, nilai kadar air dan kecerahan warna mengalami penurunan sedangkan nilai TBA mengalami kenaikan. TBA merupakan indikator keberhasilan stabilisasi enzim lipase. Oleh karena itu, TBA digunakan sebagai parameter kritis dalam pendugaan umur simpan.
Pendugaan umur simpan dibuat dengan menghubungkan waktu penyimpanan dengan nilai TBA masing-masing suhu penyimpanan (35, 45, dan 50oC). Grafik hubungan antara waktu penyimpanan (minggu) sebagai absis dan kenaikan nilai TBA sebagai ordinat disajikan pada Gambar 12. Langkah selanjutnya adalah membuat analisis regresi linear dari masing masing suhu penyimpanan seperti gambar berikut.
0,0
Gambar 14. Regresi linear peningkatan nilai TBA bekatul terstabilisasi selama penyimpanan suhu 35, 45, dan 50oC
Berdasarkan Gambar 14 diperoleh persamaan linear peningkatan nilai TBA pada setiap suhu penyimpanan sebagai berikut.
Suhu 35oC y = 0,00416 x + 0,2414 R2 = 0,9597 Suhu 45oC y = 0,0427 x + 0,2793 R2 = 0,979 Suhu 50oC y = 0,0427 x + 0,3315 R2 = 0,9416
30
Nilai kemiringan garis tersebut merupakan nilai –E/R dari persamaan Arrhenius. Besarnya energi aktivasi dari bekatul terstabilisasi adalah sebagai berikut.
-E/R = -176 K
R = 1,986 kal /mol K E = 88,45 kal/mol
Nilai intersep garis merupakan nilai ln ko dari persamaan Arrhenius, sehingga diperoleh nilai ko sebagai berikut.
ln ko = -2,6 ko = 0,074
Berdasarkan nilai E/R dan ko yang telah diperoleh, maka persamaan Arrhenius dapat disusun sebagai berikut.
k = ko e –E/RT k = 0,074 e -176 (1/T)
31 15oC atau 288 K k = 0,074 e -176 (1/288)
k = 0,0342
25oC atau 298 K k = 0,074 e -176 (1/298) k = 0,0409
30oC atau 303 K k = 0,074 e -176 (1/303) k = 0,0413
Setelah didapatkan nilai laju peningkatan TBA, maka dapat diduga umur simpan produk pada masing-masing suhu berdasarkan persamaan berikut.
Umur simpan = nilai kritis TBA – nilai TBA awal Laju peningkatan TBA
Titik kritis yang digunakan dalam pendugaan umur simpan produk ditentukan berdasarkan pengujian organoleptik ketika produk mulai ditolak panelis. Besarnya titik kritis yang diperoleh adalah 0,51 mg malonaldehid/kg sampel. Titik kritis tersebut tercapai pada bahan yang disimpan dalam inkubator suhu 50oC selama 4 minggu. Pendugaan umur simpan bekatul terstabilisasi pada beberapa suhu penyimpanan adalah sebagai berikut.
32 V. KESIMPULAN DAN SARAN
A. KESIMPULAN
Lama pengeringan yang digunakan untuk mengeringkan bekatul segar adalah 4 jam dengan laju pengeringan 1 x 10-4 g/det hingga kadar air 5 %. Lama waktu pengeringan tersebut digunakan sebagai dasar waktu pengeringan bekatul terstabilisasi.
Karakteristik bekatul segar meliputi kadar air 6,86 %, lemak 16,84 % (bk), abu 7,43 % (bk), protein 13,72 % (bk), serat kasar 7,25 % (bk), karbohidrat by different 47,9 % (bk), dan TBA 0,68 mg malonaldehid/kg sampel, kelarutan 11,95 %, swelling power 5,96 %, sineresis 95,50 %, jumlah total koloni 1,65 x 106, dan tidak ditemukan koloni E. coli. Berdasarkan parameter uji kadar air, lemak, dan TBA terpilihlah bekatul dengan lama pengukusan 5 menit. Karakteristik bekatul terstabilisasi tersebut memiliki kadar air 5,61 %, lemak 14,23 % (bk), dan TBA 0,23 mg malonaldehid/kg sampel.
Parameter mutu yang digunakan dalam penyimpanan bekatul terstabilisasi adalah kadar air, TBA, dan kecerahan warna. Selama penyimpanannya terjadi penurunan kadar air dan kecerahan warna, serta terjadi peningkatan nilai TBA.
Parameter mutu kritis yang digunakan dalam pendugaan umur simpan bekatul terstabilisasi adalah nilai TBA (Thiobarbituric Acid). Nilai titik kritis yang digunakan sebesar 0,51 mg malonaldehid/kg sampel. Persamaan Arrhenius bekatul terstabilisasi yang diperoleh adalah k = 0,074 e -176 (1/T). Umur simpan bekatul terstabilisasi diduga selama 50 hari (suhu penyimpanan 15oC), 40 hari (suhu 25oC), dan 39 hari (suhu 30oC).
B. SARAN
33 DAFTAR PUSTAKA
Apriyantono, A., D. Fardiaz, dan N. L. Puspitasari. 1989. Analisis Pangan. IPB Press, Bogor.
Ardiansyah. 2006. Bekatul untuk Menurunkan Hipertensi dan Hiperlipimedia. www.beritaiptek.com. [16 Oktober 2008]
Arpah. 2001. Buku dan Monograf Penentuan Kadaluarsa Produk. Program Studi Ilmu Pangan IPB, Bogor.
Association of Official Analytical Chemist. 1995. Official Method of The Association of Official Chemist. AOAC. Inc, Virginia.
Association of Official Analytical Chemist. 1999. Official Method of The Association of Official Chemist. AOAC. Inc, Virginia.
Badan Pusat Statistik. 2008. Produksi Gabah Kering tahun 2008. www.bps.co.id. [21 November 2008]
Badan Standardisasi Nasional. 1994. SNI 01-3549-1994 : Tepung Beras. Badan Standardisasi Nasional, Jakarta.
Badan Standardisasi Nasional. 1998. SNI 01-4439-1998 : Bekatul. Badan Standardisasi Nasional, Jakarta.
Champagne, E. T. 1994. Rice Chemistry and Technology. American Association of Cereal Chemists. Inc, St. Paul. Characteristics of Some Indonesia Rice Varieties. Bogor Agricultural University, Bogor.
Damardjati, D. S, B.A. Santosa, dan Munarso. 1990. Studi Kelayakan dan Rekomendasi Teknologi Pabrik Pengolahan Bekatul. Balai Penelitian Pangan, Subang.
34 Himmelblau, D. M. 1996. Basic Prinsiples and Calculations in Chemical Engineering 6th edition. Terjemahan. Asnanta, I. (Penerjemah). Prinsip-Prinsip Dasar dan Kalkulasi dalam Teknik Kimia. PT Prenhallindo, Jakarta.
Juliano, B. O. 1985. Rice bran. Di dalam. Champagne, E. T. (Ed). Rice Chemistry and Technology 3th edition. American Association of Cereal Chemists. Inc, St. Paul.
Kahlon, T. S, A. A. Bethsart, C. Chiu, dan Saunders. 1994. Effect of rice bran and cholesterol in hamster. Di dalam. Champagne, E. T. (Ed). Rice Chemistry and Technology 3th edition. American Association of Cereal Chemists. Inc, St. Paul.
Ketaren, S. 1986. Pengantar Teknologi Minyak dan Lemak Pangan. UI Press, Jakarta.
Kuswanto, H. 2003. Teknologi Pemrosesan Pengemasan dan Penyimpanan. Penerbit Kanisius, Yogyakarta.
Labuza, T. P. 1982. Open Shelf Life Dating of Foods. Food Science and Nutrition Press. Inc, Westport.
Lawless, H. T. dan Heyman. 1999. Sensory Evalution of Food: Principles and Practises. Kluwer Academic Publishers, New York.
Luh, B. 1991. Rice Utilization Vol II. Van Nostrand Reinhold, New York.
McCabe. 1985. Unit Operations of Chemical Engineering. Mc Graw Hill Book, New York. Isolation and partial characterization of banana starches. Journal Agric. Food Chem. 47:854-857.
35 Setyowati, K., A. Iskandar, Sugiarto, I. Yuliasih. 2000. Bahan dan Disain
Kemasan. Jurusan Teknologi Industri Pertanian IPB, Bogor.
Singh, P. R. 2001. Postharvest Technology. Science Publishers. Inc, USA.
Syarif, R. dan Halid. 1993. Teknologi Penyimpanan Pangan. Pusat Studi Antar Universitas IPB, Bogor.
37 Lampiran 1. Prosedur analisa sifat fisikokimia dan mikroorganisme bekatul
1. Kadar air (AOAC, 1999)
Penetapan kadar air dilakukan dengan metode oven. Prinsip kadar air adalah menguapkan air yang ada dalam bahan pangan dengan jalan pemanasan. Cawan kosong dikeringkan dalam oven pada suhu 105oC selama 10 menit. Sebanyak 2-3 gram sampel ditimbang didalam cawan yang telah dikeringkan dan diketahui bobotnya. Sampel dikeringkan dalam oven bersuhu 105oC selama 5 jam. Sampel didinginkan dalam desikator selama 15 menit dan ditimbang bobot akhirnya. Pekerjaan ini diulangi hingga bobotnya tetap.
Kadar air (%) = bobot awal sampel (g) – bobot akhir sampel (g) x 100 % bobot awal sampel (g)
2. Kadar abu (AOAC, 1999)
Cawan porselin dikeringkan dalam oven bersuhu 105oC kemudian didinginkan dalam desikator dan ditimbang bobotnya. Sampel sebanyak 3-5 gram ditimbang dan diletakkan kedalam cawan porselin. Sebelum diabukan, sampel terlebih dahulu dipanaskan di atas penangas destruksi hingga terbentuk arang dan tidak berasap lagi. Selanjutnya sampel diabukan dalam tanur listrik pada suhu 600oC hingga terbentuk warna abu-abu. Sampel kemudian didinginkan dalam desikator. Bobot akhirnya ditimbang dan diulangi hingga bobot akhirnya tetap.
Kadar abu = bobot abu (g) x 100 % bobot awal sampel (g)
3. Kadar protein metode mikro Kjeldahl (AOAC, 1999)
38 Kadar protein = (ml titrasi (sampel-blanko)) x N x 14,007 x 6,25 x 100 %
gram sampel x 1000 Keterangan: N = Normalitas H2SO4
4. Kadar lemak kasar metode Soxhlet (AOAC, 1995)
Kertas saring yang telah dibentuk seperti tabung dikeringkan pada suhu 105oC selama 1 jam. Sampel yang telah kering (sampel setelah kadar air) dimasukkan di dalam kertas saring, ditutup, dan dikeringkan kembali di dalam oven, didinginkan pada desikator dan ditimbang. Sampel yang telah diketahui bobot tetapnya dimasukkan kedalam Soxhlet, ekstraksi menggunakan heksan atau petroleum eter secukupnya. Proses dilanjutkan dengan refluks selama + 6 jam sampai pelarut turun kembali ke labu lemak menjadi bening. Selesai ekstraksi sampel dikeluarkan dari Soxhlet dan dikering anginkan. Setelah tidak ada pelarutnya, sampel dikeringkan di dalam oven pada suhu 105oC sampai bobotnya tetap. Setelah dikeringkan sampai bobotnya tetap, sampel didinginkan dalam desikator.
Kadar lemak (%) = gram awal sampel – gram akhir sampel x 100 % gram awal sampel
5. Kadar serat kasar (AOAC, 1995)
Sebanyak 2-5 gram sampel dimasukkan ke dalam labu erlenmeyer 500 ml dan ditambahkan 100 ml H2SO4 0,325 N. Campuran kemudian dihidrolisis dalam autoklaf suhu 105oC selama 15 menit, didinginkan, serta ditambahkan 50 ml NaOH 1,25 N. Sampel dihidrolisis kembali dalam autoklaf selama 15 menit. Sampel disaring menggunakan kertas saring yang telah dikeringkan dan deketahui bobotnya. Kertas saring tersebut dicuci berturut-turut menggunakan air panas, 25 ml H2SO4 0,325 N, air panas, dan 25 ml aseton/alkohol. Kertas saring tersebut dikeringkan dalam oven bersuhu 105oC selama 1 jam dan dilanjutkan hingga bobotnya tetap. Kadar serat ditentukan dengan rumus:
39 6. Kadar karbohidrat total (by difference)
Kadar karbohidat total dihitung dengan rumus berikut.
Kadar karbohidrat (% bk) = 100 % - kadar air (% bb) - kadar abu (% bk) - kadar protein (% bk) - kadar lemak (% bk) - serat kasar (% bk)
7. Penentuan bilangan TBA (Thiobarbituric Acid) (Apriyantono et al., 1989) Bilangan TBA (Thiobarbituric Acid) digunakan untuk mengetahui kerusakan sampel (ketengikan) akibat proses oksidasi lemak menjadi asam lemak dan gliserol. Sebanyak 10 gram sampel dimasukkan kedalam waring blander kemudian ditambahkan 50 ml aquades dan dihancurkan selama 2 menit. Sampel dipindahkan secara kuantitatif kedalam labu destilasi sambil dicuci dengan 47,5 ml aquades. Sampel kemudian ditambah 2,5 ml HCl 4 M. Batu didih ditambahkan secukupnya untuk mencegah pembentukan busa (anti foaming agent) dan labu destilasi dipasangkan pada alat destilasi. Destilasi dijalankan dengan suhu tinggi sehingga diperoleh 50 ml destilat. Destilat diaduk merata kemudian dipipet sebanyakk 5 ml kedalam tabung reaksi bertutup, ditambahkan 5 ml pereaksi TBA, ditutup, dicampur merata lalu dipanaskan selama 35 menit dalam air mendidih. Blanko dibuat dengan mencampurkan 5 ml aquades dan 5 ml pereaksi TBA, dilakukan seperti penetapan sampel. Tabung reaksi didinginkan dengan air dingin selama + 10 menit kemudian diukur absorbansinya pada 528 nm dengan larutan blanko sebagai titik nol. Digunakan sampel sel berdiameter 1 cm. Bilangan TBA dinyatakan dalam mg malonaldehid per kg sampel.
Bilangan TBA = 3 x 7,8 x D bobot sampel
(D = nilai absorbansi sampel - nilai absorbansi blanko)
8. Warna (L)
Analisis warna dilakukan dengan menggunakan alat colormeter Pengukuran menggunakan alat ini menghasilkan nilai L.