EVALUASI KUALITAS DAN KECERNAAN KULIT
SINGKONG, BIJI KARET, KOPRA,
BIJI KAPUK, DAN
PALM
KERNEL MEAL
DIFERMENTASI
Saccharomyces cerevisiae
PADA JUVENIL IKAN NILA
Oreochromis niloticus
ASEP EL-QUSAIRI
DEPARTEMEN BUDIDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
ABSTRAK
ASEP EL-QUSAIRI. Evaluasi kualitas dan kecernaan kulit singkong, biji karet, kopra, biji kapuk, dan palm kernel meal difermentasi Saccharomyces cerevisiae
pada juvenil ikan nila Oreochromis niloticus. Dibimbing oleh MUHAMMAD AGUS SUPRAYUDI dan MIA SETIAWATI.
Pakan menyumbang sekitar 40-85% dalam komponen biaya produksi perikanan budidaya air tawar. Mahalnya harga pakan disebabkan oleh bahan baku yang digunakan masih mengandalkan impor untuk ketersediaannya seperti tepung ikan, bungkil kedelai, dan tepung terigu. Hal ini yang menyebabkan harga pakan tidak kompetitif. Oleh karena itu, diperlukan alternatif bahan baku pakan lokal (BBL) yang berpotensi mengurangi atau bahkan menggantikan komposisi bahan baku pakan impor dalam pakan. Akan tetapi rendahnya kualitas nutrisi BBL akibat tingginya kandungan serat kasar dan keberadaan zat faktor antinutrisi membuat BBL sulit dikembangkan. Oleh karena itu perlu dilakukan pengolahan terlebih dahulu, salah satunya dengan metode fermentasi. Penelitian ini menggunakan lima perlakuan, dua faktor, satu ulangan. Ikan uji yang digunakan pada penelitian ini adalah juvenil ikan nila Oreochromis niloticus yang memiliki bobot 16,26±2,43 gram. Pakan diberikan secara at satiation, tiga kali sehari. Bahan baku yang digunakan adalah kulit singkong, biji karet, biji kapuk, kopra, dan bungkil kelapa sawit (Palm Kernel Meal, PKM). Fermentasi oleh
Saccharomyces cerevisiae mampu meningkatkan protein bahan uji antara 16,85-31,11% dan menurunkan serat kasar antara 2,46-31,65% serta meningkatkan kecernaan protein antara 0,25-11,7%, meningkatkan kecernaan energi antara 4,29-11,17% kecuali bahan uji kulit singkong dan juga mampu meningkatkan kecernaan bahan uji 1,37-61,19% pada juvenil ikan nila O. niloticus.
Kata kunci: bahan baku lokal, fermentasi, kecernaan.
ABSTRACT
ASEP EL-QUSAIRI. Evaluation of quality and digestibility of cassava peel,
rubber seed, copra, cottonseed, and palm kernel meal fermented by
Saccharomyces cerevisiae in juvenile of nile tilapia Oreochromis niloticus.
Supervised by MUHAMMAD AGUS SUPRAYUDI and MIA SETIAWATI.
to developed. This low quality caused by high crude fiber content and the presence of anti-nutritional substances factor, so it needs to be processed first by fermentation methods. This study used five treatments, two factors, and one replicates. Fish used in this study were juvenile of nile tilapia Oreochromis niloticus which has weight about 16,26±2,43 grams. Diets given at satiation, three times a day. The feedstuffs used are cassava peel, rubber seed, cottonseed, copra, and (Palm Kernel Meal, PKM). The result of this study showed some enhancements in fish content. The fermentation by Saccharomyces cerevisiae can increase fish (test material) protein around 16,85%-31,11%, decrease crude fiber around 2,46%-31,65%, increase protein digestibility around 0,25%-11,7%, increase digestibility of energy around 4,29%-11,17% (except for digestibilty in the cassava peel) and also increase the digestibility of feedstuffs around 1,37%-61,19% in juvenile of nile tilapia O. niloticus.
EVALUASI KUALITAS DAN KECERNAAN KULIT
SINGKONG, BIJI KARET, KOPRA,
BIJI KAPUK, DAN
PALM
KERNEL MEAL
DIFERMENTASI
Saccharomyces cerevisiae
PADA JUVENIL IKAN NILA
Oreochromis niloticus
ASEP EL-QUSAIRI
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Program Studi Teknologi dan Manajemen Perikanan Budidaya
Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor
DEPARTEMEN BUDIDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul :
EVALUASI KUALITAS DAN KECERNAAN KULIT SINGKONG, BIJI KARET, KOPRA, BIJI KAPUK, DAN PALM KERNEL MEAL DIFERMENTASI Saccharomyces cerevisiae PADA JUVENIL IKAN NILA Oreochromis niloticus
adalah benar merupakan hasil karya yang belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Juli 2011
Evaluasi Kualitas dan Kecernaan Kulit Singkong, Biji Karet,
Kopra, Biji Kapuk, dan Palm Kernel Meal Difermentasi
Saccharomyces cerevisiae pada Juvenil Ikan Nila Oreochromis
PENGESAHAN
Judul :
Nama : Asep El-Qusairi
NIM : C14070097
Departemen : Budidaya Perairan
Disetujui,
Pembimbing I Pembimbing II
Dr. Muhammad Agus Suprayudi Dr. Mia Setiawati
NIP. 19650418 199103 1 003 NIP. 19641026 199203 2 001
Diketahui,
Ketua Departemen Budidaya Perairan
Dr. Odang Carman NIP. 19591222 198601 1 001
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang senantiasa melimpahkan
nikmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Evaluasi Kualitas dan Kecernaan Kulit Singkong, Biji Karet, Kopra,
Biji Kapuk, dan Palm Kernel Meal Difermentasi Saccharomyces cerevisiae pada Juvenil Ikan Nila Oreochromis niloticus” ini sebagai salah satu persyaratan untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor.
Penelitian ini dilakukan pada Bulan Februari sampai dengan April 2011.
Analisis proksimat bahan baku pakan, pakan uji, dan feses ikan dilakukan di
Laboratorium Nutrisi Ikan, pembuatan pakan dilakukan di Laboratorium
Pembuatan Pakan, pemeliharaan ikan dan proses fermentasi dilakukan di
Laboratorium Basah Nutrisi Ikan, Departemen Budidaya Perairan, Fakultas
Perikanan dan Ilmu Kelautan. Analisis energi feses dilakukan di Laboratorium
Ilmu Nutrisi dan Makanan Ternak, Departemen Ilmu Nutrisi dan Teknologi
Pakan, Fakultas Peternakan, Institut Pertanian Bogor.
Semoga skripsi ini bermanfaat.
Bogor, Juli 2011
UCAPAN TERIMA KASIH
Penulisan skripsi ini banyak dibantu oleh berbagai pihak, baik secara
langsung maupun tidak. Oleh karena itu, penulis mengucapkan banyak terima
kasih kepada Dr. Muhammad Agus Suprayudi dan Dr. Mia Setiawati sebagai
Dosen Pembimbing skripsi ini yang telah bersedia meluangkan waktunya untuk
selalu memberikan bimbingan kepada penulis. Kementerian Agama Republik
Indonesia yang telah membiayai penuh kuliah penulis dari awal hingga akhir masa
studi. Bapak Wasjan dan ibu Retno atas bimbingannya selama di laboratorium.
Bapak Maryanta dan ibu Yuli saat mengurus administrasi studi. Seluruh keluarga
besar penulis terutama ayah dan ibu yang senantiasa memberikan dukungan, doa,
dan semangat kepada penulis. Keluarga penerima Beasiswa Santri Berprestasi
Community of Santri Shoolars of Ministry of Religious Affair (CSS MoRA) IPB khususnya angkatan 2007. Sdri. Gebbie Edriani yang telah bekerjasama dan
membantu penulis selama penelitian hingga proses penulisan skripsi. Sdri. Rizki
Andini yang banyak membantu selama proses penelitian. Keluarga BDP 44
khususnya Dina Silmina, Nurfadhilah, Annisa Khairani Aras, Ridha Nugraha dan
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di Tangerang pada tanggal 17 Desember 1988 dari
pasangan Bapak Nurhasan dan Ibu Jumriah. Penulis merupakan anak kedua dari
empat bersaudara. Setelah menyelesaikan pendidikan di MA Daarul Muqimien
Tangerang tahun 2007, penulis melanjutkan studi di Institut Pertanian Bogor
melalui jalur Beasiswa Utusan Daerah (BUD) program Beasiswa Kementerian
Agama Republik Indonesia pada program studi Teknologi dan Manajemen
Perikanan Budidaya, Departemen Budidaya Perairan, Fakultas Perikanan dan
Ilmu Kelautan.
Selama masa perkuliahan, penulis aktif di Organisasi Mahasiswa Penerima
Beasiswa Kementerian Agama RI (CSS MoRA) sebagai divisi Infokom
(2007-2008) dan divisi Sosial Lingkungan (2008-2009). Penulis pernah menjadi asisten
praktikum pada beberapa mata kuliah yaitu Ikhtiologi (2009-2010), Nutrisi Ikan
(2011), dan Teknologi Produksi Plankton, Benthos dan Alga (2011). Penulis juga
pernah mengikuti Program Krativitas Mahasiswa (PKM) bidang Penelitian yang
berjudul Efektivitas Ekstrak Buah Mengkudu Morinda citrifolia L. Dengan Metode Bioenkapsulasi Terhadap Sifat Kanibalisme Larva Ikan Lele Clarias sp. PKM Artikel Ilmiah yang berjudul Studi Mikrobiologis Air pada Beberapa
Sumber Air Disekitar Kampus IPB Dramaga Bogor, dan Deteksi Koi Herpes
Virus (KHV) Dengan Metode Polymerase Chain Reaction (PCR).
Penulis juga pernah melakukan praktek lapangan pembenihan ikan gurame
Osphronemus gouramy di Loka Riset Budidaya Perikanan Air Tawar Sukamandi, Subang, Jawa Barat pada Februari 2009 dan ikan koi Cyprinus carpio di Isaku Koi Farm, Blitar, Jawa Timur pada Juni-Agustus 2010. Tugas akhir di perguruan
tinggi diselesaikan penulis dengan menulis skripsi berjudul “Evaluasi Kualitas dan Kecernaan Kulit Singkong, Biji Karet, Kopra, Biji Kapuk, dan Palm Kernel Meal Difermentasi Saccharomyces cerevisiae pada Juvenil Ikan Nila Oreochromis niloticus”.
DAFTAR ISI
Halaman
DAFTAR TABEL ... ii
DAFTAR LAMPIRAN ... iii
I. PENDAHULUAN ... 1
II. METODOLOGI ... 4
2.1 Proses Fermentasi... 4
2.2 Pakan Uji ... 4
2.3 Pemeliharaan Ikan dan Pengumpulan Data ... 5
2.4 Analisis Kimia ... 6
2.5 Analisis Kecernaan ... 6
2.6 Parameter yang Diukur ... 7
2.6.1 Jumlah konsumsi pakan ... 7
2.6.2 Kecernaan ... 7
2.6.3 Sintasan (Survival Rate, SR)... 8
2.6.4 Konversi pakan (Feed Conversion Ratio, FCR) ... 8
2.6.5 Laju pertumbuhan harian ... 8
2.7 Analisis Data ... 8
III. HASIL DAN PEMBAHASAN ... 9
3.1 Hasil ... 9
3.2 Pembahasan ... 12
IV. KESIMPULAN DAN SARAN ... 23
4.1 Kesimpulan ... 23
4.2 Saran ... 23
DAFTAR PUSTAKA ... 24
LAMPIRAN ... 27
DAFTAR TABEL
1. Komposisi pakan acuan dan pakan uji kulit singkong, biji karet, kopra, biji kapuk, dan Palm Kernel Meal (PKM) tanpa dan difermentasi oleh
Saccharomyces cerevisiae ... 4 2. Kisaran nilai kualitas air akuarium pemeliharaan juvenil ikan nila O.
niloticus ... 6 3. Komposisi proksimat kulit singkong, biji karet, kopra, biji kapuk,
bungkil kelapa sawit (Palm Kernel Meal, PKM) tanpa dan difermentasi oleh Saccharomyces cerevisiae (% bobot kering) dan % perubahannya .. 9
4. Komposisi proksimat pakan dengan campuran bahan uji kulit singkong, biji karet, kopra, biji kapuk, PKM tanpa dan difermentasi
Saccharomyces cerevisiae (% bobot kering), dan % perubahannya ... 10 5. Nilai kecernaan protein, kecernaan energi, dan kecernaan bahan dengan
penambahan 30% bahan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh Saccharomyces cerevisiae pada ikan nila O. niloticus (% bobot kering), dan % perubahannya ... 11
6. Nilai Laju Pertumbuhan Harian (LPH), konversi pakan (Feed
Conversion Ratio, FCR), Jumlah Konsumsi Pakan (JKP), dan sintasan (Survival Rate, SR) pada juvenil ikan nila dan % perubahannya ... 12
Halaman
DAFTAR LAMPIRAN
1. Metode fermentasi... 27
2. Pembuatan pakan perlakuan untuk 600 g pakan ... 27
3. Skema tata letak akuarium perlakuan ... 27
4. Data kualitas air pada awal dan akhir pemeliharaan ikan perlakuan ... 28
5. Prosedur analisis proksimat ... 28
5.1 Prosedur analisis kadar air ... 28
5.2 Prosedur analisis serat kasar ... 28
5.3 Prosedur analisis kadar protein ... 29
5.4 Prosedur analisis kadar lemak ... 30
5.5 Prosedur analisis kadar abu... 30
6. Analisis Cr2O3 ... 31
7. Kecernaan protein pakan ikan nila Oreochromis niloticus pada bahan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh Saccharomyces cerevisiae ... 32
8. Kecernaan energi pakan ikan nila O. niloticus pada bahan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh S. cerevisiae ... 33
9. Kecernaan bahan pakan ikan nila O. niloticus pada bahan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh S. cerevisiae ... 34
10.Sintasan ikan nila O. niloticus setelah dipelihara selama 30 hari pada uji kecernaan bahan kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh S. cerevisiae ... 35
11.Jumlah Konsumsi Pakan (JKP) dan konversi pakan (Feed Conversion Ratio, FCR) ikan nila O. niloticus setelah dipelihara selama 30 hari pada uji kecernaan bahan kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh S. cerevisiae ... 35
12.Laju Pertumbuhan Harian (LPH) ikan nila O. niloticus setelah dipelihara selama 30 hari pada uji kecernaan bahan kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh S. cerevisiae... 36
Halaman
1
I.
PENDAHULUAN
Pakan menyumbang sekitar 40-85% dalam komponen biaya produksi
perikanan budidaya air tawar (Suprayudi, 2010). Komponen utama pakan yang
dibutuhkan ikan sebagai sumber energi adalah protein, karbohidrat, dan lemak.
Protein yang terdapat dalam pakan sebagian besar bersumber dari tepung ikan dan
bungkil kedelai, sementara sumber karbohidrat berasal dari tepung pollard dan tepung terigu. Sebagian besar bahan baku tersebut harus diimpor untuk
ketersediaannya, sehingga menyebabkan harga pakan menjadi tidak kompetitif
terutama untuk pakan ikan budidaya air tawar. Oleh karena itu, harus ada
alternatif bahan baku lokal yang harganya lebih kompetitif dari bahan impor,
jumlahnya melimpah dan terjaga kontinuitasnya, sehingga diharapkan dapat
mengurangi atau bahkan menggantikan penggunaan bahan baku pakan impor
tersebut.
Syarat yang harus dipenuhi sebagai bahan baku adalah mengandung nutrien
yang dibutuhkan ikan untuk pertumbuhan, diutamakan dari sumber nabati, tidak
berkompetisi dengan kebutuhan manusia, berbasis hasil samping, jumlah
melimpah, dan tidak mengandung hazard material (Suprayudi, 2010). Beberapa bahan baku pakan lokal yang mempunyai potensi sebagai bahan baku pakan
alternatif yang berasal dari hasil samping agroindustri diantaranya kulit singkong,
biji karet, kopra, biji kapuk, dan bungkil kelapa sawit (Palm Kernel Meal, PKM). Bahan-bahan tersebut sangat mudah diperoleh di Indonesia dalam jumlah yang
cukup melimpah. Selain itu, pemanfaatan terhadap hasil samping agroindustri
tersebut masih belum maksimal karena lebih banyak dibuang dan tidak
termanfaatkan.
Kulit Singkong Manihot utilissima merupakan hasil samping agroindustri dari industri pengolahan singkong seperti industri tepung tapioka dan keripik
singkong di Indonesia yang jumlahnya melimpah. Menurut Badan Pusat Statistik
(2008), produksi singkong di Indonesia mencapai 21.756.991 ton. Sekitar 15-20%
bagian singkong adalah kulit dan sisanya adalah umbinya. Kulit singkong
mengandung protein sebesar 8,2%, lemak 3,1%, abu 6,4%, serat kasar 12,5%, dan
2 antinutrisi (Anti-Nutritional Factors, ANFs) seperti HCN dan asam fitat (Oboh, 2005).
Biji Karet Havea brasiliensis merupakan salah satu kandidat bahan baku pakan alternatif yang bisa digunakan untuk pakan ikan. Menurut Badan Pusat
Statistik (2008), jumlah produksi karet di Indonesia tahun 2008 mencapai 586.081
ton. Jumlah produksi yang besar menyebabkan potensi hasil samping yang besar
pula, sehingga ketersediaan biji karet cukup melimpah di Indonesia. Biji karet
mengandung protein 21,90%, serat kasar 5,1%, lemak 15,8%, dan abu 2,3%.
Namun, biji karet juga mengandung racun yang merupakan hasil dari aktivitas
enzim yang terdapat pada tanaman itu sendiri yaitu cyanoenic glucosidal yang menghasilkan asam sianida (HCN) (Oyewushi et al., 2007).
Biji Kapuk Gossypum hirsitum merupakan hasil samping agroindustri dari industri pembuatan kapas yang berpotensi digunakan sebagai bahan baku pakan.
Biji kapuk mengandung protein yang cukup tinggi yaitu 31,70%. Akan tetapi,
kandungan serat kasarnya juga tinggi yaitu sebesar 20,50%. Biji kapuk juga
mengandung ANFs berupa gosipol sebesar 0,3%-3,4%. Terdapat dua jenis gosipol
yaitu gosipol bebas yang bersifat racun, dan gosipol terikat yang tidak berbahaya.
Kandungan gosipol bebas bervariasi tergantung spesies tanaman, jenis tanah, dan
iklim. Proses pengepresan disertai pemanasan akan meningkatkan kandungan
protein dan terjadi konversi gosipol bebas menjadi bentuk terikat (Murni et al., 2008).
Kopra Cocos nucifera merupakan produk hasil samping dari ekstraksi minyak kelapa yang jumlahnya juga melimpah di Indonesia. Nutrien yang
terkandung dalam kopra diantaranya karbohidrat 48%, protein 21%, dan lemak
5,7% serta mengandung lignin sebesar 5% (Sundu et al., 2006). Selain itu, kopra juga mengandung polisakarida yang tidak dapat dicerna seperti mannan dan
galaktomannan (Hatta dan Sundu, 2009)
Bungkil Kelapa Sawit (Palm Kernel Meal, PKM) Elaeis guineensis
merupakan salah satu limbah yang dihasilkan pada proses pengolahan minyak
kelapa sawit. Indonesia mampu memproduksi PKM sebanyak 2.646.577 ton per
tahunnya (BPS, 2008), sehingga jumlahnya sangat melimpah. PKM mengandung
3 Sedangkan menurut Ezieshi dan Olomu (1995), PKM mengandung protein
16,0-21,3%, serat kasar 6,7-17,5%, dan abu 4,3%. Selain itu, ANFs yang terdapat
dalam PKM adalah Non-Starch Polysaccharides (NSPs) berupa mannan dan galaktomannan.
Upaya pemanfaatan bahan baku pakan lokal tersebut masih mengalami
kendala yaitu tingginya kandungan serat kasar, adanya zat faktor antinutrisi, dan
rendahnya kandungan protein. Oleh sebab itu, perlu dilakukan pengolahan bahan
baku pakan lokal tersebut sebelum digunakan sebagai bahan pakan, salah satunya
dengan fermentasi. Menurut Pamungkas (2010), teknologi untuk meningkatkan
mutu bahan pakan adalah dengan fermentasi. Secara umum semua produk akhir
fermentasi biasanya mengandung senyawa yang lebih sederhana dan mudah
dicerna dari pada bahan asalnya (Sari dan Purwadaria, 2004). Fermentasi dapat
dilakukan dengan memanfaatkan mikroorganisme seperti kapang, khamir, dan
bakteri. Salah satu khamir yang digunakan dalam kegiatan fermentasi bahan
pakan adalah khamir Saccharomyces cerevisiae (Labuza, 1980 dalam Deman, 1997). Merujuk pada penyataan tersebut, maka penelitian ini menggunakan
khamir S. cerevisiae. Pemanfaatan bahan baku pakan lokal hasil samping agroindustri yang ditingkatkan nilai nutrisinya melalui teknik fermentasi
diharapkan dapat mencukupi kebutuhan bahan baku sumber protein dan
karbohidrat sehingga mampu mengurangi penggunaan tepung ikan, bungkil
kedelai, dan tepung terigu yang masih impor.
Penelitian ini dilakukan untuk mengevaluasi kadar nutrien terutama
peningkatan protein dan penurunan serat kasar dalam beberapa bahan baku pakan
diantaranya kulit singkong, biji karet, kopra, biji kapuk, dan PKM melalui proses
fermentasi menggunakan S. cerevisiae dan menguji kecernaan bahan baku tersebut meliputi kecernaan protein, kecernaan energi, dan kecernaan bahan
terhadap juvenil ikan nila Oreochromis niloticus. Ikan nila dipilih sebagai ikan uji karena merupakan salah satu komoditas perikanan air tawar unggulan yang cocok
dibudidayakan dalam sistem intensif karena memiliki karakteristik unggulan
seperti pertumbuhan cepat, kemampuan untuk bertahan hidup yang baik pada
4
II.
BAHAN DAN METODE
2.1 Proses Fermentasi
Bahan yang digunakan sebagai bahan baku pakan difermentasi
menggunakan khamir Saccharomyces cerevisiae 0,9% w/w selama 24 jam dalam
kondisi aerob. Setelah itu bahan dioven selama dua jam pada suhu 60 oC.
Kemudian bahan yang sudah difermentasi dianalisis proksimat. Penggunaan dosis
khamir yaitu 0,9% w/w selama 24 jam didasarkan pada hasil penelitian
pendahuluan yaitu fermentasi pada PKM menggunakan dosis 0,3%, 0,6%, dan
0,9% selama 24 jam dan 48 jam. Hasil yang terbaik diperoleh pada dosis 0,9%
w/w selama 24 jam. Metode fermentasi dapat dilihat pada Lampiran 1.
2.2 Pakan Uji
Pakan perlakuan yang digunakan adalah pakan pembanding yang terdiri
dari 100% pakan komersil dan pakan uji yang terdiri dari 70% pakan komersil dan
30% bahan. Semua pakan perlakuan ditambahkan kromium trioksida (Cr2O3)
sebanyak 0,5% sebagaiindikator kecernaan (NRC, 1993). Semua pakan perlakuan
dibuat dalam bentuk pelet kering. Proses pembuatan pakan dapat dilihat pada
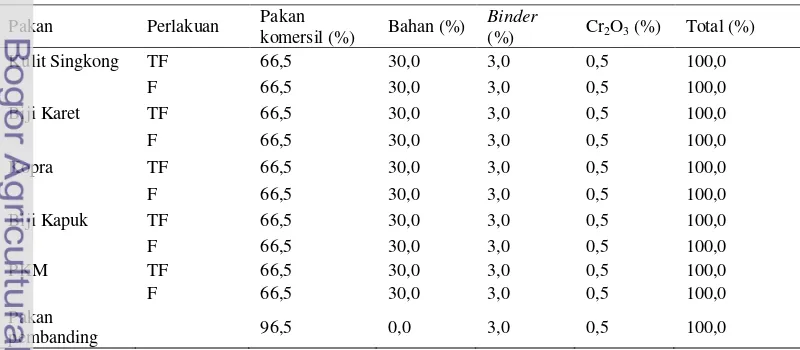
Lampiran 2. Komposisi pakan pembanding, pakan uji kulit singkong, biji karet,
kopra, biji kapuk, dan Palm Kernel Meal (PKM) ditunjukkan pada Tabel 1.
Tabel 1. Komposisi pakan acuan dan pakan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh Saccharomyces cerevisiae
Pakan Perlakuan Pakan
5
2.3 Pemeliharaan Ikan dan Pengumpulan Data
Ikan uji yang digunakan pada penelitian ini adalah juvenil ikan nila
Oreochromis niloticus yang memiliki bobot 16,26±2,43 gram. Sebelum ditebar, ikan dikarantina dalam akuarium karantina selama lima hari menggunakan larutan
garam untuk membunuh parasit yang menempel pada tubuh ikan. Selama masa
karantina, air akuarium diganti 70% setiap dua kali sehari dan suhu air
dipertahankan 29-30 oC menggunakan termostat. Setelah itu ikan ditebar ke
masing-masing akuarium dengan jumlah enam ekor per akuarium.
Wadah yang digunakan untuk masing-masing ikan adalah akuarium
berukuran 50 x 40 x 35 cm sebanyak 12 buah serta satu buah bak fiber sebagai
tandon. Skema tata letak akuarium perlakuan dapat dilihat pada Lampiran 3.
Keseluruhan akuarium dirangkai membentuk suatu sistem resirkulasi. Akuarium
diisi dengan ketinggian air efektif 30 cm dan diaerasi selama 24 jam. Sisi wadah
ditutup dengan plastik hitam sebagai pencegahan stres ikan akibat aktivitas orang
disekitarnya. Empat buah termostat diletakkan pada tandon untuk menjaga
kestabilan suhu pada kisaran 28-30°C.
Sebelum perlakuan dimulai, ikan dipuasakan selama 48 jam guna
menghilangkan sisa pakan dalam saluran pencernaan. Pemeliharaan ikan
dilakukan selama 30 hari. Pengukuran bobot ikan uji dilakukan pada awal dan
akhir pemeliharaan, sebelum ditimbang ikan dipuasakan selama 24 jam. Apabila
terdapat ikan yang mati pada masa pemeliharaan, ikan tersebut segera dikeluarkan
dari dalam akuarium untuk ditimbang dan dicatat bobotnya. Pakan diberikan tiga
kali sehari yaitu pukul 08.00, 12.00, dan 16.00 WIB secara at satiation (hingga kenyang). Sisa-sisa pakan yang tidak termakan dikumpulkan untuk menghitung
Jumlah Konsumsi Pakan (JKP) sebenarnya pada akhir penelitian. Pakan
ditimbang pada awal perlakuan dan sisa pakan diakhir perlakuan.
Faktor kualitas air yang diperhatikan antara lain adalah suhu yang diamati
setiap pagi, siang, dan sore hari sebelum pemberian pakan. Pengukuran suhu
6 dari volume awal air tandon. Data kualitas air akuarium pemeliharaan ikan dapat
dilihat pada Tabel 2. Hasil pengukuran kualitas air pada awal dan akhir
pemeliharaan ikan dapat dilihat pada Lampiran 4.
Tabel 2. Kisaran nilai kualitas air akuarium pemeliharaan juvenil ikan nila
Oreochromis niloticus
Parameter Kisaran Nilai Satuan
Suhu 28-29 oC
DO 4,00-4,74 ppm
pH 5,87-6,90 -
Alkalinitas 18-20 mg CaCO3
Kesadahan 96,10-100,1 mg CaCO3
TAN 0,38-0,47 ppm
2.4 Analisis Kimia
Analisis proksimat dilakukan terhadap bahan baku pakan sebelum dan
sesudah difermentasi serta pakan perlakuan. Analisis yang dilakukan meliputi
kadar protein, lemak, serat kasar, kadar abu, kadar air, dan Bahan Ekstrak Tanpa
Nitrogen (BETN). Analisis energi dilakukan terhadap pakan uji dan feses
menggunakan alat Bomb Kalorimeter.
Analisis proksimat untuk protein dilakukan dengan metode Kjeldahl, lemak
kering dilakukan dengan metode Soxchlet, kadar abu dengan pemanasan sampel
dalam tanur bersuhu 600 oC, serat kasar menggunakan metode pelarutan sampel
dengan asam dan basa kuat serta pemanasan, dan kadar air dengan pemanasan
dalam oven bersuhu 105-110 oC (Takeuchi, 1988). Metode analisis proksimat
dapat dilihat pada Lampiran 5.
2.5 Analisis kecernaan
Pengukuran kecernaan dilakukan pada akhir penelitian yaitu setelah
pemeliharaan selama 30 hari dan pengukuran kinerja pertumbuhan telah selesai.
Setelah lima hari pemberian pakan yang dicampur dengan Cr2O3, feses mulai
dikumpulkan setiap harinya (Silva, 1989) dan disimpan dalam lemari pendingin.
Proses pengumpulan feses dilakukan selama 21 hari. Feses yang telah terkumpul
kemudian dikeringkan menggunakan oven bersuhu 105-110 oC selama 5-6 jam.
7 feses yang sudah dikeringkan. Analisis protein feses dilakukan dengan metode
Kjeldahl. Analisis Cr2O3 dalam pakan dan feses dilakukan dengan proses oksidasi
dan dilanjutkan dengan pembacaan nilai absorban menggunakan spektrofotometer
dengan panjang gelombang 350 nm. Metode analisis kecernaan dapat dilihat pada
Lampiran 6.
2.6 Parameter yang Diukur
Parameter yang diukur dalam penelitian ini adalah sebagai berikut;
2.6.1 Jumlah Konsumsi Pakan (JKP)
Pengukuran JKP ditentukan dengan menghitung selisih berat jumlah pakan
yang diberikan dengan jumlah pakan yang tidak dimakan. Pakan yang diberikan
selama percobaan dijumlahkan kemudian dikurangi dengan sisa pakan yang
dikumpulkan dan sudah dikeringkan.
2.6.2 Kecernaan
Parameter kecernaan yang diukur adalah kecernaan protein, kecernaan
energi, dan kecernaan bahan. Nilai kecernaan protein, dan kecernaan energi
(Takeuchi, 1988) dan kecernaan bahan (Watanabe, 1988) dihitung berdasarkan
persamaan;
Kecernaan protein = [1-(b’/b) x (a/a’)] x 100%
Energi tercerna = Ep –[Ef x n/n’]
Kecernaan energi = [Energi tercerna/Energi pakan] x 100%
Kecernaan Bahan = ADT− 0,7 AD
ADT = nilai kecernaan energi (kecernaan total) pakan uji
8
2.6.3 Sintasan (Survival Rate, SR)
Nilai SR ikan dapat diketahui dengan menghitungnya dengan persamaan
berikut ini;
SR = Nt
No x 100%
Keterangan :
Nt = Jumlah ikan akhir pemeliharaan No = Jumlah ikan awal pemeliharaan
2.6.4 Konversi pakan (Feed Conversion Ratio, FCR)
Nilai FCR dihitung dengan menggunakan persamaan sebagai berikut;
FCR = F
Wt + D −Wo
Keterangan :
F = Jumlah pakan yang diberikan selama pemeliharaan
Wt = Biomassa ikan diakhir pemeliharaan Wo = Biomassa awal ikan
D = Biomassa ikan mati
2.6.5 Laju Pertumbuhan Harian (LPH)
Nilai LPH ikan uji dapat dihitung menggunakan rumus berikut ini;
LPH = wt
wo
t
−1 x 100%
Keterangan:
wt = Bobot akhir rata-rata ikan uji (gram) wo = Bobot awal rata-rata ikan uji (gram)
t = Lama waktu pemeliharaan (hari)
2.7 Analisis Data
Penelitian ini menggunakan rancangan percobaan berupa rancangan acak
kelompok. Nilai kecernaan energi, kecernaan protein, kecernaan bahan, sintasan
9
III.
HASIL DAN PEMBAHASAN
3.1 Hasil
Hasil analisis proksimat bahan uji sebelum dan sesudah difermentasi
terdapat pada Tabel 3. Sedangkan hasil analisis proksimat pakan pembanding dan
pakan uji ditunjukkan pada Tabel 4.
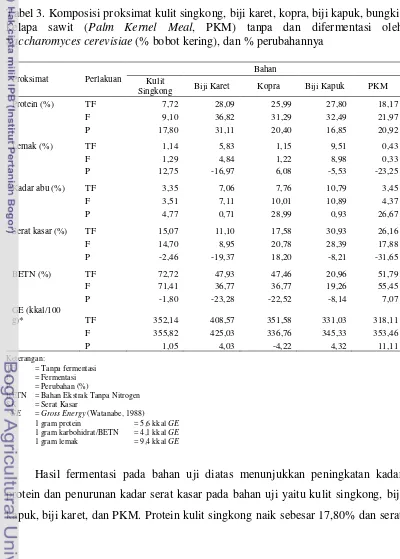
Tabel 3. Komposisi proksimat kulit singkong, biji karet, kopra, biji kapuk, bungkil
kelapa sawit (Palm Kernel Meal, PKM) tanpa dan difermentasi oleh
Saccharomyces cerevisiae (% bobot kering), dan % perubahannya
Proksimat Perlakuan
BETN = Bahan Ekstrak Tanpa Nitrogen SK = Serat Kasar
*GE = Gross Energy (Watanabe, 1988)
1 gram protein = 5,6 kkal GE
1 gram karbohidrat/BETN = 4,1 kkal GE
1 gram lemak = 9,4 kkal GE
Hasil fermentasi pada bahan uji diatas menunjukkan peningkatan kadar
protein dan penurunan kadar serat kasar pada bahan uji yaitu kulit singkong, biji
10 kasar turun sebesar 2,46%, protein biji karet naik 31,11% dan serat kasar turun
19,37%, protein biji kapuk naik 16,85%, dan serat kasar turun 8,21%, serta
protein PKM naik 20,92% dan serat kasar turun 31,65%. Namun pada kopra
menunjukkan hasil yang sebaliknya, terjadi kenaikan serat kasar sebesar 18,20%
setelah bahan tersebut difermentasi.
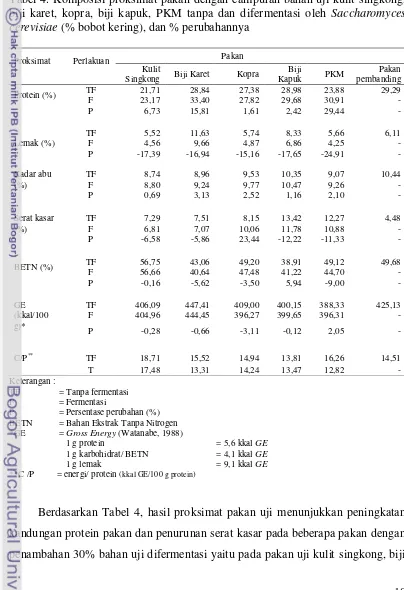
Tabel 4. Komposisi proksimat pakan dengan campuran bahan uji kulit singkong, biji karet, kopra, biji kapuk, PKM tanpa dan difermentasi oleh Saccharomyces cerevisiae (% bobot kering), dan % perubahannya
Proksimat Perlakuan Pakan
Kulit
Singkong Biji Karet Kopra
Biji BETN = Bahan Ekstrak Tanpa Nitrogen *GE = Gross Energy (Watanabe, 1988)
1 g protein = 5,6 kkal GE
1 g karbohidrat/ BETN = 4,1 kkal GE
1 g lemak = 9,1 kkal GE
**C /P = energi/ protein (kkal GE/100 g protein)
Berdasarkan Tabel 4, hasil proksimat pakan uji menunjukkan peningkatan
kandungan protein pakan dan penurunan serat kasar pada beberapa pakan dengan
11 karet, biji kapuk, dan PKM. Protein kulit singkong naik sebesar 6,73% dan serat
kasar turun sebesar 6,58%, protein biji karet naik 15,81% dan serat kasar turun
5,86%, protein biji kapuk naik 2,42% dan serat kasar turun 12,22%, serta protein
PKM naik 29,44% dan serat kasarnya turun 11,33%. Namun pada pakan uji
dengan penambahan 30% kopra difermentasi terjadi kenaikan serat kasar sebesar
23,44%. Serat kasar pakan pembanding masih yang terendah dibandingkan
dengan pakan uji yaitu sebesar 4,48%.
Hal pertama yang harus dilakukan untuk mengevaluasi potensi sebuah
bahan baku untuk digunakan pada pakan adalah mengukur kecernaannya
(Watanabe, 1988). Nilai kecernaan menunjukkan besarnya nutrien yang mampu
diserap tubuh dan tidak dikeluarkan melalui feses. Nilai kecernaan protein,
kecernaan energi, dan kecernaan bahan pada juvenil ikan nila dapat dilihat pada
Tabel 5. Data tiap ulangan dapat dilihat pada Lampiran 7-9.
Tabel 5. Nilai kecernaan protein, kecernaan energi, dan kecernaan bahan dengan penambahan 30% bahan uji kulit singkong, biji karet, kopra, biji kapuk, dan PKM tanpa dan difermentasi oleh Saccharomyces cerevisiae pada ikan nila O. niloticus
(% bobot kering), dan % perubahaannya
Parameter
TF 79,19±2,00 83,93±2,31 79,93±5,10 76,28±0,98 78,16±0,76
F 79,40±0,57 88,98±1,09 81,49±2,64 79,95±3,12 86,82±1,40
P 0,25 6,02 1,94 4,80 11,07
TF 46,34±0,52 61,44±0,69 38,95±3,27 22,33±0,31 24,62±0,79
F 46,98±0,12 75,11±5,55 41,61±1,07 29,23±3,43 39,69±0,52
P 1,37 22,24 6,83 30,87 61,19
Keterangan: Nilai yang tertera merupakan nilai rata-rata ± standar deviasi. TF (tanpa fermentasi), F (difermentasi), P (perubahan (%))
Berdasarkan Tabel 5, nilai kecernaan protein dan kecernaan bahan dengan
penggunaan 30% bahan uji difermentasi lebih tinggi dibandingkan dengan bahan
uji tanpa fermentasi. Nilai kecernaan protein tertinggi diperoleh pada pakan biji
karet fermentasi yaitu 88,98±1,09% dan terendah adalah biji kapuk yaitu
76,28±4,03%. Sedangkan nilai kecernaan energi kulit singkong mengalami
12 Nilai kecernaan energi tertinggi diperoleh pada pakan biji karet fermentasi yaitu
78,16±1,50% dan nilai terendah adalah pakan uji PKM yaitu 60,01±0,24%. Nilai
kecernaan bahan tertinggi diperoleh pada pakan biji karet fermentasi dengan nilai
sebesar 75,11±5,55% dan nilai terendah adalah biji kapuk yaitu 22,34±0,38%.
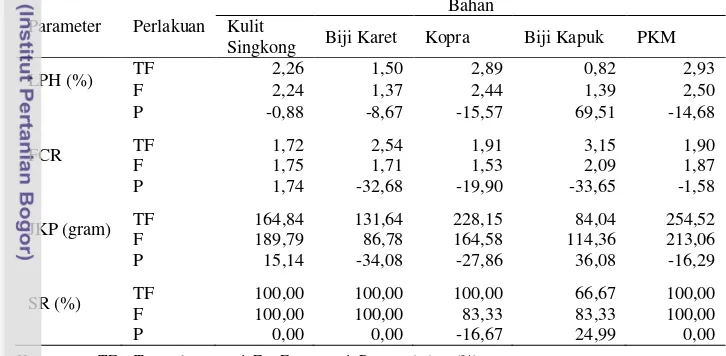
Nilai Laju Pertumbuhan Harian (LPH), konversi pakan (Feed Conversion Ratio, FCR), Jumlah Konsumsi Pakan (JKP), dan sintasan (Survival Rate, SR) pada juvenil ikan nila O. niloticus dapat dilihat pada Tabel 6. Data perhitungan nilai LPH, FCR, JKP, dan SR dilihat pada Lampiran 10-12.
Tabel 6. Nilai Laju Pertumbuhan Harian (LPH), konversi pakan (Feed Conversion Ratio, FCR), Jumlah Konsumsi Pakan (JKP), dan sintasan (Survival Rate, SR) pada juvenil ikan nila O. niloticus dan % perubahannya
Parameter Perlakuan
Keterangan: TF = Tanpa fermentasi, F = Fermentasi. P = perubahan (%)
Nilai JKP tertinggi diperoleh pada perlakuan pakan PKM yaitu 254,52 g dan
terendah yaitu pakan biji kapuk yaitu 84,04 g. Nilai LPH pakan uji tertinggi
diperoleh pada pakan PKM yaitu 2,93%. Efisiensi pakan uji yang tertinggi
diperoleh pada pakan kopra fermentasi dengan nilai FCR 1,53. Kematian ikan uji
terjadi pada pakan perlakuan biji kapuk dengan tingkat mortalitas (mortality rate, MR) sebesar 33,33%, biji kapuk fermentasi 16,67%, dan kopra 16,67%.
3.2 Pembahasan
Pemanfaatan bahan baku pakan alternatif telah banyak dilakukan untuk
mengatasi masalah mahalnya bahan baku pakan konvensional sumber protein
13 tepung terigu yang masih mengandalkan pasokan impor untuk ketersediaannya,
sehingga bahan baku lokal menjadi alternatif bahan baku pakan karena mudah
didapat dan biasanya berupa hasil samping yang belum termanfaatkan secara
optimal. Akan tetapi, upaya pemanfaatan bahan baku lokal tersebut masih
mengalami kendala yaitu tingginya kandungan serat kasar dan rendahnya
kandungan protein kasar. Hal ini sesuai dengan pernyataan Hertrampf dan Pascual
(2000) bahwa kelemahan bahan baku pakan yang berasal dari bahan nabati adalah
keberadaan zat anti nutrisi, serat kasar dan kadar abu yang tinggi. Hal ini
menyebabkan kecernaan bahan yang rendah sehingga diperlukan upaya
pengolahan bahan baku pakan lokal tersebut sebelum digunakan sebagai bahan
pakan. Menurut Pamungkas (2010), teknologi untuk meningkatkan mutu bahan
pakan adalah dengan fermentasi. Secara umum semua produk akhir fermentasi
biasanya mengandung senyawa yang lebih sederhana dan mudah dicerna daripada
bahan asalnya (Sari dan Purwadaria, 2004).
Mikroorganisme yang digunakan untuk memfermentasi bahan uji dalam
penelitian ini adalah khamir Saccharomyces cerevisiae. Dosis yang digunakan adalah 0,9% w/w dan air yang ditambahkan sebanyak 60% w/w. Fermentasi
dilakukan dalam keadaan aerob. Hal ini merujuk pada Labuza (1980) dalam
Deman (1997), yaitu salah satu khamir yang digunakan dalam kegiatan fermentasi
bahan pakan adalah khamir S. cerevisiae yang bersifat aerobik. Dalam menumbuhkannya diperlukan oksigen yang cukup agar proses fermentasi
berlangsung. Selain oksigen, air dan glukosa merupakan komponen penting dalam
proses pertumbuhan khamir. Air merupakan komponen penting yang mampu
mempengaruhi besarnya laju pertumbuhan mikroba. Khamir tumbuh baik dengan
kondisi air pada substrat 70-80% (Fardiaz, 1988), oleh karena itu pada proses
fermentasi ini dilakukan penambahan air sebanyak 60% w/w dari total substrat
untuk mendukung pertumbuhan khamir karena bahan yang digunakan
mengandung air sekitar 8-14%, sementara glukosa digunakan sebagai sumber
energi bagi khamir untuk tumbuh yang diperoleh dari bahan berkarbohidrat,
karena sumber energi utama bagi khamir adalah atm C, O, dan H yang merupakan
14 enzim meliputi amilase, lipase, dan protease (Abun, 2005) yang dapat melisis
komponen karbohidrat, lemak, dan protein.
Hasil fermentasi menunjukkan peningkatan kadar protein dan penurunan
kadar serat kasar pada bahan uji yaitu kulit singkong, biji kapuk, biji karet, dan
Palm Kernel Meal (PKM). Protein kulit singkong naik sebesar 17,80% dan serat kasar turun sebesar 2,45%, protein biji karet naik 31,11% dan serat kasar turun
19,37%, protein biji kapuk naik 16,85%, dan serat kasar turun 8,21%, serta
protein PKM naik 20,92% dan serat kasar turun 31,65%. Hal ini sesuai dengan
pernyataan Oboh (2006), bahwa proses fermentasi dapat meningkatkan
kandungan nutrisi suatu bahan melalui biosintesis vitamin, asam amino essensial
dan protein, serta meningkatkan kualitas protein dan kecernaan serat. Peningkatan
protein tertinggi dan penurunan kadar serat kasar terbaik dicapai pada bahan uji
PKM yaitu masing-masing sebesar 20,92% dan -31,65%, artinya jumlah biomassa
S. cerevisiae terbesar terdapat pada PKM serta aktivitas enzimatis yang optimal terjadi pada proses fermentasi PKM, karena menurut Muhiddin et al. (2000) peningkatan protein berasal dari biomassa sel khamir yang tumbuh pada media.
Kandungan Protein Sel Tunggal (PST) pada khamir berkisar 39-65% dari total
berat kering sel (Fardiaz, 1988). Penurunan serat kasar yang cukup signifikan
diduga S. cerevisiae mengandung enzim mannanase, glukosidase, dan
galaktosidase yang cukup tinggi, karena menurut (Yopi et al., 2006) mannan merupakan komponen serat setelah selulosa dan xylan yang banyak terdapat pada
limbah perkebunan kelapa sawit. Untuk proses hidrolisa mannan tersebut, selain
mannanase juga diperlukan enzim glukosidase atau galaktosidase. Berdasarkan
hasil tersebut, diduga bahwa khamir S. cerevisiae dapat hidup dengan baik pada substrat PKM dan memperoleh nutrisi yang cukup dari PKM untuk pertumbuhan
dan perkembangannya. Sehingga, dibandingkan dengan bahan uji lainnya, S. cerevisiae lebih cocok digunakan untuk memfermentasi PKM.
Hasil yang berbeda terjadi pada kopra karena menunjukkan hasil yang
sebaliknya, serat kasar naik sebesar 18,23% setelah bahan tersebut difermentasi.
Akan tetapi, sebenarnya komponen serat yang dominan terdapat pada kopra
adalah mannan dan galaktomannan (Hatta dan Sundu, 2009) sama seperti yang
15 fermentasi PKM, seharusnya serat kasar pada kopra juga mengalami penurunan.
Namun, kondisi tersebut (kenaikan serat kasar) pada kopra diduga karena khamir
S. cerevisiae tidak mendapatkan nutrisi yang mencukupi untuk proses pertumbuhan dan perkembangannya. Hal ini berdasarkan pada pernyataan Aisjah
et al. (2007), bahwa terjadinya peningkatan serat kasar pada bahan dapat disebabkan adanya serat-serat yang berasal dari miselium kapang yang
menyebabkan peningkatan serat kasar bahan. Serat kasar dari misellium terjadi
akibat kapang yang ditumbuhkan pada media mati karena nutrisi yang dibutuhkan
untuk tumbuh tidak mencukupi dengan jumlah kapang yang tersedia. Begitu pula
dengan khamir, kekurangan nutrien pada substrat menyebabkan kematian
sehingga terjadi akumulasi biomassa sel yang mengandung serat kasar pada
dinding selnya berupa glukan (selulosa) dan mannan. Glukan dan mannan
merupakan komponen terbesar penyusun dinding sel khamir, yakni
masing-masing sekitar 30-35% dan 30% (Fardiaz, 1989b). Oleh karena itu, peningkatan
serat kasar pada kopra diduga akibat akumulasi dari sel khamir yang mati dan
proses enzimatis untuk menghidrolisis senyawa kompleks menjadi senyawa yang
lebih sederhana belum berjalan optimal akibat keterbatasan nutrien.
Nilai nutrisi dari pakan tidak hanya semata-mata berdasarkan komposisi
kimia tetapi juga berdasarkan jumlah nutrien atau energi yang dapat diserap atau
digunakan oleh ikan. Kecernaan merupakan kombinasi mekanik dan kimia pada
proses penghancuran pakan menjadi bentuk yang lebih sederhana yang siap
diserap oleh dinding usus dan masuk kedalam sistem peredaran darah melalui
serangkaian proses menggunakan enzim. Tingkat kecernaan terhadap suatu jenis
pakan bergantung kepada kualitas pakan, komposisi bahan pakan, kandungan gizi
pakan, jenis serta aktivitas enzim-enzim pencernaan pada sistem pecernaan ikan,
ukuran dan umur ikan serta sifat fisik dan kimia perairan (NAS, 1983). Umumnya
kecernaan yang diukur sebagai salah satu parameter kualitas bahan baku pakan
adalah kecernaan protein, kecernaan energi, dan kecernaan bahan.
Secara keseluruhan, nilai kecernaan protein mengalami peningkatan setelah
bahan uji difermentasi. Nilai kecernaan protein pakan dengan pemakaian 30%
PKM difermentasi mengalami peningkatan tertinggi dibandingkan dengan
16 lurus dengan hasil fermentasi dimana peningkatan protein tertinggi dan penurunan
serat kasar terbaik dihasilkan pada proses fermentasi PKM, diduga hasil tersebut
yang menyebabkan peningkatan nilai kecernaan protein bahan tersebut. Namun,
nilai kecernaan protein tertinggi diperoleh pada pakan dengan penambahan 30%
biji karet difermentasi. Hal tersebut menunjukkan bahwa protein pada biji karet
dapat dimanfaatkan dengan baik oleh juvenil ikan nila O. niloticus. Tingginya nilai kecernaan protein pakan uji biji karet yang difermentasi diduga disebabkan
oleh cukup tingginya kandungan protein dan rendahnya serat kasar yang
terkandung di dalamnya. Menurut Oyewushi et al. (2007), biji karet mengandung 21,90% protein dan 5,1% serat kasar. Berdasarkan hasil analisa proksimat,
kandungan protein biji karet setelah difermentasi sebesar 36,8% dan serat kasar
8,9%, sementara kandungan protein dalam pakan uji menggunakan 30% biji karet
fermentasi sebesar 33,4% dan serat kasar 7,1%. Kandungan serat kasar pada
pakan tersebut merupakan nilai paling rendah diantara pakan uji lainnya sehingga
termasuk memiliki kandungan serat kasar yang cukup rendah untuk bahan baku
yang bersumber dari nabati.
Peningkatan kecernaan protein terendah diperoleh pada pakan uji kulit
singkong difermentasi yaitu hanya 0,25%. Hasil ini menunjukkan bahwa proses
fermentasi menggunakan S. cervisiae tidak memberikan pengaruh yang signifikan terhadap peningkatan kecernaan nutrien kulit singkong. Hal tersebut diduga
terkait pada hasil fermentasi kulit singkong yang paling sedikit menurunkan serat
kasar dibandingkan bahan uji lainnya, yaitu 2,45%. Selain itu, diduga bahwa
komposisi nutrien yang terkandung dalam kulit singkong tidak cukup memenuhi
kebutuhan nutrisi S. cerevisiae. Menurut Aisjah et al. (2007), kandungan serat kasar produk menurun sejalan dengan meningkatnya dosis inokulum dan lama
proses fermentasi, namun lama waktu fermentasi akan menghasilkan nilai serat
kasar yang rendah jika didukung oleh nilai nutrisi dari bahan. Selain itu, diduga
bahwa komponen serat kasar yang dominan terdapat di kulit singkong yaitu lignin
tidak mampu diuraikan dengan optimal terkait jumlah enzim lignase yang minim
terdapat dalam S. cerevisiae.
Peningkatan nilai kecernaan protein pakan dengan penambahan 30% bahan
17 kasar pada bahan uji sehingga memudahkan enzim dalam saluran pencernaan ikan
memecahkan nutrien yang terkandung dalam pakan. Namun, kandungan serat
kasar pakan uji berkisar antara 7-13%, masih lebih tinggi dibadingkan kadar serat
kasar yang dianjurkan terkandung dalam pakan yaitu tidak lebih dari 5% agar
pertumbuhan ikan maksimum (Anderson et al., 1984 dalam Mjoun et al., 2010). Nilai tersebut yang kemudian membuat nilai kecernaan protein pakan uji dianggap
masih belum optimal.
Halver (1989) menyatakan bahwa faktor yang mempengaruhi kecernaan
energi pada ikan yaitu spesies, stadia, aktivitas, dan temperatur. Spesies terkait
dengan kemampuan ikan dalam memanfaatkan komponen pakan selain protein
sebagai sumber energi (protein sparing effect). Ikan lebih memanfaatkan protein dan lemak sebagai sumber energi dibandingkan karbohidrat yang disebabkan oleh
terbatasnya kemampuan ikan untuk memanfaatkan karbohidrat. Kemampuan ikan
dalam mencerna karbohidrat salah satunya dipengaruhi spesies ikan. Menurut
Pandian (1989), ikan herbivor dan ikan omnivor lebih mampu menyerap energi
yang bukan berasal dari protein. Ikan nila O. niloticus merupakan jenis ikan omnivor sehingga berdasarkan pernyataan diatas, ikan nila merupakan jenis ikan
yang mampu memanfaatkan karbohidrat lebih baik sebagai sumber energi
dibandingkan ikan karnivor seperti ikan lele Clarias sp.. Nilai kecernaan energi mengalami peningkatan hampir pada semua pakan uji setelah difermentasi kecuali
pada pakan uji kulit singkong yang mengalami penurunan. Peningkatan tertinggi
diperoleh pada pakan uji biji kapuk yaitu 11,17% diikuti oleh pakan uji PKM
sebesar 10,48%. Peningkatan kecernaan energi terjadi salah satunya disebabkan
oleh proses fermentasi, karena seperti yang telah disebutkan, fermentasi mampu
menyederhanakan senyawa kompleks menjadi lebih sederhana melalui proses
enzimatis. Akibat fermentasi pada bahan uji diduga karbohidrat telah terurai
menjadi senyawa yang lebih sederhana sehingga mampu dimanfaatkan lebih baik
oleh ikan sebagai sumber energi. Dari segi fisiologi, ikan nila merupakan ikan
omnivora yang memiliki enzim amilase dalam saluran pencernaannya sehingga
mampu mencerna karbohidrat cukup baik. Tripsin, amilase, dan esterase
ditemukan dalam saluran pencernaan tilapia (NAS, 1983). Sehingga ikan nila
18 karbohidrat lebih banyak lagi karena bantuan fermentasi. Penurunan nilai
kecernaan energi pakan uji kulit singkong setelah difermentasi sebesar 0,34%
dianggap bahwa proses fermentasi tidak memberikan pengaruh terhadap
peningkatan kecernaan energi pakan. Sama halnya dengan hasil kecernaan protein
pakan yang hanya mengalami sedikit peningkatan.
Nilai kecernaan energi pada pakan uji difermentasi masih berada pada
kisaran 66-70% pada pakan uji selain biji karet difermentasi yaitu 78%. Hal ini
menunjukkan bahwa proses fermentasi pada bahan-bahan tersebut masih belum
optimal untuk meningkatkan kecernaan energi pada bahan nabati, karena menurut
Halver (1989), ikan perairan tropis dapat mencerna sekitar 85% energi kasar yang
berasal dari tepung ikan dan sumber-sumber protein hewani lainnya yang
mengandung banyak protein dan lemak, dan hanya dapat mencerna sekitar 70%
energi kasar yang berasal dari bungkil kedelai dan bungkil biji-bijian lainnya yang
banyak mengandung karbohidrat.
Secara keseluruhan, nilai kecernaan bahan mengalami peningkatan setelah
bahan uji difermentasi. Peningkatan tertinggi diperoleh pada pakan uji PKM
fermentasi yaitu 61,19%. Peningkatan protein dan penurunan serat kasar yang
paling besar pada PKM diduga sebagai alasan tingginya persentase peningkatan
kecernaan bahan pada pakan uji PKM. Sedangkan nilai kecernaan bahan pada
pakan uji biji karet fermentasi sebesar 75,11% menunjukkan hasil yang paling
baik diantara pakan uji lainnya. Hasil tersebut berkorelasi positif terhadap nilai
kecernaan protein dan kecernaan energi yang dihasilkan, dimana kesemuanya
merupakan nilai yang tertinggi dibandingkan pakan uji lainnya. Nilai kecernaan
bahan uji biji kapuk merupakan yang paling rendah diantara bahan uji lainnya
yaitu 22,34%. Tingginya kandungan serat kasar dalam biji kapuk yang mencapai
30,93% menyebabkannya sulit untuk dicerna. Fermentasi pada biji kapuk dapat
meningkatkan kecernaan bahan sebesar 30,87%, hal ini diduga disebabkan oleh
penurunan serat kasar pada pakan yang mengandung bahan tersebut yang
mencapai -12,23% sehingga bahan tersebut lebih mudah dicerna. Nilai kecernaan
bahan pada bahan uji lainnya berkisar antara 24-62%. Hasil tersebut menunjukkan
bahwa meskipun mengalami peningkatan kecernaan, proses fermentasi
19 terdapat pada bahan-bahan uji karena masih rendahnya persentase bahan yang
dicerna oleh ikan nila O. niloticus.
Peningkatan nilai kecernaan pada pakan dengan campuran 30% bahan
difermentasi tidak hanya disebabkan oleh peningkatan protein dan penurunan
serat kasar, tetapi juga disebabkan adanya penurunan nilai zat antinutrisi pada
bahan. Seperti yang telah disebutkan sebelumnya, keberadaan zat antinutrisi
dalam bahan nabati menjadi salah satu kendala pemanfaatan bahan nabati dalam
komponen pakan. Beberapa zat faktor antinutrisi yang umum terdapat dalam
bahan nabati adalah sianogen (asam sianida, HCN), gosipol, fitat, aflatoksin, dan
tannin (Murni, et al., 2008). Kadar HCN dan fitat dapat dihilangkan melalui proses fermentasi yang menggunakan Saccharomyces cerevisiae, Lactobacillus delbruckii dan Lactobacillus coryneformis. Penurunan fitat pada proses fermentasi disebabkan adanya reaksi enzim phytase yang terdapat pada mikroorganisme yang digunakan untuk fermentasi (Oboh, 2006). Adamafio et al. (2010) menyatakan bahwa Saccharomyces cerevisiae pada bahan mampu menurunkan aktivitas linamarase yang bisa menurunkan tingkat sianogen pada kulit singkong, sehingga
pengaruh zat anti nutrisi bisa diminimalkan. Selain fermentasi, kandungan zat
antinutrisi juga dapat dihilangkan atau dikurangi jumlahnya dengan cara
pengeringan, perendaman, pengukusan, dan pengepresan (Murni, et al., 2008). Oleh karena itu, penurunan dan ketiadaan zat antinutrisi dalam bahan baku pakan
akibat pengaruh fermentasi diharapkan mampu meningkatkan kecernaan bahan
tersebut.
Dalam uji kecernaan, tidak semua perlakuan memberikan pertumbuhan
yang baik yang diduga disebabkan oleh komposisi nutrien yang tidak seimbang
pada pakan. Hal tersebut karena uji kecernaan hanya bertujuan mengukur
kecernaan suatu bahan pakan terhadap ikan. Adapun parameter pertumbuhan
hanya digunakan sebagai pembanding antar perlakuan karena untuk mencapai
pertumbuhan optimal, hubungan antara rasio kadar protein dengan energi penting
dalam nutrisi ikan. Perumbuhan optimal dicapai ketika protein yang dikandung
pakan dan energi yang disediakan oleh karbohidrat dan lemak seimbang sesuai
kebutuhan ikan. Rasio kadar protein dengan energi bervariasi tergantung umur
20 Halver, 1989). Pakan dengan kandungan protein 30-36% membutuhkan energi
sebesar 240-340 kkal/100 gram pakan untuk pertumbuhan optimal ikan mas
Cyprinus carpio, lele Clarias sp., dan nila Oreochromis sp.. Rasio antara energi dengan protein pada ikan nila yang optimum adalah 8-9 kkal DE/g protein
(Halver, 1989) Selain itu, kelengkapan mineral, asam amino esensial, dan asam
lemak dalam pakan juga mempengaruhi pertumbuhan ikan, kekurangan atau
kelebihan salah satunya bisa menyebabkan defisiensi dalam pertumbuhan ikan.
Oleh karena itu, pada penelitian ini kinerja pertumbuhan tidak menjadi parameter
utama dalam menentukan kualitas pakan.
Salah satu faktor yang mempengaruhi konsumsi pakan adalah palatabilitas,
yaitu tingkat penerimaan pakan oleh ikan (Halver, 1989). Jumlah Konsumsi Pakan
(JKP) pada pakan uji dengan penambahan 30% bahan uji yang difermentasi lebih
sedikit dari bahan uji yang tidak difermentasi. Peningkatan JKP pada perlakuan
pakan uji biji kapuk tidak menunjukkan hasil yang baik karena tingkat
palatabilitas pakan yang masih lebih rendah dari pakan uji lainnya. Peningkatan
tersebut diduga akibat pengaruh lama fermentasi yang optimal sehingga tidak
menyebabkan bau yang tidak disukai ikan. Penurunan palatabilitas terhadap pakan
uji yang difermentasi diduga diakibatkan oleh mikroba proteolitik yang memecah
protein dan komponen-komponen nitrogen lainnya sehingga menghasilkan bau
busuk yang tidak diinginkan apabila waktu fermentasi tidak terkontrol (Abun,
2005). Selain itu, aroma asam yang dikeluarkan pakan fermentasi disebabkan oleh
proses fermentasi yang menghasilkan asam juga diduga menyebabkan pakan lebih
sukar diterima oleh ikan. Asam pada fermentasi disebabkan oleh aktivitas ragi
yang menghasilkan asam-asam organik, hal ini dapat mempengaruhi pH dari
bahan yang difermentasi (Balia, 2004). Asam organik yang dihasilkan oleh
khamir sebagai produk metabolit sekunder diantaranya asam asetat, asam
propoinat, asam suksinat, dan asam laktat (Fardiaz, 1989b).
Nilai Laju Pertumbuhan Harian (LPH) pada pakan uji kulit singkong, biji
karet, kopra, dan PKM yang difermentasi lebih rendah dari bahan uji yang tidak
difermentasi. Hal ini berbanding lurus dengan jumlah konsumsi pakan. Dengan
asumsi, lebih sedikit pakan yang dikonsumsi maka energi dan protein yang masuk
21 keseimbangan rasio protein dan energi dalam pakan yang tidak dikontrol juga
dapat mempengaruhi LPH. Rasio kandungan energi dengan protein dalam pakan
juvenil ikan nila O. niloticus yang optimum adalah 8-9 kkal DE/g protein (Halver, 1989) sementara C/P pakan uji berkisar antara 12-18 kkal DE/g protein, artinya
terjadi kelebihan kandungan energi dalam pakan uji yang digunakan. Peningkatan
LPH pada pakan uji biji kapuk difermentasi diduga disebabkan oleh penurunan
pengaruh gosipol akibat fermentasi oleh S. cerevisiae. Adanya kandungan gosipol dalam pakan ikan akan menurunkan laju pertumbuhan ikan dan penurunan
pemanfaatan pakan oleh ikan untuk pertumbuhan (NAS, 1983).
Nilai konversi pakan (Feed Conversion Ratio, FCR) dapat menggambarkan efisiensi suatu pakan untuk pertumbuhan. Pertumbuhan yang lebih tinggi dari
konsumsi pakan yang lebih rendah menunjukkan penggunaan pakan yang lebih
efisien. Nilai FCR pakan uji fermentasi lebih kecil dari pakan uji yang tidak
difermentasi kecuali pada pakan uji kulit singkong, artinya beberapa pakan uji
difermentasi lebih efisien. Hasil tersebut berbanding lurus dengan perubahan nilai
kecernaan energi, kecernaan protein, dan kecernaan bahan setelah difermentasi.
Nilai kecernaan yang meningkat akibat fermentasi menunjukkan ikan nila lebih
mampu memanfaatkan nutrien dari bahan yang difermentasi untuk pertumbuhan.
Sintasan pada perlakuan pakan uji kopra 83,33%, biji kapuk 66,67%, dan
biji kapuk fermentasi 83,33%, sementara untuk perlakuan lainnya 100%.
Kematian pada perlakuan pakan uji kopra diduga akibat ikan terserang penyakit
yang ditandai dengan ciri-ciri ikan yang bergerak lemas kepermukaan dengan
warna tubuh ikan sedikit pucat. Kematian pada perlakuan pakan kopra tanpa
fermentasi tidak disebabkan oleh pengaruh pakan, karena ikan lainnya pada
perlakuan tersebut mampu tumbuh dengan baik yang salah satunya dicirikan oleh
nilai LPH sebesar 2,89%. Sementara kematian pada perlakuan pakan uji biji
kapuk diduga diakibatkan oleh adanya zat antinutrisi yaitu gosipol bebas dalam
pakan ikan, karena menurut (NAS, 1983) gosipol mampu menyebabkan kematian
pada ikan. Sementara itu, nilai sintasan perlakuan pakan biji kapuk fermentasi
yang lebih tinggi dibandingkan perlakuan pakan biji kapuk diduga akibat
22 Kulit Singkong, biji karet, kopra, biji kapuk, dan PKM berpotensi untuk
dikembangkan dan mampu dimanfaatkan lebih baik melalui proses fermentasi
menggunakan S. cerevisiae. Kelima bahan tersebut memiliki nilai kecernaan yang baik pada ikan nila O. niloticus. Berdasarkan lima bahan diatas, bahan yang berpotensi besar untuk dikembangkan yaitu PKM. Produksi PKM yang melimpah
(2.829.201 ton) pada tahun 2009 (BPS, 2008), nilai kecernaannya yang tinggi, dan
palatabilitas yang baik menjadikan bahan ini berpotensi untuk dikembangkan
selanjutnya sebagai bahan baku pakan. Kecernaan PKM meningkat setelah
mengalami proses fermentasi, oleh karena itu dalam pemanfaatanya perlu
didukung dengan pengembangan teknologi pengolahan bahan termasuk
fermentasi. Selain PKM, urutan bahan lainnya yang berpotensi untuk
dikembangkan sebagai bahan baku pakan adalah biji karet, kulit singkong, kopra
23
IV.
KESIMPULAN
4.1 Kesimpulan
Fermentasi kulit singkong, biji karet, kopra, biji kapuk, dan bungkil kelapa
sawit (Palm Kernel Meal, PKM) dengan Saccharomyces cerevisiae mampu menurunkan serat kasar sebesar 2,45-31,65% dan meningkatkan protein sebesar
16,85-31,11%. Fermentasi juga mampu meningkatkan kecernaan protein sebesar
1,94-11,07%, kecernaan energi 4,29-11,17% dan kecernaan bahan uji sebesar
6,83-61,19% pada juvenil ikan nila Oreochromis niloticus. Namun fermentasi tidak memberikan pengaruh yang signifikan terhadap peningkatan kecernaan kulit
singkong. Bahan baku yang paling efektif digunakan dalam proses fermentasi
menggunakan S. cerevisiae adalah PKM.
4.2 Saran
Saran yang dapat diberikan dari hasil penelitian ini adalah perlunya
dilakukan penelitian lanjutan untuk menentukan jumlah bahan uji dalam pakan
yang dapat menggantikan sebagian perananan protein nabati dan sumber
karbohidrat untuk mencapai pertumbuhan optimal, efisiensi pakan tinggi, dan
24
DAFTAR PUSTAKA
Abun. 2005. Efek suplementasi produk fermentasi dalam ransum terhadap komponen darah kelinci. [Makalah Ilmiah]. Departemen Nutrisi dan Makanan Ternak, Fakultas Peternakan, Universitas Padjajaran, Bandung. p. 14-17.
Adamafio N.A., Sakyiamah M., Tettey J. 2010. Fermentation in casasava (Manihot esculenta crantz) pulp juice improve nutritive value of cassava peel. Biochemistry 4 (3), 51-58.
Aisjah T., Widjastuti T., Tanuwiria H., Abun. 2007. Suplementasi mineral Zn dan Cu melalui bioproses oleh Saccharomyces cerevisiae sebagai imbuhan pakan dan implementasinya pada pertumbuhan ayam broiler. [Artikel Ilmiah]. Departemen Nutrisi dan Makanan Ternak, Fakultas Peternakan, Universitas Padjajaran, Bandung. p. 3-15.
Azaza M.S., et al. 2009. Nutritional evaluation of waste date fruit as partial substitute for soybean meal in practical diets of juvenil nile tilapia
Oreochromis niloticus. Aquaculture Nutrition 15, 262-272.
[BPS] Badan Pusat Statistik. 2008. Produksi perkebunan besar menurut jenis
tanaman, Indonesia (ton) 1995-2008.
http://www.bps.go.id/tab_sub/view.php?tabel=1&daftar=1&id_subyek=54& notab=2 [23 Desember 2010].
Balia R.L., 2004. Potensi dan prospek yeast (khamir) dalam meningkatkan diversifikasi pangan di Indonesia. Pidato Pengukuhan Jabatan Guru Besar Tetap dalam Ilmu Mutu Pangan. Fakultas Peternakan, Universitas Padjajaran. Bandung. p. 10-22.
Dairo F.A.S., dan Fasuyi A.O. 2007. Evaluation of fermented palm kernel meal and fermented coprameal proteins as substitute for soybean meal protein in laying hens diets. Central European Agriculture 9 (1), 35-44.
Deman J.M. 1997. Kimia Makanan. Terjemahan dari: Food chemistry. Penerjemah Kosasih Padmawinata. Edisi Kedua. Gadjah Mada University Press, Yogyakarta.
Ezieshi E.V., Olomu J.M. 2007. Nutritional evaluation of palm kernel meal types:1. proximate composition and metabolizable energi values. Biotechnology 6 (21), 2484-2486.
25 Fardiaz S. 1989b. Mikrobiologi Pangan. Pusat Antar Universitas Pangan dan Gizi,
Institut Pertanian Bogor. p. 224.
Halver J.E. 1989. Fish Nutrition. 2nd Edition. Academic Press. London. p. 1-23.
Hatta U., Sundu B. 2009. Effects of copra meal fermented by Aspergillus niger
and Trichoderma spp. on performance of broiler. [Artikel Ilmiah]. Di dalam: The 1st International Seminar on Animal Industry. Bogor. p. 332-335.
Hertrampf J.W., dan Pascual F.P. 2000. Handbook Ingredients For Aquaculture Feeds. Kluwer Academic Publishers. London. p. 445-454.
Mjoun K., Rosentrater K.A., Brown M.L. 2010. Tilapia: Environmental Biology and Nutritional Requirements. [Artikel Ilmiah]. Department of Wildlife and Fisheries Sciences. South Dakota State University. Brookings. p. 1-5.
Muhiddin N.H., Juli N., Aryantha I.N.P. 2001. Peningkatan kandungan kulit ubi kayu melalui proses fermentasi. JMS 6, 2.
Murni R., Suparjo, Akmal, Ginting B.L. 2008. Buku Ajar Teknologi Pemanfaatan Limbah Untuk Pakan. Laboratorium Makanan Ternak, Fakultas Peternakan, Universitas Jambi. Jambi.
[NAS] National Academy of Science. 1983. Nutrient requirement of warmwater fish and shellfish. Revised Edition. National Academic Press, Washington DC, pp. 1-50.
[NRC] Nutritional Research Council. 1993. Nutrient Requirement of Fish. National Academic Press, Washington DC, pp. 43-44.
Oboh G. 2006. Nutrient enrichment of Cassava peels using a mixed culture of
Saccharomyces cerevisae and Lactobacillus spp. Solid media fermentation techniques. Biotechnology 9 (1), 46-48.
Oyewushi P.A., Akintayo E.T., Olaofe O. 2007. The proximate and amino acid composition of defatted rubber seed meal. Journal of Food, Agriculture & Environment 5 (3-4), 115-118.
Pamungkas W. 2010. Teknologi Fermentasi, Alternatif Solusi Dalam Upaya Pemanfaatan Bahan Pakan Alternatif. [Artikel Ilmiah]. Loka Riset Pemuliaan dan Teknologi Budidaya Perikanan Air Tawar. Sukamandi. Jawa Barat.
26 Sari L., Perwadaria T. 2004. Pengkajian nilai gizi hasil fermentasi mutan
Aspergillus niger pada substrat bungkil kelapa dan bungkil inti sawit. Biodiversitas 5 (2), 48-51.
Silva D. 1989. Digestibility evaluations of natural and artificial diets, p. 36-45. In
S.S. De Silva (ed.) Fish Nutrition Research in Asia. Proceedings of the Third Asian Fish Nutrition Network Meeting. Asian Fish. Soc. Spec. Pubhl.4, 166 p. Asian Fisheris Society, Manila, Philippines.
Sundu B., Kumar A., Dingle J. 2006. Response of broiler chicks fed increasing levels of copra meal and enzymes. Poultry Science 5 (1), 13-18.
Suprayudi M.A. 2010. Bahan Baku Pakan Lokal. Tantangan dan Harapan Akuakultur Indonesia. Abstrak. Simposium Nasional Bioteknologi Akuakultur III. IPB International Convention Center, Bogor, Oktober 2010, p.31.
Takeuchi T. 1988. Laboratory Work Chemical Evaluation of Dietary Nutriens. In: Fish Fish Nutrition and Mariculture. Watanabe, T. Department of Aquatic Biosience. Tokyo University of Fisheries. JICA p. 179-226.
Watanabe T. 1988. Fish Nutrition and Mariculture. Department of Aquatic Biosience. Tokyo University of Fisheries. JICA. p. 79-82.
Webster C.D. and Liem C. 2002. Nutrient Requirements and Feeding of Finfish for Aquaculture. Aquaculture Research Center. Kentucky State University. p. 245-258.
27
LAMPIRAN
Lampiran 1. Metode fermentasi
Tahapan fermentasi bahan uji yang dilakukan pada penelitian ini adalah:
1. Bahan uji ditimbang sebanyak 400 gram dan khamir S. cerevisiae 3,6 gram, 2. Dicampur dan diaduk hingga khamir tersebar merata,
3. Dicampur air sebanyak 60%, khamir dan bahan uji diaduk merata,
4. Bahan diletakkan pada wadah plastik dibiarkan dalam kondisi aerob (penutup
wadah dibuat sirkulasi udara),
5. Inkubasi pada suhu kamar selama satu hari (24 jam).
Lampiran 2. Pembuatan pakan perlakuan untuk 600 g pakan
1. Pakan komersil dihaluskan
2. Bahan uji sebanyak 30% dari total pakan (180 g) dicampurkan ke dalam 399 g
pakan komersil, kemudian di aduk rata
3. Sebanyak 3 g Cr2O3 dicampurkan ke dalam pakan, aduk merata.
4. Tambahkan air 600 ml air panas ke dalam wadah berisi 18 g binder (sagu), aduk merata
5. Campurkan binder pada adonan pakan, aduk merata.
6. Pakan dicetak sesuai ukuran, dan dioven selama 4-5 jam pada suhu 60 ⁰C.
Lampiran 3. Skema tata letak akuarium perlakuan
Keterangan :
A = Pakan uji kulit singkong, B = Pakan uji biji karet, C = Pakan uji kopra, D = Pakan uji biji kapuk, E = Pakan uji PKM, F = Pakan pembanding, A1 = Pakan uji kulit singkong fermentasi B1 = Pakan uji biji karet fermentasi, C1 = Pakan uji kopra fermentasi, D1 = Pakan uji biji kapuk fermentasi, E1 = Pakan uji PKM fermentasi.
TANDON
A C
B1
F C1 E1 B
28 Lampiran 4. Data kualitas air pada awal dan akhir pemeliharaan ikan perlakuan
Parameter Nilai Satuan
Lampiran 5.1 Prosedur analisis kadar air
�� = +� −
� � %
Lampiran 5.2 Prosedur analisis kadar serat kasar
Larutan disaring dengan bahan pembilasan secara berurutan sebagai berikut:
1. 50 ml air panas 2. 50 ml H2SO4
3. 50 ml air panas 4. 25 ml aceton
Dipanaskan pada suhu 105-110 0C selama 1 jam, didinginkan, dan ditimbang (X2)
Dipanaskan dalam tanur pada suhu 600 0C hingga berwarna putih, didinginkan, dan ditimbang (X3)
Kertas saring dipanaskan pada labu Buchner yang telah terhubung dengan
vacumm pump Bahan ditimbang 0,5 gr (A), lalu dimasukkan ke
dalam Erlenmeyer 250 ml
50 ml H2SO4 0,3 N ditmbahkan dalam Erlenmeyer,
lalu dipanaskan di atas hotplate
Setelah 30 menit ditambahkan 25 ml NaOH 1,5 N, lalu dipanaskan kembali selama 30 menit
Kertas saring dipanaskan dalam oven,
Cawan porselen dipanaskan pada suhu 105-110 0Cselama 1 jam, dan kemudian
didinginkan dalam desikator dan ditimbang (X1)
Bahan ditimbang 2-3 gr (A) lalu dimasukkan ke dalam cawan