UJI TOKSISITAS AKUT EKSTRAK DAUN KAMBOJA
(
Plumiera rubra
L.) PADA IKAN NILA MERAH
(
Oreochromis niloticus
)
RANGGA WARSITO
100302069
PROGRAM STUDI MANAJEMEN SUMBERDAYA
PERAIRAN
FAKULTAS PERTANIAN
UJI TOKSISITAS AKUT EKSTRAK DAUN KAMBOJA
(
Plumiera rubra
L.) PADA IKAN NILA MERAH
(
Oreochromis niloticus
)
SKRIPSI
RANGGA WARSITO
100302069
PROGRAM STUDI MANAJEMEN SUMBERDAYA
PERAIRAN
FAKULTAS PERTANIAN
UJI TOKSISITAS AKUT EKSTRAK DAUN KAMBOJA
(
Plumiera rubra
L.) PADA IKAN NILA MERAH
(
Oreochromis niloticus
)
SKRIPSI
RANGGA WARSITO
100302069
Skripsi sebagai satu diantara beberapa syarat untuk memperoleh gelar Sarjana Perikanan di Program Studi Manajemen Sumberdaya Perairan,
Fakultas Pertanian, Universitas Sumatera Utara, Medan
PROGRAM STUDI MANAJEMEN SUMBERDAYA
PERAIRAN
FAKULTAS PERTANIAN
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Saya yang bertanda tangan dibawah ini : Nama : Rangga Warsito
Nim : 100302069
Menyatakan bahwa skripsi yang berjudul “Uji Toksisitas Akut Ekstrak Daun Kamboja (Plumiera rubra L.) pada Ikan Nila Merah (Oreochromis niloticus)” adalah benar merupakan hasil karya saya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Medan, Maret 2015
LEMBAR PENGESAHAN
Judul Penelitian : Uji Toksisitas Akut Ekstrak Daun Kamboja (Plumiera rubra L.) pada Ikan Nila Merah (Oreochromis niloticus) Nama Mahasiswa : Rangga Warsito
NIM : 100302069
Program Studi : Manajemen Sumberdaya Perairan
Disetujui oleh : Komisi Pembimbing
Dr. Ir. Yunasfi, M.Si Zulham Apandy Harahap S.Kel, M.Si Ketua Anggota
Mengetahui
Dr. Ir. Yunasfi, M.Si
Ketua Program Studi Manajemen Sumberdaya Perairan
ABSTRAK
RANGGA WARSITO. Uji Toksisitas Akut Ekstrak Daun Kamboja (Plumiera
rubra L.) pada Ikan Nila Merah (Oreochromis niloticus). Dibimbing oleh
YUNASFI dan ZULHAM APANDY HARAHAP.
Budidaya ikan yang dilakukan secara intensif sangat rentan terserang wabah penyakit. Penggunaan antibiotik dalam pencegahan penyakit bakterial dapat menimbulkan efek negatif bagi kesehatan manusia. Antibiotik dapat digantikan dengan penggunaan ekstrak tumbuhan yang mengandung senyawa antibakteri, salah satunya daun kamboja (Plumiera rubra L.). Penelitian ini bertujuan untuk mengetahui nilai LC50 dalam 96 jam dan konsentrasi aman dari ekstrak daun kamboja terhadap benih ikan nila merah. Penelitian terbagi atas dua tahap, yaitu uji pendahuluan dan uji defenitif. Uji pendahuluan dilakukan untuk mengetahui konsentrasi ambang atas dan ambang bawah, dimana konsentrasi uji pendahuluan yaitu 0 ppm, 50 ppm, 100 ppm, 200 ppm, dan 750 ppm. Uji defenitif menggunakan konsentrasi 0 ppm; 98,40 ppm; 193,65 ppm; 381,10 ppm; dan 750,00 ppm yang didapatkan dari perhitungan berdasarkan konsentrasi ambang atas sebesar 750 ppm dan ambang bawah sebesar 50 ppm. Persentase mortalitas ikan nila merah pada uji pendahuluan dari konsentrasi terendah sampai tertinggi sebesar 3,33%; 16,67%; 46,67%; dan 76,67%. Persentase mortalitas diubah kedalam bentuk probit dan digunakan dalam analisis probit sehingga didapatkan nilai LC50 dalam 96 jam sebesar 510,63 ppm. Konsentrasi aman sebesar 10% dari LC50 dalam 96 jam, yaitu 50,2 ppm. Nilai LC50 dalam 96 jam menunjukkan bahwa ekstrak daun kamboja termasuk dalam kategori toksisitas sedang.
ABSTRACT
RANGGA Warsito. Acute Toxicity Test Extract Frangipani Leaves (Plumiera rubra L.) on the Red Tilapia (Oreochromis niloticus). Guided by YUNASFI and ZULHAM APANDY HARAHAP.
Fish farming is done intensively highly susceptible to outbreaks of diseas. The use of antibiotics in the prevention of bacterial diseases can cause negative effects to human health. Antibiotics can be replaced with the use of plant extracts containing antibacterial compounds, one of which leaves frangipani (Plumiera rubra L.). This study aims to determine the 96-hour LC50 value and safe concentration of frangipani leaf extract of red tilapia fish seeds. The study is divided into two stages, namely the preliminary test and the definitive test. Preliminary test was conducted to determine threshold concentrations above and below the threshold, where the concentration of the preliminary test is 0 ppm, 50 ppm, 100 ppm, 200 ppm, and 750 ppm. Definitive test using a concentration of 0 ppm; 98,40 ppm; 193,65 ppm; 381,10 ppm; and 750,00 ppm were obtained from calculations based on the threshold concentration of 750 ppm and below the threshold of 50 ppm. Percentage mortality of red tilapia in a preliminary test of the lowest to highest concentration of 3,33%; 16,67%; 46,67%; and 76,67%. Percentage mortality converted into the form used in the probit and probit analysis to obtain the 96-hour LC50 value of 510,63 ppm. Safe concentration of 10% of the LC50 within 96 hours, which is 50,2 ppm. In the 96-hour LC50 valuesindicate that the leaf extract of frangipani included in the category of moderate toxicity.
RIWAYAT HIDUP
Penulis lahir di Kota Medan, Provinsi Sumatera Utara pada tanggal 06 Januari 1993, dari Ayahanda Nanang Sumarsono S.Sos. dan Ibunda Basariyah. Penulis merupakan anak pertama dari dua bersaudara.
Penulis mengawali pendidikan formal di TK Arafah pada tahun 1997 – 1998. Pada tahun 1998 – 2004, penulis melanjutkan pendidikan di SD Negeri 068003 Medan dan pendidikan menengah pertama ditempuh dari tahun 2004 – 2007 di SMP Negeri 10 Medan. Penulis menyelesaikan pendidikan menengah atas di SMA Negeri 5 Medan dengan jurusan IPA pada tahun 2007 – 2010.
Penulis melanjutkan pendidikan di Program Studi Manajemen Sumberdaya Perairan Fakultas Pertanian, Universitas Sumatera Utara melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN). Penulis melaksanakan Praktik Kerja Lapangan (PKL) di Balai Benih Ikan Air Laut Aceh.
KATA PENGANTAR
Puji dan syukur penulis Ucapkan ke Hadirat Allah SWT atas karunia dan rahmat Nya, sehingga penulis dapat menyelesaikan Tugas Akhir Skripsi dengan judul “Uji Toksisitas Akut Ekstrak Daun Kamboja (Plumiera rubra L.) pada
Ikan Nila Merah (Oreochromis niloticus)”. Skripsi ini merupakan tugas akhir dalam menyelesaikan studi pada Program Studi Manajemen Sumberdaya Perairan, Fakultas Pertanian, Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih kepada ayahanda Nanang Sumarsono, S.Sos. dan Ibunda Basariyah yang telah memberikan dukungan moral maupun materil sehingga penulis dapat menyelesaikan skripsi ini.
Ucapan terima kasih juga penulis sampaikan kepada Bapak Dr. Ir. Yunasfi, M.Si selaku ketua komisi pembimbing sekaligus Ketua Program Studi Manajemen Sumberdaya Perairan dan Bapak Zulham Apandy Harahap, S.Kel, M.Si selaku anggota komisi pembimbing yang telah memberikan arahan dan ilmu yang berharga bagi penulis dalam penyelesaian skripsi ini.
mutu di UPTD Budidaya Dinas Pertanian dan Kelautan Kota Medan yang telah banyak membantu penulis dalam segala kegiatan penelitian yang dilakukan.
Penulis juga mengucapkan terima kasih kepada Sarah Diba Sandy sebagai seseorang yang paling dekat dengan penulis yang telah banyak membantu dalam penelitian dan penulisan skripsi ini. Terima kasih kepada Henny Christien dan Parlinggoman Sianturi, serta seluruh teman-teman seperjuangan diangkatan 2010 Program Studi Manajemen Sumberdaya Perairan.
Terima kasih juga penulis ucapkan kepada kakanda Rico Febri, Dedi Ismail Siregar, Novi Karlina, Erma Esikari, dan semua pegawai UPTD Budidaya Dinas Pertanian dan Kelautan Kota Medan; kakanda Wan Nita Ulfani Barus dan semua mahasiswa Manajemen Sumberdaya Perairan angkatan 2009 yang telah memberikan masukan bagi skripsi ini; serta kepada berbagai pihak yang telah banyak membantu penulis dalam menyelesaikan skripsi ini.
Penulis berharap semoga skripsi ini bermanfaat dalam pengembangan ilmu pengetahuan khususnya dala bidang manajemen sumberdaya perairan.
Medan, Maret 2015
DAFTAR ISI
Halaman
ABSTRAK ... i
ABSTRACT ... ii
RIWAYAT HIDUP ... iii
KATA PENGANTAR ... iv
DAFTAR ISI ... vi
DAFTAR GAMBAR ... viii
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 2
Kerangka Pemikiran ... 2
Tujuan Penelitian ... 4
Manfaat Penelitian ... 4
Hipotesis ... 4
TINJAUAN PUSTAKA ... 5
Kamboja (Plumiera rubra) ... 5
Ikan Nila Merah (Oreochromis niloticus) ... 7
Kualitas Air ... 9
Oksigen Terlarut ... 9
pH ... 12
Toksisitas ... 12
METODE PENELITIAN ... 17
Waktu dan Tempat Penelitian ... 17
Bahan dan Alat ... 17
Metode Penelitian... 17
Prosedur Penelitian... 18
Ekstraksi Daun Kamboja ... 18
Pembuatan Larutan Uji ... 18
Pengujian Fenolik ... 18
Pengujian Alkaloid ... 19
Pengujian Terpenoid/Steroid ... 19
Pengujian Saponin ... 19
Pengujian Flavonoid ... 20
Aklimatisasi Hewan Uji ... 20
Persiapan Wadah ... 20
Uji Pendahuluan ... 20
Uji Defenitif ... 21
Analisis Data ... 22
Mortalitas ... 22
LC50 ... 22
Analisis Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO ... 23
HASIL DAN PEMBAHASAN ... 24
Hasil ... 24
Uji Fitokimia Daun Kamboja ... 24
Uji Pendahuluan ... 24
Uji Defenitif ... 26
Persentase Mortalitas ... 27
Analis Probit ... 27
Analisis Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO ... 28
Pembahasan ... 30
Uji Fitokimia Daun Kamboja ... 30
Uji Pendahuluan ... 31
Uji Defenitif ... 32
LC50 dalam 96 Jam ... 33
Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO... 34
KESIMPULAN DAN SARAN ... 36
Kesimpulan ... 36
Saran ... 36
DAFTAR PUSTAKA ... 37
DAFTAR GAMBAR
No. Teks Halaman
1. Kerangka Pemikiran Penelitian ... 3
2. Kamboja (Plumeria rubra L.) ... 5
3. Benih Ikan Nila Merah ... 8
4. Diagram Uji Pendahuluan ... 25
DAFTAR TABEL
No. Teks Halaman 1. Contoh Kepekatan Minimum Oksigen Terlarut
yang Diterima dalam Air Tawar ... 9
2. Toksisitas Berdasarkan LC50 ... 15
3. Hasil uji fitokimia ekstrak daun kamboja ... 24
4. Kualitas Air Uji Defenitif ... 27
5. Persentase Mortalitas Ikan Uji ... 27
6. Analisis Probit Konsentrasi Ekstrak Daun Kamboja terhadap Ikan Nila ... 28
7. Kesimpulan Model ... 28
8. Anovab ... 29
DAFTAR LAMPIRAN
No. Teks Halaman
1. Alat dan Bahan Penelitian ... 41
2. Uji Fitokimia ... 46
3. Uji Pendahuluan dan Uji Defenitif ... 47
4. Mortalitas Ikan ... 49
5. Kualitas Air ... 51
PENDAHULUAN
Latar Belakang
Ikan nila merupakan jenis ikan konsumsi air tawar dengan bentuk tubuh memanjang dan pipih kesamping dan warna putih kehitaman. Ikan nila berasal dari Sungal Nil dan danau-danau sekitarnya. Sekarang ikan ini telah tersebar ke negara-negara di lima benua yang beriklim tropis dan subtropis. Sedangkan di wilayah yang beriklim dingin, ikan nila tidak dapat hidup baik Ikan nila disukai oleh berbagai bangsa karena dagingnya enak dan tebal seperti daging ikan kakap merah (Menegristek, 2001).
Menurut Mariyono dan Sundana (2002), untuk memenuhi permintaan produk perikanan yang terus meningkat, penerapan intensifikasi budidaya tidak dapat dihindarkan. Namun, intensifikasi budidaya dapat menimbulkan berbagai dampak negatif antara lain penyakit. Penyakit yang sering muncul pada usaha budidaya ikan air tawar adalah Motile Aeromonas Septicemia (MAS), penyakit akibat infeksi bakteri Aeromonashydrophila.
Daun Kamboja (Plumiera rubra L.) pada Ikan Nila Merah (Oreochromis niloticus)”.
Perumusan Masalah
Apakah konsentrasi uji invitro dapat digunakan pada uji invivo dengan hewan uji ikan nila merah (Oreochromis niloticus).
1. Berapakah konsentrasi maksimum ekstrak daun kamboja yang masih aman untuk ikan nila.
2. Berapakah nilai LC50 ekstrak daun kamboja terhadapa ikan nila dan kategori toksisitasnya.
Kerangka Pemikiran
Budidaya yang dilakukan secara intensif sangat rentan terserang wabah penyakit. Tingkat kepadatan ikan yang sangat padat dalam satu kolam sangat mempengaruhi kualitas air dalam kolam. Kualitas air yang buruk akan menyebabkan ikan mudah stress. Stress berhubungan dengan penurunan daya tahan tubuh ikan. Ikan yang masih berukuran benih lebih mudah stress sehingga sering terserang penyakit seperti Motile Aeromonas Septicemia (MAS).
berkemungkinan pada konsentrasi tertentu dapat juga membunuh ikan budidaya terutama pada ukuran benih.
Ikan yang digunakan dalam uji lethal concentration (LC50) adalah ikan nila merah. Ikan nila digunakan karena salah satu ikan yang dapat menjadi bioindikator dan sedikit lebih tahan penyakit. Menurut Suyanto (1998) diacu oleh Alamsyah (2007), penggunaan ikan Nila sebagai bioindikator karena bersifat respiroregulator, osmoregulator, euryhaline dan bukan labirynthici, sehingga ikan ini termasuk dalam ikan yang mempunyai daya tahan sedang terhadap perubahan lingkungannya termasuk adanya perubahan-perubahan akibat adanya pencemaran, sehingga dapat mewakili jenis-jenis ikan lain yang lebih tahan terhadap perubahan lingkungan. Kerangka pemikiran dapat dilihat pada Gambar 1.
Gambar 1. Skema Kerangka Pemikiran Penelitian Budidaya Ikan Nila Merah
Penyakit
Penyakit Bakterial
Ekstrak Daun Kamboja
Hama Kualitas Air
Uji LC50 dalam (96 Jam)
Tujuan Penelitian
Tujuan dari penelitian adalah :
1. Mengetahui nilai LC50 dalam 96 jam dari ekstrak daun kamboja terhadap benih ikan nila merah dan kategori toksisitasnya.
2. Mengetahui rentang konsentrasi yang aman dari ekstrak daun kamboja untuk benih ikan nila merah.
Manfaat Penelitian
Manfaat yang diharapkan pada penelitian adalah memberikan informasi mengenai nilai LC50 atau pada konsentrasi berapakah dapat mematikan setengah dari hewan uji dan rentang konsentrasi aman dari ekstrak daun kamboja terhadap ikan nila merah yang dapat digunakan sebagai zat antibakteri.
Hipotesis
Hipotesis yang diajukan dalam penelitian adalah :
1. Ekstrak daun kamboja dapat digunakan sebagai antibakteri dan tidak bersifat toksik dalam konsentrasi rendah.
TINJAUAN PUSTAKA
Kamboja (Plumiera rubra)
Kamboja merupakan salah satu jenis bunga yang banyak ditanam di Indonesia, khususnya pulau Jawa dan Bali cukup banyak ditemukan pohon kamboja. Bunga kamboja merupakan bunga yang berbau sangat harum dan cukup awet (Kumari dkk., 2012). Bunga ini sering digunakan pada acara-acara adat juga keagamaan karena mengeluarkan aroma yang khas dan warnanya yang indah (Megawati dan Saputra, 2012).
Gambar 2. Kamboja (Plumeria rubra L.) Klasifikasi kamboja menurut ITIS (2014):
Kingdom : Plantae
Superorder : Asteranae Order : Gentianales Family : Apocynaceae Genus : Plumeria L. Species : Plumeria rubra L.
Menurut Syamsulhidayat dan Hutapea (1991), akar dan daun (Plumeria
acuminate, W.T.Ait) mengandung senyawa saponin, flavonoid, dan
polifenol, selain itu daunnya juga mengandung alkaloid. Daun kamboja (Plumeria acuminata) mengandung senyawa saponin, flavonoid, polifenol, dan alkaloid. Tumbuhan ini juga mengandung minyak atsiri yang kandungannya terdiri atas geraniol, farsenol, sitronela, fenetilalkohol, dan linalool (Samuel dan Shelburne, 2004).
Hasil penelitian Barus (2013), perbedaan dosis esktrak daun kamboja menyebabkan perbedaan kandungan senyawa antibakteri dalam media uji dan perbedaan tekanan osmosis antara cairan di dalam dengan di luar sel bakteri yang menyebabkan perbedaan daya hambat terhadap pertumbuhan bakteri. Daya hambat terbesar dijumpai pada perlakuan dosis ekstrak 10% dengan diameter zona hambatnya 12.2 mm, sedangkan dosis hambat minimal adalah 2 % dengan zona hambat 6.4 mm.
Ikan Nila Merah (Oreochromis niloticus)
Ikan nila merupakan jenis ikan konsumsi air tawar dengan bentuk tubuh memanjang dan pipih kesamping dan warna putih kehitaman. Ikan nila berasal dari Sungal Nil dan danau-danau sekitarnya. Sekarang ikan ini telah tersebar ke negara-negara di lima benua yang beriklim tropis dan subtropis. Sedangkan di wilayah yang beriklim dingin, ikan nila tidak dapat hidup baik Ikan nila disukai oleh berbagai bangsa karena dagingnya enak dan tebal seperti daging ikan kakap merah (Menegristek, 2001).
Gambar 3. Benih Ikan Nila Merah
Klasifikasi ikan nila menurut Luna (2015) adalah sebagai berikut: Kelas : Osteichthyes
Sub-kelas : Acanthoptherigii Ordo : Perciformes Famili : Cichlidae Genus : Oreochromis
Spesies : Oreochromis niloticus
Kualitas Air Oksigen Terlarut
Oksigen terlarut (Dissolved Oxygen = DO) dibutuhkan oleh semua jasad hidup untuk pernapasan, proses metabolisme atau pertukaran zat yang kemudian menghasilkan energi untuk pertumbuhan dan pembiakan. Disamping itu, oksigen juga dibutuhkan untuk oksidasi bahan-bahan organik dan anorganik dalam proses aerobik. Sumber utama oksigen dalam suatu perairan berasal sari suatu proses difusi dari udara bebas dan hasil fotosintesis organisme yang hidup dalam perairan tersebut (Salmin, 2000 diacu oleh Salmin, 2005).
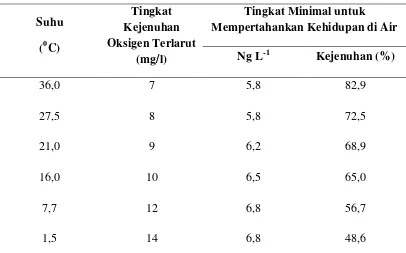
Tabel 1. Contoh Kepekatan Minimum Oksigen Terlarut yang Diterima dalam Air Tawar
Suhu (0C)
Tingkat Kejenuhan Oksigen Terlarut
(mg/l)
Tingkat Minimal untuk Mempertahankan Kehidupan di Air
Ng L-1 Kejenuhan (%)
36,0 27,5 21,0 16,0 7,7 1,5 7 8 9 10 12 14 5,8 5,8 6,2 6,5 6,8 6,8 82,9 72,5 68,9 65,0 56,7 48,6 Sumber: USEPA (1972) diacu oleh Connell dan Miller (1995)
adanya respirasi dan pembusukan bahan organik pada dasar perairan (Department of Primary Industries and Resources of South Australia, 2003).
Kandungan oksigen terlarut (DO) minimum adalah 2 ppm dalam keadaan nornal dan tidak tercemar oleh senyawa beracun (toksik). Kandungan oksigen terlarut minimum ini sudah cukup mendukung kehidupan organisme (Swingle, 1968 diacu oleh Salmin 2005). Idealnya, kandungan oksigen terlarut tidak boleh kurang dari 1,7 ppm selama waktu 8 jam dengan sedikitnya pada tingkat kejenuhan sebesar 70 % (Huet, 1970 diacu oleh Salmin 2005).
Oksigen berperan sebagai pengoksidasi dan pereduksi bahan kimia beracun menjadi senyawa lain yang lebih sederhana dan tidak beracun. Disamping itu, oksigen juga sangat dibutuhkan oleh mikroorganisme untuk pernapasan. Organisme tertentu, seperti mikroorganisme, sangat berperan dalam menguraikan senyawa kimia beracun menjadi senyawa lain yang lebih sederhana dan tidak beracun (Salmin, 2005).
Konsentrasi oksigen terlarut juga dipengaruhi oleh faktor biologis seperti kepadatan organisme perairan, karena semakin padat organisme perairan maka laju respirasi juga akan semakin meningkat. Adanya peningkatan respirasi tersebut akan menyebabkan berkurangnya oksigen terlarut di dalam air (Schramm, 1997).
Tetapi jika pengambilan oksigen tidak cukup, akan terjadi kegiatan otot yang tidak cukup seringkali akan menyebabkan kematian makhluk hidup tersebut (Erichsen Jones, 1964 diacu oleh Connell dan Miller, 1995).
Jika zat-zat yang kaya karbon organik ditambahkan ke dalam sistem, beberapa jalur meningkat jaraknya dan juga beberapa sumber karbon organik meningkat ukurannya. Ini mengakibatkan meningkatnya pernapasan, terutama melalui pernapasan mikroorganisme, yang menyebabkan meningkatnya jumlah karbon dioksida dan metana (Connell dan Miller, 1995).
Menurut Connell dan Miller (1995), oksigen yang diperlukan untuk pernapasan aerobik didapat dari oksigen yang terlarut dalam massa air. Oksigen ini biasanya berasal dari atmosfer dan diubah ke dalam karbon dioksida yang dibuang ke dalam massa air dan akhirnya ke atmosfer. Pernapasan yang meningkat, yang disebabkan meningkatnya jumlah karbon organik di dalam air, mengakibatkan berubahnya jarak jalur dan sumber oksigen. Yang terpenting, terdapat keperluan terhadap cadangan oksigen yang terlarut didalam massa air yang hanya sedikit karena oksigen terbatas kelarutannya di dalam air, biasanya beranah dari sekitar 6 sampai 14 mg/l. Dengan demikian, dapat terjadi penurunan besar dalam oksigen terlarut yang mempunyai dampak yang nyata terhadap makhluk hidup air.
pH
Menurut Sutika (1989), derajat keasaman atau kadar ion H dalam air merupakan salah satu faktor kimia yang sangat berpengaruh terhadap kehidupan organisme yang hidup di suatu lingkungan perairan. Tinggi atau rendahnya nilai pH air tergantung dalam beberapa faktor yaitu: kondisi gas-gas dalam air seperti CO2, konsentrasi garam-garam karbonat dan bikarbonat, proses dekomposisi bahan organik di dasar perairan.
Organisma air dapat hidup dalam suatu perairan yang mempunyai nilai pH netral dengan kisaran toleransi antara asam lemah sampai basa lemah (Baur 1987 Brehm & Meijering 1990, Brakke dkk., 1992 diacu oleh Barus, 2004). Nilai pH yang ideal bagi kehidupan orgamsma air pada umumnya terdapat antara 7 sampai 8,5. Kondisi perairan yang bersifat sangat asam maupun sangat basa akan membahayakan kelangsungan hidup organisma karena akan menyebabkan terjadinya gangguan metabolisma dan respirasi. Disamping itu pH yang sangat rendah akan menyebabkan mobilitas berbagai senyawa logam berat terutama ion Aluminium yang bersifat toksik, semakin tinggi yang tentunya akan mengancam kelangsung hidup orgamsma air. Sedangkan pH yang tinggi akan menyebabkan keseimbang antara amonium dan amoniak dalam air akan terganggu. Kenaikan pH diatas netral akan meningkatkan konsentrasi amoniak yang juga bersifat sangat toksik bagi orgamsma (Barus, 2004).
Toksisitas
Toksisitas adalah suatu sifat relatif dari suatu bahan kimia dalam hal potensi untuk menimbulkan dampak yang membahayakan bagi organisme. Toksisitas merupakan fungsi konsentrasi bahan kimia dan durasi pemaparan. Difusi merupakan jalur utama bahan kimia asing ke dalam tubuh orgamsme dengan jalan difusi pasif melalui membran semi-permiabel seperti insang, belahan mulut atau saluran gastro-intestinal. Insang yang merupakan organ ikan yang paling rentan, karena desainnya yang memaksimalkan difusi. Membran insang merupakan struktur yang tipis dengan ketebalan antara 2 - 4 µm, dan umumnya mewakili sekitar 2-10 kali area permukaan tubuh. Sedangkan kulit pada ikan, karapaks pada krustase dan kutikula pada serangga umumnya relatif bersifat impermiabel, karena kerapatan strukturnya serta keberadaan bagian mati dari strukturnya, baik yang hidrofobik maupun hidrofilik. Difusi pasif dapat terjadi melalui halangan (barrier) apa saja yang bersifat permiabel bagi bahan kimia dan menembus suatu gradasi
konsentrasi (ΔC), yang merupakan proses fisis yang tidak membutuhkan
pengerahan energi dari organisme (Tahir, 2012).
Menurut Mangkoediharjo dan Samudro (2009), tingkat toksisitas dapat dipengaruhi oleh faktor-faktor sebagai berikut: toksisitas toksikan dapat dipengaruhi oleh komposisi toksikan. Ada kemungkinan komponen toksikan mempunyai perbedaan toksisitas. Faktor lain adalah sifat-sfat fisik kimia toksikan sebagaimana telah disebutkan di atas; toksikan akan menghasilkan efek negatif jika kontak dan bereaksi dengan target biota pada konsentrasi tertentu dan cukup waktu. Faktor-faktor yang berkaitan dalam pemaparan toksikan adalah : jenis toksikan, durasi pemaparan, frekuensi pemaparan, konsentrasi toksikan; Sifat-sifat lingkungan sebagaimana yang mempengaruhi toksikan di atas juga mempengaruhi toksisitas toksikan; toksisitas toksikan berbeda untuk berbagai spesies biota, karena adanya perbedaan ketahanan dan kemudahan spesies biota menerima toksikan. Perbedaan diantara spesies biota tersebut berkaitan dengan faktor-faktor genetik, umur dan status kesehatan.
organisme perairan lainnya untuk menemukan makanan atau tidak mampu menghindari predator yang berakhir pada kematian.
Pada beberapa jenis ikan dan organisme akuatik, efek yang timbul dalam hitungan jam, hari atau minggu dianggap akut. Efek akut biasanya berdampak parah dan mematikan (severe) yang umumnya diukur melalui dalam bentuk kematian (mortalitas atau lethalitas). Suatu bahan kimia dianggap bersifat akut toksisitasnya jika aksi langsungnya mampu membunuh paling sedikit 50% dari populasi uji dalam jangka waktu singkat, yaitu 96 jam hingga 14 hari (Tahir, 2012).
Terdapat 2 jenis efek, yaitu: efek akut yang terjadi secara cepat sebagai hasil pemaparan jangka pendek, dan efek kronik atau subkronik yang terjadi secara perlahan (latency) sebagai akibat dari pemaparan tunggal atau berulang dalam jangka waktu yang lama (Tahir, 2012).
Tabel 2. Toksisitas Berdasarkan LC50
Sifat Toksik Nilai LC50
Non toksik (Non toxic)
Hampir tidak toksik (Almost non toxic) Toksisitas rendah (Slightly toxic) Toksisitas sedang (Moderately toxic)
Toksik (Toxic) Sangat toksik (Very toxic)
> 100.000 mg/l 10.000 – 100.000 mg/l
1000 – 10.000 mg/l 100 – 1000 mg/l
1 – 100 mg/l < 1 mg/l Sumber : Swan dkk., 1994 diacu oleh Efendi dkk., 2012
sesuai dengan konsentrasi yang telah ditetapkan. Organisme kontrol dan uji dimasukkan ke dalam wadah uji dan tidak dilakukan pergantian air sesuai durasi uji yang diinginkan. Walaupun sangat mudah dalam pelaksanaannya, uji statik memiliki beberapa kelemahan terutama dalam hal bahan uji yang dapat dengan mudah menguap, terdegradasi, atau terserap oleh wadah uji. Selain itu, masalah utama adalah kemungkinan terdapatnya BOD yang tinggi yang dapat menutupi efek toksik akibat terjadinya penurunan DO
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan September 2014 sampai dengan bulan Desember 2014. Kegiatan ekstraksi daun kamboja bertempat di Laboratorium Kimia Bahan Alam, Fakultas Matematika Ilmu Pengetahuan Alam Universitas Sumatera Utara, sedangkan uji toksisitas dilakukan di UPTD Budidaya Dinas Perikanan dan Kelautan Jalan Bunga Gayong, Kelurahan Ladang Bambu, Kecamatan Medan Tuntungan, Sumatera Utara.
Bahan dan Alat
Bahan yang digunakan adalah ikan nila merah ukuran 5-7 cm sebanyak 300 ekor, daun kamboja yang berasal dari TPU Polonia di Jalan Padang Golf Kecamatan Medan Polonia Kota Medan, metanol, pereaksi FeCl3, pereaksi Wagner, pereaksi dragendroff, pereaksi Meyer, pereaksi Bouchard, CeSO4, etil asetat, akuades, tisu, ekstrak daun kamboja, makanan ikan, dan air bersih. Alat yang digunakan adalah akurium berukuran 40 x 20 x 20 cm, bak berukuran 200 cm x 100 cm x 50 cm, ember, aerator, gelas ukur, gelas Beaker, tabung reaksi, maserator, water bath, labu Erlenmeyer, rotary evaporator, kertas saring, pipet tetes, selang, tangguk, blender, kamera digital, kertas millimeter, timbangan digital, pH meter dan DO meter.
Metode Penelitian
Prosedur Penelitian Ekstraksi Daun Kamboja
Daun Kamboja segar dicuci dengan menggunakan air bersih. Kemudian daun kamboja dikering-anginkan. Daun kamboja yang sudah kering diblender sehingga diperoleh bubuk kering. Daun kamboja tersebut kemudian dimasukkan ke dalam meserator yang sudah berisi metanol 95 % dan dimaserasi selama 2 x 24 jam. Selanjutnya hasil (filtrat ekstrak metanol) disaring dengan menggunakan kertas saring dan ditampung dalam labu Erlenmeyer sehingga diperoleh filtrat ekstrak metanol yang bebas dari kotoran. Filtrat ekstrak metanol kemudian dievaporasi dengan menggunakan rotary evaporator pada suhu ± 40 0C dengan kecepatan 120 rpm sampai tidak terjadi lagi pengembunan pelarut pada kondensor.
Uji Fitokimia Ekstrak Pembuatan Larutan Uji
Pembuatan larutan uji untuk uji fitokimia dilakukan dengan cara melarutkan simplisia daun kamboja di dalam maserator dan direndam selama 24 jam. Ekstrak metanol daun kamboja diambil sebanyak 100 ml dengan gelas Beaker. Ekstrak metanol daun kamboja digunakan untuk semua uji fitokima kecuali uji flavonoid yang menggunakan pelarut etil asetat.
Pengujian Golongan Fenolik
Pengujian Golongan Alkaloid
Ekstrak sampel diambil 4 ml dimasukkan masing-masing 1 ml kedalam 4 tabung reaksi. Tabung pertama ditambah 2 tetes pereaksi Bouchardat, apabila terbentuk endapan berwarna cokelat sampai hitam maka sample positif alkaloid. Tabung kedua ditambah 2 tetes pereaksi dragendroff, apabila terbentuk endapan berwarna merah/jingga maka sampel positif alkaloid. Tabung ketiga ditambah 2 tetes pereaksi Mayer, apabila terbentuk endapan berwarna putih/kuning maka sampel positif alkaloid. Tabung keempat ditambah 2 tetes pereaksi Wagner, apabila terbentuk endapan berwarna cokelat maka sampel positif alkaloid.
Pengujian Golongan Terpenoid/Steroid
Ekstrak diambil sebanyak 2 ml dimasukkan ke dalam tabung reaksi, kemudian ditambahkan 2 tetes pereaksi Lieberman-Bouchard. Apabila terbentuk warna biru/hijau menunjukkan adanya terpenoid/steroid. Pengujian dengan CeSO4 dilakukan dengan metode Thin Layer Cromatography (TLC) dengan cara ekstrak sampel diteteskan ke plat TLC kemudian disemprot dengan pereaksi CeSO4 dan dipanaskan di atas hot plate. Perubahan warna yang terjadi di plat diamati dan dibandingkan dengan standar tripenoid dan β-sitosterol yang terbentuk.
Pengujian Golongan Saponin
Pengujian Flavonoid
Ekstrak sampel diambil 1 ml dimasukkan ke dalam tabung reaksi kemudian ditambah FeCl3 1% jika terjadi perubahan warna menjadi merah jingga maka positif terdapat senyawa fenolik.
Aklimatisasi Hewan Uji
Hewan-hewan uji ikan nila merah yang akan digunakan dalam pengujian terlebih dahulu dipelihara dalam kondisi laboratorik selama 4 hari, dan 2 hari menjelang pengujian, hewan-hewan tersebut tidak diberi makan.
Persiapan Wadah
Persiapan wadah dan air pada uji pendahuluan dan uji defenitif berfungsi untuk menghindari terjadinya error akibat faktor lain selain perlakuan yang diberikan kepada hewan uji. Wadah dicuci sampai bersih dan dikering-anginkan. Kemudian wadah diisi air sebanyak 10 L dan diberi aerasi selama 2 hari agar kadar oksigen terlarut mencapai konsentrasi maksimal yaitu 6 – 8 ppm.
Uji Pendahuluan
Uji pendahuluan dilakukan untuk mengetahui ambang batas atas dan ambang batas bawah dalam menentukan konsentrasi perlakuan uji defenitif. Batas ambang atas adalah konsentrasi terkecil yang dapat membunuh seluruh hewan uji dalam waktu 24 jam yang disimbolkan dengan “N”. Batas ambang bawah adalah konsentrasi terbesar yang tidak membunuh hewan uji dalam waktu 48 jam yang disimbolkan dengan “n”.
berbagai konsentrasi tersebut dimasukkan ke dalam masing-masing wadah yang telah disiapkan sebelumnya. Volume larutan ekstrak yang dimasukkan sesuai dengan volume air yang dikeluarkan, sehingga volume air tetap 10 L. Air pada wadah diaduk secara perlahan bertujuan agar seluruh larutan ekstrak bercampur. Hewan uji dimasukkan sebanyak 10 ekor dan dilakukan pengamatan selama 48 jam. Pengamatan mortalitas ikan dilakuan pada jam ke 0 , 2, 4, 8, 16, 24, dan 48. Pengamatan pada uji pendahuluan dilakukan tanpa diberikan aerasi dan pakan.
Uji Defenitif
Uji defenitif dilakukan untuk mendapatkan data mortalitas dari konsentrasi yang diberikan berdasarkan uji pendahuluan. Data mortalitas kemudian akan digunakan untuk menentukan LC50 (Lethal Concentration 50%) dari ekstrak daun kamboja terhadap ikan nila merah.
Konsentrasi uji defenitif ditentukan berdasarkan rumus menurut Syakti dkk. (2012) diacu oleh Sianturi (2014), yaitu:
Keterangan:
Keterangan:
N : Konsentrasi ambang atas
n : Konsentrasi ambang bawah
k : Jumlah konsentrasi yang diuji
Persiapan wadah dan ikan uji dilakukan sama dengan uji pendahuluan sebelumnya. Larutan ekstrak dengan konsentrasi yang telah didapatkan, dimasukkan ke dalam masing-masing wadah dengan mengeluarkan air sebanyak volume larutan yang dimasukkan. Setiap wadah diberikan aerasi dan dilakukan pengamatan mortalitas ikan selama 96 jam tanpa diberikan pakan dengan waktu pengamatan pada jam ke 0, 2, 4, 8, 16, 24, 36, 48, 72 dan 96. Pengukuran kualitas air dilakuan setiap hari selama pengamatan dilakukan, yang mencakup parameter oksigen terlarut (DO), pH, dan suhu.
Analisis Data Mortalitas
Persentase mortalitas ikan uji diperoleh dengan mengikuti rumus menurut Nurhayati dkk. (2006):
Keterangan:
M : Persentase mortalitas hewan uji (%)
LC50
Dengan nilai a dan b diperoleh berdasarkan persamaan sebagai berikut.
Persamaan regresi: Y = a + bx
LC50 = anti log m
Keterangan:
Y : Nilai Probit Mortalitas
X : Logaritma konsentrasi bahan uji
a : Konstanta
b : Slope/kemiringan
m : Nilai X pada Y = 5
n : Jumlah hewan uji per akuarium
Analisis Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO
HASIL DAN PEMBAHASAN
Hasil
Uji Fitokimia Daun Kamboja
Hasil Uji fitokimia ekstrak daun kamboja diketahui bahwa daun kamboja mengandung senyawa fenolik, terpenoid/steroid, dan alkaloid dengan pereaksi
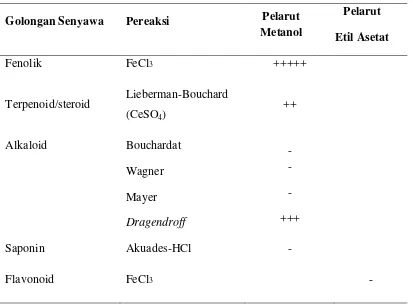
[image:39.595.108.521.307.611.2]dragendroff. Hasil uji fitokimia daun kamboja dapat dilihat pada Tabel 3. Tabel 3. Hasil uji fitokimia ekstrak daun kamboja
Golongan Senyawa Pereaksi Pelarut Metanol
Pelarut Etil Asetat
Fenolik FeCl3 +++++
Terpenoid/steroid Lieberman-Bouchard (CeSO4)
++
Alkaloid Bouchardat Wagner Mayer
Dragendroff
- - - +++ Saponin Akuades-HCl -
Flavonoid FeCl3 -
Uji Pendahuluan
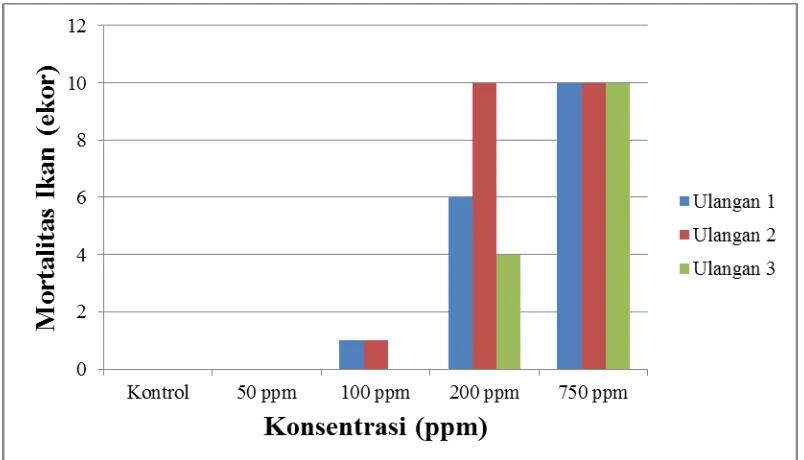
dalam waktu kurang dari 24 jam. Konsentrasi 100 sampai 200 ppm masih ditemukan kematian ikan uji dan pada konsentrasi 50 ppm tidak ada ikan uji yang mati. Konsentrasi ambang bawah dan atas dapat ditentukan dari uji pendahuluan yang kedua, dimana konsentrasi ambang atas 750 ppm dan konsentrasi ambang bawah 50 ppm. Hasil pengamatan dapat dilihat pada Lampiran 4. Perilaku ikan uji pada konsentrasi 200 sampai 750 ppm terlihat ikan berenang ke permukaan air dan mengambil udara, namun pada konsentrasi 50 sampai 100 ppm perilaku ikan cenderung tenang dan hanya sesekali berenang ke permukaan. Mortalitas ikan selama 48 jam dapat dilihat pada Gambar 3.
Gambar 3. Diagram Uji Pendahuluan
Uji Defenitif
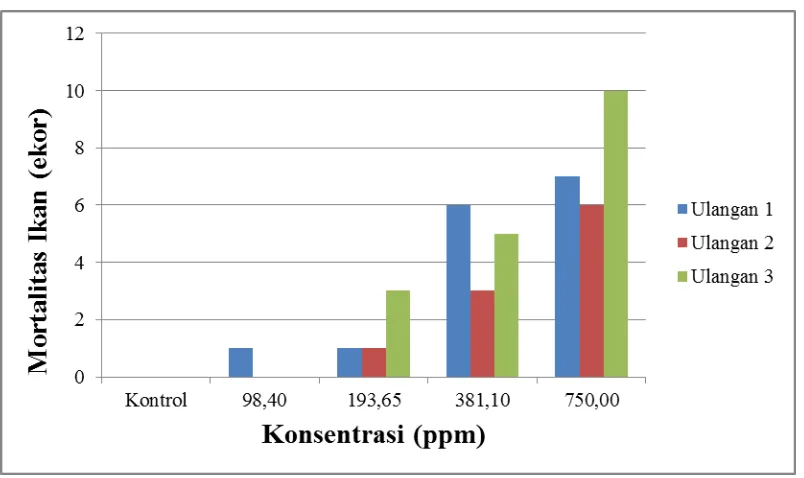
Lampiran 4. Kematian terbesar terdapat pada konsentrasi 750 ppm dan 381,1 ppm. Peningkatan kematian ikan uji dapat dilihat pada Gambar 4.
Gambar 4. Diagram Uji Defenitif
Tabel 4. Kualitas Air Uji Defenitif
Konsentrasi
Parameter
Suhu (0C) DO (mg/l) pH
0 26,6-30,3 6-7,5 7,9-8,4 98,40 26,5-30,6 6,4-7,6 7,7-8,5 193,65 26,6-30,9 6,3-7,8 7,5-8,4 381,10 26,7-31 6,2-8 7,8-8,4 750,00 27,1-31 6,2-8,2 7,4-8,5
Persentase Mortalitas
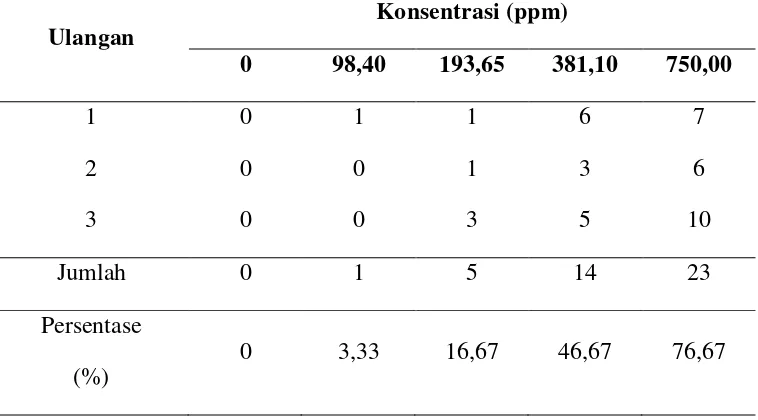
Persentase mortalitas semakin tinggi sesuai dengan kenaikan konsentrasi terhadap ikan uji. Persentase mortalitas setiap konsentrasi digunakan dalam analisis probit untuk menentukan nilai LC50 selama 96 jam. Persentase mortalitas pada Lampiran 6. dapat dilihat dalam bentuk tabel pada Tabel 5.
Tabel 5. Persentase Mortalitas Ikan Uji
Ulangan
Konsentrasi (ppm)
0 98,40 193,65 381,10 750,00
1 0 1 1 6 7
2 0 0 1 3 6
3 0 0 3 5 10
Jumlah 0 1 5 14 23
Persentase (%)
[image:42.595.111.490.477.687.2]Analisis Probit
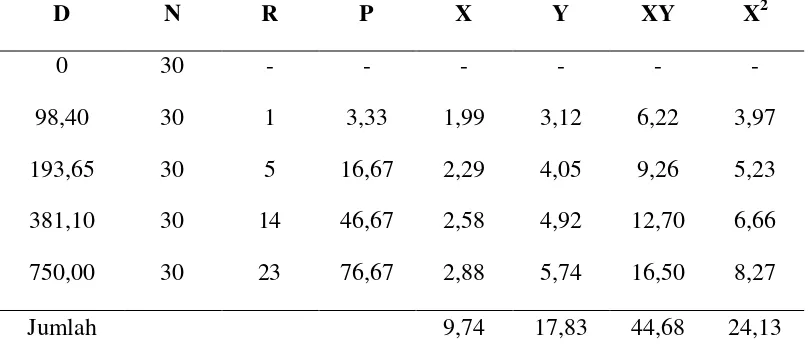
[image:43.595.108.512.224.404.2]Analisis probit dilakukan dengan mengubah persentase mortalitas kedalam bentuk probit menggunakan tabel probit. Analisis probit uji defenitif dapat dilihat pada Tabel 6.
Tabel 6. Analisis Probit Konsentrasi Ekstrak Daun Kamboja terhadap Ikan Nila
D N R P X Y XY X2
0 30 - - - -
98,40 30 1 3,33 1,99 3,12 6,22 3,97 193,65 30 5 16,67 2,29 4,05 9,26 5,23 381,10 30 14 46,67 2,58 4,92 12,70 6,66 750,00 30 23 76,67 2,88 5,74 16,50 8,27 Jumlah 9,74 17,83 44,68 24,13
Berdasarkan analisis probit dan persamaan regresi untuk penentuan LC50 selama 96 jam yang terdapat pada Lampiran 6, maka diperoleh nilai LC50 selama 96 jam sebesar 510,63 ppm. Artinya ikan uji mati sebanyak 50% dalam waktu 96 jam pada konsentrasi 510,63 ppm dalam kondisi diberikan aerasi.
Analisis Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO Analisis Determinasi (R2)
Tabel 7. Kesimpulan Model
Model R R Kuadrat R Kuadrat yang disesuaikan
Standar Eror dari Perkiraan
1 .622a .386 .342 1.25752 a. Prediktor: (Konstan), DO, pH, Konsentrasi, Suhu
b. Variabel Dependen: Mortalitas
Uji Koefisien Regresi Secara Bersama-sama (Uji F)
Uji F digunakan untuk mengetahui pengaruh variabel independen secara serentak terhadap variable dependen, apakah pengaruhnya signifakan atau tidak. Uji F dapat dilihat pada Tabel 8.
Tabel 8. ANOVAb
Model Jumlah
Kuadrat df
Nilai Tengah
Kuadrat F Sig.
1 Regresi 54.758 4 13.690 8.657 .000a Sisa 86.975 55 1.581
Total 141.733 59 a. Prediktor: (Konstan), DO, pH, Konsentrasi, Suhu b. Variabel Dependen: Mortalitas
Uji Koefisien Regresi Secara Parsial (Uji t)
[image:44.595.114.508.353.447.2]Tabel 9. Koefisien-koefisien Model Koefisien Tidak Standar Koefisien Standar
t Sig. B Standar
Eror Beta
1 (Konstan) 6.080 10.237 .594 .555 Konsentrasi .003 .001 .529 3.500 .001 Suhu -.246 .242 -.162 -1.017 .314 pH .865 .783 .169 1.105 .274 DO -.833 .668 -.197 -1.247 .218 a. Variabel Dependen: Mortalitas
Pembahasan
Uji Fitokimia Daun Kamboja
Uji fitokimia fenolik terhadap ekstrak daun kamboja dengan pelarut metanol menunjukan hasil positif, terlihat adanya reaksi perubahan warna hijau menjadi berwarna hitam yang kuat (pekat) setelah diberikan FeCl3 seperti yang terlihat pada Lampiran 2. Harborne (1987) menyatakan Cara klasik untuk mendeteksi senyawa fenol sederhana ialah dengan menambahkan larutan besi (III) klorida 1% dalam air atau etanol kepada larutan cuplikan, yang menimbulkan warna hijau, merah ungu, biru, atau hitam yang kuat.
Uji fitokimia alkaloid ekstrak daun kamboja dengan pelarut metanol menunjukkan hasil dari pereaksi dragendroff yang ditandai dengan perubahan warna merah jingga dan adanya endapan seperti terlihat pada Lampiran 2. Menurut Harborne Menurut Harbone (1987) uji alkaloid dilakukan berdasarkan reaksi warna dengan pereaksi dragendroff dan terbentuk endapan merah jingga diperkirakan endapan tersebut adalah kalium alkaloid.
Uji fitokimia saponin pada ekstrak daun kamboja dengan pelarut metanol menunjukkan hasil negatif, karena tidak adanya buih yang stabil selama 30 detik setelah diberi akuades-HCl dan dikocok selama ±10 detik seperti terlihat pada Lampiran 2. Menurut Harborne (1987), saponin merupakan senyawa aktif permukaan yang bersifat seperti sabun, serta dapat dideteksi berdasarkan kemampuannya memberntuk busa dan menghemolisis sel darah.
Uji fitokima flavonoid pada ekstrak daun kamboja dengan pelarut etil asetat menunjukkan hasil negatif, karena tidak ada perubahan warna menjadi jingga seperti yang terlihat pada Lampiran 2. Hasil uji ini berbeda dengan pernyataan Syamsuhidayat dan Hutapea (1991) diacu oleh Rolliana (2010) bahwa daun kamboja (Plumeria alba Linn), mengandung senyawa flavonoid, terpenoid, glycoside dan alkaloid.
Uji Pendahuluan
atas) dan pada konsentrasi 1 ppm semua hewan uji masih hidup selama waktu dedah 48 jam (ambang bawah).
Penentuan konsentrasi untuk uji defenitif dihitung dari konsentrasi ambang atas dan bawah. Konsentrasi hasil perhitungan digunakan dalam penentuan LC50 selama 96 jam pada uji defenitif. Rudianti dan Ekasari (2009) menyatakan uji pendahuluan bertujuan untuk menentukan ambang daya racun lethal pestisida dengan bahan aktif terhadap ikan uji.
Pengamatan pergerakan ikan menunjukkan perilaku yang sama sesuai dengan kenaikan konsentrasi yang diberikan. Semakin tinggi konsentrasi yang diberikan, ikan akan berenang keatas dan mengambil udara di permukaan. Sebaliknya pada konsentrasi yang semakin rendah ikan berenang tenang dan normal. Aerasi yang tidak diberikan dapat menurunkan kadar oksigen dalam air dan dimasukkannya ekstrak juga akan menurunkan kadar oksigen. Connell dan Miller (1995) menyatakan Jika zat-zat yang kaya karbon organik ditambahkan ke dalam sistem mengakibatkan meningkatnya pernapasan, terutama melalui pernapasan mikroorganisme, yang menyebabkan meningkatnya jumlah karbon dioksida dan metana.
Uji Defenitif
mekanis, dan fotosintesis tanaman akuatik. Oksigen terlarut yang hilang akibat respirasi ikan dan mikroorganisme dapat terganti dari aerasi yang diberikan.
Mortalitas ikan diduga akibat senyawa fenolik dan alkaloid dari daun kamboja. Menurut Qadeer dan Rehan (1998) diacu oleh Dewilda dkk. (2012) menyatakan Fenol merupakan senyawa yang dapat menimbulkan bau tidak sedap, bersifat racun dan korosif terhadap kulit (iritasi), menyebabkan gangguan kesehatan manusia dan kematian pada organisme yang terdapat pada air dengan nilai konsentrasi tertentu. Harborne (1987) menyatakan Alkaloid sering kali beracun bagi manusia dan banyak mempunyai kegiatan fisiologi yang menonjol; jadi digunakan secara luas dalam bidang pengobatan.
Kualitas air yang diamati selama uji defenitif menunjukkan tidak adanya perubahan yang besar. Suhu air semua perlaukan berkisar 26,5 – 31 0C yang masih tergolong normal. Kadar oksigen terlarut berkisar antara 6 – 8,2 mg/l yang menunjukkan bahwa oksigen terlarut masih tergolong normal. Suhu dan oksigen terlarut memiliki keterkaitan yaitu menurut USEPA (1972) diacu oleh Connell dan Miller (1995), suhu 36 – 27,5 0C memiliki tingkat kejenuhan oksigen terlarut sebesar 7 – 8 mg/l. Kadar pH di semua perlakuan berkisar 7,4 – 8,5 yang masih tergolong normal. Barus (2004) menyatakan Nilai pH yang ideal bagi kehidupan orgamsma air pada umumnya terdapat antara 7 sampai 8,5.
LC50 dalam 96 Jam
ke dalam persamaan regresi dan didapatkan nilai LC50 selama 96 jam sebesar 510,63 ppm. Menurut Swann dkk. (1994) diacu oleh Effendi dkk. (2012) menyatakan nilai LC50 sebesar 100 – 1000 mg/l termasuk ke dalam katergori bersifat toksisitas sedang (moderately toxic). Konsentrasi aman sebesar 10% dari nilai LC50 dalam 96 jam adalah 51,06 ppm. Nedi dkk. (2006) diacu oleh Wibisono (1989) menyatakan untuk menentukan nilai konsentrasi aman (safety concentration) dipakai faktor aplikasi menurut yakni 10% dari nilai LC50-96 jam.
Hubungan Mortalitas terhadap Konsentrasi, Suhu, pH, dan DO
Hasil analisis regresi pada Tabel 7. diperoleh angka R2 (R Kuadrat) sebesar 0,386 atau (38,6%). Hal ini menunjukkan bahwa presentase sumbangan pengaruh DO, pH, konsentrasi, dan suhu terhadap mortalitas sebesar 38,6%. Menurut Hartono (2008), besar koefisien (R kuadrat) determinasi mengandung pengertian bahwa pengaruh variabel bebas (independen) terhadap perubahan variabel dependen.
Uji F dilakukan dengan mencari F kritis ditentukan dengan menggunakan tingkat keyakinan 95% yaitu α = 5% = 0,05; df 1 = k – 1 = 4 (k adalah jumlah variabel); dan df 2 = n – k = 55 (n dalah jumlah kasus). F kritis dicari dengan Ms Excell dengan rumus “=finv(0,05;4;55)” yaitu sebesar 2,540. Menurut Priyatno (2013), pengambilan keputusan uji F dengan kriteria jika F hitung ≤ F kritis maka H0 diterima dan jika F hitung > F kritis maka H0 ditolak. F hitung dari tabel 8. (8,657) > F kritis (2,540) maka H0 ditolak. Artinya DO, pH, konsentrasi, suhu secara serentak berpengaruh terhadap mortalitas.
KESIMPULAN
Kesimpulan
1. Nilai LC50 dalam 96 jam dari ekstrak daun kamboja terhadap ikan nila sebesar 510,63 ppm dimana tergolong bersifat toksisitas sedang. Diduga, kematian ikan disebabkan oleh senyawa fenolik dan alkaloid.
2. Konsentrasi yang aman dari ekstrak daun kamboja adalah 51,06 ppm dimana konsentrasi aman sebesar 10% dari nilai LC50 dalam 96 jam.
Saran
DAFTAR PUSTAKA
Alamsyah, B. 2007. Pengelolaan Limbah di Rumah Sakit Pupuk Kaltim Bontang untuk Memenuhi Baku Mutu Lingkungan. [Tesis]. Program Pascasarjana Universitas Diponegoro. Semarang.
Barus, T.A. 2004. Pengantar Limnologi Studi tentang Ekosistem Air Daratan. USU Press. Medan.
Barus, W.N.U. 2013. Uji Efektivitas Antibakteri Ekstrak Daun Kamboja (Plumiera rubra) pada Konsentrasi yang Berbeda terhadap Pertumbuhan
Aeromonas hydrophila Secara In Vitro. [Skripsi]. Fakultas Pertanian Universitas Sumatera Utara. Medan.
Connell, D.W. dan G.J. Miller. 1995. Kimia dan Ekotoksikologi Pencemaran. UI-PRESS. Jakarta.
Department of Primary Industries and Resources of South Australia. 2003. Water Quality In Freshwater Aquaculture
Ponds.
Diakses pada tanggal 8 Maret 2014.
Dewilda, Y., R. Afrianita, dan F.F. Iman. 2012. Degradasi Senyawa Fenol oleh Mikroorganisme Laut. Jurnal Teknik Lingkungan UNAND Vol. 9 No. 1 Hal. 59-73.
Effendi, H., A.H. Emawan, Y. Wardiatno, dan M. Krisanti. 2012. Toksisitas Akut (LC50) Serbuk Bor (Cuttings) terhadap Daphnia sp. Jurnal Bumi Lestari Vol. 12 No. 2 Hal. 321 – 326.
Harborne, J.B. 1987. Metode Fitokimia: Penuntun Cara Modem Menganalisis Tumbuhan. Edisi ke-2. Penerjemah: Dr. Kosasih Padmawinata dan Iwang Soediro. ITB. Bandung.
Hartono. 2008. SPSS 16.0 Analisis Data Statistika dan Penelitian. Pustaka Pelajar. Yogyakarta.
Haryani, A., R. Grandiosa, I.D. Buwono, dan A. Santika. 2012. Uji Efektivitas Daun Pepaya (Carica papaya) untuk Pengobatan Infeksi Bakteri Aeromonas hydrophila pada Ikan Mas Koki (Carassius auratus). Jurnal Perikanan dan Kelautan Vol. 3, No. 3 Hal: 213-220.
Irmayanti, P.Y., C.I.S. Arisanti, dan N.P.A.D Wijayanti. 2014. Uji Pendahuluan Serbuk Simplisia dan Skrining Fitokimia Ekstrak Etanol Kulit Buah Manggis (Garcinia mangostana L.) yang Berasal dari Desa Luwus, Kecamatan Baturiti, Tabanan, Bali. Jurnal Universitas Udayana Bali.
ITIS. 2014. Plumeria rubra L. http://www.itis.gov/servlet/SingleRpt/SingleRpt? search_topic=TSN&search_value=30200. Diakses pada tanggal 19 Juni 2014.
Kumari, S., A. Mazumder, dan S. Bhattacharya. 2012. In-vitro Antifungal Activity of The Essential Oil of Flowers of Plumeria alba Linn. (Apocynaceae). International Journal of PharmTech Research Vol. 4 No. 1 Hal. 208-212.
Luna, S.M. 2015. Oreochromis niloticus. http://www.fishbase.org/summary/2. Diakses pada tanggal 4 Maret 2015.
Mariyono dan A. Sundana. 2002. Teknik Pencegahan dan Pengobatan Penyakit Bercak Merah pada Ikan Air Tawar yang Disebabkan oleh Bakteri
Aeromonas hydrophila. Jurnal Buletin Teknik Pertanian Vol. 7 No. 1.
Megawati dan S.W.D. Saputra. 2012. Minyak Atsiri dari Kamboja Kuning, Putih, dan Merah dari Ekstraksi dengan N-Heksana. Jurnal Bahan Alam Terbarukan Vol. 1 No. 1.
Menegristek. 2001. Budidaya Ikan Nila (Oreochromis niloticus). http://www.warintek.ristek.go.id/perikanan/air%20tawar/nila.pdf. Diakses pada tanggal 20 Oktober 2014.
Nedi, S., Thamrin, dan H. Marnis. 2006. Toksisitas Deterjen terhadap Benih Ikan Kakap Putih (Lates calcarifer, Bloch). Jurnal Berkala Perikanan Terubuk Vol. 33 No. 2.
Nurhayati, A.P.D., N. Abdulgani, dan R. Febrianto. 2006. Uji Toksisitas Ekstrak
Eucheuma alvarezii terhadap Artemia salina sebagai Studi Pendahuluan Potensi Antikanker. Akta Kimindo Vol. 2 No. 1 Hal. 41-46.
Priyatno, D. Analisis Korelasi, Regresi, dan Multivariate dengan SPSS. Gava Media. Yogyakarta.
Rolliana, E.R. 2010.Uji Toksisitas Akut Ekstrak Etanol Daun Kamboja (Plumeria alba Linn) terhadap Larva Artemia salina Leach Dengan Metode Brine Shrimp Lethality Test (BST). [Skripsi]. Fakultas Kedokteran Universitas Diponegoro. Semarang.
Samuel dan Shelburne. 2004. Infectious Diseases: Viral & Rickettsial. In: Current Medical Diagnosis & Treatment 2004 43rd edition. Lawrence M Tierney, dkk (Editors). McGraw Hill Corp. USA.
Schramm. 1997. The Oxygen Factor pada tanggal 8 Maret 2014.
Sianturi, P. 2014. Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.). [Skripsi]. Fakultas Pertanian Universitas Sumatera Utara Medan.
Syamsuhidayat, S.S. dan J.R. Hutapea. 1991. Inventaris Tanaman Obat Indonesia (I). Departemen Kesehatan RI. Jakarta. Hal: 452-453
Tahir, A. Ekotoksikologi dalam Perspektif Kesehatan Ekosistem Laut. Karya Putra Darwati. Bandung.
LAMPIRAN
Lampiran 1. Alat dan Bahan Penelitian
Blender Corong
Gelas Beaker Rotary Evaporator
Lampiran 1. Lanjutan
Akuarium pH Meter
DO Meter Timbangan Digital
Lampiran 1. Lanjutan
Daun Kamboja Daun Kamboja Kering
Metanol Pereaksi FeCl3
Lampiran 1. Lanjutan
Pereaksi Meyer Pereaksi Bouchard
Pereaksi CeSO4 Etil Asetat
Lampiran 1. Lanjutan
Tabung Reaksi Berisi Ekstrak Metanol Aquadest Daun Kamboja
Lampiran 2. Uji Fitokimia
Uji Flavonoid Uji Terpenoid/Steroid
Lampiran 3. Uji Pendahuluan dan Uji Defenitif Persiapan Wadah
Pengeringan Akuarium Pengendapan dan Pengaerasian Air
Uji Defenitif
Konsentrasi 193,65 ppm Konsentrasi 381,10 ppm
Lampiran 3. Lanjutan
Konsentrasi 750,00 ppm
Lampiran 4. Mortalitas Ikan
Uji Pendahuluan
Jam Ke- 0 2 4 8 16 24 48
A
U1 - - - -
U2 - - - -
U3 - - - -
B
U1 - - - -
U2 - - - -
U3 - - - -
C U1 - - - 1
U3 - - - -
D U1 - - 1 - - 1 4
U2 - - - 10
U3 - - - 2 2
E U1 - - 1 - 9 - -
U2 - - 1 - 9 - -
U3 - - 1 - 9 - -
Keterangan :
A = 0 ppm C = 100 ppm E = 750 ppm B = 50 ppm D = 200 ppm
Lampiran 4. Lanjutan
Uji Defenitif
Jam Ke- 0 2 4 8 16 24 36 48 72 96
A
U1 - - - - U2 - - - - U3 - - - -
B
U1 - - - 1 U2 - - - - U3 - - - -
C
U1 - - - 1 U2 - - - 1 U3 - - - 1 2
D
U3 - - - 1 1 4
E
U1 - - - 2 5 U2 - - - 1 1 4 U3 - - - 1 8 1
Keterangan :
A = 0 ppm C = 193,65 ppm E = 750,00 ppm B = 98,40 ppm D = 381,10 ppm
Lampiran 5. Kualitas Air
Uji Defenitif
Hari Ke- 0 I II III IV
Ulangan 1 2 3 1 2 3 1 2 3 1 2 3 1 2 3
Suhu (oC)
A 26,6 26,7 26,7 30 30 30 30,2 30,1 30,1 30 30,1 30,3 27,6 27,7 27,8
B 26,5 26,5 26,6 30,3 30,5 30,6 29,9 29,9 29,9 30,2 30,1 30,1 27,8 27,8 27,9
C 26,6 26,6 26,7 30,8 30,9 30,9 29,6 29,7 29,7 30 30 30,2 28 28 28,1
D 26,9 26,8 26,7 31 30,9 30,9 29,4 29,5 29,5 30,2 30,2 30,1 28,2 28,6 28,4 E 27,5 27,2 27,1 31 31 31 29,5 29,4 29,3 30,1 30,1 30,2 28,3 28,4 28,2
pH
A 8,4 8,4 8,3 8,4 8,4 8,4 8,4 8,3 8,4 7,9 7,9 7,9 8,4 8,3 8,4 B 8,5 8,5 8,5 8,1 8,1 8,2 8,2 8,2 8,3 7,7 7,8 7,9 8,2 8,2 8,3 C 8,4 8,4 8,4 7,7 7,7 7,9 7,7 7,6 7,8 7,6 7,6 7,5 8,1 8 8,1 D 8,4 8,4 8,4 8,1 8 7,8 8,2 8,1 8 7,8 7,8 7,8 8,3 8,3 8,3 E 8,4 8,5 8,4 7,4 7,5 7,5 7,5 7,8 7,5 7,6 7,5 7,5 7,9 7,9 7,9
DO (mg/L)
C 7,8 6,3 7,7 7,2 7 6,9 7,4 7,3 7 7,3 7,1 6,9 6,6 6,5 6,3 D 8 6,9 7,1 7,2 6,9 6,8 7,4 7,4 7,1 7,2 7 7 6,3 6,2 6,4 E 8,1 8,2 6,9 7 6,9 6,8 7 7 7,1 7,3 7 7 6,3 6,3 6,2
Keterangan :
A = 0 ppm C = 193,65 ppm E = 750,00 ppm B = 98,40 ppm D = 381,10 ppm
Lampiran 6. Perhitungan Konsentrasi Uji Defenitif
Dik : = 750 ppm = 50 ppm = 4 Dit :
Jawab :
= = = = =
= 2,875061764 =
Lampiran 6. Lanjutan Persentase Mortalitas
Dik : Jumlah Ikan yang Mati 0 ppm = 0 ekor 98,40 ppm = 1 ekor 193,65 ppm = 5 ekor 381,10 ppm = 14 ekor 750,00 ppm = 23 ekor Dit :
Jawab :
Lampiran 6. Lanjutan LC50 dalam 96 Jam
Konsetrasi 0 ppm :
Konsetrasi 98,40 ppm :
Konsetrasi 193,65 ppm :
Konsetrasi 381,10 ppm :
Dik : = 9,79 = 17,83 = 44,68 = 24,13 = 30 Dit : LC50
Jawab :