49
LAMPIRAN 1
DATA HASIL PENELITIAN
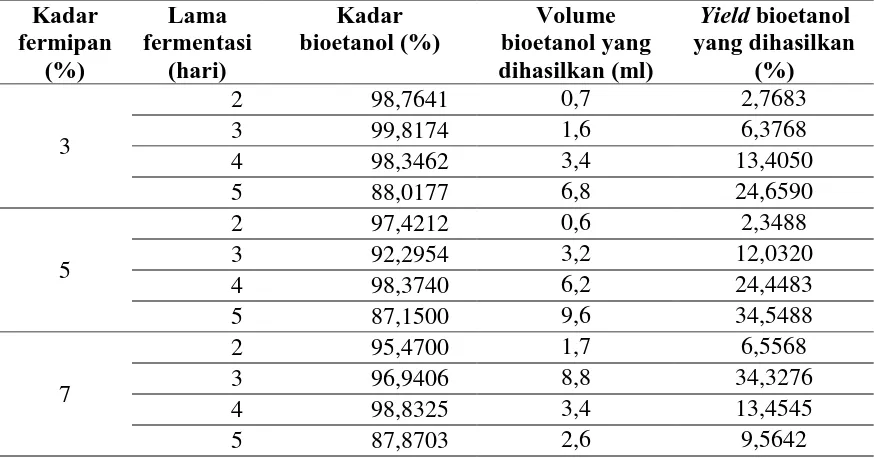
L1.1 DATA HASIL PENELITIAN KADAR BIOETANOL Tabel L1.1 Data Penelitian Analisa Kuantitatif Kadar Bioetanol
Kadar fermipan
(%)
Lama fermentasi
(hari)
Kadar bioetanol (%)
Volume bioetanol yang dihasilkan (ml)
Yield bioetanol yang dihasilkan
(%)
3
2 98,7641 0,7 2,7683
3 99,8174 1,6 6,3768
4 98,3462 3,4 13,4050
5 88,0177 6,8 24,6590
5
2 97,4212 0,6 2,3488
3 92,2954 3,2 12,0320
4 98,3740 6,2 24,4483
5 87,1500 9,6 34,5488
7
2 95,4700 1,7 6,5568
3 96,9406 8,8 34,3276
4 98,8325 3,4 13,4545
5 87,8703 2,6 9,5642
L1.2 HASIL UJI INDEKS BIAS BIOETANOL
50
LAMPIRAN 2
CONTOH PERHITUNGAN
L2.1 PERHITUNGAN KADAR FERMIPAN
Volume hidrolisat yang difermentasi setelah penetralan dengan NaOH 4 M = 300 ml Kadar fermipan yang digunakan = 3%, 5%, dan 7% (w/w)
Kadar fermipan (%) = � x 100% [ ] Kadar fermmipan (%) Waktu fermentasi (hari) Volume hidrolisat (ml) Massa larutan (gr) Massa fermipan (%) 3%
2 hari 300 337,0609 10,1118
3 hari 300 343,1300 10,2939
4 hari 300 345,7858 10,3735
5 hari 300 357,5686 10,7270
5%
2 hari 300 347,9400 17,3970
3 hari 300 350,6412 17,5320
4 hari 300 357,6700 17,8835
5 hari 300 364,5963 18,2298
7%
2 hari 300 357,2200 25,0054
3 hari 300 366,8300 25,6781
4 hari 300 355,2512 24,8675
5 hari 300 336,1700 23,5319
L2.2 PERHITUNGAN YIELD BIOETANOL
Yield = � �� �� �� [ ]
Dimana,
Berat sampel sebanyak 20 gram
Kemurnian = kadar etanol diperoleh dari hasil GC
51 Kadar
fermipan (%)
Waktu fermentasi
(hari)
Kadar bioetanol
(%)
Volume bioetanol yang dihasilkan (ml)
Massa etanol (gr)
Yield bioetanol yang dihasilkan (%) 3%
2 hari 98,7641 0,7 0,5606 2,7683
3 hari 99,8174 1,6 1,2777 6,3768
4 hari 98,3462 3,4 2,7261 13,4050
5 hari 88,0177 6,8 5,6032 24,6590
5%
2 hari 97,4212 0,6 0,4822 2,3488
3 hari 92,2954 3,2 7,9268 12,0320
4 hari 98,3740 6,2 4,9705 24,4483
5 hari 87,1500 9,6 2,6073 34,5488
7%
2 hari 95,4700 1,7 1,3736 6,5568
3 hari 96,9406 8,8 7,0822 34,3276
4 hari 98,8325 3,4 2,7227 13,4545
5 hari 87,8703 2,6 2,1769 9,5642
Yield = i e
e e � kemurnian Yield = 0, 0
52
LAMPIRAN 3
DOKUMENTASI PENELITIAN
L3.1 DOKUMENTASI PROSES PEMBUATAN BIOETANOL L3.1.1 Persiapan Bahan Baku
53 L3.1.2 Hidrolisis Bubuk Kulit Buah Kakao
54 L3.1.3 Setelah Penambahan NaOH 4M
Gambar L3.3 Hidrolisat Kulit Buah Kakao Setelah Penambahan NaOH 4M
L3.1.4 Pengaturan pH Hidrolisat menjadi 4,5
55 L3.1.5 Fermentasi
Gambar L3.5 Fermentasi
L3.1.6 Rangkaian Distilasi
56 L3.1.7 Larutan Bioetanol
57 L3.1.8 Foto Hasil GC
58
42
DAFTAR PUSTAKA
[ ]Nur Robi’ah Adawiyah Mahmud. “Penentuan Nilai Kalor Berbagai Komposisi Campuran Bahan Bakar Minyak Nabati.” Skripsi, Program Sains Fakultas Sains Dan Teknologi Universitas Islam Negeri (UIN) Maulana Malik Ibrahim Malang, Malang, 2010, hal. 23.
[ ]Wawan W Effendi (2012), “Bioetanol Kulit Buah Kakao; Menuju Indonesia Mandiri Bahan Bakar Nabati.” Artikel Bioetanol Kulit Buah Kakao. Diakses Pada 20 September 2014.
www.academia.edu.com
[ ]A.Rachman Fauzi, Didik Haryadi, Slamet Priyanto, “Pengaruh Waktu Fermentasi dan Efektivitas Adsorben dalam Pembuatan Bioetanol Fuel Grade dari Limbah POD Kakao (Theobroma Cacao),” Jurnal Teknologi Kimia dan Industri Universitas Diponegoro, 1(1) 2012 : hal.182-184.
[ ]Hermiati E., Djumali Mangunwidjaja, Titi Candra Sunarti, Ono Suparno, dan Bambang Prasetya, “Pemanfaatan Biomassa Lignoselulosa Ampas Tebu Untuk Produksi Bioetanol,” Jurnal Litbang Institut Pertanian Bogor 2010 Diakses pada 23 September 2014 dari pustaka penelitian Departemen Pertanian
http:www. pustaka.litbang.deptan.go.id
[ ]Sukumaran, R.K. 2008. Cellulose production using biomassa feedstock and its application in lignocellulossa sacharification for bioethanol production, Renewable energy, vol 30, hal 1-4
[ ]Endah R D, Sperisa D, Adrian Nur, Paryanto, “Pengaruh Kondisi Fermentasi Terhadap Yield Etanol Pada Pembuatan Bioetanol Dari Pati Garut.” Gema Teknik Majalah Ilmiah Teknik, Nomor 2/Tahun X Juli 2007, Hal.85.
[ ]Putu Kristiani K, La Ode Sabarudin, Rima Melati, Haeruddin, “Waktu Optimum Fermentasi Limbah Pulp Kakao (Theobroma Cacao L.) Menggunakan Kulit Bakau (Sonneratia Sp.) Dalam Produksi Bioetanol,” Universitas Haluoleo, Kendari. Diakses Pada 20 September 2014 dari Direktorat Penelitian dan Pengabdian Kepada Masyarakat.
43
[ ]Agustinus Eka P, Amran Halim, “Pembuatan Bioethanol Dari Nira Siwalan Secara Fermentasi Fese Cair Menggunakan Fermipan,” Universitas Diponegoro, Semarang, 2009.
[ ]Dianrifiya Nisa, Widya Dwi Rukmi Putri, “Pemanfaatan Selulosa Dari Kulit Buah Kakao (Teobroma Cacao L.) Sebagai Bahan Baku Pembuatan Cmc (Carboxymethyl Cellulose),” Jurnal Pangan dan Agroindustri Universitas Brawijaya Malang 2(3) Juli 2014 : hal.34-42.
[ ]Novianti, Mappiratu, Musafira, “Pemanfaatan Limbah Serbuk Gergaji Untuk Produksi Bioetanol Menggunakan Sel Ragi Imobil Secara Berulang,” Jurnal ISSN: 2338-0950 Online Jurnal of Natural Science, 2(3) Desember 2013 : hal. 9-19.
[ ]M. Zain, “Substitusi Rumput Lapangan dengan Kulit Buah Coklat Amoniasi Dalam Ransum Domba Lokal.” Jurnal ISSN 0126-0472 32 (1) April 2009 : hal. 47-52
Terakreditasi B SK Dikti No: 43/DIKTI/Kep/2008.
[ ]Pusat Penelitian dan Pengembangan Perkebunan (2014). “Indonesia Targetkan jadi Penghasil Kakao Terbesar di Dunia.” Tanggal akses 23 September 2014 dari http://nationalgeographic.co.id/berita/2012/07/2014-indonesia-targetkan-jadi-penghasil-kakao-terbesar-di-dunia.
[ ]Ellyta Sari, Erti Praputri, Ade Rahmat, dan Arif Okdiansyah. “Peningkatan Kualitas Pektin dari Kulit Kakao melalui Metode Ekstraksi dengan Penambahan NaHSO3.”
PROSIDING SNTK TOPI 2012 ISSN. 1907–0500 Universitas Bung Hatta. Padang, Diseminarkan pada11 Juli 2012 di Pekanbaru.
[ ]Badan Pusat Statistik (BPS) (2014), “Luas Tanaman Perkebunan Besar Menurut Jenis Tanaman, Indonesia (000 Ha), 1995–2013,” Direktorat Jenderal Perkebunan. http://www.bps.go.id. Tanggal akses pada 23 September 2014.
[ ]Badan Pusat Statistik (BPS) (2014), “Produksi Perkebunan Menurut Provinsi dan Jenis Tanaman (ribu ton),” Direktorat Jenderal Perkebunan. Tanggal akses pada 23 September 2014.
44
Peternakan (April 2011), Terakreditasi B SK Dikti No: 43/DIKTI/Kep/2008, hlm.
35-41.
[ ]Suwanto, Yuke Octavianty, Silvia Hermawati, Top 15 Tanaman Perkebunan (Jakarta Timur: Penebar Swadaya, 2014), hal. 42
[ ]Fredrik Depparaba, “Penggerek Buah Kakao (Conopomorpha cramerella Snellen) dan Penanggulangannya.” Jurnal Litbang Pertanian Balai Pengkajian Teknologi Pertanian Sulawesi Tengah 21(2) 2002 : hal:69-74.
[ ]Misri Gozan, Teknologi Bioetanol Generasi Kedua (Jakarta: Penerbit Erlangga, 2014), hal.3-5, 10.
[ ]Kirk-Othmer, Encyclopedia of Chemical Technology (New York : International Science. Dursion of John Wiley and Sons, 1967) edisi 2. volume 9 hal.402.
[ ]Trisanti Anindyawati, “Potensi Selulase dalam Mendegradasi Lignoselulosa Limbah Pertanian untuk Pupuk Organik,” Berita Selulosa, 45(2) Desember 2010 : hal. 70–77.
[ ]M. Dashtban, Schraft, H., Qin, W, “Fungal Bioconversion of Lignocellulosic Residue: Opportunities & Perspectives,” International. Journal of Biology 5(6) 2009 : hal. 578-595.
[ ]James H. Clark dan Fabien E. I. Deswarte, Introduction To Chemicals From Biomass (United Kingdom: John Wiley and Sons, Ltd, Publication, 2008), hal. 17.
[ ]M. Edy Shofiyanto, “Hidrolisis Tongkol Jagung Oleh Bakteri Selulolitik Untuk Produksi Bioetanol Dalam Kultur Campuran.”Skripsi, Progam Sarjana Fakultas
Teknologi Pertanian Institut Pertanian Bogor, Bogor, 2008, hal. 20,23.
[ ]Howard, R.L., E. Abotsi, J.E.L. van Rensburg, S. Howard, “Lignocellulose Biotechnology: Issues Of Bioconversion And Enzyme Production.” African Journal Biotechnology, 2(12) 2003 : hal 606,609
[ ]Tesar Dzikrullah, Pengaruh Nisbah Reaktan Lignin-NaHSO3 Dan pH Pada Produk Natrium Lignosulfonat, Institut Pertanian Bogor, Bogor, 2007.
45
[ ]Diah Restu Setiawati, Anastasia Rafika Sinaga, Tri Kurnia Dewi, “Proses Pembuatan Bioetanol Dari Kulit Pisang Kepok.” Jurnal Teknik Kimia Universitas Sriwijaya. Palembang 1(19) Januari 2013 : hal 11-12.
[ ]Fessenden, R . J dan Fessenden, J. S, Kimia Organik Edisi Ketiga. Jilid 2. (Jakarta: Erlangga, 1986).
[ ]Ulrik Larsen, Troels Johansen, Jesper Schramm, “Ethanol As A Fuel For Road Transportation.” Report by The Danish Energy Authority (EFP 2006) (Mai 2009), hal. 11, Technical University of Denmark. Denmark.
[ ]Graeme M Walker, Bioethanol:Science and Technology of Fuel Alcohol (Scotland:Graeme M.Walker&Ventus Publishing Aps. Scotland., 2010).
[ ]Fifi Nurfiana, Umi Mukaromah, Vicki Citra Jeannisa, Sugili Putra, “Pembuatan Bioetanol dari Biji Durian Sebagai Sumber Energi Alternatif.” Jurnal ISSN 1978-0176 Sekolah Tinggi Teknologi Nuklir Badan Tenaga Nuklir Nasional (STTN-BATAN), Disampaikan dalam Seminar Nasional V SDM Teknologi Nuklir Yogyakarta, 5 November 2009.
[ ]I Wayan Arnata. “Pengembangan Alternatif Teknologi Bioproses Pembuatan Bioetanol Dari Ubi Kayu Menggunakan Trichoderma Viride, Aspergillus Niger Dan Saccharomyces Cerevisiae.” Tesis, Program Magister Sains Fakultas Teknologi Industri Pertanian IPB, Bogo, 2009, hal 9-11, 18.
[ ]Ashok Pandey, Handbook of Plant-Based Biofuels, (New York: CRC Press Taylor & Francis Group, 2009), hal.8,23.
[ ]Badger, P.C. “Ethanol from Cellulose: A General Review. In Trend New Crops and New Uses,” Reprinted from J.Jannick and A.Whipkey (eds). Alexandria, VA:ASHS Press 2002 : hal.17-22
[ ]Euis Hermiati, Djumali Mangunwidjaja, Titi Candra Sunarti, Ono Suparno, dan Bambang Prasetya, “Pemanfaatan Biomassa Lignoselulosa Ampas Tebu Untuk Produksi Bioetanol,” Jurnal Litbang Pertanian, 29(4) 2010 : hal:126.
46 www.epa.gov/region7/priorities/agriculture.
[ ]Caye M. Drapcho, Nghiem Phu Nhuan, Terry H. Walker, Biofuels Engineering Process Technology (New York: McGraw Hill, 2008), hal.20, 39-40.
[ ]N. Azizah, A.N. Al-Baarri, dan S. Mulyani, “Pengaruh Lama Fermentasi Terhadap Kadar Alkohol, pH, Dan Produksi Gas Pada Proses Fermentasi Bioetanol Dari Whey Dengan Substitusi Kulit Nanas,” Jurnal Aplikasi Teknologi Pangan, 1(2) 2012: hal. 75.
[ ]Rosdiana Moeksin, Shinta Francisca, “Pembuatan Etanol Dari Bengkuang Dengan Variasi Berat Ragi, Waktu, Dan Jenis Ragi”, Jurnal Teknik Kimia Universitas Sriwijaya Palembang, 2(17) April 2010 : hal.26.
[ ]H.M. Hatta Dahlan, RM. Zulkifli, “Konversi Biomassa Dari Buah Markisa Menjadi Bioetanol Sebagai Sumber Energi Alternatif”, Jurnal ISSN 1693-9050, III (November 2008), hal. 50.
[ ]Nadia Zahrotul Firdausi, Nugraha Bayu Samudro, Hargono, “Pemanfaatan Pati Singkong Karet (Manihot glaziovii) untuk Produksi Bioetanol Fuel Grade Melalui Proses Distilasi-Dehidrasi Menggunakan Zeolit Alam,” Jurnal Teknologi Kimia dan Industri Universitas Diponegoro, 2(3) 2013 : hal. 77.
[ ]Ninik Agustin, Lina Wahyuningrum, Dewanto Harjunowibowo, “ Rancang Bangun Teknologi Destilasi Bioetanol Untuk Bahan Bakar Terbarukan,” Universitas Sebelas Maret 2012 : hal.2.
[ ]M. Moniruzzaman, B.S. Dien, C.D. Skory, Z.D. Chen, R.B. Hespell, N.W.Y. Ho, B.E. Dale, R.J. Bothast, “Fermentation Of Corn Fibre Sugars By An Engineered Xylose Using Saccharomyces Yeast Strain,” World Journal of Microbiology and Biotechnology, XIII (1997), hal. 342.
[ ]Harimbi Setyawati, Nanik Astuti Rahman, “Bioetanol Dari Kulit Nanas Dengan Variasi Massa Saccharomyces Cereviceae Dan Waktu Fermentasi,” Institut Teknologi Nasional 2010 : hal.2.
47
[ ]Rozanna Sri Irianty, Silvia Reni Yenti, “Pengaruh Perbandingan Pelarut Etanol-Air Terhadap Kadar Tanin Pada Sokletasi Daun Gambir (Uncaria Gambir Roxb),” Jurnal ISSN, 1(13) Maret 2014 : hal. 1-7.
[ ]Asriyah Firdausi, Tri Agus Siswoyo, dan Soekadar Wiryadiputra, “Identifikasi Tanaman Potensial Penghasil Tanin-protein Kompleks Untuk Penghambatan Aktivitas α-amylase Kaitannya Sebagai Pestisida Nabati,” Jurnal Pelita Perkebunan, 29(1) Januari 2013 : hal. 31-43.
[ ]Nailul Hana. “Formulasi Tablet Hisap Ekstrak Etanol Gambir (Uncaria gambir Roxb) Dengan Variasi Konsentrasi Polyvynil Pyrrolidone (PVP) Sebagai Pengikat Dan Pengaruhnya Terhadap Kadar CD4 Dalam Darah.” Skripsi, Program Fakultas Kedokteran dan Ilmu Kesehatan Universitas Negeri Islam Syarif Hidayatulloh, Jakarta, 2010, hal. 19-20 dan 30.
[ ]Yuli Setyo Indartono, “Krisis Energi di Indonesia: Mengapa dan Harus Bagaimana,” Majalah INOVASI, ISSN: 0917-8376, Volume 5 /XVII/ Agustus 2005. Hal. 21-24
[ ]Haryadi, Sarjono,” Model Pengukuran Produktivitas Berdasarkan Pendekatan Rasio Output Per Input,” Jurnal The Winners, 02 (02). ISSN 1412 – 1212, 2001.
[ ]M.Syamsuri, H.Saptoadi, B.H.Tambunan, N.A.Pambudi, “A Preliminary Study On Use Of Cocoa Pod Husk As A Renewable Source Of Energy In Indonesian,” International Energy Initiative Published By Elsevier, Vol (16), Novemebr 2011,
Hal.74-77.
[ ]Gambir (Uncaria gambir) Diakses dari www.indonetwork.net pada 5 November 2015
[ ]Musa Trading Limited Diakses dari www.musatrading.com pada 5 November 2015
[ ]CNG Europe, ”Fuel Calorific Values,” diakses melalui www.CNG Europe.com pada 4 November 2015
[ ]Armon B.Christophe, “Structural Modified Food Fats, Shynthesis, Biochemistry, and Use,” The American Of Chemistru Society, 1998, Hal.49.
48
[ ]Ni Ketut Sari, “Pembuatan Bioetanol Dari Rumput Gajah Dengan Distilasi Batch,” Jurnal Teknik Kimia Indonesia Universitas Pembangunan Nasional Veteran Jawa Timur,
8(3) Desember 200, hal. 94-103.
[59]DR.Ir.M.Turmuzi Lubis, M.S., DR.Ir. Fatimah Batubara, M.T., Maya Sarah, S.T.M.T., Netty Herlina, S.T.M.T., “Kompilasi Buku Ajar Bioproses,” (Hibah Kompetisi Konten Matakuliah E-Leatning USU-INHERENT 2006, Hal.IV-3,IV 6-7). [ ]Mira Amalia Hapsari, Alice Pramashinta “Pembuatan Bietanol Dari Singkong Karet (Manihot Glaziovii) Untuk Bahan Bakar Kompor Rumah Tangga Sebagai Upaya Mempercepat Konversi Minyak Tanah Ke Bahan Bakar Nabati,” Jurnal Teknologi Kimia Dan Industri, 2(2) 2013. Hal. 240-245.
[ ]R.A. Day, Jr, A.L. Underwood, Analisa Kimia Kuantitatif. (Jakarta: Erlangga, 2002), hal. 54
24
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Kimia Analisa, Kimia Organik, Operasi Teknik Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan serta Laboratorium Biokimia serta Laboratoium Kimia Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam (MIPA) Universitas Sumatera Utara, Medan. Penelitian ini dilakukan selama lebih kurang 6 bulan.
3.2 BAHAN
Pada penelitian ini bahan yang digunakan antara lain: 1. Hidrolisat limbah kulit buah cokelat (Theobroma cacao, L) 2. Aquadest
3. Natrium hidroksida (NaOH) 4. Tanin
5. Fermipan yang diproduksi oleh Lesaffre di Perancis dan di Indonesia brand fermipan didistribusikan oleh PT. Sangra Ratu Boga, Jakarta Utara
3.3 PERALATAN
Pada penelitian ini peralatan yang digunakan antara lain: 1. Oven
2. Botol
3. Alumunium foil 4. Ball mill
5. Labu distilasi 6. Gabus
7. Termometer 8. Beaker Glass
25 12.Refluks kondensor
13.Rotary evaporator merk Ruchi Evaporator R-205
14.Spatula 15.Pipet Tetes 16.Kertas saring 17.pH meter 18.Corong gelas
3.4 RANCANGAN PENELITIAN
Penelitian ini menggunakan faktorial 3 x 4 dengan 3 kali pengulangan. Perlakuan awal limbah kulit kakao matang dikeringkan dan digiling dalam ball mill hingga berbentuk bubuk yang telah dihidrolisis menghasilkan hidrolisat kulit
kakao. Hidrolisat yang digunakan adalah volume total dari larutan hasil hidrolisis. Penelitian ini dilakukan dengan variabel bebas massa fermipan yang digunakan (E1, E2, dan E3) dan waktu fermentasi (t). Variasi jumlah fermipan yang ditambahkan adalah sebanyak 3% (w/w); 5% (w/w); 7% (w/w), jumlah tanin yang ditambahkan 4 gram, dan waktu fermentasi 2, 3, 4, dan 5 hari dengan kondisi anerobik. Adapun kombinasi perlakuan penelitian dapat dilihat pada tabel 3.1 berikut:
Tabel 3.1 Rancangan Penelitian
massa fermipan waktu (t, hari)
2 hari (t1) 3 hari (t2) 4 hari (t3) 5 hari (t4)
3% (w/w) E1t1 E1t2 E1t3 E1t4
5% (w/w) E2t2 E2t2 E2t3 E2t4
26 3.5 PROSEDUR
3.5.1 Prosedur Penelitian
Fermentasi Hidrolisat Limbah Kulit Kakao
a. Proses Fermentasi
Prosedur proses fermentasi diadopsi dari [7], [28], [58], [48], [46] sebagai berikut: 1. Hasil glukosa terbaik yang diperoleh dari proses hidrolisis, yaitu glukosa
yang diperoleh dari hidrolisis kulit kakao.
2. Diatur pH-nya menjadi 4,5 yang diukur dengan pH-meter. Pengaturan pH dilakukan dengan menambahkan NaOH 4 M.
3. Hidrolisat tersebut kemudian didinginkan hingga mencapai suhu ruangan.
4. Dilakukan sterilisasi alat beserta hidrolisat kulit buah kakao dengan menggunakan oven.
5. Masukkan fermipan ke dalam hidrolisat kulit kakao dengan konsentrasi 3, 5, 7 % (w/w) dari volume total hidrolisat.
6. Ditambahkan tanin 4 gram.
7. Lalu diaduk diaduk selama 5 menit sampai homogen.
8. Menutup rapat botol.
9. Selanjutnya larutan difermentasi selama 2, 3, 4, dan 5 hari.
10.Hasil dari fermentasi yang didapat dimasukkan ke dalam labu distilasi. 11.Dilakukan distilasi pada suhu 80 oC hingga tidak ada lagi distilat yang
keluar.
12.Distilat yang keluar diperoleh berupa etanol.
13.Dianalisis kadar etanolnya menggunakan instrumen GC di PPKS (Pusat Penelitian Kelapa Sawit) Medan
Analisis hasil penelitian berupa:
27 Uji Indeks Bias Bioetanol
Prosedur analisis indeks bias bioetanol dilakukan menggunakan alat refraktometer ABBE untuk sampel hasil kondisi optimum di laboratorium kimia fisika fakultas MIPA Universitas Sumatera Utara.
3.6 FLOWCHART 3.6.1 Flowchart Penelitian
Fermentasi Hidrolisat Limbah Kulit Kakao
a. Proses Fermentasi
Dimasukkan glukosa yang diperoleh dari hidrolisis kulit kakao ke dalam erlenmeyer
Diaduk selama 5 menit sampai homogen Mulai
Dimasukkan ragi ke dalam hidrolisat kulit kakao dengan konsentrasi 3; 5; 7 % (w/w) dari volume total
hidrolisat
Ditambahkan tanin 4 gram
Ditambahkan NaOH 4 M untuk mengatur pH-nya menjadi 4,5 yang diukur dengan pH-meter
Hidrolisat tersebut kemudian didinginkan hingga mencapai suhu ruangan
Dilakukan sterilisasi alat beserta hidrolisat kulit buah kakao dengan menggunakan oven
28
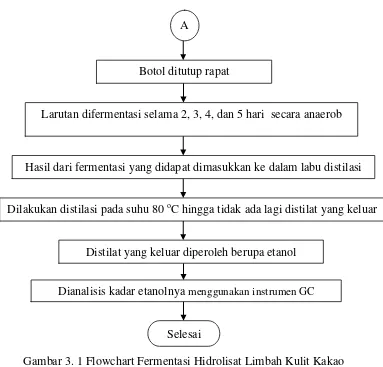
Gambar 3. 1 Flowchart Fermentasi Hidrolisat Limbah Kulit Kakao Hasil dari fermentasi yang didapat dimasukkan ke dalam labu distilasi
Dilakukan distilasi pada suhu 80 oC hingga tidak ada lagi distilat yang keluar
Dianalisis kadar etanolnya menggunakan instrumen GC Distilat yang keluar diperoleh berupa etanol
Selesai Botol ditutup rapat
29
BAB IV
HASIL DAN PEMBAHASAN
4.1 PENGARUH VARIABEL PERCOBAAN TERHADAP KADAR BIOETANOL SELAMA PROSES FERMENTASI
4.1.1 Pengaruh Waktu Fermentasi Terhadap Yield Bioetanol
Adapun hasil penelitian pembuatan bioetanol dari kulit buah cokelat menggunakan hidrolisis asam sulfat terhadap variasi waktu fermentasi sebagai berikut:
Gambar 4.1 Pengaruh Waktu Fermentasi Terhadap Yield Bioetanol
Hubungan antara pengaruh waktu fermentasi terhadap yield etanol dapat dilihat pada grafik 4.1. diatas. Dari grafik terlihat pada kadar fermipan 3% dan 5% (w/w) mengalami peningkatan yield bioetanol seiring berjalannya waktu fermentasi, pada kadar fermipan 7% (w/w) mengalami peningkatan pada hari ke-3 lalu mengalami penurunan pada hari ke-4 dan ke-5. Dari hasil tersebut dapat disimpulkan pada kadar fermipan 5% (w/w) merupakan hasil yang cukup bagus terhadap yield yang dihasilkan karena jumlah yield terbanyak dihasilkan pada kadar 5% (w/w) hari ke-5 yaitu 34,5488%.
Enzim dalam ragi pertama-tama mengubah karbohidrat yang terdapat dalam kulit buah cokelat yaitu selulosa, hemiselulosa menjadi karbohidrat yang lebih sederhana seperti
0 5 10 15 20 25 30 35 40
2 3 4 5
Y ield B ioet an ol (% )
Waktu Fermentasi (hari)
30
glukosa dan fruktosa, keduanya C6H12O6, lalu mengubah karbohidrat sederhana tersebut
diubah menjadi etanol dan karbon dioksida, sedangkan lignin sudah terhidrolisis oleh asam sulfat pada saat proses hidrolisis asam berlangsung.
Reaksi pembentukan etanol terjadi karena adanya aktivitas dari yeast yang ada pada substrat.
Yeast akan menggunakan materi yang mengandung karbon seperti glukosa untuk proses respirasi.
Reaksi yang terjadi adalah sebagai berikut [ ] : C6H12O6 + 6O2→ 6CO2 + 6H2O + energi
Apabila kondisi ini tidak ada oksigen, maka reaksi yang terjadi adalah reaksi pembentukan etanol. Reaksi selengkapnya dari fermentasi glukosa menggunakan ragi sebagai berikut: Glikolisis: Glukosa (+ 2 ADP + 2 NAD+) → 2 Piruvat + 2 ATP + 2 NADH
Fermentasi:
2 Piruvat → 2 Asetaldehid + 2 CO2
2 Asetaldehid + 2 NADH → 2 Etanol + 2 NAD
Reaksi fermentasi glukosa selengkapnya yang menggunakan ragi tidak melibatkan pertumbuhan sel
Glukosa (+ 2 ADP) → 2 Etanol + 2 CO2 + 2 ATP
C6H12O6 (+ 2 ADP) → 2 C2H5OH + 2 CO2 + 2 ATP
[ ]
Hal ini berarti selama berlangsungnya fermentasi terjadi pengurangan glukosa sebagai substrat karena glukosa tersebut digunakan oleh khamir Saccharomyces cerevisiae yang ada dalam fermipan sebagai sumber nutrisi untuk mengonversi menjadi etanol. Jadi semakin banyak terjadinya pengurangan glukosa maka jumlah etanol yang dihasilkan pun semakin banyak.
31
Fase pertumbuhan diperlambat mulai pada akhir fasa eksponensial. Pertumbuhan mikroba yang begitu cepat tidak diimbangi tersedianya nutrisi yang cukup. Jika fermentasi dilakukan secara batch, dimana umpan nutrisi dimasukkan hanya pada awal proses fermentasi, pada waktu tertentu saat jumlah mikroba yang mengonsumsi nutrisi tersebut melebihi daya dukung nutrisi akan terjadi kekurangan nutrisi. Hal lain yang memperlambat pertumbuhan mikroba adalah terjadinya inhibisi ataupun represi yang terjadi karena terakumulasinya produk metabolit sekunder hasil aktifitas fermentasi mikroorganisme [59]. Hal inilah yang terjadi pada kadar fermipan 7%. Pada hari ke-3 proses fermentasi masih bergejolak mengonversikan menjadi bioetanol dan kadar bioetanol yang dihasilkan 96,9406% dengan yield 34,3276%. Pada hari ke-4 yield yang dihasilkan menurun menjadi 13,4545% tetapi kadar bioetanol yang dihasilkan yaitu 98,8325% karena pada saat ini sedang berlangsung katabolisme primer menghasilkan senyawa metabolit primer untuk kelangsungan proses fermentasi dan juga sedang berlangsung anabolisme sekunder menghasilkan senyawa metabolit sekunder sehingga walaupun yield yang dihasilkan menurun tetapi kadar yang dihasilkan mengalami peningkatan. Untuk menghasilkan yield yang lebih bnyak lagi disarankan untuk melakukan penambahan kadar fermipan.
Metabolik primer adalah produk yang berkaitan dengan pertumbuhan Metabolit sekunder berkaitan dengan fase tanpa pertumbuhan [59]. Contoh metabolit primer misalnya asam amino, asetil CoA, gula-gula, nukleotida, asam sitrat, lipid, protein, dan karbohidrat, sedangkan contoh metabolit sekunder misalnya senyawa yang diturunkan dari metabolit primer seperti protein, lipid, asam nukleat, dan karbohidrat.
Hal ini sesuai pada penelitian sebelumnya yang dilakukan oleh Agustinus Eka P dan Amran Halim, (2009) melakukan fermentasi nira siwalan dengan variasi kadar starter fermipan 5%, 10%, 15% seiring bertambahnya hari fermentasi besarnya kadar fermipan maka yield etanol yang dihasilkan semakin besar yaitu sebanyak 48,16% [ ]..
32
Sehingga dari hasil penelitian yang telah dilakukan semakin lama waktu fermentasi yaitu sebanyak 2, 3, 4, 5 hari maka yield bioetanol yang dihasilkan pun semakin besar.
4.1.2 Pengaruh Waktu Fermentasi Terhadap Kadar Bioetanol
Etanol dan bioetanol memiliki rumus molekul yang sama yaitu etanol atau etil alkohol, yang merupakan golongan alkohol dengan kandungan dua buah atom karbon. Istilah bioetanol muncul karena bahan baku yang digunakan berasal dari alam yang mengandung karbohidrat dan dengan proses fermentasi memanfaatkan bahan terbarukan tersebut dengan bantuan mikroba menguraikannya menjadi etanol.
Kulit buah cokelat diperoleh dari kota Padang, Binjai, dan Serbelawan. Hal pertama yang dilakukan yaitu pengeringan kulit buah cokelat dengan memanfaatkan sinar matahari lalu penggilingan di ball mill hingga terbentuk bubuk kulit buah cokelat. Kemudian proses selanjutnya yaitu hidrolisis dengan menggunakan asam sulfat 4 M selama 2 jam dengan suhu 100 oC lalu hidrolisatnya difermentasi selama 2, 3, 4, dan 5 hari menggunakan ragi roti dan
diberi tanin.
Proses hayati pembuatan bioetanol sering disebut sebagai proses fermentasi. Sebenarnya proses yang terjadi tidak hanya fermentasi. Namun, fermentasi menjadi jantung utama dari pembuatan bioetanol [ ]. Proses fermentasi menggunakan mikroorganisme untuk mengonversikan karbohidrat sederhana misalnya glukosa menjadi etanol. Dalam penelitian ini digunakan yaitu berupa yeast atau ragi roti dengan nama merk dagang yaitu fermipan yang mengandung khamir Saccharomyces cerevisiae yang diproduksi oleh Lesaffre di Perancis dan di Indonesia brand fermipan didistribusikan oleh PT. Sangra Ratu Boga, Jakarta Utara.
33
Gambar 4.2 Grafik Pengaruh Waktu Fermentasi Terhadap Kadar Bioetanol
Hubungan antara pengaruh waktu fermentasi terhadap kadar bioetanol dapat dilihat pada grafik 4.2 diatas. Dari grafik 4.2 hasil dapat dilihat bahwa grafik mengalami fluktuatif pada kadar fermipan 5% (w/w). Penurunan kadar etanol terjadi pada hari ke-3 yaitu dari 97,4212% pada hari ke-2 menjadi 92,2954% pada hari ke-3 lalu meningkat pada hari ke-4 dan menurun pada hari ke-5. Sesuai dari persamaan rumus tentang penghitungan yield yang terlampir di lampiran 2 yaitu yield berbanding terbalik dengan kadar selain itu pada hari ke-3 tersebut terjadi penurunan kadar etanol karena terjadi pengurangan sumber-sumber nutrisi.
Dari grafik 4.2 terlihat pada kadar fermipan 3% (w/w) mengalami peningkatan kadar bioetanol pada hari ke-3 lalu penurunan kadar bioetanol pada hari ke-4 dan ke-5, pada kadar fermipan 5% (w/w) mengalami penurunan pada hari ke-3 lalu mengalami peningkatan pada hari ke-4 dan penurunan pada hari ke-5, pada kadar fermipan 7% (w/w) mengalami peningkatan kadar bioetanol namun akhirnya mengalami penurunan kadar bietanol pada hari ke-5. Dari hasil tersebut dapat disimpulkan pada kadar fermipan 3% (w/w) merupakan hasil yang bagus terhadap penelitian yang telah dilakukan karena kadar bioetanol terbesar terdapat disini. Selain itu, kadar bioetanol pada hari ke-2 menuju hari ke-3 mengalami peningkatan artinya pada masa itu mulai terjadi peningkatan pengonversian glukosa yang terdapat pada substrat menjadi bioetanol dan kadar bioetanol juga meningkat lalu menuju hari ke-4 mulai terjadi penurunan kadar bioetanol tetapi perbedaan harga kadar tidak terlalu signifikan, lalu selanjutnya mengalami penurunan kadar bioetanol menuju hari ke-5.
70 75 80 85 90 95 100
2 3 4 5
K ad ar B ioet an ol (% )
Waktu Fermentasi (hari)
34
Penggunaan mikroba dalam fermentasi alkohol merupakan salah satu faktor penting dalam proses fermentasi. Sebagaimana dalam teori disebutkan bahwa dalam fermentasi alkohol umumnya menggunakan khamir karena khamir dapat mengonversi gula menjadi alkohol dengan adanya enzim zimase [ ].
Faktor yang berperan penting dalam proses ini adalah enzim yang berasal dari sel fungi uniseleluler yang biasa disebut ragi atau yeast. Adapun fase-fase pertumbuhan ragi adalah fase lambat, fase cepat, fase stasioner, dan fase kematian [ ]. Ini berarti berkaitan dengan pertumbuhan dari Saccharomyces cerevisiae.s
Hal ini sesuai pada kadar fermipan 7% (w/w) dimana pada kadar fermipan 7% (w/w) mengalami peningkatan kadar bioetanol namun akhirnya mengalami penurunan kadar bietanol pada hari ke-5. Pada hari ke-2, ke- 3 dan ke-4 terjadi peningkatan kadar bioetanol hingga jumlah maksimum yaitu pada hari ke-4 dapat dilihat dari kadar etanol yang dihasilkan. Kemudian pada hari ke-5 terjadi penurunan kadar etanol karena terjadi pengurangan sumber-sumber nutrisi atau pembentukan zat racun sebagai akhir metabolisme.
Hal ini sesuai teori yaitu pada fase cepat jumlah sel yang terbetuk dipengaruhi oleh beberapa faktor, antara lain pH dan kandungan nutrisi, suhu, kadar oksigen, cahaya, dan keberadaan mikroorganisme lainnya [ ] kemudian aktivitas metabolisme akan menurun setelah mikroorganisme melewati fase puncak pertumbuhannya, fase penurunan ini disebut death phase [ ]. Pada penelitian ini mempunyai variasi waktu fermentasi yaitu 2, 3, 4, dan 5 hari dan waktu optimum untuk fermentasi yaitu 4 hari dan pada kadar fermipan 3% (w/w) pada hari ke-3 merupakan hasil kadar terbanyak.
Pada penelitian ini juga menggunakan tambahan tanin, yaitu berupa gambir kandungan tanin sebesar 30-40% [ ] yang berfungsi sebagai penghambat terbentuknya asam asetat karena senyawa tanin dapat larut dalam air. Hal ini sesuai teori yaitu semua jenis tanin dapat larut dalam air. Kelarutannya besar, dan akan bertambah besar apabila dilarutkan dalam air panas. Tanin akan terurai menjadi pyrogallol, pyrocatechol dan phloroglucinol bila dipanaskan sampai suhu 210 °F-215 °F (98,89 °C-101,67 °C). Tanin dapat dihidrolisa oleh asam, basa dan enzim [ ].
Hal ini sesuai pada penelitian sebelumnya yang dilakukan oleh Putu Kristiani K, dkk (2013) melakukan fermentasi selama 14 hari menggunakan filtrat cairan pulp kakao dan Saccharomyces cerevisiae dengan tambahan kulit bakau sebagai sumber tanin menghasilkan
35
oleh Agustinus Eka P dan Amran Halim (2009) melakukan fermentasi nira siwalan dengan fermipan menghasilkan kadar etanol maksimum yang diperoleh adalah 6,17% pada hari ke-4
[ ]. Sehingga dari penelitian yang dilakukan bahwa dengan adanya tambahan gambir sebagai sumber tanin dalam proses fermentasi kulit buah cokelat dapat menghambat terbentuknya
asam asetat dan menghasilkan bioetanol dengan kadar yang cukup bagus.
4.1.3 Pengaruh Kadar Fermipan Terhadap Kadar Bioetanol
Dalam penelitian ini digunakan fermipan dengan kadar yaitu 3%, 5%, dan 7% (w/w). Adapun hasil penelitian pembuatan bioetanol dari kulit buah cokelat menggunakan hidrolisis asam sulfat terhadap variasi waktu fermentasi sebagai berikut:
Gambar 4.3 Grafik Pengaruh Kadar Fermipan 3% (w/w) Terhadap Kadar Bioetanol 82
84 86 88 90 92 94 96 98 100 102
2 3 4 5
K
ad
ar
B
ioet
an
ol (%
)
36
[image:30.595.181.418.387.562.2]Gambar 4.4 Grafik Pengaruh Kadar Fermipan 5% (w/w) Terhadap Kadar Bioetanol
Gambar 4.5 Grafik Pengaruh Kadar Fermipan 7% (w/w) Terhadap Kadar Bioetanol
Hubungan antara pengaruh kadar fermipan terhadap kadar bioetanol dapat dilihat pada grafik 4.3, 4.4, dan 4.5. diatas. Dari grafik 4.4 hasil dapat dilihat bahwa grafik mengalami fluktuatif, sedangkan pada grafik 4.3 dan 4.5 terlihat bagus.
Dari grafik 4.4 hasil dapat dilihat bahwa grafik mengalami fluktuatif. Dari grafik terlihat pada kadar fermipan 3% (w/w) mengalami penurunan kadar bioetanol pada hari ke-4 dan ke-5, pada kadar fermipan 5% (w/w) mengalami penurunan pada hari ke-3 lalu mengalami peningkatan pada hari ke-4 dan penurunan pada hari ke-5. Dari grafik 4.5 pada
80 82 84 86 88 90 92 94 96 98 100
2 3 4 5
K adar Bi oe tanol (% )
Waktu Fermentasi (hari)
82 84 86 88 90 92 94 96 98 100
2 3 4 5
K ad ar B ioet an ol (% )
37
kadar fermipan 7% (w/w) mengalami peningkatan kadar bioetanol namun akhirnya mengalami penurunan kadar bietanol pada hari ke-5. Dari hasil tersebut dapat disimpulkan pada kadar fermipan 7% (w/w) merupakan hasil yang bagus terhadap penelitian yang telah dilakukan.
Sebelum berlangsungnya proses fermentasi, fermipan dimasukkan sesuai dengan kadarnya dan tanin juga dimasukkan lalu dihomogenkan dan campuran dibiarkan pada keadaan suhu ruangan (sekitar 30 oC) selama beberapa hari sampai fermentasi berlangsung sempurna. Udara tidak dibiarkan masuk ke dalam campuran tersebut untuk menghindari terjadinya oksidasi etanol menjadi asam etanoat, asam asetat, ataupun senyawa ester.
Enzim dalam ragi pertama-tama mengubah karbohidrat yang terdapat dalam kulit buah cokelat yaitu selulosa, hemiselulosa menjadi karbohidrat yang lebih sederhana seperti glukosa dan fruktosa, keduanya C6H12O6, lalu mengubah karbohidrat sederhana tersebut
diubah menjadi etanol dan karbon dioksida, sedangkan lignin sudah terhidrolisis oleh asam sulfat pada saat proses hidrolisis asam berlangsung.
Hal ini berarti selama berlangsungnya fermentasi terjadi pengurangan glukosa sebagai substrat karena glukosa tersebut digunakan oleh khamir Saccharomyces cerevisiae yang ada dalam fermipan sebagai sumber nutrisi untuk mengonversi menjadi etanol. Jadi semakin banyak terjadinya pengurangan glukosa maka jumlah etanol yang dihasilkan pun semakin banyak dan semakin besar persen starter maka kadar etanol yang dihasilkan semakin besar juga.
Hal ini sesuai pada kadar fermipan 7% (w/w) yaitu seiring berjalannya waktu fermentasi, kadar etanol yang dihasilkan meningkat, sedangkan pada kadar fermipan 3% (w/w) grafik yang dihasilkan cukup bagus dan pada kadar fermipan 5% (w/w) mengalami fluktuatif tetapi tidak banyak perbedaan kadar etanol yang dihasilkan antara hari 3 dan ke-4. Hal ini disebabkan menurunnya metabolisme khamir Saccharomyces cerevisiae yang ada dalam fermipan karena berkurangnya sumber nutrisi selama fermentasi.
38
yang lebih bnyak lagi disarankan untuk melakukan penambahan kadar fermipan karena masih berpotensi menghasilkan yield yang lebih banyak dengan kadar yang meningkat.
Hal ini sesuai pada penelitian sebelumnya yang dilakukan oleh Agustinus Eka P dan Amran Halim, (2009) melakukan fermentasi nira siwalan dengan variasi kadar starter fermipan 5%, 10%, 15% seiring bertambahnya hari fermentasi besarnya kadar fermipan maka kadar etanol yang dihasilkan semakin besar yaitu pada kadar 15% [ ]..
Hal ini sesuai pada penelitian sebelumnya yang dilakukan oleh Mira Amalia Hapsari dan Alice Pramashinta (2013) melakukan fermentasi etanol singkong karet menggunakan ragi yang mengandng Saccharomyces cerevisiae dengan variasi massa fermipan 5, 10, dan 15 gram seiring bertambahnya massa fermipan kadar etanol yang dihasilkan meningkat yaitu pada 15 gram [ ].
Hal ini sesuai pada penelitian sebelumnya yang dilakukan oleh Osvaldo Z. S., Panca Putra S., M. Faizal (2012) melakukan hidrolisis menggunakan asam sulfat dan fermentasi pembuatan bioetanol menggunakan alang-alang dengan variasi fermipan dan ragi tape 5%, 10%, 15%, 20%, dan 25% dari berat feed seiring bertambahnya masa fermipan kadar etanol yang dihasilkan meningkat yaitu pada kadar fermipan 25% sebesar pada fermipan yaitu 4,8% sedangkan pada ragi tape yaitu 5% [ ].
Sehingga dari hasil penelitian yang telah dilakukan kadar fermipan 7% (w/w) merupakan kadar yang cukup bagus untuk kenaikan kadar bioetanol seiring berjalannya waktu fermentasi pada fermentasi hidrolisat kulit kakao ini.
4.1.4 Indeks Bias Bioetanol
Indeks bias adalah perbandingan antara kecepatan cahaya dalam udara dengan kecerahan cahaya dalam zat. Indeks bisa digunakan untuk mengidentifikasi zat dan mendeteksi ketidakmurnian cairan. Refraktometer adalah alat yang tepat dan cepat untuk menetapkan nilai indeks bias. [ ]. Indeks bias merupakan salah satu sifat fisika yang dimiliki etanol. Sampel diuji dengan menggunakan alat refraktometer ABBE di laboraotrium kimia fisika FMIPA USU.
39
40
BAB V
KESIMPULAN
5.1 KESIMPULAN
Adapun kesimpulan dari hasil penelitian yang telah dilakukan adalah:
1) Berdasarkan hasil GC pengujian kadar bioetanol, pada kadar fermipan 3%(w/w) kadar etanol terbesar terdapat pada waktu fermentasi selama 3 hari yaitu 99,8174%, pada kadar fermipan 5%(w/w) kadar etanol terbesar terdapat pada waktu fermentasi selama 2 hari yaitu 97,42125, pada kadar fermipan 7%(w/w) kadar etanol terbesar terdapat pada waktu fermentasi selama 4 hari yaitu 98,8325 2) Pada kadar fermipan 5% (w/w) merupakan hasil yang cukup bagus terhadap yield yang dihasilkan karena jumlah yield terbanyak dihasilkan pada kadar 5% (w/w) hari ke 3 yaitu 9,6 ml, tetapi di hari selanjutnya jumlah yield mengalami penurunan hingga hari ke-5.
3) Hasil uji indeks bias etanol yaitu 1,3285.
4) Adanya tambahan gambir sebagai sumber tanin dalam proses fermentasi kulit buah cokelat dapat menghambat tejadinya oksidasi pada etanol misalnya
terbentuknya asam asetat maupun senyawa ester dan menghasilkan etanol
dengan kadar yang cukup bagus.
5) Pada kadar fermipan 7% (w/w) berpotensi untuk dilakukan penambahan kadar pada proses fermentasinya. Hal ini dapat dilihat pada hari ke-4 fermentasi
mengalami peningkatan kadar bioetanol tetapi yield yang dihasilkan menurun
karena pada saat ini juga dihasilkan senyawa metabolit primer dan senyawa
41 5.2 SARAN
Adapun saran yang dapat diberikan demi hasil yang lebih baik lagi dari hasil penelitian yang telah dilakukan adalah:
1) Disarankan untuk memberi tambahan nutrisi untuk proses fermentasi selain dari glukosa yang terdapat dalam bahan baku untuk menghasilkan volume etanol yang lebih banyak.
6
BAB II
TINJAUAN PUSTAKA
2.1 BUAH KAKAO (Theobroma cacao L.)
Indonesia merupakan tiga negara terbesar penghasil buah kakao (Theobroma cacao L.) didunia. Data dari Badan PBB untuk Pangan dan Pertanian (FAO) menyebutkan, Indonesia memproduksi 574.000 ton kakao di tahun 2010 menyumbang sekitar 16% dari produksi kakao secara global [ ].
[image:36.612.160.352.368.482.2]Kakao merupakan salah satu komoditas andalan perkebunan yang peranannya cukup penting bagi perekonomian nasional, khususnya sebagai penyedia lapangan kerja, sumber pendapatan dan devisa negara [ ]. Luas perkebunan kakao di Indonesia sudah mencapai 84.700 ha pada tahun 2013 [ ].
Tabel 2.1 Produksi kakao (ribu ton) di Sumatera Utara [ ] Tahun Produksi (ribu ton)
2007 64,8
2008 60,3
2009 67,3
2010 63,4
2011 54,5
2012 37,16
2013 36,19
7
Tabel 2.2 komposisi kulit buah kakao [ ][ ][ ]
Komponen Jumlah (%)
serat kasar 40,03%
protein 9,71%
selulosa 36,23%
hemiselulosa 1,14%
lignin 20%-27,95%
abu 41,60%
lemak kasar 21,74%
Bahan Ekstrak Tanpa Nitrogen (BETN) 31,41% Total Digestible Nutrient (TDN) 52,88% Neutral Detergent Fiber (NDF) 75,36% Acid Detergent Fiber (ADF) 68,70%
(Dari tabel 2.2 di atas dengan komposisi selulosa yang cukup banyak dapat dilihat bahwa kulit kakao memiliki potensi untuk mengonversi glukosa yang ada pada substratnya menghasilkan bioetanol).
Selain biji, limbahnya sangant sangat bermanfaat, baik kulit buah, pulp, maupun plasentanya. Kulit buah cokelat dapat digunakan untuk campuran bahan makanan ternak, sumber gas bio, dan bahan pembuatan pectin. Pulp dan plasenta sebagai limbah pada fermentasi biji cokelat berguna untuk pembuatan alkohol dan cocoa jelly [ ].
Melihat kondisi di atas, maka sebenarnya Indonesia memiliki potensi yang luar biasa untuk mengembangkan BBN (Bahan Bakar Nabati) dari kulit buah kakao. Terlebih lagi kakao telah benar-benar dicanangkan untuk dikembangkan secara besar-besaran oleh pemerintah. Hal ini akan menjadi nilai positif bagi Indonesia karena produksi bijinya ditingkatkan secara kualitas maupun kuantitas serta limbahnya dimanfaatkan sebagai BBN (Bahan Bakar Nabati). Jadi tidak akan ada limbah yang terbuang percuma dan akan menjadi keuntungan bagi Indonesia [ ].
Kakao merupakan satu-satunya dari 22 jenis marga Theobroma, suku Sterculiaceae, yang diusahakan secara komersial. Menurut Tjitrosoepomo (1988) sistematika tanaman ini sebagai berikut:
8
Anak kelas : Dialypetalae Bangsa : Malvales Suku : Sterculiaceae Marga : Theobroma
[image:38.612.211.399.93.320.2]Jenis : Theobroma cacao, L
Gambar 2.1 Buah Kakao (Theobroma cacao, L)[ ]
PT. Perkebunan XXVI (1991) melaporkan bahwa daging buah, pulp dan plasenta merupakan bagian dari buah kakao yang dimasukkan sebagai kulit. Sedangkan dari 15 Kg buah akan diperoleh lebih kurang 12 Kg kulit buah kakao basah, dan lebih kurang 3 Kg biji kakao basah (sekitar 1 Kg biji kakao kering). Jika memang secara garis besar produksi kakao tersebut dalam bentuk biji, maka akan diperoleh limbah yang sangat melimpah. Misalnya saja pada tahun 2008 Indonesia dapat menghasilkan biji kakao 803.594 ton maka limbah yang tersedia sekitar 3.214.367 ton. Dengan demikian, kulit buah kakao sangat berpotensi digunakan sebagai bahan baku pembuatan BBN yang berupa bioetanol [ ].
2.2 SELULOSA
9
selulosa pada kayu rata-rata 48-50% sedangkan pada bagas berkisar antara 49-55% [ ], sedangkan pada kulit buah kakao sebesar 36,23% [ ].
Teknologi untuk mengonversi selulosa menjadi etanol sudah ada, tetapi stoikiometri dari prosesnya merugikan. Walaupun setiap langkah dalam proses konversi fermentasi glukosa menjadi etanol menghasilkan yield 100%, hampir dua per tiga selulosanya menghilang, terkonversi menjadi karbon dioksida saat fermentasi glukosa menjadi etanol [ ].
Bahan lignoselulosa merupakan komponen organik berlimpah di alam, yang terdiri dari tiga polimer yaitu selulosa, hemiselulosa dan lignin. Komponen terbesar adalah selulosa (35-50%), hemiselulosa (20-35%) dan lignin (10-25%) [ ].
Selulosa adalah unsur pokok pada tanaman dan merupakan biopolimer linier dari molekul anhidroglukopiranosa pada ikatan β-1,4 glukosidik yang berlimpah di alam [ ].
Selulosa [C6(H2O)5]n [ ]merupakan bahan yang kaya akan karbon. Karbon yang
[image:39.612.202.477.450.535.2]terkandung dalam selulosa dapat dimanfaatkan dalam proses fermentasi mikroba. Sebelum difermentasi, selulosa tersebut harus disakarifikasi terlebih dahulu menjadi gula-gula sederhana (glukosa dan fruktosa) [ ].
Gambar 2.2 Molekul Selulosa [ ]
Hemiselulosa [C5(H2O)4]n [ ]merupakan istilah umum bagi polisakarida yang larut dalam alkali. Hemiselulosa sangat dekat asosiasinya dengan selulosa dalam dinding
sel tanaman [ ].
Lignin [C10H12O4]n [ ] adalah polimer yang tersusun oleh unit fenil propana.
10
eter (C–O–C), sedangkan sisanya oleh ikatan karbon (C–C). Ikatan tersebut menyebabkan lignin tahan terhadap hidrolisis. Akan tetapi, lignin terurai menjadi asam format, metanol, asam asetat, aseton, dan vanilin pada suhu tinggi. Pereaksi yang biasa digunakan untuk mengendapkan lignin ialah H2SO4 pekat dan HCl pekat [ ].
2.3 BIOETANOL
Bioetanol dapat dibuat dari bahan-bahan bergula atau bahan berpati seperti tebu, nira nipah, sagu, sorgum, ubi kayu, ubi jalar, ganyong, dan lain-lain. Bahan-bahan tersebut banyak tersedia di Indonesia, sehingga sangat berpeluang untuk digunakan sebagai energi alternatif. Bioetanol sangat berpotensi dikembangkan di Indonesia, karena didukung oleh potensi lahan yang luas, sumberdaya manusia (petani), keanekaragaman hayati, dan sumberdaya alam yang melimpah [ ].
Bioetanol sering ditulis dengan rumus EtOH. Rumus molekul etanol adalah C2H5OH, sedang rumus empirisnya C2H6O atau rumus bangunnya CH3-CH2-OH.
Bioetanol merupakan bagian dari kelompok metil (CH3-) yang terangkai pada kelompok
metilen (-CH2-) dan terangkai dengan kelompok hidroksil (-OH). Secara umum akronim
[image:40.612.291.390.442.505.2]dari bioetanol adalah EtOH (Ethyl-(OH)) [ ].
Gambar 2.3. Rumus Bangun Bioetanol [ ]
Bioetanol memiliki potensi untuk mengurangi gas rumah kaca berdasarkan metode produksinya. Bioetanol ini berpotensi untuk mengganti bahan bakar minyak fosil menjadi bahan bakar yang terbarukan sehingga menjadi alasan utama mengapa etanol dipertimbangkan dan diimplementasikan[ ].
11
difermentasi. Bioetanol dapat dimanfaatkan sebagai bahan bakar cair untuk mesin pembakaran internal, baik sebagai bahan bakar tunggal yang digunakan maupun bercampur dengan minyak bumi [ ].
2.4 ETANOL
Etanol yang disebut juga sebagi etil alkohol, mempunyai sifat berupa cairan yang tidak stabil, mudah terbakar dan tidak berwarna. Etanol merupakan alkohol rantai lurus dengan rumus molekul C2H5OH [ ], larut dalam air, eter, aseton, benzene, dan semua
[image:41.612.200.456.331.490.2]pelarut organik, serta memiliki bau khas alkohol. Sifat-sifat kimia dan fisis ethanol sangat tergantung pada gugus hidroksil. Pada tekanan > 0,114 bar (11,5 kPa) etanol dan air dapat membentuk larutan azeotrop [ ].
Tabel 2.3 Sifat Fisika Etanol [ ]
Properti Nilai
Berat Molekul (g/mol) 46,1
Titik Beku (oC) -114,1
Titik Didih Normal (oC) 78,32
Densitas (g/ml) 0,7983
Viskositas (Cp) 1,17
Panas penguapan normal (J/kg) 839,31 Panas pembakaran (J/kg) 29676,6
Panas jenis (J/kg) 2,42
Nilai oktan Indeks Bias
106-111 1,36143
Etanol terbagi dalam tiga grade, yaitu grade industri dengan kadar alkohol 90-94%, netral dengan kadar alkohol 96-99,5% umumnya digunakan untuk minuman keras atau bahan baku farmasi dan grade bahan bakar dengan kadar alkohol diatas 99,5% [ ].
12
cepat sampai tahun 2015 karena adanya larangan penggunaan metil tert-butyl eter (MTBE) dalam bensin. Peraturan perundang-undangan baru yang mendukung penggunaan bahan bakar bio sudah diterapkan di Brazil dan belahan lain dunia [ ].
2.5 FERMENTASI
Proses sintesis bioetanol meliputi perlakuan awal, hidrolisis, fermentasi dan
distilasi. Bahan yang mengandung gula dapat langsung difermentasi, akan tetapi bahan
yang mengandung pati dan selulosa harus dihidrolisis terlebih dahulu menjadi
komponen yang sederhana [ ].
Pada tahap sakarifikasi, selulosa diubah menjadi selobiosa dan selanjutnya menjadi
gula-gula sederhana seperti glukosa. Hidrolisis selulosa dapat dilakukan menggunakan
larutan asam atau secara enzimatis [ ].
Hidrolisis yang paling sering digunakan untuk menghidrolisis selulosa adalah
hidrolisis secara asam. Beberapa asam yang umum digunakan untuk hidrolisis asam
antara lain adalah asam sulfat (H2SO4), asam perklorat dan HCl. Keuntungan dari
penggunaan asam ini mengandung konversi gula hingga mencapai konversi 90% [ ].
Dalam hidrolisis menggunakan bahan kimia, perlakuan awal dan hidrolisis dapat dilakukan dalam satu langkah. Ada dua jenis dasar dari proses hidrolisis asam yang umum digunakan, yakni asam encer dan asam pekat. Keuntungan terbesar dari asam encer proses reaksi berlangsung cepat. Asam pekat menggunakan suhu relatif rendah sehingga memerlukan tekanan yang memompa bahan dari suatu bejana ke bejana lain. Hidrolisis asam pekat biasanya membutuhkan waktu lebih lama daripada menggunakan asam encer [ ].
Proses sakarifikasi menggunakan asam bersifat tidak spesifik. Selain glukosa,
sakarifikasi dengan asam dapat menghasilkan produk samping seperti senyawa furan,
fenolik, dan asam asetat [ ]. Produk samping tersebut apabila tidak dihilangkan dapat
menghambat proses selanjutnya, yakni fermentasi. Sakarifikasi menggunakan asam juga
13
Hidrolisis bahan lignoselulosik dapat dilakukan dengan asam atau enzim. Perlakuan awal terhadap substrat lignoselulosik diperlukan agar substrat mudah bereaksi dengan asam atau enzim. Perlakuan awal yang efisien harus dapat membebaskan struktur kristal selulosa dengan memperluas daerah amorf serta membebaskan dari lapisan lignin [ ].
Pada penelitian yang telah dilakukan adalah hidrolisat kulit buah kakao (Theobroma cacao L.)yang menggunakan asam sulfat saat proses hidrolisisnya.
Tahap berikutnya adalah fermentasi proses, yang melibatkan menambahkan ragi untuk mengkonversi gula untuk etanol dan karbon dioksida [ ].
Fermentasi adalah proses produksi energi dalam sel dalam keadaan anaerobik (tanpa oksigen). Secara umum, fermentasi adalah salah satu bentuk respirasi anaerobik, akan tetapi, terdapat definisi yang lebih jelas yang mendefinisikan fermentasi sebagai respirasi dalam lingkungan anaerobik dengan tanpa akseptor elektron eksternal [ ].
Tahap fermentasi merupakan tahap kedua dalam proses produksi bioetanol. Pada tahap ini terjadi pemecahan gula-gula sederhana menjadi etanol dengan melibatkan enzim dan ragi. Fermentasi dilakukan pada kisaran suhu 27–32 oC. Pada tahap ini akan dihasilkan gas CO2 dengan perbandingan stokiometri yang sama dengan etanol yang
dihasilkan yaitu 1:1[ ].
Pada penelitian yang telah dilakukan adalah fermentasi hidrolisat kulit kakao menggunakan ragi roti yang mengandung Saccharomyces cereviceae. Reaksi selengkapnya dari fermentasi glukosa menggunakan ragi sebagai berikut:
Glikolisis: Glukosa (+ 2 ADP + 2 NAD+) → 2 Piruvat + 2 ATP + 2 NADH Fermentasi:
2 Piruvat → 2 Asetaldehid + 2 CO2
2 Asetaldehid + 2 NADH → 2 Etanol + 2 NAD
Reaksi fermentasi glukosa selengkapnya yang menggunakan ragi tidak melibatkan pertumbuhan sel
Glukosa (+ 2 ADP) → 2 Etanol + 2 CO2 + 2 ATP
C6H12O6 (+ 2 ADP) → 2 C2H5OH + 2 CO2 + 2 ATP
14
15
Variabel yang berpengaruh pada proses fermentasi adalah bahan baku, suhu, pH, konsentrasi ragi, lama fermentasi, kadar gula,dan nutrisi ragi [ ].
1) Bahan baku
Etanol merupakan bahan bakar berbasis alkohol yang dihasilkan dari fermentasi tanaman gula, yang berasal dari produk pertanian dan limbah makanan, yang mengandung gula, pati, atau selulosa, yang kemudian dapat difermentasi dan didistilasi menjadi etanol [ ]. Bahan baku yang digunakan pada penelitian ini adalah hidrolisat kulit buah kakao (Theobroma cacao L.).
2) Suhu
Suhu fermentasi mempengaruhi lama fermentasi karena pertumbuhan mikroba dipengaruhi suhu lingkungan fermentasi. Mikroba memiliki kriteria pertumbuhan yang berbeda-beda. Saccharomyces cerevisiae memliki kisaran suhu pertumbuhan antara 20-30 °C. Jika suhu terlalu rendah, maka fermentasi akan berlangsung secara lambat dan sebaliknya jika suhu terlalu tinggi maka Saccharomyces Cerevisiae akan mati sehingga proses fermentasi tidak akan berlangsung[ ].
Ragi tape dan ragi roti mempunyai temperatur maksimal sekitar 40–50 oC dengan
temperatur minimum 0 oC. Pada interval 15–30 oC fermentasi mengikuti pola bahwa semakin tinggi suhu, fermentasi makin cepat berlangsung. Suhu optimum untuk ragi roti adalah 19–32 oC dan suhu optimum untuk ragi tape adalah 35–47 oC. Oleh karena itu, pengaturan suhu dibuat dalam range tersebut [ ]. Pada penelitian yang akan dilakukan menggunakan temperatur ruangan.
3) pH
Secara umum khamir dapat tumbuh dan memproduksi etanol secara efisien pada pH 3,5-6,0 dan suhu 28-35 oC [ ]. Pada umumnya pH untuk fermentasi dibutuhkan keasaman 3,4–4, ini didasari lingkungan hidup dari starter yang dapat tumbuh dan melakukan metabolisme pada pH tersebut [ ] .
4) konsentrasi ragi
16
sedikitnya massa yang akan menguraikan glukosa menjadi etanol maka akan dibutuhkan substrat yang lebih banyak karena substrat yang ada tidak cukup [ ]. Konsentrasi ragi yang digunakana adalah 3%; 5%; dan 7% (w/v).
5) Lama fermentasi
Lama fermentasi biasanya ditentukan pada jenis bahan dan jenis ragi serta gula. Fermentasi berhenti ditandai dengan tidak terproduksinya lagi CO2. Kadar etanol yang dihasilkan akan semakin tinggi sampai waktu optimal dan setelah itu kadar etanol yang dihasilkan menurun[ ]. Pada penelitian ini fermentasi akan dilakukan selama 2, 3, 4, dan 5 hari.
6) Kadar gula
Kadar gula yang optimum untuk aktivitas pertumbuhan starter adalah 10 – 18%. Gula disini sebagai substrat, yaitu sumber karbon bagi nutrient Saccharomyces cereviceae yang mempercepat pertumbuhan untuk selanjutnya menguraikan karbohidrat menjadi etanol. Jika kadar gula di bawah 10% fermentasi dapat berjalan tetapi etanol yang dihasilkan terlalu encer sehingga tidak efisien untuk didestilasi dan biayanya mahal. Jika kadar gula di atas 18% fermentasi akan menurun dan alkohol yang terbentuk akan menghambat aktivitas ragi, sehingga waktu fermentasi bertambah lama dan ada sebagian gula yang tidak terfermentasi [ ].
7) Nutrisi ragi
Nutrisi diperlukan sebagai tambahan makanan bagi pertumbuhan ragi. Nutrisi yang diperlukan misalnya: garam ammonium (NH4Cl) dan garam fosfat [ ].
Produk baku didistilasi setelah dilakukan fermentasi. Penyulingan memisahkan cairan etanol dari residu yang mengendap ke bawah setelah fermentasi [ ].
Distilasi adalah suatu proses penguapan dan pengembunan kembali, yaitu untuk memisahkan campuran dua atau lebih zat cair ke dalam fraksi-fraksinya berdasarkan perbedaan titik didihnya. Pada pemisahan hasil fermentasi glukosa menggunakan sistem uap-cairan, dan terdiri dari komponen-komponen tertentu yang mudah tercampur[ ].
17
tekanan uap murni atau titik didih masing-masing komponen yang terdapat dalam campuran [ ].
Pada umumnya hasil fermentasi berupa bioetanol atau alkohol yang mempunyai kemurnian sekitar 30–40% belum dapat diketegorikan sebagai fuel based ethanol. Untuk memurnikan bioetanol menjadi berkadar lebih dari 95% agar dapat dipergunakan sebagai bahan bakar, harus melewati proses distilasi untuk memisahkan alkohol dengan air dengan memperhitungkan perbedaan titik didih kedua bahan tersebut yang kemudian diembunkan kembali untuk memperoleh bioetanol dengan kemurnian hingga 99,5-99,8% [ ].
2.6 SACCHAROMYCES CEREVISIAE
Saccharomyces cerevisiae termasuk ke dalam kelas Ascomycetes yang dicirikan dengan pembentukan askus yang merupakan tempat pembentukan askospora. S. serevisiae memperbanyak diri secara aseksual yaitu dengan bertunas. Dinding sel S. cerevisiae terdiri dari komponen-komonen glukan, manan, protein, kitin dan lemak [ ]. Saccharomyces cerevisiae memiliki beberapa kelebihan dibandingkan dengan mikroorganisme lain yang dapat memproduksi bioetanol. Kelebihan tersebut antara lain lebih mudah beradaptasi dengan lingkungan, lebih tahan terhadap kadar alkohol tinggi, dan lebih mudah didapat [ ], kemampuannya untuk menghasilkan etanol secara anaerobik pada pH rendah dan kondisi lingkungan yang osmolaritasnya tinggi dengan produktivitas yield yang banyak [ ], sangat tahan dan toleran terhadap kadar etanol yang tinggi (12-18% v/v), tahan pada kadar gula yang cukup tinggi dan tetap aktif melakukan fermentasi pada suhu 4-32 oC [ ].
Pemilihan sel khamir didasarkan pada jenis karbohidrat yang digunakan, sebagai medium untuk memproduksi alkohol dari pati dan gula digunakan Saccharomyces cerevisiae. Suhu yang baik untuk proses fermentasi berkisar antara 25-30 °C. Derajat
18
Saccharomyces cerevisiae adalah salah satu spesies khamir yang memiliki daya konversi gula menjadi etanol sangat tinggi. Mikroba ini biasanya dikenal dengan baker’s yeast dan metabolismenya telah dipelajari dengan baik. Produk metabolit utama adalah etanol, CO2, dan air, sedangkan beberapa produk lain dihasilkan dalam jumlah sedikit.
Khamir ini bersifat fakultatif anaerobik. Saccharomyces cerevisiae memerlukan suhu 30
oC dan pH 4,0 -4,5 agar dapat tumbuh dengan baik. Selama proses fermentasi akan
timbul panas. Bila tidak dilakukan pendinginan, suhu akan terus meningkat sehubungan proses fermentasi terhambat [ ].
S. cerevisiae mempunyai aktivitas optimum pada suhu 30–35 oC dan tidak aktif pada suhu lebih dari 40 oC. S. cerevisiae dapat memfermentasi glukosa, sukrosa, galaktosa serta rafinosa. Biakan S. cerevisiae mempunyai kecepatan fermentasi optimum pada pH 4,48 [ ].
Jenis ragi yang digunakan dalam penelitian ini adalah ragi roti yang biasa dikenal dengan nama fermipan.
Ragi roti merupakan khamir jenis Saccharomyces cerevisiae yang telah diseleksi sebelumnya untuk tujuan komersil. Ragi roti merupakan khamir jenis Saccharomyces cerevisiae tipe tertentu yang umumnya cepat tumbuh di dalam adonan roti. Di dalam
kondisi anaerob ragi roti tetap menghasilkan gas CO2, meskipun tidak secepat dalam
kondisi aerob [ ].
Ragi roti dibuat dari molasses, nitrogen, urea, kecambah malt, garam organik, faktor pertumbuhan dalam bentuk ekstrak sayur, serelia, khamir, dan sejumlah kecil vitamin. Semakin banyak ragi yang ditambahkan maka kadar etanol yang dihasilkan juga semakin besar karena dengan semakin banyak ragi yang ditambahkan, maka bakteri yang mengurai glukosa menjadi etanol pun semakin banyak [ ]. Sehingga pada penelitian yang telah dilakukan diberi variasi kadar fermipan terhadap waktu fermentasi.
2.7 TANIN
19
kandungan tanin sebesar 30-40% [ ] . Gambir mengandung berbagai senyawa fungsional, antara lain zat samak (22%), kuersetin (2-4%), fluoreisin gambir (1-3%), pyrocathecol (20-30%), lendir, lemak, lilin (1-2%), dan polifenol [ ] .
Tanin memiliki sifat umum, yaitu memiliki gugus phenol dan bersifat koloid. Karena itu di dalam air bersifat koloid dan asam lemah. Semua jenis tanin dapat larut dalam air. Kelarutannya besar, dan akan bertambah besar apabila dilarutkan dalam air panas. Tanin akan terurai menjadi pyrogallol, pyrocatechol dan phloroglucinol bila dipanaskan sampai suhu 210 °F-215 °F (98,89 °C-101,67 °C). Tanin dapat dihidrolisa oleh asam, basa dan enzim. Ikatan kimia yang terjadi antara tanin protein atau polimer-polimer lainnya terdiri dari ikatan hidrogen, ikatan ionik dan ikatan kovalen [ ].
[image:49.612.238.397.301.499.2]
Gambar 2.5 Tanin [ ]
Selanjutnya hasil penelitian terdahulu yang dilakukan oleh Putu Kristiani K, dkk.,
(2013) menggunakan bahan baku pulp kakao dan Saccharomyces cereviseae dan ada
tambahan kulit bakau sebagai sumber tanin sebagai penghambat pembentukan asam asetat dari proses fermentasi lebih lanjut. Tanin merupakan senyawa yang dapat larut dalam air, gliserol, alkohol, dan hidroalkohol, tetapi tidak larut dalam petroleum eter, benzene dan eter. terdekomposisi pada suhu 210 oC, titik nyala 210 oC, dan terbakar pada suhu 526 oC [ ].
HO
R2
R3
OH R1
O
20
Dalam penelitian yang telah dilakukan menggunakan tanin dari gambir sebanyak 4 gram di setiap run fermentasi sebagai penghambat terbentuknya asam asetat sehingga dapat meningkatkan kadar etanol yang terbentuk.
2.8 ANALISIS EKONOMI
[image:50.612.115.540.259.392.2]Dalam penelitian ini, maka dilakukan suatu analisis ekonomi sederhana terhadap pembuatan bioetanol dari hidrolisat limbah kulit buah kakao dengan cara konvensional. Adapun rincian biaya terdapat dalam tabel 2.4
Tabel 2.4 Rincian Biaya Pembuatan Bioetanol dari Hidrolisat Limbah Kulit Buah Kakao Bahan dan Peralatan Jumlah Harga (Rp) Biaya Total (Rp)
Kulit buah kakao 1 kg 0,-/1 kg 0,-
Asam sulfat 264 ml 500,-/ml 132.000,-
Fermipan 211,6314 gr 13.500,-/11 g 259.671,- Gambir 48 gr 20000/ kg 960,-
Total biaya 392.631,-
Dari rincian biaya di atas yang telah dilakukan maka total biaya yang diperlukan untuk pembuatan bioetanol per kilogram limbah kulit buah kakao adalah sebesar Rp. 392.631-. Walaupun biaya yang dikeluarkan cukup besar, tetapi penelitian ini mengindikasikan bahwa bioetanol dapat diperoleh dari limbah kulit kakao melalui proses fermentasi dengan kadar yang cukup bagus.
2.9 ANALISIS POTENSI ENERGI
21
Semakin meningkatnya produksi kakao baik karena pertambahan luas areal pertanaman maupun yang disebabkan oleh peningkatan produksi per satuan luas, akan meningkatkan jumlah limbah buah kakao. Pod kakao merupakan limbah perkebunan kakao yang sangat potensial dan mempunyai nilai produktif yang bisa dikembangkan. Pod kakao merupakan limbah lignoselulosik lignin, selulosa, dan hemiselulosa [ ]. Selulosa dan hemiselulosa dapat dikonversi menjadi etanol, sedangkan lignin sudah terlignifikasi saat proses hidrolisis berlangsung. Karena memiliki potensi yang cukup besar, limbah kulit buah kakao diharapkan dapat menjadi sumber alternatif bahan baku untuk pembuatan bioetanol guna mencukupi kebutuhan bahan bakar dalam negeri yang semakin tinggi.
Dalam hal prestasi mesin, bioetanol dan gasohol (kombinasi bioetanol dan bensin) tidak kalah dengan bensin; bahkan dalam beberapa hal, bioetanol dan gasohol lebih baik dari bensin. Pada dasarnya pembakaran bioetanol tidak menciptakan CO2 neto
ke lingkungan karena zat yang sama akan diperlukan untuk pertumbuhan tanaman sebagai bahan baku bioetanol [50]. Adapun peluang untuk mengembangkan potensi bioetanol sendiri di Indonesia cukup besar terutama untuk bahan baku farmasi maupun bahan campuran bensin untuk menghasilkan pembakaran mesin yang sempurna. Salah satu cara yang paling efektif untuk membandingkan perbedaan sumber-sumber energi dan mengukur profabilitas dari masing- masing sumber-sumber energi disebut energi profit rasio (EPR), yaitu rasio dari energi output terhadap energi [51], seperti rumus dibawah ini
��� =� ���� � ���� � [51]
22
[image:52.612.108.545.148.235.2]yang dipakai pada proses pembuatan bioetanol. Pada perhitungan analisis potensi energi menggunakan basis memproduksi 1 kg bioetanol.
Tabel 2.5 Kebututhan Listrik Proses Pembuatan Bioetanol
Nama Alat Daya (watt) Waktu pemakaian
(jam)
Pemakaian listrik (kwh/kg bioetanol)
Rotary evaporator 1.000 1 1
Hot Plate 350 2 0,75
Oven 400 1 0,4
Jumlah* 2,15
[image:52.612.119.538.337.509.2]Untuk menghitung EPR diperlukan jumlah energi output dan juga jumlah energi input seperti yang dapat dilihat pada Tabel 2.6 dan Tabel 2.7 Berikut:
Tabel 2.6 Total Energi Input [52], [53], [54], [55] Bahan Masukan Kandungan Energi
Bahan (kal/ gram)
Total Energi (kkal/kg bioetanol)
Hidrolisat Kulit Buah Kakao 3900 300
NaOH 7911,089 47,466
Asam Sulfat 2222 26,664
Gambir 5622 1686,6
Fermipan 3650 17,844
Air 10 60
Jumlah energi bahan baku 2138,574
Kebutuhan Energi Listrik Peralatan*
860 kkal/kwh 3719,5
Total 5858,074
Tabel 2.7 Jumlah Energi Output [38]
Produk Kandungan Energi
Bahan (kal/gram)
Total Energi (kkal/ kg bioetanol)
Etanol 5612,87 4613,317
Total 4613,317
23
��� =� ���� � ���� � = ,, = ,
Dari perhitungan didapatkan nilai produktivitas sebesar 0,787, dimana nilai produktivitas lebih kecil dari 1 (satu). Dapat disimpulkan bahwa pembuatan bioetanol dari hidrolisat kulit kakao menggunakan fermipan membutuhkan energi input yag lebih besar dari energi output yang dihasilkan. Hal ini disebabkan tahapan pembuatan bioetanol yang cukup panjang dimana dibutuhkan energi yang besar pada tahapan fermentasinya. Oleh karena itu perlunya dicari metode alternatif untuk memproses hidrolisat kulit buah kakao menjadi bioetanol dengan energi input yang rendah sehingga didapatkan nilai produktivitas > 1. Hasil ini belum bernilai secara ekonomi tetapi bisa dijadikan scientific study untuk penelitian selanjutnya dan pemilihan alterantif proses yang lain.
Semakin tinggi harga EPR untuk untuk sebuah bahan bakar, semakin tinggi jumlah energi bersih dan semakin berharga bahan bakar tersebut karena energi tersebut dapat digunakan untuk penggunaan yang lain. Minyak konvensional, batubara, dan gas alam memiliki harga EPR yang tinggi dibandingkan sumber energi yang lain sehingga menjadikan mereka sangat bernilai [56].
1
BAB I
PENDAHULUAN
1.1LATAR BELAKANG
Krisis energi yang terjadi akhir-akhir ini mendorong pemerintah menggalakkan sumber enegi terbarukan dari komoditas perkebunan atau dikenal dengan bahan bakar nabati (BBN). Beberapa komoditas perkebunan yang potensial sebagai sumber bahan bakar nabati (BBN) / biofuel adalah kelapa sawit, kelapa, jarak pagar, dan jarak kepyar [ ] . Namun apabila dipahami lebih jauh, dengan menggunakan bahan baku tersebut akan mengakibatkan alih fungsi dan berkurangnya bahan pangan. Kakao merupakan salah satu komoditas unggulan sub sektor perkebunan dari 15 komoditas yang dicanangkan untuk dikembangkan secara besar-besaran di Indonesia [ ].
Komponen limbah buah kakao yang terbesar berasal dari kulit buahnya atau bisa disebut pod kakao yaitu sebesar 75% dari total buah. Pod kakao merupakan limbah lignoselulosik yang mengandung lignin, selulosa, dan hemiselulosa. Kandungan selulosa dan hemiselulosa pada pod kakao ini yang berpotensi untuk diolah lebih lanjut menjadi etanol [ ].
Penggunaan bioetanol sebagai bahan bakar meningkat karena cadangan minyak bumi yang makin menipis, harga minyak bumi yang cenderung meningkat, berlakunya peraturan reduksi emisi gas rumah kaca, dan kebijakan penghapusan methyl tertiarybuthyl ether (MTBE), serta adanya kecenderungan beralihnya konsumsi pada sumber energi ramah lingkungan dan terbarukan [ ].
2
Tabel 1.1 Penelitian Terdahulu Mengenai Pembuatan Bioetanol dari Kulit Kakao (Theobroma Cacao L.)
Tahun Peneliti Keterangan 2013 Putu Kristiani
K, La Ode Sabarudin, Rima Melati, Haeruddin
[ ]
Bahan baku: Filtrat cairan pulp kakao sebanyak 500 ml Metode:
- Fermentasi anaerob selama 14 hari setiap 24 jam sekali waktu fermentasi.
- penambahan 7,5 gram serbuk kulit bakau
- suhu fermentasi diatur agar tetap memenuhi persyaratan optimal pertumbuhan dari Saccharomyces cerevisiae
Optimum:
- kadar alkohol tertinggi adalah 12 hari fermentasi dengan kadar alkohol 4,85%
2009 Agustinus Eka P dan Amran Halim
[ ]
Bahan baku: Nira siwalan sebanyak 200 ml Met