RENI RAHMALIA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Kajian Mikroenkapsulasi Ekstrak Vanili dan Retensi Vanilin Selama Penyimpanan” adalah karya saya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2008
ABSTRACT
RENI RAHMALIA. Study on Microencapsulation of Vanilla Extract and
Vanillin Retention During Storage. Under supervision of SUGIYONO and DWI
SETYANINGSIH.
The objectives of this research were to observe the effects of microencapsulation process on the flavour physicochemical characteristics, and to observe the vanillin retention during storage.
The research was conducted in four steps. The first step of this research: material preparation including ‘curing’ to produce the half dried vanilla which would be processed further in extraction step. The second step: choosing the suitable coating material for vanilla extract microencapsulation. The content of vanillin in the vanilla powder, vanilla powder solubility and aw (water activity)
were observed. Based on these parameters, the two best coating materials were chosen for microencapsulation in the third step. The third step: formulations of vanilla extract microencapsulation. The effect of coating materials which were obtained from the previous step, concentration of coating material (10%, 20%, 30%) and ratio between vanilla extract and coating material (3:2, 2:1, 3:1), were evaluated. The following parameters were measured: vanilla powder solubility, aw
(water activity), content of vanillin in the vanilla powder, yield and vanillin recovery. The forth step: observing vanillin retention during storage. The vanilla powder was stored at 4°C, 30°C and 55°C for 6 weeks. The decrease of vanillin retention rate during storage was measured using Arrhenius, Avrami equation and half life.
The results showed that the two best coating materials from the second step were maltodextrin and a mixture of maltodextrin-modified cassava starch Flomax 8 (2:1). Coating material, coating concentration and ratio between vanilla extract and coating material gave a significant difference to the yield, vanillin content and vanillin recovery. The low ratio of vanilla extract and coating material gave a high vanillin recovery of vanilla powder (the 3:2 ratio gave a higher recovery than those of the 2:1 and 3:1 ratios). The vanilla powder coated by maltodextrin and modified cassava starch Flomax 8 (2:1) had a higher yield, vanillin content and vanillin recovery compared to vanilla powder coated by only maltodextrin. The highest coating concentration (30%) gave the highest vanillin content of vanilla powder, and the higher ratio between extract and coating material, the higher vanillin content. The type of coating material gave a significant effect to the solubility of vanilla powder. Vanilla powder coated with maltodextrin had a higher solubility than that of vanilla powder coated with a mixture of maltodextrin and modified cassava starch Flomax 8 (2:1). The concentration of coating material and ratio between extract vanilla and coating material did not effect the solubility. The type of coating materials, coating material concentration and ratio between vanilla extract and coating material did not effect water activity of the obtained vanilla powder.
powder B (a mixture of maltodextrin-modified cassava starch Flomax 8 as coating material) during storage was higher than that of vanilla powder A (maltodekstrin as coating material). According to Avrami equation, the decrease of vanillin retention was the highest at 55°C, followed 30°C and 4°C. The vanilla powder A stored at 4°C, 30°C and 55°C had half lives of 11.47, 7.65 and 6.52 weeks respectively. The vanilla powder B stored at 4°C, 30°C and 55°C had half lives of 11.87, 10.93 and 6.88 weeks respectively.
RINGKASAN
RENI RAHMALIA. Kajian Mikroenkapsulasi Ekstrak Vanili Dan Retensi Vanilin Selama Penyimpanan. Dibimbing oleh SUGIYONO dan DWI SETYANINGSIH.
Vanili merupakan salah satu flavoring agent yang penggunaannya cukup luas di industri pangan, farmasi dan kosmetik. Vanili alami memiliki lebih dari 250 komponen organik yang memberikan flavor dan aroma yang khas. Vanili dapat diolah menjadi bubuk vanili dengan cara mikroenkapsulasi. Mikroenkapsulasi flavor dilakukan untuk memproduksi bubuk flavor sehingga dapat mencegah kehilangan flavor, memperpanjang umur simpan dan membuat flavor mudah digunakan. Mikroenkapsulasi ekstrak vanili diharapkan dapat menahan komponen volatil vanili dalam waktu lama.
Tujuan penelitian ini yaitu Mempelajari pengaruh proses mikroenkapsulasi ekstrak vanili dan sifat fisiokimia mikrokapsul (bubuk vanili) yang dihasilkan serta mempelajari pola retensi vanilin bubuk vanili selama penyimpanan.
Penelitian ini dilakukan dalam empat tahap. Tahap pertama penelitian yaitu persiapan bahan meliputi proses curing untuk mendapatkan vanili ½ kering yang selanjutnya dilanjutkan proses ekstraksi vanili. Tahap kedua penelitian yaitu pemilihan bahan penyalut untuk mendapatkan bahan penyalut yang tepat untuk mikroenkapsulasi ekstrak vanili. Parameter yang diamati pada tahap ini adalah kadar vanilin pada bubuk, kelarutan bubuk vanili dan aw (water activity). Dari
tahap ini dipilih 2 perlakuan bahan penyalut yang memberikan hasil terbaik dari parameter yang diamati. Tahap ketiga penelitian yaitu formulasi mikroenkapsulasi ekstrak vanili. Faktor yang diuji adalah jenis penyalut, konsentrasi penyalut dan rasio ekstrak vanili dengan penyalut. Penyalut yang digunakan adalah dua penyalut terbaik dari penelitian pemilihan penyalut. Penyalut dibuat dengan konsentrasi 10%, 20% dan 30%. Ekstrak vanili dengan penyalut dibuat dengan rasio 3 : 2, 2 : 1 dan 3 : 1. Parameter yang diamati kelarutan bubuk vanili, aw
(water activity), rendemen dan recovery vanilin bubuk vanili. Tahap keempat penelitian yaitu retensi vanilin selama penyimpanan. Pada tahap keempat ini dipilih dua perlakuan untuk mengetahui retensi vanilin selama penyimpanan. Penyimpanan dilakukan pada suhu 4oC, 30oC dan 55oC selama tujuh minggu. Pengukuran laju penurunan retensi vanilin selama penyimpanan menggunakan persamaan Arrhenius, persamaan Arami dan waktu paruh. Parameter aw diamati
pada minggu ke-0 dan minggu ke-4.
Bubuk vanili dengan penyalut campuran maltodekstrin dan pati tapioka termodifikasi Flomax 8 (2 : 1) menghasilkan rendemen, kadar vanilin dan recovery vanilin lebih tinggi dibanding bubuk vanili dengan penyalut maltodekstrin saja. Kadar vanilin bubuk vanili tertinggi pada konsentrasi paling besar(30%), semakin besar rasio ekstrak terhadap penyalut, kadar vanili semakin besar. Jenis penyalut berpengaruh nyata terhadap kelarutan bubuk vanili. Bubuk vanili dengan penyalut maltodekstrin memiliki kelarutan lebih tinggi dibanding dengan bubuk vanili dengan penyalut campuran maltodekstrin dan pati tapioka termodifikasi Flomax 8 (2 : 1). Konsentrasi penyalut dan rasio ekstrak vanili terhadap penyalut tidak berpengaruh nyata terhadap kelarutan. Jenis penyalut, konsentrasi penyalut dan rasio eksrak vanili dengan penyalut tidak berpengaruh terhadap aw bubuk vanili yang dihasilkan.
Pola retensi vanilin pada bubuk vanili selama penyimpanan memperlihatkan kecenderungan menurun dengan semakin lama penyimpanan. Suhu dan lama penyimpanan berpengaruh nyata terhadap retensi vanilin selama penyimpanan bubuk vanili. Suhu dan lama penyimpanan berpengaruh nyata terhadap aw bubuk vanili. Berdasarkan persamaan Avrami, penurunan retensi
vanilin paling besar terjadi pada suhu 55oC, diikuti oleh suhu 30oC dan 4oC. Berdasarkan uji akselerasi menggunakan persamaan Arrhenius, retensi vanilin bubuk vaniliB (campuran maltodekstrin dan pati tapioka termodifikasi Flomax 8 sebagai penyalut) selama penyimpanan lebih tinggi dibanding retensi vanilin bubuk vaniliA (maltodekstrin sebagai penyalut). Bubuk vanili A yang disimpan pada suhu 4°C, 30°C dan 55°C memiliki waktu paruh 11.47, 7.65 dan 6.52 minggu. Bubuk vanili B yang disimpan pada suhu 4°C, 30°C dan 55°C memiliki waktu paruh 11.87, 10.93 dan 6.88 minggu.
.
@ Hak Cipta milik IPB, tahun 2008
Hak Cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
KAJIAN MIKROENKAPSULASI EKSTRAK VANILI
DAN RETENSI VANILIN SELAMA PENYIMPANAN
RENI RAHMALIA
Tesis
sebagai salah satu syarat untuk memperoleh gelar
Magister Sains pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PRAKATA
Syukur alhamdulillah penulis panjatkan ke hadhirat Allah SWT atas segala rahmat dan karunia-Nya sehingga karya ini berhasil diselesaikan. Penelitian Kajian Mikroenkapsulasi Ekstrak Vanili dan Retensi Vanilin Selama Penyimpanan dilaksanakan atas dana dari Riset Unggulan Terpadu Kementerian Negara Riset dan Teknologi. Penelitian ini berlangsung dari bulan April 2006 sampai dengan September 2007 di Laboratorium Departemen Ilmu dan Teknologi Pangan Institut Pertanian Bogor dan SEAFAST Center.
Terima kasih dan penghargaan sebesar-besarnya penulis sampaikan kepada Bapak Dr. Ir. Sugiyono, M.App.Sc dan Ibu Dr. Ir. Dwi Setyaningsih, MSiselaku dosen pembimbing yang telah banyak memberikan bimbingan dan arahan. Terima kasih kepada Bapak Dr. Ir. Nugraha Edhi Suyatma atas kesediaannya sebagai penguji luar komisi. Terima kasih kepada rekan-rekan IPN angkatan 2004: Mira, Iin, Marleni, Agnani, Neni, Sandi, Reno, Dorkas, Santi, dan rekan-rekan yang tidak bisa disebutkan satu per satu, serta adikku Ganes terima kasih telah banyak membantu serta memberi motivasi kepada penulis. Terima kasih kepada Bapak dan Ibu Teknisi di laboratorium Departemen Ilmu dan Teknologi Pangan Institut Pertanian Bogor dan SEAFAST Center atas segala bantuan dan kerjasamanya.
Ungkapan terima kasih yang tidak terhingga penulis persembahkan kepada orang-orang tercinta, yang selalu men-support penulis dengan doa : Ibunda, Ayahanda, kakak dan adik terima kasih atas dukungan dan kasih sayangnya. Kepada suamiku, terima kasih atas segala motivasi, keikhlasan, dan do’a, terima kasih atas cintanya. Kepada Soleh Kecil Rafan, terima kasih selalu menceriakan hari-hari ibu, semoga menjadi anak soleh dan berbakti.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juni 2008
RIWAYAT HIDUP
Penulis dilahirkan di Sumedang pada tanggal 13 Februari 1977 dari Bapak U.R. Munawar dan Ibu Salamah. Penulis adalah putri kedua dari 4 bersaudara.
Pendidikan SD sampai SMA ditempuh penulis di Sumedang sejak tahun 1983 sampai dengan 1995. Penulis diterima sebagai mahasiswa pada Jurusan Teknologi Pangan dan Gizi, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur PMDK pada tahun 1995. Gelar sarjana diperoleh penulis pada tahun 1999, dengan skripsi berjudul “Mempelajari Kadar Timbal Pada Daun Teh dan Seduhannya dari Lokasi yang Dilalui Jalan Raya”.
DAFTAR ISI III. Formulasi mikroenkapsulasi ekstrak vanili ... IV. Retensi vanilin selama penyimpanan... II. Pengaruh jenis penyalut terhadap aw, kadar vanili dan kelarutan
produk bubuk vanili...
Nilai aw...
Kadar vanilin.... Kelarutan ... III. Pengaruh jenis penyalut, konsentrasi penyalut dan rasio ekstrak
vanili dengan penyalut terhadap rendemen, aw, kelarutan dan retensi vanilin selama pengeringan produk bubuk vanili
Rendemen... Nilai aw...
Kelarutan... Kadar vanilin... Recovery vanilin... IV. Retensi vanilin selama penyimpanan... Laju penurunan retensi vanilin berdasarkan persamaan Arrhenius.... Laju penurunan retensi vanilin berdasarkan persamaan Avrami... Waktu paruh bubuk vanili...
SIMPULAN DAN SARAN...
Simpulan ... Saran ...
DAFTAR PUSTAKA ...
LAMPIRAN ... 35 36 36 38 40 42 45 47 49
59
59 60
61
DAFTAR TABEL
Halaman
1 Komponen utama vanili cured... 6
2 Aplikasi metode enkapsulasi dalam industri pangan ... 13
3 Karakteristik bahan penyalut untuk enkapsulasi flavor ... 16
4 Karakteristik pati tapioka termodifikasi Flomax 8... 27
5 Aw, kelarutan dan kadar vanilin bubuk vanili ... 29
6 Parameter persamaan Arrhenius bubuk vanili A dan B ... 41
7 Nilai Ea dan jenis reaksi yang terjadi... 47
8 Hasil perhitungan persamaan Avrami... 48
DAFTAR GAMBAR Aw bubuk vanili dari tiap perlakuan...
Kelarutan bubuk vanili dari tiap perlakuan... Kadar vanilin bubuk vanili dari tiap perlakuan... Retensi vanilin (%) selama pengeringan dari tiap perlakuan... Pola retensi vanilin bubuk vaniliA... Pola retensi vanilin bubuk vaniliB... Hubungan ln k dengan waktu penyimpanan bubuk vanili A... Hubungan ln k dengan waktu penyimpanan bubuk vanili B... Bubuk vanili A setelah penyimpanan minggu ke-4... Bubuk vanili B setelah penyimpanan minggu ke-4... Nilai aw bubuk vanili A dan B pada minggu ke-0 dan minggu ke-4...
DAFTAR LAMPIRAN
Halaman
1 Gambarproses kuring vanili½ kering modifikasi... 68
2 Gambar proses ekstraksi vanili ... 69
12 Uji beda Duncan jenis penyalut terhadap rendemen... 73
13 Uji beda Duncan konsentrasi terhadap rendemen... 73
14 Uji beda Duncan rasio terhadap rendemen ... 73
21 Uji beda Duncan konsentrasi terhadap kelarutan... 76
22 Uji beda Duncan rasio terhadap kelarutan ... 76
23 Sidik ragam kadar vanilin penelitian tahap III... 76
24 Uji beda Duncan jenis penyalut terhadap kadar vanilin... 77
25 Uji beda Duncan konsentrasi terhadap kadar vanilin... 77
26 Uji beda Duncan rasio terhadap kadar vanilin ... 77
27 Sidik ragam recovery vanilin ... 77
28 Uji beda Duncan jenis penyalut terhadap recovery vanilin ... 78
29 Uji beda Duncan konsentrasi terhadap recovery vanilin... 78
30 Uji beda Duncan rasio terhadap recovery vanilin ... 78
31 Sidik ragam retensi vanilin bubuk vanili A selama penyimpanan... 79
32 Uji beda Duncan suhu penyimpanan terhadap retensi vanilin bubuk vanili A selama penyimpanan ... 79
33 Uji beda Duncan lama penyimpanan terhadap retensi vanilin bubuk vanili A selama penyimpanan ... 79
34 Sidik ragam retensi vanilin bubuk vanili B selama penyimpanan ... 79
35 Uji beda Duncan suhu penyimpanan terhadap retensi vanilin bubuk vanili B selama penyimpanan ... 80
36 Uji beda Duncan lama penyimpanan terhadap retensi vanilin bubuk vanili B selama penyimpanan ... 80
37 Sidik ragam aw bubuk vanili A selama penyimpanan ... 80
bubuk vanili A selama penyimpanan ... 81 40 Sidik ragam aw bubuk vanili A selama penyimpanan ... 81
41 Uji beda Duncan pengaruh lama penyimpanan terhadap aw
bubuk vanili A selama penyimpanan ... 81 42 Uji beda Duncan pengaruh suhu penyimpanan terhadap aw
PENDAHULUAN
Latar Belakang
Vanili merupakan salah satu flavoring agent yang penggunaannya cukup luas di industri pangan, farmasi dan kosmetik. Vanili yang biasa digunakan dan dikenal masyarakat kita adalah vanili sintetik. Bahan makanan yang mengandung flavor sintetik sering dihindari, karena dugaan konsumen terhadap flavor sintetik mengandung senyawa toksik dan berbahaya bagi kesehatan (Teixeira et al. 2004). Vanili alami memiliki lebih dari 250 komponen organik, semua komponen tersebut memberikan flavor dan aroma yang khas yang berbeda dengan vanili sintetik.
Indonesia merupakan salah satu penghasil utama vanili di dunia. Negara lain penghasil vanili adalah Madagaskar, Meksiko, Guatemala, Costa Rica, Uganda, China, India, Papua New Guinea, Tonga, Fiji, Tahiti, dan Pilipina (Anonim 2005). Budidaya vanili di Indonesia terutama di daerah Bali, Jawa Tengah, Sumatera Utara, Jawa Timur, Sumatra Selatan, Lombok, Flores, Sulawesi Utara dan Sulawesi Selatan (Anonim 2005). Untuk daerah lain di Indonesia juga memungkinkan dilakukan pengembangan budidaya vanili, karena tanaman vanili cocok untuk daerah tropik seperti Indonesia.
Dalam hal kualitas, vanili Indonesia lebih unggul dibanding vanili yang dihasilkan negara-negara lain. Vanili Indonesia memiliki kandungan vanillin 2,75 %, sementara yang lain lebih rendah (Meksiko 1,5 %). Kandungan vanillin vanili Indonesia yang lebih tinggi kemungkinan disebabkan iklim Indonesia cocok untuk budidaya vanili. Kualitas ini masih bisa ditingkatkan jika pengelolaan budidaya dan pasca panen dilakukan lebih baik (Anonim 2003).
Produk turunan vanili cukup banyak, antara lain ekstrak vanili, pasta vanili, concentrated vanilla extract, vanilla flavouring, concentrated vanilla flavouring, oleoresin vanili, dan bubuk vanili. Dari beberapa produk turunan vanili tersebut, bubuk vanili menawarkan kemudahan pemanfaatan dan penggunaannya. Vanili dalam bentuk bubuk memiliki umur simpan lama, bentuk sangat praktis sehingga penyimpanan lebih hemat tempat, siap pakai dan penggunaannya lebih luas.
Pada penelitian ini, ekstrak vanili diolah menjadi bubuk vanili dengan cara mikroenkapsulasi. Mikroenkapsulasi flavor merupakan suatu teknologi yang mengubah bahan flavor likuid menjadi bahan padat, sehingga dapat mengurangi degradasi atau penurunan aroma selama proses dan penyimpanan (Soottitantawat et al. 2004). Selain itu mikroenkapsulasi memberikan keawetan flavor seragam dan terhindar dari kontaminasi karena terlindungi oleh dinding kapsul.
Senyawa flavor sebagian besar bersifat volatil. Mikroenkapsulasi flavor dilakukan untuk memproduksi bubuk flavor sehingga dapat mencegah kehilangan flavor karena penguapan, memperpanjang umur simpan dan membuat flavor mudah digunakan (Usha dan Pothakamury 1995). Vanili merupakan campuran kompleks lebih dari 170 komponen volatil yang terdapat dalam vanili cured (Rao dan Ravishankar 2000). Teknik mikroenkapsulasi diharapkan dapat menahan komponen volatil vanili dalam waktu lama.
Pada proses mikroenkapsulasi, pemilihan penyalut sangat penting karena sangat mempengaruhi sifat emulsi sebelum pengeringan dan sifat mikrokapsul yang dihasilkan. Pemilihan penyalut tergantung dari keperluan dan produk yang diharapkan, sifat dari inti (core), proses enkapsulasi dan biaya (Amrita et al. 1999).
Tujuan Penelitian
Tujuan penelitian ini yaitu :
1. Mempelajari pengaruh proses mikroenkapsulasi ekstrak vanili dan sifat fisiokimia mikrokapsul (bubuk vanili) yang dihasilkan
2. Mempelajari pola retensi vanilin dari bubuk vanili selama penyimpanan.
Manfaat Penelitian
Manfaat penelitian ini yaitu :
1. Memberikan informasi mengenai pembuatan salah satu produk turunan ekstrak vanili yaitu bubuk vanili.
TINJAUAN PUSTAKA
Vanili
Vanili (Vanili sp) termasuk dalam famili Orchidaceae. Diperkirakan sebanyak 110 spesies tanaman teridentifikasi, namun hanya tiga spesies diantaranya yang ditanam secara komersial, yaitu V. fragnas (Salisbury) Ames atau juga dikenal dengan V. planifolia Andrwes, V. pompona Schiede dan V. tahitensis JW Moore (Rao dan Ravishankar 2000)
Vanili merupakan tanaman monokotil. Perakarannya serabut dan mendatar. Akar vanili terdiri dari akar perekat, akar gantung dan akar tanah. Akar perekat dan akar gantung tumbuh di setiap ruas batang. Batang vanili disebut juga sulur yang membantu tanaman untuk menjalar. Panjang batang mencapai 100 cm. Tanaman vanili berdaun tunggal dan letaknya berselang seling. Panjang daun 9 – 22 cm dan lebarnya 3 – 7 cm dengan tulang sejajar (Rismunandar dan Sukma 2003).
Buah vanili yang baru dipanen mengandung air sekitar 80% yang dikeringkan menjadi sekitar 20% pada saat proses kuring. Dalam 100 g buah kira-kira terkandung 20 g air, 3-5 g protein, 11 g lemak, 7-9 g gula, 15-20 g serat, 5-10 g abu, 1.5-3 g vanilin, 2 g resin dan asam vanilin (Guzman dan Siemonsma 1999). Buah vanili segar dapat dilihat pada Gambar 1.
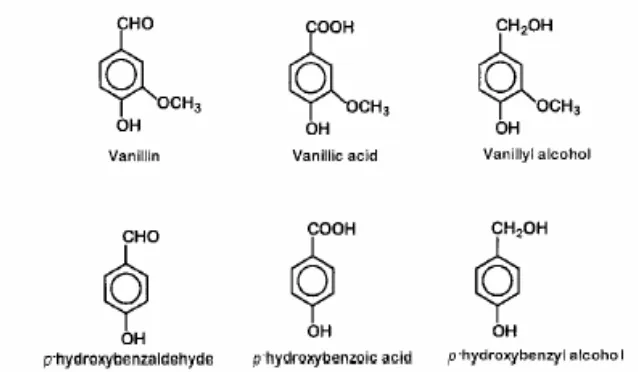
Buah vanili segar hampir tidak mempunyai bau. Flavor khas vanili merupakan campuran kompleks lebih dari 170 komponen volatil yang terdapat dalam vanili cured. Komponen utama pembentuk flavor vanili adalah vanilin, asam vanilat, vanilil alkohol, p-hidroksi benzaldehid, asam p-hidroksibenzoat & p-hidroksi benzil alkohol. Struktur dari tiap-tiap komponen dapat dilihat pada Gambar 2. (Rao dan Ravishankar 2000).
Gambar 2. Struktur kimia komponen utama vanili
Vanilin adalah senyawa aromatik dominan yang terdapat pada buah vanili dan merupakan komponen yang menentukan kelas mutu buah vanili. Hidrolisis glukovanilin (prekursor vanilin) oleh enzim β-glukosidase menghasilkan vanilin dan satu molekul β-D-glukosa. Enzim β-glukosidase terdapat pada bagian sitoplasma atau periplasma sel mesokrap dan endokrap buah vanili. Substrat glikovanilin terdapat pada bagian jaringan plasenta di sekitar biji (Setyaningsih 2006).
Tabel 1. Komponen utama vanili cured
Komponen Kimia Kandungan (g/kg berat kering)
Vanilin 20
Asam Vanilat 1
p-hidroksi benzaldehid 2
p-hidroksibenzil metil eter 0.2
Gula 250 Lemak 150 Selulosa 150-300 Mineral 60 Air 350 Sumber : (Rao dan Ravishankar 2000)
Vanilin terbentuk dari glukovanilin yang terjadi selama curing polong buah vanili. Kandungan glikosil dari vanilin atau campuran fenol lain, mannosa, galaktosa dan rhamnosa ditemukan pada sejumlah polong vanili yang sedang dalam masa perkembangan. Peningkatan kandungan glukovanilin dalam polong vanilin yang sedang berkembang pada tanaman rambatannya terjadi selama tiga bulan dan menurun (sampai berhenti) pada tahap akhir perkembangan polong. Glukovanilin umumnya dapat dilihat secara terpisah pada jaringan sebelah dalam plasenta yang berwarna putih yang letaknya di sekitar biji (Havkin dan Frenkel 2004).
Berdasarkan hasil isolasi dan identifikasi komponen glikosida buah vanili segar dan cured, komposisi senyawa yang terdeteksi menurut golongannya adalah asam, aldehid alifatik, alkohol alifatik, ester alifatik, alkana, alkanon, amin, lakton, dan senyawa turunan benzen yang terdiri dari benzen ester, benzen keton, benzen eter, benzen alkohol dan fenol (Setyaningsih et al. 2003).
pengeringan hari ke-5, sementara kadar vanilin terus meningkat selama proses pengeringan. Suhu optimum kerja enzim adalah 40oC.
Perlakuan perendaman buah segar dalam aktivator enzim β-glukosidase butanol 0.3 M dan sistein 1mM selama 2 jam menghasilkan aktivitas enzim, kadar vanilin, dan kadar gula yang lebih tinggi dibandingkan pengeringan standar (Metode Balitro II). Peningkatan kadar vanilin tertinggi terjadi pada pengeringan hari ke-5 (2,8%, standar 1,2%) dengan kadar air sekitar 70% (Setyaningsih et al. 2003).
Ekstraksi Vanili
Ekstraksi merupakan proses pemisahan pelarut yang melibatkan perpindahan zat terlarut ke dalam pelarut (Aguilera 1999). Pelarut yang digunakan merupakan pelarut organik yang mempunyai titik didih rendah, tidak beracun, dan tidak mudah terbakar (Ma’mun dan Laksanahardja 1998).
Ekstrak vanili dibuat dari buah kering yang dipotong-potong dengan panjang 0,5 cm. Potongan tersebut ditempatkan di dalam jar dan ditambah dengan etanol, gula dan air. Jar disimpan di tempat gelap dan dibiarkan selama 2-3 minggu. Sesekali jar tersebut dikocok. Setelah itu ekstrak disaring dengan menggunakan penyaring. Hasil ekstrak ditambah dengan sirup gula dan dikocok sampai rata. Untuk hasil yang baik, ekstrak harus disimpan selama minimal satu bulan sebelum digunakan (Arvillal 2001).
Balai Besar Industri Agro memiliki alat ekstraksi yang berupa rangkaian alat yang terdiri dari bak ekstraksi, penangas air, bak penampung larutan atau cairan ekstrak I dan II, serta pompa. Alat ini bisa digunakan untuk proses maserasi atau perkolasi (Suwandi dan Yuni 2004)
Proses ektraksi dilakukan pada suhu 50oC, agitasi selama 4-36 jam, dan pelarut ditambah dengan 20-30% larutan sodium laktat 50%. Cara ekstraksi ini dilakukan untuk menghasilkan ekstrak yang memiliki flavor yang tajam dan bebas dari bau segar (Takeji dan Thosie 2000).
kematangan buah, metode pengeringan, metode ekstraksi dan waktu penuaan ekstrak (Anonim 2005).
Hasil penelitian Melawati (2006) menunjukkan bahwa cara maserasi satu tahap dapat menghasilkan ekstrak vanili dengan kadar vanilin yang tinggi dibandingkan cara maserasi dua tahap. Pengerjaannya lebih sederhana dan mencegah pertumbuhan jamur pada saat maserasi. Komposisi etanol : air yang paling tepat untuk maserasi buah vanili setengah kering adalah 7 : 3. Waktu ekstraksi, sukrosa dan gliserin berpengaruh terhadap kadar vanilin.
Waktu maserasi dan sukrosa optimum pada waktu maserasi 12 hari dan sukrosa sebanyak 7 g dengan kadar vanilin sebesar 1509,39 mikrogram/g berat kering. Nilai kadar vanilin maksimal sebesar 1280,503 mikrogram/g dicapai pada perlakuan waktu ekstraksi 21 hari dan gliserin sebanyak 21 ml. Perlakuan waktu maserasi 12 hari, sukrosa 7 g dan gliserin 4,7 g menghasilkan kadar vanilin sebesar 3,8 g/l (Melawati 2006).
Mikroenkapsulasi
Mikroenkapsulasi merupakan suatu teknik di mana suatu bahan atau campuran bahan dilapisi atau diperangkap dalam bahan atau sistem lain (Madene et al. 2006). Mikroenkapsulasi memberikan perlindungan terhadap reaksi degradasi, mencegah kehilangan flavor dan mempertahankan stabilitas flavor dalam kapsul. Sebagai tambahan, enkapsulasi dapat digunakan untuk mengontrol pelepasan flavor selama pengolahan pangan dan penyimpanan (Soottitantawat et al. 2003).
Menurut McNamee (1998), mikroenkapsulasi didefinisikan sebagai suatu teknik mengemas atau melapisi bahan berupa cairan, padatan atau gas dengan suatu dinding atau lapisan tipis sehingga dapat menghambat volatilisasi dan melindungi dari kerusakan kimia. Enkapsulasi flavor dilakukan untuk melindungi flavor dalam penyalut spesifik sehingga stabil terhadap panas dan dapat memperpanjang umur simpan (Krishnan et al. 2005).
dari reaksi degradatif, mencegah kehilangan komponen flavor dan meningkatkan stabilitas komponen flavor, serta menekan kerugian selama penyimpanan dan pendistribusian (Hustiany 2006).
Industri pangan melakukan proses mikroenkapsulasi dengan beberapa alasan (Desai & Park 2005). Mikroenkapsulasi dilakukan diantaranya untuk melindungi inti dari degradasi dengan mengurangi reaksi inti dengan lingkungan luar, mengurangi evaporasi atau laju transfer inti ke lingkungan luar serta karakteristik bahan asal dapat dimodifikasi dan menjadi bahan yang mudah ditangani.
Proses enkapsulasi senyawa sensitif terdiri dari dua tahap. Tahap pertama pembuatan emulsi bahan inti (core) dengan bahan penyalut seperti polisakarida dan protein, tahap kedua pendinginan atau pengeringan emulsi. Enkapsulasi dapat mempertahankan aroma produk makanan selama pengeringan, melindungi flavor dari interaksi yang tidak diinginkan dengan makanan, meminimalkan interaksi flavor dengan flavor, menjaga reaksi yang dipicu oleh cahaya dan atau oksidasi, meningkatkan umur simpan flavor dan dapat berfungsi sebagai pengontrol pelepasan flavor (Tari dan Singhal 2002).
Retensi flavor berhubungan dengan sifat inti (core) meliputi berat molekul, fungsional kimia, polaritas dan volatilitas relatif, sifat bahan penyalut serta teknologi enkapsulasi. Berdasarkan proses enkapsulasi yang digunakan, matriks enkapsulasi akan berada dalam berbagai bentuk (film, sphere, partikel tidak beraturan), berbagai struktur (porous atau padat) dan berbagai sifat fisik (amorphous atau kristalin, rubber atau gelas) yang akan mempengaruhi difusi flavor maupun stabilitas produk makanan selama penyimpanan (Madene et al. 2006).
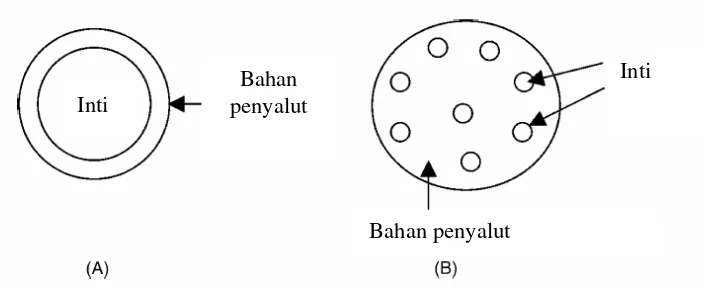
3A). Inti terlindungi di dalam kulit atau dinding dengan ketebalan bervariasi. Sedangkan Gambar 3B memperlihatkan beberapa inti berada dalam satu mikrokapsul (Desai & Park 2005).
Gambar 3 Skema struktur mikrokapsul
Ukuran partikel yang dibentuk selama proses enkapsulasi terdiri dari beberapa kisaran ukuran. Apabila ukuran partikelnya > 5000 μm disebut makrokapsul, ukuran partikelnya antara 0,2 - 5000 μm disebut mikrokapsul dan apabila ukuran partikelnya antara < 0,2μm - 2000 Ao disebut nanokapsul (King 1995). Ukuran mikrokapsul < 1 μm (Crouzet 1998). Menurut Krishnan et al. (2005), mikrokapsul berukuran 0,2–5000 μm dan memiliki bermacam bentuk tergantung bahan dan metode yang digunakan.
Teknologi mikroenkapsulasi telah berkembang dengan baik dan diterima di bidang farmasi, kimia, kosmetik, pangan dan industri percetakan (Augustin et al. 2001; Heinzen 2002). Penelitian di bidang pangan telah banyak dilakukan dengan berbagai metode enkapsulasi, bahan penyalut, komposisi bahan penyalut dan rasio inti terhadap bahan penyalut.
Jeon et al. (2002) telah melakukan mikroenkapsulasi flavor sintetik menggunakan pati asli dan pati temodifikasi suksinilat dan oktenil suksinilat, untuk mengurangi kehilangan flavor dan meningkatkan stabilitas flavor. Dari hasil penelitian diketahui pati suksinilat jagung dan barley lebih efektif dibanding pati asli dan pati oktenil suksinilat dalam ketahanan flavor. Pati suksinilat menunjukkan kemampuan ketahanan flavor dibandingkan β-siklodekstrin di mana
Inti
Bahan penyalut
Bahan penyalut
banyak digunakan sebagai bahan penyalut dalam mikroenkapsulasi minyak atsiri atau flavor.
Partanen et al. (2002) telah melakukan mikroenkapsulasi ekstrak jinten dengan teknik spray drying. Dari hasil penelitian, diketahui mikrokapsul dengan pati termodifikasi sebagai penyalut lebih toleran terhadap panas dibanding yang menggunakan β-siklodektrin. Selama pemanasan, β-siklodektrin melindungi senyawa volatil dari evaporasi sampai suhu 100oC sedangkan pati termodifikasi sampai suhu 140oC. Perlindungan senyawa volatil dari panas oleh maltodekstrin tergantung bahan yang dienkapsulasi (160oC untuk limonene dan 120oC untuk carvone).
Bouthboul et al. (2002) telah melakukan mikroenkapsulasi pada komponen aroma d-limonene, ethyl hexanoate, octanal dan 1-hexanol. Penyalut yang digunakan pati jagung asli, pati jagung termodifikasi asetilasi dan pregelatinisasi dan maltodekstrin. Dari hasil penelitian menunjukkan maltodekstrin merupakan bahan penyalut paling efisien untuk retensi flavor.
Apintanapong dan Noomhorm (2003) telah melakukan mikroenkapsulasi 2-acetyl-1-pyrroline dengan berbagai perbandingan gum arab dan maltodekstrin sebagai bahan penyalut menggunakan teknik spray drying. Kombinasi gum arab dan maltodekstrin 70 : 30 menghasilkan hasil terbaik.
Liu et al. (2004) telah melakukan mikroenkapsulasi flavor jamur Agaricus bisporus dengan teknik spray drying. Dari hasil penelitian, perbandingan bahan penyalut yang memberikan retensi flavor terbaik yaitu 10% protein kacang kedelai, 1% gum arab dan dekstrin 15%. Hasil penelitian menunjukkan produk ideal dapat diperoleh dengan suhu udara inlet 130–140oC dan suhu udara outlet 70–80oC.
Soottitantawat et al. (2005) telah melakukan mikroenkapsulasi l-menthol dengan teknik spray drying, menggunakan gum arab dan pati termodifikasi (CAPSUL, HI-CAP 100) sebagai penyalut. Hasil penelitian menunjukkan retensi l-menthol meningkat dengan meningkatnya konsentrasi padatan.
Krishnan et al. (2005) telah melakukan mikroenkapsulasi oleoresin cardamon dengan gum arab, maltodekstrin dan pati termodifikasi sebagai penyalut. Penyalut dengan perbandingan gum arab, maltodekstrin dan pati termodifikasi 4/6 : 1/6 : 1/6 memberikan hasil terbaik dibanding yang menggunakan 100% gum arab sebagai bahan penyalutnya.
Spray drying
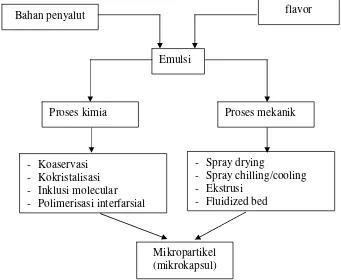
Sejumlah metode dilakukan untuk proses mikroenkapsulasi. Menurut Madene et al. (2006), beberapa teknik enkapsulasi yang telah dilakukan yaitu koaservasi, kokristalisasi, spray drying, fluid bed drying, spray cooling, ekstrusi dan inklusi molekular. Skema proses mikroenkapsulasi flavor dapat dilihat pada Gambar 4. Aplikasi metode enkapsulasi dalam industri pangan dapat dilihat pada Tabel 2.
Gambar 4 Skema proses mikroenkapsulasi flavor (Desai & Park 2005)
Bahan penyalut flavor
Emulsi
Proses kimia Proses mekanik
- Koaservasi - Kokristalisasi - Inklusi molecular - Polimerisasi interfarsial
- Spray drying
- Spray chilling/cooling - Ekstrusi
- Fluidized bed
Di antara sejumlah metode, spray drying merupakan metode paling populer untuk mikroenkapsulasi flavor (Soottitantawat et al. 2003). Dua metode yang banyak digunakan untuk enkapsulasi flavor yaitu spray drying dan ekstrusi (Goubet et al. 1998). Freeze drying, koaservasi dan teknik adsorpsi juga digunakan di industri.
Tabel 2 Aplikasi metode enkapsulasi dalam industri pangan Teknik enkapsulasi Bentuk produk Aplikasi Koaservasi
Spray drying merupakan teknik mikroenkapsulasi tertua. Metode ini telah digunakan sejak tahun 1930, digunakan untuk mengenkapsulasi flavor menggunakan gum arab sebagai penyalut (Bayram et al. 2005). Menurut Gadet et al. (2005), di antara sejumlah proses enkapsulasi metode yang sering digunakan yaitu spray drying dan freeze drying, spray drying lebih banyak digunakan karena biayanya lebih rendah dibanding freeze drying.
Menurut Teixeira et al. (2004), teknik spray drying menyediakan ketahanan aroma yang tinggi selama pengeringan. Keuntungan dari metode spray drying adalah melindungi komponen flavor dan mengontrol pelepasan komponen flavor selama penyimpanan. Keuntungan penggunaan pengering semprot adalah dapat menangani bahan-bahan yang tidak stabil terhadap panas (Hustiany 2006).
Mikroenkapsulasi flavor menggunakan spray drying telah dikembangkan dengan pelepasan panas terkontrol (Cho & Park 2002). Teknik mikroenkapsulasi yang umum digunakan dalam industri pangan adalah spray drying, karena spray drying dianggap metode paling mudah diterapkan dan paling ekonomis. Di samping itu peralatan yang digunakan untuk mikroenkapsulasi dengan metode spray drying banyak tersedia (Clarke 2000).
Mikroenkapsulsi dengan teknik spray drying memiliki tiga tahapan utama (Desai & Park 2005, Bayram et al. 2005). Tahap pertama yaitu persiapan dispersi atau emulsi, kemudian homogenisasi dispersi dan tahap akhir yaitu atomisasi dispersi dalam chamber pengering. Menurut Soottitantawat et al. (2005), tahap umum mikroenkapsulasi dengan teknik spray drying yaitu mentransformasikan bahan bentuk likuid berupa larutan, dispersi atau emulsi menjadi partikel kering dengan cara men-spray bahan dalam udara panas.
Menurut Liu et al. (2003), suhu sebaiknya tidak terlalu tinggi karena akan menyebabkan penguapan beberapa komponen volatil. Suhu udara inlet berhubungan erat dengan kecepatan pengeringan dan kemampuan untuk mengeringkan produk, untuk memperoleh struktur granula dengan kandungan air yang cocok untuk stabilitas produk mikroenkapsul..
Ketika suhu udara inlet rendah, kemampuan evaporasi tidak cukup untuk membentuk membran kapsul yang baik. Produk yang dihasilkan memiliki kandungan air tinggi dan memiliki fluiditas rendah sehingga mudah lengket. Sebaliknya, ketika suhu udara inlet tinggi, evaporasi yang berlebih dapat menyebabkan keretakan dalam membran maupun kehilangan komponen flavor melalui penguapan dan terdekomposisinya komponen sensitif panas pada suhu tinggi. Hal ini juga menyebabkan off-flavor (Liu et al. 2003).
Suhu udara outlet memiliki pengaruh yang nyata terhadap kadar air produk dan struktur mikroenkapsul. Suhu udara outlet dan inlet harus dikontrol. Suhu udara outlet tinggi, akan membantu untuk membentuk suatu kesatuan dan struktur dinding yang padat serta meningkatkan pengaruh pengeringan. Apabila suhu udara outlet terlalu tinggi, produk akan retak karena overheating (Liu et al. 2003).
memberikan beberapa keuntungan dibanding metode lain yaitu biaya operasi rendah, produk kapsul yang dihasilkan berkualitas tinggi dan cepat larut, berukuran kecil dan memiliki stabilitas tinggi (Madene et al. 2006). Kekurangan metode ini yaitu mikrokapsul yang dihasilkan tidak seragam dan keterbatasan pemilihan bahan penyalut (viskositas rendah pada konsentrasi tinggi).
Bahan Penyalut
Enkapsulasi merupakan suatu teknik di mana suatu atau campuran bahan disalut dengan sistem atau bahan lain. Bahan yang disalut disebut bahan inti (core) dan bahan penyalut disebut cangkang (shell), bahan dinding (wall material), carrier atau enkapsulan (Madene et al. 2006).
Bahan penyalut yang ideal menurut Desai & Park (2005) harus memiliki sifat sebagai berikut :
1. Memiliki sifat reologi yang baik pada konsentrasi tinggi dan penanganannya mudah selama proses enkapsulasi
2. Mampu mendispersi dan mengemulsi bahan inti dan menstabilkan emulsi 3. Tidak bereaksi dengan bahan yang akan dienkapsulasi selama proses dan
penyimpanan
4. Mampu melindungi bahan inti selama proses dan penyimpanan
5. Mampu melepaskan pelarut padaa proses pengeringan atau tahap penghilangan pelarut
6. Mampu memberikan perlindungan maksimum bahan inti dari lingkungannya (oksigen, panas, cahaya, kelembaban)
7. Larut dalam pelarut yang diperbolehkan di industri pangan (air, etanol) 8. Tidak mahal, food-grade
Tabel 3 Karakteristik bahan penyalut untuk enkapsulasi flavor
Sifat penyalut yang optimal untuk proses spray drying yaitu memiliki kelarutan yang tinggi dalam air, viskositas rendah pada konsentrasi tinggi, memiliki sifat emulsifier dan pembentuk film yang baik dan pengeringan yang efisien (Re-MI 1998). Karbohidrat merupakan bahan yang banyak digunakan sebagai penyalut di industri pangan.
Karbohidrat seperti pati, maltodekstrin, sirup glukosa dan gum akasia menjadi pilihan untuk bahan enkapsulasi karena kemampuannya berikatan dengan flavor, harga rendah dan dapat digunakan untuk aneka ragam industri (Dziezak 1988; Mutka & Nelson 1988). Bahan penyalut yang dapat digunakan dengan teknik spray drying adalah gum arab, pati termodifikasi (esterifikasi dan suksinilasi) dan pati hidrolisis (maltodektrin). Semua bahan ini mempunyai viskositas yang rendah pada konsentrasi tinggi (King 1995). Pati dan produk turunannya seperti maltodekstrin dan β-siklodekstrin banyak digunakan untuk enkapsulasi flavor (Madene et al. 2006).
Pengikatan senyawa volatil oleh pati diklasifikasikan dalam dua tipe. Di satu sisi senyawa flavor dikelilingi oleh heliks amylase melalui ikatan hidrofobik, di sisi lain terjadi interaksi polar dengan adanya ikatan hidrogen antara grup hidroksil pati dengan senyawa flavor (Arvisenet et al. 2002; Boutboul et al. 2002). Pati dan produk berbahan dasar pati seperti pati termodifikasi, maltodekstrin dan β-siklodekstrin digunakan secara luas di industri pangan untuk melindungi komponen volatil.
Gum arab sangat efektif sebagai bahan penyalut karena mampu melindungi koloid dengan baik (Krishnan et al. 2005). Gum arab mampu menstabilkan emulsi pada range pH yang lebar. Gum arab dapat digunakan bersama dengan gum lain, karbohidrat dan protein. Namun harga yang tinggi dan ketersediaan yang terbatas membatasi penggunaan gum arab untuk enkapsulasi. Maltodekstrin dan pati termodifikasi telah diinvestigasi sebagai pengganti gum arab (McNamee 1998).
Pati Termodifikasi
Pati asli sangat terbatas penggunaannya karena memiliki viskositas tinggi, sangat kohesif, stabil pada suhu rendah, tidak tahan pada makanan dengan pH rendah (Jobling 2004). Di samping sebagai zat gizi, pati biasanya ditambahkan ke dalam bahan makanan sebagai pengental, pengikat, pembentuk gel, perekat, bahan enkapsulasi, pembentuk film, penstabil, pembentuk tekstur, pengganti lemak atau untuk tujuan proses. Pati termodifikasi adalah pati asli yang telah diubah sifat-sifat fisik dan/atau kimianya. Walaupun penampilan pati modifikasi menyerupai pati asli, modifikasi mempertinggi daya guna pati dengan memperbaiki kualitas fungsional spesifik seperti suhu gelatinisasi, kejernihan pasta, viskositas dan kemampuan membentuk film (Ferris et al. 2001).
Menurut Wurzburg (1986), metode modifikasi pati antara lain adalah derivatisasi (substitusi atau stabilisasi) yaitu mengganti gugus hidroksil pati dengan gugus fungsional lain seperti propilen oksida (hidroksipropilasi) pada kondisi alkali, atau dengan asetat (asetilasi), suksinat, oktenil suksinat, fosfat atau hidroksietil dan kationik. Derivatisasi ini menghambat asosiasi amilosa dalam pati tergelatinisasi, memperbaiki kejernihan, menurunkan kemampuan membentuk gel, memperbaiki kapasitas menahan air, memperbaiki kekentalan dan stabilitas pembekuan (freeze-thawing) serta menurunkan retrogradasi/sineresis. Pati modifikasi jenis ini dapat digunakan untuk mikroenkapsulasi.
Pati termodifikasi secara kimia oktenil suksinilat (n-OSA) memiliki sifat fungsional mendekati gum arab (Jeon et al. 2002). Pati n-OSA menstabilkan emulsi melalui berbagai kemungkinan mekanisme. Pati n-OSA dilaporkan lebih unggul dibanding gum akasia dalam sifat emulsi dan menahan flavor volatil selama spray drying. Kelebihan pati hasil modifikasi ini tidak berasa (Kuentz et al. 2005). Walaupun demikian, pati termodifikasi memiliki kekurangan, sering memiliki off-taste yang tidak diharapkan dan bukan pelindung yang baik dari oksidasi (Qi dan Xu 1999).
Maltodekstrin
Maltodekstrin merupakan produk yang dibentuk melalui hidrolisis parsial pati dengan asam atau enzim, dapat dibuat dengan berbagai DE (Dextrose Equivalent). DE merupakan suatu ukuran derajat hidrolisis polimer pati (Madene 2006). Apabila dalam satu molekul hidrolisat amilosa dan amilopektin mengandung 100 unit anhidroglukosa dan terdapat 1 gugus gula pereduksi, maka nilai DE-nya adalah 1. Nilai DE sama dengan 50 adalah maltosa (Wuzburg 1989). Nilai DE sama dengan 100 adalah murni dekstrosa (glukosa) dan nilai DE sama dengan 0 adalah pati asli. Hidrolisat dengan DE di bawah 20 adalah maltodekstrin, sedangkan DE diantara 20 dan 100 adalah sirup glukosa (Murphy 2000).
keseimbangan panjangnya polimer, yang menolong untuk menangkap komponen flavor pada permukaan droplet yang diinginkan (Kenyon 1995).
Penggunaan maltodektrin sebagai penyalut dapat mengurangi biaya karena harganya murah, memiliki viskositas yang rendah pada rasio padatan yang tinggi dan tersedia dalam beberapa berat molekul yang berbeda (Apintanapong dan Noomhorm 2003). Kekurangan maltodekstrin sebagai penyalut yaitu memiliki sifat emulsifier yang rendah dan retensi volatil rendah (Buffo dan Reineccius 2000).
METODOLOGI
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian dan Laboratorium South East Asian Food & Agriculture Science & Technology (SEAFAST) Center IPB. Penelitian dimulai dari bulan April 2006 sampai dengan September 2007.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini terdiri atas bahan-bahan untuk kuring vanili, ekstraksi vanili, mikroenkapsulasi dan bahan-bahan untuk analisis. - Bahan yang digunakan untuk kuring vanili terdiri atas vanili segar (Vanilla
planifolia Andrews) yang diperoleh dari Kuningan Jawa Barat, sistein 1 mM dan butanol 0.3 M.
- Bahan untuk ekstraksi vanili terdiri atas vanili ½ kering hasil kuring, etanol 60% dan sukrosa.
- Bahan untuk mikroenkapsulasi terdiri atas pati tapioka termodifikasi Flomax 8 dan maltodekstrin DE 10 dari National Starch, CMC dan air destilata.
- Bahan untuk analisa terdiri atas vanilin standar, etanol p.a., NaOH, air destilata, kertas saring.
Alat yang digunakan dalam penelitian ini terdiri atas alat-alat untuk kuring vanili, ekstraksi vanili, mikroenkapsulasi dan alat-alat untuk analisis.
- Alat yang digunakan untuk kuring vanili yaitu kotak peram, waterbath, oven, pisau, wadah plastik dan timbangan.
- Alat yang digunakan untuk ekstraksi vanili yaitu pisau, timbangan analitik, gelas ukur, wadah gelas, pengaduk kayu dan rotary vacuum evaporator. - Alat yang digunakan untuk mikroenkapsulasi yaitu homogenizer, spray dryer
dan neraca analitik.
Metode Penelitian I. Persiapan bahan
Pada tahap ini dilakukan proses pengeringan vanili untuk mendapatkan vanili ½ kering, selanjutnya vanili ½ kering ini dijadikan sebagai bahan ekstraksi vanili untuk mendapatkan ekstrak vanili.
1. Proses kuring vanili ½ kering modifikasi
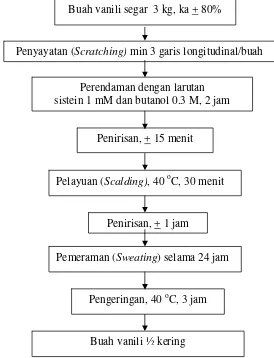
Proses kuring dilakukan mengikuti metode yang dilakukan oleh Setyaningsih (2006). Pada buah vanili segar dilakukan penggoresan (scratching) minimal 3 garis longitudinal tiap buah, kemudian dilakukan perendaman dengan larutan butanol 0,3 M dan sistein 1 mM selama 2 jam, setelah itu dilakukan penirisan selama 15 menit. Selanjutnya dilakukan pemanasan (scalding) pada suhu 40oC selama 30 menit, kemudian dilakukan pemeraman (sweating) selama 24 jam, dan dikeringkan pada suhu 40oC selama 3 jam (Gambar 5).
Penyayatan (Scratching) min 3 garis longitudinal/buah
Perendaman dengan larutan sistein 1 mM dan butanol 0.3 M, 2 jam
Penirisan, + 15 menit
Pelayuan (Scalding), 40 oC, 30 menit
Penirisan, + 1 jam
Pemeraman (Sweating) selama 24 jam
Pengeringan, 40 oC, 3 jam Buah vanili segar 3 kg, ka + 80%
Buah vanili ½ kering
Gambar proses kuring vanili ½ kering modifikasi dapat dilihat pada Lampiran 1.
2. Proses Ekstraksi Vanili
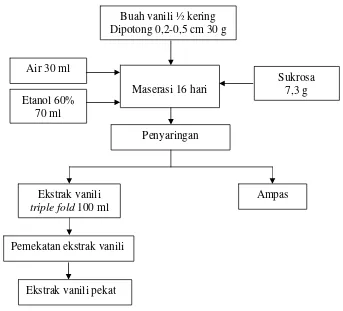
Proses ekstraksi vanili mengikuti metode yang telah dilakukan oleh Melawati (2006). Buah vanili ½ kering sebanyak 30 g dipotong 0,2-0,5 cm, selanjutnya vanili diekstrak dengan menggunakan pelarut etanol dan air (7 : 3), kemudian ditambah sukrosa sebanyak 7,3 g. Proses maserasi dilakukan selama 16 hari kemudian dilakukan penyaringan sehingga didapatkan ekstrak vanili triple fold 100 ml. Selanjutnya dilakukan penguapan etanol menggunakan rotary vacuum evaporator pada suhu 40 oC, kecepatan 150 rpm selama 3 jam, dari 300 ml ekstrak yang diuapkan didapatkan 160-170 ml (Gambar 6). Gambar proses ekstraksi vanili dapat dilihat pada Lampiran 2.
Gambar 6 Proses ekstraksi vanili (Melawati 2006) Buah vanili ½ kering
Dipotong 0,2-0,5 cm 30 g
Maserasi 16 hari Air 30 ml
Etanol 60% 70 ml
Sukrosa 7,3 g
Penyaringan
Ekstrak vanili triple fold 100 ml
Ampas
Pemekatan ekstrak vanili
II. Pemilihan bahan penyalut
Tahap penelitian ini bertujuan untuk mendapatkan bahan penyalut yang tepat untuk mikroenkapsulasi ekstrak vanili. Dari tahap ini dipilih 2 perlakuan bahan penyalut yang memberikan hasil terbaik dari parameter yang diamati. Bahan penyalut yang digunakan maltodekstrin DE 10 dan pati tapioka termodifikasi Flomax 8 dibuat dengan perbandingan 1 : 0, 0 : 1, 1 : 2, 2 : 1 dan 1 : 1.
Mikroenkapsulasi dengan spray dryer mengikuti metode Krishnan et al. (2005) yang telah dimodifikasi. Bahan-bahan penyalut dilarutkan dalam air destilata dengan konsentrasi 30%, kemudian ditambahkan ekstrak vanili. Perbandingan ekstrak vanili dan bahan penyalut = 3 : 2. Setelah itu campuran direhidrasi pada suhu 10-12oC selama 12 jam. Pada proses mikroenkapsulasi ekstrak vanili ini sebelum dikeringkan dengan spray dryer ditambah CMC 0,5% untuk membantu kestabilan emulsi. Campuran dihomogenisasi dengan homogenizer selama 5 menit pada kecepatan 3000 rpm. Spray dryer diatur suhunya, suhu inlet 140–150oC dan suhu outlet 70–80oC (Gambar 7). Sampel disimpan di suhu -30 oC sampai dianalisis. Parameter yang diamati pada tahap ini adalah kadar vanilin pada powder mengikuti metode Jeon et al (2003) yang telah dimodifikasi, kelarutan bubuk vanili dan aw (water activity).
III. Formulasi mikroenkapsulasi ekstrak vanili
Faktor yang diuji adalah jenis penyalut, konsentrasi penyalut dan perbandingan ekstrak vanili dengan penyalut. Penyalut yang digunakan adalah dua penyalut terbaik dari penelitian pemilihan penyalut. Penyalut dalam air destilata dibuat dengan konsentrasi 10%, 20% dan 30%. Ekstrak vanili dengan penyalut dibuat dengan perbandingan 3 : 2, 2 : 1 dan 3 : 1. Sampel disimpan di suhu -30 oC sampai dianalisis. Parameter yang diamati meliputi kelarutan, aw
IV. Retensi vanilin selama penyimpanan
Pada tahap ketiga ini dipilih dua perlakuan untuk mengetahui retensi vanilin selama penyimpanan. Penyimpanan dilakukan pada suhu 4oC, 30oC dan 55oC selama tujuh minggu. Sampel disimpan di botol kaca bertutup. Pengamatan terhadap kadar vanilin dilakukan setiap minggu. Pengukuran laju penurunan retensi vanilin selama penyimpanan menggunakan persamaan Arrhenius dan persamaan Avrami. Pada tahap ini juga dilakukan perhitungan waktu paruh bubuk vanili. Parameter aw diamati pada minggu ke-0 dan minggu ke-4. Bentuk
bubuk diamati pada minggu ke-4 menggunakan Scanning Electron Microscopy (SEM).
- Persamaan Arrhenius yaitu : k = ko.e-Ea/RT
di mana : ko = konstanta laju absolut
k = konstanta laju penurunan pada suhu T Ea = Energi aktivasi (J/mol)
Maltodekstrin DE 10 dan pati tapioka termodifikasi Flomax 8
Pencampuran
Pengeringan dengan spray dryer suhu inlet 130–140 oC, suhu outlet 70–80 oC.
Bubuk vanili Air destilata
Penyimpanan pada suhu 10-12 oC, 12 jam
Pembuatan emulsi dengan homogenizer pada kecepatan 3000 rpm selama 10 menit Ekstrak
vanili
R = Konstanta gas ideal (8,314 JK-1mol-1) T = Suhu absolut (oK)
- Persamaan Avrami yaitu : R = exp [- (kt)n
]
di mana : n = parameter untuk menentukan mekanisme laju penurunan retensi vanilin
k = konstanta laju penurunan vanilin R = retensi vanilin selama penyimpanan t = waktu penyimpanan.
- Waktu paruh (t½) yaitu :
t½ = 0,693/k
di mana : k = slope dari persamaan regresi yang menghubungkan ln persen retensi vanilin selama penyimpanan dengan waktu penyimpanan
Prosedur analisis dari parameter-parameter yang diamati :
a. Kadar vanilin dengan metode spektrofotometer (AOAC 1995)
1. Pembuatan kurva standar
absorbansinya dengan menggunakan spektrofotometer pada panjang gelombang 348 nm. Kurva standar dibuat dengan cara memplotkan antara konsentrasi vanilin (ppm) dengan selisih absorbansi (larutan + NaOH dikurangi larutan blanko). 2. Penentuan absorbansi larutan sampel
Larutan sampel dipipet sebanyak 1000 μl dengan menggunakan pipet mikron, dimasukkan ke dalam labu takar 10 ml, ditambahkan akuades sampai tanda tera. Larutan ini disebut larutan 1. Larutan 1 dipipet sebanyak 200 μl dimasukkan ke dalam labu ukur 10 ml, ditambahkan 200 μl 0.1 N NaOH dan akuades sampai tanda tera. Larutan blanko dibuat tanpa penambahan 0.1 N NaOH. Masing-masing larutan diukur absorbansinya pada panjang gelombang 348 nm, dihitung selisih absorbansi antara larutan yang ditambah dengan 0,1 N NaOH dan larutan blanko. Kemudian dihitung konsentrasi vanilinnya berdasarkan kurva standar.
Kadar vanilin (μg/g berat kering) = Y x 500 x V W x (100 - H) Di mana :
Y : Konsentrasi vanilin berdasarkan kurva standar (μg/ml) atau ppm V : Volume ekstrak single fold (ml)
W : Bobot buah vanili yang diekstrak H : Kadar air (%)
500 : Faktor pengenceran sampel
b. Kelarutan mikrokapsul (Aini 2001)
Perhitungan tingkat bahan terlarut dapat ditentukan dengan persamaan :
Aw produk mikroenkapsulasi diukur dengan menggunakan Aw-meter WA-360 Shibaura Electronics Co. Ltd. Sebelum dilakukan pengukuran, alat dikalibrasi dengan larutan garam NaCl jenuh. Kalibrasi selesai dan dinyatakan berhasil apabila angka yang tertera di alat menunjukkan 0,750. Selanjutnya sampel dimasukkan ke dalam tempat sampel dengan cawan khusus kemudian ditutup. Tombol start ditekan. Pengukuran selesai apabila nilai sudah stabil dan tertera tulisan completed.
Recovery vanilin bubuk vanili disajikan dalam bentuk persen (%) dihitung berdasarkan perbandingan antara jumlah vanilin setelah dienkapsulasi (g/100g) dengan jumlah vanilin sebelum dienkapsulasi (g/100g) dikalikan 100.
Recovery vanilin (%) = jumlah vanilin setelah dienkapsulasi (g/100g) x 100 jumlah vanilin sebelum dienkapsulasi (g/100g)
f. Retensi vanilin selama penyimpanan
Retensi vanilin selama penyimpanan dihitung dengan rumus : Retensi vanilin (%) = (C/Co) x 100
C = retensi vanilin hari ke-x; Co = retensi vanilin hari ke-0
g. Bentuk mikrokapsul
Bentuk mikrokapsul diamati menggunakan Scanning Electron Microscopy (SEM). Sampel yang diamati yaitu bubuk vanili yang sudah disimpan 4 minggu. Sampel ditempatkan pada potongan spesimen yang telah
diberi karbon, kemudian spesimen disapuh dengan lapisan emas selama 4 menit, arus listrik 100 mA dan ketebalan penyapuhan 400 Å. Sampel yang telah disapuh dimasukkan ke dalam alat Scanning Electron Microscope yang dilengkapi kamera foto dengan pembesaran 3500x.
Analisis statistik
Penelitian pemilihan bahan penyalut menggunakan Rancangan Acak Lengkap (RAL) satu faktor dengan tiga ulangan. Perlakuan yang diuji yaitu jenis penyalut yang digunakan tunggal dan kombinasi dua bahan penyalut. Bahan penyalut yang digunakan maltodekstrin DE 10 dan pati tapioka termodifikasi Flomax 8 dengan perbandingan 1 : 0, 0 : 1, 1 : 2, 2 : 1 dan 1 : 1.
Penelitian formulasi mikroenkapsulasi ekstrak vanili menggunakan Rancangan Acak Lengkap (RAL) tiga faktor dengan dua ulangan. Faktor pertama yaitu jenis penyalut yang merupakan dua penyalut terbaik dari penelitian pemilihan penyalut. Faktor kedua yaitu konsentrasi penyalut (10%, 20% dan 30%). Faktor ketiga yaitu rasio ekstrak vanili dengan penyalut (3 : 2, 2 : 1 dan
3 : 1).
Penelitian pengaruh suhu dan lama penyimpanan terhadap nilai aw
menggunakan Rancangan Acak Lengkap (RAL) dua faktor dengan dua ulangan. Faktor pertama lama penyimpanan (0 dan 4 minggu) dan faktor kedua suhu penyimpanan (4, 30 dan 55oC).
Penelitian retensi vanilin selama penyimpanan menggunakan rancangan petak terpisah (Split plot Design) RAL dua faktor dengan dua ulangan. Faktor pertama suhu penyimpanan (4, 30 dan 55oC) dan faktor kedua, waktu penyimpanan (0, 7, 14, 21, 28, 35, 42).
HASIL DAN PEMBAHASAN
IV.Pembuatan ekstrak vanili
Sebelum dilakukan ekstraksi vanili, pada vanili dilakukan proses kuring mengikuti metode yang dilakukan oleh Setyaningsih et al. (2003). Proses kuring yang dilakukan yaitu kuring vanili ½ kering hasil modifikasi. Pada metode kuring ini, dilakukan perendaman buah vanili segar dengan butanol 0,3 M dan sistein 0,001 M selama 2 jam. Kedua zat tersebut berperan sebagai aktivator enzim β -glukosidase yang dapat menghidrolisis senyawa prekursor glukovanilin menjadi vanilin yang merupakan salah satu senyawa pembentuk flavor vanili yang dominan.
Vanili yang telah dipanen masih memiliki jaringan hidup dan melangsungkan aktivitas fisiologisnya. Dalam proses kuring vanili, perlu untuk menghentikan perkembangan vegetative dan merusak struktur sel, sehingga sejumlah enzim dapat kontak dengan substratnya. Struktur sel dapat rusak diantaranya dengan cara pelayuan dengan air panas, pemanasan dengan sinar matahari atau oven dan pembekuan. Proses ini disebut killing, proses ini juga merusak fungsi respirasi dengan merusak sel membran. Di antara sejumlah proses, killing dengan air panas serta panas dengan oven dan sinar matahari metode yang banyak digunakan (Rao dan Ravishankar 2000).
Pada penelitian ini, proses killing dilakukan yaitu dengan pelayuan pada suhu 40oC. Proses pelayuan ini menyebabkan sel menjadi rusak sehingga memungkinkan terjadinya difusi substrat untuk bertemu dengan enzim dan mempercepat proses kuring. Pada proses ini inhibitor yang menghambat kerja enzim juga mati. Selanjutnya dilakukan pemeraman, aktivitas sebagian besar enzim aktif pada tahap ini.
atas kadar vanilin yang dihasilkan dari hasil penelitian metode Balitro II yaitu sebesar 1,2%.
Vanili ½ kering hasil kuring selanjutnya digunakan sebagai bahan untuk ekstraksi vanili. Metode ekstraksi yang dilakukan yaitu metode ekstraksi dengan cara maserasi yang dilakukan oleh Melawati (2006). Metode maserasi yaitu metode ekstraksi dengan cara merendam bahan yang akan diekstrak dalam wadah.
Pada buah vanili setengah kering tadi dipotong berukuran 0,2-0,5 cm. Pengecilan ukuran ini bertujuan meningkatkan daya ekstraksi. Daya ekstraksi akan semakin meningkat dengan semakin kecilnya ukuran bahan. Hal ini disebabkan kontak antara bahan yang diekstrak merupakan proses osmosis yang berjalan lambat. Apabila bahan terlalu halus dapat membentuk suspensi dengan pelarut, selain itu juga dapat terjadi penguapan senyawa volatil yang berlebihan sebelum proses ekstraksi (Ketaren dan Suastawa 1994).
Pada penelitian ini, dibuat ekstrak vanili triple fold. Pelarut yang digunakan 100 ml sedangkan vanili sebanyak 30 gram. Pelarut yang digunakan pada penelitian ini yaitu etanol dengan konsentrasi 60% dan air, kedua pelarut ini dibuat dengan perbandingan 7 : 3. Sukrosa yang ditambahkan pada larutan ini dapat meningkatkan viskositas, membantu mengekstrak senyawa aromatik, meningkatkan warna, menghambat penguapan alkohol dan menahan aroma vanilin dalam ekstrak (Ruhnayat 2001). Sedangkan menurut Purseglove et al. (1981), penambahan gula untuk memberikan kesan smoothness dan kekentalan pada ekstrak, membantu memantapkan komponen aroma, serta dapat memperpanjang umur simpan. Proses maserasi dilakukan menggunakan wadah gelas, dilakukan pengadukan sebanyak dua kali setiap harinya. Proses maserasi dilakukan selama 16 hari. Setelah 16 hari dilakukan penyaringan untuk memisahkan ekstrak vanili dengan ampasnya. Selanjutnya dilakukan pemekatan ekstrak vanili dengan rotary vacuum evaporator.
V. Pengaruh jenis penyalut terhadap aw, kadar vanilin dan kelarutan
produk ekstrak vanili terenkapsulasi (bubuk vanili)
Pada proses mikroenkapsulasi, pemilihan penyalut sangat penting karena sangat mempengaruhi sifat emulsi sebelum pengeringan dan sifat mikrokapsul (bubuk) yang dihasilkan. Pada penelitian ini digunakan bahan penyalut pati tapioka termodifikasi Flomax 8 dan maltodekstrin DE 10. Kedua bahan ini di dapat dari PT National Starch.
Pati tapioka termodifikasi Flomax 8 merupakan jenis pati yang aplikasinya diperuntukkan untuk enkapsulasi flavor dengan spray drying. Mikrokapsul atau bubuk yang didapat dengan menggunakan penyalut pati tapioka termodifikasi Flomax 8 jenis ini memiliki daya alir yang baik dan dapat direkonstitusi dengan air. Selain itu pati jenis ini memiliki viskositas rendah dan tidak berasa sehingga cocok untuk enkapsulasi flavor (National Starch 2006). Adapun karakteristik dari pati tapioka termodifikasi Flomax 8 dapat dilihat pada Tabel 4.
Tabel 4 Karakteristik pati tapioka termodifikasi Flomax 8
Karakteristik Keterangan
oleh Yoshii et al. (2001), maltodekstrin dengan DE 10 telah memberikan retensi flavor terbaik pada penelitian yang dilakukan pada duabelas jenis flavor. Dengan meningkatnya DE (DE 10, DE 15, DE 20, DE 25 and DE 36,5), retensi flavor menurun.
Penelitian Shiga et al. (2003) mengenkapsulasi komponen flavor lenthionine dengan penyalut yang memiliki DE 8, 11 dan 25. Hasil penelitiannya menyebutkan nilai DE bahan penyalut berpengaruh terhadap retensi komponen flavor. Retensi flavor meningkat dengan semakin menurunnya nilai DE. Goubet et al. (1998) melaporkan hasil yang sama mengenai pengaruh DE terhadap retensi flavor. Menurut Voiley dan Simatos et al. (1980), retensi flavor meningkat dengan meningkatnya berat molekul disebabkan karena berkurangnya difusi flavor selama pengeringan. Bang dan Reineccius (1990) menerangkan bahwa laju pembentukan crust mikrokapsul (bubuk) meningkat dengan meningkatnya berat molekul penyalut.
Produk dengan DE sedang atau lebih rendah lebih efisien digunakan untuk enkapsulasi dengan spray drying. Hal ini kemungkinan disebabkan adanya keseimbangan panjangnya polimer, yang menolong untuk menangkap komponen flavor pada permukaan droplet yang diinginkan (Kenyon 1995). Dari hasil beberapa penelitian yang telah dilakukan, maka pada penelitian ini digunakan maltodekstrin yang memiliki nilai DE rendah yaitu DE 10.
Hasil penelitian menunjukkan adanya pengaruh jenis penyalut yaitu maltodekstrin dan pati tapioka termodifikasi Flomax 8 yang dibuat dengan perbandingan 1 : 0, 0 : 1, 1 : 2, 2 : 1 dan 1 : 1 terhadap aw, kelarutan dan kadar
vanilin yang bervariasi dari produk ekstrak vanili terenkapsulasi (bubuk vanili). Data nilai aw, kelarutan dan kadar vanilin dari bubuk vanili dapat dilihat pada
Tabel 5.
Nilai aw (water activity)
Pada penelitian ini aw yang dihasilkan berkisar 0,442-0,478 (Tabel 5).
Hasil sidik ragam menunjukkan jenis dan komposisi penyalut yang digunakan pada penelitian ini tidak berpengaruh nyata terhadap aw bubuk vanili(Lampiran 5
Tabel 5 Nilai aw, kelarutan dan kadar vanilin bubuk vanili Keterangan : Huruf yang sama dalam baris dan kolom menunjukkan tidak ada
beda nyata antar perlakuan (p = 0.05).
Retensi komponen flavor dipengaruhi oleh aw (aw = RH/100). Produk yang
dianggap paling baik yaitu produk dengan aw terendah dihasilkan dari perlakuan
menggunakan penyalut maltodekstrin dan penyalut maltodekstrin dengan pati tapioka termodifikasi Flomax 8 dengan perbandingan 2 : 1 yaitu 0,442. Pada aw
rendah, kapsul berada pada keadaan glassy, kondisi ini menyebabkan flavor yang dienkapsulasi memiliki mobilitas rendah sehingga laju pelepasan flavor pun rendah. Sekali saja struktur kapsul rusak dengan masuknya air, laju pelepasan pun meningkat. Ini dapat disebabkan mobilitas tinggi dari flavor yang dienkapsulasi, di mana kapsul mulai berada pada kondisi plastis (Soottitantawat et al. 2005). Hasil penelitiannya pada produk l-menthol terenkapsulasi menunjukkan pada aw rendah hanya sejumlah kecil l-menthol yang lepas dari
mikrokapsul. Semakin besar nilai aw maka semakin besar pula mobilitas
l-menthol terenkapsulasi. L-menthol mulai lepas dari penyalut pada aw lebih besar
dari 0,5.
Kadar vanilin
pada semua perlakuan sama yaitu 3 : 2 terhadap penyalut, sementara jenis dan komposisi penyalut tidak berpengaruh nyata terhadap kadar vanilin bubuk vanili.
Kelarutan
Kelarutan bubuk vanili yang dilarutkan pada air suhu 40oC berkisar antara 26,69 - 90,28 % (Tabel 5). Hasil sidik ragam menunjukkan jenis dan komposisi penyalut yang digunakan pada penelitian ini berpengaruh nyata terhadap kelarutan produk bubuk vanili (Lampiran 9). Dari hasil uji lanjut Duncan, kelarutan produk bubuk vaniliberbeda antar perlakuan (Lampiran 10). Kelarutan bubuk vanili terbesar pada perlakuan dengan penyalut maltodekstrin sebesar 92,28% dan kelarutan terendah pada perlakuan dengan penyalut pati tapioka termodifikasi Flomax 8 sebesar 26,69%. Perbedaan kelarutan ini disebabkan karakteristik awal dari 2 jenis penyalut ini berbeda, maltodekstrin memiliki sifat lebih mudah larut daripada pati tapioka termodifikasi Flomax 8. Hal ini berpengaruh terhadap kelarutan bubuk vanili yang dihasilkan.
VI. Pengaruh jenis penyalut, konsentrasi penyalut dan rasio ekstrak vanili dengan penyalut terhadap rendemen, aw, kelarutan dan retensi vanilin
selama pengeringan produk ekstrak vanili terenkapsulasi (bubuk vanili)
Dari penelitian tahap II, diketahui jenis dan komposisi penyalut tidak berpengaruh nyata terhadap aw dan kadar vanilin, tetapi berpengaruh nyata
terhadap kelarutan. Berdasarkan penelitian tahap II, maka dua penyalut yang dipilih yang memberikan kelarutan tertinggi yaitu maltodekstrin dan campuran maltodekstrin dan pati tapioka termodifikasi Flomax 8 dengan perbandingan 2 : 1. Hasil penelitian menunjukkan jenis penyalut, konsentrasi penyalut dan rasio antara ekstrak vanili dengan penyalut memberikan hasil yang berbeda terhadap rendemen, aw, kelarutan, kadar vanilin dan recovery vanilin bubuk vanili.
Rendemen
Flomax 8 (2 : 1), dengan konsentrasi penyalut 10% dan rasio ekstrak vanili dengan penyalut 3 : 1. Rendemen paling rendah sebesar 18,68% didapat dari perlakuan menggunakan bahan penyalut maltodekstrin, dengan konsentrasi penyalut 30% dan rasio ekstrak vanili dengan penyalut 3 : 2.
Dari hasil sidik ragam menunjukkan bahwa jenis penyalut, konsentrasi bahan penyalut dan rasio ekstrak vanili dengan penyalut berpengaruh nyata terhadap rendemen bubuk vanili yang dihasilkan (Lampiran 11). Hasil uji lanjut Duncan menunjukkan rendemen bubuk vanili dengan penyalut maltodektrin dan maltodekstrin dan pati tapioka termodifikasi Flomax 8 (2 : 1) memiliki perbedaan yang nyata (Lampiran 12). Perlakuan dengan jenis penyalut maltodekstrin dan pati tapioka termodifikasi Flomax 8 menghasilkan rendemen yang lebih besar dibandingkan dengan perlakuan menggunakan jenis penyalut maltodektrin saja. Hal ini disebabkan karakteristik awal dari kedua sifat penyalut ini berbeda. Pati termodifikasi dengan DE tertentu cenderung membentuk kerak pada dinding tabung pengering (Che Man et al. 1999). Hal ini dapat menyebabkan rendahnya rendemen yang dihasilkan dengan menggunakan spray drying.
31,80
Hasil uji lanjut Duncan pengaruh konsentrasi terhadap rendemen, didapatkan hasil konsentrasi penyalut (10, 20, 30%) dan rasio ekstrak vanili dengan penyalut (3 : 2, 2 : 1, 3 : 1) menghasilkan nilai yang berbeda nyata terhadap rendemen bubuk vanili (Lampiran 13 dan Lampiran 14). Dari hasil penelitian, semakin tinggi konsentrasi jenis penyalut dan semakin besar rasio penyalut terhadap ekstrak vanili semakin rendah rendemen yang dihasilkan, hal ini disebabkan karena viskositas bahan yang akan dikeringkan semakin tinggi. Menurut Young et al. (1993), viskositas yang terlalu tinggi mengganggu proses atomisasi dan mengakibatkan pembentukan droplet yang besar dan panjang yang menyebabkan kecepatan pengering berkurang sehingga rendemen mikrokapsul berkurang.
Menurut Hustiany (2006), semakin besar jumlah penyalut semakin besar pula rendemen produk flavor terenkapsulasi. Hal ini disebabkan jumlah penyalut sangat berperan terhadap rendemen produk flavor terenkapsulasi. Sementara itu, air dan komponen flavor ada yang menguap selama proses pengeringan dan peranannya kecil terhadap rendemen produk flavor terenkapsulasi. Meskipun peningkatan konsentrasi atau viskositas akan meningkatkan rendemen mikrokapsul tetapi masing-masing bahan mempunyai batas maksimal untuk peningkatan viskositas sampai akhirnya tidak tidak terjadi peningkatan viskositas lagi, bahkan peningkatan viskositas akan menurunkan rendemen mikrokapsul (Bhandari et al. 1992).
Nilai aw
Nilai aw bubuk vanili dari berbagai perlakuan berkisar 0,437 - 0,451
(Gambar 9). Dari hasil sidik ragam didapatkan hasil bahwa jenis penyalut, konsentrasi bahan penyalut dan rasio ekstrak vanili dengan penyalut tidak berpengaruh nyata terhadap aw bubuk vanili yang dihasilkan (Lampiran 15).
Kelarutan
berpengaruh nyata terhadap kelarutan bubuk vanili (Lampiran 19 dan Lampiran 20). Bubuk vanili dengan penyalut maltodekstrin memiliki kelarutan lebih tinggi dibanding dengan menggunakan bahan penyalut maltodekstrin dan pati tapioka termodifikasi Flomax 8. Hal ini disebabkan sifat asal dari bahan penyalut, maltodekstrin memiliki kelarutan lebih tinggi dibanding pati tapioka termodifikasi Flomax 8. Hal ini berpengaruh terhadap kelarutan bubuk vanili yang dihasilkan.
0,437 0,451
Gambar 9 Aw bubuk vanili dari tiap perlakuan
78,06
Rasio ekstrak vanili dengan penyalut Rasio ekstrak vanili dengan penyalut
Maltodekstrin Maltodekstrin : Flomax 8
Kadar vanilin
Kadar vanilin bubuk vanili dari berbagai perlakuan berkisar 0,40 - 2,17 g/100g (Gambar 11). Kadar vanilin tertinggi didapat dari perlakuan bubuk vanili dengan penyalut maltodekstrin dan pati tapioka termodifikasi (2 : 1), konsentrasi penyalut 30% dan rasio ekstrak vanili dengan penyalut (3 : 1). Dari hasil sidik ragam didapatkan bahwa jenis penyalut, konsentrasi bahan penyalut dan rasio ekstrak vanili dengan penyalut berpengaruh nyata terhadap kadar vanilin bubuk vanili(Lampiran 23).
Gambar 11 Kadar vanilin dari tiap perlakuan