i
KOMPOSISI ISOTOP STABIL MAKROZOOBENTOS
DAN PRODUSEN PRIMER DI EKOSISTEM LAMUN
DAN MANGROVE
Mardiansyah
C 551090111
PROGRAM STUDI ILMU KELAUTAN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ii
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis KomposisiIsotop Stabil
Makrozoobentosdan Produsen Primer diEkosistemLamundanMangroveadalah
karya saya sendiri dengan arahan komisi pembimbing dan belum diajukan dalam
bentuk apa pun kepada perguruan tinggi mana pun.Sumber informasi yang
berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari
penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka
di bagian akhir tesis ini.
Bogor, Agustus 2012
iii
ABSTRACT
MARDIANSYAH. The Composition of Stable Isotopes of Macrozoobenthos and Primary Producer withinSeagrass and Mangrove Ecosystem. Under supervision of TRI PRARTONO and YUSLI WARDIATNO.
Seagrass and mangrove some of the premier producers become food sources for biota that lives in mangrove and seagrass ecosystems. To indentify those potential food sources in mangrove and seagrass stable isotopes of δ13C
and δ15
N were measured from primary producers and macrobenthos. The research was conducted in two places, the seagrass ecosystem in Pari Islands, DKI Jakarta, Indonesia and Manko mangrove ecosystem in Okinawa, Japan. Values of δ13C in Chlamydinae spp. and Haliclona spp.Pari Islands were -13.74 ‰ and -19.82 ‰, for δ15N 5.25 ‰ and 3.97 ‰, respectively. Value of δ13C and
δ15
N from potential food materialof E. acoroides was -5.56 ‰ and 2.41 ‰, and C. rasemosa -17.11 ‰ and 3.31 ‰, respectively. Value of δ13C class gastropod from mangrove Manko ranged -22.58 ‰ to -22.4 ‰ and for δ15N 8 ‰ to 8.6 ‰,
class crustacea had value δ13
C ranged-24.3 ‰ to -21.87 ‰ and for δ15N 10.6 ‰ to 11.5 ‰, respectively. This study show that Chlamydinae spp. didnot consumeseagrass and mangrove materials, but class gastropod and crustacea consumed sediment.
iv
RINGKASAN
MARDIANSYAH. KomposisiIsotop Stabil Makrozoobentosdan Produsen Primer diEkosistemLamun dan Mangrove. Dibimbing oleh TRI PRARTONO dan YUSLI WARDIATNO.
Makrozoobentos yang hidup di ekosistem mangrove dan lamun mendapatkan sumber makanan yang berbeda-beda. Tumbuhan mangrove dan lamun merupakan salah satu produsen primer yang menjadi sumber makanan. Analisis isotop stabil (SIA) digunakan untuk mengkaji potensi sumber makanan di ekosistem mangrove di Jepang dan ekosistem lamun di Indonesia seperti daun mangrove, daun lamun, sedimen, spons, makroalga dan makrozoobentos.
Tujuan dari penelitian ini yang pertama adalah mengidentifikasi nilai isotop δ13C dan δ15
N pada sumber makanan dan makrozoobentos di ekosistem mangrove dan lamun.Kedua, mengidentifikasi sumber makanan makrozoobentosdi ekosistem mangrove dan lamun. Penelitian ini dilakukan di dua tempat yaitu ekosistem lamun di Pulau Pari, DKI Jakarta, Indonesia pada bulan Juni dan ekosistem mangrove Manko, Okinawa Jepang yang dilaksanakan pada bulan Agustus 2011. Metode yang digunakan untuk pengambilan biota adalah metode acak (random sampling) pada setiap stasiun dengan biota yang dikoleksi adalah makrozoobentos dan potensi sumber makanan kemudian di analisis dengan menggunakan isotop stabil.
Hasil penelitian di ekosistem lamun Pulau Pari, nilai isotop karbon (δ13C) dan nitrogen (δ15
N) pada konsumen seperti kerang (Chlamydinae spp.) adalah -13,74 ‰ dan 5,25 ‰. Pada produsen primer, nilai isotop karbon (δ13C) dan nitrogen (δ15
N) seperti daun lamun (E. acoroides) adalah -5,56 ‰ dan 2,41 ‰, makroalga (C. rasemosa) adalah -17,11 ‰ dan 3,31 ‰, spons (Haliclona spp.) adalah -19,82 ‰ dan 3,97 ‰, dan makroalga Sargassum spp. -13,6 ‰ dan 3,10 ‰, secara berurutan. Nilai isotop karbon dan nitrogen konsumen di ekosistem mangrove dari kelas gastropoda seperti Cerithidea spp. adalah -22,4 ‰ dan 8,6 ‰, C. mustelina adalah -25,06 ‰ dan 8 ‰, P.verruculata adalah -22,58 ‰ dan 8 ‰, untuk kelas krustacea seperti Grapsidae spp. nilai isotop karbon dan nitrogennya adalah -24,3 ‰ dan 10,6 ‰, Uca spp. adalah -21,87 ‰ dan 11,5 ‰. Nilai isotop karbon dan nitrogen dari produsen primer seperti daun mangrove (K.
candel) adalah -29,81 ‰ dan 11 ‰ dan sedimen adalah -24,23 ‰ dan 7,2 ‰, secara berurutan.
v
© Hak cipta milik IPB, tahun 2012
Hak cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tidak merugikan kepentingan yang wajar IPB.
vi
KOMPOSISI ISOTOP STABIL MAKROZOOBENTOS
DAN PRODUSEN PRIMER DI EKOSISTEM
LAMUNDAN MANGROVE
Mardiansyah
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Kelautan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
vii
viii
LEMBAR PENGESAHAN
Judul Tesis : KomposisiIsotop Stabil Makrozoobentosdan Produsen
Primer diEkosistemLamun dan Mangrove
Nama
:
MardiansyahNIM
:
C551090111Disetujui
Komisi Pembimbing
Dr. Ir. Tri Prartono, M.Sc Dr. Ir. Yusli Wardiatno, M.Sc
Ketua Anggota
Diketahui
Ketua Program Studi Ilmu Kelautan
Dekan Sekolah Pascasarjana
Dr.Ir. Neviaty P. Zamani, M.Sc Dr.Ir. Dahrul Syah, M.Sc. Agr
ix PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT yang Maha Pengasih dan
Penyayang karena dengan berkat dan rahmat-Nya penulis dapat menyelesaikan
tesis ini. Tema yang telah diajukan sejak Desember 2010 ini ialah
KomposisiIsotop Stabil Makrozoobentosdan Produsen Primer
diEkosistemLamundanMangrove.
Penulis juga berterima kasih kepada:
1. Orang tua tercinta Ayahanda H. Sayuti dan Ibunda Hj Muslimah, istriku
tercinta Rifqiah Awaliah SS dan anakku M Fahrezy Awliansyah Assuyuti,
Kakakku Sapta Mulyana dan Istri, Adikku Desliana Fajrin, dan Keponakan ku
yang ku sayangi Nida, Adel, dan Aka. Penulis mengucapkan terimakasih
yang sedalam dalamnya atas segala doa, semangat, dan dukungannya
selama penulis melaksanakan studi di IPB.
2. Ketua komisi pembimbing: Dr. Ir. Tri Prartono, M.Sc yang telah mendukung
dan membimbing penulis dengan kehangatan seorang bapak sekaligus
pendidik, sehingga penulis mendapatkan banyak ilmu dan dapat
menyampaikannya dalam suatu tulisan.
3. Anggota komisi pembimbing: Dr. Ir. Yusli Wardiatno, M.Scuntuk nasehat,
teguran, diskusi hangat, argumentasi, dan kegiatan penelitian ke Jepang
sehingga tesis ini menjadi lebih berisi melampaui perkiraan penulis pada saat
pertama kali topik ini diajukan.
4. Terimakasih kepada Dr. Ir. Neviaty P. Zamani, M.Sc sebagai ketua program
studi yang telah memberikan ilmu kepada penulis selama kuliah di IPB.
5. Prof. Dr. Makoto Tsuchiya atas bimbingan, arahan, dan masukan selama
penulis melakukan penelitian di Universitas Ryukyus, Okinawa, Jepang.
6. Dr. Hiroyuki Fujimura yang telah memberikan izin dan membantu dalam
menganalisis sampel di Departemen Kimia, Universitas Ryukyus, Okinawa,
Jepang.
7. Dr. Ir. Isdradjad Setyobudiandi, M.Sc sebagai penguji tamu pada ujian akhir
tesisyang telah memberikan masukan berharga dan semangat baik pada
saat ujian maupun pada saat penulis melaksanakan penelitian.
8. Kementrian Agama Dirjen Pendidikan Islam yang telah memberikan Bantuan
x
9. Teman-teman IKL 2009: Muliari, Kaharuddin, Maria Ulfah, Khoirol Imam
Fatoni, Wahyu A’idin Hidayat, Lumban Nauli Lumban Touruan, Achmad
Zamroni, Anna Ida Sunaryo, Dian Respati Widianari, Emmy Syafitri, Reza
Cordova, Yulianto Sutedja, Yuliana Fitri Syamsuni, Citra Satrya Utama Dewi
dan Heidi Retnoningtyas. Terima kasih atas dukungan, semangat, bantuan,
canda, SMS, telepon, kerjasama, konflik, dan kebersamaannya. Untuk editor,
terima kasih kepada Patih Megawanda Gulam, M.Si.
10. Terima kasih teman-teman baristar yang telah memberikan tempat, canda
dan tawanya selama ini.
11. Terima kasih kepada lingkungan ku, baik yang hidup atau benda.
Penulis menyadari, hasil ini belum memadai karena keterbatasan dana dan
waktu, oleh karenanya masukan kritik dan saran sangat penulis hargai. Penulis
mengharapkan, semoga tulisan ini dapat bermanfaat untuk memacu
perkembangan tentang mengetahui manfaat dari sebuah makhluk hidup di muka
bumi ini.
Bogor, Agustus2012
xi
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada 10 Maret 1985 dari pasangan Bapak
Sayuti dan Ibu Muslimah. Penulis merupakan anak keduadari tiga bersaudara.
Setelah lulus pendidikan menengah atas di MAN Sukamanah, pada tahun 2003
selanjutnya penulis melanjutkan pendidikan tinggi pada program studi S1 Biologi
Fakultas Sains dan Teknologi di Universitas Islam Negeri Jakarta dan lulus pada
tahun 2008. Selanjutnya, pada tahun 2009 penulis melanjutkan pendidikan
strata-2 (S2) pada Program Studi Ilmu Kelautan, Sekolah Pascasarjana, Institut
xii
1.2. Kerangka Pemikiran ... 2
1.3. Perumusan Masalah ... 3
1.4. Tujuan dan Manfaat ... 5
2. TINJAUAN PUSTAKA ... 6
2.1. Ekosistem Mangrove dan Lamun ... 6
2.2. Bioekologi Makrozoobentos ... 9
2.3. Isotop Stabil ... 13
2.3.1. Sifat Kimiawi Isotop Stabil ... 13
2.3.2. Manfaat Isotop Stabil ... 14
2.3.3. Siklus Isotop Stabil di Laut ... 16
3. METODE PENELITIAN ... 20
3.1. Waktu dan Lokasi Penelitian ... 20
3.2. Alat dan Bahan ... 21
3.3. Pengambilan Data ... 22
3.3.1. Menentukan Stasiun Pengamatan ... 22
3.3.2. Koleksi Sampel ... 22
3.4. Preparasi Isotop Stabil ... 24
3.4.1. Preparasi Makrozoobentos ... 24
3.4.2. Preparasi Sedimen ... 24
3.4.3. Preparasi Mangrove, Lamun, makroalga, dan Spons ... 24
3.5. Analisis Isotop Stabil ... 25
3.6. Analisis Data ... 26
4. HASIL DAN PEMBAHASAN ... 27
4.1. Kondisi Umum Lokasi Penelitian ... 27
4.1.1. Lokasi Penelitian di Pulau Pari ... 27
4.1.2. Lokasi Penelitian di Ekosistem Mangrove Manko... 27
4.2. Isotop Karbon dan Nitrogen Sumber Makanan ... 29
4.2. Isotop Karbon dan Nitrogen Makrozoobentos ... 33
4.3. Isotop Stabil Makrozoobentos dan Sumber Makanan ... 36
5. SIMPULAN DAN SARAN ... 42
5.1. Simpulan ... 42
5.2. Saran ... 42
DAFTAR PUSTAKA ... 40
xiii
DAFTAR TABEL
No Hal
1. Alat dan bahan penelitian... 21
2. Rerata nilai (SD) δ15N dan δ13C (‰) potensi sumber makanan di ekosistem lamun Pulau Pari ... 29
3. Nilai kisaran δ13C dan δ15N potensi sumber makanan di ekosistem lamun ... 30
4. Rerata nilai (SD) δ15N dan δ13C (‰)potensi sumber makanan di ekosistem mangrove Manko ... 31
5. Nilai kisaran δ13C dan δ15N potensi sumber makanan di ekosistem mangrove ... 31
6. Rerata nilai (SD) δ15N dan δ13C (‰)makrozoobentos di ekosistem lamunPulau Pari ... 33
7. Nilai kisaran δ13C dan δ15NChlamydinaespp. di ekosistem lamun ... 33 8. Rerata nilai (SD) δ15N dan δ13C (‰)makrozoobentosdi ekosistem
mangrove Manko ... 34
9. Nilai kisaran δ13C dan δ15Nmakrozoobentos di ekosistem mangrove ... 35 10. Nilai asimilasi rasio δ13C dan δ15N Chlamydinae spp. dengan sumber
makan di ekosistem lamun Pulau Pari ... 36
xiv
DAFTAR GAMBAR
No Hal
1. Kerangka pemikiran penelitian ... 3
2. Distribusi global ekosistem mangrove (Polidoro et al. 2010) ... 6
3. Keanekaragaman lamun di dunia (Spalding et al. 2003) ... 8
4. Jaring-jaring makanan di wilayah intertidal (Karleskint et al. 2010) ... 11
5. Ilustrasi jaring-jaring makanan di ekosistem lamun dan mangrove (a. Kneer et al. 2008; b. Marguillier et al. 1997; c. Zieman et al. 1984; d. Nordhaus and Wolff 2007; e. Meziane and Tsuchiya 2000; f. Sheaves and Molony 2000; g. Tewfik et al. 2005) ... 13
6. Siklus isotop stabil karbon (δ 13C) di alam (Peterson and Fry 1987) ... 16
7. Siklus isotop stabil nitrogen (δ 15N) di alam (Peterson and Fry 1987) ... 18
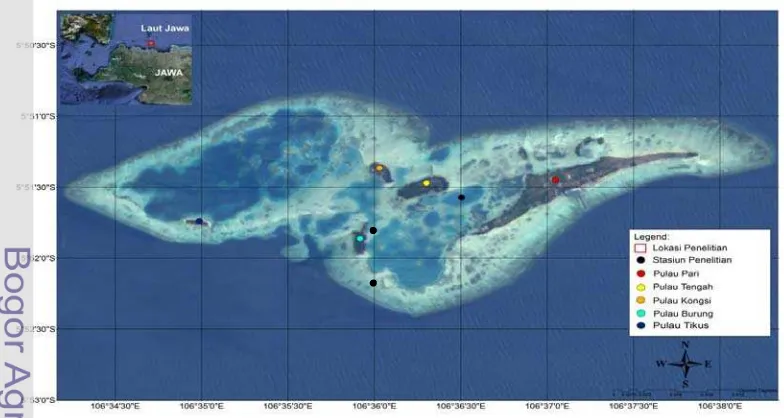
8. Peta lokasi penelitian dan pengamatan pengamatan Pulau Pari ( ) ... 20
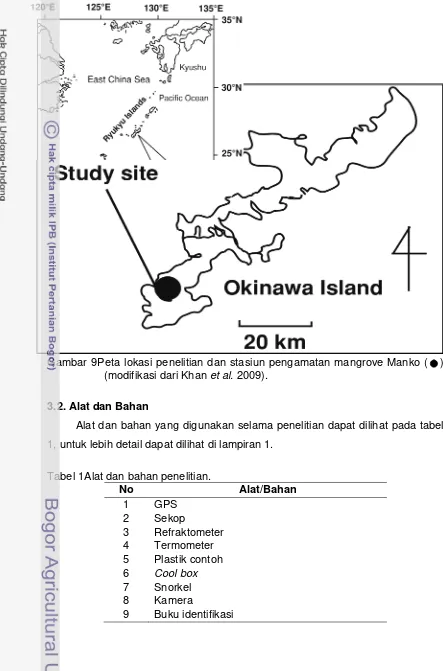
9. Peta lokasi penelitian dan stasiun pengamatan mangrove Manko ( ) ... 21
10. Nilai rasio isotop stabil (Error bars mean± SD; n=3) Chlamydinae spp. dan produsen primer di ekosistem lamun Pulau Pari ... 35
xv
DAFTAR LAMPIRAN
No Hal
1. Alat dan bahan penelitian ... 54
2. Analisis deskriftif δ13C dan δ15N ekosistem lamun Pulau Pari ... 56
3. Uji normalitas (Kolmogorov-Smirnov) data δ13C dan δ15N ekosistem lamun Pulau Pari ... 57
4. Analisis ANOVA δ13C dan δ15N Pulau Pari ... 58
5. Uji Tukeybiota δ13C dan δ15N Pulau Pari ... 59
6. Analisis deskriftif δ13C dan δ15N produsen ekosistem mangrove Manko ... 60
7. Analisis deskriftif δ13C dan δ15N konsumen ekosistem mangrove Manko... 61
8. Uji normalitas (Kolmogorov-Smirnov) data δ13C dan δ15N ekosistem mangrove Manko ... 62
9. Analisis ANOVA δ13C dan δ15N konsumen dan produsen ekosistem mangrove Manko ... 63
10. Uji Tukey δ15N konsumen ekosistem mangrove Manko ... 64
11. Uji Tukey δ13C konsumen ekosistem mangrove Manko ... 65
12. Hasil pengambilan biota di ekosistem lamun dan mangrove ... 66
1
1. PENDAHULUAN
1.1. Latar Belakang
Ekosistem mangrove dan lamun memiliki fungsi diantaranya sebagai
habitat dan penyedia sumber makanan yang dimanfaatkan oleh
makrozoobentos, seperti kelas gastropoda, bivalvia, dan krustacea.
Makrozoobentos yang tergolong kedalam filum moluska dan arthropoda secara
ekologi berfungsisebagai sumber makanan predator dalam sebuah rantai
makanan dan secara ekonomi sebagai sumber makanan manusia.
Linse et al. (2006) wilayah Asia seperti negara Indonesia dan Jepang
merupakan daerah terbesar distribusi kelas bivalvia dan gastropoda. Lebih lanjut
Linse et al. (2006) menyatakan bahwa kelas bivalvia di Indonesia mencapai
sekitar 1200 spesies, sedangkan kelas gastropoda di Jepang berkisar antara 200
sampai dengan 600 spesies. Kelas bivalvia menjadi jenis komuditas secara
komersial mempunyai nilai yang tinggi seperti kerang dari jenis scallop di
Indonesia (Brand 2006).
Konservasi merupakan kegiatan menjaga kelestarian dan keseimbangan
alam. Salah satu kegiatan konservasi biota laut adalah dengan analisis sumber
makanan. Analisis sumber makanan makrozoobentos di ekosistem mangrove
dan lamun menggunakan 4 metode, seperti analisis gut content/isi perut, fatty
acid, isotop stabil, dan DNA molekuler. Hasil penelitian sebelumnya tentang
sumber makanan makrozoobentos yang menggunakan ke empat metode
tersebut di ekosistem mangrove, diketahui bahwa kelas bivalvia berasal dari fito,
zooplankton, dan detritus (Hari 1999), sumber makanan kelas gastropoda
berasal dari mikroalga, zooplankton, mangrove, dan lain-lain (Alfaro 2008), dan
sumber makanan dari kelas krustacea yaitu kepiting berasal dari daun mangrove,
diatom (Meziane et al. 2002), materi tumbuhan yang tidak teridentifikasi, dan
material biota (Nordhaus dan Wolff 2007). Sumber makanan, kelas bivalvia di
ekosistem lamun berasal dari partikel organik terlarut (POM) (Kasai et al. 2004),
daun lamun, fitoplankton (Vonk et al. 2008), dan detritus, mikro, dan
mesozooplankton (Davenport et al. 2011).Hasil penelitian di atas menunjukkan
bahwa sumber makanan di ekosistem mangrove dan lamun dipengaruhi dari
dalam dan luar ekosistem. Hal ini menunjukkan bahwa ekosistem pesisir seperti
2
metode analisis sumber makanan yang dapat mengetahui asal mula sumber
makanan yaitu isotop stabil.
1.2. Kerangka Pemikiran
Secara makro melalui ketiga fungsinya ekosistem pesisir merupakan
penopang bagi produktifitas perairan. Keseimbangan dari ketiga aspek tersebut
dalam penelitian ini menganalisa kebutuhan makrozoobentosuntuk
memanfaatkan ekosistem sebagai sumber makanan. Beberapa hal yang
diperhatikan ialah: potensi sumber makanan yang ada di ekosistem tersebut,
seperti tumbuhan terestrial (serasah), tumbuhan asosiasi (epifit), lamun,
plankton, alga, dan mikroorganisme, menjadi fokus dalam menentukan faktor
yang mempengaruhi ketersedian dari sumber makanan di ekosistem tersebut.
Adapun beberapa penyebabnya adalah seperti, zonasi ekosistem pesisir dan
faktor fisik (pasut, masukkan dari daratan, dan iklim).
Pengaruh dari dalam dan luar ekosistem pesisir serta pengaruh faktor fisik,
kimia, dan biologi menyebabkan ekosistem mangrove dan lamun menjadi
kompleks untuk mengetahui informasi potensi sumber makanan yang di asimilasi
makrozoobentos. Oleh karena itu diperlukan pendekatan metode untuk
mengetahui organisme autotrof atau potensi sumber makanan
makrozoobentossebagai sumber makanan di ekosistem pesisir.
Terdapat 4 metodeanalisis sumber makanan makrozoobentos di ekosistem
mangrove dan lamun telah dilakukan di beberapa penelitian sebelumnya seperti
melihat langsung di lapangan dan di sistem pencernaan (Hari 1999; Nordhaus
dan Wolff 2007;Davenport et al. 2011; biomarker (fatty acid) (Meziane et al.
2002), isotop stabil (Alfaro 2008; Kasai et al. 2004; dan Vonk et al. 2008) dan
DNA molekuler(Blankenship dan Yayanos 2005).Metode pengamatan sumber
makanan di lapangan dan di sistem pencernaan telah ditemukan beberapa
kekurangan seperti, terdapat bias dari data yang dihasilkan, tidak
merepresentasikan hasil secara keseluruhan, tidak ada keterangan dari organic
terlarut yang biasa digunakan pada ikan (Pasquaud et al. 2007), terdapat
misleading (menyesatkan) pada informasi isi usus jenis kerang karena tidak
mampu membedakan bahan yang tidak dicerna (Kasai et al. 2006). Metode ini
sulit diterapkan bagi organisme kecil, sedangkan metode pengamatan langsung
3
Metode biomarker seperti penanda asam lemak (fatty acid) dan metode
DNA barcode merupakan metode yang dapat digunakan untuk mengetahui asal
sumber makanan. Kekurangan pada metode ini terletak pada
ketidakmampuannya dalam menghitung suatu tingkatan dari tropik level. Menurut
Pasquaud et al. (2007) metode isotop stabil merupakan metode yang dapat
membedakan asal mula organik terlarut, membedakan dari jaring-jaring
makanan, dan dapat menghitung suatu tingkatan organisme dalam sebuah tropik
level di rantai dan jaring-jaring makanan. Selain itu metode isotop stabil juga
mampu menganalisis sumber makanan pada makrozoobentos.Teknik ini belum
pernah dilakukan di ekosistem mangrove Manko Jepang dan juga di ekosistem
lamunmakrozoobentosIndonesia. Hal tersebut merupakan pertimbangan
perlunya dilakukan penelitian tentang analisis sumber makanan makrozoobentos.
Metode isotop stabil telah berhasil merunut dan menjelaskan sumber
makanan yang ada di ekosistem perairan darat dan laut. Sumber makanan yang
diasimilasi makrozoobentos pada kelas gastropoda, bivalvia, dan krustacea
dianalisis dengan isotop stabil merupakan dasar dari penelitian ini. Kerangka
pemikiran penelitian dapat dilihat pada Gambar 1.
1.3. Perumusan Masalah
Meningkatnya kebutuhan manusia secara langsung berdampak pada
eksploitasi sumber daya alam. Salah satu kerusakan akibat eksploitasi tersebut
terjadi pada ekosistem mangrove dan lamun yang menjadi habitat
makrozoobentos. Eksistensi biota seperti makrozoobentos tergantung pada
ketersediaan sumber makanan dari ekosistem mangrove dan lamun. Dengan
adanya kerusakan habitat, berakibat luas terutama pada sumber makanan dari
makrozoobentos.
Sumber makanan merupakan tropik level pertama atau sebagai produsen
primer dalam sistem rantai makanan. Produsen primer di ekosistem mangrove
dan lamun berasal dari dalam dan luar ekosistem, seperti tumbuhan mangrove,
tumbuhan epifit, bentik alga, filamen alga, tumbuhan lamun, makroalga,
fitoplankton, dan mikroorganisme. Produsen primer tersebut berfungsi penting
sebagai sumber makanan makrozoobentos, sedangkan fungsi makrozoobentos
sebagai konsumen pertama dalam rantai makanan.Sistem rantai makanan
apabila terputus atau hilang, maka akan merubah atau bahkan dapat
4
Sumber makanan pada makrozoobentos di ekosistem lamun dan
mangrove memiliki kesulitan untuk di identifikasi. Hal ini dikarenakan ekosistem
lamun dan mangrove merupakan zona yang kompleks yang memiliki masukkan
atau percampuran material dari daratan dan daratan, sehingga sulit diketahui
apakah sumber makanan makrozoobentos berasal dari dalam atau luar
ekosistem lamun dan mangrove. Selain itu, bentuk dan ukuran sistem
pencernaan dari makrozoobentos kecil sehingga sulit untuk mengetahui material
sumber makanan.Untuk itu dibutuhkan identifikasi untuk mengetahui sumber
makanan makrozoobentos demi kelangsungan makrozoobentos dengan metode
isotop stabil.
Isotop stabil merupakan salah satu metode analisis di bidang ekologi untuk
mengetahui rantai dan jaring-jaring makanan pada sistem akuatik darat dan laut
dan sistem metabolisme biota. Isotop stabil digunakan untuk menganalisis
sumber makanan pada semua tingkatan tropik (trophic level). Sumber makanan
4
5 1.4. Tujuan dan Manfaat
1. Menentukan komposisi isotop δ13C dan δ15
2. Menduga sumber makanan (potential food sources) yang diasimilasi
makrozoobentos dengan isotop stabil di Pulau Pari, DKI Jakarta,
Indonesia dan di ekosistem mangrove Manko, Okinawa, Jepang.
N dari produsen primer dan
makrozoobentos di Pulau Pari, DKI Jakarta, Indonesia dan di ekosistem
mangrove Manko, Okinawa, Jepang.
Manfaat dari hasil penelitian ini diharapkan memberikan informasi bagian
kecil dari proses rantai makanan di ekosistem mangrove dan lamun, dan untuk
6
2. TINJAUAN PUSTAKA
2.1. Ekosistem Mangrove dan Lamun
Mangrove merupakan spesies tumbuhan sejati atau tidak sejati yang
beradapatasi dengan perairan laut. Mangrove kebanyakan di dominansi oleh
tumbuhan sejati yang terdapat di habitat tepi pantai atau estuaria. Mangrove
didefinisikan sebagai pohon-pohon kayu dan semak belukar yang berkembang di
habitat mangrove (Hogarth 2007) yang berada di pantai tropis dan subtropis
yang didominansi oleh beberapa jenis pohon yang mampu tumbuh dan
berkembang pada daerah pasang-surut (Bengen 2004). Mangrove di Indonesia
tersebar diseluruh Pulau dengan memiliki area mangrove yang terbesar di dunia
yaitu sekitar 3.112.989 juta m2 atau 22,6% total luasan di dunia (Giri et al. 2010) dan mangrove di kawasan Asia tenggara sekitar 76% (Hutomo dan Moosa 2005)
yang secara global memiliki keanekaragamanan yang paling tinggi (Gambar 2;
Polidoro et al. 2010).
Gambar 2 Distribusi global ekosistem mangrove (Polidoro et al. 2010).
Mangrove di dunia terdiri dari 20 genus (Hogarth 2007) dengan 70 spesies
yang terdiri dari pohon, semak, dan pakis (Ricklefs et al. 2006). Indonesia
memiliki 202 jenis, dengan 33 jenis mangrove sejati dan 10 jenis perdu (Noor et
al. 2006) dengan tipe habitat berbeda-beda. Habitat mangrove berdasarkan tipe
substratnya, mangrove berada di substrat berupa pasir, berlumpur, lempung,
campuran pecahan karang, tergenang air laut secara berkala, menerima
pasokan air tawar yang cukup, dan terlindung dari gelombang besar dan arus
7
mangrove mempengaruhi sebaran jenis-jenis mangrove. Habitat mangrove
memiliki fungsi baik secara fisik, ekologi, dan sosial-ekonomi terhadap faktor
biotik dan abiotik.
Fungsi ekosistem mangrove secara fisik seperti pelindung dari badai,
pasang surut, dan gelombang untuk masyrakat pesisir dan biota yang ada
(Giesen et al. 2006). Fungsi sosial-ekonomi mangrove secara umum seperti
sumber mata pencaharian masyarakat baik berupa makanan atau wisata. Fungsi
ekologi dari ekosistem mangrove adalah pendukung jaring makanan, penyerap
karbon (Giesen et al. 2006) sumber makanan, tempat memijah, tempat
berkembang biak, dan tempat berlindung bagi biota akuatik dan darat.
Daerah pantai tropis merupakan salah satu tempat tumbuh dan
berkembang tumbuhan mangrove. Karakteristik dari ekosistem mangrove adalah
dapat berkembang maksimum pada daerah-daerah yang bercurah hujan tinggi
atau daerah sungai yang memiliki masukkan air tawar yang cukup untuk
mencegah hipersalin (Nybakken 1992). Selain itu menurut Bengen (2004),
ekosistem mangrove memiliki karakteristik seperti jenis tanah berlempung,
berlumpur, campuran karang atau pasir, daerahnya tergenang air laut secara
berkala, terdapat masukan air tawar dari darat, dan air bersalinitas payau.
Hewan yang ada di ekosistem mangrove berasal dari darat dan laut, baik
hewan vertebrata dan invertebrata yang asli dari mangrove, fakultatif (sebagian),
dan pendatang. Hewan vertebrata yang berasosiasi dengan ekosistem mangrove
seperti dari jenis burung-burung air, ikan, katak, kura-kura, buaya, ular
(Nagelkerken et al. 2008), dan dari jenis mamalia seperti onta (Hogarth 2007),
bekantan, kera ekor panjang, dan kelelawar. Hewan invertebrata yang ada di
ekosistem mangrove seperti zooplankton, sponges, krustacea (udang-udangan),
kepiting, serangga (insekta), gastropoda dan bivalvia (Kathiresan dan Bingham
2001; Hogarth 2007; Nagelkerken et al. 2008). Selain dengan hewan, mangrove
berasosiasi dengan tumbuhan tingkat rendah, tingkat tinggi, dan mikroorganisme
seperti bakteri, fungi, mikroalga, makroalga, dan beberapa tumbuhan epifit lain
seperti anggrek (Kathiresan dan Bingham 2001).
Pada ekosistem pesisir, selain tumbuhan mangrove terdapat tumbuhan
lamun. Tumbuhan lamun merupakan tumbuhan angiospermae yang dapat hidup
di seluruh laut dibandingkan dengan mangrove. Distribusi dari tumbuhan lamun
hampir diseluruh lautan di dunia yang terdiri dari 2 famili yaitu
8
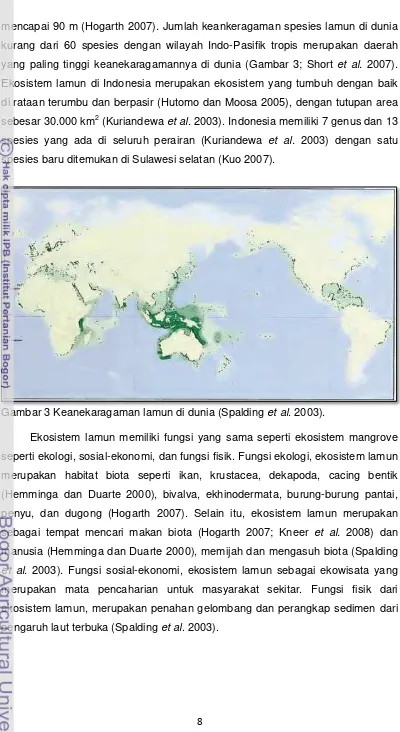
mencapai 90 m (Hogarth 2007). Jumlah keankeragaman spesies lamun di dunia
kurang dari 60 spesies dengan wilayah Indo-Pasifik tropis merupakan daerah
yang paling tinggi keanekaragamannya di dunia (Gambar 3; Short et al. 2007).
Ekosistem lamun di Indonesia merupakan ekosistem yang tumbuh dengan baik
di rataan terumbu dan berpasir (Hutomo dan Moosa 2005), dengan tutupan area
sebesar 30.000 km2 (Kuriandewa et al. 2003). Indonesia memiliki 7 genus dan 13 spesies yang ada di seluruh perairan (Kuriandewa et al. 2003) dengan satu
spesies baru ditemukan di Sulawesi selatan (Kuo 2007).
Gambar 3 Keanekaragaman lamun di dunia (Spalding et al. 2003).
Ekosistem lamun memiliki fungsi yang sama seperti ekosistem mangrove
seperti ekologi, sosial-ekonomi, dan fungsi fisik. Fungsi ekologi, ekosistem lamun
merupakan habitat biota seperti ikan, krustacea, dekapoda, cacing bentik
(Hemminga dan Duarte 2000), bivalva, ekhinodermata, burung-burung pantai,
penyu, dan dugong (Hogarth 2007). Selain itu, ekosistem lamun merupakan
sebagai tempat mencari makan biota (Hogarth 2007; Kneer et al. 2008) dan
manusia (Hemminga dan Duarte 2000), memijah dan mengasuh biota (Spalding
et al. 2003). Fungsi sosial-ekonomi, ekosistem lamun sebagai ekowisata yang
merupakan mata pencaharian untuk masyarakat sekitar. Fungsi fisik dari
ekosistem lamun, merupakan penahan gelombang dan perangkap sedimen dari
9 2.2. Bioekologi Makrozoobentos
Biota bentik (zoobentos) berdasarkan ekologi terbagi kedalam 3 bagian,
yaitu infauna, epifauna, dan epibentos. Infauna merupakan spesies yang seluruh
atau sebagian hidupnya dengan substrat, salah satu contohnya adalah kerang
dan cacing. Spesies infauna dominan di substrat halus dibagian subtidal, dengan
sebagian pada substrat berpasir atau keras. Epifauna merupakan spesies yang
hidup di atas atau menempel di permukaan seperti karang, bintang laut, teritip,
dan sponges. Organisme zoobentos yang ada masuk kedalam kategori epifauna
yaitu sekitar 80%. Habitat epifauna berada di semua substrat, dengan sebagian
kecil epifauna berada disubstrat keras dan sebagian besar kelimpahan dan
keanekaragman epifauna berada disubstrat berbatu dan terumbu karang. Bentik
epibentos merupakan organisme yang hidup didasar laut dan berenang, seperti
kepiting dan udang-udangan. Berdasarkan ukuran organisme bentik terbagi
kedalam 3, yaitu makrofauna, meiofauna, dan mikrofauna (Lalli dan Parsons
2004). Makrobentik merupakan organisme yang masuk kedalam makrofauna.
Makrozoobentos dapat ditemukan di darat, air tawar, dan laut.
Makrozoobentos di ekosistem laut dapat ditemukan dari kedalaman 0 yaitu
supralittoral sampai dengan hadal pelagik. Jenis kelompok makrozoobentos yang
dapat ditemukan seperti dari filum protozoa (foraminifera), porifera, cnidaria,
moluska (bivalvia, gastropoda), ekhinodermata, arthropoda (krustacea), kordata
(tunikata) (Lalli dan Parsons 2004) yang menempati substrat seperti pasir kasar
dan halus, berlumpur sampai dengan berbatu. Kelompok organisme terbanyak
yang pernah dilaporkan pertama adalah arthropoda (kepiting, udang, teritip,
laba-laba laut), dan yang kedua adalah dari kelompok moluska dengan jumlah yang
diketahui lebih dari 200,000 spesies (Castro dan Huber 2003). Menurut
Nybakken (1992) kelompok organisme yang dominan di substrat halus terdiri dari
4 kelompok yaitu kelas krustacea (seperti kepiting), kelas Polychaeta, filum
ekhinodermata, dan moluska seperti bivalvia dan gastropoda.
Makrozoobentos habitat di ekosistem mangrove adalah krustacea
(udang-udangan), kepiting, gastropoda, bivalvia (Hogarth 2007), dan sponges
(Nagelkerken et al. 2008), sedangkan makrozoobentos di habitat ekosistem
lamun sama seperti di mangrove, tetapi terdapat makrozoobentos lainnya yaitu
dari filum ekhinodermata (Hogarth 2007) dan policaeta (Hemminga dan Duarte
10
Makrozoobentos di ekosistem mangrove dan lamun memiliki perbedaan
dalam kebiasaan (tipe) makan dan sumber makanan. Sumber makanan untuk
biota yang hidup di dasar perairan terdiri dari detritus, plankton, mikroorganisme
yang melekat di dasar (Barnes 1987), dan tumbuhan yang ada di lingkungan
pesisir. Berdasarkan kebiasaan makan, makrozoobentos digolongkan menjadi
herbivora, karnivora, omnivor, pemakan bangkai, filter atau suspensionfeeder,
pemakan deposit, dan parasit. Makrozoobentos seperti moluska (gastropoda dan
bivalvia) memiliki kebiasan makan filter atau suspension dan depositfeeder,
sedangkan krustacea seperti kepiting memiliki kebiasaan makan sebagai
pemakan deposit.
Mekanisme cara makan dari biota yang memiliki kebiasaan makan dengan
filter atau suspension feeder adalah dengan memasukkan air kedalam tubuhnya
melalui sifon ventral karena adanya gerakan silium-silium di permukaan tubuh.
Makanan dan oksigen dilewatkan melalui insang dan karena insang berlubang,
maka air terus dilewatkan ke kanal suprabranchial di atas insang, yang akhirnya
keluar melalui sifon dorsal. Partikel-partikel makanan disaring ke luar dan
terperangkap oleh lendir yang menutupi insang. Kemudian silium membawa
makanan dan lendir bersama-sama menuju “palp”, tempat dilakukannya
pemisahan material yang berguna dan tidak berguna. Makanan yang sesuai
akan dibawa memasuki mulut dan dicerna (Soewignyo et al. 2005). Biota yang
memiliki kebiasaan makan sebagai deposit feeder, mekanisme cara makannya
adalah dengan dua cara yaitu memasukkan makanan ke mulut dengan
menggunakan tangan dan tanpa menggunakan tangan yaitu langsung dengan
mulutnya.
Hasil penelitian sebelumnya, menunjukkan bahwa sumber makanan
makrozoobentosfilter atau suspension feeder seperti bivalvia adalah foraminifera
(Broom 1985), plankton dan detritus (Rudi 1999), bentik mikroalga (Yokoyama
dan Ishihi 2003), POM (Kasai et al. 2004; 2006), material lamun (Vonk et al.
2008), fitoplankton (Fukumori et al. 2008b; Yokoyama et al. 2009; Antonio et al.
2010), mikro dan mesozooplankton, partikel-partikel pasir (Davenport et al.
2011). Sumber makanan gastropoda sebagai deposit feeder adalahmakroalga
(Smith et al. 1985), mikroalga epifit di lamun (Kharlamenko et al. 2001),
zooplankton (Alfaro 2008), dan bentik mikroalga, sedimen, tumbuhan epifit, daun
mangrove (Lopes et al. 2009). Sumber makanan makrozoobentos seperti
11
dan Wowor 1989), tumbuhan mangrove (Nordhaus dan Wolff 2007), dan biota
mangrove (Nordhaus et al. 2011). Sumber makanan pada ekosistem intertidal
tidak bergantung pada satu sumber makanan (Alfaro et al. 2006), akan tetapi
bergantung pada beberapa sumber produsen primer yang berasal dari dalam
(autochthonous) atau luar ekosistem (allochthonous). Sumber makanan yang
berbeda-beda dipengaruhi oleh beberapa faktor seperti mikrohabitat, arus,
pasang surut, musim, dan morfologi. Faktor-faktor tersebut yang dapat
menjadikan pola distribusi dari makrozoobentos di suatu habitat. Menurut Lee
(2008) struktur dari kumpulan makrozoobentos dipengaruhi oleh kondisi
lingkungan lokal, ketersediaan bahan organik, dan karakteristik sedimen.
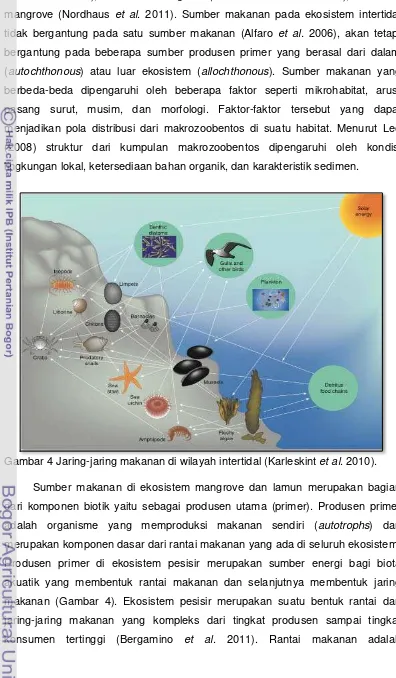
Gambar 4 Jaring-jaring makanan di wilayah intertidal (Karleskint et al. 2010).
Sumber makanan di ekosistem mangrove dan lamun merupakan bagian
dari komponen biotik yaitu sebagai produsen utama (primer). Produsen primer
adalah organisme yang memproduksi makanan sendiri (autotrophs) dan
merupakan komponen dasar dari rantai makanan yang ada di seluruh ekosistem.
Produsen primer di ekosistem pesisir merupakan sumber energi bagi biota
akuatik yang membentuk rantai makanan dan selanjutnya membentuk jaring
makanan (Gambar 4). Ekosistem pesisir merupakan suatu bentuk rantai dan
jaring-jaring makanan yang kompleks dari tingkat produsen sampai tingkat
12
perpindahan organik dari tingkat trofik level ke trofik level lainnya melalui
peristiwa makan memakan yang dengan produsen primer sebagai trofik level
yang pertama (Campbell et al. 2008). Komponen utama dari produsen primer
adalah hasil dari fotosintesis dan respirasi (Gambar 4). Fotosintesis berasal dari
tumbuhan dan alga yang menyerap dari sinar matahari dan pigmen (zat hijau
daun) yang menghasilkan energi berupa karbon, hidrogen, dan oksigen,
sedangkan respirasi yang berasal dari fotosintesis dimanfaatkan oleh bakteri
yang menghasilkan nitrogen. Selain itu, bakteri memberikan kontribusi terhadap
pembentukan dekomposisi lamun dan mangrove, sehingga material dekomposisi
dapat dijadikan sumber makanan (Zieman et al. 1984).
Karbon dan nitrogen dari produsen primer berpindah ke trofik level pertama
yaitu konsumen primer. Konsumen primer di zona intertidal berupa organisme
herbivora seperti dari kelas ikan kecil, bivalvia, gastropoda, atau dari krustacea.
Konsumen primer kemudian dimakan oleh organisme karnivora seperti ikan
besar, yang disebut dengan konsumen sekunder. Organisme karnivora yang
memakan konsumen sekunder disebut dengan konsumen tersier, dan di atas
tersier disebut konsumen kuaterner yaitu konsumen tertinggi dalam tingkat trofik
contohnya manusia (Gambar 5). Menurut Campbell et al. (2008) dalam satu
ekosistem yang membentuk rantai makanan kemudian membentuk hubungan
makan-memakan yang saling menjalin dan selanjutnya membentuk jaring-jaring
makanan.
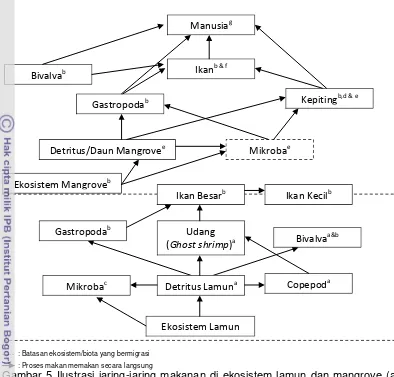
Ekosistem lamun dan mangrove memiliki keterkaitan satu sama lain
(Marguillier et al. 1997; Gambar 5). Biota yang berasal dari ekosistem lamun,
seperti ikan, bermigrasi ke ekosistem mangrove untuk mencari makan dan
memijah. Ikan yang berada di ekosistem lamun memakan material tumbuhan
lamun, ikan-ikan kecil, gastropoda, dan udang. Kemudian ikan bermigrasi ke
ekosistem mangrove dan mencari makan. Sumber makanan ikan yang ada di
ekosistem mangrove seperti material dari tumbuhan mangrove, ikan-ikan kecil,
gastropoda, bivalvia, dan kepiting. Proses makan memakan terjadi secara
13
--- : Batasan ekosistem/biota yang bermigrasi : Proses makan memakan secara langsung
Gambar 5 Ilustrasi jaring-jaring makanan di ekosistem lamun dan mangrove (a. Kneer et al. 2008; b. Marguillier et al. 1997; c. Zieman et al. 1984; d. Nordhaus dan Wolff 2007; e. Meziane dan Tsuchiya 2000; f. Sheaves dan Molony 2000; g. Tewfik et al. 2005).
Karbon dan nitrogen merupakan unsur utama yang dibutuhkan oleh setiap
organisme yang di darat dan laut. Karbon dan nitrogen merupakan salah satu
unsur esensial yang ada di dalam proses kehidupan dan dibutuhkan dalam
jumlah besar (Campbell et al. 2008). Proses perpindahan sumber makanan
merupakan proses satu kesatuan dengan perpindahan karbon dan nitrogen.
Sumber karbon dan nitrogen dari produsen primer memiliki nilai yang bervariasi
dan dipengaruhi faktor lingkungan seperti fisik, kimia, dan biologi.
2.3. Isotop Stabil
2.3.1. Sifat Kimiawi Isotop Stabil
Isotop adalah unsur bernomor atom sama, tetapi memiliki jumlah neutron
14
(radioaktif) (Hoefs 2009). Isotop stabil didefinisikan sebagai elemen isotop yang
stabil secara aktif dan tidak membusuk (decay) dan tidak termasuk radioaktif
(Sulzman 2007). Menurut Hoefs (2009) sejauh ini jumlah isotop stabil di alam
yaitu 300, sedangkan isotop tidak stabil 1.200.
Karbon yang utama memiliki fraksi yang besar di alam berupa isotop
12 (98,89%), fraksi karbon yang rendah (1,11%) terdapat pada
karbon-13. Nitrogen yang berlimpah dalam bentuk isotop nitrogen-14, sedangkan
nitrogen yang rendah adalah nitrogen-15 (0,36%). Sulfur memiliki 4 bentuk stabil,
yaitu sulfur-32 yang banyak ditemukan (95,02%), sulfur-34 (4,21%), sulfur-33
(0,75%), dan fraksi sulfur yang kecil adalah sulfur-36 (0,02%) (Ehleringer dan
Rundel 1989). Isotop stabil berkembang menjadi salah satu alat analisis atau
metode sidik jari (finger print) yang digunakan pada bidang geologi, kimia, dan
biologi yang dikenal dengan stable isotope analysis (SIA).
2.3.2. Manfaat Isotop Stabil
Pada bidang biologi, analisis isotop stabil digunakan untuk studi ekologi
dan lingkungan, seperti untuk mengetahui sumber dan jaring-jaring makanan,
sirkulasi di biosfer, kontaminasi perairan, pola migrasi nutrient dan hewan, input
nutrien, ukuran tubuh spesies (Jardine et al. 2003; Fry 2006), mengetahui
partikel-partikel mangsa (prey) yang masuk di pemangsa (predator),
mengidentifikasi sumber polutan, mengetahui proses-proses penilaian nitrifikasi,
dan estimasi rata-rata C di tanah (Sulzman 2007).
Menurut Jardine et al. (2003) terdapat 3 elemen yang digunakan pada
stable isotope untuk ekologi yaitu karbon, nitrogen, dan sulfur. Elemen yang
banyak digunakan untuk ekosistem laut adalah karbon dan nitrogen (Carabel et
al. 2006). Dalam bidang ekologi, nilai isotop stabil pada karbon digunakan untuk
membedakan komponen sumber karbon produsen primer yang diasimilasi oleh
tingkat konsumen yang lebih tinggi (Peterson dan Fry 1987) dan untuk
mengetahui proses metabolisme di tubuh biota invertebrata (Paulet et al. 2006).
Asimilasi karbon dan nitrogen oleh konsumen disebut dengan fraksinasi atau
perpindahan karbon dan nitrogen (Δδ13C dan Δδ15N) (DeNiro dan Epstein 1978, 1981; Dubois et al. 2007). Isotop stabil karbon di konsumen memiliki nilai yang
sama atau merefleksikan dari sumbernya makanannya (DeNiro dan Epstein
1978), sama seperti dengan karbon, nitrogen pada hewan dapat memberikan
informasi dari komposisi nitrogen konsumen yang sama dengan isotop nitrogen
15
lebih sering digunakan pada tingkatan trofik dikomunitas (Wada et al. 1991),
struktur tropik di ekosistem akuatik (Minagawa dan Wada 1984) atau
menggambarkan jaring-jaring makanan (Vonk et al. 208) dan untuk mengetahui
proses metabolisme biota laut (Lorrain et al. 2002). Oleh karena itu, isotop
karbon digunakan untuk mengetahui atau merunut sumber makanan pada
konsumen, sedangkan isotop nitrogen digunakan untuk mengetahui dan
menghitung tingkatan konsumen di tropik level dalam rantai dan jaring-jaring
makanan.
Analisis isotop stabil merupakan salah satu metode yang digunakan untuk
mengetahui dinamika jaring makanan di sistem akuatik, pola dan sumber bahan
organik pada biota perairan darat dan laut seperti di ekosistem mangrove
(Bouillon et al. 2002;Hsieh et al. 2002) dan lamun (Lepoint et al. 2004). Selain itu,
terdapat metode lain untuk mengetahui pola dan sumber bahan organik pada
hewan invertebrata laut seperti yaitu pengamatan di lapangan, analisis isi usus
(gut content), biomarker seperti asam lemak (fatty acid)(Dalsgaard et al. 2003)
atau dengan metode DNA (Blankenship dan Yayanos 2005).Metode isotop stabil
dalam merunut sumber makanan atau menghitung tropik level memiliki
keuntungan seperti mengetahui sumber-sumber organik terlarut, mengetahui
dasar atau awal dari jaring-jaring makanan, dan dapat menghitung tropik level di
rantai atau jaring-jaring makanan (Pasquaud et al. 2007).
Metode dengan menggunakan pengamatan pada sistem pencernaan
merupakan metode yang mudah (Alfaro 2008), akan tetapi hanya dapat
digunakan pada ikan dan beberapa krustacea, tetapi metode ini tidak dapat
digunakan pada hewan berukuran kecil, membutuhkan pengujian kembali
(Kaehler dan Pakhomov 2001), masih terdapat bias dan kurang mewakili
keseluruhan (Pasquaud et al. 2007), dan metode yang misleading
(menyesatkan) pada isi usus kerang karena tidak dapat membedakan bahan
ingested yang tidak dicerna (Kasai et al. 2006). Metode pengamatan pola dan
sumber organik di lapangan merupakan metode yang membutuhkan waktu yang
panjang. Pada biota laut seperti makrozoobentos, analisis sumber organik yang
dapat mewakili dan mengetahui sumber organik dapat digunakan analisis isotop
stabil. Menurut Davenport et al. (2011), analisis isotop stabil dapat menjelaskan
organik terlarut yang kompleks dilingkungan kolom perairan dan materi yang
berasosiasi. Selain itu, metode analisis isotop stabil berhasil dalam menjelaskan
16
ekosistem mangrove (Bouillon et al. 2002;Hsieh et al. 2002) dan ekosistem
lamun (Lepoint et al. 2004; Vonk et al. 2008).
Nilai rasio fraksinasi isotop stabil dari karbon dan nitrogen di konsumen
yaitu makrozoobentos, menjadi petunjuk untuk mengetahui asal mula atau aliran
sumber makanan (produsen). Makrozoobentos di zona intertidal memegang
peran penting dalam transfer aliran energi terhadap konsumen teratas atau trofik
yang lebih tinggi di dalam rantai organik. Apabila makrozoobentos hilang atau
berkurang, maka transfer energi karbon dan nitrogen di ekosistem tersebut
terganggu atau menjadi tidak seimbang dan bahkan dapat menyebabkan
kepunahan sehingga pemanfaatan dari fungsi bivalvia tidak dapat dimanfaatkan
kembali oleh manusia (konsumen teratas) sebagai fungsi sosial-ekonomi dan
ekologi.
2.3.3. Siklus Isotop Stabil di Laut
Variasi isotop dapat ditemukan dari material dengan klasifikasi proses yang
berbeda-beda, seperti reaksi dan perbedaan sumber seperti sumber dari luar
angkasa atau bumi (Hoefs 2009). Proses reaksi dari isotop stabil di bumi
terdapat di seluruh material yang merupakan bagian dari siklus di alam. Siklus
isotop stabil, seperti karbon dan nitrogen, di bumi berada di atmosfir, daratan,
dan lautan memiliki keterkaitan satu sama lain dari masing-masing ekosistem.
17
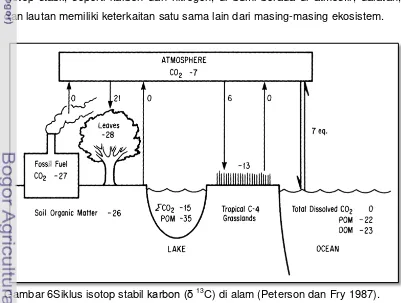
Karbon di laut berasal dari pertukaran CO2 antara atmosfir dengan
ekosistem terestrial dan permukaan laut (Gambar 6; Peterson dan Fry 1987; Hoefs 2009). Nilai δ 13
C CO2 di atmosfir menjadi menurun akibat respon
masukkan dari pembakaran minyak bumi dan dekomposisi yang selama lebih
dari 30 tahun turun 1 ‰. Karbon uptake di daratan seperti dari tumbuhan C3
memiliki proses fraksinasi 21 ‰ antara atmosfir memiliki -7 ‰ dan biomassa
tumbuhan -28 ‰, sedangkan uptake karbon tumbuhan C4 seperti tumbuhan
tropis dan laut lebih rendah (-13 ‰) yaitu 6 ‰. Karbon organik terlarut yang ada
di tanah merupakan hasil dari campuran antara karbon dari atmosfir atau
biomassa tumbuhan karena secara umum memiliki nilai karbon yang kemiripan
dengan tumbuhan (Peterson dan Fry 1987). Lebih lanjut, menurut Peterson dan
Fry (1987) dan Hoefs (2009) menyatakan bahwa siklus karbon di air tawar
berbeda dengan air laut dikarenakan perbedaan komposisi dan sumber CO2
terlarut, dimana masukkan sumber karbon di air laut yang lebih kuat berasal dari
respirasi. Selain itu, siklus karbon dilaut karena pertukaran antara CO2 di atmosfir
dengan permukaan laut.
Nilai isotop stabil karbon di makhluk hidup berbeda, seperti di tumbuhan
dan hewan. Menurut O’Leary (1981), nilai isotop karbon (δ13C) di tumbuhan dapat dibedakan berdasarkan tipe proses fotosintesis terbagi kedalam 3
kelompok, yaitu tumbuhan C3, C4, dan CAM (Crassulacean Acid Metabolism).
Karbon δ13
C tumbuhan C4 memiliki nilai -15 ‰ sampai -9 ‰ (Hemminga dan
Mateo 1996), sedangkan C3 didarat seperti tumbuhan mangrove pada saat
berfotosintesis memiliki nilai antara -24 ‰ dan -30 ‰. Tumbuhan CAM memiliki
nilai melebihi tumbuhan C3 dan C4 (Bouillon et al. 2008). Tumbuhan lamun,
memiliki nilai isotop karbon (δ13
C) dengan kisaran antara -3,0 ‰ sampai dengan
-23,8 ‰ yang tergolong kedalam tumbuhan tipe C4 akan tetapi secara umum
metabolisme pada saat berfotosintesis tergolong kedalam C3 (Hemminga dan
Mateo 1996).
Produsen primer seperti fitoplankton di laut memiliki nilai isotop karbon (δ13
C) -17 ‰ sampai -23 ‰, sedangkan fitoplankton di air tawar memiliki nilai
yang lebih rendah dari fitoplankton laut. Penelitian yang dilakukan Lopes et al.
(2009) di sedimen ekosistem mangrove, nilai isotop karbon -20 ‰ sampai
dengan -23 ‰. Nilai isotop karbon (δ13C) pada tumbuhan darat C3, C4, dan CAM
dapat berbeda-beda karena terdapat perbedaan jenis, kandungan nutrien, dan
18
hidup memiliki nilai yang sama dengan dekomposisi mangrove dan lamun
(Zieman et al. 1984).
Nitrogen yang ada di makhluk hidup sebagian besar berasal atmosfir dalam
bentuk gas N2 (Peterson dan Fry 1987) dan sebagai nutrien yang terbatas di laut
(Hoefs 2009). Komposisi nilai nitrogen di biosfer memiliki mendekati 0 ‰ atau
dapat dikatakan lebih rendah karbon, dengan kisaran -10 sampai dengan + 10 ‰
(Gambar 7). Menurut Peterson dan Fry (1987) penyebab utama nilai nitrogen
yang rendah dikarenakan terbatasnya suplai dari reaksi di tumbuhan dan bakteri.
Nitrogen yang terlarut dalam bentuk N2 di permukaan laut, memiliki nilai + 1
kemudian dimanfaatkan oleh partikel organik terlarut seperti fitoplankton.
Gambar 7Siklus isotop stabil nitrogen (δ 15N) di alam (Peterson dan Fry 1987).
Nitrogen yang masuk ke dalam produsen primer seperti tumbuhan dalam
bentuk N2 yang sebagian besar berasal dari reduksi oleh mikroorganisme. Nilai
nitrogen dalam produsen primer sama seperti nilai karbon, nilainya bervariasi
karena dipengaruhi oleh faktor fisik, kimia, dan biologi. Tumbuhan epifit memiliki nilai δ15
N -8 ‰ sampai dengan -6 ‰ (Bouillon et al. 2004). Penelitian yang
dilakukan oleh Lopes et al. (2009) pada daun mangrove Avicennia marina dan
19
2008), dan fitoplankton di laut, memiliki nilai isotop stabil δ15N antara 7 dan 10 ‰ (Ogawa dan Ogura (1997) dalam Kasai et al. (2006)).
Karbon dan nitrogen dalam ekosistem akuatik dihasilkan oleh produsen
primer yaitu tumbuhan dan fitoplankton (alga dan bakteri) dari hasil fotosintesis
dan respirasi. Proses fotosintesis menghasilkan energi yang digunakan kembali
oleh tumbuhan dan fitoplankton (alga dan bakteri) sebagai bahan bakar untuk
respirasi seluler dan bahan pembangun untuk pertumbuhan. Karbon dan
nitrogen berpindah ke organisme yang lebih tinggi tingkatan trofiknya melalui
peristiwa rantai organik dan jaring organik dalam satu ekosistem atau sebagai
satu siklus.
Sumber karbon dan nitrogen di daerah estuari, rasio isotop bervariasi
dikarenakan ada percampuran antara organik terlarut dari daratan seperti
plankton, serasah tumbuhan darat, dan dari laut seperti plankton laut, alga, dan
serasah tumbuhan laut. Menurut Wada et al. (1991) variasi isotop dikarenakan
adanya sumber yang berasal dari organik terlarut dari darat seperti fitoplankton
dan tumbuhan lamun. Selain itu, menurut Bouillon et al. (2000, 2002, 2004),
masukkan dari organik seperti serasah daun mangrove memberikan kontribusi
terhadap adanya percampuran karbon dan nitrogen yang tinggi.
Karbon dan nitrogen di produsen primer diasimilasi oleh konsumen dan
memiliki nilai rasio dari fraksinasi isotop stabil karbon dan nitrogen. Rasio δ13C yang diasimilasi oleh konsumen memiliki nilai 0-1 ‰, sedangkan pada sistem akutik nilai δ13
C lebih kaya dan bervariasi antara -2.1 dan +2.8 ‰ (Bouillon et al.
2008). Rasio fraksinasi untuk δ15N merupakan nilai yang tinggi, yaitu 2,7 (Bouillon et al. 2008) sampai dengan 3,4 ‰ antara sumber makanan dengan
jaringan tubuh (Minagawa dan Wada 1984). Akan tetapi nilai rata-rata penuh dari δ15
N yaitu antara -0,7 dan +9,2 ‰ (Bouillon et al. 2008), sedangkan jumlah nilai
rata-rata fraksinasi pertropik level, memiliki jumlah 2,5 sampai dengan 5 ‰ untuk δ15
20
3. METODE PENELITIAN
3.1. Waktu dan Lokasi Penelitian
Penelitian ini akan dilaksanakan di 2 lokasi, pertama di Pulau Pari
Kepulauan Seribu, DKI Jakarta pada (5o 50’ 00” – 50o 52’ 25” LS dan 106o 34’ 30” dan 106o 38’ 20” BT) bulan Juni 2011, musim kemarau. Kedua, di mangrove Manko, Pulau Okinawa, Jepang (26o 11’ N, 127o 40’ E)pada bulan Agustus 2011, musim panas. Peta lokasi stasiun pengambilan contoh ini dapat dilihat pada
Gambar 8 dan 9.
Kegiatan pengambilan sampel di lapangan Pulau Pari, Indonesia dilakukan
selama 1 bulan dan preparasi di laborarium 1 bulan, sedangkan pengambilan
sampel di lapangan ekosistem mangrove Manko dan preparasi di laboratorium
dilakukan selama 2 bulan. Preparasi contoh kerang, daun lamun, makroalga, dan
spons dilakukan di Laboratorium Prolink, Teknologi Hasil Perikanan (THP)
Fakultas Perikanan dan Ilmu Kelautan, IPB Bogor, dan Laboratorium Ekologi dan
Sistematik, Fakultas Sains, Universitas Ryukyus, Jepang. Analisis isotop stabil
dilakukan di Laboratorium Kimia Analis, Departemen Kimia, Fakultas Sains,
Universitas Ryukyus, Jepang.
21
Gambar 9Peta lokasi penelitian dan stasiun pengamatan mangrove Manko ( ) (modifikasi dari Khan et al. 2009).
3.2. Alat dan Bahan
Alat dan bahan yang digunakan selama penelitian dapat dilihat pada tabel
1, untuk lebih detail dapat dilihat di lampiran 1.
Tabel 1Alat dan bahan penelitian.
No Alat/Bahan
1 GPS
2 Sekop
3 Refraktometer
4 Termometer
5 Plastik contoh
6 Cool box
7 Snorkel
8 Kamera
22 3.3. Pengambilan Data
3.3.1. Menentukan Stasiun Pengamatan
Stasiun pengamatan di Pulau Pari, DKI Jakarta, ditentukan dengan survey
pendahuluan dan mendapatkan informasi dari nelayan tentang keberadaan
kerang di ekosistem lamun. Setelah mendapatkan informasi dan data awal,
penentuan dan pengambilan biota dilakukan di Pulau Tengah, Kongsi, dan
Burung dengan masing-masing Pulau terdiri dari 3 stasiun dan 3 kali
pengulangan.
Stasiun pengambilan sampel di ekosistem mangrove Manko, Okinawa,
Jepang, dilakukan dengan survey awal. Stasiun pengambilan sampel terdiri dari
3 transek dengan panjang transek 100 m. Transek ditarik dari pinggir daratan
kearah dalam mangrove. Lokasi sampling di ekosistem mangrove dan lamun
dipilih secara acak di wilayah ekosistem lamun karena tujuan dari analisis
sumber makanan dengan isotop stabil adalah untuk mengetahui komposisi
isotop stabil dan dari informasi isotop stabil dapat diketahui asal mula sumber
makanan.
3.3.2. Koleksi Sampel
Koleksi sampel di ekosistem lamun Pulau Pari di lakukan dengan menarik
garis 3 transek dari bibir pantai ke arah lepas pantai dengan setiap transek
sepanjang 300 m.Kemudian setiap transek diletakkan kuadrat ukuran 1x1 m
dengan jarak kuadrat 50 m. Setelah transek dan kuadrat dibentuk, kemudian
kuadrat di acakuntuk mengkoleksi sampel. Pengambilan sampel pada surut
rendah (low tide). Sampel biota yang masuk ke dalam kuadrat kemudian
dikoleksi semuanya. Sampel yang dikoleksi adalah spesiesChlamydinae spp.,
sedangkan potensi sumber makanannya adalah organisme yang berada di
sekitar biota seperti tumbuhan lamun, makrolaga dan spons.
Sampel kerang dan potensi sumber makanan diambil dengan
menggunakan tangan dan snorkel, kemudian dimasukkan kedalam plastik
contoh dan kemudian disimpan kedalam cool box yang telah di isi dengan dry ice
atau es batu dan selanjutnya dibawa ke laboratorium.Sampel kerang yang
diambil dengan ukuran panjang dan lebar cangkang yang lebih dari 5 cm.
Sampel kerang dibagi dua, pertama sampel kerang untuk identifikasi dan kedua
sampel kerang untuk analisis isotop stabil. Identifikasi sampel kerang
menggunakan Dijkstra (2011).Semua sampel dibawa ke Laboratorium Prolink
dan Teknologi Hasil Perikanan (THP) Fakultas Perikanan dan Ilmu Kelautan, IPB
23
Stasiun pengambilan sampel di ekosistem mangrove Manko, Okinawa,
Jepang, dilakukan dengan survey awal. Stasiun pengambilan sampel terdiri dari
3 transek dengan panjang transek 100 m. Transek ditarik dari pinggir daratan
kearah dalam mangrove. Setiap transek terdiri dari 5 kuadrat ukuran 50x50 cm.
Setelah semua transek dan kuadrat terbentuk, kemudian dipilih secara acak.
Sampel biota yang masuk ke dalam kuadrat kemudian dikoleksi semuanya.
Waktu pengambilan sampel dilakukan pada surut rendah (low tide). Sampel biota
yang dikoleksi di fokuskan pada makrozoobentos kelas gastropoda seperti
unidentifiedcerithidea, Cassidulae mustelina, Peroniverruculata,
unidentifiedgrapsidae, dan unidentifieduca, sedangkan potensi sumber
makanannya adalah tumbuhan mangrove dan sedimen.Untuk sampel daun
mangrove yang masih hidup diambil secara acak yang didalam dan dekat
kuadrat untuk mengurangi bias (Bouillon et al. 2004), dengan menggunakan
gunting. Sampel sedimen permukaan yang berada didalam kuadrat diambil
dengan kedalaman 1-2 cmdiambil dengan menggunakan sekop.
Semua sampel yang dikoleksi di ekosistem mangrove dan lamun tidak ada
pengulangan dalam 1 kuadrat karena jumlah yang dibutuhkan untuk analisis
isotop stabil 1 mg dari setiap spesies.Tubuh dari makrozoobentos di ukurkarena
untuk mengetahui umur dan dari perbedaan umur makrozoobentos berbeda pula
sumber makanannya (Lopes et al. 2009).
Sampel makrozoobentos, tumbuhan mangrove, dan sedimen diambil
dengan menggunakan tangan. Sampel dimasukkan kedalam plastik contoh dan
kemudian disimpan kedalam cool box yang ditambahkan dengan dry ice atau es
batu dan selanjutnya dibawa ke laboratorium. Setalah sampai laboratorium,
sampel makrozoobentos dibagi dua, pertama sampel makrozoobentos untuk
identifikasi dan kedua sampel makrozoobentos untuk analisis isotop stabil.
Identifikasi makrozoobentos menggunakan buku petunjuk Okutani (2000) dan
Sakai (1976).Semua sampel dibawa ke Laboratorium Ekologi dan Sistematik,
Fakultas Sains, Universitas Ryukyus, Jepang untuk identifikasi dan preparasi
analisis isotop stabil.
Setelah sampai dilaboratorium, semua sampel di Pulau Pari dan Manko
disimpan didalam lemari pendingin dengan suhu lebih dari -18 oC sampai preparasi contoh kerang selesai. Penyimpanan didalam lemari pendingin dengan
24 3.4. Preparasi Isotop Stabil
3.4.1. Preparasi Makrozoobentos
Metode yang digunakan dalam preparasi makrozoobentos adalah metode
dari Carabel et al. (2006), Ng et al. (2007), dan Jaschinski et al.(2008) yang telah
di modifikasi. Sampel makrozoobentos dicuci dengan Millie-Q water, kemudian
dipisahkan dari cangkang dan tubuh dengan menggunakan pinset dan mortar.
Seluruh tubuh makrozoobentos digunakan untuk analisis isotop stabil, kecuali
kepiting yang dipisahkan jaringan tubuh di karapas. Setelah dipisahkan, jaringan
tubuh dicuci dengan Millie-Q water, kemudian jaringan tubuh makrozoobentos
dicuci dengan HCl 1,2 N setetes demi setes untuk menghilangkan karbonat
(CaCO3) sampai tidak ada gelembung udara. Kemudian dicuci dengan Millie-Q
water dengan tiga kali pengulangan. Pencucian dengan HCl tidak mempengaruhi nilai dari δ13C dan δ15
N (Ng et al. 2007), kemudian dicuci dengan Millie-Q water
(Carabel et al. 2006; Ng et al. 2007; Jaschinski et al. 2008). Sampel disimpan
didalam lemari pendingin sampai dilakukan pengeringan dan analisis isotop
stabil.
3.4.2. Preparasi Sedimen
Metode yang digunakan dalam preparasi sedimen adalah metode dari
Bouillon et al. (2004), Carabel et al. (2006), Ng et al. (2007), Jaschinski et
al.(2008), dan Lopes et al. (2009) yang telah di modifikasi. Sampel sedimen di
saring menggunakan saringan 0.25 mm (No. Mesh size 60) untuk
menghilangkan partikel yang besar dan non sedimen. Sampel sedimen direndam
dengan HCl 1,2 N selama 6 jam untuk menghilangkan karbonat, setelah itu
dicuci dengan Millie-Q water(Carabel et al. 2006; Ng et al. 2007; Jaschinski et al.
2008). Kemudian direndam kembali dengan HCl 6 N selama 24 jam untuk
menghilangkan dan memastikan karbonat di sedimen, kemudian dicuci kembali
dengan Millie-Q water sebanyak 3 kali pengulangan dengan memisahkan air dan
sedimen menggunakan sentrifugasi. Sampel disimpan didalam lemari pendingin
sampai dilakukan pengeringan dan analisis isotop stabil.
3.4.3. Preparasi Mangrove, Lamun, makroalga, dan Spons
Metode yang digunakan dalam preparasi adalah metode dari Bouillon et al.
(2004), Carabel et al. (2006), Ng et al. (2007), Jaschinski et al.(2008), dan Lopes
et al. (2009) yang telah di modifikasi. Sampel daun mangrove, daun lamun,
25
2007; Jaschinski et al. 2008). Setelah dicuci, semua sampel dipotong menjadi
kecil. Sampel disimpan didalam lemari pendingin sampai dilakukan pengeringan
dan analisis isotop stabil.
Metode yang digunakan dalam preparasi adalah metode dari Carabel et al.
(2006) yang telah di modifikasi. Semua sampel dikeringkan dengan
menggunakan freeze dry untuk menghilangkan uap air selama 24 jam. Kemudian
ditumbuk dengan mortar dan pastle sampai menjadi serbuk. Setelah menjadi
serbuk, sampel dimasukkan dan dibungkus kedalam tin capsule (Santis 5 x 9
mm) dengan pengulangan tiga kali. Berat sampel jaringan tubuh
makrozoobentos, daun mangrove, daun lamun, makroalga, dan spons ditimbang
dengan timbangan analitik sebanyak 0,8 sampai dengan 1 mg, sedangkan berat
sampel sedimen 1,8 sampai dengan 2,5 mg.
3.5. Analisis Isotop Stabil
Sampel di analisis δ13C dan δ15N menggunakan alat spektrometer masa (Delta V Advantage, IRMS) yang terhubung dengan elemen-elemen analisis
(NA-2500, CE Instruments) dengan persentasi koreksi 0.15 ‰ yang dilakukan di
Departemen Kimia Analis, Fakultas Sains, Universitas Ryukyus, Jepang. Nilai
rasio isotop stabil menggunakan standar konvensional (VPDB batu gamping
untuk karbon dan N2 atmosfer untuk nitrogen) (Hoefs 2009) dengan rumus:
δ13C or δ15
N = (Rsample/Rstandard – 1) 1000 (‰)………(1)
dimana Rsample adalah elemen 13C atau 15N, sedangkan Rstandard adalah rasio
12
C atau 14N berdasarkan PDB. Standar karbon δ13C menggunakan Pee Dee Belemnite (PDB), sedangkan nitrogen δ15N menggunakan standar N2 gas
atmosfir.
Untuk menghitung sumber makanan yang di asimilasi hewan (rasio δ13C atau δ15
N), digunakan rumus (DeNiro dan Epstein 1978, 1981):
∆Animal-Diet………(2)
26 3.6. Analisis Data
Untuk mengetahui nilai rata-rata dari δ13C dan δ15N setiap sampel maka digunakan statistic descriptive. Selain itu, digunakan uji normalitas data dari
masing-masing nilai δ13C dan δ15N setiap sampel menggunakan uji Kolmogorov-Smirnov. Untuk membedakan nilai δ13C dan δ15N dari makrozoobentos dan sumber makanan digunakan ANOVA dan uji Tukey (α = 0.05). Pengolahan data
27
4. HASIL DAN PEMBAHASAN
4.1. Kondisi Umum Lokasi Penelitian
4.1.1. Lokasi Penelitian di Pulau Pari
Perairan Pulau Pari terletak di bagian paling selatan dari Pulau-Pulau di
kePulauan Seribu, sekitar 40 km sebelah Barat laut Kota Jakarta. Daerah Pulau
Pari meliputi luas sekitar 15 km2 dengan terdiri dari Pulau-Pulau kecil yaitu Pulau Kongsi, Pulau Tengah, Pulau Burung, Pulau Tikus, dan Pulau Pari. Selain
memiliki Pulau-Pulau kecil, Pulau Pari memiliki delapan goba besar dan kecil
(lagoon), kloran atau pintu keluar masuk air di pinggiran terumbu yang
menghubungkan perairan didalam terumbu dengan perairan diluarnya, dan
daerah pinggiran terumbu (tubir) yang melingkar (reef edge). Salinitas perairan
Pulau Pari bervariasi yaitu antara 27 sampai dengan 34 ‰ dengan rerata total
dari semua lokasi adalah 31,6 ‰. Salinitas di Pulau Pari dipengaruhi oleh
pasang surut yang setiap harinya dengan nilai rata-rata pasang tertinggi 1,20 m
dan pasang terendah 0,18 m (Kiswara 1992).
Keanekaragaman biota dan tumbuhan Pulau Pari diantaranya adalah
gastropoda, bivalvia, spons, makroalga, mangrove, dan lamun. Kelas bivalvia
merupakan kelas yang terdistribusi luas di Pulau Pari (Cappenberg dan
Panggabean 2005). Kerang yang dikoleksi dalam penilitian ini merupakan jenis
dari Chlamydinae spp. dan ditemukan di goba-goba dengan rerata kedalaman 83
cm (Lampiran 13) dengan tipe substrat berlumpur. Tipe substrat di Pulau Pari
terdiri dari substrat pasir kasar, halus, berlumpur (Kiswara 2010), dan pecahan
karang (rubble). Vegetasi lamun di Pulau Pari terdiri dari Enhalus acoroides,
Halophila ovalis, Thalassia hemprichii dan Cymodocea rotundata yang tumbuh di
substrat lumpur, pasir, dan terumbu (Kiswara 1992). Potensi sumber makanan
yang berada di sekitarChlamydinae spp. di Pulau Pari yang dikoleksi dalam
penelitian ini adalah tumbuhan lamun, spons, dan makroalga. Tumbuhan lamun
Enhalus acoroides, spons, dan makrolaga yang ditemukan dalam penilitian ini
memiliki substrat berlumpur.
4.1.2. Lokasi Penelitian di Ekosistem Mangrove Manko
Okinawa (26o 11’ N, 127o 40’ E) merupakan Pulau semi tropis yang lokasinya berada di selatan Jepang. Ekosistem mangrove di Mankomerupakan
28
masukan dari sungai Kokuba dan Noha dengan pasang-surut dari laut Cina
selatan. Sampel yang didapatkan dalam penelitian ini adalah mangrove jenis
Kandelia candel, sedimen, dan makrozoobentos seperti unindetified cerithidae,
Cassidulae mustelina, Peroni verruculata, unindetifiedgrapsidae, dan
unindetifieduca dengan kedalaman perairan 0 cm (Lampiran 13).
Ekosistem mangrove di Manko memiliki jenis seperti Kandelia candel,
Bruguiera gymnorhiza, Rhizopora stylosa, dan Excoecaria agallocha. Menurut
Mchenga et al. (2007)mangrove jenis K. candel yang ditemukan merupakan jenis
yang dominan di Manko area. Karakteristik dari sedimen Manko adalah black,
soft clay atau sandy mud (Islam et al. 2004). Menurut Islam et al. (2002)
ekosistem mangrove Manko ditemukan makrozoobentos seperti krustacea,
moluska, ikan, dan policaeta dengan 13 famili yang pola distribusinya
berbeda-beda dan dipengaruhi oleh tempat makan.
Makrozoobentos yang dapat ditemukan didalam Manko area adalah dari
kelas gastropoda dan krustacea. Kelas gastropoda yang tidak ditemukan di
Manko area oleh Islam et al. (2002) adalah dari famili Onchidiidae dan
Potamididae, akan tetapi dapat ditemukan dalam penilitian ini dan dapat
ditemukan hampir diseluruh wilayah Jepang (Okutani 2000). Famili Onchidiidae
merupakan jenis gastropoda yang tidak bercangkang yang ditemukan di
ekosistem darat sampai ke ekosistem mangrove. Spesies yang ditemukan di
Manko adalah Peroni verruculata merupakan jenis keong yang habitatnya di
mangrove. Selain itu, ada beberapa spesies dari Onchidiidae yang habitatnya di
ekosistem mangrove di Jepang seperti Onchidium struma (Okutani 2000).
Potamididae merupakan famili yang dominan ditemukan di ekosistem mangrove
(Okutani 2000; Lopes et al. 2009; Mujiono 2009).
Famili Grapsidae merupakan burrowing sesarmid dan Ocypodidae
merupakan tipe fiddler (Kristensen 2008), dari kelas krustacea yang dominan
ditemukan di ekosistem mangrove (Lee 2008). Keanekaragaman dan kepadatan
yang tinggi Grapsidae berada di ekosistem mangrove, dengan sebagian berada
di barat Indo-pasifik, merupakan famili yang memiliki fungsi penting
hubungannya dengan nutrien terlarut di ekosistem mangrove (Nagelkerken et al.