STUDI PERBANDINGAN KADAR TIMBAL (Pb) DALAM
HATI KAMBING POTONG PADA KAWASAN INDUSTRI
DAN NON INDUSTRI DENGAN METODE
SPEKTROFOTOMETRI
SERAPAN ATOM (SSA)
SKRIPSI
NORA MARIHOT PURBA
090802002
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
STUDI PERBANDINGAN KADAR TIMBAL (Pb) DALAM
HATI KAMBING POTONG PADA KAWASAN INDUSTRI
DAN NON INDUSTRI DENGAN METODE
SPEKTROFOTOMETRI
SERAPAN ATOM (SSA)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
NORA MARIHOT PURBA
090802002
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : STUDI PERBANDINGAN KADAR Pb DALAM HATI KAMBING POTONG PADA KAWASAN INDUSTRI DAN NON INDUSTRI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
Kategori : SKRIPSI
Nama : NORA MARIHOT PURBA
Nomor Induk Mahasiswa : 090802002
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMUPENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, April 2014
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs. Chairuddin, M.Sc. Drs. Ahmad Darwin Bangun.M,Sc. NIP. 195912311987011001 NIP. 195211161980031001
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
Dr. Rumondang Bulan Nst, Ms. NIP. 1954 0830 1985 032001
PERNYATAAN
STUDI PERBANDINGAN KADAR TIMBAL (Pb) DALAM HATI KAMBING POTONG PADA KAWASAN INDUSTRI DAN NON
INDUSTRI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, April 2014
NORA MARIHOT PURBA 090802009
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus Yang Maha Pengasih, karena berkat kasih dan pernyetaanNya sehingga penulis dapat menjalani studi hingga dapat menyelesaikan penelitian dan penulisan skripsi ini dalam waktu yang telah ditetapkan.
Terima kasih yang setulusnya penulis sampaikan kepada Ayah tersayang T.P.Purba dan Ibu tercinta K.Tambunan, yang telah memberikan segalanya bagi penulis baik dukungan moral maupun materi terlebih doa-doa yang selalu menguatkan penulis dalam pengerjaan penelitian dan skripsi ini, begitu juga dengan saudara penulis kak watty, kak merry, kak ria, kak maya dan adik tersayang paulus penulis sampaikan terima kasih untuk doa-doa dan semangat yang tak pernah hilang. Ucapan terima kasih juga penulis sampaikan kepada Bapak Drs. Ahmad Darwin Bangun.M,Sc Dan Bapak Drs. Chairuddin, M.Sc selaku dosen pembimbing yang telah banyak memberikan bimbingan, arahan, ilmu dan waktu selama penulis melakukan penelitian hingga penulisan skripsi ini selesai. Ucapan terima kasih juga ditujukan kepada Ibu Dr.Rumondang Bulan Nst,Ms selaku ketua Departemen Kimia, Bapak Drs.Albert Pasaribu,M.Sc selaku sekretaris Departemen Kimia, Bapak Prof.Harlem Marpaung selaku dosen wali, Bapak dan Ibu dosen serta Pegawai Departemen Kimia FMIPA USU, juga kepada sahabat-sahabat penulis Able, sudirman, iwan, sabam, roiman, sheyla, melda, reh malem, Emilia dan juga sahabat tersayang penulis satriani dan Jennifer, begitu juga ucapan terima kasih untuk kakak kelompok penulis kak mutiara saragih, untuk seluruh teman-teman asisten dan laboran kimia Analitik, serta temen-teman stambuk 2009. Terima kasih untuk seluruh teman atau saudara yang tidak bisa penulis sebutkan satu per satu, yang telah memberikan doa dan semangat kepada penulis selama pengerjaan skripsi ini. Terima Kasih. Tuhan Yesus Memberkati.
Penulis.
STUDI PERBANDINGAN KADAR TIMBAL (Pb) DALAM HATI KAMBING POTONG PADA KAWASAN INDUSTRI DAN NON
INDUSTRI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
ABSTRAK
Telah dilakukan penelitian tentang perbandingan kadar Timbal (Pb) dalam hati kambing potong pada kawasan industri dan non industri. Sampel di destruksi kering dengan pelarutan abunya menggunakan HNO3(p). Uji kualitatif dilakukan dengan alat Inductively CaoupledPlasma – Optical Emission (ICP-OES) dimana diperoleh hasil sampel I (kawasan Industri) = 0.088 ppm, sampel II (kawasan Industri) = 0.080 ppm, sampel III (Kawasan Industri) = 0.086 ppm dan sampel IV (Kawasan Non Industri) = 0.022 ppm dan uji kuantitatif penentuan kandungan logam Pb dilakukan dengan metode Spektrofotometri Serapan Atom (SSA) pada panjang gelombang 217.0 nm. Hasil yang diperoleh dari penelitian ini adalah sampel A (kawasan non industri) = 0.4585 mg/Kg, sampel B (kawasan non industri) = 0.4490 mg/Kg, sampel C (kawasan Industri) = 0.8761 mg/Kg, dan sampel D (kawasan Industri) = 0.8622 mg/Kg. Hasil akhir menunjukkan bahwa kandungan Pb masih memenuhi batas maksimum sesuai keputusan SNI 7387:2009 yaitu 1.0 mg/Kg.
COMPARATIVE STUDY OF PLUMBUM (Pb) IN GOAT LIVER IN AN INDUSTRIAL AREA AND NON INDUSTRY WITH METHODS
ATOMIC ADSORPTION SPECTROPHOTOMETRY (AAS)
ABSTRACT
DAFTAR ISI
Daftar Lampiran xi
BAB 1. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Permasalahan 2
1.3. Pembatasan Masalah 2
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 3
1.6. Lokasi Penelitian 3
1.7. Metode Penelitian 3
BAB 2. TINJAUAN PUSTAKA
2.1. Logam Berat 5
2.2. Logam Timbal (Pb) 5
2.2.1. Keberadaan Timbal (Pb) Pada Lingkungan 6
2.2.2. Pencemaran Logam Timbal (Pb) 8
2.2.3. Toksisitas Logam Timbal (Pb) 9
2.2.4. Mekanisme Toksisitas Pb 11
2.3. Destruksi Logam 13
2.3.1. Destruksi Basah 13
2.3.2. Destruksi Kering 14
2.4. Inductively Coupled Plasma-OES 14
2.4.1. Prinsip Kerja ICP-OES 15
2.5. Spektrofotometer Serapan Atom 16
2.5.1. Prinsip Dasar Spektrofotometer Serapan Atom 17
2.5.2. SSA Nyala dan Tanpa Nyala 20
2.5.3. Gangguan Pada SSA dan Cara Mengatasinya 21 BAB 3. METODE PENELITIAN
3.1. Alat dan Bahan 22
3.1.1. Alat 22
3.1.2. Bahan 23
3.2. Prosedur Penelitian 23
3.2.1. Pembuatan Larutan Standar Pb2+
c. Larutan Standar Pb2+ 10 mg/L 23 d. Larutan Standar Pb2+ 0,3;0,5;0,7;0,9 dan 1,1 mg/L 24 3.2.2. Pembuatan Kurva Kalibrasi Larutan Standar Pb2+ 24
3.2.3. Pengambilan Sampel 24
3.2.3. Pengabuan Sampel 24
3.2.4. Penyediaan Larutan Sampel 25
3.2.5. Penentuan Pb2+ dalam Sampel 25
3.3. Bagan Penelitian 26
3.3.1. Penentuan Kurva Kalibrasi Timbal (Pb) 27 3.3.2. Penentuan Logam Pb dalam Sampel (SNI 01-3552-2000) 27 BAB 4. HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 28
4.1.1. Logam Timbal 28
4.1.1.1. Penurunan Persamaan Garis Regresi 28 4.1.1.2. Penentuan Koefisien Korelasi Timbal 30 4.1.1.3. Penentuan Kadar Timbal (Pb) dalam Sampel 31 4.1.1.3.1. Penentuan Kadar Timbal Sampel A 31
4.1.2. Penentuan Beda Rataan 36
4.1.2.1. Beda Rataan Kadar Timbal Sampel A dan C 37 4.1.2.2. Beda Rataan Kadar Timbal Sampel B dan D 38
4.2. Pembahasan 38
BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 41
5.2. Saran 41
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1 Proses Penghambat Hemoglobin Oleh Pb 13
2.2 Skematis Ringkasan Peralatan Spektrofotometer 18 Serapan Atom
DAFTAR TABEL
Nomer Judul Halaman
Tabel
2.1 Konsentrasi Pb dalam Pakan yang Dapat Mengakibatkan 10 Keracunan Pada Hewan Ruminansia
2.2 Hasil Analisa Pada Ginjal, Hati, Daging, Darah, dan Susu 11
2.3 Jenis-jenis Gas Pembakar pada SSA Nyala 19
DAFTAR LAMPIRAN
No. Judul Halaman
Lampiran
1 Kondisi alat SAA Pada Pengukuran Pb 39
5 Data Kadar Timbal Pb Semua Sampel 42
6 Data Perbandingan Kadar Timbal Dalam Sampel 43 Dengan SNI
STUDI PERBANDINGAN KADAR TIMBAL (Pb) DALAM HATI KAMBING POTONG PADA KAWASAN INDUSTRI DAN NON
INDUSTRI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
ABSTRAK
COMPARATIVE STUDY OF PLUMBUM (Pb) IN GOAT LIVER IN AN INDUSTRIAL AREA AND NON INDUSTRY WITH METHODS
ATOMIC ADSORPTION SPECTROPHOTOMETRY (AAS)
ABSTRACT
The comparison of Plumbum in goat liver in an industrial area and non industry. The goat liver was dry digestion and then the ash of goat liver dissolved with HNO3(p). Qualitative test using Inductively Coupled Plasma – Optical Emission (ICP – OES) where the sampel results obtained I (Industrial area) = 0.088 ppm, sample II (Industrial area) = 0.080 ppm, sample III (Industrial area) = 0.086 ppm and sample IV (Non Industrial area) = 0.022 ppm and Quantitative test determination of Pb content using Atomic Absorption Spectrophotometry (AAS) at wavelength for Pb 217.0 nm. The result of determination showed that the content in plumbum of sample A (Non Industrial Area) = 0.4585 mg/Kg, sample B (Non Industrial Area) = 0.4490 mg/Kg, sample C (Industrial area) = 0.8761 mg/Kg and sample D (Industrial area) = 0.8622 mg/Kg. However Pb of metal content were fulfilling SNI 7387:2009 that 1.0 mg/Kg.
BAB I
PENDAHULUAN
1.1..Latar Belakang
Timbal atau dikenal sebagai logam Pb dalam susunan unsur merupakan logam berat yang terdapat secara alami di dalam kerak bumi dan tersebar ke alam dalam jumlah kecil melalui proses alami termasuk letusan gunung berapi dan proses geokimia. Pb merupakan logam lunak yang berwarna kebiru-biruan atau abu-abu keparakan dengan titik leleh pada 327,5 oC dan titik didih 1.740 oC pada tekanan etmosfer. Timbal mempunyai nomor atom tersebar dari semua unsur yang stabil, yaitu 82. Dari golongan IV A dengan bobot atom 207,2. Namun logam ini sangat beracun.
Pencemaran lingkungan bukanlah suatu hal yang baru, karena pencemaran lingkungan telah terjadi sejak dahulu sampai sekarang. Pencemaran yang paling besar disebabkan oleh pembungan senyawa kimia tertentu dari kegiatan industri dan transportasi. Salah satu bahan pencemar terbesar yang dihasilkan adalah timbal (Pb). Banyak industri yang pada proses produksinya menggunakan Timbal (Pb) seperti industri pembuatan baterai, industri cat, pestisida, pembuatan pipa,
dan industry keramik. Timbal (Pb) juga digunakan sebagai bahan aditif pada bahan bakar, khususnya bensin sebagai anti knocking (anti letup). Timbal (Pb) termasuk salah satu zat kimia berbahaya yang dapat mengganggu kesehatan bila masuk ke dalam tubuh manusia. Gangguan kesehatan yang ditimbulkan oleh
keracunan Timbal (Pb) seperti anemia, gangguan janin pada ibu hamil, peningkatan permiabilitas pembuluh darah, kerusakan pada otak besar, epilepsi, halusinasi, dan delirium, yaitu sejenis penyakit gula. (Palar.H,2004)
hewan ruminansia tersebut, dimana makanan seperti rerumputan, alang dan
dedaunan lainnya terkontaminasi oleh logam Pb begitu juga minuman yang sering di ambil dari air aliran sungai ular telah terkontaminasi oleh limbah industri baik itu dari gas buangan limbah atau pun dari limbah padat dan cair dari proses industri seperti pupuk pestisida, gas buangan kendaraan transportasi yang di
hasilkan dari bahan bakar bensin terkontaminasi pada makanan dan minuman kambing yang kemudian masuk ke dalam tubuh hewan diabsorpsi oleh darah, berikatan dengan dengan protein darah dan didistribusikan ke seluruh jaringan tubuh. Akumulasi logam yang tertinggi biasanya dalam organ detoksikasi hati dan ekskresi ginjal. Di dalam kedua jaringan tersebut biasanya logam juga berikatan dengan berbagai jenis protein baik enzim maupun protein lain yang disebut metalotionein (Darmono, 2001).
Logam berat Pb dapat masuk ke dalam tubuh makhluk hidup melalui saluran pencernaan dan saluran pernapasan dan akan terakumulasi dalam sistem organ metabolisme tubuh. Penelitian mengenai analisa jeroan hewan ini telah dilakukan sebelumnya, dimana menganalis Pb pada hati sapi kawasan Deli Serdang dengan kadar Pb 0,2 ppm (Merry Irasanti, 2012), analisis hati sapi Cirebon 0,2931mg/Kg (Evi, 2006). Sehingga peneliti tertarik untuk menganalisa logam berat Pb pada hati kambing potong dikawasan industri daerah Perbaungan dengan hati kambing potong dikawasan non industri di daerah Sei Rampah agar dijadikan perbandingan untuk membandingkan kadar Pb dalam hati Kambing
1.2. Permasalahan
a. Berapakah kadar kandungan logam (Pb) dalam hati kambing potong di kawasan industri dengan kawasan non industri ?
b. Apakah kandungan logam Timbal (Pb) pada hati kambing potong memenuhi
batas persyaratan Standar Nasional Indonesia (SNI) ?
1.3.Pembatasan Masalah
a. Penelitian ini membatasi kandungan logam yang dianalisis yaitu Timbal (Pb). b. Pengambilan sampel tidak memperhatikan waktu pemotongan, jenis kelamin,
dan umur kambing.
1.4.Tujuan Penelitian
a. Penelitian ini bertujuan untuk mengetahui kandungan logam Timbal (Pb) pada hati kambing potong dikawasan Industri dengan Non industri.
b. Untuk mengetahui apakah kadar logam Timbal (Pb) masih memenuhi batas persyaratan Standar Nasional Indonesia (SNI).
1.5.Manfaat Penelitian
a. Sebagai informasi kepada masyarakat mengenai kemungkinan adanya kadar
Timbal (Pb) pada hati kambing.
b. Sebagai masukkan kepada pemerintah dan instansi terkait dalam menentukan kebijakan yang berkaitan dengan sanitasi peternakan kambing potong khususnya dalam hal pemberian pakan dan minum ternak, dan lokasi peternakan.
1.6.Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Matematika dan Ilmu Pengetahuan Alam, Laboratorim Penelitian Farmasi Universitas Sumatera Utara dan Balai Laboratorium Kesehatan Medan.
1.7.Metodologi Penelitian
a. Penelitian ini merupakan eksperimen laboratorium
b. Metode pengambilan sampel dilakukan secara sembarang dan dalam satu kali pengambilan, sampel Hati Kambing Potong A dan B merupakan sampel kawasan non industri yang berasal dari pasar tradisional sei rampah, sedangkan sampel Hati Kambing Potong C dan D merupakan sampel kawasan Industri yang berasal dari pasar tradisonal Perbaungan.
c. Sampel hati kambing potong kemudian dihilangkan kadar airnya dengan pamanasan dalam oven pada suhu 105oC kemudian dihaluskan
d. Destruksi sampel hati kambing potong yang telah dihaluskan dilakukan dengan metode destruksi kering dengan pemanasan dalam tanur 550oC selama 7 jam dan dilanjutkan dengan pelarutan sampel menggunakan HNO3(p).
e. Uji kualitatif dilakukan dengan metode ICP-OES.
f. Penentuan kadar Timbal pada sampel hati kambing Potong dilakukan dengan
BAB 2
TINJAUAN PUSTAKA
2.1. Logam Berat
Logam dapat dibagi menjadi dua bagian, yaitu logam esensial dan logam nonesensial. Logam esensial adalah logam yang sangat membantu dalam proses fisiologis makhluk hidup dengan jalan membantu kerja enzim atau pembentukan organ dari makhluk yang bersangkutan, yang termasuk logam esensial adalah seng (Zn), tembaga (Cu), besi (Fe), cobalt (Co), mangan (Mn), selenium (Se).
Logam nonesensial adalah arsen (As), merkuri (Hg), Cadmium (Cd), timbale (Pb), kromium (Cr) dan aluminium (Al), tetapi beberapa jenis logam lain yang termasuk kelompok logam esensial dapat pula bersifat racun bila keberadaannya telah melebihi dari kebutuhan pada proses fisioligi dalam makhluk hidup (Darmono, 1995).
2.2. Logam Timbal (Pb)
Timbal (Pb) pada awalnya adalah logam berat yang berbentuk secara alami. Namun, Timbal (Pb) juga bisa berasal dari kegiatan manusia bahkan mampu mancapai jumlah 300 kali lebih banyak dibandingkan Timbal (Pb) alami. Timbal (Pb) meleleh pada suhu 328oC (662oF); titik didih 1740oC (3164oF); dan memiliki gravitasi 11,34 dengan berat 207,20 (Widowati, 2008)
Timbal banyak digunakan untuk berbagai keperluan. Hal ini dikarenakan timbal memiliki sifat-sifat sebagai berikut :
2) Timbal (Pb) merupakan logam yang lunak sehingga mudah diubah
menjadi berbagai bentuk.
3) Sifat kimia Timbal (Pb) menyebabkan logam ini dapat berfungsi sebagai lapisan pelindung jika kontak langsung dengan udara lembab.
4) Timbal (Pb) dapat membentuk alloy dengan logam lainnya, dan alloy yang terbentuk mempunyai sifat berbeda dengan Timbal (Pb) yang murni.
5) Densitas Timbal (Pb) lebih tinggi dibandingkan dengan logam lainnya kecuali emas dan merkuri (Fardiaz, 1992)
2.2.1. Keberadaan Timbal (Pb) Pada Lingkungan
1. Timbal di Udara
Timbal (Pb) di udara dapat berbentuk gas dan partikel. Di daerah tanpa penghuni dipegunungan California (USA), kadar Timbal sebesar 0,008 mikrogram/m3 sedangankan mutu di udara adalah 0,025 – 0,04 gr/Nm3 (Mukono, 2002)
2. Timbal di Air
Timbal (Pb) dapat berada dalam badan perairan secara alamiah dan sebagai dampak dari aktivitas manusia. Secara alamiah, Timbal dapat masuk ke badan perairan melalui pengkristalan Timbal di udara dengan bantuan air hujan
dan proses korosifikasi dari batuan mineral akibat hempasn gelombang dan angin. Timbal dari aktivitas manusia terdapat pada limbah industri yang mengandung Timbal yang dibuang ke badan air. Baku mutu (WHO) Timbal dalam air 0,1 mg/liter dan KLH No. 02 tahun 1988 yaitu 0,05 - 1 mg/liter (Palar,H., 2004)
3. Timbal (Pb) di Tanah
Rata-rata timbal yang terdapat di dalam tanah adalah sebesar 5 – 25 mg/kg. Keberadaan timbal di dalam tanah dapat berasal dari emisi kendaraan bermotor, dimana partikel timbal yang terlepas ke udara, secara alami dengan adanya gaya gravitasi, maka timbal tersebut akan turun ke tanah (Widowati, 2008)
4. Timbal di Batuan
Timbal secara alami terdapat sebagai timbal sulfida, timbal karbonat, timbal sulfat, dan timbal klorofosfat. Kandungan Timbal dari beberapa batuan kerak bumi sangat beragam. Batuan eruptif seperti granit dan riolit memiliki kandungan Pb kurang lebih 200 ppm (Diapari, 2009)
5. Timbal di Tumbuhan
Bahwa pencemaran udara terhadap tanaman dapat mempengaruhi: pertumbuhan, yaitu dengan mengurangi pertumbuhan kambium, akar dan bagian reproduktif, termasuk pertumbuhan akar dan pertumbuhan daun. Sedangkan menurut Mukono (2002), secara alamiah tumbuhan dapat mengandung timbal. Kadar timbal pada dedaunan adalah 2,5 mg/kg berat daun kering (Kozlowski, 1991)
6. Timbal di Makanan
Semua bahan pangan alami mengandung Timbal dalam konsentrasi kecil,
2.2.2. Pencemaran Logam Timbal (Pb)
Ada beberapa pencemaran logam berat timbal (Pb), diantaranya adalah sebagai berikut :
a. Pencemaran Secara Alami
Kadar timbal (Pb) yang secara alami dapat ditemukan dalam bebatuan sekitar 13 mg/kg. Khusus timbal (Pb) yang tercampur dengan batu fosfat dan terdapat didalam batu pasir kadarnya lebih besar yaitu 100 mg.kg. Timbal yang terdapat di tanah berkadar sekitar 5-25 mg/kg dan air bawah tanah berkisar antara 1-60
μg/liter (Sudarmaji, 2006).
b. Pencemaran dari Industri
Industri yang berpotensi sebagai sumber pencemaran timbal adalah semua industri yang menggunakan timbal sebagai bahan baku maupun bahan penolong, seperti industri pengecoran, pembuatan baterai, kabel, dan industri kimia dalam pembuatan cat, karena toksisitasnya relatif lebih rendah jika dibandingkan dengan logam pigmen yang lain.
c. Pencemaran dari Transportasi
Timbal (Pb) berupa tetra ethyl lead dan tetra methyl lead banyak dipakai sebagai anti knock pada bahan bakar. Timbal (Pb) sebagai salah satu zat yang
dicampurkan ke dalam bahan bakar yaitu (C2H5)4Pb atau TEL (Tetra Ethyl Lead). Timbal (Pb) yang bercampur dengan bahan bakar tersebut akan bercampur dengan oli dan melalui proses di dalam mesin maka logam berat Timbal (Pb) akan keluar dari knalpot bersama dengan gas buang lainnya (Sudarmaji, 2006)
Penggunaan Timbal (Pb) dalam bensin lebih disebabkan oleh keyakinan
bahwa tingkat sensitivitas Timbal (Pb) tinggi dalam menaikkan angka oktan. Setiap 0,1 gram Timbal (Pb) perliter bensin mampu menaikkan angka oktan 1,5. Penggunaan sampai 2 satuan. Selain itu, harga Timbal (Pb) relatif murah untuk meningkatkan satu oktan dibandingkan dengan senyawa lainnya (Santi, 2001)
2.2.3. Toksisitas Logam Timbal (Pb)
Timbal adalah logam berat konvensional yang sering menyebabkan keracunan pada hewan ruminansia, Rumput pakan ternak yang terkontaminasi oleh Pb dari udara sering menyebabkan keracunan kronis, tetapi padang rumput yang terkontaminasi cemaran dari limbah peleburan logam ataupun dari limbah baterai/aki sering menyebabkan toksisitas yang akut. Pada hewan ruminansia gejala khas dari keracunan Pb ini ada tiga bentuk yaitu sebagai berikut :
a. Gastro-enteritis, hal ini disebabkan karena terjadi reaksi dari mukosa saluran pencernaan bila kontak dengan garam Pb, sehingga terjadi pembengkakan. Gerak kontraksi rumen dan usus terhenti, sehingga menyebabkan terjadinya konstipasi dan kadang-kadang diare.
b. Anemia, di dalam darah timbale berikatan dengan sel darah merah
sehingga sel darah mudah pecah. Bila sel darah pecah, terjadi gangguan terhadap sintesis Hb yang dapat menyebabkan anemia. Gejala ini ditandai dengan adanya anisositosis, polikromasia, dan jumlah sel darah muda (retikulosit) meningkat. Sel darah bernukleus juga meningkatkan, dan
ditemukan basofilik stipling yang merupakan cirri khas keracunan Pb.
c. Ensepalopati, logam ini juga menyebabkan terjadinya kerusakan sel endotel dari kapiler darah otak, sehingga bentuk protein berukuran
Tabel 2.1. Konsentrasi Pb dalam Pakan yang Dapat Mengakibatkan Keracunan pada Hewan Ruminansia
Diagnosis keracunan Pb secara kronis dapat dilakukan dengan analisis kandungan Pb dalam darah, kadar enzim delta amino levunik dehidrasi
(delta-ALA) dan kadar eritrosit porfirin bebas (FEP) dalam darah (Darmono, 2001).
Kasus keracunan Pb dapat dialami oleh hewan ruminansia sapi, pada penelitian terdahulu melakukan analisa kandungan logam Pb, Cu dan Cd dalam
hati sapi lokal dan impor dengan metode SSA. Hasil penelitian menunjukkan bahwa kandungan rata-rata logam Pb, Cu dan Cd pada hati sapi Jakarta dalam
bobot basah adalah: 0,1667 μg/g; 3,4202 μg/g dan 0,0220 μg/g. Sementara untuk logam Pb, Cu dan Cd dalam hati sapi Bogor adalah: 0,3578 μg/g; 3,8305 μg/g dan 0,0286 μg/g. Sedangkan untuk logam Pb, Cu dan Cd dalam hati sapi Cirebon
adalah: 0,2931 μg/g; 2,9121 μg/g dan 0,0112 μg/g. Kandungan rata-rata logam Pb,
Cu dan Cd dalam hati sapi New Zealand adalah: 0,2915 μg/g; 1,9110 μg/g dan 0,0608 μg/g. Sedangkan kandungan rata-rata logam Pb,Cu dan Cd dalam hati sapi
Australia adalah: 0,2280 μg/g; 2,8626 μg/g dan 0,0360 μg/g. Kandungan logam
Pb, Cu dalam hati sapi Bogor lebih besar bila dibandingkan dengan hati sapi Jakarta, Cirebon, New Zealand dan Australia. Sedangkan kandungan logam Cd dalam hati sapi New Zealand lebih besar bila dibandingkan dengan hati sapi Jakarta, Bogor, Cirebon dan Australia. Kadar Pb, Cu dan Cd dari semua contoh yang dianalisis tersebut masih memenuhi syarat yang ditetapkan oleh Direktorat
Jenderal Pengawasan Obat dan Makanan yaitu maksimal 2,0 μg/g untuk Pb, 5,0 μg/g untuk Cu sedangkan untuk Cd memenuhi persyaratan menurut United State
Food and Drug Administration ( FDA) yaitu maksimal 1,0 μg/g. (Evi, 2006)
Keracunan Pb pada sapi perah telah dilaporkan pula oleh Oskarsson dkk.
(1992) di Swedia, di mana Pb di-transfer ke air susu. Keracunan terjadi setelah sapi merumput pada padang rumput bekas tempat pembuangan baterai/aki bekas. Barang tersebut dibakar dan sampahnya dibuang pada padang penggembalaan. Setelah selang waktu tiga hari, sapi yang merumput di sekitar tempat itu,
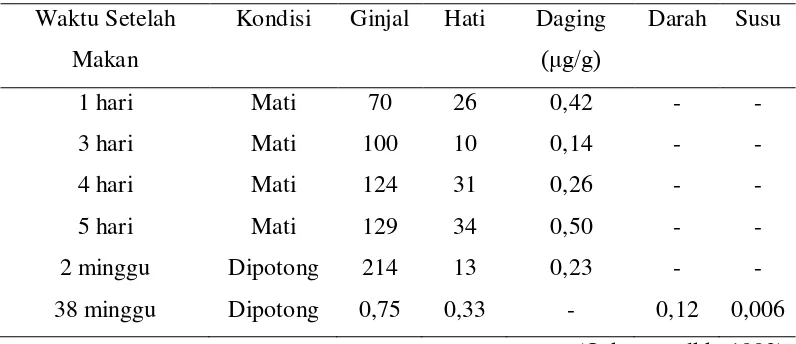
ditemukan mati mendadak. Sebelas ekor sapi perah yang merumput pada lokasi yang sama tidak mengalami keracunan, empat di antaranya sedang bunting. Beberapa ekor sapi yang terlihat mengalami gejala keracunan segera dipotong. Hasil analisis kandungan Pb dalam ginjal, hati, daging, darah dan susunya dapat dilihat pada tabel dibawah ini :
Tabel 2.2. Hasil Analisa Pada Ginjal, Hati, Daging, Darah, dan Susu
Waktu Setelah
stomata) diambil dari empat jalan yang berbeda tingkat kepadatan lalu lintasnya
yaitu : Jalan Kyai Gde Utama, Kapten Tendean, Ir. H. Djuanda dan Siliwangi. Hasilnya menunjukkan bahwa konsentrasi Pb di seluruh sampel daun berkisar
antara 0.038 sampai 2.281 μg/g. Uji ANOVA dengan selang kepercayaan 95 % menunjukkan bahwa konsentrasi Pb daun dari keempat jalan tidak berbeda nyata.
Hasil analisis regresi linear menunjukkan adanya kecenderungan penurunan kandungan klorofil, luas permukaan daun dan jumlah stomata seiring dengan naiknya konsentrasi Pb daun, namun nilai koefisien korelasi untuk ketiga parameter tersebut sangat kecil, (0.0132, 0.0109, 0.0003). Secara umum dapat disimpulkan bahwa S. macrophylla mampu menyerap dan mengakumulasi Pb pada daun dan akumulasi Pb tidak menunjukkan pengaruh terhadap kondisi daun, paling tidak dalam kisaran konsentrasi antara 0.038- 2.281 μg/g, sehingga jenis ini dapat dipertimbangkan sebagai agen bioremediasi polusi timbal. (Ebynthalina, 2006).
2.2.4. Mekanisme Toksisitas Pb
Walaupun mekanisme secara pasti bagaimana Pb menghambat respon kekebalan belum begitu jelas, gangguan terhadap sistem retikuloendotelial dan gangguan fungsi hati telah banyak dilaporkan. Hal tersebut secara tidak langsung dapat menghambat sistem kekebalan. Beberapa peneliti melaporkan bahwa Pb
mengganggu proses aktivitas pagosit dari leukosit polimorfonuklear dan menurunkan produksi aktif (Koller, 1980).
Karena timbal adalah logam toksik yang bersifat kumulatif sehingga
mekanisme toksisitasnya dibedakan menurut beberapa organ yang dipengaruhinya yaitu sebagai berikut :
a. Sistem hemopoietik: Pb menghambat system pembentukan hemoglobin sehingga menyebabkan anemia.
c. Sistem ginjal: dapat menyebabkan aminoasiduria, fosfaturia, glukosuria,
nefropati, fibrosis dan atrofi glomeruler.
d. Sistem gastro-intestinal: menyebabkan kolik dan konstipasi.
e. Sistem kardiovaskuler: menyebabkan peningkatan permeabilitas kapiler pembeluh darah, system reeproduksi pada ibu hamil, system indokrin.
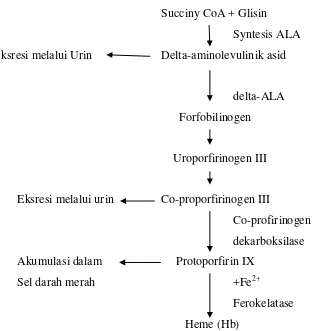
Timbal didalam tubuh terutaman terikat dalam gugus –SH dalam molekul protein dan hal ini menyebabkan hambatan pada aktivitas kerja system enzim. Timbal menggangu system sisntesis Hb dengan jalan menghambat konversi delta aminolevunik asid (delta-ALA) menjadi forfobilinogen dan juga menghambat korporasi dari Fe ke dalam protoporfin IX untuk membentuk Hb, dengan jalan menghambat enzim delta-aminolevunik asid-dehidratase (delta-ALAD) dan ferokelatase. Hal ini mengakibatkan meningkatnya ekskresi koproporfin dalam urin dan delta-ALA serta menghambat sintesis Hb. Berikut merupakan skema penghambatan produksi hemoglobin oleh logam berat Pb :
Succiny CoA + Glisin Syntesis ALA Eksresi melalui Urin Delta-aminolevulinik asid
delta-ALA Forfobilinogen
Uroporfirinogen III
Eksresi melalui urin Co-proporfirinogen III
Co-profirinogen
dekarboksilase Akumulasi dalam Protoporfirin IX
Sel darah merah +Fe2+
Ferokelatase Heme (Hb)
2.3. Destruksi Logam
2.3.1.Destruksi Basah
Teknik destruksi basah adalah dengan memanaskan sampel organik dengan
penambahan asam mineral pengoksidasi atau campuran asam-asam mineral tersebut. Penambahan asam mineral pengoksidasi dan pemanasan yang cukup dalam beberapa menit dapat mengoksidasi sampel secara sempurna, sehinga menghasilkan ion logam dalam larutan asam sebagai sampel anorganik untuk dianalisis selanjutnya. Destruksi basah biasanya menggunakan H2SO4, HNO3 dan HClO4 atau campuran dari ketiga asam mineral tersebut.
2.3.2.Destruksi Kering
Destruksi kering merupakan teknik yang umum digunakan untuk mendekomposisi bahan organik. Sampel diletakkan di dalam krusibel dan dipanaskan sampai semua materi organik terurai dan meninggalkan residu anorganik yang tidak menguap dalam logam oksida. Temperatur yang paling umum digunakan adalah 500 – 550oC. Selain unsur C, H dan N, beberapa logam akan hilang dengan destruksi kering ini, diantaranya halogen, S, Se, P, As, Sb, Ge, Ti, Hg (Anderson, 1987)
2.4. ICP (Inductively Couple Plasma) OES
Seiring semakin pedulinya pencemaran terhadap lingkungan terutama
Inductively couple plasma adalah alat yang dapat mendeteksi senyawa
logam dengan pembakaran menggunakan plasma. Plasma yang dihasilkan dari gas argon akan membakar sampel yang telah ternebulasi sehingga terjadi atomisasi dilanjutkan dengan ionisasi. Elektron yang tereksitasi kemudian kembali lagi/beremisi dan mengeluarkan energi cahaya dengan panjang gelombang yang
spesifik di setiap senyawa logam. Sistem pembacaan yang multi element memudahkan bagi analisa untuk mempercepat keluarnya hasil.
2.4.1.Prinsip Kerja ICP-OES
Proses ini terjadi oleh plasma yang dilengkapi dengan tabung konsentrasi yang disebut torch, paling sering dibuat dari quartz. Torch ini terletak di dalam water-cooled coil of a radio frequency (r,f.) generator. Gas yang mangalir kedalam Torch diaktifkan dan gas di coil region menghasilkan electrically conductive. Ini sama seperti prinsip kerja radio frekuensi pada antena.
Pembentukan induksi plasma sangat bergantung pada kekuatan magnetic field dan pola yang menikuti aliran gas. Gas argon di pantik dengan tesla. Setelah plasma menyala, tesla mati kembali. Perawatan plasma biasanya dengan inductive heating dari gas mengalir. Induksi dari magnetic field yang menghasilkan frekuensi tinggi annular arus listrik di dalam konduktor. Yang mengakibatkan
pemanasan dari konduktor akibat dari ohmic resistance. Suhu yang dihasilkan dari plasma berkisar 700 K.
Untuk mencegah kemungkinan short-circuiting serta meltdown, plasma
Sampel yang akan dianalisis harus dalam larutan. Untuk sampel padatan
diperlukan preparasi sampel dengan proses digestion pada umumnya dengan acid digestion. Peristaltik pump mendorong sampel masuk ke nebulizer. Nebulizer berfungsi untuk mengubah larutan sampel menjadi erasol. Gas yang digunakan untuk mengkabutkan biasanya adalah gas argon. Sprying dari nebulizer kemudian
di ionisasi di dalam plasma.
Energi yang kuat dari plasma mengeksitasi electron dari senyawa ke orbital terluar. Setelah itu diemisikan kembali dan melepaskan energy cahaya dengan panjang gelombang yang spesifik. Cahaya emisi oleh atom suatu unsure pada ICP harus dikonversi ke suatu sinyal listrik yang dapat di ukur banyaknya. Ini diperoleh dengan mengubah cahaya tersebut ke dalam komponen radiasi (hamper selalu dengan cara difraksi kisi) dan kemudian mengukur intensitas cahaya dengan photomultiplier tube pada panjang gelombang spesifik untuk setiap elemen. Cahaya emisi oleh atom atau ion dalam ICP dikonversikan ke sinyal listrik oleh photomultiplier dalam spectrometer. Intensitas dari sinyal di bandingkan intensitas standar yang diketahui konsentrasinya yang telah diukur sebelumnya (Nugroho, 2005).
2.5. Spektrofotometri Serapan Atom
Apabila suatu larutan yang mengandung garam logam (senyawa logam) dilewatkan ke dalam suatu nyala, terbentuk uap yang mengandung atom-atom logam itu menyerap energi, maka electron pada keadaan dasar akan naikbke tingkat energy yang lebih tinggi disebut keadaan tereksitasi. Banyaknya energy
yang diserap berbanding lurus dengan jumlah atom yang terserap. Hal ini merupakan dasar penentuan kuantitatif logam-logam dengan menggunakan Spektrofotometer Serapan Atom.
panjang gelombang tertentu oleh atom-atom bentuk gas dalam keadaan dasar.
Perpanjangan Spektrofotometri Serapan atom ke unsur-unsur lain semula merupakan akibat perkembangan spektroskopi pancaran nyala. Telah lama ahli kimia menggunakan kimia pancaran radiasi oleh atom yang dieksitasikan dalam suatu nyala sebagai alat analitis. Suatu nyala lain, kebanyakan atom berada dalam
keadaan elektronik dasar bukannya berada dalam keadaan eksitasi. (Skoog, West, Holler,1996)
2.5.1. Prinsip Dasar Spektrofotometeri Serapan Atom
Metode SSA berinsip pada absorpsi cahaya oleh atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung pada unsurnya. Cahaya pada panjang gelombang tertentu mempunyai cukup energy untuk mengubah tingkat electron suatu atom. Transisi elektron suatu unsur bersifat spesifik. Dengan absorpsi energi, berarti memperoleh lebih banyak energy, suatu atom pada keadaan dasar akan tereksitasi ke tingkat energi yang lebih tinggi (Khopkar, 2003)
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala yang mengandung atom-atom yang bersangkutan, maka sebagian cahaya itu diserap dan jauhnya penyerapan berbanding lurus dengan banyaknya atom keadaan dasar
yang berada dalam nyala.
Proses terbentuknya uap yang mengandung atom-atom dalam nyala, dapat diringkaskan sebagai berikut; bila suatu larutan yang mengandung senyawa yang
cocok dari yang akan diselidiki itu dilewatkan kedalam nyala, terjadilah peristiwa berikut secara berurutan :
a. Penghilangan pelarut atau evaporasi yang meninggalkan residu padat
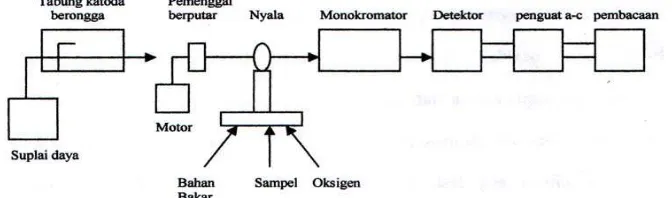
Berikut merupakan skema Instrumentasi Spektrofotometeri Serapan Atom :
Gambar 2.2. Komponen Spektrofotometri Serapan Atom
1. Sumber Sinar
Sumber sinar yang lazim dipaki adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan yang tinggi (600 volt), maka katoda akan memancarkan berkas-berkas electron yang bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi. Elektron dengan gas-gas mulia yang di isikan tadi. Akibat dari
tabrakkan-tabrakkan ini membuat unsur-unsur gas mulia akan kehilangan electron dan menjadi ion bermuatan positif ini selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi pula. Sebagaimana disebutkan diatas, pada katoda terdapat unsur-unsur ini akan terlempar keluar dari permukaan katoda. Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat
energy-energi electron yang lebih tinggi dan akan memancarkan spectrum pancaran dari unsur yang sama dengan unsur yang akan dianalisis. (Rohman, 2007)
2. Bahan Bakar dan Bahan Pengoksidasi
hati-hati agar proses atomisasinya sempurna. Ionisasi harus dihindarkan dan ini
dapat terjadi bila temperatur terlalu tinggi. Gambar dibawah ini menunjukkan suatu tipe atomiser nyala (Khopkar, 2002).
Umumnya bahan bakar yang digunakan adalah hidrogen, asetilen dan
propana, sedangkan oksidatornya adalah udara, oksigen dan NO2.
Tabel 2.2. Jenis-jenis Gas Pembakar pada SSA
Bahan bakar Oksidan Temperatur
Mkasimum (oK)
Monokromator digunakan untuk memisahkan garis emisi sesuai dengan panjang gelombangnya. Monokromator digunakan dalam analisa multi unsur
dengan cara memindai cepat dari satu garis emisi ke garis emisi lainnya. Kisi difraksi merupakan inti dari spectrometer, kisi memecah cahaya putih menjadi beberapa panjang gelombang yang berbeda.
4. Detektor
5. Lampu Katoda Berongga (Hollow Cathode Lamp)
Lampu katoda berongga terdiri atas tabung gelas yang di isi dengan gas argon (Ar) atau neon (Ne) bertekanan rendah (4-10 torr) dan di dalamnya dipasang sebuah katoda berongga dan anoda. Rongga katoda berlapis logam
murni dari unsur obyek analisis. Misalnya : untuk pengukuran Pb diperlukan lapisan logam Pb. Batang anoda terbuat dari logam wolfram / tungsten (Boss,C.B. and Freeden, K.J. 1997).
2.5.3. Spektrofotometer Serapan Atom Tanpa Nyala dan Dengan Nyala
Metode spektrofotometri Serapan Atom mempunyai beberapa kelebihan dibandingkan metode spektrofotometri nyala. Pada metode spektrofotometri nyala, emisi tergantung pada sumber eksitasi. Bila eksitasi dilakukan secara termal maka ia tergantung pada temperature sumber. Selain itu eksitasi termal tidak selalu spesifik, dan eksitasi secara serentak pada berbagai jenis logam dalam suatu sampel dapat saja terjadi. Pada metode Spektrofotometri Serapan Atom, perbandingan banyaknya ataom yang tereksitasi terhadap atom yang berada pada tingkat dasar harus cukup besar, karena metode serapan atom hanya tergantung pada perbandingan ini dan tidak bergantung pada nyala. Metode serapan sangatlah spesifik. Logam-logam yang membentuk campuran kompleks dapat dianalisa dan
2.5.3. Gangguan Pada SSA dan Cara Mengatasinya
Gangguan diartikan sebagai suatu faktor kimia atau fisika yang akan mempengaruhi jumlah atom pada analit dalam keadaan dasar (ground state) sehingga akan menyebabkan bertambah atau berkurangnya bacaan nilai serapan
atau unsure yang dianalisis.
Ada beberapa faktor gangguan dalam menggunakan SSA :
- Suhu yang sesuai, suhu gas pembakar harus sesuai dengan suhu unsur yang akan dianalisis.
- Konsentrasi sampel tidak boleh melebihi kesensitifan dari alat detector SSA. Ini akan menyebebkan gangguan terhadap garis spectrum dan mengakibatkan kerusakan pada alat detector SSA.
BAB 3
METODE PENELITIAN
3.1. Alat dan Bahan
3.1.1. Alat
- Inductively Coupled Plasma-Optical Emission Varian 715-ES (ICP-OES)
- Spektrofotometer Serapan Atom Z-2000 Series
- Labu Takar Pyrex
- Gelas Ukur Pyrex
- Pipet Volumetri Pyrex
- Gelas Beaker Pyrex
- Bola Karet -
- Hot Plate Cimarec
- Pipet Skala Pyrex
- pH meter WalkLAB
- Kaca arloji -
- Pipet tetes -
- Botol Aquadest -
- Oven Fisher
- Corong -
3.1.2. Bahan
- Hati Kambing Potong
- Larutan induk Pb 1000 mg/L p.a.E.Merck
- HNO3(p) p.a.E.Merck
- Aquades
3.2. Prosedur Penelitian
3.2.1. Pembuatan Larutan Standart Pb2+
a. Larutan Standar Pb2+ 1000 mg/L
Sebanyak 1,5990 g Pb(NO3)2 dimasukkan ke dalam labu Erlenmeyer yang telah berisi aquadest, diaduk hingga seluruh kristal larut sempurna, dimasukkan ke dalam labu ukur 1000 mL, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
b. Larutan Standar Pb2+ 100 mg/L
Sebanyak 10 mL larutan standar Pb 1000 mg/L dimasukkan ke dalam labu takar
100 mL lalu diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
c. Larutan Standart Pb2+ 10 mg/L
d. Larutan Standart Pb2+ 0,3; 0,5; 0,7; 0,9 dan 1,1 mg/L
Dipipet sebanyak masing-masing 1,5; 2,5; 3,5; 4,5 dan 5,5 mL larutan standart Pb2+ 10 mg/L dimasukkan ke dalam labu ukur 50 mL, ditambahkan aquadest sampai garis tanda dan dihomogenkan.
3.2.2. Pembuatan Kurva Kalibrasi Larutan Standart Pb2+
Sebanyak 50 ml larutan seri standart Pb2+ 0,3 mg/L diukur absorbansinya dengan
Spektrofotometri Serapan Atom (SSA) pada λ = 217,0 nm dan dilakukan hal yang
sama untuk seri standart Pb2+ 0,5; 0,7; 0,9 dan 1,1 mg/L.
3.2.3. Pengambilan Sampel
Tipe metode pengambilan yang dilakukan pada penelitian ini adalah random sampling, dimana sampel yang dianalisa berasal dari beberapa Pasar Tradisional yang dipilih secara acak secara manual, dan dapat di tunjukkan bahwa pada sampel A dan B merupakan sampel Hati Kambing Potong kawasan Non industri yang berasal dari Pasar Tradisonal Sei Rampah, dan sampel C dan D merupakan sampel Hati Kambing Potong kawasan Industri yang berasal dari Pasar
Tradisional Perbaungan yang diambil dari kawasan industri Perbaungan.
3.2.4. Pengabuan Sampel
3.2.5. Penyediaan Larutan Sampel
Sebanyak 10 gr abu sampel yang diperoleh pada destruksi kering dimasukkan kedalam beaker glass 250 ml kemudian ditambahkan 10 ml HNO3 pekat dicampur ratakan sehingga diperoleh larutan sampel dan dipanaskan selama 30 menit dan
didinginkan. Larutan sampel tersebut ditambahkan 5 ml HNO3 pekat kemudian dipanaskan diatas hot plate hingga setengah volume awal, disaring dengan kertas saring whatman No.42, dicuci dengan aquadest panas, kemudian filtrat dimasukkan kedalam labu ukur 10 ml dan diatur pH=3 dan ditambahkan akuadest hingga garis tanda lalu dihomogenkan.
3.2.6. Penentuan Pb2+ dalam Sampel
3.3. Bagan Penelitian
3.3.1. Penentuan Kurva Kalibrasi Timbal (Pb)
50 mL larutan seri standart Pb2+ 0,3 mg/L
dibuat pada pH = 3
ditentukan absorbansinya pada panjang gelombang = 217,0 nm dengan menggunakan alat Spektrofotometer Serapan Atom
dilakukan hal yang sama untuk larutan seri standart 0,5; 0,7; 0,9 dan 1,1 mg/L
3.3.2. Penentuan logam Pb dalam Sanpel (SNI 01-3552-2000) Sampel Hati Kambing Potong
dipotong kecil-kecil sebesar 80 mesh dimasukkan kedalam cawan penguap dikeringkan dalam oven hingga berat konstan pada suhu 105oC
didinginkan
diabukan dalam tanur listrik pada suhu 550oC
didinginkan dalam desikator
ditimbang sebanyak 10 gr abu sampel Abu sampel
dimasukkan kedalam beaker glass 250 ml
ditambahkan 10 ml HNO3(p)
dipanaskan diatas hot plate selama 30 menit
didinginkan
Larutan sampel
ditambahkan 5 ml HNO3(p)
dipanaskan diatas hot plate hingga setengah volume awal
didinginkan
disaring dengan kertas saring whatman no.42
filtrat residu
dibilas dengan aquades panas
filtrat residu
dimasukkan kedalam labu ukur 10 ml
diatur pH hingga mencapai pH=3
diencerkan dengan aquades hingga garis tanda
diuji secara dengan ICP-OES kemudian ditentukan kandungan Pb pada panjang gelombang 217,0 nm dengan SSA.
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Logam Timbal
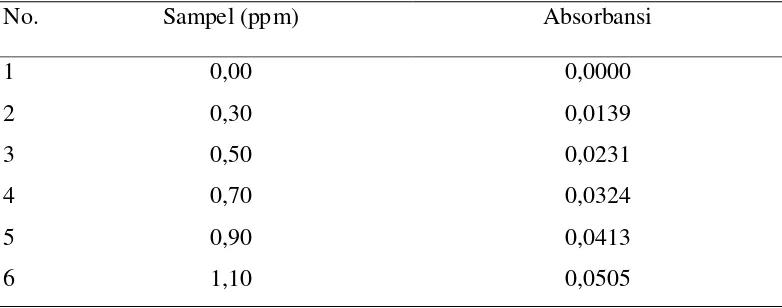
Tabel 4.1. Data pengukuran absorbansi larutan seri standar Timbal (Pb)
No. Sampel (ppm) Absorbansi
1 0,00 0,0000
2 0,30 0,0139
3 0,50 0,0231
4 0,70 0,0324
5 0,90 0,0413
6 1,10 0,0505
4.1.1.1. Penurunan Persamaan Garis Regresi Dengan Metode Least Square
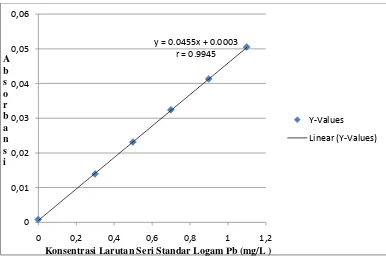
Data absorbansi yang diperoleh untuk suatu larutan standar Pb diplotkan terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa garis linear seperti pada gambar 4.1. Persamaan garis regresi ini diturunkan dengan metode
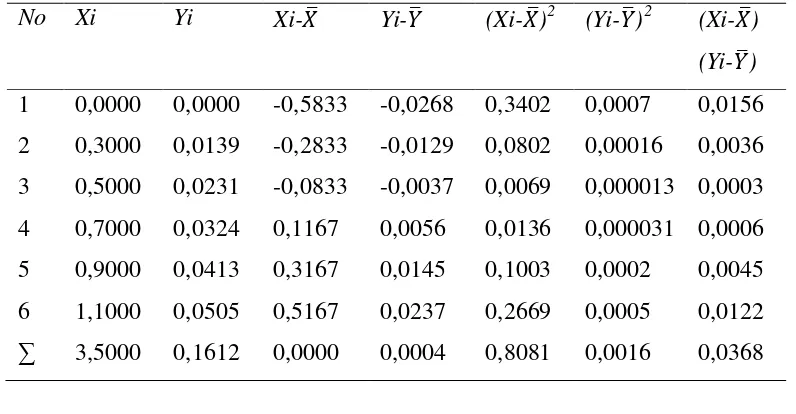
Tabel 4.2. Penurunan persamaan garis regresi untuk penentuan konsentrasi logam Timbal (Pb) berdasarkan pengukuran absorbansi larutan standar Timbal (Pb)
No Xi Yi Xi-�� Yi-�� (Xi-��)2 (Yi-��)2 (Xi-��)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
Y = aX + b Dimana : a = slope b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square sebagai berikut :
a = ∑(��−�� )(��−�� )
∑ (��−�� )2
b = Y – a X
a = 0,0368
0,8081 = 0,0455
b = 0,0268 – (0,0455 ) (0,5833) = 0,0268 – 0,0265
= 0,0003
Maka persamaan garis yang diperoleh adalah :
Y = 0,00455X + 0,0003
4.1.1.2. Penentuan Koefisien korelasi untuk Timbal (Pb)
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
r = ∑(��−�� )(��−�� )
�(��−��)2 (��−��)2
Koefisien korelasi untuk Timbal (Pb) adalah :
r = 0,0368
�(0,8081)(0,0016) = 0,9945
Gambar 4.1. Kurva Kalibrasi Larutan Seri Standart Logam Pb (mg/L)
4.1.1.3. Penentuan Kadar Timbal (Pb) dalam Sampel
Kadar Timbal (Pb) dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan mensubsitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran terhadap persamaan garis regresi dari kurva kalibrasi.
4.1.1.3.1.Penentuan Kadar Timbal (Pb) yang terkandung dalam Sampel Hati Kambing Potong A (Kawasan Non Industri) dengan metode Spektrofotometri Serapan Atom dalam mg/L.
Dari data pengukuran absorbansi Timbal (Pb) untuk sampel Hati Kambing Potong
A diperoleh serapan (A) sebagai berikut : A1 = 0,0215
A2 = 0,0209 A3 = 0,0211
Dengan mensubsitusikan nilai Y (Absorbansi) ke persamaan garis regresi
Y = 0,0455X + 0,0003, maka diperoleh :
X1 = 0,4659 X2 = 0,4527 X3 = 0,4571
Dengan demikian kadar Timbal pada Hati Kambing Potong A yang adalah :
�̅ = ∑��
Catatan : Data hasil perhitungan untuk sampel B, C dan D dapat di lihat pada lampiran 2, 3 dan 4. derajat kepercayaan 95% (p=0,05), t-4,30
maka, d = t(0,05 x n-1) Sx
d = 4,30 x 0,1 x 0,0038 = 0,0016
Dari data hasil pengukuran kadar Pb pada sampel Hati Kambing Potong A adalah sebesar :
0,4585 ± 0,0016 mg/L
4.1.1.3.2.Penentuan Kadar Timbal (Pb) pada Sampel Hati Kambing Potong B (Kawasan non Industri) dengan metode Spektrofotometri Serapan Atom dalam mg/L
Dari data pengukuran absorbansi Timbal (Pb) untuk sampel Hati Kambing Potong A diperoleh serapan (A) sebagai berikut :
A1 = 0,0208 A2 = 0,0208 A3 = 0,0206
Y = 0,0455X + 0,0003, maka diperoleh :
X1 = 0,4505 X2 = 0,4505 X3 = 0,4461
Dengan demikian kadar Timbal pada Hati Kambing Potong A yang adalah :
�̅ = ∑��
� =
1,3471
3 = 0,4490
(X1-��)2 = (0,4505 – 0,4490)2 = 2,25x10-6 (X2-��)2 = (0,4505 – 0,4490)2 = 2,25x10-6 (X3-��)2 = (0,4461 – 0,4490)2 = 8,41x10-6
∑ (Xi - ��)2 = 1,29x10-5
maka, S =
�
∑(��−��)2
�−1 =
�
1,29�10−5
2 = 0,0025
Didapatkan harga, Sx = �
√� =
0,0025
1,7320 = 0,0014
Dari data hasil distribusi untuk n = 3, derajat kebebasan (dk) = n- 1 = 2 untuk derajat kepercayaan 95% (p=0,05), t-4,30
maka, d = t(0,05 x n-1) Sx
d = 4,30 x 0,1 x 0,0014 = 0,0006
Dari data hasil pengukuran kadar Pb pada sampel Hati Kambing Potong B adalah sebesar :
4.1.1.3.3.Penentuan Kadar Timbal (Pb) pada Sampel Hati Kambing Potong C (Kawasan industri) dengan metode Spektrofotometri Serapan Atom dalam mg/L
Dari data pengukuran absorbansi Timbal (Pb) untuk sampel Hati Kambing Potong C diperoleh serapan (A) sebagai berikut :
A1 = 0,0404 A2 = 0,0400 A3 = 0,0401
Dengan mensubsitusikan nilai Y (Absorbansi) ke persamaan garis regresi Y = 0,0455X + 0,0003, maka diperoleh :
X1 = 0,8813 X2 = 0,8725 X3 = 0,8747
DengaN demikian kadar Timbal pada Hati Kambing Potong A yang adalah :
�̅ = ∑�� derajat kepercayaan 95% (p=0,05), t-4,30
maka, d = t(0,05 x n-1) Sx
d = 4,30 x 0,1 x 0,0083 = 0,0035
Dari data hasil pengukuran kadar Pb pada sampel Hati Kambing Potong C adalah sebesar :
4.1.1.3.4.Penentuan Kadar Timbal (Pb) pada Sampel Hati Kambing Potong D (kawasan Industri) dengan metode Spektrofotometri Serapan Atom dalam mg/L
Dari data pengukuran absorbansi Timbal (Pb) untuk sampel Hati Kambing Potong D diperoleh serapan (A) sebagai berikut :
A1 = 0,0398 A2 = 0,0395 A3 = 0,0393
Dengan mensubsitusikan nilai Y (Absorbansi) ke persamaan garis regresi Y = 0,0455X + 0,0003, maka diperoleh :
X1 = 0,8681 X2 = 0,8615 X3 = 0,8571
DengaN demikian kadar Timbal pada Hati Kambing Potong A yang adalah :
�̅ = ∑�� derajat kepercayaan 95% (p=0,05), t-4,30
maka, d = t(0,05 x n-1) Sx
d = 4,30 x 0,1 x 0,0031 = 0,0013
Dari data hasil pengukuran kadar Pb pada sampel Hati Kambing Potong A adalah sebesar :
4.1.1.3.5. Penentuan Kadar Timbal (Pb) yang terkandung dalam Sampel Hati Kambing Potong A (Kawasan Non Industri) dengan Metode Spektrofotometri Serapan Atom dalam mg/Kg.
kadar logam timbal = ��������� �������
����� ����� ℎ x 10
6
mg/Kg
Dengan mengkalikan hasil penentuan Timbal dari sampel di atas, maka diperoleh hasil pengukuran kadar Timbal dari 10 gram sampel sebesar :
Kadar Timbal pada 10 gram sampel dapat dihitung sebagai berikut :
kadar =
Maka diperoleh kadar logam Timbal (Pb) pada sampel Hati Kambing Potong A adalah 0,4585 mg/Kg.
Catatan : Dari hasil perhitungan kadar Timbal untuk sampel B,C dan D dapat dilihat pada lampiran 2.
4.1.2. Penentuan Beda Rataan
Penentuan beda rataan menggunakan motode deviasi standar, dimana persamaan yang digunakan adalah sebagai berikut :
�2 : nilai rataan variabel kedua
S2 : nilai simpangan baku variabel kedua
��2 : nilai rataan variabel kedua
4.1.2.1 Beda rataan kadar Timbal (Pb) pada Sampel A (Kawasan Non Industri) dan C (Kawasan Industri)
Dari hasil perhitungan kadar Timbal (dalam mg/Kg) di atas diperoleh data sebagai berikut :
Kadar Pb pada sampel A (�̅1) = 0,4585 ; Simpangan baku (S1) = 0,0038 Kadar Pb pada sampel C (�̅2) = 0,8761 ; Simpangan baku (S2) = 0,0083
Dengan mensubstitusikan nilai S dari kedua jenis Sampel ke dalam persamaan 4.1.2.1, maka diperoleh simpangan baku gabungan :
S2 = {(2−1)(0,0038)
2+ (2−1)(0,0083)2
(2+2−1) = 4,16x10
-5
S = 0,0064
Dengan mensubstitusikan nilai �̅ dan nilai simpangan baku gabungan ke dalam persamaan 4.1.2.2 , maka diperoleh :
t = (0,4585−0,8761) 4,16�10−5�1
2+ 1 2
= −0,4176
4,16�10−5 = -10038,4
dengan melihat nilai derajat kebebasan = 8, nilai |t| (P=0,05) adalah 2,31. Karena nilai hasil perbandingan, |t| lebih besar daripada 2,31 (yaitu 10038,4 > 2,31 ) maka selisih kadar Timbal dari kedua jenis Sampel A dan C dianggap berarti dan
4.1.2.2. Beda rataan kadar Timbal (Pb) pada Sampel B (Kawasan Non Industri) dan D (Kawasan Industri)
Dari hasil perhitungan kadar Timbal (dalam mg/Kg) di atas diperoleh data sebagai berikut :
Kadar Pb pada sampel A (�̅1) = 0,4490 ; Simpangan baku (S1) = 0,0025 Kadar Pb pada sampel C (�̅2) = 0,8622 ; Simpangan baku (S2) = 0,0031
Dengan mensubstitusikan nilai S dari kedua jenis Sampel ke dalam persamaan diatas, maka diperoleh simpangan baku gabungan :
S2 = {(2−1)(0,0025)
2+ (2−1)(0,0031)2
(2+2−1) = 7,93x10
-6
S = 0,0028
Dengan mensubstitusikan nilai �̅ dan nilai simpangan baku gabungan ke dalam
persamaan di atas , maka diperoleh :
t = (0,4490−0,8622) 7,93�10−6�1
2+ 1 2
= −0,4132
7,93�10−6 = -52105,9
dengan melihat nilai derajat kebebasan = 8, nilai |t| (P=0,05) adalah 2,31. Karena nilai hasil perbandingan, |t| lebih besar daripada 2,31 (yaitu 52105,9 > 2,31 ) maka
selisih kadar Timbal dari kedua jenis Sampel A dan C dianggap berarti dan dianggap sangat menunjukkan perbedaan yang signifikan.
4.2. Pembahasan
Penentuan kadar Timbal (Pb) di dalam Hati Kambing Potong yang terdapat pada kawasan industri dan Non industri dilakukan dengan mendestruksi sampel dengan metode destruksi basah. Penentuan logam Timbal (Pb) dengan menggunakan HNO3. Pemilihan pelarut yang digunakan berdasarkan analisa pemisahana kualitatif penggolangan kation. Dimana Pb merupakan kation golongan 1 dan pemisahan kation ini dengan menggunakan HN03 (Vogel, 1985).
Pengatuaran pH = 3 dilakukan karena pada pH dibawah 2 dapat menyebabkan kerusakan alat dan korosi dan di atas pH 4 menyebabkan pengendapan logam yang terdapat dalam sampel. Kemudian ditentukan nilai absorbansi dan konsentrasi dari sampel menggunakan alat Spektrofotometer Serapan Atom pada panjang gelombang 217,0 nm.
Kurva standar larutan seri standar logam Timbal (Pb) dibuat dengan memvariasikan konsentrasi larutan seri standar dengan menggunakan Metode Least Square sehingga diperoleh persamaan garis linear untuk logam Timbal Y = 0,0455X + 0,0003.
Dalam penelitian ini diperoleh koefisien korelasi untuk logam Timbal (Pb) = 0,9945. Hal ini menunjukkan adanya hubungan atau korelasi positif antara konsentrasi dengan absorbansi. Pada penelitian analitik, grafik kurva standar yang
baik ditunjukkan dengan harga lebih kecil sama dengan 0,99.
Dimana pada penelitian terdahulu, Analisa logam Pb, pada Hati sapi local dan impor diperoleh kandungan rata-rata logam pada hati sapi Jakarta dalam
bobot basah adalah: 0,1667 μg/g. Sementara untuk logam Pb dalam hati sapi Bogor adalah: 0,3578 μg/g. Sedangkan untuk logam Pb dalam hati sapi Cirebon
adalah: 0,2931 μg/g. Kandungan rata-rata logam Pb dalam hati sapi New Zealand
adalah: 0,2915 μg/g. Sedangkan kandungan rata-rata logam Pb dalam hati sapi
besar bila dibandingkan dengan hati sapi Jakarta, Cirebon, New Zealand dan
Australia.(Evi, 2006)
Dari penelitian yang dilakukan diperoleh kadar logam Timbal (Pb) pada sampel A (Kawasan non industri) = 0,4585 mg/Kg, sampel B (kawasan non
Industri) = 0,4490 mg/Kg, sampel C (Kawasan Industri) = 0,8761 mg/Kg, dan sampel D (Kawasan Industri) = 0,8622 mg/Kg. Kadar logam Timbal dalam sampel Hati Kambing Potong yang diperoleh apabila dibandingkan dengan data yang ada dalam lampiran surat keputusan SNI 7387:2009, menunjukkan bahwa kandungan logam Pb dalam Hati Kambing Potong yang diperoleh masih berada dibawah ambang batas yang diizinkan SNI 7387:2009 yaitu 1,0 mg/Kg. Dalam lampiran data SNI ambang batas Pb pada hati kambing.
Dengan melihat data hasil analisa kadar Timbal, dimana nilai beda rataan dari kadar timbal pada hati kambing potong kawasan industri dan non industri adalah signifikan atau dengan kata lain dapat diperhatikan.
Adanya logam Timbal (Pb) di dalam hati kambing potong tersebut berasal dari beberapa faktor, diantaranya dari makanan, minuman ruang lingkup udara yang tercemar dari limbah pembuangan industri, gas buangan kendaraan transportasi dimana seperti pada makanan yaitu rumput atau alang yang di konsumsi oleh hewan ruminansia seperti kambing telah tercemar oleh logam berat
Pb begitu juga dari minuman yang dikonsumsi oleh hewan rumansia tersebut, yang kemudian memungkinkan logam tersebut terakumulasi dalam hati kambing potong dan berikatan dengan enzim yang berada dalam hati kambing potong tersebut baik dalam bentuk komplek organik maupun kompleks anorganik dalam
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
a. Data hasil penelitian yang telah dilakukan diperoleh kesimpulan sebagai berikut : Kadar logam Timbal (Pb) pada sampel A (kawasan non Industri) = 0,4585 mg/Kg, sampel B (kawasan non Industri) = 0,4490 mg/Kg, sampel C (kawasan Industri) = 0,8761 mg/Kg, dan sampel D (kawasan Industri) = 0,8622 mg/Kg b. Kadar logam Timbal (Pb) didalam hati kambing potong baik kawasan industri
maupun non industri masih memenuhi standar yang ditetapkan oleh SNI 7387:2009 yaitu 1,0 mg/Kg.
5.2. Saran
DAFTAR PUSTAKA
Anderson, R. 1987. Sampel Pretreatment and Separation. New York: Jhon Wiley and Sons
Boss, C. B. and Freeden, K. J. 1997. Concepts, Intrumentation, and Techniques in Inductively Coupled Plasma Optical Emision Spectrometry. USA: Perkin Elmer.
Darmono. 1995. Logam Dalam Sistem Biologi Makhluk Hidup. Jakarta : UI-Press
Darmono. 2001. Lingkungan Hidup dan Pencemaran. Jakarta : UI-Press
Diapari, D. 2009. Dampak Pencemaran Timbal (Pb) Akibat Hujan Asam Terhadap Produksi Ternak Lokal Jantan, Disertai Sekolah Pascasarjana Institut Pertanian Bogor.
Ebynthalina, Sembiring., (2006), Akumulasi Pb dan Pengaruhnya Pada Kondisi Daun Swietenia Macropyhlla King, ITB, Bandung
Evi, Dian., (2006), Analisis Kandungan Timbal (Pb), Tembaga (Cu), dan Kadmium (Cd) Dalam Hati Sapi Secara Spektrofotometri Serapan Atom, Jakarta : UI-Press.
Fardiaz, S. 1992. Polusi Air dan Udara. Yogyakarta : Kanisius.
Khopkar. S. M. 2002. Konsep Dasar Kimia Analitik. Penerjemah : Saptorahardjo. Jakarta : UI-Press.
Koller, L. D. 1980. Immunotoxicology of Heavy Metals. London : Academic Press Inc.
Kozlowski, T.T.P.J, Kramer, and S.G, Pallardy. 1991. The Physiological Ecology of Woody Plants. London : Academic Press Inc.
Mukono, H.J. 2002. Epidemiologi Lingkungan. Surabaya : Airlangga University Press.
Nugroho. 2005. Metode Analisis Menggunakan Alat ICP-AES Plasma 40 Untuk Penentuan Unsur As dan Sb. Bandung : ITB.
Oskarson, A., L. Jorhem, J. Sundberg, N.G. Nilsson And L. Albans. 1992. Lead Poisoning in Cattle-transfer of Lead to Milk. USA : The Science of the Total Environment.
Rohman, A. I. 2007. Kimia Farmasi Analitis. Yogyakarta : Pustaka Pelajar.
Santi, N. 2001. Pencemaran Udara Oleh Timbal (Pb) Serta Penanggulangannya. Medan : Universitas Sumatera Utara.
Skoog, W.H. 1996. Fundamental Of Aanalytical Chemistry. 6th edition. USA : Saunders Publishing.
Sudarmaji, Mukono H.J, Corie I.P, 2006, Toksikologi Logam Berat B3 dan Dampaknya Terhadap Kesehatan, Jurnal Kesehatan Lingkungan, (Http//www.journal.unair.ac.id/filerpdf/kesling-2-2-03.pdf) Diakses tanggal 20 November 2013.
Vogel, A. I. 1994. Kimia Analisis Kuantitatif Anorganik. Edisi Kelima. Jakarta :PT Kalman Media Pustaka.
Lampiran 1. Kondisi alat Spektrofotometer Serapan Atom merek Z-2000 Series
pada pengukuran konsentrasi logam Timbal (Pb)
No. Parameter Logam Pb
Kecepatan aliran gas pembawa (L/min) Kecepatan aliran Udara (L/min)
Lebar celah (nm)
Lampiran 2. Data Kadar Timbal (Pb) pada Hati Kambing Potong untuk masing-masing Sampel.
No. Sampel Hati Kambing Potong Kadar Pb (mg/Kg)
1 2. 3 4
Sampel A (kawasan non Industri) Sampel B (kawasan non Industri)
Sampel C (kawasan Industri) Sampel D (Kawasan Industri)
Lampiran 3. Kondisi Alat ICP – OES Merek Varian pada Uji Kualitatif Timbal
dalam Hati Kambing potong
No. Parameter Kondisi
1
Kecepatan Aliran Gas Plasma (L/min) Kecepatang gas pendukung (L/min) Ketinggian tungku (nm)
Tekanan nebulizer (kPa)
Penundaan Penyerapan Sampel (s) Lama Pembilasan
Waktu Pembacaan Replikasi (s)
Lampiran 4. Perbandingan Konsentrasi Logam Timbal (Pb) dalam Sampel Hati
Kamping Potong di Kawasan Industri dan Non Industri dengan Standar SNI 7387:2009 Tentang Batas Maksimum Cemaran Logam Berat Dalam Pangan